KOMBINASI KITOSAN DENGAN KALIUM SORBAT,
NATRIUM BENZOAT DAN EKSTRAK TERUNG PUNGO
(
Solanum
sp.) TERHADAP AKTIVITAS ANTIBAKTERI DAN
DAYA AWET BANDENG PRESTO
BAGUS FAJAR PAMUNGKAS
SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI TESIS DAN
SUMBER INFORMASI
Dengan ini saya menyatakan bahwa tesis Kombinasi Kitosan dengan Kalium Sorbat, Natrium Benzoat dan Ekstrak Terung Pungo (Solanum sp.) terhadap Aktivitas Antibakteri dan Daya Awet Bandeng Presto adalah karya saya dengan arahan dari Komisi Pembimbing dan belum diajukan dalam bentuk apapun kepada perguruan tinggi manapun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir tesis ini.
Bogor, Agustus 2008
Bagus Fajar Pamungkas NIM. C351050041
ABSTRACT
BAGUS FAJAR PAMUNGKAS. The Combination of Chitosan and Potassium Sorbate, Sodium Benzoate, Terung Pungo (Solanum sp.) Extract on the Antibacterial Activity and Preservative Agent of Cooked Milkfish. Supervised by LINAWATI HARDJITO and JOKO SANTOSO
The study investigated antibacterial activity of chitosan and its combination of potassium sorbate (S), sodium benzoate (B) and terung pungo (Solanum sp.) extract (T) against Escherichia coli and Staphylococcus aureus. Combination of 0.05% chitosan with 0.05% S, 0.05% B and 20 µg/ml T did not show synergystic inhibition against bacteria, however 0.1% chitosan showed higher antibacterial activities in comparison to others. Application of 0.1% chitosan in pre-cooked milkfish increased shelflife from 16 to 38 hours at 28-30
o
C. Chitosan was able to reduce the formation of TVB and TBA during preservation period. The results indicated that chitosan was an effective preservative agent for cooked milkfish.
RINGKASAN
BAGUS FAJAR PAMUNGKAS. Kombinasi Kitosan dengan Kalium Sorbat, Natrium Benzoat dan Ekstrak Terung Pungo (Solanum sp.) terhadap Aktivitas Antibakteri dan Daya Awet Bandeng Presto. Dibimbing oleh LINAWATI HARDJITO and JOKO SANTOSO
Kitosan dan senyawa turunannya diketahui memiliki aktivitas antibakteri yang bersifat biocompatible, bioantigenik, biofungsional dan tidak toksik, sehingga diharapkan dapat meningkatkan daya awet produk pangan. Permasalahan kitosan sebagai pengawet pangan adalah daya awet yang masih rendah, terutama untuk menggantikan bahan kimia yang dilarang seperti formalin. Oleh karena itu dibutuhkan penelitian kitosan yang dikombinasikan dengan bahan lain untuk meningkatkan aktivitas antibakteri dan daya awetnya pada produk pangan. Penelitian ini bertujuan mencari aktivitas antibakteri terbaik dari kitosan dan kombinasinya dengan kalium sorbat, natrium benzoat dan ekstrak terung pungo (Solanum sp.). Perlakuan yang memiliki aktivitas antibakteri terbaik selanjutnya diaplikasikan produk bandeng presto untuk mengetahui daya awetnya. Penelitian dilakukan dua tahap, tahap I adalah pengujian aktivitas antibakteri dari kitosan dan kombinasinya dengan kalium sorbat, natrium benzoat dan ekstrak Solanum sp., sedangkan tahap II adalah aplikasi dari perlakuan aktivitas antibakteri terbaik tahap I pada bandeng presto untuk mengetahui daya awetnya. Pengujian aktivitas antibakteri menggunakan metode kontak medium cair dan dianalisis secara kuantitatif menggunakan metode total plate count
(TPC). Bakteri uji yang digunakan adalah Staphylococcus aureus dan Escherichia coli. Perlakuan yang digunakan adalah: kitosan 0,1%; kitosan 0,05%; kitosan 0,05% + kalium sorbat 0,05% (KS); kitosan 0,05% + natrium benzoat 0,05% (KB); kitosan 0,05% + ekstrak Solanum sp. 20 µg/ml (KT), kalium sorbat 0,1% (S), natrium benzoat 0,1% (B); ekstrak Solanum sp. 20 µg/ml (T); asam asetat 0,07% (AA); kontrol atau tanpa perlakuan (C). Perlakuan terbaik dari penelitian tahap I diaplikasikan pada bandeng presto. Prosedurnya adalah bandeng yang telah diberi bumbu, direndam dalam larutan yang mengandung perlakuan terbaik selama 2x15 menit. Setelah proses pemasakan, dilanjutkan pengemasan non
-vacuum dengan plastik HDPE steril dan disimpan pada suhu kamar (28-30 oC). Pengamatan dilakukan setiap 24 jam sampai jam ke 120 dengan parameter yang diamati adalah TPC dan pH, sedangkan TVB, TBA, aw dan kadar air dilakukan
pada penyimpanan jam ke 0 dan 72.
Hasil pengujian aktivitas antibakteri menunjukkan bahwa kombinasi kitosan dengan bahan lain tidak memberikan efek antibakteri yang sinergis. Kitosan 0,05% memiliki aktivitas antibakteri lebih baik daripada KS, KB dan KT dengan jumlah bakteri lebih rendah yaitu 2,21 ± 0,07 log cfu/ml terhadap S. aureus dan 3,94 ± 0,63 log cfu/ml terhadap E. coli. Jumlah bakteri pada KS sebesar 2,65 log cfu/ml terhadap S. aureus dan 4,38 ± 0,20 log cfu/ml terhadap E.
coli, sedangkan KB sebesar 2,58 ± 0,11 log cfu/ml terhadap S. aureus dan 4,31 ± 0,10 log cfu/ml terhadap E. coli, dan KT sebesar 2,36 ± 0,01 log cfu/ml terhadap
jumlah bakteri paling rendah yaitu 1,17 ± 0,06 log cfu/ml terhadap S. aureus dan 1,43 ± 0,27 log cfu/ml terhadap E. coli, dan dipilih untuk diaplikasikan pada produk bandeng presto
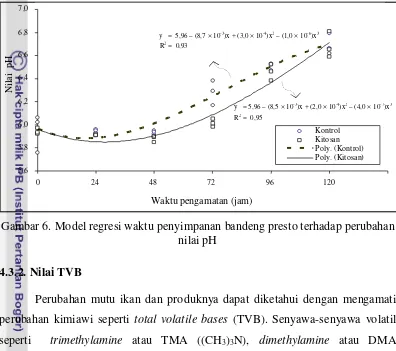
Hasil pengamatan jumlah bakteri bandeng presto mengalami peningkatan selama penyimpanan. Berdasarkan SNI 01-4106-1996, jumlah bakteri total yang diijinkan pada bandeng presto adalah < 2 x 105 cfu/g atau sama dengan < 5,3 log cfu/g, sehingga dengan menggunakan model regresi diketahui bandeng presto yang direndam kitosan 0,1% memiliki daya awet selama 38 jam, sedangkan kontrol hanya 16 jam. Hasil pengamatan nilai pH bandeng presto yang direndam kitosan maupun kontrol relatif sama.
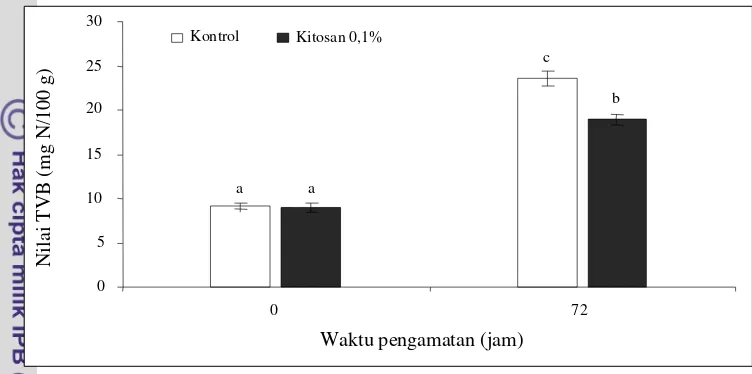
Nilai TVB bandeng presto yang direndam kitosan adalah 8,97 ± 0,53 mg N/100 g (jam ke 0) dan 18,95 ± 0,61 mg N/100 g (jam ke 72), sedangkan kontrol adalah 9,14 ± 0,39 mg N/100 g (jam ke 0) dan 23,6 ± 0,81 mg N/100 g (jam ke 72). Nilai TBA bandeng presto yang direndam kitosan tidak mengalami peningkatan signifikan setelah disimpan selama 72 jam yaitu 1,45 ± 0,59 mg mal/kg (jam ke 0) menjadi 1,66 ± 0,31 mg mal/kg (jam ke 72), sedang kontrol mengalami peningkatan nilai TBA yang nyata setelah penyimpanan yaitu 1,45 ± 0,59 mg mal/kg (jam ke 0) menjadi 8,51 ± 0,66 mg mal/kg (jam ke 72). Hasil ini menunjukkan kitosan efektif menghambat terbentuknya basa-basa volatil dan oksidasi lipida pada produk bandung presto.
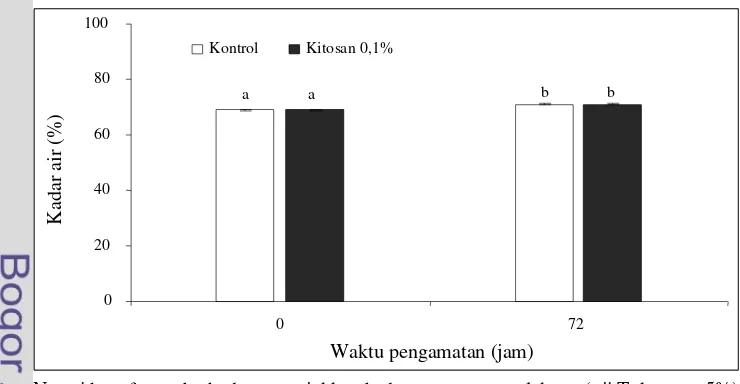
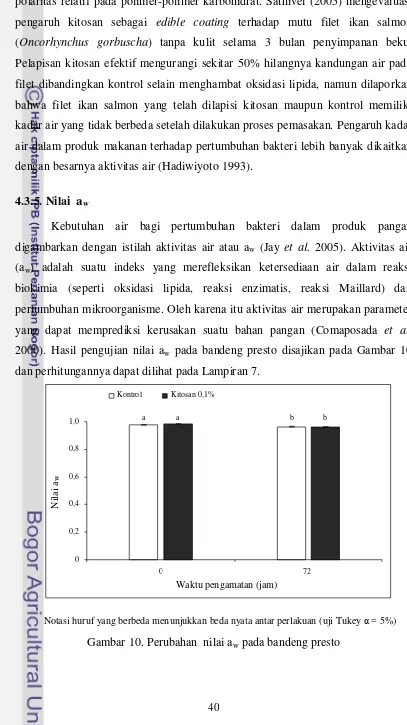
Hasil pengamatan kadar air bandeng presto yang direndam kitosan 0,1% adalah 68,92 ± 0,32% (jam ke 0) dan 70,94 ± 0,36% (jam ke 72), sedangkan kontrol adalah 68,95 ± 0,27% (jam ke 0) dan 71,08 ± 0,32% (jam ke 72). Nilai aw
bandeng presto yang direndam kitosan 0,1% adalah 0,982 ± 0,001 (jam ke 0) dan 0,963 ± 0,001 (jam ke 72), sedangkan kontrol adalah 0,980 ± 0,001 (jam ke 0) dan 0,964 ± 0,001 (jam ke 72). Hasil pengamatan kadar air dan nilai aw menunjukkan
bahwa bandeng presto adalah produk yang memiliki kandungan air yang tinggi dan berpotensi sebagai media yang baik bagi pertumbuhan bakteri.
Hasil pengujian aktivitas antibakteri memperlihatkan kombinasi kitosan 0,05% dengan kalium sorbat 0,05%, natrium benzoat 0,05% maupun ekstrak
© Hak Cipta milik IPB, tahun 2008 Hak Cipta dilindungi Undang-undang
1. Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumber.
a. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik atau tinjauan suatu masalah.
b. Pengutipan tidak merugikan kepentingan yang wajar IPB. 2. Dilarang mengumumkan dan memperbanyak sebagian atau seluruh
KOMBINASI KITOSAN DENGAN KALIUM SORBAT,
NATRIUM BENZOAT DAN EKSTRAK TERUNG PUNGO
(
Solanum
sp.) TERHADAP AKTIVITAS ANTIBAKTERI DAN
DAYA AWET BANDENG PRESTO
BAGUS FAJAR PAMUNGKAS
Tesis
sebagai salah satu syarat untuk memperoleh gelar Magister Sains pada
Program Studi Teknologi Hasil Perairan
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
Judul Tesis : Kombinasi Kitosan dengan Kalium Sorbat, Natrium Benzoat dan Ekstrak Terung Pungo (Solanum sp.) terhadap Aktivitas Antibakteri dan Daya Awet Bandeng Presto
Nama : Bagus Fajar Pamungkas NIM : C351050041
Disetujui Komisi Pembimbing
Dr. Ir. Linawati Hardjito, M.Sc Dr. Ir. Joko Santoso, M.Si
Ketua Anggota
Diketahui
Ketua Program Studi Teknologi Hasil Perairan
Dekan Sekolah Pascasarjana
Dr. Ir. Sri Purwaningsih, M.S Prof. Dr. Ir. Khairil Anwar Notodiputro, M.S
PRAKATA
Puji dan syukur penulis panjatkan kepada Allah SWT atas segala rahmat dan karunia-Nya sehingga karya ilmiah ini berhasil diselesaikan. Shalawat serta salam penulis sampaikan kepada Rasulullah Muhammad SAW beserta sahabat dan pengikutnya. Laporan tesis ini berjudul Kombinasi Kitosan dengan Kalium Sorbat, Natrium Benzoat dan Ekstrak Terung Pungo (Solanum sp.) terhadap Aktivitas Antibakteri dan Daya Awet Bandeng Presto. Penulis mengucapkan terima kasih kepada :
1. Ibu Dr. Ir. Linawati Hardjito, M.Sc sebagai ketua komisi pembimbing yang bersedia membimbing dan sekaligus mendanai sebagian besar penelitian ini. 2. Bapak Dr. Ir. Joko Santoso, M.Si sebagai anggota komisi pembimbing yang
telah memberikan semangat, saran dan bimbingan selama penelitian dan penyusunan tesis ini.
3. Bapak Dr. Ir. Nugraha Edhi Suyatma, DEA sebagai dosen penguji luar komisi yang telah memberikan masukan dan saran dalam tesis ini.
4. Rektor Universitas Mulawarman dan Dekan Fakultas Perikanan dan Ilmu Kelautan Unmul yang telah memberikan rekomendasi tugas belajar.
5. Isteri tercinta Ita Zuraida, dan Hafidz Zufar Faiz, buah hati kami yang memberikan inspirasi dan semangat untuk menyelesaikan tesis ini. Ibu, Bapak, Mertua dan Kakak-kakak atas segala doa, bantuan dan pengertiannya. 6. Sahabat-sahabatku di THP dan adik-adikku di Laboratorium Bioteknologi
Hasil Perairan atas bantuan dan kerjasama yang solid.
7. Semua pihak yang turut berperan dalam penelitian dan penyusunan tesis ini. Akhirnya penulis hanya dapat memohon agar Allah SWT membalas semua budi baik yang telah diberikan dan semoga penelitian ini memberikan manfaat bagi yang memerlukannya.
Bogor, Agustus 2008
RIWAYAT HIDUP
Penulis lahir di Samarinda, tanggal 4 Januari 1980 sebagai anak bungsu dari empat bersaudara keluarga Bapak Marsono dan Ibu Hj. Nurlianti. Saat ini penulis telah menikah dengan Ita Zuraida dan dikaruniai seorang putra bernama Hafidz Zufar Faiz.
Penulis menyelesaikan pendidikan sarjana (S1) pada Program Studi Teknologi Hasil Perikanan, Jurusan Perikanan, Fakultas Pertanian, Universitas Gadjah Mada pada tahun 2003. Tahun 2005, penulis mendapat tugas belajar dari Universitas Mulawarman untuk melanjutkan pendidikan magister (S2) dengan mengambil Program Studi Teknologi Hasil Perairan, Sekolah Pascasarjana, Institut Pertanian Bogor. Beasiswa pendidikan pascasarjana diperoleh dari BPPS Dikti, Departemen Pendidikan Nasional Republik Indonesia.
xii DAFTAR ISI
Halaman
DAFTAR TABEL ... xiv
DAFTAR GAMBAR ... xv
DAFTAR LAMPIRAN ... xvi
1. PENDAHULUAN 1.1. Latar Belakang ... 1
1.2. Perumusan Masalah ... 2
1.3. Tujuan dan Manfaat ... 3
1.4. Hipotesis ... 3
2. TINJAUAN PUSTAKA 2.1. Deskripsi dan Karakteristik Kitosan ... 4
2.2. Kitosan sebagai Antibakteri dan Antioksidan ... 5
2.2.1. Aktivitas antibakteri pada kitosan dan mekanismenya ... 5
2.2.2. Aktivitas antioksidan pada kitosan dan mekanismenya ... 7
2.3. Kombinasi Kitosan dengan Bahan Lain sebagai Bahan Antibakteri .. 10
2.4. Keamanan Kitosan ... 12
2.5. Bahan Pengawet Kimiawi ... 13
2.5.1. Asam sorbat ... 14
2.5.2. Asam benzoat ... 15
2.6. Ekstrak Terung Pungo (Solanum sp.) sebagai Bahan Antibakteri ... 15
2.7. Bandeng Presto ... 16
3. METODOLOGI 3.1. Waktu dan Tempat Penelitian ... 17
3.2. Bahan dan Alat ... 17
3.3. Tahapan Penelitian ... 18
3.3.1. Penelitian tahap I: pengujian aktivitas antibakteri ... 18
3.3.2. Penelitian tahap II: aplikasi perlakuan bahan antibakteri terbaik pada pengawetan bandeng presto ... 19
3.4. Prosedur Analisis ... 21
3.4.1. Jumlah bakteri total (Fardiaz 1993) ... 21
3.4.2. Nilai pH (AOAC 1995) ... 21
3.4.3. Nilai TVB (AOAC 1995)... 22
3.4.5. Kadar air (AOAC 1995) ... 23
3.4.6. Nilai aw (water activity) ... 23
3.5. Analisis Statistik ... 24
4. HASIL DAN PEMBAHASAN 4.1. Karakteristik Kitosan ... 25
4.2. Aktivitas Antibakteri pada Kitosan dan Kombinasinya dengan Kalium Sorbat, Natrium Benzoat dan Ekstrak Solanum sp. ... 26
4.3. Penggunaan Kitosan terhadap Daya Awet Bandeng Presto ... 30
4.3.1. Jumlah bakteri total dan nilai pH ... 30
4.3.2. Nilai TVB ... 33
4.3.3. Nilai TBA ... 35
4.3.4. Kadar air ... 39
4.3.5. Nilai aw ... 40
5. KESIMPULAN DAN SARAN 5.1. Kesimpulan ... 42
5.2. Saran ... 42
DAFTAR PUSTAKA ... 43
xiv
DAFTAR TABEL
DAFTAR GAMBAR
Halaman
1. Struktur kimia selulosa, kitin dan kitosan ... 4
2. Diagram alir pengujian aktivitas antibakteri ... 19
3. Diagram alir aplikasi bahan antibakteri terbaik pada bandeng presto ... 20
4. Hasil pengujian aktivitas antibakteri ... 27
5. Model regresi waktu penyimpanan bandeng presto terhadap perubahan jumlah bakteri ... 31
6. Model regresi waktu penyimpanan bandeng presto terhadap perubahan nilai pH ... 33
7. Perubahan nilai TVB pada bandeng presto ... 34
8. Perubahan nilai TBA pada bandeng presto ... 36
9. Perubahan kadar air pada bandeng presto ... 39
xvi
DAFTAR LAMPIRAN
Halaman 1. Hasil perhitungan jumlah bakteri total pada pengujian aktivitas
antibakteri ... 50
2. Hasil perhitungan jumlah bakteri total bandeng presto ... 56
3. Hasil perhitungan nilai pH bandeng presto ... 60
4. Hasil perhitungan nilai TVB bandeng presto ... 61
5. Hasil perhitungan nilai TBA bandeng presto ... 62
6. Hasil perhitungan kadar air bandeng presto ... 63
1. PENDAHULUAN
1.1. Latar Belakang
Kitosan dan senyawa turunannya diketahui memiliki aktivitas antibakteri (Shahidi et al. 1999). Aktivitas antibakteri pada kitosan telah dilaporkan mampu menghambat pertumbuhan berbagai jenis bakteri seperti Escherichia coli dan
Staphylococcus aureus (Darmadji dan Izumimoto 1994; Tsai et al. 2002; Rao et al. 2005), Pseudomonas aeruginosa, Vibrio parahaemolyticus dan Vibrio cholerae (Tsai et al. 2002), serta Bacillus cereus (Devlieghere et al. 2004; Rao et al. 2005). Sifat-sifat kitosan untuk membentuk film dan antimikroba menjadi sumber yang potensial sebagai bahan pelapis dan pengawet produk pangan alami (No et al. 2007).
Kitosan memiliki sifat biocompatible, bioantigenik, biofungsional dan tidak toksik, sehingga telah diijinkan sebagai bahan tambahan pangan di Jepang sejak 1983 dan Korea sejak 1995 (No et al. 2007). Sejak tahun 2005, kitosan dari kulit udang diakui sebagai GRAS (generally recognized as safe) oleh US-FDA (US FDA 2008). Berdasarkan SK Badan POM RI No. HK.00.05.52.6581 tahun 2007, kitosan diperbolehkan untuk digunakan pada produk pangan di Indonesia.
Kitosan berpotensi sebagai bahan pengawet untuk memperpanjang umur simpan produk-produk pangan (Rhoades dan Roller 2000). Adanya aktivitas antibakteri pada kitosan telah diaplikasikan untuk memperpanjang umur simpan produk pangan, seperti daging (Darmadji dan Izumimoto 1994; Sagoo et al.
2002a; Rao et al. 2005; Kanatt et al. 2008), sayur-sayuran dan buah-buahan (Devlieghere et al. 2004; Park et al. 2005), serta ikan dan produk makanan laut (Skonberg 2000; Jeon et al. 2002;Tsai et al. 2002; Sathivel 2005).
2
antibakteri lainnya dalam pengawetan caviar. Sagoo et al. (2002b) melaporkan kemampuan kitosan dan natrium benzoat untuk menghambat pertumbuhan khamir. Penambahan lisosim pada film kitosan dilaporkan dapat meningkatkan aktivitas antibakteri (Park et al. 2004a; Duan et al. 2007). Zivanovich et al. (2005) melakukan penambahan lemak esensial pada film kitosan untuk meningkatkan daya simpan sosis panggang
Permasalahan dari kitosan sebagai pengawet pangan adalah daya awet yang masih rendah terutama sebagai alternatif pengganti bahan kimia yang dilarang seperti formalin. Darmadji dan Izumimoto (1994) melaporkan jumlah total bakteri pada daging yang ditambahkan kitosan 1% dan disimpan pada suhu 30 oC telah mencapai 7,32 log cfu/g pada pengamatan jam ke 12. Produk tahu memiliki daya awet 24 jam pada suhu kamar dengan penambahan 0,03% kitosan yang dicampur dalam air rendaman tahu (Hardjito 2006). Oleh karena itu dibutuhkan penelitian kitosan yang dikombinasikan dengan bahan lain untuk meningkatkan aktivitas antibakteri dan daya awetnya pada produk pangan.
Ada beberapa bahan sintetis seperti kalium sorbat dan natrium benzoat maupun senyawa alami seperti ekstrak terung pungo (Solanum sp.) yang diketahui memiliki aktivitas antibakteri dan diharapkan memiliki efek sinergis bila dikombinasikan dengan kitosan. Kalium sorbat dan natrium benzoat telah digunakan sebagai bahan pengawet pangan yang diijinkan Pemerintah (Depkes 1999). Selain itu, ekstrak terung pungo (Solanum sp.) yang merupakan tanaman pesisir telah dilaporkan mengandung senyawa aktif antibakteri (Haswirna 2006).
Upaya untuk meningkatkan aktivitas antibakteri pada kitosan yang dikombinasikan dengan bahan lain masih menarik untuk diteliti. Penelitian ini bertujuan mencari aktivitas antibakteri terbaik dari kitosan dan kombinasinya dengan kalium sorbat, natrium benzoat, dan ekstrak Solanum sp. Perlakuan yang memiliki aktivitas antibakteri terbaik selanjutnya diaplikasikan pada produk bandeng presto untuk mengetahui daya awetnya.
1.2. Perumusan Masalah
diperlukan upaya mencari alternatif lain yang aman. Kitosan memiliki aktivitas antibakteri dan diharapkan dapat sebagai alternatif bahan pengawet yang aman. Upaya meningkatkan aktivitas antibakteri pada kitosan dengan menambahkan bahan antibakteri lainnya, baik yang berasal dari bahan kimia sintetis yang diijinkan pemerintah maupun bahan aktif alami dari tanaman pesisir menarik untuk diteliti dan diharapkan dapat diaplikasikan sebagai bahan pengawet produk pangan terutama pada produk hasil perikanan.
1.3. Tujuan dan Manfaat
Tujuan dari penelitian ini adalah:
1). Mencari aktivitas antibakteri terbaik dari kitosan dan kombinasinya dengan kalium sorbat, natrium benzoat dan ekstrak Solanum sp.
2). Mengetahui daya awet bandeng presto dengan penambahan kitosan atau kombinasinya dengan kalium sorbat, natrium benzoat dan ekstrak Solanum sp. yang memperlihatkan aktivitas antibakteri terbaik.
Manfaat penelitian ini adalah sebagai informasi mengenai alternatif bahan pengawet makanan bagi masyarakat. Penggunaan kitosan atau kombinasinya dengan kalium sorbat, natrium benzoat dan ekstrak Solanum sp. diharapkan dapat diaplikasikan sebagai bahan pengawet makanan dan menggantikan bahan kimia yang dilarang digunakan dalam makanan.
1.4. Hipotesis
Hipotesis dari penelitian ini adalah:
1). Kombinasi kitosan dengan kalium sorbat, natrium benzoat dan ekstrak
Solanum sp. akan meningkatkan aktivitas antibakteri.
2. TINJAUAN PUSTAKA
2.1. Deskripsi dan Karakteristik Kitosan
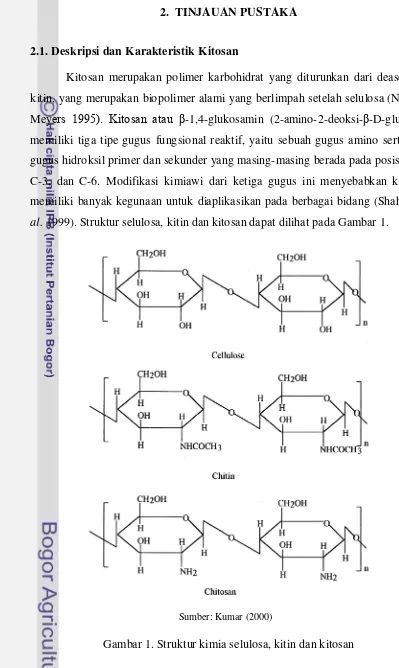
Kitosan merupakan polimer karbohidrat yang diturunkan dari deasetilasi kitin, yang merupakan biopolimer alami yang berlimpah setelah selulosa (No dan Meyers 1995). Kitosan atau β-1,4-glukosamin (2-amino-2-deoksi-β-D-glukosa) memiliki tiga tipe gugus fungsional reaktif, yaitu sebuah gugus amino serta dua gugus hidroksil primer dan sekunder yang masing-masing berada pada posisi C-2, C-3, dan C-6. Modifikasi kimiawi dari ketiga gugus ini menyebabkan kitosan memiliki banyak kegunaan untuk diaplikasikan pada berbagai bidang (Shahidi et al. 1999). Struktur selulosa, kitin dan kitosan dapat dilihat pada Gambar 1.
Gambar 1. Struktur kimia selulosa, kitin dan kitosan
Oleh karena sifat-sifat fungsional yang dimilikinya, kitosan dapat diaplikasikan sebagai bahan antimikroba, edible film, bahan tambahan pangan, perbaikan kualitas gizi pangan, pemulihan bahan-bahan padat dari limbah pengolah makanan, pemurni air dan aplikasi lainnya (Shahidi et al. 1999). Kitosan sebagai antimikroba bersifat bakterisidal (Darmadji dan Izumimoto 1994; Tsai et al. 2002) dan fungisidal (Sagoo et al. 2002b; Park et al. 2005). Kitosan sebagai bahan tambahan pangan antara lain berfungsi sebagai pengemulsi, menstabilkan warna dan bahan pengemulsi (Knorr 1982; Knorr 1983; Cho et al. 1998), bahan pengendali tekstur, penstabil dan pengental (Shahidi et al. 1999), antioksidan (Darmadji dan Izumimoto 1994; Kamil et al. 2002; Kim dan Thomas 2007) serta bahan penjernih dan penurun tingkat keasaman pada jus buah-buahan (Devlieghere et al. 2004; Park et al. 2005). Kitosan dilaporkan bersifat hipokolesterolemik dan hipolipidemik (Winterowd dan Standford 1995) dan bahan enkapsulasi mikronutrien (Han et al. 2008).
2.2. Kitosan sebagai Antibakteri dan Antioksidan
2.2.1. Aktivitas antibakteri pada kitosan dan mekanismenya
Kitosan merupakan bahan pengawet pangan alami yang potensial karena memiliki kemampuan aktivitas antimikroba terhadap mikroba perusak makanan maupun patogen, baik bakteri, khamir dan jamur (Sagoo et al. 2002a). Sifat-sifat penting kitosan antara lain disebabkan memiliki muatan positif dalam larutan asam, dimana gugus amina pada molekul kitosan mengikat proton sesuai dengan persamaan reaksi: kitosan-NH2 + H3O+ ↔ kitosan-NH3+ + H2O, dimana
kitosan-NH3+ juga memiliki aktivitas antimikroba terhadap berbagai
mikroorganisme (Rhoades dan Rastall 2006).
Kitosan dilaporkan mampu menghambat pertumbuhan berbagai jenis bakteri seperti Escherichia coli dan Staphylococcus aureus (Darmadji dan Izumimoto 1994; Tsai et al. 2002; Rao et al. 2005), Pseudomonas aeruginosa,
Vibrio cholerae dan V. parahaemolyticus (Tsai et al. 2002), serta Bacillus cereus
(Devlieghere et al. 2004; Rao et al. 2005). Yadav dan Bhise (2000) melaporkan bahwa kitosan efektif menghambat pertumbuhan Salmonella enterica var.
6
Beberapa penelitian mengenai penggunaan kitosan sebagai bahan pengawet pangan telah dilaporkan. Rhoades dan Roller (2000) melaporkan bahwa jus apel yang telah dipasteurisasi dan disimpan pada suhu 7 oC dan ditambahkan 0,3 g kitosan/l dapat mencegah pertumbuhan khamir selama 13 hari pengamatan. Oh et al. (2000) melaporkan penggunaan kitosan untuk menghambat pertumbuhan bakteri perusak pada mayonis yaitu Lactobacillus plantarium, L. fructivorans dan
Zygosaccharomyces bailii. Hasilnya menunjukkan bahwa penambahan kitosan pada semua konsentrasi perlakuan (100, 500, 1000 ppm) yang disimpan pada suhu 25 oC mampu mempertahankan stabilitas emulsi mayonis sampai 10 minggu.
Aplikasi kitosan untuk memperpanjang umur simpan produk perikanan juga telah dilakukan. Skonberg (2000) melaporkan penggunaan larutan kitosan 1,75% sebagai film pelapis untuk memperpanjang umur simpan filet ikan salmon atlantik dan ikan haddock pada suhu 5 oC. Hasilnya menunjukkan selama 7 hari pertama penyimpanan filet ikan mengindikasikan nilai TVB, pH, dan TPC yang rendah. Jeon et al. (2002) melaporkan pengaruh pelapisan kitosan dengan berat molekul yang berbeda untuk memperpanjang umur simpan filet ikan cod atlantik (Gadus morhua) dan ikan hering (Clupea harangus) yang dievaluasi selama 12 hari penyimpanan dingin (4 ± 1 oC). Hasilnya menunjukkan bahwa pelapisan kitosan pada filet ikan dapat mereduksi oksidasi lemak kitosan dan kerusakan kimiawi seperti basa nitrogen dan hipoksantin. Tsai et al. (2002) juga melaporkan pelapisan kitosan dengan konsentrasi yang bervariasi (0,2%; 0,5%; 1,0%) pada filet salmon yang disimpan pada suhu 4 oC. Hasilnya menunjukkan bahwa semakin tinggi konsentrasi kitosan yang diberikan pada filet ikan, lebih efektif menghambat laju pertumbuhan bakteri psikrotropik dan bakteri mesofilik serta pembentukan basa-basa volatil dibandingkan kontrol setelah 9 hari penyimpanan.
Shahidi et al. (1999) menjelaskan bahwa mekanisme kerja kitosan dalam menghambat pertumbuhan mikroba adalah adanya interaksi antara muatan positif (gugus NH3+) pada molekul kitosan dengan muatan negatif pada membran sel
Tsai dan Su (1999) menjelaskan bahwa kitosan berinteraksi dengan permukaan sel bakteri dimana kemungkinan adanya kekuatan elektrostatis. Setelah terjadi pengikatan, perubahan dalam permeabilitas membran menyebabkan pecahnya komponen intraseluler seperti glukosa dan laktat dehidrogenase (LDH) yang akhirnya menyebabkan kematian sel. Sejumlah proton bermuatan positif (NH3+) pada kitosan dan elektronegativitas permukaan sel
bakteri mempengaruhi interaksi ini. Russel (2005) menjelaskan bahwa bahan-bahan pengkelat logam diketahui dapat meningkatkan permeabilitas membran luar pada bakteri Gram-negatif, dimana pengkelatan kation anorganik seperti Mg2+ akan mengekstrak lipopolisakarida, protein maupun lipida.
Shahidi et al. (1999) juga menjelaskan bahwa kitosan bertindak sebagai bahan pengikat lemak, dan menghambat berbagai aktivitas enzim. Selain itu, pengikatan kitosan dengan DNA dan penghambatan sintesis mRNA terjadi melalui penetrasi kitosan yang memiliki berat molekul rendah pada nuclei
mikroorganisme menyebabkan terhambatnya sintesis mRNA dan protein. Russel (2005) menjelaskan bahwa membran sitoplasma kaya akan enzim yang umumnya berasosiasi dengan rantai transpor elektron yang digunakan pada proton sebagai kekuatan transpor aktif. Beberapa bahan antibakteri akan berinteraksi dengan gugus thiol (sulfihidril, -SH) yang terdapat di dalam struktur protein dan enzim. Gugus thiol yang diturunkan dari residu sistein memiliki peranan penting pada aktivitas sejumlah enzim dan gugus ini bereaksi dengan bahan antimikroba menyebabkan inaktivasi sel bakteri. Rusaknya membran sitoplasma oleh bahan antibakteri umumnya disebabkan oleh lepasnya komponen intraseluler, dimana pada awalnya ion kalium (K+) akan terlepas dilanjutkan fosfat anorganik (Pi), asam-asam amino, kemudian membesarnya berat molekul bahan-bahan (seperti RNA/DNA) sebagai indikasi kerusakan sel bakteri.
2.2.2. Aktivitas antioksidan pada kitosan dan mekanismenya
8
penyimpanan selama 3 hari pada suhu 4 oC. Shahidi et al. (2002) melaporkan bahwa kitosan dengan konsentrasi yang rendah (50-200 ppm), mampu melindungi ikan masak terhadap oksidasi dan timbulnya bau (off-flavor) selama penyimpanan dan kitosan dengan viskositas 14 Cp pada konsentrasi 200 ppm sudah sangat efek-tif dalam mengendalikan oksidasi lipida pada sampel ikan cod. Kim dan Thomas (2007) meneliti nilai TBA pada ikan salmon yang ditambahkan kitosan pada kon-sentrasi 0,2%, 0,5% dan 1% (w/v) dan disimpan selama 15 hari pada suhu 4 oC. Hasilnya memperlihatkan bahwa nilai TBA tertinggi terdapat pada ikan salmon yang tidak diberi perlakuan (kontrol), sebaliknya nilai TBA terendah terdapat pa-da ikan salmon yang diberi kitosan. Hasil ini membuktikan bahwa pemberian ki-tosan mampu menghambat laju oksidasi lipida pada ikan salmon. Yen et al.
(2008) melaporkan kitosan yang berasal dari kepiting memiliki sifat-sifat antiok-sidan yang baik, terutama pada aktivitas antiokantiok-sidan, kemampuan mengikat gugus radikal hidroksil, dan kemampuan mengkelat ion-ion ferous.
Yen et al. (2008) melaporkan dengan menggunakan metode konjugasi diena, kitosan yang berasal dari kepiting memperlihatkan aktivitas antioksidan, yaitu sekitar 58,3–70,2% pada konsentrasi 1 mg/ml dan 79,9–85,2% pada 10 mg/ml. Meningkatnya konsentrasi kitosan akan meningkatkan kemampuan aktivitas antioksidan. Kemampuan kitosan dalam mengikat DPPH (1,1-diphenyl -2-picrylhydrazyl) juga telah dilaporkan. Lin dan Chou (2004) melaporkan bahwa turunan kitosan disakarida N-alkilasi pada konsentrasi 0,1 mg/ml memperlihatkan kemampuan mengikat radikal DPPH yang tinggi yaitu 80–95%, namun Xing et al.
(2005) melaporkan bahwa turunan kitosan sulfat 0,05 mg/ml kurang efektif mengikat radikal DPPH, dan Yen et al. (2008) melaporkan kitosan yang berasal dari kepiting kurang efektif mengikat radikal DPPH, yaitu sekitar 46,4-52,3%. Hal ini menunjukkan bahwa kemampuan scavenging pada kitosan meningkat setelah proses N-alkilasi disakarida dan menurun setelah proses sulfasi (Yen et al. 2008)
stabil dan menjadi produk yang tidak radikal. Antioksidan sekunder lebih mengarah kepada pencegahan terhadap proses oksidasi, dimana antioksidan ini bekerja untuk memperlambat laju oksidasi dengan beberapa aksi, namun tidak dapat mengubah radikal bebas menjadi produk yang lebih stabil. Mekanisme kerja antioksidan sekunder antara lain dapat mengkelat logam-logam yang merupakan pro-oksidan dan mendeaktivasi-nya, menyediakan hidrogen untuk antioksidan primer, mendekomposisi hidroperoksida menjadi jenis yang tidak radikal, deaktivasi singlet oksigen, mengabsorbsi radiasi sinar ultraviolet, atau bertindak sebagai pengikat oksigen (Reische et al. 2002).
Berdasarkan mekanisme antioksidan tersebut, kitosan dilaporkan dapat bertindak sebagai antioksidan primer maupun antioksidan sekunder (Yen et al.
2008). Park et al (2004b) menjelaskan bahwa kitosan mampu mengurangi berbagai radikal bebas yang bereaksi dengan gugus nitrogen pada posisi C-2. Kim dan Thomas (2007) menyatakan bahwa aktivitas pengikatan radikal bebas oleh kitosan dipengaruhi oleh konsentrasi dan berat molekulnya. Aktivitas pengikatan radikalpada kitosan mengalami peningkatan pada konsentrasi 0,2% - 1%, namun dilaporkan menurun pada berat molekul tinggi (120 kDa). Mekanisme antioksidan sekunder pada kitosan adalah adanya kemampuan dalam mengkelat logam dan mengikat lipida.
Xie et al. (2001) menjelaskan bahwa mekanisme pengikatan radikal bebas oleh kitosan berhubungan dengan fakta bahwa gugus radikal OH• dari proses oksidasi lipida dapat bereaksi dengan ion hidrogen dari gugus ion amonium (NH3+) pada kitosan membentuk suatu molekul yang lebih stabil. Aktivitas
pengikatan oleh kitosan terhadap gugus radikal OH• dapat terjadi sebagai berikut: 1. Gugus hidroksil di dalam unit polisakarida pada kitosan dapat bereaksi
dengan OH• oleh tipe reaksi pemutusan gugus atom H.
2. Gugus OH• dapat bereaksi dengan gugus amino bebas (NH2) membentuk
radikal molekul yang stabil.
3. Gugus NH2 dapat membentuk gugus amonium NH3+ dengan mengabsorbsi
10
pengkelatan Cu2+ oleh kitosan terjadi pada gugus hidroksil di C6 dan gugus amino
di C2, dan mekanisme serupa juga terjadi pada pengkelatan ion ferous (Fe2+) oleh
kitosan. Qin (1993) mengindikasikan bahwa kemampuan mengkelat ion pada kitosan dipengaruhi oleh derajat deasetilasi, dimana keberadaan gugus asetil akan melemahkan aktivitas pengkelatan pada kitosan. Transisi ion-ion logam dapat menginisiasi peroksidasi lipida dan memulai suatu reaksi rantai yang menyebabkan kerusakan citarasa dan bau dalam makanan. Oleh karena ion ferous sangat efektif sebagai pro-oksidan di dalam sistem makanan, maka kemampuan mengkelat ion ferous oleh kitosan akan bermanfaat bila diformulasikan dalam makanan (Yen et al. 2008).
Kemampuan kitosan mengikat lipida juga dapat berperan dalam menghambat proses oksidasi. Hennen (1996) menjelaskan bahwa mekanisme kitosan mengikat lipida belum dipahami secara jelas, tetapi ada dua mekanisme dasar yang berperan. Mekanisme pertama melibatkan daya tarik muatan yang berlawanan, dimana muatan positif (NH3+) pada kitosan menarik muatan negatif
(ROO-) pada asam lemak. Mekanisme kedua adalah proses penjerapan lipida oleh kitosan dalam suatu jaringan, dimana kitosan memerangkap di sekitar droplet lemak dan mencegah lipida diuraikan oleh enzim-enzim lipida.
2.3. Kombinasi Kitosan dengan Bahan Lain sebagai Bahan Antibakteri Beberapa penelitian mengenai kitosan yang dikombinasikan dengan bahan lain untuk meningkatkan aktivitas antimikroba telah dilaporkan. Keuntungan dari mengkombinasikan kitosan dengan bahan antimikroba lainnya adalah dapat digunakan untuk mengawetkan makanan terutama terhadap kontaminasi bakteri perusak (Cagry et al. 2004).
Leuconostoc lactis, Streptococcus pyogenes, Saccharomyces cerevisiae, Candida
utilis, Cryptococcus laurentii, Rhodotorula rubra, dan Torulopsis candida.
Ouattara et al. (2000) mengkaji peningkatan efektivitas film kitosan yang memiliki aktivitas antimikroba dengan menambahkan asam asetat, asam propionat dan asam laurat. Mereka melaporkan karakteristik film kitosan sebagai bahan antimikroba yang ditambahkan dengan bahan-bahan tersebut dan menyarankan dapat diaplikasikan pada pengawetan bahan pangan.
Kombinasi kitosan dengan asam sorbat dan bahan antibakteri lainnya (tidak disebutkan) untuk memperpanjang umur simpan caviar (telur ikan salmon dan ikan sejenis) telah dipatenkan di Rusia. Bykova et al. (2001) menggunakan campuran dari 0,05-0,1% kitosan, 0,1% asam sorbat dan 0,3-0,5% antibac yang diklaim mampu meningkatkan aktivitas antimikroba, antioksidasi dan memperpanjang umur simpan dari caviar.
Sagoo et al. (2002b) meneliti aktivitas antimikroba dari kombinasi kitosan dengan natrium benzoat terhadap khamir perusak yaitu Saccharomyces exiguus, S.
ludwigii dan Torulaspora delbrueckii. Hasilnya menunjukkan bahwa kitosan 0,005% yang dikombinasikan natrium benzoat 0,025% mampu menghambat pertumbuhan khamir hampir dua kali dibandingkan dengan masing-masing bahan diuji tunggal, dimana dapat menghambat pertumbuhan khamir sekitar log 1-2 sampai log 2-4, tergantung pada pH dan jenis organismenya.
Park et al. (2004a) melaporkan sifat-sifat antimikroba dari kombinasi kitosan dengan lisosim. Mereka menggabungkan larutan kitosan 2% dengan larutan lisosim 10% dengan rasio pencampuran 0%, 20%, 60%, dan 100% (w lisosim/w kitosan). Hasilnya adalah kecenderungan penghambatan sinergis ada pada perlakuan 60% yang dapat mengurangi jumlah Escherichia coli dan
Streptococcus faecalis masing-masing mencapai 3,8 log cfu/g dan 2,7 log cfu/g. Duan et al. (2007) melaporkan kitosan yang ditambahkan 60% lisosim (per berat kering kitosan) untuk digunakan sebagai film pelapis pada keju (mozarella cheese). Keju yang telah dilapisi film kitosan-lisosim kemudian diinokulasi dengan Listeria monocytogens, Escherichia coli dan Pseudomonas fluorescens
12
monocytogenes, E. coli dan P. fluorescens masing-masing 0,32-1,35 log cfu/g, 0,43-1,25 log cfu/g dan 0,40-1,40 log cfu/g pada keju.
Zivanovich et al. (2003) meneliti penggunaan kitosan dan minyak esensial sebagai biopestisida untuk mempertahankan mutu buah stroberi, arbei, dan anggur pascapanen. Buah-buah tersebut diberi larutan pembentuk lapisan yang dibuat dari kombinasi kitosan 1% dan minyak esensial 4%, lalu dikemas dalam kantong
poliethylene dan disimpan pada suhu 4 oC. Hasilnya menunjukkan semua buah yang diberi pelapisan kitosan-minyak esensial memperlihatkan reduksi mikroba yang sempurna dengan tidak ada pertumbuhan jamur selama 18 hari penyimpanan. Pelapisan kitosan pada buah anggur, arbei dan stroberi mampu mencegah pertumbuhan jamur masing-masing 9 hari, 6 hari dan 0 hari masa penyimpanan, sedangkan buah-buah yang tidak diberi perlakuan memperlihatkan pertumbuhan jamur yang tinggi sejak diawal percobaan. Lebih lanjut, Zivanovich
et al. (2005) melakukan penambahan lemak esensial pada film kitosan untuk meningkatkan umur simpan sosis panggang. Mereka melaporkan bahwa kombinasi asam lemak oregano 1% dan 2% pada kitosan dapat mengurangi jumlah Listeria monocytogenes sampai 3,6 log cfu/g dan 4 log cfu/g.
2.4. Keamanan Kitosan
Arai (1968), diacu dalam Winterowd dan Sandford (1995) telah melaporkan nilai keamanan pada kitosan dengan menentukan nilai LD50-nya,
yaitu > 17,9 g/hari/kg berat badan tikus. Landes dan Bough (1976) diacu dalam Winterowd dan Sandford (1995) melaporkan nilai LD50 kitosan adalah 16,5
g/hari/kg berat badan tikus dan menganjurkan konsentrasi kitosan yang diberikan adalah kurang dari 5% dari total makanan yang dikonsumsi karena tidak ditemukan efek samping yang merugikan.
Hennen (1996) menjelaskan faktor keamanan kitosan dengan nilai LD50 16
g/hari/kg berat badan tikus. Tikus bukan manusia, sehingga untuk tujuan keamanan, data yang diperoleh dari tikus dibagi 12 untuk memperoleh nilai ekuivalen pada manusia, sehingga nilai LD50 relatif pada manusia adalah 1,33
menjadi toksik bagi orang tersebut bila mengkonsumsi > 90 g/hari, namun untuk lebih aman lagi, jumlah tersebut dihitung dibawah tingkat 10% yaitu 9 g/hari.
Koide (1998) menjelaskan beberapa efek samping yang dapat terjadi bila mengkonsumsi kitosan. Kitosan adalah suatu serat yang membentuk gel dalam lambung yang bersifat asam. Kitosan memiliki sifat dapat mengikat lipida dan mineral, sehingga berpotensi pula mengikat vitamin larut lemak seperti A, D, E dan K. Defisiensi vitamin tersebut dalam tubuh dapat merugikan dalam jangka panjang. Kitosan dapat mempengaruhi metabolisme tulang karena mengurangi kalsium dan mengabsorbsi vitamin D, sehingga tidak dianjurkan dikonsumsi oleh wanita yang sedang hamil.
2.5. Bahan Pengawet Kimiawi
Antimikroba makanan adalah bahan yang memiliki kemampuan menghambat mikroorganisme perusak sehingga diharapkan dapat memperpanjang umur simpan dan mempertahankan mutu makanan. Penggunaan antimikroba pada makanan disebut juga sebagai bahan pengawet makanan, meskipun istilah bahan pengawet sering termasuk bahan yang memiliki sifat antioksidan (Davidson dan Harrison 2002)
14
sorbat dan asam benzoat diharapkan dapat memberikan efek sinergis dalam memperpanjang umur simpan makanan bila dikombinasikan dengan kitosan. 2.5.1. Asam sorbat
Asam sorbat (CH3-CH=CH-CH=CH-COOH) tergolong asam lemak
monokarboksilat yang berantai lurus dan mempunyai ikatan tidak jenuh (-diena). Bentuk sorbat yang digunakan umumnya adalah garam Na- dan K- sorbat digunakan untuk menghambat pertumbuhan kapang dan bakteri. Sorbat aktif pada pH di atas 6,5 dan aktivitasnya menurun dengan meningkatnya pH (Winarno 2004). Garam kalium sorbat memiliki kelarutan yang lebih besar daripada asamnya, sehingga bentuk garamnya lebih sering digunakan. Garam ini mempunyai aktivitas yang hampir sama dengan bentuk asamnya, karena pada produk perikanan, garam ini akan dihidrolisis menjadi asam sorbat yang aktif (Germinder 1959, diacu dalam Jenie et al. 1993).
Mekanisme asam sorbat dalam mencegah pertumbuhan mikroba adalah dengan mencegah kerja enzim dehidrogenase terhadap asam lemak. Struktur -diena pada asam sorbat dapat mencegah oksidasi asam lemak oleh enzim tersebut. Sebaliknya hewan tingkat tinggi dapat memetabolisasi asam sorbat seperti asam lemak biasa (Winarno 2004). Daya kerja efektif sorbat adalah pada pH 6-6,5 (Stophfort et al. 2005).
Konsentrasi penghambatan mikroba yang efektif dari asam dan garam sorbat umumnya sekitar 0,05-0,3%. Bakteri yang dihambat pertumbuhannya antara lain Acetobacter, Achromobacter, Clostridium, Escherichia, Pseudomonas, Proteus, Salmonella, Staphylococcus dan Vibrio. Konsentrasi penghambatan ini masih di bawah nilai LD50 untuk sorbat, yaitu pada kisaran 4,2-10,5 g/kg berat
badan (Stophfort et al. 2005). Depkes (1999) menentukan batas maksimum asam sorbat dan bentuk garamnya yang boleh digunakan adalah 3 g/kg untuk sediaan keju olahan dan 1 g/kg untuk keju dan margarin.
Kalium sorbat telah diteliti secara luas sebagai bahan antimikroba yang digunakan untuk memperpanjang umur simpan produk hewani dengan menghambat pertumbuhan patogen (Elliot et al. 1985, diacu dalam Jenie et al.
selama 1 menit dan dikemas CO2 yang disimpan pada suhu 4 oC memiliki umur
simpan sampai 15 hari. Waliszewski (2000) menggunakan kombinasi potasium sorbat, asam askorbat, dan asam sitrat untuk memperpanjang umur simpan ikan tilapia pada suhu -10 oC. Hasilnya menunjukkan tilapia yang tidak diberi bahan pengawet memiliki kadar hipoksantin yang telah melewati batas konsentrasi, sedangkan yang diberi tambahan bahan pengawet diketahui konsentrasi
trimethylamine, hipoksantin dan jumlah bakteri total masih pada angka yang dapat diterima setelah 63 hari penyimpanan.
2.5.2. Asam benzoat
Asam benzoat (C6H5COOH) merupakan bahan pengawet yang luas
penggunaannya dan sering digunakan pada bahan makanan yang bersifat asam. Bahan ini digunakan untuk mencegah pertumbuhan khamir dan bakteri. Benzoat efektif pada pH 2,5-4,0. Oleh karena kelarutan garamnya lebih besar maka umumnya digunakan dalam bentuk garam Na-benzoat, sedangkan di dalam bahan makanan, garam benzoat terurai menjadi bentuk efektif yaitu bentuk asam benzoat yang tidak terdisosiasi. Tubuh manusia memiliki mekanisme detoksifikasi terhadap asam benzoat, sehingga tidak terjadi penumpukan asam benzoat. Asam benzoat akan bereaksi dengan glisin menjadi asam hipurat yang akan dibuang oleh tubuh (Winarno 2004). Meskipun banyak digunakan untuk menghambat pertumbuhan jamur dan khamir, natrium benzoat dan asam benzoat juga dapat menghambat bakteri pengurai dan patogen, seperti Escherichia coli, Listeria monocytogenes, Bacillus cereus, dan Salmonella thypimurium (Cagry et al. 2004).
2.6. Ekstrak Terung Pungo (Solanum sp.) sebagai Bahan Antibakteri
Terung pungo (Solanum sp.) merupakan tanaman di daerah pesisir yang telah turun temurun digunakan sebagai obat tradisional oleh masyarakat Aceh. Tanaman ini terutama daunnya telah dimanfaatkan untuk mengobati sakit gigi. Khasiat dari tanaman ini diduga berasal dari senyawa 1,2-benzenedicarboxylic acid, bis (2-ethylhexyl) ester berdasarkan identifikasi menggunakan GC-MS dan LC-MS yang memiliki kemampuan aktivitas antibakteri (Haswirna 2006).
16
metode difusi agar dengan konsentrasi ekstrak 300 µg/paper disc memperlihatkan zona hambat terhadap pertumbuhan Escherichia coli dan Staphylococcus aureus. Meskipun Solanum sp. memperlihatkan aktivitas antibakteri, namun zona hambat yang dihasilkan masih lebih rendah dibandingkan dengan kontrol yang menggunakan kloramfenikol (Haswirna 2006).
2.7. Bandeng Presto
Jenis olahan bandeng presto atau bandeng duri lunak merupakan salah satu diversifikasi pengolahan hasil perikanan terutama sebagai modifikasi pemindangan yang mempunyai kelebihan yaitu tulang dan duri dari ekor hingga kepala menjadi lunak sehingga tidak menimbulkan gangguan pada mulut saat dimakan. Prinsip pengolahan bandeng presto adalah dengan menggunakan suhu tinggi (115-121 oC) dengan tekanan 15 psi. Suhu dan tekanan yang tinggi dapat dicapai dengan menggunakan autoclave atau pressure cooker (Hadiwiyoto dan Naruki 1999). Persyaratan mutu bandeng presto dapat dilihat pada Tabel 1.
Tabel 1. Persyaratan mutu bandeng presto berdasarkan SNI 01-4106-1996
Jenis Uji Satuan Persyaratan Mutu
a) Organoleptik
1. Berat bersih sesuai label
3. METODOLOGI
3.1. Waktu dan Tempat Penelitian
Penelitian dilakukan sejak Desember 2006 sampai dengan Nopember 2007. Pengujian aktivitas antibakteri dilakukan di Lab. Bioteknologi Hasil Perairan, pembuatan bandeng presto dilakukan di Lab. Pengolahan Hasil Perikanan dan analisis TVB dan pH dilakukan di Lab. Mikrobiologi Hasil Perairan Dep. THP FPIK IPB. Analisis TBA,
a
w dan kadar air dilakukan diLaboratorium Biokimia PAU-Pangan dan Gizi IPB.
3.2. Bahan dan Alat
Bahan-bahan yang digunakan dalam penelitian ini terdiri atas:
1). Kitosan diproduksi oleh PT Araminta Sidhakarya menggunakan teknologi dari Dep. THP FPIK IPB. Stok larutan dibuat 3%, dimana sebanyak 9 g kitosan dilarutkan dalam akuades 300 ml yang telah ditambahkan asam asetat 2%, lalu disaring untuk memisahkan partikel yang tidak terlarut.
2). Kalium sorbat dan natrium benzoat menggunakan bahan teknis yang umumnya dibeli pedagang makanan. Stok larutan yang dibuat adalah 2,5%, dimana sebanyak 125 mg bahan dilarutkan dalam 5 ml akuades.
3). Ekstrak terung pungo (Solanum sp.) diperoleh dari Lab. Bioteknologi Hasil Perairan Dep. THP FPIK IPB. Stok bahan dibuat 0,1% dengan melarutkan 1 mg bahan dalam 1 ml metanol.
4). Media nutrient broth (NB) dibuat dengan melarutkan 10 g peptone, 5 g yeast extract dan 15 g NaCl dalam 1 liter akuades pH 7, kemudian disterilisasi pada suhu 121 C selama 15 menit. Media nutrient agar (NA) dibuat sama seperti NB dengan ditambahkan bacto agar 15 g.
5). Bakteri uji yang digunakan adalah Escherichia coli dan Staphylococcus aureus diperoleh dari Lab. Bioteknologi Hasil Perairan Dep. THP FPIK IPB. 6). Ikan bandeng (Chanos sp.) segar dan bumbu-bumbu (garam, kunyit, lengkuas
18
Alat-alat yang digunakan adalah timbangan analitik, timbangan manual,
clean bench, grinder, erlenmeyer, kertas saring, hot plate stirrer, corong,
evaporator, bunsen, refrigerator, botol ekstrak, spatula, aluminium foil, tabung reaksi, gelas ukur, pipet volumetrik, mikropipet, kapas, autoclave, cawan petri, jarum ose, baki, pisau. Selain itu digunakan pula peralatan untuk pengujian kimia, antara lain cawan conway, gelas porselin, kertas pH-standar dan pH meter, aw
meter dan spektrofotometer. 3.3. Tahapan Penelitian
Penelitian dilakukan dua tahap. Tahap I adalah pengujian aktivitas antibakteri dari kitosan dan kombinasinya dengan kalium sorbat, natrium benzoat dan ekstrak Solanum sp. Tahap II adalah aplikasi perlakuan aktivitas antibakteri terbaik dari tahap I pada bandeng presto untuk mengetahui daya awetnya.
3.3.1. Penelitian tahap I: pengujian aktivitas antibakteri
Bakteri uji yang digunakan dalam pengujian aktivitas antibakteri adalah
Staphylococcus aureus dan Escherichia coli. Sebelum pengujian aktivitas antibakteri, dilakukan penyegaran terlebih dahulu pada bakteri uji. Stok bakteri yang ada dalam agar miring ditanam sebanyak 1 ose ke dalam 20 ml media cair NB pada erlenmeyer 100 ml kemudian digoyang menggunakan shaker selama 18 jam pada suhu ruang.
Gambar 2. Diagram alir pengujian aktivitas antibakteri
3.3.2. Penelitian tahap II: aplikasi perlakuan bahan antibakteri terbaik pada pengawetan bandeng presto
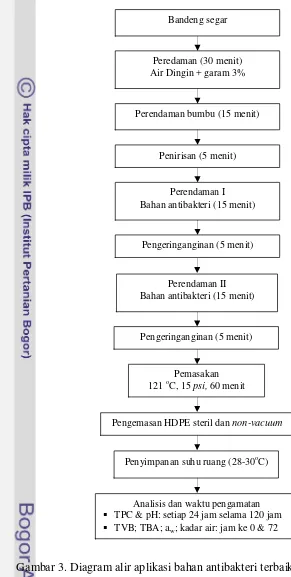
Perlakuan yang memberikan aktivitas antibakteri terbaik dari penelitian tahap I diaplikasikan pada bandeng presto untuk mengetahui daya awetnya. Prosedur pembuatan bandeng presto mengacu pada Hadiwiyoto dan Naruki (1999). Bumbu-bumbu yang digunakan adalah campuran dari garam 100 g, bawang putih 20 g, kunyit 25 g dan lengkuas 15 g yang dilarutkan dalam 1000 ml air. Daun pisang digunakan sebagai pemisah bandeng selama pemasakan agar produk tidak hancur. Pengemasan dilakukan non-vacuum menggunakan plastik jenis HDPE yang telah disterilkan. Proses pemasakan bandeng presto menggunakan autoklaf pada suhu 121 oC dan 15 psi selama 60 menit. Prosedur aplikasi perlakuan bahan antibakteri terbaik pada pengawetan bandeng presto dapat dilihat pada Gambar 3.
Media nutrient broth steril 50 ml dalam erlenmeyer 250 ml Perlakuan:
1. Kitosan 0,1% 2. Kitosan 0,05%
3. Kitosan 0,05% + Kalium sorbat 0,05% 4. Kitosan 0,05% + Natrium benzoat 0,05% 5. Kitosan 0,05% + Ekstrak Solanum sp. 20 µg/ml 6. Kalium sorbat 0,1%
7. Natrium benzoat 0,1% 8. Ekstrak Solanum sp. 20 µg/ml 9. Kontrol (tanpa perlakuan) 10.Asam asetat 0,07%
Masing-masing bahan dimasuk-kan dalam media
sesuai perlakuan
Bakteri uji diinokulasi 1 ml
Diinkubasi menggunakan shaker
pada suhu ruang selama 24 jam
20
Gambar 3. Diagram alir aplikasi bahan antibakteri terbaik pada bandeng presto
Perendaman II Bahan antibakteri (15 menit)
Pemasakan 121 oC, 15 psi, 60 menit
Pengemasan HDPE steril dan non-vacuum
Penyimpanan suhu ruang (28-30oC) Pengeringanginan (5 menit)
Analisis dan waktu pengamatan
TPC & pH: setiap 24 jam selama 120 jam
TVB; TBA; aw; kadar air: jam ke 0 & 72
Bandeng segar
Peredaman (30 menit) Air Dingin + garam 3%
Perendaman bumbu (15 menit)
Penirisan (5 menit)
Perendaman I Bahan antibakteri (15 menit)
3.4. Prosedur Analisis
3.4.1. Jumlah bakteri total (Fardiaz 1993)
Perhitungan jumlah bakteri total menggunakan metode total plate count
(TPC). Prinsip dari pengamatan ini adalah menentukan populasi bakteri yang terdapat pada bahan pangan. Prosedur kerjanya adalah sebagai berikut:
(1) Tahap persiapan. Menimbang 5 g sampel secara aseptis dan representatif, dimasukkan dalam blender jars steril dan menambahkan 45 ml NaCl 0,85% steril lalu di-blender sampai homogen. Larutan yang diperoleh adalah pengenceran 1:10.
(2) Tahap inokulasi. Mengambil 1 ml dari larutan 1:10 untuk dimasukkan dalam cawan petri steril, lalu ditambahkan larutan media plate count agar steril bersuhu 45 0C sebanyak 15 ml dan dibiarkan selama 15-20 menit sampai agar memadat. Proses ini dilakukan juga pada larutan dengan pengenceran 1:100 sampai 1:10.000.000, secara duplo.
(3) Tahap inkubasi. Setelah media yang telah diinokulasi memadat, kemudian cawan petri diinkubasi pada suhu 37 0C dengan posisi terbalik selama 48 jam (4) Perhitungan jumlah bakteri berdasarkan ISO Standards for Microbiological
Methods (Harrigan 1998), yaitu:
Dimana:
∑c = jumlah koloni bakteri pada semua cawan yang mengandung 30-300 koloni n1 = jumlah cawan petri yang masuk perhitungan pada pengenceran pertama
n2 = jumlah cawan petri yang pada masuk perhitungan pengenceran berikutnya
d = faktor pengenceran pertama
3.4.2. Nilai pH (AOAC 1995)
Pengukuran nilai pH dilakukan menggunakan pH-meter (TOA HM-11P) yang telah dikalibrasi menggunakan buffer pH 7 dan pH 4. Sampel yang ditambahkan akuades (perbandingan 1:10 w/v), dan dihancurkan dengan
homogenizer. Elektroda dicelup dalam larutan sampel sampai diperoleh pembacaan angka yang stabil, lalu nilai pH dicatat.
22 3.4.3. Nilai TVB(AOAC 1995)
Prinsip penetapan total volatile bases (TVB) adalah menguapkan senyawa-senyawa basa volatil (amonia, mono-, di-, tri- metil amin, dll) di dalam ekstrak sampel yang bersifat basa pada suhu 35 0C selama 2 jam atau suhu kamar selama semalam. Senyawa-senyawa tersebut akan diikat oleh asam borat kemudian dititrasi dengan HCl. Prosedur kerjanya adalah sebagai berikut:
1). Menimbang 25 g sampel, kemudian menggilingnya dengan ditambahkan 75 ml larutan TCA 7% (w/v) dengan homogenizer selama 1 menit. Larutan disaring dengan kertas saring sehingga diperoleh filtrat yang jernih.
2). Menyiapkan cawan conway, yaitu dengan menuang 1 ml asam borat dalam
inner chamber, sedangkan filtrat dan K2CO3 jenuh dituang dalam outer
chamber pada arah yang berlawanan masing-masing sebanyak 1 ml.
3). Setelah cawan ditutup rapat (ditambahkan vaseline), kemudian dimasukkan dalam inkubator (suhu 35 0C) selama 2 jam dan sebelumnya cawan digoyang dengan hati-hati sampai filtrat dan K2CO3 bercampur.
4). Setelah diinkubasi, larutan asam borat dalam inner chamber dititrasi dengan larutan HCl N/70 sampai larutan asam borat berubah warna.
5). Pada blanko, filtrat diganti dengan TCA 7% dengan prosedur sama dengan poin (1) sampai (4).
6). Nilai TVB diukur dengan persamaan sebagai berikut:
Dimana : a = ml titrasi HCl pada sampel b = ml titrasi HCl pada blanko 3.4.4. Nilai TBA (Apriyantono et al. 1989)
Prinsip analisis adalah malonaldehida pada sampel direaksikan dengan
2-thiobarbituric acid (pereaksi TBA) membentuk warna merah. Intensitas warna yang terbentuk diukur absorbansinya dengan spektrofotometer dan dilaporkan sebagai nilai TBA, dinyatakan dalam mg malonaldehida/kg sampel. Prosedur kerjanya sebagai berikut:
1). Menimbang bahan sebanyak 10 g, dimasukkan dalam waring blender dan ditambahkan 50 ml akuades dan dihancurkan selama 2 menit.
2). Memindahkan secara kuantitatif dalam labu distilasi sambil dicuci dengan 47,5 ml akuades, nilai pH diatur dengan menambahkan ± 2,5 ml HCl 4 M. 3). Melakukan destilasi dengan pemanasan tinggi, sampai diperoleh 50 ml
destilat selama 10 menit pemanasan.
4). Destilat yang diperoleh diaduk merata dan dipipet sebanyak 5 ml ke dalam tabung reaksi tertutup.
5). Menambahkan 5 ml pereaksi TBA, ditutup dan dicampur merata lalu dipanaskan selama 35 menit dalam air mendidih
6). Dibuat blanko dengan menggunakan 5 ml akuades dan 5 ml pereaksi, dan dilakukan seperti penetapan sampel.
7). Tabung reaksi didinginkan dengan air pendingin selama ± 10 menit, lalu diukur absorbansinya (D) pada panjang gelombang 528 nm dengan larutan blanko sebagai titik nol.
8). Perhitungan nilai TBA dinyatakan dalam mg malonaldehida / kg sampel. Nilai TBA = 7,8 D x 10/g berat sampel
3.4.5. Kadar air (AOAC 1995)
Cawan porselen dikeringkan pada suhu 105 0C selama 1 jam, kemudian didinginkan dan ditimbang. Sampel ditimbang sebanyak 5 g. Cawan yang telah berisi sampel dimasukkan dalam oven bersuhu 105 0C selama 1 jam, kemudian didinginkan dalam desikator selama 15 menit, lalu ditimbang. Pengeringan di oven dilakukan kembali sampai berat sampel konstan. Kadar air dihitung berdasarkan persamaan berikut:
3.4.6. Nilai aw (water activity)
Pengukuran nilai aw menggunakan aw-meter (Shibawa aw-meter WA-360).
Cara pengoperasian alat adalah sebagai berikut:
1). Memastikan probe dan tempat sampel bersih, kering dan bebas lemak. 2). Alat dihubungkan dengan arus listrik, lalu menekan tombol Power “on/off”. 3). Menekan tombol Menu dan dipilih Mode menggunakan tanda panah turun,
dipilih “standard”, kemudian menekan Enter.
24 4). Didiamkan selama 30 menit.
5). Sebelum pengujian sampel, dilakukan kalibrasi menggunakan humidity standard berturut-turut 35% RH, 80% RH, 95% RH, 10% RH, dan 0,5% RH. Bila sampel yang diukur memiliki nilai rata-rata RH di bawah 20% RH, maka cukup dikalibrasi menggunakan humidity standard 80% RH.
6). Memasukkan ± 3 g sampel (telah dihancurkan) pada probe dan Enter ditekan. 7). Pembacaan dianggap stabil apabila tanda panah pada monitor tidak berubah. 8). Mencatat nilai aw dan suhu yang tertera pada layar.
9). Ditekan Enter untuk keluar dari Data.
10). Mematikan alat dengan menekan Power “ on/off” dan stop kontak dicabut.
3.5. Analisis Statistik
4. HASIL DAN PEMBAHASAN
4.1. Karakteristik Kitosan
Karakteristik kitosan yang digunakan pada penelitian ini disajikan pada Tabel 2. Kadar air, kadar abu, derajat deasetilasi dan logam berat pada kitosan masih berada pada angka yang masih diijinkan oleh BPOM RI. Menurut No dan Meyers (1995) produk kitosan komersial memiliki kadar air < 10%, kadar abu < 2% dan derajat deasetilasi > 70%.
Tabel 2. Karakteristik kitosan
a. Kitosan produksi PT Araminta Sidhakarya (Maulana 2007)
b. Berdasarkan SK Badan POM RI No. HK.00.05.52.6581 tentang kitosan dalam produk pangan
Pengukuran kadar abu merupakan indikator keefektifan proses demineralisasi untuk membuang kalsium karbonat dari kulit udang sebagai bahan baku. Kadar abu pada kitosan merupakan parameter penting yang dapat mempengaruhi kelarutan mengakibatkan viskositas yang rendah atau dapat mempengaruhi karakteristik pada produk akhir (No dan Meyers 1995).
26
4.2. Aktivitas Antibakteri pada Kitosan dan Kombinasinya dengan Kalium Sorbat, Natrium Benzoat dan Ekstrak Solanum sp.
Penelitian aktivitas antibakteri menggunakan E. coli dan S. aureus sebagai bakteri uji. Kedua jenis ini mewakili jenis bakteri Gram-negatif dan Gram-positif, selain ikut berperan dalam kontaminasi dan kerusakan makanan. E. coli
merupakan bakteri Gram-negatif yang berasal dari kotoran hewan maupun manusia, sehingga sering dijadikan bakteri indikator adanya polusi kotoran dan kondisi sanitasi (Fardiaz 1993). Tidak semua jenis E. coli menyebabkan penyakit pada manusia, namun ada potensi bahaya bila jenis bakteri ini terdeteksi pada makanan dan dikonsumsi manusia (Batt 1999). Bakteri S. aureus merupakan bakteri Gram-positif berbentuk kokus dengan diameter 0,7-0,9 µm dan tumbuhnya secara anaerobik fakultatif. Bakteri ini memproduksi enterotoksin yang menyebabkan keracunan dan sering ditemukan pada jenis makanan yang mengandung protein tinggi seperti ikan, telur dan daging. Enterotoksin yang diproduksi oleh S. aureus bersifat tahan panas dan masih aktif setelah dipanaskan pada suhu 100 oC selama 30 menit (Fardiaz 1993).
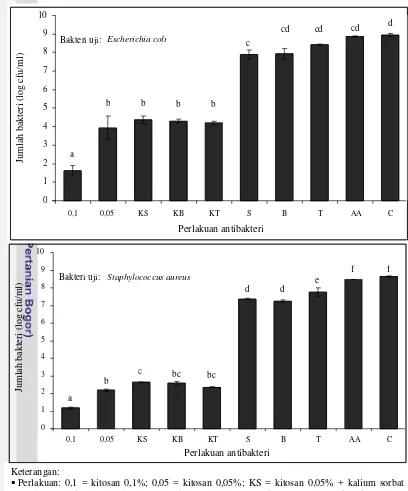
Bahan antibakteri yang digunakan pada penelitian ini adalah kitosan dan kombinasinya dengan kalium sorbat, natrium benzoat dan ekstrak Solanum sp. Perlakuan yang digunakan adalah: kitosan 0,1%; kitosan 0,05%; kombinasi kitosan 0,05% dengan kalium sorbat 0,05%; kombinasi kitosan 0,05% dengan natrium benzoat 0,05%; dan kombinasi kitosan 0,05% dengan terung pungo 20 µg/ml. Dilakukan juga pengujian untuk kontrol (tanpa diberi perlakuan); kalium sorbat 0,1%; natrium benzoat 0,1%; ekstrak Solanum sp. 20 µg/ml; dan asam asetat 0,07%. Hasil pengujian aktivitas antibakteri disajikan pada Gambar 4 dan hasil perhitungannya dapat dilihat pada Lampiran 1.
Kombinasi kitosan dengan kalium sorbat, natrium benzoat maupun ekstrak
Solanum sp., tidak memberikan efek antibakteri yang sinergis. Hal ini terlihat pada kitosan 0,05% yang memiliki aktivitas antibakteri yang lebih tinggi daripada kombinasinya dengan kalium sorbat, natrium benzoat maupun ekstrak Solanum
jumlah bakteri paling sedikit, baik terhadap S. aureus yaitu 1,17 ± 0,06 log cfu/ml maupun terhadap E. coli yaitu 1,43 ± 0,27 log cfu/ml.
Gambar 4. Hasil pengujian aktivitas antibakteri.
Aktivitas antibakteri pada kitosan 0,05% yang dikombinasikan dengan kalium sorbat 0,05% memiliki jumlah bakteri sebesar 2,65 ± 0,01 log cfu/ml 0,05%; KB = kitosan 0,05% + natrium benzoat 0,05%; KT = kitosan 0,05% + ekstrak Solanum
sp. 20 µg/ml; S = kalium sorbat 0,1%; B = natrium benzoat 0,1%; T = ekstrak Solanum sp. 20 µg/ml; AA = asam asetat 0,07%; dan C =kontrol (tanpa diberi perlakuan).
Notasi huruf yang berbeda menunjukkan beda nyata antar perlakuan (uji Tukey α = 5%). Bakteri uji: Staphylococcus aureus
28
kombinasi kitosan 0,05% dengan natrium benzoat 0,05% memiliki jumlah bakteri sebesar 2,58 ± 0,11 log cfu/ml terhadap S. aureus dan 4,31 ± 0,10 log cfu/ml E. coli. Kombinasi yang dilakukan antara kitosan dengan kalium sorbat ataupun natrium benzoat tidak memberikan efek sinergis karena diduga terjadi reaksi saat kedua bahan dikombinasikan. Kitosan yang memiliki gugus muatan positif NH3+
pada struktur molekulnya diduga bereaksi dengan gugus sorbat dan benzoat yang bermuatan negatif membentuk garam. Hal ini dapat diamati secara visual saat mencampurkan kitosan dan kalium sorbat maupun natrium benzoat pada media cair yang terlihat keruh dan membentuk flokulan berwarna putih susu pada media. Percobaan yang dilakukan dengan menambahkan kalium sorbat lebih banyak pada media yang mengandung kitosan (di luar metode penelitian), memperlihatkan terbentuknya gumpalan-gumpalan berwarna putih yang lebih besar. Proses inilah yang diduga melemahkan aktivitas antibakteri pada kitosan, sehingga kombinasi kitosan dengan kalium sorbat dan natrium benzoat justru memiliki aktivitas antibakteri yang tidak sinergis.
Kombinasi kitosan 0,05% dengan ekstrak terung pungo (Solanum sp.) 20 µg/ml memperlihatkan aktivitas antibakteri dengan jumlah bakteri sebesar 2,36 ± 0,01 log cfu/ml terhadap S. aureus dan 4,20 ± 0,09 log cfu/ml terhadap E. coli. Aktivitas penghambatan bakteri dari kombinasi ini tidak berbeda nyata dibandingkan kitosan 0,05%. Hal ini menunjukkan kedua bahan ini tidak memberikan efek antibakteri yang sinergis bila dikombinasikan. Hasil ini memperlihatkan kemampuan aktivitas antibakteri pada kitosan lebih baik dibandingkan kombinasi kitosan dengan kalium sorbat, natrium benzoat dan ekstrak Solanum sp.
pertumbuhan bakteri bila dibandingkan kitosan 0,1%. Pengujian aktivitas antibakteri pada terung pungo 20 µg/ml memperlihatkan kemampuan yang rendah, dengan jumlah bakteri sebesar 7,75 ± 0,25 log cfu/ml terhadap S. aureus
dan 8,42 ± 0,05 log cfu/ml terhadap E. coli. Dilakukan juga pengujian aktivitas antibakteri terhadap asam asetat, karena senyawa ini digunakan dalam melarutkan kitosan. Konsentrasi 0,07% dihitung dari jumlah asam asetat untuk melarutkan kitosan 0,1%. Aktivitas antibakteri asam asetat 0,07% menunjukkan rendahnya aktivitas penghambatan bakteri dari senyawa ini dengan jumlah bakteri sebesar 8,46 log cfu/ml terhadap S. aureus dan 8,87 ± 0,04 log cfu/ml terhadap E. coli, sedangkan kontrol adalah 8,66 ± 0,04 log cfu/ml terhadap S. aureus dan 8,95 ± 0,09 log cfu/ml terhadap E. coli.
Mekanisme antibakteri pada kitosan telah dilaporkan oleh beberapa peneliti. Menurut Tsai dan Su (1999), aktivitas antibakteri pada kitosan tergantung pada muatan positif pada kitosan dan muatan negatif pada permukaan mikroba yang diperlihatkan oleh kekuatan elektrostatis antara proton gugus NH2 pada
kitosan dan residu negatif pada permukaan sel bakteri. Oleh karena itu, kitosan yang memiliki derajat deasetilasi (DD) tinggi akan memiliki muatan positif yang tinggi menyebabkan adanya aktivitas antibakteri yang tinggi pula, dimana keberadaan sejumlah gugus NH2 terprotonasi pada kitosan akan meningkat
dengan meningkatnya DD (Tsai et al. 2002). Aktivitas antibakteri pada kitosan tergantung pada beberapa faktor antara lain DD, suhu dan berat molekul. Kitosan dengan DD yang tinggi lebih efektif melawan mikroorganisme. Kitosan dengan berat molekul yang rendah dapat masuk dalam sel-sel mikroba dan merusak metabolisme pada sel, dan pada kitosan dengan berat molekul tinggi akan membentuk film di sekitar sel, sehingga menghambat masuknya nutrisi dalam sel (Zheng dan Zhu 2003).
30
polimer (film) sehingga menghambat absorbsi nutrisi ke dalam sel. Mekanisme kedua adalah kitosan dengan berat molekul yang rendah mampu menembus masuk ke dalam sel sehingga mampu mengabsorbsi senyawa elektronegatif dan memflokulasinya, mengakibatkan terjadi kerusakan pada aktivitas fisiologis bakteri dan akhirnya membunuhnya. Mekanisme pertama lebih dominan terhadap
S. aureus dan mekanisme kedua terhadap E. coli.
Tsai dan Su (1999) melaporkan bahwa kitosan menyebabkan lepasnya glukosa dan laktat dehidrogenase dari sel E. coli. Menurut Liu et al. (2004), kitosan dapat meningkatkan permeabilitas membran luar (outer membrane) dan membran dalam (inner membrane) dan akhirnya merusak membran sel pada bakteri dengan melepaskan kandungan seluler. Kerusakan ini diduga disebabkan oleh interaksi elektrostatis antara gugus NH3+ pada kitosan asetat dengan gugus
fosforil dari komponen fosfolipida pada membran sel.
4.3. Penggunaan Kitosan terhadap Daya Awet Bandeng Presto
Tujuan penelitian ini adalah menggunakan bahan yang memiliki aktivitas antibakteri terbaik dari penelitian tahap I untuk diaplikasikan sebagai bahan pengawet pada produk perikanan. Hasil penelitian tahap I memperlihatkan bahwa kitosan dengan konsentrasi 0,1% memiliki kemampuan antibakteri lebih baik dibandingkan dengan kitosan yang dikombinasikan dengan kalium sorbat, natrium benzoat maupun ekstrak Solanum sp. Produk yang digunakan dalam penelitian ini adalah bandeng presto yang disimpan pada suhu kamar (28-30 oC).
4.3.1. Jumlah bakteri total dan nilai pH
Parameter mikrobiologis pada produk perikanan merupakan faktor kunci dalam menentukan keamanan untuk konsumsi manusia. Kontaminasi bakteri pada produk perikanan dapat terjadi saat panen, penanganan, distribusi maupun penyimpanan dan proses pengolahan (Wekell et al. 1994). Oleh karena itu, lembaga standardisasi pangan di beberapa negara telah mengatur batasan jumlah bakteri total yang aman pada produk pangan untuk dikonsumsi.
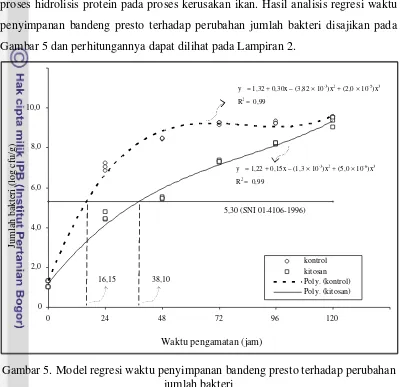
Selama proses pembusukan, jumlah bakteri proteolisis dari jumlah bakteri total dalam daging ikan sekitar 30%, sehingga bakteri dapat berperan nyata dalam proses hidrolisis protein pada proses kerusakan ikan. Hasil analisis regresi waktu penyimpanan bandeng presto terhadap perubahan jumlah bakteri disajikan pada Gambar 5 dan perhitungannya dapat dilihat pada Lampiran 2.
Gambar 5. Model regresi waktu penyimpanan bandeng presto terhadap perubahan jumlah bakteri
Jumlah bakteri total yang diamati pada bandeng presto yang direndam kitosan 0,1% maupun kontrol pada pengamatan jam ke-0 adalah < 1,20 ± 0,17 log cfu/g dan < 1,10 ± 0,17 log cfu/g. Jumlah total bakteri yang rendah pada jam ke 0 disebabkan oleh proses pemasakan pada suhu 121oC, tekanan 15 psi selama 60 menit (Hadiwiyoto dan Naruki 1999) menyebabkan bakteri akan mati karena kondisi pengolahannya sama dengan proses sterilisasi bahan pangan.
Batasan maksimal jumlah bakteri total berdasarkan SNI 01-4106-1996 pada produk bandeng presto adalah 2 x 105 cfu/g yang sama dengan 5,3 log cfu/g. Oleh karena itu, dengan menggunakan model regresi waktu penyimpanan bandeng presto terhadap perubahan jumlah bakteri menunjukkan bahwa kitosan