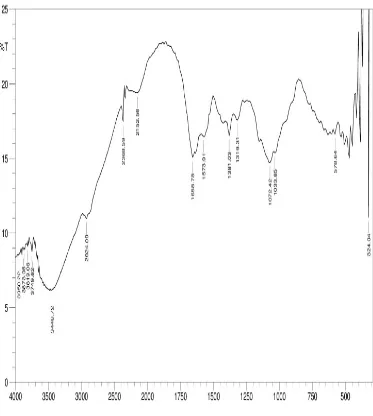
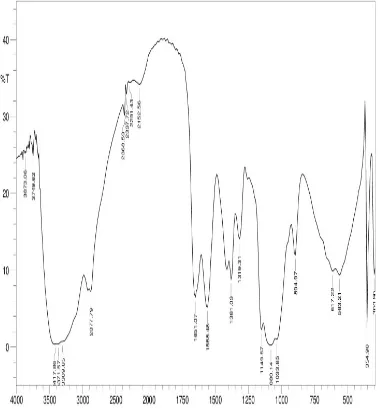
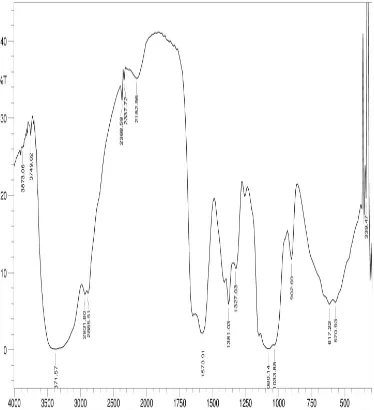
Lampiran 1. Spektrum FT-IR
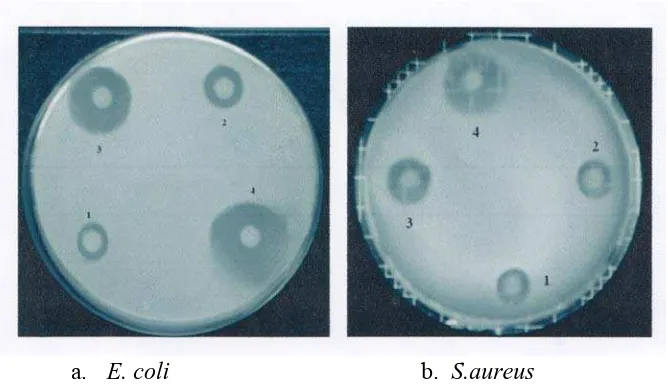
Lampiran 2. Foto Uji Bakteri
a. E. coli b. S.aureus
Gambar 2.1 Uji Antibakteri Escherichia coli Keterangan gambar:
1. Larutan Zn 2. Larutan kitosan
3. Larutan kitosan nanopartikel 4. Larutan kitosan nanopartikel + Zn
Lampiran 3. Perhitungan Indeks Antimikrobial 1. Untuk bakteri E.coli
- Larutan Zn
Diameter zona hambat = 5,3 mm Diameter cakram = 4 mm
= 0,05
Lampiran 4. Perhitungan Derajat Deasetilasi (DD)
Penentuan derajat deasetilasi dari kitosan menggunakan persamaan Domszy dan Roberts (Sugita, 2009).
1. Kitosan Nanopartikel
%
2. Kitosan Nanopartikel + Zn
DAFTAR PUSTAKA
Allan, C.R. and Hadwiger, I.A. 1979. The Fungicidal Effect of Chiosan on Fungi of Varying Cell Wall Composition. Experimental Mycology.
Buckle, K.A. 2007. Ilmu Pangan. UI-Press. Jakarta.
Cheung, W.H., Szeto, S. And McKay, G. 2008. Enchancing The adsorption Capacities Of Acid Dyes By A Chitosan NanoParticle.Department of Chemical Engineering. University of Science and Technology.Hongkong
Darmono. 1995. Logam Dalam Sistem Biologi Makhluk Hidup. UI Press. Jakarta.
Dewi, A. 2010. Pengaruh Waktu Penggunaan Ultrasonik Bath Terhadap Sifat-Sifat Karakteristik Kitosan Nanopartikel. [Skripsi]. Medan: Universitas Sumatera Utara.
Goosen,M.F.A.1997.Applications of Chitin and Chitosan.Technomic.USA.
Harianingsih. 2010. Pemanfaatan Limbah Cangkang Kepiting Menjadi Kitosan Sebagai Bahan Pelapis (Coater) Pada Buah Stroberi. [Tesis]. Semarang: Universitas Diponegoro.
Hasyimi, H.M. 2010. Mikrobiologi dan Parasitologi Untuk Mahasiswa Keperawatan. Trans Info Media. Jakarta.
Kaban, J. 2009. Modifikasi Kimia dari Kitosan dan Aplikasi Produk yang Dihasilkan. Pidato Pengukuhan guru Besar. USU.
Li du, W., Shan Niu, S., Lei Xu, Y., Rong Xu, Z. and Li Fan, C. 2009. Antibacterial Activity of Chitosan Tripolyphosphate Nanoparticles Loaded With various Metal Ion.Carbohydrate Polymers. 75: 385-389.
Mardliyati E. 2010.Pengenalan Pemanfaatan Nanopartikel Kitosan sebagai Matriks Enkapsulasi. Jakarta: Badan Pengkaji dan Penerapan Teknologi.
Mohanraj, U.J. and Chen, Y. 2006. Nanoparticles. Tropical Journal of Pharmaceutical Research. 5(1): 561-573.
Pelczar, M.J. 2005. Dasar-Dasar Mikrobiologi. UI-Press. Jakarta.
Sagala, B.D.M. 2012. Formulasi Beads Kitosan Untuk Sistem Pelepasan Obat Terkendali. [Skripsi]. Depok: Universitas Indonesia.
Shu, X.Z. and Zhu, K.J. 2002. Controlled Drug Release Properties of Ionically Cross-Linked Chitosan beads: The Influence of Anion Structure. International Journal of Pharmaceutics. 233: 217-225.
Svehla, G. 1979. Buku Teks Analisis Anorganik Kualitatif Makro dan Semimikro. Edisi kelima. Bagian I. PT.Kalman Media Pusaka. Jakarta.
Stevens, M.P. 2001. Kimia Polimer. Pradnya Paramita. Jakarta.
Sugita, P. 2009. Sumber Biomaterial Masa Depan Kitosan. IPB Press. Bandung.
Suhartono, M.T. 2006. Pemanfaatan Kitin, Kitosan, Kitooligosakarida. Foodreview. 6: 30 – 33.
Suptijah, P., Jacoeb, A.M. dan Deviyanti, N. 2012. Karakterisasi dan Bioavailabilitas Nanokalsium Cangkang Udang Vannamei (Litopenaeus Vannamei). Jurnal Akuatika. III: 63-73.
Suslick, K.S. and Price, G.J. 1999. Application of Ultrasound to Materials Chemistry. Annual Reviews. 29: 295-326.
Szeto Yau-shan and Zhigang Hu.2007.Article Exploring Nanochitosan.ATA-Journal for Asia on Textile & Apparel.China
Tabata, M. 1980. Chem.Phys.Lett. 73: 178.
Varum, K.M. 1994. Water Solubility of Partially N-Acetylated Chitosans as a Function On pH Effect of Chemical Composition and Depolymerisation. CarbohydratePolymers.
Wibowo, S. 2010. Penelitian Pemanfaatan Limbah Perikanan Udang Untuk produksi Turunan Kitosan dan Aplikasinya Untuk Mendukung Industri Pangan.
Wirjosentono, B. 1995.Analisis dan Karakterisasi Polimer. Cetakan Pertama.
BAB 3
METODOLOGI PENELITIAN
3.1 Alat dan Bahan
3.1.1 Alat-alat
- Neraca analitis Chyo Electronic Balance
- Alat-alat gelas Pyrex
- Ultrasonik bath Kerry Pulsatron
- Sentrifugal
- Batang pengaduk
- Cawan petri
- Jarum ose
- Bunsen
- Autoklaf Yamato
- Inkubator Fischer
- Hot plate
- Oven Gallenkamp
- Jangka sorong
- Mikropipet
- Blank dish
- Freeze dryer
3.1.2 Bahan-bahan
- Kitosan
- Akuades
- Natrium tripolifosfat
- Serbuk ZnO Merck
- Media Nutrient Agar (NA) Merck
- Media Muller Hinton Agar (MHA) Oxoid
- Biakan Escherichia coli - Biakan Staphylococcus aureus
3.2 Prosedur penelitian
3.2.1 Pembuatan Larutan Pereaksi
a. Larutan asam asetat 1%
Sebanyak 10 mL asam asetat glacial dimasukkan ke dalam labu takar 1000
dihomogenkan.
b. Larutan natrium tripoliphosfat 1%
Sebanyak 1 g natrium tripoliphosfat dilarutkan dengan 50 mL akuades.
Kemudan dimasukkan ke dalam labu takar 100 mL dan diencerkan dengan
akuades sampai garis tanda, lalu dihomogenkan.
c. Larutan kitosan 0,3%
Sebanyak 3 g kitosan dilarutkan dengan 1000 mL larutan asam asetat 1%.
3.2.2 Pembuatan Kitosan Nanopartikel
Ditambahkan 40 mL larutan tripoliphosfat ke dalam 1000 mL larutan kitosan
0,3%. Diaduk dengan pengaduk selama 20 menit. Larutan tersebut diletakkan
pada ultrasonik bath selama 30 menit. Disentrifugasi pada 1.200 rpm selama 10
menit kemudian didekantasi. Endapan dimasukkan ke dalam freeze dryer
1.2.2 Pembuatan Kitosan Nanopartikel yang Bermuatan Ion Logam
Dilarutkan 0,3 g kitosan nanopartikel ke dalam 100 mL asam asetat 1%.
Ditambahkan larutan ion Zn2+ hingga konsentrasi 120 μg/mL dan diaduk selama 12 jam pada temperatur kamar. Sebagian larutan tersebut dicetak film pada plat
kaca. Film tersebut dikeringkan hingga benar-benar kering kemudian diuji
karakterisasinya dengan FT-IR dan sebagian larutan digunakan untuk uji aktivitas
antibakteri.
1.2.4 Pembuatan Media Padat Nutrient Agar (NA)
Dilarutkan 2 g NA dalam 100 mL akuades. Dipanaskan di atas hot plate sambil
diaduk menggunakan batang pengaduk sampai mendidih. Dibagi dalam beberapa
tabung reaksi sebanyak 5 mL. Ditutup rapat dengan kapas. Disterilisasi dalam
autoklaf pada suhu 1210C tekanan 1-2 atm selama 15 menit. Dibiarkan sampai
memadat dalam keadaan miring.
1.2.5 Pembuatan Media Padat Muller Hinton Agar (MHA)
Dilarutkan 3,4 g MHA dalam 100 mL akuades. Dipanaskan di atas hot plate
sambil diaduk menggunakan batang pengaduk sampai mendidih. Ditutup rapat
1.2.6 Penyedian Biakan Stok Bakteri
Satu ose biakan Escherichia coli dan Staphylococcus aureus masing-masing digoreskan dalam media pertumbuhan NA. Diinkubasi di dalam inkubator pada
suhu 350C selama 1-2 hari.
1.2.7 Penentuan Aktivitas Antibakteri
Uji aktivitas antibakteri dilakukan secara aseptik dengan metode difusi cakram.
Biakan bakteri Escherichia coli dan Staphylococcus aureus digoreskan di atas media MHA. Kemudian dimasukkan blank dish yang telah ditetesi larutan kitosan
nanopartikel yang bermuatan ion logam Zn2+ dengan konsentrasi 0,05%; 0,10%;
0,15%; 0,20% dan 0,25%. Kultur bakteri diinkubasi dalam inkubator dengan cara
terbalik pada suhu 350C selama 24 jam. Perlakuan dilakukan sebanyak 2
pengulangan pada masing-masing konsentarsi. Diukur besarnya aktivitas
antibakteri berdasarkan diameter zona bening yang terbentuk di sekitar cakram
3.3 Bagan Penelitian
3.3.1 Pembuatan Larutan Kitosan 0,3% (Wen Li Du, 2009)
Dilarutkan dalam 1000 mL larutan asam asetat 1%
3.3.2 Pembuatan Kitosan Nanopartikel (Wen Li Du, 2009)
Ditambahkan 40 mL larutan tripoliphosfat
Diaduk campuran dengan pengaduk selama 20 menit
Diultrasonik bath selama 30 menit
Disentrifugasi pada 1.200 rpm selama 10 menit
Didekantasi
Dimasukkan ke dalam freeze dryer
3 g kitosan
Larutan Kitosan
1000 mL larutan kitosan 0,3 %
Endapan Filtrat
Kitosan Nanopartikel
Karakterisasi Kitosan Nanopartikel
3.3.3 Pembuatan Kitosan Nanopartikel yang Bermuatan Ion Logam
Disuspensikan ke dalam 100 mL asam asetat 1%
Ditambahkan larutan ion logam Zn2+
hingga konsentrasi 120 μg/mL dan diaduk selama 12
jam pada temperatur kamar
Dibagi menjadi 2 bagian
Dicetak pada plat kaca Diuji aktivitas antibakterinya
Dikeringkan hingga benar-
benar kering
Dianalisis denganFT-IR
0,3 g Kitosan Nanopartikel
Bagian 1 Bagian 2
3.3.4 Pembuatan Media Padat Nutrient Agar (NA) (Nurfadilah, 2013)
Dimasukkan ke dalam erlenmeyer
Dilarutkan dengan 100 mL akuades
Dipanaskan di atas hot plate sambil diaduk
menggunakan batang pengaduk sampai mendidih
Didinginkan
Dimasukkan sebanyak 5 mL ke dalam beberapa
tabung reaksi
Ditutup rapat dengan kapas
Disterilisasi di dalam autoklaf pada suhu 1210C
tekanan 1-2 atm selama 15 menit
Dibiarkan hingga memadat dalam keadaan miring 2 g nutrient agar
Media Nutrient Agar
3.3.5 Pembuatan Media Padat Muller Hinton Agar (MHA)
Dimasukkan ke dalam erlenmeyer
Dilarutkan dengan 100 mL akuades
Dipanaskan di atas hot plate sambil diaduk
menggunakan batang pengaduk sampai mendidih
Didinginkan
Ditutup rapat dengan kapas
Disterilisasi di dalam autoklaf pada suhu 1210C
tekanan 1-2 atm selama 15 menit
3.3.6 Penyedian Biakan Stok Bakteri (Nurfadilah, 2013)
Digoreskan satu ose bakteri Escherichia coli
Diinkubasi dalam inkubator pada suhu 350C selama 2x24 jam
Catatan : dilakukan prosedur yang sama untuk bakteri Staphylococcus aureus 3,8 g Muller Hinton Agar
Media Muller Hinton Agar
Hasil
Media Nutrient Agar
3.3.7 Penentuan Aktivitas Antibakteri
Ditetesi dengan larutan kitosan Digoreskan di atas media Nanopartikel MHA di dalam cawan petri
Diletakkan kertas cakram yang
telah ditetesi larutan kitosan
nanopartikel
Diinkubasi secara terbalik pada suhu
350C selama 24 jam
Diukur diameter zona bening yang
terbentuk di sekitar kertas cakram
Catatan : dilakukan prosedur yang sama untuk larutan Zn, larutan kitosan dan
larutan kitosan nanopartikel yang mengandung logam Zn terhadap bakteri
Staphylococcus aureus.
Kertas cakram Suspensi bakteri E.coli
Kertas cakram basah
Media MHA + suspensi bakteri
BAB 4
HASIL DAN PEMBAHASAN
4.1 Hasil Penelitian
Hasil uji aktivitas antibakteri kitosan nanopartikel dan kitosan nanopartikel yang
bermuatan ion logam Zn2+ terhadap bakteri Escherichia coli dan Staphylococcus aureus menunjukkan adanya aktivitas penghambatan pertumbuhan, hal ini dapat dilihat dari hasil pengukuran diameter zona bening yang terbentuk yaitu berupa
wilayah jernih di sekeliling cakram kertas yang mengandung larutan Zn, larutan
kitosan, larutan kitosan nanopartikel dan larutan kitosan nanopartikel yang
bermuatan ion logam Zn2+ dengan menggunakan jangka sorong.
4.1.1 Uji Aktivitas Antibakteri
Data hasil pengukuran diameter zona hambat kitosan nanopartikel terhadap
bakteri Escherichia coli dan Staphylococcus aureus dapat dilihat pada tabel 4.1.
Tabel 4.1 Data Diameter Zona Hambat (mm) Kitosan Nanopartikel Terhadap
Bakteri Escherichia coli dan Staphylococcus aureus
Sampel Diameter Zona Hambat
E.coli S.aureus
Larutan Zn 6,3 6,2
Larutan Kitosan 7,2 7,0
Larutan Kitosan Nanopartikel 11,1 8,4
4.2 Pengolahan Data
4.2.1 Mencari Nilai Indeks Antimikrobial dari Kitosan Nanopartikel Terhadap Bakteri Escherichia coli danStaphylococcus Aureus.
Dari pengukuran diameter zona hambat dihasilkan indeks antimikrobial kitosan
nanopartikel terhadap bakteri Escherichia coli dan Staphylococcus Aureus berdasarkan rumus.
Dengan diameter cakram = 0,6 cm / 6 mm
Indeks antimikrobial terhadap bakteri Escherichia coli dan Staphylococcus Aureus dapat dilihat pada tabel 4.2 dimana perhitungannya dapat dilihat pada lampiran.
Tabel 4.2 Indeks Antimikrobial Kitosan Nanopartikel Terhadap Bakteri
Escherichia coli dan Staphylococcus Aureus
Sampel Indeks Antimikrobial
E.coli S.aureus
Larutan Zn 0,05 0,03
Larutan Kitosan 0,20 0,16
Larutan Kitosan Nanopartikel 0,85 0,40
4.3 Pembahasan
4.3.1 Pembuatan Kitosan Nanopartikel
Pembuatan kitosan nanopartikel dilakukan dengan melarutkan kitosan di dalam
asam asetat 1% dan diaduk hingga homogen untuk memperoleh larutan kitosan.
Penambahan larutan tripolifosfat ke dalam larutan kitosan sehingga diperoleh
emulsi kitosan. Ditempatkan dalam ultrasonik bath untuk memecah
partikel-partikel gel kitosan menjadi lebih kecil. Disentrifugasi pada 1.200 rpm untuk
memisahkan gel kitosan dari larutannya. Endapan yang berupa gel kitosan
dimasukkan ke dalam freeze dryer sehingga diperoleh serbuk kitosan
nanopartikel.
Kitosan nanopartikel yang dihasilkan dianalisa dengan menggunakan SEM
(Scanning Elektron Microscopy). Dari hasil SEM pada gambar 4.3 menunjukkan
bahwa kitosan yang dihasilkan memiliki ukuran 200 nm dan dapat digolongkan
ke dalam nanopartikel karena sesuai dengan pengertian nanopartikel yang
dijelaskan Mohanraj dan Chen (2006) yaitu nanopartikel adalah partikel yang
memiliki ukuran 10-1000 nm. Nanopartikel dengan ukuran yang sangat kecil,
memiliki kelarutan yang lebih baik sehingga dapat lebih mudah dalam
pengaplikasiannya.
4.3.2 Pembuatan Kitosan Nanopartikel yang Bermuatan Ion Logam Zn2+
Kitosan nanopartikel yang dihasilkan dilarutkan dalam asam asetat 1%.
Ditambahkan logam Zn (serbuk ZnO) dan diaduk dengan stirer selama 12 jam
pada temperatur ruang. Dicetak pada plat kaca dan dikeringkan pada temperatur
ruang hingga benar-benar kering. Kemudian dianalisa dengan FT-IR. Dari hasil
FT-IR kitosan nanopartikel (lampiran) dan kitosan nanopartikel yang bermuatan
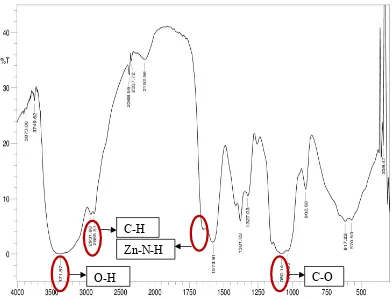
ion logam Zn2+ terdapat perbedaan pita serapan pada daerah bilangan gelombang 1651,07 (tekuk N-H). Hal ini menunjukkan terjadinya perubahan intensitas gugus
terjadi ikatan antara unsur nitrogen pada gugus amino yang mempunyai sepasang
elektron yang dapat membentuk ikatan aktif dengan kation logam.
Kitosan menunjukkan afinitas yang tinggi terhadap logam
golongan transisi. Interaksi kitosan dengan ion logam terjadi karena proses
pengkompleksan membentuk kompleks logam kitosan dimana pertukaran ion,
penyerapan dan pengkhelatan terjadi selama proses berlangsung (Muzzarelli,
1973).
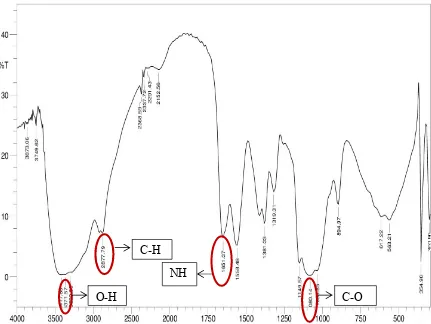
Gambar 4.1 Spektrum FT-IR Kitosan Nanopartikel O-H
C-H
NH
Gambar 4.2 Spektrum FT-IR Kitosan Nanopartikel yang Bermuatan Ion Logam Zn2+
4.3.3 Analisa Spektrum FT-IR
Analisa dengan spektroskopi FT-IR ini dapat digunakan sebagai informasi
mengenai perubahan gugus yang mengindikasikan terdapatnya interaksi secara
kimia. Pada polimer kitosan nanopartikel cangkang belangkas yang
dikarakterisasi terdapat beberapa gugus lain seperti ulur O-H, ulur N-H, ulur C-H,
dan ulur C-O. Ulur O-H pada polimer nanokitosan cangkang belangkas terlihat
spektra yang membentuk pita melebar ke bawah sehingga ulur N-H yang juga
terdapat pada daerah ini tidak dapat diamati. Adanya ulur N-H dapat diperjelas
dengan adanya tekuk N-H pada spektrum tersebut.
Spektrum tersebut menunjukkan adanya serapan pada daerah bilangan
gelombang (cm-1) : 3417,86 (N-H bending dan O-H stretching ), 2877,79 (C-H stretching), 1651,07 (C=O amida), dan 1080,14 (C-O). Munculnya puncak amida
O-H C-H
Zn-N-H
disebabkan kitosan cangkang belangkas yang digunakan mempunya derajat
deasetilasi (DD) sebesar 82,5%. Ulur C-H pada spektrum kitosan cangkang
belangkas tersebut berasal dari rantai utama polimer. Adanya ulur C-H tersebut
akan diperkuat dengan tekukan C-H dari metil atau metilen. Namun dikarenakan
daerah tekuk C-H melebar maka sulit untuk diamati. Sedangkan ulur C-O berasal
dari gugus metanol yang melekat pada rantai polimer.
4.3.4 Analisa Scanning Elektron Microcopy (SEM)
Analisa permukaan dilakukan dengan instrumen SEM ZEISS dan perbesaran yang
diinginkan agar diperoleh foto yang baik dan jelas. Nanokitosan disinari dengan
pancaran elektron bertenaga 15 kV dengan perbesaran 50.000 x.
Dari hasil yang diperoleh, uji morfologi dengan menggunakan alat SEM
menunjukkan bahwa nanokitosan yang dihasilkan memenuhi kriteria dari
nanoteknologi sebagaimana yang terlihat pada gambar 4.3 dibawah ini dengan
perbesaran 50.000 x. Nanopartikel adalah partikel yang memiliki ukuran 10-1000
nm, dimana sebagian atau keseluruhan komponen dari kitosan berukuran
nanometer. Dari gambar hasil hasil analisa morfologi menunjukkan bahwa ukuran
Gambar 4.3 Hasil SEM Kitosan Nanopartikel Dengan Perbesaran 50.000 x
4.3.5 Aktivitas Antibakteri
Pada tabel 4.1 dan tabel 4.2 di atas dilihat bahwa larutan Zn, larutan kitosan,
larutan kitosan nanopartikel dan larutan kitosan nanopartikel yang bermuatan ion
logam Zn2+ dapat menghambat pertumbuhan bakteri Escherichia coli dan
Staphylococcus aureus. Kitosan nanopartikel lebih aktif menghambat pertumbuhan koloni bakteri Escherichia coli dibandingkan koloni bakteri Staphylococcus aureus, hal ini dapat dilihat dari diameter zona bening yang terbentuk disekeliling cakram yang diletakkan pada media pertumbuhan bakteri
Escherichia coli lebih lebar daripada yang diletakkan pada media pertumbuhan bakteri Staphylococcus aureus. Hal ini disebabkan oleh perbedaan sifat sensitivitas dari bakteri Escherichia coli dan Staphylococcus aureus terhadap larutan kitosan nanopartikel. Larutan kitosan nanopartikel memiliki kemampuan
dalam menghambat pertumbuhan bakteri karena adanya gugus asam amino bebas
Diameter zona bening yang terbentuk terhadap bakteri semakin meningkat
dari larutan nanokitosan dan larutan kitosan dengan penambahan logam Zn
dibandingkan dengan daya hambat dari larutan kitosan dan larutan Zn. Hal ini
terjadi karena ukuran dari partikel nanokitosan lebih kecil sekitar 200 nm
sehingga lebih mudah masuk ke dalam dinding sel dari bakteri Escherichia coli yang berukuran 1,1-1,5 μm x 2,0-6,0 μm dan bakteri Staphylococcus aureus berukuran 0,5-1,5 μm. Dan semakin meningkat dengan penambahan Zn karena
ZnO merupakan salah satu oksida logam yang memiliki efek yang baik sebagai
anti mikroorganisme.
Mekanisme kerja kitosan sebagai zat antimikroba adalah dengan merusak
struktur-struktur utama dari sel mikroba seperti dinding sel, sitoplasma, ribosom
dan membrane sitoplasma. Dengan adanya larutan kitosan yang bersifat asam
akan menyebabkan denaturasi protein. Keadaan ini menyebabkan inaktivasi
enzim, sehingga sistem metabolisme terganggu atau menjadi rusak dan akhirnya
tidak ada aktivitas sel mikroba. Sebagai kation kitosan mempunyai potensi untuk
mengikat banyak komponen seperti protein. Muatan positif dari gugus NH3+ pada
kitosan dapat berinteraksi dengan muatan negative pada permukaan sel bakteri.
(Helander et al, 2001).
Adanya kerusakan pada dinding sel mengakibatkan kelemahan kekuatan
dinding sel, bentuk dinding sel menjadi abnormal dan pori-pori dinding sel
membesar. Hal ini mengakibatkan dinding sel tidak mampu mengatur pertukaran
zat-zat dari dan ke dalam sel, kemudian membrane sel menjadi rusak dan
mengalami lisis sehingga aktivitas metabolisme akan terhambat dan pada
BAB 5
KESIMPULAN DAN SARAN
5.1Kesimpulan
Dari penelitian yang telah dilakukan diperoleh hasil sebagai berikut:
- Nanokitosan yang dihasilkan dari cangkang belangkas memenuhi kriteria
dari nanoteknologi, karena memiliki diameter 200 nm sebagaimana
terlihat pada analisa morfologi.
- Aktivitas antibakteri terhadap bakteri Escherichia coli lebih sensitif daripada terhadap Stapylococcus aureus dan diameter zona bening semakin besar dengan adanya penambahan logam Zn ke dalam larutan
nanokitosan. Diameter zona bening dan indeks antimikrobial terhadap
bakteri Escherichia coli 14,3 mm dan 1,38 sedangkan untuk bakteri Stapylococcus aureus 11,4 mm dan 0,90.
5.2 Saran
Untuk penelitian selanjutnya sebaiknya dilakukan pengujian terhadap aktivitas
antibakteri dengan penambahan logam seperti Fe dan menggunakan metode uji
BAB 2
TINJAUAN PUSTAKA
2.1 Kitosan
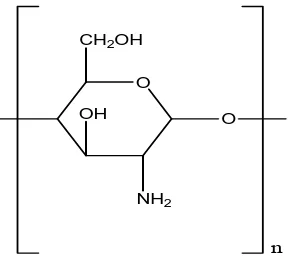
Kitosan adalah poli-(2-amino-2-deoksi-β(1-4)-D-glukopiranosa) dengan rumus molekul (C6H11NO4)n yang diperoleh dari deasetilasi kitin. Kitosan juga dijumpai
secara alamiah di beberapa organisme (Sugita, 2009).
O CH2OH
NH2
OH O
n
Gambar 2.1 Struktur Kitosan
(Mardliyati, 2010).
Proses deasetilasi kitosan dapat dilakukan dengan cara kimiawi maupun enzimatik. Proses kimiawi menggunakan basa misalnya NaOH dan dapat menghasilkan kitosan dengan derajat deasetilasi yang tinggi, yaitu mencapai 85-93%. Namun proses kimiawi menghasilkan kitosan dengan bobot molekul yang beragam dan deasetilasinya juga sangat acak, sehingga sifat fisik dan kimia kitosan tidak seragam. Selain itu proses kimiawi juga dapat menimbulkan pencemaran lingkungan, sulit dikendalikan, dan melibatkan banyak reaksi
dengan karakteristik yang lebih seragam agar dapat memperuas bidang aplikasinya (Sugita, 2009).
2.1.1 Sifat Fisika-Kimia Kitosan
Sifat dan penampilan produk kitosan dipengaruhi oleh perbedaan kondisi seperti jenis pelarut, konsentrasi, waktu, dan suhu proses ekstraksi. Kitosan dapat diperoleh dengan berbagai macam bentuk morfologi diantaranya struktur yang tidak teratur, bentuknya kristalin atau semikristalin (Harianingsih, 2010).
Kitosan merupakan padatan amorf yang berwarna putih kekuningan dengan rotasi spesifik [α]D11 -3 hingga -10o (pada konsentrasi asam asetat 2%).
Kitosan larut pada kebanyakan larutan asam organik pada pH sekitar 4,0, tetapi tidak larut pada pH lebih besar dari 6,5, juga tidak larut dalam pelarut air, alkohol, dan aseton. Dalam asam mineral pekat seperti HCl dan HNO3, kitosan larut pada
konsentrasi 0,15-1,1%, tetapi tidak larut pada konsentrasi 10%. Kitosan tidak larut dalam H2SO4 pada berbagai konsentrasi, sedangkan di dalam H3PO4 tidak larut
pada konsentrasi 1% sementara pada konsentrasi 0,1% sedikit larut. Perlu kita
ketahui, bahwa kelarutan kitosan dipengaruhi oleh bobot molekul, derajat deasetilasi, dan rotasi spesifiknya yang beragam bergantung pada sumber dan metode isolasi serta transformasinya (Sugita, 2009).
rasio padatan dan larutan yang tinggi dapat memfasilitasi proses deasetilasi menghasilkan kitosan yang memiliki siaft fisiko-kimia yang memenuhi syarat untuk berbagai aplikasi (Ramadhan, dkk. 2010).
2.1.2 Kegunaan kitosan
Kitosan telah dimanfaatkan dalam berbagai keperluan industri seperti industri kertas dan tekstil sebagai zat aditif, industri pembungkus makanan berupa film khusus, industri metalurgi sebagai adsorban untuk ion-ion metal, industri kulit untuk perekat, photografi, industri cat sebagai koagulan, pensuspensi, dan flokulasi, serta industri makanan sebagai aditif dan penghasil protein tunggal (Suptijah, dkk. 1992).
Di bidang industri, kitosan berperan antara lain sebagai koagulan polielektrolit pengolahan limbah cair, pengikat dan penyerap ion logam, mikroorganisme, mikroalga, pewarna, residu pestisida, lemak, tannin, PCB ( poliklorinasi bifenil ), mineral dan asam organik, media kromatografi afinitas gel dan pertukaran ion, penyalut berbagai serat alami dan sintetik, pembentuk film
Karena adanya gugus amino, kitosan merupakan polielektrolit kationik (pKa = 6,5), hal yang sangat jarang terjadi secara alami. Karena sifatnya yang basa ini, maka kitosan :
a. Dapat larut dalam media asam encer membentuk larutan kental, sehingga dapat digunakan untuk pembuatan gel dalam beberapa variasi konfigurasi seperti butiran, membran, pelapis kapsul, serat dan spons.
b. Membentuk kompleks yang tidak larut dalam air dengan polielektrolit anion yang dapat juga digunakan untuk pembuatan butiran gel, kapsul dan membran.
c. Dapat digunakan sebagai pengkelat ion logam berat dimana gelnya menyediakan sistem proteksi terhadap efek destruksi dari ion (Kaban, 2009).
2.1.3 Sifat Antibakteri Kitosan dan Turunannya
Sifat yang penting dari kitosan adalah muatan positif dalam larutan yang bersifat asam. Hal ini disebabkan terdapatnya amin primer pada molekul kitosan yang mengikat proton mnurut persamaan :
Chit-NH2 + H3O+ → Chit-NH3+ + H2O
Harga pKa untuk persamaan di atas sekitar 6,3. Kitosan larut apabila lebih dari
50% dari gugus asam amino diprotonasi, sehingga kelarutan dari pembuatan kitosan kebanyakan menurun dengan tajam pada saat pH larutan naik di atas 6,0-6,5. Konsentrasi yang larut maksimum bervariasi untuk kitosan yang berbeda tapi pada umumnya sekitar 10-20 gl-1 (Varum, 1994).
Salah satu pemanfaatan kitosan dalam bidang farmasi adalah kitosan dapat berperan sebagai antibakteri. Kemampuan antibakteri kitosan diakibatkan terdapatnya gugus NH3 glukosamin yang mampu berinteraksi dengan permukaan
merupakan polimer alami hasil senyawa turunan kitin sehingga diharapkan aman bagi manusia (Henry, 2007).
Aktivitas antibakteri kitosan berkorelasi erat dengan karakteristik permukaan sel mikroba tersebut. Hal ini dikarenakan muatan positif yang berasal gugus asam amino dalam suasana pH asam (dibawah 6,5) yang menyebabkan depolarisasi membran seluler mikroba sebagai akibat terganggunya integritas dinding sel dari hubungan molekul yang menyebabkan kematian bagi mikroba. Kitosan bersifat antimikroba terhadap berbagai jenis organisme target. Aktifitas sangat bervariasi dengan tipe dari kitosan, organisme target dan lingkungan dimana dilakukan aplikasi (Allan & Hadwiger, 1979).
2.2 Kitosan Nanopartikel
Nano kitosan yaitu kitosan yang memiliki pertikel yang berbentuk padat dengan ukuran sekitar 10 – 1000 nm. Kitosan dalam bentuk nanopartikel ini pun bersifat netral, tidak toksik, dan memiliki stabilitas yang konstan. Nanopartikel ini digunakan dalam berbagai aplikasi yang sangat tidak invasive. Dalam sistem
pengantaran obat, nanopartikel berperan sebagai pembawa (carrier) dengan cara melarutkan, menjebak, mengenkapsulasi, atau menempelkan obat di dalam matriksnya. Baru-baru ini, nanopartikel yang berasal dari bahan polimer digunakan sebagai sistem pengantaran obat yang potensial karena kemampuan penyebarannya di dalam organ tubuh selama waktu tertentu, dan kemampuannya untuk mengantarkan protein atau peptida (Mohanraj, 2006).
dan dibilas dengan aquades sampai netral kemudian ditempatkan pada ultrasonic bath untuk memecah partikel gel kitosan menjadi lebih kecil (Szeto, 2007).
Sebagian ahli juga mencoba metode lain untuk menyiapkan kitosan nano dengan menambahkan larutan tripoliposfat kedalam larutan kitosan sehingga diperoleh emulsi kitosan sambil distirer dengan kecepatan 1200 rpm kemudian emulsi di buat pH 3,5 dengan menambahkan asam asetat hasilnya akan berupa suspensi kitosan (Cheung, 2008).
2.3 Natrium Tripolifosfat
Natrium tripolifosfat adalah zat anorganik yang mempunyai rumus Na5P3O10 dan
mempunyai berat molekul 367,864. Natrium tripolifosfat adalah garam natrium dari polifosfat penta anion yang berbentuk bubuk putih dan merupakan konjugat basa trifosforic asam. Memiliki kelarutan dalam air 14.5 g/100 mL dan densitas 2.52 g/cm3. Digunakan sebagai komponen dari berbagai produk industri seperti
detergen. Natrium tripolifosfat dihasilkan dengan memanaskan campuran stoikiometri dinatrium fosfat (Na2HPO4) dan monosodium fosfat (NaH2PO4) pada
kondisi yang dikendalikan secara hati-hati.
2 Na2HPO4 + NaH2PO4→ Na5P3O10 + H2O
(Sagala, 2012).
2.4 Logam Seng (Zn)
Zink adalah logam yang berwarna putih-kebiruan, logam ini cukup mudah ditempa dan liat pada suhu 110-150oC. Zink melebur pada 410oC dan mendididih pada 906oC. Logamnya yang murni melarut lambat sekali dalam asam (Svehla, 1979).
Zink merupakan salah satu dari golongan logam esensial yang terdapat pada kebanyakan makanan khususnya makanan yang kadar proteinnya tinggi seperti kerang dan makanan-makanan laut. Zink dapat menimbulkan efek toksik bila dikonsumsi pada dosis tinggi. Zink tidak bersifat toksik pada manusia jika dikonsumsi 1 gram/hari tetapi berbahaya jika dikonsumsi lebih dari 10 gram/hari. Pada manusia seng merupakan unsur yang terlibat dalam sejumlah besar enzim yang mengkatalisis reaksi metabolik yang vital. Karena fasilitasnya yang digunakan dalam sintesis DNA dan RNA dan partisipasinya dalam metabolisme protein (Darmono, 1995).
2.5 Ultrasonik Bath
Ultrasonic menggunakan gelombang suara dengan frekuensi tinggi untuk proses agitasi dalam larutan. Kavitasi gelembung disebabkan oleh proses agitasi pada kontaminan yang terdapat dalam substrat. Proses ini juga berguna dalam blind-hole, peretakan dan peredaman (Todd, 1970). Proses degradasi bergantung kepada berat molekul, yaitu molekul dengan rantai panjang lebih utama dihilangkan dan polidispersitas polimer berubah. Dengan demikian degradasi dapat digunakan sebagai proses tambahan sebagai parameter dalam mengontrol distribusi berat molekul. Produk utama degradasi diperoleh ketika bahan radikal yang timbul dari kerusakan ikatan homolytic sepanjang rantai (Tabata, 1980).
volatilitas yang lebih rendah juga. Sonikasi pada suhu yang lebih tinggi atau dalam pelarut yang mudah menguap menghasilkan uap lebih banyak masuk ke gelembung dan terjadi penurunan pelunakan sehingga tingkat kekerasannya berkurang. Dalam larutan encer rantai polimer tidak terjerat dan bebas untuk bergerak dalam daerah aliran sekitar gelembung. Degradasi lebih efisien pada intensitas ultrasonik yang lebih tinggi karena semakin banyak jumlah gelembung dengan jari-jari yang lebih besar (Suslick & Price, 1999).
Efek kimia dari gelombang ultrasonik, tidak secara langsung berinteraksi dengan molekul-molekul untuk menginduksi suatu perubahan kimiawi. Ini karena panjang gelombang ultrasonik yang terlalu panjang jika dibandingkan dengan panjang gelombang molekul–molekul. Interaksi gelombang ultrasonik dengan molekul–molekul terjadi melalui media perantara berupa cairan. Gelombang yang dihasilkan oleh tenaga listrik (lewat tranduser) diteruskan oleh media cair ke medan yang dituju melalui fenomena kavitasi akustik yang menyebabkan terjadinya temperatur dan tekanan lokal ektrem dalam cairan dimana reaksi terjadi (Wardiyati et al, 2004).
2.6 Bakteri
Bakteri merupakan mikroba dengan dinding sel yang berfungsi melindungi protoplast. Protoplast terdiri dari membran sitoplasma yang memagari komponen-komponen dalam struktur lainnya antara lain ribosom dan kromosom yang ada di dalamnya. Bakteri adalah salah satu kelompok protista yang termasuk dalam prokariotik yaitu protista yang tidak memiliki membran inti (Hasyimi, 2010).
0,5 - 10μ dan lebar 0,5 – 2,5μ. Bakteri memiliki berat jenis 1,05 – 1,1 g cm-3 dan berat sekitar 10-12 g sebagai partikel kering (Buckle, 2007).
2.6.1 Bioindikator Bakteri
a. Escherichia
Berbentuk batang lurus, 1,1-1,5 μm x 2,0-6,0 μm, motil dengan flagelum peritrikus atau nonmotil. Gram negatif dan dapat tumbuh dengan mudah pada medium nutrien sederhana (Pelczar, 2005). Klasifikasi Escherichia coli adalah menurut Fardiaz (1993) adalah sebagai berikut:
Kingdom : Eubacteria Divisio : Proteobacteria
Classis : Gamma Proteobacteria
Ordo : Enterobacteriales
Familia : Enterobacteriaceae Genus : Escherichia
Species : Escherichia coli
Gambar 2.2 Bentuk koloni Escherichia coli
b. Staphylococcus
Staphylococcus aureus merupakan bakteri gram positif yang memiliki hanya satu dinding sel sehingga senyawa yang bersifat sebagai antibakteri akan lebih mudah untuk merusak dinding sel bakteri ini (Gambar 2.3). Staphylococcus aureus dapat menyebabkan beberapa macam kerugian yaitu menyebabkan makanan menjadi beracun, sindrom racun, infeksi kulit dan luka sehigga perlu diketahui senyawa yang dapat menghambat pertumbuhan bakteri ini (Kunkel, 1999).
Gambar 2.3 Bentuk koloni Staphylococcus aureus
Klasifikasi Staphylococcus aureus menurut Fardiaz (1993) adalah sebagai
berikut :
Divisio : Firmicutes Classis : Bacilli Ordo : Bacillales
Familia : Staphylococcaceae
Genus : Staphylococcus
Species : Staphylococcus aureus
Sel-sel berbentuk bola, berdiameter 0,5 sampai 1,5 μm, terdapat tunggal dan berpasangan, dan secara khas membelah diri pada lebih dari satu bidang sehingga membentuk gerombol yang tak teratur. Nonmotil dan merupakan gram positif. Tidak diketahui adanya stadium istirahat. Dinding sel mengandung dua komponen utama: peptidoglikan serta asam tekoat yang berkaitan dengannya. Kemoorganotrof, anaerob fakultatif, metabolisme dengan respirasi dan fermentatif serta tumbuh lebih cepat dan lebih banyak dalam keadaan aerobik. Suhu optimim 35 sampai 40oC. Terutama berasosiasi
dengan kulit, kelenjar kulit dan selaput lendir hewan berdarah panas. Kisaran inangnya luas dan banyak galur merupakan patogen potensial (Pelczar, 2005).
2.6.2 Pengujian Antibakteri
Pengujian mikrobiologi memanfaatkan mikroorganisme sebagai indikator pengujian. Kegunaan uji antimikroba adalah diperolehnya senyawa antibakteri yang efektif dan efisien. Terdapat bermacam-macam metode uji antimikroba seperti dijelaskan berikut ini:
1. Metoda difusi agar
a) Cara Kirby Bauer / disc diffusion
Beberapa koloni kuman dari pertumbuhan 24 jam diambil, disuspensikan ke dalam 0,5 ml BHI cair, diinkubasikan 5-8 jam pada 37°C. Suspensi ditambah akuades steril hingga kekeruhan tertentu sesuai dengan standar konsentrasi bakteri 108 CFU per ml. Kapas lidi steril dicelupkan ke dalam suspensi bakteri lalu ditekan-tekan pada dinding tabung hingga kapasnya tidak terlalu basah, kemudian dioleskan pada permukaan media agar hingga rata. Kemudian kertas samir (disk) yang mengandung antibakteri diletakkan di atasnya, diinkubasi pada 37° selama 18-24 jam. Hasilnya dibaca:
1) Zona radikal yaitu suatu daerah di sekitar disk dimana sama sekali tidak ditemukan adanya pertumbuhan bakteri. Potensi antibakteri diukur dengan mengukur diameter dari zona radikal.
2) Zona irradikal yaitu suatu daerah di sekitar disk dimana pertumbuhan bakteri dihambat oleh antibakteri tetapi tidak dimatikan.
b) Cara Sumuran / cup plat
Beberapa koloni kuman dari pertumbuhan 24 jam diambil, disuspensikan ke dalam 0,5 ml BHI cair, diinkubasikan 5-8 jam pada suhu 37°C. Suspensi ditambah akuades steril hingga kekeruhan tertentu sesuai dengan standar konsentrasi bakteri 108 CFU per ml. Kapas lidi steril dicelupkan ke dalam suspensi bakteri lalu
ditekan-tekan pada dinding tabung hingga kapasnya tidak terlalu basah, kemudian dioleskan pada permukaan media agar hingga rata. Media agar dibuat sumuran dengan garis tengah tertentu, ke dalam sumuran diteteskan larutan antibakteri kemudian diinkubasi pada 37°C selama 18-24 jam. Hasilnya dibaca seperti pada cara Kirby Bauer
c) Cara silinder plat
2. Metoda dilusi
Metode dilusi dibedakan menjadi dua, yaitu dilusi cair (broth dilution) dan dilusi padat (solid dilution).
a. Metode dilusi cair, digunakan unutk mengukur MIC atau kadar hambat minimum dan MBC atau kadar bunuh minimum. Cara yabg dilakukan adalah dengan memberi seri pengenseran agen antimikroba pada medium cair yang ditambahkan dengan mikroba uji. Larutan uji agen antimikroba pada kadar terkecil yang terlihat jernih tanpa adanya pertumbuhan mikroba uji ditetapkan sebagai KHM. Larutan yang ditetapkan sebagi KHM tersebut selanjutnya dikultur ulang pada media cair tanpa penambahan mikroba uji ataupun agen antimikroba dan diikubasi selama 18-24 jam. Media cair yang tetap terlihat jernih setelah diinkubasi ditetapkan sebagai KMB.
b. Metode dilusi padat, metode ini serupa dengan metode dilusi cair namun menggunakan media padat (soil). Keuntungan metode ini adalah suatu konsentrasi agen antimikroba yang diuji dapat digunakan untuk menguji beberapa mikroba uji (Pratiwi, 2008).
2.7 Spektroskopi FT-IR
Pengukuran pada spektrum inframerah dilakukan pada cahaya inframerah tengah (mid-infrared) yaitu pada panjang gelombang 2,5 – 50 μm atau bilangan gelombang 4000 – 200 cm-1. Energi yang dihasilkan oleh radiasi ini akan menyebabkan vibrasi atau getaran pada molekul. Pita absorbsi inframerah sangat khas dan spesifik untuk setiap tipe ikatan kimia atau gugus fungsi. Spektrum yang dihasilkan berupa grafik yang menunjukkan persentase transmitan yang bervariasi pada setiap frekuensi radiasi inframerah (Dachriyanus, 2004).
Jumlah energi yang diserap juga bervariasi untuk setiap ikatan. Hal ini disebabkan terjadinya perubahan momen ikatan suatu absorbsi. Ikatan non polar (C-H atau C-C) pada umumnya akan memberikan absorbansi lemah, sedangkan ikatan polar (C-O) akan terlihat sebagai absorbansi yang kuat. Spektroskopi FTIR dapat digunakan untuk analisa kualitatif maupun kuantitatif. Analisa kualitatif spektroskopi FTIR secara umum dipergunakan untuk identifikasi ggus-gugus fungsional yang terdapat dalam suatu senyawa yang dianalisa (Silverstein, 1986).
Analisa kuantitatif dari spektroskopi FTIR dapat dilakukan berdasarkan spektra inframerah yang dihasilkan, salah satu contohnya adalah penentuan derajat deasetilasi dari kitin dan kitosan menggunakan persamaan Domszy dan
Roberts (Sugita, 2009).
dimana : A1655 = absorbansi pada bilangan gelombang 1655 cm-1
A3450 = absorbansi pada bilangan gelombang 3450 cm-1
1,33 = tetapan yang diperoleh dari perbandingan A1655 / A3450
2.8Scanning Elektron Microscopy (SEM)
SEM adalah alat yang dapat membentuk bayangan permukaan spesimen secara makroskopik. Berkas elektron dengan diameter 5-10 nm diarahkan pada spesimen interaksi berkas elektron dengan spesimen menghasilkan beberapa fenomena yaitu hamburan balik berkas elektron, sinar x, electron sekunder, absorbs elektron. Adanya material lain dalam suatu matriks seperti dispersi material tersebut menyebabkan terjadinya perubahan pada permukaan spesimen. Untuk melihat parubahan dalam bahan tersebut dapat dilakukan suatu analisa permukaan, dimana alat yang biasa digunakan adalah SEM.
Teknik SEM pada hakikatnya merupakan pemeriksaan dan analisa permukaan. Data atau tampilan yang diperoleh adalah data dari permukaan atau dari lapisan yang tebalnya sekitar 20 µm dari permukaan yang diperoleh merupakan gambar tofografi dengan segala tonjolan, lekukan, dan lubang permukaan. Gambar tofografi diperoleh dari penangkapan elektron sekunder yang dipancarkan oleh spesimen. Sinyal elektron sekunder yang dihasilkan ditangkap oleh detektor dan diteruskan ke monitor. Pada monitor akan diperoleh gambar yang khas yang menggambarkan struktur permukaan spesimen. Selanjutnya
gambar di monitor dapat dipotret dengan menggunakan film hitam putih atau dapat pula direkam kedalam suatu disket. (wirjosentono, 1996)
BAB 1
PENDAHULUAN
1.1Latar Belakang
Dalam beberapa tahun terakhir penerapan antimikroba alami telah mendapat
perhatian yang serius. Eksplorasi biopolimer alami seperti polisakarida dan
protein (enzim/biokatalis) sekarang ini mendapat banyak perhatian di berbagai
bidang karena biokompabilitas, biodegradabilitas serta tidak beracun dan
memiliki potensi untuk digunakan sebagai antibakteri alami. Permintaan akan
biopolimer juga terus meningkat seiring dengan kebutuhannya untuk keperluan
sintesa berbagai bahan obat-obatan yang kompleks, bahan industri makanan,
pakan, serta bahan-bahan kimia tertentu untuk berbagai keperluan (Wibowo,
2008).
Kitosan sangat menarik dan dianggap penting karena kombinasi unik dari
sifat-sifatnya seperti pengkompleks logam dan memiliki aktivitas antibakteri.
Aktivitas antibakteri dari kitosan telah dieksplor secara luas. Sejumlah turunan
kitosan dengan modifikasi yang berbeda telah disiapkan untuk meningkatkan
aktivitas antibakteri. Baru-baru ini kompleks kitosan dengan logam yang berbeda
telah disiapkan untuk meningkatkan aktivitas antibakteri, seperti kompleks
kitosan Ag+ dan kompleks kitosan Cu2+ menunjukkan aktivitas antibakteri yang
tinggi in vitro (Li Du et al. 2009).
Penggunaan bahan alam dan pemanfaatan limbah sebagai bahan baku
merupakan salah satu alternatif yang menjanjikan baik dari segi keamanan
maupun ekonomi karena Indonesia merupakan negara kepulauan terbesar di
dunia, dengan keanekaragaman hayatinya, sehingga menyimpan potensi yang luar
Salah satu limbah yang sangat potensial untuk diolah di Indonesia adalah
limbah cangkang belangkas (Tachypleus gigas), yang dapat diolah menjadi kitin dan kitosan dengan rentang pemanfaatan yang luas, dapat diaplikasikan di bidang
nutrisi, pangan, medis, kosmetik, lingkungan, dan pertanian. Kitosan yang
dihasilkan dari belangkas kadarnya lebih tinggi serta memiliki kandungan abu dan
logam berat yang rendah (Suhartono, 2006).
Kitosan adalah polisakarida alami hasil dari proses deasetilasi
(penghilangan gugus-COCH3) kitin. Kitin merupakan penyusun utama
eksoskeleton dari hewan air golongan crustacea seperti kepiting dan udang. Kitin
tersusun dari unit-unit N-asetil-D-glukosamin
(2-asetamida-2-deoksi-D-glukopiranosa) yang dihubungkan secara linier melalui ikatan β-(1→4). Kitin
berwarna putih, keras, tidak elastis, merupakan polisakarida yang mengandung
banyak nitrogen, sumber polusi utama di daerah pantai (Goosen, 1997).
Nanopartikel dibuat dari polimer alami atau polimer buatan dengan ukuran
10-1000 nm. Satu nanometer adalah 10-9 m. Sehingga nanopartikel mempunyai
luas permukaan yang lebih besar. Kitosan nanopartikel tripoliposfat telah
disintesis dan digunakan secara umum sebagai pembawa obat seperti dilaporkan
pada penelitian sebelumnya (Li Du et al. 2009).
Dewi (2010) telah meneliti pengaruh waktu ultrasonik bath terhadap
karakterisasi kitosan nanopartikel, dimana semakin lama waktu penggunaan
ultrasonik bath maka nilai derajat deasetilasinya semakin meningkat. Li Du et al. (2009) telah membuat kompleks kitosan nanopatikel dengan logam Cu2+ yang
menunjukkan aktivitas antibakteri yang tinggi in vitro. Sedangkan menurut Tsai
dan Su (1999) telah meneliti adanya efek bakterial dari kitosan udang terhadap
Escherichia coli. Yamamoto (2001) juga melaporkan bahwa aktivitas antibakteri
meningkat dengan menurunnya ukuran partikel. Adams et al (2006) melaporkan
bahwa ZnO memiliki efek yang lebih baik pada mikroorganisme dari oksida
Berdasarkan latar belakang ini, peneliti tertarik untuk meneliti tentang
pembuatan kitosan nanopartikel dari cangkang belangkas (Tachypleus gigas) dengan tripolifosfat yang bermuatan ion logam Zn2+ untuk uji aktivitas bakteri.
1.2 Permasalahan
Bagaimana pembuatan kitosan nanopartikel dari cangkang belangkas
dengan tripolifosfat yang bermuatan ion logam Zn2+ untuk uji aktivitas bakteri.
1.3 Pembatasan Masalah
Penelitian ini hanya dibatasi pada penyediaan kitosan nanopartikel dari
cangkang belangkas dengan tripolifosfat yang bermuatan ion logam Zn2+ dengan
konsentrasi 0,3% serta aktivitas antibakterinya terhadap Escherichia coli dan
Staphylococcus aureus.
1.4 Tujuan penelitian
Tujuan dari penelitian ini untuk melakukan pembuatan kitosan
nanopartikel dari cangkang belangkas dengan tripolifosfat yang bermuatan ion
logam Zn2+ untuk uji aktivitas antibakteri.
1.5 Manfaat Penelitian
Dari hasil penelitian ini diharapkan dapat memberikan informasi tentang
kegunaan kitosan nanopartikel dari cangkang belangkas dengan tripolifosfat yang
bermuatan ion logam Zn2+ sebagai antibakteri serta dapat diterapkan dalam bidang
1.6 Lokasi penelitian
Penelitian ini dilakukan di Laboratorium Penelitian FMIPA USU, di
Laboratorium Mikrobiologi FMIPA USU, Laboratorium Kimia Organik FMIPA
UGM dan Laboratorium Fisika FMIPA UNIMED.
1.7 Metodologi Penelitian
Penelitian ini adalah eksperimental laboratorium, dimana kitosan diubah
menjadi kitosan nanopartikel dengan cara melarutkan kitosan sebanyak 3 g
didalam 1000 ml asam asetat 1%, diaduk hingga homogen. Kemudian 1000 mL
larutan kitosan ditambahkan 40 mL larutan tripolifosfat kemudian diaduk hingga
homogen dengan menggunakan pengaduk selama 20 menit. Diletakkan pada
ultarasonik bath selama 30 menit. Disentrifugasi pada 1.200 rpm selama 10 menit
kemudian didekantasi. Endapan dimasukkan ke dalam freeze dryer untuk
menghasilkan kitosan nanopartikel kemudian diuji karakterisasinya dengan SEM
dan FT-IR. Kitosan nanopartikel dilarutkan dalam asam asetat 1% ditambahkan
larutan ion Zn2+ hingga konsentrasi 120 μg/mL dan diaduk selama 12 jam pada
temperatur kamar. Larutan tersebut dicetak film pada plat kaca. Film tersebut
dikeringkan hingga benar-benar kering kemudian diuji karakterisasinya dengan
FTIR dan diuji aktivitas antibakterinya dengan mengukur diameter zona bening
PEMBUATAN KITOSAN NANOPARTIKEL DARI CANGKANG BELANGKAS (Tachypleus gigas) DENGAN TRIPOLIFOSFAT
YANG BERMUATAN ION LOGAM Zn2+ UNTUK UJI
AKTIVITAS BAKTERI
ABSTRAK
Telah dilakukan penelitian untuk pembuatan kitosan nanopartikel dari cangkang belangkas (tachypleus gigas) dengan ukuran partikel nanokitosan yang dihasilkan 200 nm. Pengujian aktivitas antibakteri kitosan nanopartikel dari cangkang belangkas (tachypleus gigas) dengan tripolifosfat yang bermuatan ion logam Zn2+
terhadap bakteri Escherichia coli dan Stapylococcus aureus menggunakan metode difusi cakram. Hasil uji pengaruh kitosan nanopartikel dan kitosan nanopartikel yang bermuatan ion logam Zn2+ menunjukkan aktivitas antibakteri terhadap
bakteri Escherichia coli lebih sensitif daripada terhadap Stapylococcus aureus dan diameter zona bening semakin besar dengan adanya penambahan logam Zn ke dalam larutan nanokitosan. Diameter zona bening dan indekas antimikrobial terhadap bakteri Escherichia coli 14,3 mm dan 1,38 sedangkan untuk bakteri Stapylococcus aureus 11,4 mm dan 0,90.
PREPARATION OF NANOPARTICLES CHITOSAN FROM HORSESHOE CRAB SHELLS (Tachypleus gigas) WITH
TRIPOLYPHOSFAT LOADED Zn2+ METAL ION FOR
BACTERIAL ACTIVITY
ABSTRACT
Research has been done of nanoparticles chitosan from horseshoe crab shells (tachypleus gigas) with a particle size nanokitosan produced 200 nm. Testing of antibacterial activity of chitosan nanoparticles of horseshoe crab shells (tachypleus gigas) with tripolyphosphate loaded metal ions Zn2+ against
Escherichia coli and Stapylococcus aureus used the disc diffusion method . The results of test and the effect of chitosan nanoparticles and chitosan nanoparticles loaded with metal ions Zn2+ showed antibacterial activity against Escherichia coli
bacteria are more sensitive than the Stapylococcus aureus and the larger the diameter of the clear zone with the addition of Zn metal into solution nanokitosan. Diameter of clear zone and indeks antimicrobials against Escherichia coli 14.3 mm and 1,38 while Stapylococcus aureus 11.4 mm and 0,90.
PEMBUATAN KITOSAN NANOPARTIKEL DARI
CANGKANG BELANGKAS (Tachypleus gigas) DENGAN
TRIPOLIFOSFAT YANG BERMUATAN ION LOGAM
Zn
2+UNTUK UJI AKTIVITAS BAKTERI
SKRIPSI
RAISSA ADELIA HARAHAP
090802035
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
MEDAN
PEMBUATAN KITOSAN NANOPARTIKEL DARI CANGKANG BELANGKAS (Tachypleus gigas) DENGAN TRIPOLIFOSFAT
YANG BERMUATAN ION LOGAM Zn2+ UNTUK UJI
AKTIVITAS BAKTERI
SKRIPSI
Diajukan untuk melengkapi tugas dan memenuhi syarat mencapai gelar Sarjana Sains
RAISSA ADELIA HARAHAP 090802035
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATERA UTARA
PERSETUJUAN
Judul : Pembuatan Kitosan Nanopartikel Dari Cangkang
Belangkas (Tachypleus gigas) Dengan
Tripolifosfat Yang Bermuatan Ion Logam Zn2+
Untuk Uji Aktivitas Bakteri
Kategori : Skripsi
Nama : Raissa Adelia Harahap
Nim : 090802035
Program studi : Sarjana (S1) Kimia
Departemen : Kimia
Fakultas : Matematika Dan Ilmu Pengetahuan Alam
Universitas Sumatera Utara
Disetujui di
Medan, Desember 2013
Komisi Pembimbing :
Pembimbing 2 Pembimbing 1
Prof.Dr. Zul Alfian,M.Sc Prof.Dr.Harry Agusnar, M.Sc, M.Phil
NIP.195504051983031002 NIP.195308171983031002
Diketahui/Disetujui oleh
Departemen Kimia FMIPA USU Ketua,
PERNYATAAN
PEMBUATAN KITOSAN NANOPARTIKEL DARI CANGKANG BELANGKAS (Tachypleus gigas) DENGAN TRIPOLIFOSFAT
YANG BERMUATAN ION LOGAM Zn2+ UNTUK UJI
AKTIVITAS BAKTERI
SKRIPSI
Saya mengakui bahwa skripsi ini adalah hasil kerja saya sendiri, kecuali beberapa kutipan dan ringkasan yang masing-masing disebutkan sumbernya.
Medan, Desember 2013
PENGHARGAAN
Puji dan syukur penulis ucapkan kepada Allah SWT yang dengan segala curahan rahmat, kasih dan sayang-Nya penelitian dan skripsi ini dapat diselesaikan sebagai salah satu persyaratan untuk meraih gelar Sarjana Sains pada jurusan Kimia di Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Sumatera Utara. Serta shalawat dan salam kepada Rasulullah Muhammad SAW, yang membuka jalan kebenaran kepada seluruh pengikutnya.
Penulis menyampaikan penghargaan dan cinta kasih yang tulus dan terdalam kepada Ayahanda tersayang H.Harapan Harahap dan Ibunda tercinta Marmina Rahayu atas segala doa, bimbingan, semangat, waktu dan pengorbanan yang telah diberikan kepada saya sehingga saya bisa menyelesaikan studi saya sampai sekarang ini. Dan saudara-saudara saya Raad Al-farizi Harahap, ST, Ferry Saputra Harahap dan Rima Aulia Harahap semoga kita dapat meraih impian kita. Terkhusus buat Nenek Hj.Raisa Zaharo Siregar, yang tiada henti memberikan doa, cinta, kasih sayang, dan dukungan materi dan semangat yang tak terhingga untuk menyelesaikan skripsi ini.
Ucapan terima kasih penulis kepada Bapak Prof. Dr. Harry Agusnar, M.Sc, M.Phill selaku dosen pembimbing 1 dan Bapak Prof. Dr. Zul Alfian, M.Sc selaku dosen pembimbing 2 yang telah banyak memberikan arahan, bimbingan, masukan dan saran sehingga skripsi ini dapat terselesaikan dengan baik. Ibu Dr. Rumondang Bulan Nst, MS dan Bapak Drs. Albert Pasaribu, M.Sc selaku ketua dan sekretaris departemen Kimia FMIPA USU. Bapak dan Ibu dosen yang telah memberikan ilmunya selama masa studi penulis di FMIPA USU, terkhusus kepada Bapak Dr. Adil Ginting, M.Sc selaku dosen wali yang telah memberikan masukan dan bimbingan demi kelancaran kuliah penulis. Seluruh rekan-rekan asisten Laboratorium Kimia Dasar LIDA USU yang telah memberikan dukungan. Teman-teman terdekat penulis Ayu, Indah, Dwi, Deasy, Rina, Mira, Ilman, Irwanto dan teman-teman stambuk 2009 yang telah memberikan semangat selama masa perkuliahan sampai saat ini. Juga tidak lupa kepada kak Ria selaku asisten laboratorium Mikrobiologi atas bantuan dan fasilitas yang disediakan. Serta untuk teman terbaik penulis Yulia Yuha dan Misra mi’ya yang tetap memberikan motivasi kepada penulis.
Penulis,
PEMBUATAN KITOSAN NANOPARTIKEL DARI CANGKANG BELANGKAS (Tachypleus gigas) DENGAN TRIPOLIFOSFAT
YANG BERMUATAN ION LOGAM Zn2+ UNTUK UJI
AKTIVITAS BAKTERI
ABSTRAK
Telah dilakukan penelitian untuk pembuatan kitosan nanopartikel dari cangkang belangkas (tachypleus gigas) dengan ukuran partikel nanokitosan yang dihasilkan 200 nm. Pengujian aktivitas antibakteri kitosan nanopartikel dari cangkang belangkas (tachypleus gigas) dengan tripolifosfat yang bermuatan ion logam Zn2+ terhadap bakteri Escherichia coli dan Stapylococcus aureus menggunakan metode difusi cakram. Hasil uji pengaruh kitosan nanopartikel dan kitosan nanopartikel
yang bermuatan ion logam Zn2+ menunjukkan aktivitas antibakteri terhadap
bakteri Escherichia coli lebih sensitif daripada terhadap Stapylococcus aureus dan diameter zona bening semakin besar dengan adanya penambahan logam Zn ke dalam larutan nanokitosan. Diameter zona bening dan indekas antimikrobial
terhadap bakteri Escherichia coli 14,3 mm dan 1,38 sedangkan untuk bakteri
Stapylococcus aureus 11,4 mm dan 0,90.
PREPARATION OF NANOPARTICLES CHITOSAN FROM HORSESHOE CRAB SHELLS (Tachypleus gigas) WITH
TRIPOLYPHOSFAT LOADED Zn2+ METAL ION FOR
BACTERIAL ACTIVITY
ABSTRACT
Research has been done of nanoparticles chitosan from horseshoe crab shells (tachypleus gigas) with a particle size nanokitosan produced 200 nm. Testing of antibacterial activity of chitosan nanoparticles of horseshoe crab shells (tachypleus gigas) with tripolyphosphate loaded metal ions Zn2+ against Escherichia coli and Stapylococcus aureus used the disc diffusion method . The results of test and the effect of chitosan nanoparticles and chitosan nanoparticles loaded with metal ions Zn2+ showed antibacterial activity against Escherichia coli bacteria are more sensitive than the Stapylococcus aureus and the larger the diameter of the clear zone with the addition of Zn metal into solution nanokitosan. Diameter of clear zone and indeks antimicrobials against Escherichia coli 14.3 mm and 1,38 while Stapylococcus aureus 11.4 mm and 0,90.
DAFTAR ISI
Daftar Lampiran xi
Bab 1 Pendahuluan 1
1.7 Metodologi Penelitian 4
Bab 2 Tinjauan Pustaka 5
2.1 Kitosan 5
2.1.1 Sifat Fisika-Kimia Kitosan 6
2.1.2 Kegunaan Kitosan 7
2.1.3 Sifat Antibakteri Kitosan dan Turunannya 8
2.2 Kitosan Nanopartikel 9
2.3 Natrium Tripolifosfat 10
2.4 Logam Seng (Zn) 11
2.5 Ultrasonik Bath 11
2.6 Bakteri 12
2.6.1 Bioindikator Bakteri 13
2.6.2 Pengujian Antibakteri 15
2.7 Spektroskopi FT-IR 17
2.8 SEM (Scanning Electron Microscopy) 19
Bab 3 Metodologi Penelitian 21
3.1 Alat dan Bahan 21
3.1.1 Alat-alat 21
3.1.2 Bahan-bahan 21
3.2 Prosedur Penelitian 22
3.2.1 Pembuatan Larutan Pereaksi 22
3.2.2 Pembuatan Kitosan Nanopartikel 22
3.2.3 Pembuatan Kitosan Nanopartikel yang Bermuatan Ion
Logam 23
3.2.4 Pembuatan Media Padat Nutrient Agar (NA) 23
3.3.6 Penyediaan Biakan Stok Bakteri 24
3.2.7 Penentuan Aktivitas Antibakteri 24
3.3 Bagan penelitian 25
3.3.1 Pembuatan Larutan Kitosan 0,3% 25
3.3.2 Pembuatan Kitosan Nanopartikel 25
3.3.3 Pembuatan Kitosan Nanopartikel yang Bermuatan Ion
Logam 26
3.3.4 Pembuatan Media Padat Nutrient Agar (NA) 27
3.3.5 Pembuatan Media Padat Muller Hinton Agar (MHA) 28
3.3.6 Penyediaan Biakan Stok Bakteri 28
3.3.7 Penentuan Aktivitas Antibakteri 29
Bab 4 Hasil dan Pembahasan 30
4.1 Hasil Penelitian 30
4.1.1 Uji Aktivitas Antibakteri 30
4.2 Pengolahan Data 31
4.2.1 Mencari Nilai Indeks Antimikrobial dari Kitosan Nanopartikel Terhadap Bakteri
Escherichia coli dan Staphylococcus aureus 31
4.3 Pembahasan 32
4.3.1 Pembuatan Kitosan Nanopartikel 32
4.3.2 Pembuatan Kitosan Nanopartikel yang Bermuatan
Ion Logam Zn2+ 32
4.3.3 Analisa Spektrum FT-IR 34
4.3.4 Analisa Scanning Elektron Microcopy (SEM) 35
Bab 5 Kesimpulan dan Saran 38
5.1 kesimpulan 38
5.2 Saran 38
Daftar Pustaka 39
DAFTAR TABEL
Nomor Judul Halaman
Tabel
4.1. Data Diameter Zona Hambat (mm) Kitosan Nanopartikel
Terhadap Bakteri Escherichia coli dan Staphylococcus aureus 30
4.2. Indeks Antimikrobial Kitosan Nanopartikel Terhadap Bakteri
DAFTAR GAMBAR
Nomor Judul Halaman
Gambar
2.1. Struktur Kitosan 5
2.2. Bentuk Koloni Escherichia coli 14
2.3. Bentuk Koloni Staphylococcus aureus 14
4.1. Spektrum FT-IR Kitosan Nanopartikel 33
4.2. Spektrum FT-IR Kitosan Nanopartikel yang Bermuatan
Ion Logam Zn2+ 34
DAFTAR LAMPIRAN
Nomor Judul Halaman
Lamp
1. Spektrum FT-IR 42
2. Foto Uji Bakteri 45
3. Perhitungan Indeks Antimikrobial 45