Lampiaran 3. Identifikasi Tumbuhan Bawang Batak
Lampiran 4. Pembuatan Variasi Konsentrasi Sampel • Pembuatan larutan 1000 ppm
0,025 mg 25 ml X 10
6
=
= 1000 ppm
• Dibuat Konsentrasi Sampel 100 ppm dari larutan induk 1000 ppm dalam labu takar 25 mL
V1.N1 = V2.N2 V1.1000 = 25.100 V1 = 2,5 mL
• Dari Konsentrasi Sampel 100 ppm dibuat konsentrasi 50 ppm dalam labu takar 25 ml V1.N1 = V2.N2
V1.100 = 25.50 V1 = 12,5 mL
• Dari Kosentrasi Sampel 50 ppm dibuat konsentrasi 5, 10, 15 dan 20 ppm.
Lampiran 5. Hasil Uji Aktivitas Antioksidan Perhitungan % peredaman Ekstrak Bawang
1. PENGUKURAN ABSORBANSI BAWANG MERAH (Allium cepa L.) No Konsentrasi Absorbansi ∑
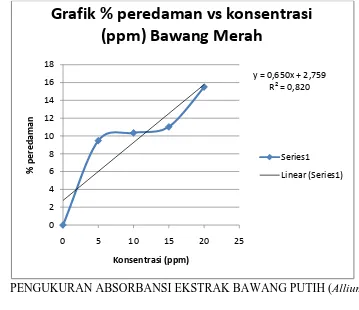
Perhitungan % Perendaman Ekstrak Bawang Merah % Peredaman = ������� −�������
������� x 100 %
1. Konsentrasi 5 ppm % peredaman = 1,035−0,937
1,035 x 100 % = 9,4686 %
2. Konsentrasi 10 ppm % peredaman =1,035−0,928
1,035 x 100 % = 10,3381 %
3. Konsentrasi 15 ppm % peredaman = 1,035−0,921
1,035 x 100 % = 11,0145 %
4. Konsentrasi 20 ppm % peredaman = 1,035−0,872
1,035 x 100 % = 15,7488 %
Perhitungan Nilai IC 50 Ekstrak Bawang Merah
X Y XY X2
a = � ( ���)−(��)(��) �( ��2)− (��)2
=5 (630,9175)−(50)(46,57)
5 (750)− (50)2
= 3154 ,5875−2328 ,8
3750−2500
= 825,7875
1250
= 0,6606
b = (��)
2 (��)−(��)(���)
�(��2)− (��)2
= (750)(46,57)−(50)(630,9175)
5 (750)− (50)2
= 3381 ,625
1250
= 2,7053
Persamaan regresi Y = 0,6606X + 2,7053 Nilai IC50 :
50 = 0,6606 X + 2,7053 0,6606 X = 50 – 2,7053
2. PENGUKURAN ABSORBANSI EKSTRAK BAWANG PUTIH (Allium sativum L.)
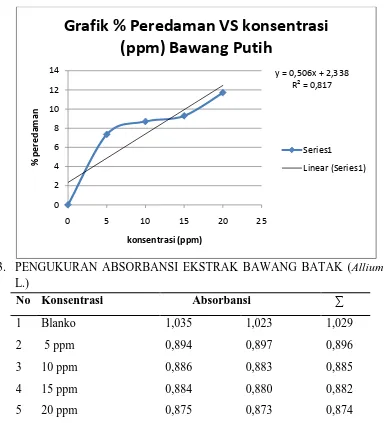
Perhitungan % Perendaman Ekstrak Bawanag Putih % Peredaman = ������� −�������
������� x 100 %
1. Konsentrasi 5 ppm % peredaman = 1,035−0,959
1,035 x 100 % = 7,3429 %
2. Konsentrasi 10 ppm % peredaman =1,035−0,945
1,035 x 100 % = 8,6956 %
3. Konsentrasi 15 ppm % peredaman = 1,035−0,939
Grafik % peredaman vs konsentrasi
(ppm) Bawang Merah
Series1
4. Konsentrasi 20 ppm % peredaman = 1,035−0,914
1,035 x 100 % = 11,6908 %
Perhitungan Nilai IC 50 Ekstrak Bawang Putih
X Y XY X2
X = Konsentrasi (ppm) Y = % Peredaman
Persamaan regresi Y = 0,4663X + 2,7381 Nilai IC50 :
50 = 0,4663 X + 2,7381 0,4663 X = 50 – 2,7381
3. PENGUKURAN ABSORBANSI EKSTRAK BAWANG BATAK (Allium chinense
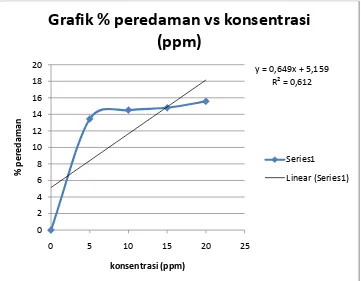
Perhitungan % Perendaman Ekstrak Bawanag Batak % Peredaman = ������� −�������
������� x 100 %
1. Konsentrasi 5 ppm % peredaman = 1,035−0,896
1,035 x 100 % = 13,4299 %
2. Konsentrasi 10 ppm % peredaman =1,035−0,885
Grafik % Peredaman VS konsentrasi
(ppm) Bawang Putih
Series1
3. Konsentrasi 15 ppm % peredaman = 1,035−0,882
1,035 x 100 % = 14,7826 %
4. Konsentrasi 20 ppm % peredaman = 1,035−0,874
1,035 x 100 % = 15,5556 %
Perhitungan Nilai IC 50 Ekstrak Bawang Merah
X Y XY X2
X = Konsentrasi (ppm) Y = % Peredaman
= (750)(58,2609)−(50)(734,9285)
5 (750)− (50)2
= 43695 ,675 −36746 ,425
1250
= 5,5594
Persamaan regresi Y = 0,5733X + 5,5594 Nilai IC50 :
50 = 0,5733 X + 5,5594 0,5733 X = 50 – 5,5594
y = 0,649x + 5,159
Grafik % peredaman vs konsentrasi
(ppm)
Series1
Lampiran 6. Pengujian Sulfur
Gambar L 6.1 Sebelum ditambah dengan NaOH dan AgNO3
Gambar L 6.2 Setelah ditambah dengan NaOH dan AgNO3
Lampiran 7. Pengujian senyawa Saponin
Gambar L 7.1 Pengujian saponin pada bawang merah
Gambar L 7.2 Pengujian senyawa saponin pada bawang putih
DAFTAR PUSTAKA
Acmad, S. 1986. Kimia Organik Bahan Alam. Universitas Terbuka. Jakarta
Anonim. 1998. Pedoman Bertanam Bawang. Penerbit Kanisius (Anggota IKAPI). Yogyakarta.
Anonim. 1999. Bawang Putih Dataran Rendah. PT. Penebar Swadaya (Anggota IKAPI). Bogor.
Bintang, M. 2010. Biokimia Teknik Penelitian. Erlangga. Departemen Biokimia Fakultas Mate-matika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Hidayah, A. S, dkk. 2015. Uji Aktivitas Antioksidan Umbi Bawang Dayak
(Euletherinebulbosa Merr.). Program Pendidikan Farmasi FMIPA, Universitas
Islam Bandung, Jl. Taman Sari No.1 Bandung
Kumalaningsih, S. 2006. Antioksidan Alami. Trubus Agrisarana. Surabaya.
Kosasih, E. N. 2004. Peran Antioksidan Pada Lanjut Usia. Jakarta :Pusat Kajian Nasional Masalah Lanjut Usia.
Pratiwi, D, dkk. 2015. Uji Aktivitas Antioksidan Daun Bawang Mekah (Eleutherina
Americana Merr.) Dengan Metode DPPH (2,2 Difenil -1- Fikrihidrazil).
Department Of Pharmacy, Faculty Of Medicine. Universitas Tangjungpura Pontianak. Kalimantan Barat
Pokornya, J.,Yanishlieva, N and Gordon, N. 2001.Antioxidants in Food. England :Woodhead Publishing Limited.
Rukmana, R. 1994. Bawang Merah. Penerbit Kanisius (Anggota IKAPI). Yogyakarta.
Rahayu, E., Nur Berlian V.A. 1999. Bawang Merah. PT. Penebar Swadaya (Anggota IKAPI). Bogor.
Siagian, P. 2012. Keajaiban Antioksidan. Jakarta :KompasGramedia.
Sianipar, J. F. 2015. Karakterisasi Morfologi Bawang Merah Lokal Samosir (Allium
Ascalonicum L.) Pada Beberapa Aksesi di Kecamatan Bakti Raja. Progam
Pendidikan Agroekoteknologi, Fakultas Pertanian. Universitas Sumatera Utara.
Sirait, M. 2011. Penuntun Fitokimia Dalam Farmasi. Institut Teknologi Bandung (ITB). Bandung.
Soebagio, B ,dkk. 2007. Pembuatan Gel Dengan Aqupec HV-505 Dari Ekstrak Umbi
Bawang Merah (Allium Cepa L.) Sebagai Antioksidan. Fakultas Farmasi,
Universitas Padjajaran. Bandung
Vadevanam, K., Srijayanta, S.,O’Reilly, J. 1999. Antiocxidant Action And Potential
Antidiabetic Of An Isovavonoid-Containing Soyabeen Phytochemical Extrak (SPE). Phytother Res.
Visner, G .A.,Dougall , W C.,Wilson, J M.1990. Regulation Of Manganese Superoxide
Dismutase By Lyppopolysaccharide, Interleukin-1, And Tumor Necrosis Factor. J Biol Chem.
Wibowo, S. 1987. Budi Daya Bawang : Bawang Putih, Bawang Merah, Bawang
Bombay . Penebar Swadaya Seri Agribisnis. Jakarta.
Winarsi, H. 2005. Isoflavon : Berbagai Sumber, Sifat Dan Manfaatnya Pada Penyakit
Degeneratif. Gajah Mada University Press. Yogyakarta.
Wijaya, A. 1996. Radikal Bebas dan Parameter Status Antioksidan. Forum Diagnosticum, Lab Klinik Prodia.
Yuliarti, N. 2007. Awas Bahaya Dibalik Lezatnya Makanan. CV.Andi Offset. Yokyakarta.
Yu Lin, H.Kuo, Y.H.Lin, Y.L. dan Chiang,W.2009.Antioxiodative effect and active
components from leaves of lotus (NelumboNucifera). Journal of Agricultural
and Food Chemistry.
Zakaria, F. R.,Nurrahman. 2003. Antioxidant And Immunoenhancement activities of
BAB 3
METODE PENELITIAN
3.1. Alat-alat
- Gelas Erlenmeyer Pyrex
- Gelas ukur Pyrex
- Beker glass Pyrex
- Labu ukur Pyrex
- Tabung reaksi Pyrex
- Pipet Volume Pyrex
- Bola Karet - Botol Vial - Pipet tetes - Aluminium foil - Kapas
- Neraca analitis Mettler AE 2000
- Spektrofotometer UV-Visible 1240 Shimadzu
- Lemari pendingin Toshiba
3.2. Bahan- bahan - Bawang Merah - Bawang Putih
- Bawang Batak/ Bawang Lokio - Aquades
- DPPH(2,2-diphenyl-1-picryl –hydrazil) p.a Aldrich
3.3. Prosedur Penelitian 3.3.1. Penyediaan Sampel
Bahan yang digunakan dalam penelitian adalah bawang merah, bawang putih dan bawang batak/bawang lokio yang diperoleh dari daerah samosir.
3.3.2. Pembuatan ekstrak air dari bawang
Bawang di kupas dan ditimbang sebanyak 150 gram. Masing -masing bawang dihaluskan dengan menggunakan blender kemudian di masukkan ke dalam enlenmeyer, di tambahkan aquadest sebanyak 600 ml, ditutup rapat dengan menggunakan plastic dan karet selanjutnya didiamkan selama 24 jam. Setelah didiamkan selama 24 jam, di pisahkan antara filtrat dan residunya dengan cara penyaringan. Selanjutnya filtrat dari bawang tersubut dipanaskan di atas penangas air sampai seluruh airnya menguap.
3.3.3. Pengujian Skrining Fitokimia 3.3.3.1. Pemeriksaan Sulfur
Tes ini digunakan untuk mengetahui adanya unsur belerang dalam sampel. Untuk mengetahui adanya unsur belerang dalam suatu sampel diuji dengan menambahkan sampel dengan NaOH, kemudian di tambahkan beberapa tetes larutan argentum nitrat (AgNO3) . Akan terbentuk larutan berwarna hitam, ini menunjukkan adanya unsur belerang dalam sampel.
Sampel + 2NaOH Na2S2O3 + H2O Na2S2O3 + AgNO3 Ag2S2O3 + NaNO3
( hitam )
3.3.3.2. Pemeriksaan Saponin
Sebanyak 0,5 gram ekstrak bawang dimasukkan kedalam tabung reaksi, lalu dilarutkan dengan aquadest, kemudian dikocok kuat-kuat selama 10 detik. Adanya terbentuk busa yang stabil menunjukkan adanya saponin.
3.3.4. Uji Sifat Antioksidan Ekstrak Bawang Dengan Metode DPPH 3.3.4.1. Pembuatan Larutan DPPH
Larutan DPPH 0,3mM dibuat dengan melarutkan 11,83 mg serbuk DPPH dalam etanol p.a dalam labu takar 100 ml, kemudian dihomogenkan.
3.3.4.2. Pembuatan Variasi Konsentrasi Ekstrak Bawang
Ekstrak bawang dibuat larutan induk 1000 ppm ; dengan melarutkan 0,025 g bawang dengan pelarut etanol p.a dalam labu takar 25 ml. Kemudian dari larutan induk dibuat larutan 100 ppm, dari larutan 100 ppm dibuat lagi larutan induk 50 ppm, dari larutan induk 50 ppm dibuat variasi konsentrasi 5, 10, 15, dan 20 ppm untuk uji aktivitas antioksidan.
3.3.4.3. Uji Aktivitas Antioksidan
a. Uji Aktivitas Antioksidan Larutan Blanko
Sebanyak 2,5 ml aquadest di tambahkan 1 ml larutan DPPH 0,3mM dalam tabung reaksi dihomogenkan dan dibiarkan selama 30 menit pada ruang gelap. Setelah itu, diukur absorbansi dengan panjang gelombang maksimum 515 nm.
b. Uji Aktivitas Antioksidan Sampel
3.4. Bagan Penelitian
3.4.1. Pembuatan esktrak air dari bawang
150 gram Bawang Merah dikupas/dibersihkan Diblender sampai halus
Dimasukkan kedalam labu enlenmeyer Ditambahkan aquades sebanyak 600 ml Didiamkan selama 24 jam
Dipisahkan filtrat dan residunya
Residu/ ampas
Dipanaskan diatas penangas air Dimasukkan kedalam botol vial
Ekstrak Bawang Merah Filtrat Bawang
Dilakukan perlakuan yang sama untuk bawang putih dan bawang batak.
3.4.2. Skrining Fitokimia Ekstrak Bawang
Ekstrak Bawang Merah
Dimasukkan kedalam tabung reaksi secukupnya Dilarutkan dengan aquadest
Diskrining fitokimia berdasarkan metode masing-masing golongan
Uji Sulfur Uji Saponin
Hasil Hasil
Ditambahkan NaOH Ditambahkan AgNO3
Ditambahkan aquades Dikocok
Dilakukan perlakuan yang sama untuk ekstrak bawang putih dan ekstrak bawang batak
3.4.3. Uji Sifat Antioksidan Ekstrak Air Bawang Dengan Metode DPPH 3.4.3.1. Pembuatan Larutan DPPH 0,3mM
11,83 mg DPPH
Larutan DPPH 0,3 mM
3.4.3.2. Pembuatan variasi konsentrasi ekstrak bawang 0,025 gram Ekstrak Bawang Merah
Dimasukkan dalam labu takar 25 ml
Ditambahkan etanol p.a hingga garis tanda
Dihomogenkan
25 ml larutan induk 1000 ppm
Dipipet 2,5 ml larutan induk 1000 ppm Dimasukkan kedalam labu takar 25 ml
Ditambahkan etanol p.a hingga garis tanda
Dihomogenkan
25 ml larutan induk 100 ppm
Dipipet 12,5 ml larutan induk 100 ppm
Dimasukkan kedalam labu takar 25 ml
Ditambahkan etanol p.a hingga garis tanda
Dihogenkan
25 ml larutan induk 50 ppm
Dibuat konsentrasi 5, 10, 15, dan 20 ppm
dipipet 2,5 ml
dipipet 10 ml dengan pipet volume
3.4.3.3. Uji Aktivitas Antioksidan a. Uji Blanko
1 ml larutan DPPH 0,3 mM
Dimasukkan kedalam tabung reaksi Ditambahkan 2,5 ml etanol p.a Dihomogenkan
Dibiarkan selama 30 menit pada ruang gelap
Diukur absorbansi pada panjang gelombang maksimum 515 nm Hasil
b. Uji aktivitas antioksidan ekstrak bawang
1 ml larutan DPPH 0,3 mM
Dimasukkan kedalam tabung reaksi Dihomogenkan
Dibiarkan selama 30 menit pada ruang gelap
Diukur absorbansi pada panjang gelombang maksimum 515 nm Hasil
Ditambahkan 2,5 ml ekstrak bawang merah 5 ppm
BAB 4
HASIL DAN PEMBAHASAN
4.1. Hasil Penelitian
4.1.1 Hasil Uji Skrining Fitokimia
Ekstrak bawang yang diperoleh dilakukan uji skrining untuk mengetahui adanya senyawa sulfur dan saponin dalam sampel. Sulfur diduga ada dalam bawang karena aroma khas yang timbul dari bawang.
Tabel 4.1 Hasil Uji Skrining Fitokimia Ekstrak Bawang
Sampel Uji Sulfur/Belerang Uji Saponin
Pereaksi Hasil Pereaksi Hasil
Bawang Merah NaOH, AgNO3 + ( Hitam) Aquadest + (Berbusa) Bawang Putih NaOH, AgNO3 + (Hitam) Aquadest + (Berbusa) Bawang Batak NaOH, AgNO3 + (Hitam) Aquadest + (Berbusa)
4.1.2 Hasil Uji Aktivitas Antioksidan Ekstrak Bawang
Tabel 4.2 Hasil Pengukuran Absorbansi Ekstrak Bawang Merah (Allium cepa L)
Sampel Absorbansi
Blanko 1,029
5 ppm 0,937
10 ppm 0,928
15 ppm 0,921
20 ppm 0,872
Dari persamaan regresi linier diperoleh nilai IC50 = 71,5935 mg/L
Tabel 4.3 Hasil Pengukuran Absorbansi Ekstrak Bawang Putih (Allium sativum L)
Sampel Absorbansi
Blanko 1,029
5 ppm 0,959
10 ppm 0,945
15 ppm 0,939
20 ppm 0,914
Dari persamaan regresi linier diperoleh nilai IC50 = 101,335 mg/L
Tabel 4.4 Hasil Pengukuran Absorbansi Ekstrak Bawang Batak (Allium chinense L)
Sampel Absorbansi
Blanko 1,029
5 ppm 0,896
10 ppm 0,885
15 ppm 0,882
20 ppm 0,874
4.2. Pembahasan
4.2.1 Kandungan Ekstrak Bawang
Berdasarkan uji skrining yang dilakukan yaitu pengujian sulfur/belerang dan pengujian saponin pada ekstrak bawang diperoleh hasil yang positif untuk kedua jenis pengujian tersebut.
Pengujian sulfur dilakukan dengan menggunakan larutan NaOH dan AgNO3 yang ditambahkan pada sampel ekstrak bawang yang diuji. Terbentuknya larutan yang berwarna hitam menunjukkan adanya senyawa sulfur dalam sampel. Seperti pada lampiran 6.
Sampel + 2NaOH Na2S2O3 + H2O Na2S2O3 + AgNO3 Ag2S2O3 + NaNO3
( hitam )
Sedangkan adanya golongan saponin dalam sampel ditandai dengan terbentuknya busa yang stabil setelah dikocok selama 10 detik, pembentukan sabun merupakan karakteristik yang paling umum dari saponin (Steiner, 1955). Saponin merupakan senyawa penting dalam bawang yang dapat berperan sebagai antikoagulan, yang berguna untuk mencegah penggumpalan darah. Saponin juga dapat berfungsi sebagai antimikroba (Jaelani,). Dari uji saponin yang dilakukan diketahui bahwa bawang batak memiliki kandungan saponin yang paling banyak. Seperti pada lampiran 7.
4.2.2 Uji Aktivitas Antioksidan Dengan Metode DPPH
Uji aktivitas antioksidan ekstrak bawang dapat dilakukan dengan metode DPPH dengan menggunakan alat spektrofotometer UV-Visible. Pengujian aktivitas antioksidan dengan metode DPPH secara spektrofotometri dilakukan dengan mereaksikan sampel dengan larutan DPPH yang berwarna ungu dan diukur dengan spektrofotometer
UV-Visible pada panjang gelombang (λ) 515 nm. Warna akan berubah dari ungu menjadi kuning lemah apabila elektron ganjil tersebut berpasangan dengan atom hidrogen yang disumbangkan senyawa antioksidan. Data yang sering dilaporkan sebagai IC50 merupakan konsentrasi antioksidan yang dibutuhkan untuk 50% peredaman radikal DPPH pada periode waktu tertentu (15 – 30 menit) (Pokorny, 2001).
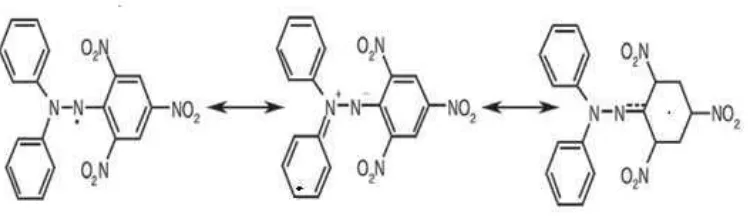
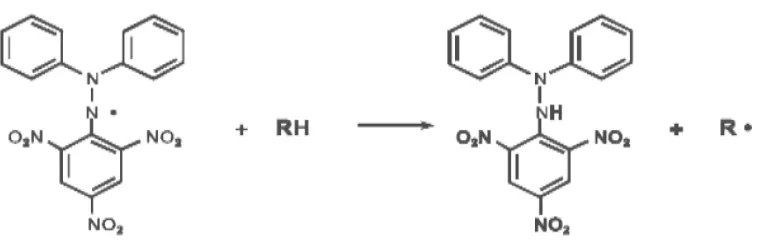
DPPH merupakan suatu molekul radikal bebas yang distabilkan oleh bentuk resonansi seperti ditunjukkan pada gambar 4.1
Gambar 4.1 Kestabilan radikal bebas DPPH
Pada uji DPPH, peredaman radikal DPPH diikuti dengan pemantauan penurunan absorbansi pada panjang gelombang maksimum yang terjadi karena pengurangan radikal oleh antioksidan atau reaksi dengan spesi radikal (R.) yang ditandai dengan berubahnya warna ungu pada larutan menjadi warna kuning lemah, apabila elektron ganjil tersebut berpasangan dengan atom hidrogen yang disumbangkan senyawa antioksidan.
adanya gugus fungsi–OH (hidroksil) bebas dan ikatan rangkap karbon-karbon lain dalam sampel (Shivaprasad,etal.,2005).
Gambar 4.2. Reaksi antara DPPH dengan atom H netral
Pada tabel 4.2 ,4.3 dan 4.4 menunjukkan telah terjadi peredaman radikal bebas yang di tandai dengan menurunnya absorbansi radikal bebas DPPH setelah penambahan ekstrak bawang dengan konsentrasi yang semakin tinggi.
Tabel 4.5 Hasil % Peredaman Ekstrak Bawang Merah
Sampel Absorbansi % Peredaman
Blanko 1,029 -
5 ppm 0,937 9,4686
10 ppm 0,928 10,3081
15 ppm 0,921 11,0145
20 ppm 0,872 15,7488
Tabel 4.6 Hasil % Peredaman Ekstrak Bawang Putih
Sampel Absorbansi % Peredaman
Blanko 1,029 -
5 ppm 0,959 7,3429
10 ppm 0,945 8,6956
15 ppm 0,939 9,2753
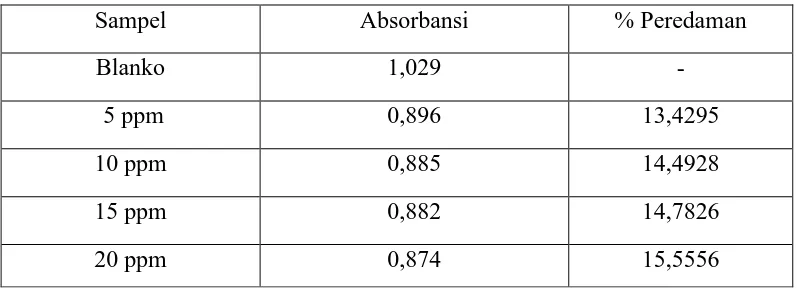
Tabel 4.7 Hasil % Peredaman Ekstrak Bawang Batak
Sampel Absorbansi % Peredaman
Blanko 1,029 -
5 ppm 0,896 13,4295
10 ppm 0,885 14,4928
15 ppm 0,882 14,7826
20 ppm 0,874 15,5556
Berdasarkan hasil analisis UV-Visible dan perhitungan dengan persamaan Least squre diperoleh nilai IC50 dari masing-masing sampel. Ekstrak bawang merah memiliki nilai IC50 = 71,5935 mg/L dan dapat dikatakan bahwa sampel bawang merah memiliki aktivitas antioksidan yang kuat. Ekstrak bawang putih memiliki nilai IC50 = 101,335 mg/L dan dapat dikatakan bahwa sampel bawang merah memiliki aktivitas antioksidan yang Sedang. Ekstrak bawang batak memiliki nilai IC50 = 77,5171 mg/L dan dapat dikatakan bahwa sampel bawang merah memiliki aktivitas antioksidan yang kuat.
Tingkat kekuatan senyawa antioksidan menggunakan metode DPPH dapat dilihat pada tabel 4.8.
Tabel 4.8 Tingkat Kekuatan Antioksidan Dengan Metode DPPH
(Ionita,2005).
Intensitas Nilai IC50
Sangat kuat < 50 mg/L
Kuat 50-100 mg/L
Sedang 101-150 mg/L
BAB 5
KESIMPULAN DAN SARAN
5.1. Kesimpulan
Dari penelitian yang telah dilaksanakan dapat disimpulkan
1. Ekstrak bawang merah memiliki nilai IC50 = 71,5935 mg/L dan dapat dikatakan bahwa
sampel bawang merah memiliki aktivitas antioksidan yang kuat.
2. Ekstrak bawang putih memiliki nilai IC50 = 101,335 mg/L dan dapat dikatakan bahwa
sampel bawang putih memiliki aktivitas antioksidan yang Sedang.
3. Ekstrak bawang batak memiliki nilai IC50 = 77,5171 mg/L dan dapat dikatakan bahwa
sampel bawang batak memiliki aktivitas antioksidan yang kuat.
5.2. Saran
BAB 2
TINJAUAN PUSTAKA
2.1. Jenis – Jenis Bawang
Ada beberapa macam bawang yang sejak dahulu diusahakan orang untuk kepentingan sendiri maupun untuk memenuhi permintaan pasar. Beberapa macam bawang tersebut termasuk dalam kelompok yang diusahakan atau di budidayakan untuk kepentingan komersil (Anonim, 1998).
Beberapa anggota allium termasuk mempunyai nilai ekonomi tinggi dan terkenal sebagai bumbu pelezat masakan diseluruh dunia, bahkan beberapa diantaranya merupakan obat tradisional yang mujarab (Wibowo. S, 2008).
Adapun tanaman bawang yang biasa dibudidayakan para petani antara lain sebagai berikut.
2.1.1. Bawang Merah ( Allium cepa L.)
Bawang merah merupakan komoditi holtikultura yang tergolong sayuran rempah. Sayuran rempah ini banyak dibutuhkan terutama sebagai pelengkap bumbu masakan guna menambah cita rasa dan kenikmatan makanan. Bawang merah tergolong tanaman semusim atau setahun. Tanaman bawang merah lebih banyak dibudidayakan di daerah dataran rendah yang beriklim kering, tanaman ini tidak menyukai tempat-tempat yang tergenangi air (Rahayu. E, 1999).
2.1.1.1 Botani tanaman bawang merah
Kedudukan tanaman bawang merah dalam tata nama atau sistematika tumbuhan, termasuk klasifikasi sebagai berikut :
Kingdom : Plantae
Divisi : Spermatophyta
Sub Divisi : Angiospermae
Class : Monocotyledonae
Famili : Liliaceae
Genus : Allium
Spesies : Allium cepa L.
Nama Lokal : Bawang Merah
Gambar 2.1 Bawang Merah (Allium cepa L.)
Tanaman ini diduga berasal dari daerah Asia Tengah, yaitu sekitar India, Pakistan sampai Palestina. Dari berbagai penelusuran dalam literature dan nara sumber terdapat kesamaan pandangan bahwa bawang merah merupakan tanaman yang tertua dari silsilah budidaya tanaman oleh manusia, hal ini antara lain ditunjukkan pada zaman I dan II Dynasti (3.200 – 2.700 SM) bangsa Mesir sering melukiskan bawang merah pada patung dan tugu-tugu mereka (Rukmana. R, 1994).
lain NTB, Sumatera Utara, Sulawesi Selatan, Bali, Sumatera Barat dan Sulawesi Tengah pada kisaran luas panen 1000-3000 hektar.
Di Indonesia bawang merah juga telah merambah ke berbagai daerah sehingga komoditi ini memiliki nama khas masing-masing daerah. Bahkan di daerah tertentu terdapat beberapa nama panggilan yang beragam. Di Minahasa misalnya, paling tidak terdapat lima nama panggilan khas untuk bawang merah. Untuk lebih jelasnya, tabel di bawah ini memuat nama –nama khas bawang merah di berbagai daerah dan Negara (Rahayu. E,1999).
Tabel 2.1 Nama bawang merah di beberapa daerah dan Negara
No. Daerah/Negara Nama- nama lain Bawang Merah
1. Nama di Daerah Sumatera
Bawang abang mirah (Aceh), Bawang megaren (Alas), pia (Batak), bawang sirah ,dasun merah (Minang), bawang abang, bawang suluh (Lampung), bawang merah, bawang abang (Melayu).
2. Nama di daerah Jawa Bawang beureum (Sunda), bawang abang, brambang (Jawa), bhabang mera (Madura).
3. Nama di Daerah Nusa Tenggara
Jasun bang, jasun Mirah (Bali), laisona piras (Roti), kalpeo meh (Timor).
4. Nama di Daerah Sulawesi
Lasuna mahamu, lasuna randang, lasuna raindang, rasuna mahendong, jantuna mopura (Minahasa), bawangi (Gorontalo), lasuna eja (Makassar), lasuna cela (Bugis).
6. Nama Asing Allium cepa var. ascalonicum, allium
ascalonicum (Nama Ilmiah), shallot
(Inggris), syalot (Belanda), eschlauch (Jerman), echalote (Prancis), tamanagi (Jepang).
Sumber : Wibowo. S ,1988.
Bawang merah termasuk salah satu sayuran multiguna, paling penting didayagunakan sebagai bahan bumbu dapur sehari-hari dan penyedap berbagai masakan. Bahkan akhir-akhir ini umbi bawang merah diolah menjadi bawang goring yang pemasarannya sudah menembus sasaran ekspor. Kegunaan lain bawang merah adalah sebagai obat tradisional untuk pelayanan masyarakat. Sudah sejak lama nenek moyang menggunakan umbi bawang merah sebagai obat nyeri perut karena masuk angin dan penyembuhan luka atau infeksi. Pada masa lalu konon bawang merah di makan segera sesudah makan sebagai tindakan pencegahan terhadap kolera, disentri dan diare. Menurut pengobatan tradisional di India , bawang merah goreng dianggap sebagai obat disentri basiler.
Berkhasiatnya umbi bawang merah sebagai obat, diduga karena mempunyai efek antiseptic dari senyawa alliin atau allisin. Senyawa alliin ataupun allisin oleh enim liase diubah menjadi asam piruvat, ammonia , dan allisin anti mikroba yang bersifat bakterisida. Dalam industri makanan, umbi bawang merah sering diawetkan dalam kaleng (canning), saus, sop kalengan, dan tepung bawang. Keuntungan mengkosumsi bawang merah, selain penyedia bahan pangan bergizi dan berkhasiat obat, juga sangat baik untuk kesehatan. Fungsi dalam tubuh antara lain memperbaiki dan memudahkan pencernaan serta menghilangkan lendir-lendir dalam kerongkongan.
Bagian tanaman bawang merah lainnya seperti daun dan tungkai bunga termasuk bahan sayuran yang melezatkan. Mengkonsumsi sayuran tersebut diduga dapat membantu pencernaan, memperbanyak air ludah, menyembuhkan penyakit kuning, memperkuat hati, dan membantu penyembuhan wasir (Rukmana. R,1994).
Ditinjau dari segi kandungan gizinya, bawang merah bukan merupakan sumber karbohidrat, protein, lemak, vitamin, atau mineral. Namun komponen-komponen tersebut ada di dalam bawang merah walaupun dalam jumlah yang sedikit. Komponen lainnya, seperti minyak atsiri juga terkandung di dalam umbi bawang merah. Komponen inilah yang sebenarnya banyak dimanfaatkan untuk penyedap rasa makanan, bakterisida, fungisida dan berkhasiat untuk obat-obatan. Daftar komposisi selengkapnya disajikan pada tabel 2.2
Tabel 2.2 Komposisi kimia umbi bawang merah per 100 gram bahan
No. Komponen Komposisi
1. Air (g) 88,00
vitamin B1 nya sendiri. Dengan demikian allicin dapat membuat vitamin B1 menjadi lebih efisien dimanfaatkan tubuh (Rahayu. E, 1999).
2.1.2. Bawang Putih (Allium Sativum L.)
Bawang putih merupakan terna yang tumbuh tegak dengan tinggi dapat mencapai 30-60 cm dan membentuk rumpun.Sebagaimana kelompok monokotiledon, akarnya serabut yang tidak terlalu dalam berada dalam tanah. Tidak seperti bawang merah, pangkal daun bawang putih tidak membentuk bengkakan sebagai cadangan makanan. Bagian pangkal bawang putih berupa selaput tipis yang mongering tetapi kuat dan merupakan selaput pembungkus umbi-umbi kecil. Bagian dasar atau pangkal umbi-umbi berbentuk cakram yang sebenarnya merupakan batang pokok yang tidak sempurna (rudimenter). Dari batang ini muncul akar-akar serabut yang tumbuh mendatar. Akar serabut tersebut merupakan akar penghisap makanan semata dan bukan pencari air dalam tanah.
2.1.2.1. Botani tanaman bawang putih
Klasifikasi dari tanaman bawang putih adalah sebagai berikut :
Kingdom : Plantae
Divisi : Spermatophyte
Sub Divisi : Angiospermae
Class : Monocotyledonae
Ordo : Lilliales /Lilliflorae
Famili : Liliaceae
Genus : Allium
Spesies : Allium Sativum L.
Gambar 2.2 Bawang Putih ( Allium Sativum L.)
Bawang putih termasuk salah satu anggota bawang-bawangan paling popular didunia. Bawang putih yang nama ilmiahnya allium sativum L. ini mempunyai nilai komersial yang tinngi dan tersebar di seluruh dunia. Oleh karena itu tidak heran jika bawang putih memiliki banyak nama. Beberapa nama daerah dan nama asing bawang putih seperti dalam tabel 2.3 di bawah ini.
Tabel 2.3 Nama daerah dan nama asing bawang putih
No. Daerah / Negara Nama-nama lain bawang putih
1. Nama di Daerah Sumatera Lasun (gayo), lasuna ( Karo dan Toba), dasun putih (Minang) bawang handak (Lampung)
2. Nama di Daerah Jawa Bawang (Jawa), bawang rodas (Sunda), bhabang phote (Madura),
3. Nama di daerah Nusa Tenggara Kasuma (Bali), langsuna (Sasak), ncuna (Bima), lansuna mawira (Sangi), laisona mabotiek (P. Roti), kalfeofolen (Timor), bawang basuhong (Ngaju)
4. Nama di daerah Kalimantan Uduh bawang (Kenya), bawang putih (Bulungan), bawang pulak (Tarakan).
(Minahasa), lasuna kulo, lasuna bido, rasuna mabida, jantuna mapusi, dasuna putih, lansuna putih, pia moputi (Gorontalo), lasuna kebo (Makassar), lasuna pute (Bugis).
6. Nama di daerah Maluku Kosai boti (Buru), bawa de are (Halmahera), bawa bodudo (Ternate), bawa iso (Tidar).
7. Nama di daerah Irian Jaya Bawa fiufer (Irian Jaya).
8. Nama asing Allium sativum .L (nama ilmiah), garlic
(inggris), knoflook (Jerman), ail,commun (Francis), aglio (Italia), ajo (Spanyol), vitlok (Swedia).
Sumber : Wibowo. S, 2008.
Bawang putih termasuk terna yang tumbuh tegak dengan tinggi dapat mencapai 30-60 cm dan membentuk rumpun. Sebagaimana warga kelompok monokitiledon, system perakarannya tidak memiliki akar tunggang dan akarnya serabut yang tidak panjang, tidak terlalu dalam berada di dalam tanah. Dengan perakaran yang demikian bawang tidak tahan terhadap kekeringan (Wibowo. S, 2008)
2.1.2.2. Komposisi kimia bawang putih
Manfaat utama bawang putih adalah sebagai bumbu penyedap masakan yang membuat masakan menjadi beraroma dan mengundang selera. Meskipun kebutuhan untuk bumbu masak hanya sedikit,namun tanpa kehadiranya masakan akan terasa hambar.
Di zaman modern, khasiat bawang putih sudah mulai di buktikan secara ilmiah. Ternyata khasiat bawang putih berhubugan erat dengan zat kimia yang terkandung di dalamnya. Meskipun sosok bawang putih tampak sederhana namun di dalamnya terkandung bermacam-macam zat kimia yang berkomposisi sedemikian rupa sehingga menimbulkan khasiat yang berguna bagi manusia (Anonim, 1999).
No. Kandungan bawang putih Jumlah
Selain zat-zat diatas bawang putih juga mengandung zat-zat kimia lain yang sebagian besar yang sebagian besar masuk dalam golongan minyak atsiri. Sifat minyak atsiri ini mudah menguap sehingga sering disebut minyak terbang atau minyak menguap.
Allicin adalah salah satu komponen utama yang berperan memberikan aroma bawang putih dan merupakan salah satu zat aktif yang diduga dapat membunuh kuman-kuman penyakit (bersifat antibakteri). Aliicin berperan ganda membunuh bakteri, yaitu garam positif dan garam negatif karena mempunyai gugus asam amino para amino benzoat.
Scordinin berupa senyawa kompleks thioglosida yang berfungsi sebagai antioksidan. Senyawa inilah yang berperan sebagai obat kuat guna membangkitkan gairah seksual dan merangsang pertumbuhan sel. Hal ini didukung oleh sebuah penelitian yang membuktikan bahwa bawang putih dapat meningkatkan produksi sperma dan mencegah kerusakan sel tubuh yang diakibatkan oleh penuaan. Senyawa lain yang terdapat pada bawang putih adalah allithiamin. Senyawa ini mrupakan senyawa hasil reaksi allicin denga thiamin dan dapat bereaksi dengan sistein. Fungsi senyawa ini hampir sama dengan vitamin B1 sehingga di kenal sebagai vitamin B1 bawang putih.
steroida-glikosida antara lain saponin yang berkhasiat sebagai anti tumor, anti hemolisis, dan penawar racun.
Zat –zat lain yang ditemukan dan berkasiat sebagai obat antara lain selenium (mikromineral penting yang berfungsi sebagai anti oksidan), enzim germanium (suatu zat yang mencegah rusaknya darah merah), antiarthritic factor (suatu zat pencegah rusaknya persendian), dan methyllallytrisulfide (zat yang mencegah terjadinya perlengketan sel darah merah (Anonim, 1999).
2.1.3. Bawang Batak (Allium Chinense L.) Klasifikasi Ilmiah dari bawang batak.
Kingdom : Plantae
Divisi : Angiospermae
Kelas : Monocotiledonae
Ordo : Asparagales
Family : Amaryllidaaceae
Subfamily : Allioideae
Genus : Allium
Spesies : Allium chinense L.
Gambar 2.3 Bawang batak (Allium Chinense L.)
makanan. Bentuk Lokio seperti bawang namun dengan ujung tangkai yang lebih panjang dan warnanya cenderung putih. Jadi mirip bawang daun berbentuk mungil dengan daun kecil panjang, dan juga bentuknya mirip seperti bawang, tapi ukurannya jauh lebih kecil, tetapi berbeda deng
Biasanya digunakan sebagai campuran asinan ataupun beberapa masakan. Banyak orang yang menyebut sayuran ini dengan nama lokio, tapi ada juga yang menyebutnya dengan sebutan bawang masakan-masakan khas Batak, salah satuny zaman, lokio atau bawang Batak ini juga digunakan pada masakan lainnya, seperti bahan masakan untuk menumis ayam, ikan, atau daging.
2..2. Skrining Fitokimia
Berbagai metode yang dapat digunakan untuk identifikasi metabolit sekunder yang terdapat pada suatu ekstrak antara lain:
2.2.1. Uji Sulfur
Belerang atau sulfur adal S da aslinya, adalah sebuah zat padat kristalin kuning. Di alam, belerang dapat ditemukan sebagai unsur murni atau sebagai mineral- minera untuk kehidupan dan ditemukan dalam dua
Belerang merupakan elemen penting bagi semua kehidupan, dan secara luas digunakan dalam proses biokimia. Belerang merupakan bagian penting dari banyak enzim dan juga dalam molekul antioksidan seperti glutathione dan thioredoxin. Belerang organik adalah komponen dari semua protein, sebagai asam amino sistein dan metionin.
Untuk mengetahui adanya unsur belerang dalam suatu sampel diuji dengan menambahkan sampel dengan NaOH pekat dan dipanaskan, kemudian di tambahkan beberapa tetes larutan argentum nitrat (AgNO3) . Akan terbentuk larutan berwarna hitam, ini menunjukkan adanya unsure belerang dalam sampel.
2.2.2. Uji Saponin
2.3. Antioksidan
2.3.1. Pengertian Antioksidan
Antioksadan adalah senyawa yang mempunyai struktur molekul yang dapat memberikan elektronnya kepada molekul radikal bebas dan dapat memutus reaksi berantai dari radikal bebas. Antioksidan merupakan senyawa pemberi elektron (electron donor) atau reduktan. Antioksidan dapat diperoleh,
1. Antioksidan yang dibuat oleh tubuh kita sendiri yang berupa enzim antara lain superoksida dismutase (SOD), gluthatione peroxidase, perxidase dan katalase. (Sri Kumalaningsih, 2006).
2. Antioksidan alami yang dapat diperoleh dari tanaman atau hewan yaitu tokoferol, vitamin C, betakaroten, flavonoid dan senyawa fenolik.
3. Antioksidan sintetik, yang dibuat dari bahan-bahan kimia yaitu butylated hroxyanisole (BHA), butil hidroksi toluen (BHT), propil galat (PG), tert-butil hidoksi quinon (TBHQ) yang di tambahkan dalam makanan untuk mencegah kerusakan lemak.
2.3.2. Jenis- Jenis Antioksidan
Berdasarkan fungsinya antioksidan dapat dibedakan sebagai berikut. a. Antioksidan Primer
Antioksidan ini berfungsi untuk mencegah terbentuknya radikal bebas baru karena ia dapat merubah radikal bebas yang ada menjadi molekul yang berkurang dampak negatifnya yaitu sebelum sempat bereaksi.
Antioksidan primer yang ada dalam tubuh yang sangat terkenal adalah enzim superoksida dismutase. Enzim ini sangat penting karena dapat melindungi hancurnya sel-sel dalam tubuh akiabat serangan radikal bebas.
b. Antioksidan Sekunder
c. Antioksidan Tersier
Antioksidan tersier merupakan senyawa yang memperbaiki sel-sel dan jaringan yang rusak karena serangan radikal bebas. Biasanya yang termasuk kelompok ini adalah jenis enzim misalnya metionim sulfoksidan reduktase yang dapat memperbaiki DNA dalam inti sel. Enzim tersebut bermanfaat untuk perbaikan DNA pada penderita kanker.
2.3.3. Pengaruh Antioksidan
Antioksidan dalam makanan dapat didefinisikan sebagai zat yang mampu menunda, memperlambat atau mencegah pengembangan ketengikan dan rasa dalam makanan atau kerusakan lainnya akibat oksidasi. Antioksidan menunda pergembangan aroma-tak sedap dengan memperpanjang periode induksi. Penambahan antioksidan setelah akhir periode ini cenderung tidak efektif dalam memperlambat pengembangan ketengikan.
Antioksidan dapat menghambat atau memperlambat oksidasi dalam dua cara: baik dengan peredaman radikal bebas, dalam hal ini senyawa tersebut digambarkan sebagai antioksidan primer, atau dengan mekanisme yang tidak melibatkan peredaman radikal bebas langsung, dalam hal ini senyawa tersebut adalah antioksidan sekunder. Antioksidan primer termasuk senyawa fenolik. Komponen ini dikonsumsi selama periode induksi. Antioksidan sekunder beroperasi dengan berbagai mekanisme termasuk mengikat ion logam, peredaman oksigen, mengubah hidroperoksida untuk spesi non-radikal, menyerap radiasi UV atau menonaktifkan oksigen singlet.
2.4. Metode Uji Senyawa Antioksidan 2.4.1. Metode Asam Tiobarbiturat
Malondialdehida (MDA) merupakan produk hasil peroksida lipid dalam tubuh dan terdapat dalam bentuk bebas atau terkompleks dengan jaringan, bahkan organ dalam tubuh. Reaksi ionisasi senyawa radikal juga dapat membentuk MDA , dan MDA ini juga merupakan produk samping biosintesis prostaglandin. Banyak MDA dalam tubuh dapat dideteksi, salah satunya dengan metode asam tiobarbiturat. Deteksi MDA pada umumnya menggunakan hati menjadi sampel penelitian. Organ hati menjadi sampel penentuan kadar MDA karena hati memiliki fungsi detoksifikasi. Bahan toksin yang masuk kedalam tubuh akan mengalami proses biotrasformasi didalam hati.
Analisis MDA merupakan analisis raadikal bebas secara tidak langsung dan mudah dalam menentukan jumlah radikal bebas yang terbentuk. Analisis radikal bebas secara langsung sangat sulit dilakukan, karena senyawa radikal sangat tidak tidak stabil dan bersifat elektrofil, selain itu reaksinyapun berlangsung sangat cepat. Pengukuran MDA dapat dilakukan dengan pereaksi asam tiobarbiturat (thiobarbituric acid, TBA) dengan mekanisme reaksi penambahan nukleofilik membentuk senyawa MDA- TBA. Senyawa ini berwarna merah muda yang dapat diukur intensitasnya dengan menggunakan spektrofotometer.
Metode yang digunakan yaitu TBARS ( thiobarbituric acid reactive substance) dengan flourofotometri. Prinsip analisis ini yaitu pemanasan akan menghidrolisis peroksida lipid, sehingga MDA yang terikat akan dibebaskan dan akan bereaksi dengan TBA dalam suasana asam membentuk kompleks MDA-TBA yang berwarna merah dan diukur pada panjang gelombang 532 nm. Analisis kadar radikal bebas ini dilakukan dengan mengukur kadar MDA organ hati dengan metode spektrofotometri menggunakan spektrofotometer
UV-Vis. Senyawa 1,1,3,3- tetraetoksipropana (TEP) digunakan dalam pembuatan kurva standar,
karena TEP dapat dioksidasi dalam suasana asam menjadi senyawa aldehida yang dapat bereaksi dengan TBA.
2.4.2. Metode DPPH (difenilpikril hidrazil)
DPPH digunakan karena merupakan radikal bebas yang stabil pada suhu ruang. DPPH ini akan menerima elektron atau radikal hydrogen dan akan membentuk molekul diamagnetik yang stabil. Interaksi antioksidan dengan DPPH baik secara transfer elektron atau radikal hidrogen pada DPPH, akan menetralkan karakter radikal bebas dari DPPH.
Prosedur dengan DPPH dilakukan dengan membuat larutan DPPH dalam etanol. Dibuat serangkaian larutan sampel dengan variasi konsentrasi kemudian ditambahkan larutan DPPH. Didiamkan selama 30 menit (dihitung setelah penambahan larutan DPPH), kemudian diukur absorbansinya pada panjang gelombang 515 nm. Data absorbansi yang diperoleh digunakan untuk menentukan % inhibisi. Dari kurva % inhibisi versus konsentrasi sampel , dapat diperoleh nilai IC50 ekstrak dengan analisis statistic menggunakan regresi linier.
Aktivitas antioksidan merupakan kemampuan suatu senyawa atau ekstrak untuk menghambat reaksi oksidasi yang dapat dinyatakan dengan persen penghambatan. Parameter yang dipakai untuk menentukan aktivitas antioksidan adalah harga konsentrasi efesien atau
efficient concentration 50 ( EC50) atau inhibition concentration 50 (IC50) , yaitu konsentrasi suatu zat antioksidan yang dapat menyebabkan 50% DPPH kehilangan karakter radikal atau konsentrasi suatu zat antioksidan yang memberikan % penghambatan sebesar 50%. Zat yang mempunyai antioksidan tinggi akan mempunya nilai EC50 atau IC50 yang rendah.
2.4.3. Metode β-Karoten
Metode ini didasarkan pada pemucatan warna emulsi system β-karoten dan asam oleat. BHT digunakan sebagai pembanding, karena BHT memiliki keefektifan sebagai antioksidan yang paling tinggi walaupun memiliki satu gugus hidroksi (-OH) dan memiliki jumlah resonansi yang sama dengan euganol, tetapi lebih besifat nonpolar dibandingkan dengan senyawa lainya karena adanya gugus alkil yang lebih tersubsitusi yaitu t-butil (C-(CH3)3). Pemucatan warna merupakan parameter terjadinya reaksi oksidasi. Semakin besar penurunan nilai absorbansinya, maka semakin tinggi tingkat oksidasi yang terjadi.
2 2
O
c selama 60 menit. Absorban diukur pada setiap 15 menit pada panjang gelombang 470 nm. Sebagai control digunakan 2 ml etanol untuk menggatikan sampel, sedangkan larutan blanko diganakan etanol.
2.5. Radikal Bebas
Radikal bebas adalah setiap molekul yang mengandung satu atau lebih elektron
yang tidak berpasangan. Radikal bebas sangat reaktif dan dengan mudah menjurus ke
reaksi yang tidak terkontrol, menghasilkan ikatan dengan DNA, protein, lipida, atau
kerusakan oksidatif pada gugus fungsional yang penting pada biomolekul ini. Radikal
bebas juga terlibat dan berperan dalam patologi dari berbagai penyakit degeneratif,
yakni kanker, aterosklerosis, jantung koroner, katarak, dan penyakit degeneratif lainnya
(Silalahi, 2006).
Pembentukan radikal bebas dan reaksi oksidasi pada biomolekul akan berlangsung
sepanjang hidup. Radikal bebas yang sangat berbahaya dalam makhluk hidup antara
lain adalah golongan hidroksil (OH-), superoksida (O- ), nitrogen monooksida (NO),
peroksidal (RO- ), peroksinitrit (ONOO-), asam hipoklorit (HOCl), hydrogen
peroksida (H2O2) (Silalahi, 2006)
2.6. DPPH (2,2-diphenyl-1-picrylhydrazil )
Pada tahun 1922, ditemukan senyawa berwarna ungu radikal bebas stabil DPPH, yang sekarang digunakan sebagai reagen kolorimetri. DPPH sangat berguna dalam berbagai penyelidikan seperti inhibisi atau radikal polimerisasi kimia, penentuan sifat antioksidan amina, fenol atau senyawa alami (vitamin, ekstrak tumbuh-tumbuhan, obat-obatan). DPPH berwarna sangat ungu seperti KMnO4 dan bentuk tereduksinya berwarna oranye-kuning.
DPPH merupakan singkatan umum untuk senyawa kimia organik yaitu
bebas yang stabil. Penyimpanan dalam wadah tertutup baik pada suhu -20°C DPPH mempunyai berat molekul 394.32 dengan rumus molekul C18H12N5O6, larut dalam air dan rumus molekul pada gambar 2.6 (Molyneux, 2004).
Gambar 2.4. Rumus Bangun DPPH
DPPH merupakan suatu radikal bebas yang stabil kerena mekanisme delokalisasi elektron bebas oleh molekulnya, sehingga molekul ini tidak mengalami reaksi dimerisasi yang sering terjadi pada sebagian besar radikal bebas lainnya. Delokalisasi juga memberikan efek warna ungu yang dalam pada panjang gelombang 515 nm dalam pelarut etanol. Zat ini berperan sebagai penangkap elektron atau penangkap radikal hidrogen bebas. Hasilnya adalah molekul yang bersifat stabil. Jika suatu senyawa antioksidan direaksikan dengan zat ini maka senyawa antioksidan tersebut akan menetralkan radikal bebas dari DPPH (Bintang, 2010).
BAB 1
PENDAHULUAN
1.1 Latar Belakang
Hampir semua masakan Indonesia menggunakan bawang sebagai salah satu bumbu penyedapnya. Proporsi penggunaannya memang tidak banyak, namun karena demikian akrab dan lekatnya bawang dengan lidah Indonesia, sungguh sulit dicari jenis masakan yang tanpa bawang (Wibowo. S, 2008).
Bawang memiliki banyak manfaat bagi kehidupan manusia, terutama sebagai penyedap masakan dan bahan membuat bahan obat-obatan (kesehatan). Ada berbagai jenis bawang yang dibudidayakan oleh petani Indonesia. Hasil bawang diambil dari bagian tanaman yang berupa umbi atau batang (semu) dan daun. Bawang yang di ambil umbinya ialah bawang merah dan bawang putih, sedangkan yang di ambil daun atau batang semunya ialah bawang daun (loncang) (Anonim, 1998).
Bahan yang terkandung dalam berbagai jenis bawang, kadar airnya cukup tinggi yaitu antara 60-85%, sedangkan komponen utamanya berupa protein, karbohidrat, dan lemak, disamping itu bawang juga mengandung zat-zat seperti kalsium, besi serta unsur kimia lainnya. Bahkan jenis bawang tertentu mengandung vitamin A dan serat (crude fibre).
Bawang bermanfaat bagi kesehatan karena mengandung unsur-unsur aktif, memiliki daya bunuh terhadap bakteri, sebagai bahan antibiotik, merangsang pertumbuhan sel tubuh, dan sebagai sumber vitamin B1. Selain itu bawang memiliki nilai gizi yang cukup tinggi dan mengandung sejumlah komponen kimia yang diperlukan untuk hidup manusia. Dewasa ini bawang putih dimanfaatkan sebagai penghambat perkembangan penyakit kanker karena mengandung komponen aktif yaitu selenium dan germanium.
Pada bawang merah, bagian kulit terluarnya mengandung 6,5% ( per berat basah) flavonol, sedangkan pada bagian jaringan lunak (yang lebih dalam) kandungan flavonol sebagai O-glikosida berkisar 100 mg/kg berat basah (Winarsi. H, 2005).
antioksidan dilakukan melalui penetapan IC50 terhadap DPPH (1,1-difenil-2-pikril
hidrazil). Hasil percobaan menunjukkan bahwa ekstrak umbi bawang merah (Allium cepa L.) mempunyai aktivitas antioksidan dengan nilai IC50 sebesar 95,995 bpj.
Dina Pratiwi ,dkk (2013) meneliti tentang aktivitas antioksidan ekstrak etanol 70% daun bawang mekah. Hasil dari penelitian tersebut menunjukkan daun bawang mekah positif
memiliki aktivitas antioksidan menggunakan pereaksi DPPH. Nilai IC50 ekstrak etanol 70% daun bawang mekah adalah sebesar 31,974µg/mL.
Anita Sarah ,dkk (2015) melakukan penelitian tentang aktivitas antioksidan tentang ekstrak etanol 70% umbi bawang dayak. Berdasarkan hasil penelitian tersebut di peroleh nilai IC50 sebesar 46,14 ppm.
1.2 Permasalahan
1. Apakah ekstrak air dari bawang merah, bawang putih dan bawang batak dapat bersifat sebagai antioksidan.
2. Bagaimanakah perbandingan sifat antioksidan antara ekstrak air dari bawang merah, bawang putih dan bawang batak .
1.3 Pembatasan Masalah
Batasan permasalahan dalam penelitian ini adalah :
1. Penentuan sifat anti oksidan ekstrak air dari bawang merah, bawang putih dan bawang batak.
2. Metode uji aktivitas antioksidan yang digunakan adalah metode DPPH.
1.4 Tujuan Penelitian
1. Untuk menguji aktivitas antioksidan ekstrak air dari bawang merah, bawang putih dan bawang batak.
2. Untuk mengetahui perbandingan aktivitas antioksidan antara ekstrak air dari bawang merah, bawang putih dan bawang batak.
1.5 Manfaat Penelitian
Penelitian diharapkan ini dapat memberikan informasi ilmiah mengenai sifat antioksidan ekstrak air dari bawang merah, bawang putih dan bawang batak serta perbandingannya masing-masing.
1.6 Lokasi Penelitian
1.7 Metodologi Penelitian
UJI ANTIOKSIDAN EKSTRAK AIR BAWANG MERAH (Allium cepa L), BAWANG PUTIH (Allium sativum L) DAN BAWANG BATAK (Allium chinense L) DENGAN
METODE DPPH
ABSTRAK
Penelitian ini bertujuan untuk mengetahui aktivitas antioksidan dari bawang merah, bawang putih dan bawang batak. Pengujian aktivitas antioksidan dilakukan dengan menggunakan metode DPPH (2,2-difenil-1-pikrilhidrazil) diukur menggunakan spektrofotometer UV-Vis dengan konsentrasi 5, 10, 15 dan 20 ppm yang diawali dengan ekstraksi secara maserasi. Bawang (150 g) dibersihkan dan diblender kemudian direndam dengan aquadest selama 24 jam pada suhu kamar. Ekstrak air yang diperoleh diuapkan dan dipekatkan menggunakan waterbath sehingga diperoleh ekstrak kental. Uji aktivitas antioksidan dari ekstrak bawang merah menunjukkan nilai IC50 sebesar 71,5935 mg/L dan merupakan antioksidan kuat, aktivitas antioksidan dari ekstrak bawang putih menunjukkan nilai IC50 sebesar 101,335 dan merupakan antioksidan yang sedang, sedangkan aktivitas antioksidan ekstrak bawang batak menunjukkan nilai IC50 sebesar 77,5171 dan merupakan antioksidan kuat.
TEST OF ANTIOXIDANT ACTIVITY EXTRACT WATER RED ONION (Allium
cepa L) , GARLIC (Allium sativum L) AND BATAK ONION (Allium chinense L) USING DPPH METHOD
ABSTRACT
This study aims to determine the antioxidant activity of onion, garlic and onions Batak. Testing of antioxidant activity using DPPH (2,2-diphenyl-1-picrylhydrazyl) was measured using a UV-Vis spectrophotometer with a concentration of 5, 10, 15 and 20 ppm beginning with extraction by maceration. Onions (150 g) was cleaned and blended and then soaked in distilled water for 24 hours at room temperature. Water extract obtained is evaporated and concentrated using a water bath in order to obtain a thick extract.
Test the antioxidant activity of onion extract showed IC50 value of 71.5935 mg / L and is a powerful antioxidant, the antioxidant activity of garlic extract showed IC50 value of 101.335 and is an antioxidant that is being, while the antioxidant activity of garlic extract Hobo show IC50 value of 77 , 5171 and is a powerful antioxidant.
UJI ANTIOKSIDAN EKSTRAK AIR BAWANG MERAH (Allium cepa
L.), BAWANG PUTIH (Allium sativum L.) DAN BAWANG BATAK
(Allium chinense L.) DENGAN METODE DPPH
SKRIPSI
GIBSON SINAGA
140822010
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
UJI ANTIOKSIDAN EKSTRAK AIR BAWANG MERAH (Allium cepa
L.), BAWANG PUTIH (Allium sativum L.) DAN BAWANG BATAK
(Allium chinense L.) DENGAN METODE DPPH
SKRIPSI
Diajukan untuk melengkapi tugas dan memenuhi syarat mencapai gelar Sarjana Sains
GIBSON SINAGA
140822010
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
PERSETUJUAN
Judul : Uji Antioksidan Ekstrak Air Bawang Merah
(Allium Cepa L.), Bawang Putih (Allium Sativum L
Bawang Batak (Allium Chinense L.) dengan Metode DPPH
Kategori : Skripsi
Nama : Gibson Sinaga
Nomor Induk Mahasiswa : 140822010
Program Studi : Sarjana (S1) Kimia Ekstensi
Departemen : Kimia
Fakultas : Matematika Dan Ilmu Pengetahuan Alam Universitas Sumatera Utara
Disetujui di Medan, Mei 2016
Komisi Pembimbing :
Pembimbing 2, Pembimbing 1,
Dr. Sovia Lenny ,M.Si Lamek Marpaung, M.Phil, Phd NIP:197510182000032001 NIP : 195208281982031001
Diketahui/Disetujui oleh
Departemen Kimia FMIPA USU
PERNYATAAN
UJI ANTIOKSIDAN EKSTRAK AIR BAWANG MERAH (Allium cepa L), BAWANG PUTIH (Allium sativum L) DAN BAWANG BATAK (Allium chinense L) DENGAN
METODE DPPH
SKRIPSI
Saya mengakui bahwa skripsi ini adalah hasil karya sendiri, kecuali beberapa kutipan dan ringkasan yang masing-masing disebutkan sumbernya.
Medan, Mei 2016
PENGHARGAAN
Puji dan syukur penulis panjatkan kepada Tuhan Yang Maha Esa yang telah melimpahkan Rahmat dan Berkat-Nya sehingga penulis dapat menyelesaikan skripsi ini sebagai salah satu syarat untuk menyelesaikan pendidikan Sarjana Sains di Fakultas MIPA Universitas Sumatera Utara. Adapun Judul skripsi ini adalah” UJI ANTIOKSIDAN EKSTRAK AIR BAWANG MERAH (Allium cepa L.), BAWANG PUTIH (Allium sativum L.) DAN BAWANG BATAK (Allium chinense L.) DENGAN METODE DPPH”.
Adapun rasa terima kasih yang ingin penulis sampaikan kepada :
1. Bapak Lamek Marpaung, M.Phil, PhD selaku Kepala Laboratorium Kimia Organik Bahan Alam dan selaku pembimbing I penulis dan Ibu Dr.Sovia Lenny,M.Si, selaku pembimbing II penulis yang telah memberikan panduan serta pemikiran dan saran selama penulis melakukan penelitian dan penyusunan sehingga penulis dapat menyelesaikan skripsi ini hingga selesai.
2. Ibu Dr.Rumondang Bulan Nst. MS Selaku Ketua Departemen Kimia FMIPA USU dan Bapak Drs Albert Pasaribu,M.Sc Selaku sekertaris Departemen Kimia FMIPA USU dan selaku Ketua Bidang Kimia Organik Bahan Alam FMIPA USU
3. Bapak dan Ibu Staf pengajar FMIPA USU serta pegawai Departemen Kimia FMIPA USU.
4. Teman-teman mahasiswa khususnya Kimia Ekstensi 2014, yang telah banyak membantu dan memberikan semangat kepada saya selama perkuliahan hingga saat ini, kepada semua asisten Laboratorium Kimia Organik Bahan Alam, terimakasih karena telah banyak membantu dan memberikan dukungan kepada saya hingga saya dapat menyelesaikan skripsi ini.
Akhirnya, penulis mengucapkan terima kasih yang sebesar-besarnya kepada Kedua orang tua tercinta Ayahanda Karpin Sinaga dan Ibunda Merli Simbolon serta saudara penulis Rimsal M G Sinaga yang telah memberikan semangat serta perhatian yang cukup besar selama masa penyelesaian skripsi ini dan perkuliahan penulis. Penulis menyadari bahwa skripsi ini masih jauh dari sempurna karena keterbatsan penulis. Semoga skripsi ini dapat bermanfaat bagi penelitian dan ilmu pengetahuan.
UJI ANTIOKSIDAN EKSTRAK AIR BAWANG MERAH (Allium cepa L), BAWANG PUTIH (Allium sativum L) DAN BAWANG BATAK (Allium chinense L) DENGAN
METODE DPPH
ABSTRAK
Penelitian ini bertujuan untuk mengetahui aktivitas antioksidan dari bawang merah, bawang putih dan bawang batak. Pengujian aktivitas antioksidan dilakukan dengan menggunakan metode DPPH (2,2-difenil-1-pikrilhidrazil) diukur menggunakan spektrofotometer UV-Vis dengan konsentrasi 5, 10, 15 dan 20 ppm yang diawali dengan ekstraksi secara maserasi. Bawang (150 g) dibersihkan dan diblender kemudian direndam dengan aquadest selama 24 jam pada suhu kamar. Ekstrak air yang diperoleh diuapkan dan dipekatkan menggunakan waterbath sehingga diperoleh ekstrak kental. Uji aktivitas antioksidan dari ekstrak bawang merah menunjukkan nilai IC50 sebesar 71,5935 mg/L dan merupakan antioksidan kuat, aktivitas antioksidan dari ekstrak bawang putih menunjukkan nilai IC50 sebesar 101,335 dan merupakan antioksidan yang sedang, sedangkan aktivitas antioksidan ekstrak bawang batak menunjukkan nilai IC50 sebesar 77,5171 dan merupakan antioksidan kuat.
TEST OF ANTIOXIDANT ACTIVITY EXTRACT WATER RED ONION (Allium
cepa L) , GARLIC (Allium sativum L) AND BATAK ONION (Allium chinense L) USING DPPH METHOD
ABSTRACT
This study aims to determine the antioxidant activity of onion, garlic and onions Batak. Testing of antioxidant activity using DPPH (2,2-diphenyl-1-picrylhydrazyl) was measured using a UV-Vis spectrophotometer with a concentration of 5, 10, 15 and 20 ppm beginning with extraction by maceration. Onions (150 g) was cleaned and blended and then soaked in distilled water for 24 hours at room temperature. Water extract obtained is evaporated and concentrated using a water bath in order to obtain a thick extract.
Test the antioxidant activity of onion extract showed IC50 value of 71.5935 mg / L and is a powerful antioxidant, the antioxidant activity of garlic extract showed IC50 value of 101.335 and is an antioxidant that is being, while the antioxidant activity of garlic extract Hobo show IC50 value of 77 , 5171 and is a powerful antioxidant.
DAFTAR ISI
Daftar Lampiran xii
BAB1. PENDAHULUAN 1
2.1.1.1 Botani Tanaman Bawang
Merah (Allium cepa L.) 5
2.1.1.2 Komposisi Kimia Bawang
Merah (Allium cepa L.) 9
2.1.2 Bawang Putih (Allium sativum L.) 10 2.1.2.1 Botani Tanaman Bawang
Putih (Allium sativum L.) 10
2.1.2.2 Komposisi Kimia Bawang
Putih (Allium sativum L.) 12
2.1.3 Bawang Batak (Allium Chinense L.) 14
2.2. Skrinning Fitokimia 15
2.2.1. Uji Sulfur 15
2.2.2. Uji Saponin 16
2.3. Antioksidan 17
2.3.1 Pengertian Antioksidan 17
2.3.2 Jenis-Jenis Antioksidan 17
2.4. Metode Uji Senyawa Antioksidan 19
2.4.1. Metode Asam Tiobarbiturat 19
2.4.2. Metode DPPH 20
2.4.3. Metode β-Karoten 20
2.5. Radikal Bebas 21
2.6. DPPH ( 2,2-Dyphenyl-1-picryhydrazil) 22
BAB 3. METODE PENELITIAN 24
3.1. Alat-Alat 24
3.2. Bahan-Bahan 24
3.3. Prosedur Penelitian 25
3.3.1. Penyediaan Sampel 25
3.3.2. Pembuatan Ekstrak Air Bawang 25
3.3.3. Pengujian Skrinning Fitokimia 25
3.3.3.1. Pemeriksaan Sulfur 25
3.3.3.2. Pemeriksaan Saponin 26
3.3.4. Uji SifatAntioksidan Ekstrak Bawang Dengan
Metode DPPH 26
3.3.4.1. Pembuatan Larutan DPPH 26 3.3.4.2. Pembuatan Variasi Konsentrasi Ekstrak
Bawang 26
3.3.4.3. Uji Aktivitas Antioksidan 26
3.4. Bagan Penelitian 27
3.4.1. Pembuatan Ekstrak Air Dari Bawang 27 3.4.2. Skrinning Fitokimia Ekstrak Bawang 28 3.4.4. Uji Sifat Antioksidan Ekstrak Bawang
dengan Metode DPPH 28
3.4.4.1. Pembuatan Larutan DPPH 0,3 mM 29 3.4.4.2. Pembuatan Variasi Ekstrak Bawang 30 3.4.4.3. Uji Aktivitas Antioksidan 30
BAB 4. HASIL DAN PEMBAHASAN 31
4.1. Hasil Penelitian 31
4.1.1.Hasil Uji Aktivitas Antioksidan Ekstrak Bawang 31
4.2. Pembahasan 33
4.2.1. Uji Aktivitas Antioksidan dengan Metode DPPH 33
BAB5. KESIMPULAN DAN SARAN 37
5.1. Kesimpulan 38
5.2. Saran 38
Daftar Pustaka 39
DAFTAR TABEL
Nomor Judul Halaman
Tabel
Tabel 2.1. Nama-nama Bawang Merah di Beberapa Daerah dan Negara 7 Tabel 2.2. Komposisi Kimia Umbi Bawang Merah Per 100 gr Bahan 9 Tabel 2.3. Nama Daerah Dan Nama Asing Bawang Putih 11
Tabel 2.4. Komposisi Kimia Bawang Putih 13
Tabel 4.1. Hasil Uji Skrining Fitokimia Ekstrak Bawang 31 Tabel 4.2. Hasil Uji Aktivitas Antioksidan Ekstrak Bawang Merah
(Allium cepa L.) 31
Tabel 4.3. Hasil Uji Aktivitas Antioksidan Ekstrak Bawang Putih
(Allium sativum L.) 32
Tabel 4.4. Hasil Uji Aktivitas Antioksidan Ekstrak Bawang Batak
(Allium chinense L.) 32
DAFTAR GAMBAR
Nomor Judul Halaman
Gambar
Gambar 2.1. Bawang Merah (Allium cepa L.) 6
Gambar 2.2. Bawang Putih (Allium sativum L.) 11
Gambar 2.3. Bawang Batak (Allium chinense L.) 15
Gambar 2.4. Rumus Bangun DPPH 22
Gambar 4.1. Kestabilan Radikal Bebas DPPH 34
DAFTAR LAMPIRAN
Nomor Judul Halaman
Lampiran
Lampiran 1 Hasil Identifikasi Tumbuhan Bawang Merah 43 Lampiran 2 Hasil Identifikasi Tumbuhan Bawang Putih 44 Lampiran 3 Hasil Identifikasi Tumbuhan Bawang Batak 45
Lampiran 4 Pembuatan Variasi Konsentrasi Sampel 46
Lampiran 5 Hasil Uji Aktivitas Antioksidan 47
Lampiran 6 Pengujian Sulfur 54