LAMPIRAN 1
DATA PERCOBAAN
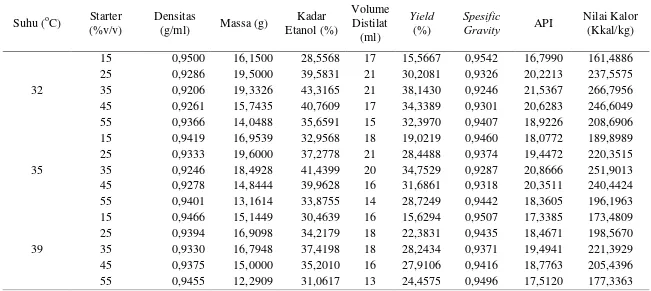
1.1 DATA HASIL PENELITIANTabel L1.1 Hasil Analisis Perolehan Bioetanol
LAMPIRAN 2
CONTOH PERHITUNGAN
2.1 DENSITAS ETANOL
Perhitungan untuk starter 35 % dengan suhu 32 oC Massa piknometer kosong = 5,7854 g
Massa piknometer kosong + distilat = 15,1813 g Massa piknometer kosong + aquades = 15,9473 g
Densitas aquades pada suhu 30 oC = 0,995647 gr/ml [56]
Maka densitas distilat dihitung dengan cara :
= 0,9206 gr/ml Dimana:
ρ1 = densitas air
m1 = massa (piknometer berisi aquades – piknometer kosong)
ρ2 = densitas distilat
m2 = massa (piknometer berisi distilat – piknometer kosong)
Untuk perhitungan densitas yang lainnya sama dengan perhitungan di atas.
2.2 KADAR ETANOL BERDASARKAN DENSITAS
Perhitungan untuk sarter 35 % dengan suhu 32 oC Densitas Bioetanol = 0,9206 gr/ml
Untuk densitas dari tabel diperoleh % kadar etanolnya adalah : antara 43 % dan 44 %
Interpolasi :
% kadar etanol =
Untuk perhitungan kadar bioetanol yang lainnya sama dengan perhitungan di atas.
2.3 YIELD ETANOL
Perhitungan untuk sarter 35 % dengan suhu 32 oC Massa gula awal = 11% x massa nira
Untuk perhitungan yield bioetanol yang lainnya sama dengan perhitungan di atas.
2.4 SPECIFIC GRAVITY DAN APY GRAVITY ETANOL
Perhitungan untuk sarter 35 % dengan suhu 32 oC Densitas bioetanol = 0,9206 gr/ml
2.5 NILAI KALOR ETANOL
API Grafity (G) = 21,5367 Nilai Kalor
(NK) =
− (18,650 + 40 ( −10) Kkal/Kg
=
− (18,650 + 40 (21,5367−10) Kkal/Kg
= 266,7956 kkal/kg
Untuk perhitungan nilai kalor yang lainnya sama dengan perhitungan di atas.
2.6 ANALISIS EKONOMI
Perhitungan analisis ekonomi meliputi perhitungan biaya kebutuhan bahan dan harga jual etanol yang diperoleh pada kondisi operasi yang telah ditetapkan dengan yield 38,1430 %.
1. Perhitungan biaya kebutuhan bahan Nira aren
Volume nira = 500 ml
Harga nira = Rp. 13.333/L
Total harga nira = 0,5 L x Rp. 13.333/L = Rp. 6.666,5,-
Fermipan
Massa = 1 g
Harga Fermipan = Rp. 4000/11 g Total harga Fermipan = 1 g x Rp. 4000/11 g
= Rp. 363,64,-
Pupuk NPK
Massa NPK = 1,4 g
Harga NPK = Rp. 2.000/kg
Total harga bahan baku = Rp. 6.666,5 + 363,64 + Rp. 2,8 = 7.032,94,-
2. Perhitungan harga jual etanol Etanol (C2H5OH)
Harga C2H5OH teknis (96%) = Rp. 35.750/960 ml
Etanol yang diperoleh dalam penelitian ini sebanyak 21 ml dengan kadar 43%. Total Harga C2H5OH = 21 ml x 43% x Rp. 35.750/960 ml
LAMPIRAN 3
DOKUMENTASI PENELITIAN
3.1 FOTO BAHAN BAKU NIRA SEGAR
Gambar L3.1 Nira Segar
3.2 FOTO ANALISIS KADAR GULA NIRA SEGAR DENGAN
REFRAKTOMETER
3.3 FOTO PROSES FERMENTASI
a. b.
c.
Gambar L3.3 Proses Fermentasi a. Saccharomyces cerevisiae b. Starter c. Hasil Fermentasi
3.4 FOTO PROSES DISTILASI
3.5 FOTO ANALISIS OKSIDASI K2Cr2O7 TERHADAP ETANOL
a. b.
Gambar L3.5 Foto Analisis Oksidasi K2Cr2O7 Terhadap Bioetanol
DAFTAR PUSTAKA
[1] Munthe, Muhammad Ginta., 2015. Pemanfaatan Cangkang Kelapa Sawit dan Limbah Kelapa Sawit (Sludge) Sebagai Bahan Baku Pembuatan Biobriket Arang. Program Studi Keteknikan Pertanian, Fakultas Pertanian, Universitas Sumatera Utara.
[2] Lee, Wen Shiang., Chen, I Chu., Chang, Cheng-Hsiung., Yang, Shang Shyng., 2012. Bioethanol Production From Sweet Potato by Co-Immobilization of Saccharolytic Molds and Saccharomyces cerevisiae. Renewable Energy 39, 216-222.
[3] Alvira, P., Pejo, E. Tomas., Ballesteros, M., Negro, M.J., Pretreatment Technologies For An Efficient Bioethanol Production Process Based On Enzymatic Hydrolysis: A Review. Bioresource Technology 101, 4851-4861.
[4] Wijaya, I Made Anom Sutrisna., Arthawan, I Gusti Ketut., Sari, Anis Novita., 2012. Potensi Nira Kelapa Sebagai Bahan Baku Bioetanol. Jurnal Bumi Lestari, Vol. 12, No.1, Hal. 85-92.
[5] Dias, M.O.S., Junqueira, T.L., Jesus, C.D.F., Rossel, C.E.V., Filho, R. Maciel., Bonomi, A., 2012. Improving Bioethanol Production-Comparison Between Extractive And Low Temperature Fermentation. Applied Energy 98, 548-555.
[6] Alvira, P., Pejo, E. Tomas., Ballesteros, M., Negro, M.J., Pretreatment Technologies For An Efficient Bioethanol Production Process Based On Enzymatic Hydrolysis: A Review. Bioresource Technology 101, 4851-4861.
[7] Mojovic, Ljiljana., Nicolic, Svetlana., Rakin, Marica., Vukasinovic, Maja., 2006. Fuel 85, 1750 1755.
[8] Petersen, Mai Ostergaard., Larsen, Jan., Thomsen, Mette Hedegaard., 2009. Optimization of Hydrothermal Pretreatment of Wheat Straw For Production of Bioethanol at Low Water Consumption Without Addition of Chemicals. Biomass and Bioenergy 33, 834-840.
[9] Kristensen, Soren Bech Pilgaard., Thomsen, Torben Birch., Rasmussen, Kjeld., 2014. Cassava as an Energy Crop: a Case Study of The Potential For an Expansion of Cassava Cultivation for Bioethanol Production in Sothern Mali. Renewable Energy, 381-390.
From Arenga Plant (Arenga pinnata MERR). Vol. 3, No.3. ISSN : 2088-5334.
[11] Tangkuman, Herling D., Rorong, Johnly A., Pandara, Dolfie., Tamuntuan, Gerald., 2010. Produksi Bioetanol dari Nira Aren Menggunakan Energi Geothermal. Chem Prog, Vol. 3, No. 1.
[12] Lin, Yan dan Tanaka, Shuzo., 2006. Ethanol Fermentation From Biomass Resources: Curent State and Prospects. Appl Microbiol Biotechnol 69, 672-642.
[13] Pontoh, Julius., Gunawan, Indriani., Fatimah, Feti., 2011. Analisa Kandungan Protein Dalam Nira Aren.Chem Prog, Vol. 4, No.2.
[14] Florido, Helen B dan Mesa, Priscilla B. De., 2003. Sugar Palm (Arenga pinnata (Wurmb.) Merr). Research Information Series on Ecosystem. Vol 15, No. 2.
[15] Effendi, Dedi Soleh., 2010. Prospek Pengembangan Tanaman Aren (Arenga pinnata Merr) Mendukung Kebutuhan Bioetanol di Indonesia. Perspektif Vol.9, No.1, Hal. 36-46. ISSN : 1412-8004.
[16] Ishak, M.R., Sapuan, S.M., Leman, Z., Rahman, M.Z.A., Anwar, U.M.K., Siregar, J.P., 2013. Sugar Palm (Arenga pinnata): Its Fibres, Polymers and Composites. Carbohydrate Polymers 91, 699-710.
[17] Generoso, Wesley Cardoso., Schadeweg, Virginia., Oreb, Mislav., Boles, Eckhard., 2015. Metabolic Engineering of Saccharomyces cerevisiae For Production of Butanol Isomers. Biotechnology 33, 1-7.
[18] Gnansounou, Edgard and Dauriat, Arnaud. 2005. Ethanol Fuel From Biomass. Journal of Scientific & Industrial Research, Vol.64, pp, 809-821. [19] Rahman, Mohamed Ali Abdel., Xiao, Yaotian., Tashiro, Yukihiro., Wang, Ying., Zendo, Takeshi., Sakai, Kenji., Sanomoto, Kenji., 2014. Fed-Batch Fermentation For Enhanced Lactic Acid Production From Glucose/Xylose Mixture Without Carbon Catabolite Repression. Journal of Bioscience and Bioengineering, Vol. xx, No. xx, 1-6.
[20] Koscher, G S and Uppal, Shivali. 2013. Fermentation Variables For The Fermentation of Glucose and Xylose Using Saccharomyces cerevisiae Y-2034 and Pachysolantannophilus Y-2460. Indian Journal of Biotechnology.Vol 122, pp 531-536.
[22] Lee, Wen Shiang., Chen, I Chu., Chang, Cheng-Hsiung., Yang, Shang Shyng., 2012. Bioethanol Production From Sweet Potato by Co-Immobilization of Saccharolytic Molds and Saccharomyces cerevisiae. Renewable Energy 39, 216-222.
[23] Cheng, Ngoh Gek., Hasan, Masitah., Kumoro, Andri Chahyo., Ling, Chew Fui., Tham, Margaret., 2009. Production of Ethanol by Fed-Batch Fermentation. Pertanika J.SCi & Technol 17 (2), 399-408. ISSN: 0128-7680.
[24] Hanum, Farida., Pohan, Nurhasmawaty., Rambe, Mulia., Primadony, Ratih., Ulyana, Mei., 2013. Pengaruh Massa Ragi dan Waktu Fermentasi Terhadap Bioetanol dari Biji Durian. Jurnal Teknik Kimia USU, Vol. 2, No.4.
[25] Utami, Lucky Indrati., 2009. Pembuatan Etanol dari Buah Mengkudu. Jurnal Teknik Kimia, Vol. 4, No. 1.
[26] Sebayang, Firman., 2006. Pembuatan Etanol dari Molase Secara Fermentasi Menggunakan Sel Saccharomyces cerevisiae yang Terimobilisasi pada Kalsium Alginat. Jurnal Teknologi Proses, 75-80. ISSN: 1412-7814.
[27] Seftian, Deky., Antonius, Ferdinand., Faizal, M., 2012. Pembuatan Etanol dari Kulit Pisang Menggunakan Metode Hidrolisis Enzimatik dan Fermentasi. Jurnal Teknik Kimia, Vol. 18, No.1.
[28] Peraturan Menteri Pertanian Republik Indonesia., 2014. Pedoman Budidaya Aren (Arenga pinnata MERR) yang Baik. Nomor 133/Permentan/OT.140/12/2013. No.17.
[29] Nurfiana, Fifi., Mukaromah, Umi., Jeannisa, Vicki Citra., Putra, Sugili., 2009. Pembuatan Bioetanol dari Biji Durian Sebagai Sumber Energi Alternatif. Seminar Nasiona V SDM Teknologi Nuklir. ISSN: 1978-0176.
[30] Hapsari, Mira Amalia dan Pramashinta, Alice., 2013. Pembuatan Bioetanol dari Singkong (Manihot glaziovii) Untuk Bahan Bakar Kompor Rumah Tangga Sebagai Upaya Mempercepat Konversi Minyak Tanah Ke Bahan Bakar Nabati. Jurnal Teknologi Kimia Industri, Vol. 2, No. 2, Hal. 240-245.
[31] Oktavianus, Ferdin., Sigiro, Roy Martua., Bustan, M. Djoni., 2013. Pembuatan Bioetanol Dari Batang Jarak Menggunakan Metode Hidrolisa Dengan Katalis Asam Sulfat. Jurnal Teknik Kimia, Vol. 19, No. 2.
[33] Lasekan, O., dan Abbas, K.A., 2010. Flavour Chemistry of Palm Toddy and Palm Juice: A Review. Trends in Food Science & Technology 21, 494-501.
[34] Ho, C.W., Aida, W.M. Wan., Maskat, M.Y., Osman, H., 2006. Changes in Volatile Compounds of Palm Sap (Arenga pinnata) During The Heating Process For Production of Palm Sugar. Food Chemistry 102, 1156-1162.
[35] Lay, Abner dan Heliyanto, Bambang., 2011. Prospek Agro-Industri Aren (Arenga pinnata). Perspektif Vol. 10 No. 1. Hal. 01-10. ISSN: 1412-8004. [36] Ali, Aidy., Sanudin, A.B., Ezzedin, Saifuliwan., 2010. The Effect of
Aging On Arenga pinnata Fiber-Reinforced Epoxy Composite. Materials and Design 31, 3550-3554.
[37] Aditiwati, Pingkan., Kusnadi., 2003. Kultur Campuran dan Faktor Lingkungan Mikroorganisme yang Berperan Dalam Fermentasi Tea-Cider. Proc. ITB Sains & Tek, Vol. 35 A, No. 2, Hal. 147-162.
[38] Salsabila, Usyqi., Mardiana, Diah., Indahyanti, Ellya., 2013. Kinetika Reaksi Fermentasi Glukosa Hasil Hidolisis Pati Biji Durian Menjadi Etanol. Jurnal Kimia, Vol. 2, No. 1.
[39] Azizah, N., Al-Baarri, A.N., Mulyani, S., 2012. Pengaruh Lama Fermentasi Terhadap Kadar Alkohol, pH, dan Produksi Gas Pada Proses Fermentasi Bioetanol Dari Whey Dengan Substitusi Kulit Nanas. Jurnal Aplikasi Teknologi Pangan, Vol. 1, No.2.
[40] Jannah, Asyeni Miftahul., 2010. Proses Fermentasi Hidrolisat Jerami Padi Untuk Menghasilkan Bioetanol. Jurnal Teknik Kimia, Vol. 17, No. 1.
[41] Dodic, Sinisa., Popou, Stevan., Dodic, Jelena., Rankovic, Jovana., Zavargo, Zoltan., Mucibabic, Rada Jevtic., 2009. Biothanol Production From Thicjuice as Intermediate of Sugar Beet Processing. Biomass and Bioenergy 33, 822-827.
[42] Betiku, Eriola., Taiwo, Abiola, Ezekiel., 2015. Modeling and Optimization of Bioethanol Production From Breadfruit Starch Hydrolizate vis-à-vis Response Surface Methodology and artificial Neural Network. Renewable Energy 74, 87-94.
[43] Niu, Hongxing., Leak, David., Shah, Nilay., Kontoravdi, Cleo., 2015. Metabolic Characterization and Modeling of Fermentation Process of an Engineered Geobacillus thermoglucosidaus Strain For Bioethanol Production With Gas Stripping. Chemical Engineering Science 122, 138-149.
Yield From Oil Palm Trunk Sap Fermented by Saccharomyces cerevisiae. Journal Of Industrial and Engineering Chemistry. JIEC-2175, No. of Page. 5.
[45] Dehkordi, Mohsen Mobini., Nahvi, Iraj., Esfahami, Hamid Zarkesh., Ghaedi, Kamran., Tavassoli, Manoochehr., Akada, Rinji., 2008. Isolation of a Novel Mutant Strain Of Saccharomyces cerevisiae by an Ethyl Methan Sulfonate-Induced Mutagenesis Approach as a High Producer of Bioethanol. Journal of Bioscience and Bioengineering. Vol. 105, No.4, 403 408.
[46] Lempang, Mody dan Mangopang, Albert D., 2012. Efektivitas Nira Aren Sebagai Bahan Pengembang Adonan Roti. Jurnal Penelitian Kehutanan Wallacea, Vol. 1, No. 1, 26-35.
[47] Kaya, E. 2013., Pengaruh Kompos Jerami dan Pupuk NPK Terhadap N- Tersedia Tanah, Serapan N-, Pertumbuhan, dan Hasil Padi Sawah (Oryza Sativa L). Agrologia. Vol. 2, No. 1, Hal. 43-50.
[48] Dahono., Ghulamahdi, M., Aziz, S.A., Adiwirman., 2011. Kombinasi Pupuk NPK dan Pupuk Kandang Dalam Meningkatkan Pertumbuhan dan Produksi Asiatikosida Tanaman Pegagan. Jurnal Littri, Vol. 17, No. 2, 51-59.
[49] Hayati, Erita., 2010. Pengaruh Pupuk Organik dan Anorganik Terhadap Kandungan Logam Berat Dalam Tanah dan Jaringan Tanaman Selada. J. Floratek 5, 113-123.
[50] Santoso, Budi., Budi, Untung Setyo., Nurnasari, Elda., 2012. Pengaruh Jarak Tanaman dan Dosos Pupuk NPK Majemuk Pertumbuhan, Produksi Bunga dan Analisis Usaha Tani Rosela Merah. Jurnal Littri 18(1), Hal. 17-23.
[51] Puslitbang Perkebunan., 2009. Info BBN Nira Aren Sebagai Bahan Baku Etanol. Vol.1, No. 5. ISSN: 2085-319X.
[52] ”Manisnya Laba Dari ula Aren,“ Medan Bisnis, Februari
[53] ”Bos Per a ina: % ebu uhan BBM RI Berasal Dari I por,“ De ik Finance, 14 Juli 2015.
[54] ”Dua S ra egi Tingka kan Produksi ula asional,“ C Indonesia, April 2015.
[55] SNI 01-3140.2., 2006. Gula Kristal-Bagian 2: Rafinasi (Refined Sugar). [56] Perry, Rober H , reen, Don W , Perry’s Che ical Engineers
[57] Jamaliah, Mustaofidatul., 2011. Sintesis Etanol Melalui Reaksi Hidrogenasi Heksil Asetat Dengan Menggunakan Berbagai Katalis. Program Studi Kimia, Fakultas Sains dan Teknologi, Universitas Islam Negeri Syarif Hidayatullah, Jakarta.
[58] Hidayanto, Eko., Rofiq, Abdul., Sugito, Heri., 2010. Aplikasi Portable Brix Meter Untuk Pengukuran Indeks Bias. Berkala Fisika, Vol.13, No. 4, Hal. 113-118. ISSN: 1410-9662.
[59] D.L. Pavia, G.M. Lampman, dan Kriz, S , “In roduc ion To
Spec roscopy : A uide for S uden s of Organic Che is ry,” Singapore:
Thomson Learning, 2001).
[60] Shidiq, Ari Syahidul., Haryono., 2014. Optimalisasi Pembuatan Bioetanol Anhydrous Dari Umbi Gembili (Discorea esculenta L) Sebagai Campuran Premium Untuk Meningkatkan Angka Oktan. ISBN: 979363174-0.
[61] Pinata, Dian., Nawfa, Refdinal., 2011. Uji Kualitatif Etanol yang Diproduksi Secara Enzimatis Menggunakan Z. Mobilis Permeabel. Jurusan Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Teknologi Sepuluh November. SK-091304.
[62] Sulistyani, M.Si., 2013. Pemanfaatan Limbah Bonggol Pisang Sebagai Bahan Baku Pembuatan Bioetanol. Jurnal Sains Dasar, Vol. 2, No. 1, Hal. 48-52. ISSN : 2085-9872.
[63] Putri, Lily Surayya Eka., Sukandar, Dede., 2008. Konversi Pati Ganyong (Canna Edulis Ker.) Menjadi Bioetanol Melalui Hidrolisis Asam dan Fermentasi. Program Studi Biologi, Fakultas Sains dan Teknologi, Universitas Islam Negeri Syarif Hidayatullah, Tangerang. ISSN: 1412-033X.
[64] Arnata, I wayan., Anggreni, Dewi A.A.M., 2013. Rekayasa Bioproses Produksi Bioetanol Dari Ubi Kayu Dengan Teknik Ko-Kultur Ragi Tape dan Saccharomyces cerevisiae. Agrointek Vol. 7, No. 1.
[65] Oktaviani, Intan., Ahmad, Adrianto., Chairul., 2015. Pengaruh Laju Pengadukan Terhadap Biokonversi Reject Nanas Menjadi Bioetanol. Jom FTeknik Vol. 2, No.1.
[66] Abogbo, F.K., Kelly, G.C., Smith, M.T., Wenger, K., Jeffries, T.W., 2007. The Efeect of Initial Cell Concentration on Xylose Fermentation by Pichia stiptis. Journal of Applied Biochemistry and Biotechnology 41: 2331-2336.
[68] Stewart, GG., 2014. Saccharomyces cerevisiae. Vol. 3, PP. 1918-1925. [69] Khak, Muhammad., Rohmatningsih, Rini Nuraini., Purwito., 2008.
Optimalisasi Fermentor Untuk Produksi Etanol dan Analisis Hasil Fermentasi Menggunakan Gas Chromatografi. Jurnal Matematika, Sains dan Teknologi. Vol. 15, No. 1, Hal. 12-20.
[70] Wardani, Agustin Krisna., Pertiwi, Fenty Nurtyastuti Eka., 2013. Produksi Etanol Dari Tetes Tebu Oleh Saccharomyces cerevisiae Pembentuk Flok (NRRL-Y 265). Agritech, Vol. 33, No. 2.
[71] Tian, Shuang Qi., Wang, Xin Wei., Zhao, Ren Yong., Ma, Sen., 2016. Effect of Doping Preatreated Corn Stover Conditions On Yield of Bioethanol in Immobilized Cell Systems. Renewable Energy 86, 858-865.
BAB III
METODOLOGI PENELITIAN
3.1 LOKASI PENELITIAN
Penelitian dilakukan di Laboratorium Mikrobiologi Teknik, Departemen Teknik Kimia, Fakultas Teknik, Universitas Sumatera Utara, Jalan Almamater Kampus USU, Medan, Indonesia.
3.2 BAHAN DAN PERALATAN
3.2.1 Bahan
Pada penelitian ini bahan yang digunakan antara lain : 1. Nira aren (Arenga pinnata Merr)
2. Biokatalis (Saccharomyces cervisiae) 3. NPK
3.2.2 Peralatan
Pada penelitian ini peralatan yang digunakan antara lain : 1. Autoclaved
2. Beaker glass
3. Corong gelas 4. Erlenmeyer 5. Gelas ukur
6. Kondensor refluks 7. Labu leher tiga 8. Neraca digital 9. Hemositometer 10. Water bath
11. Piknometer 12. Refraktometer 13. Statif dan klem 14. Stopwatch
3.3 PROSEDUR PENELITIAN
3.3.1 Prosedur Pembuatan Starter
1. Semua peralatan disterilisasi di dalam autoclave selama 15 menit pada suhu 121 oC.
2. Kadar gula nira aren (Arenga pinnata Merr) segar diukur dengan refraktometer.
3. Nira aren dipasteurisasi pada suhu 80 oC kemudian didinginkan hingga suhu ruangan.
4. Dicampurkan satu oase S.cerevisiae dengan 500 ml nira aren kemudian diaduk di rotary shaker hingga merata.
5. Starter didiamkan selama 48 jam pada suhu ruangan.
6. Dilakukan perhitungan jumlah sel hingga diperoleh konsentrasi larutan starter diatas 1.106 sel/ml dengan hemositometer.
3.3.2 Prosedur Fermentasi
1. Semua peralatan disterilisasi di dalam autoclave selama 15 menit pada suhu 121 oC.
2. Kadar gula nira aren (Arenga pinnata Merr) segar diukur dengan refraktometer.
3. Nira aren dipasteurisasi pada suhu 80 oC kemudian didinginkan hingga
suhu ruangan.
4. Dicampurkan nira aren dengan larutan starter sebanyak 15% (v/v) dari total volume campuran 500 ml.
5. Ditambahkan NPK 0,4% (m/m) ke dalam larutan.
6. Campuran dijaga pada suhu 35 oC selama 24 jam dalam kondisi anaerobik. 7. Dimasukkan hasil fermentasi ke dalam peralatan distilasi, kondisi operasi
diatur pada suhu 85 oC.
8. Distilat di tampung dengan erlenmeyer dan diukur volumenya. 9. Diambil sampel distilat untuk dianalisis.
3.3.3 Prosedur Analisis
3.3.3.1Analisis Kadar Gula Nira Segar Dengan Refraktometer
1. Dibersihkan permukaan prisma refraktometer lalu keringkan.
2. Dialirkan satu tetes aquades ke prisma refraktometer untuk menentukan titik nol.
3. Dibersihkan dan dikeringkan prisma refraktometer.
4. Diteteskan nira segar ke permukaan prisma dengan menggunakan batang plastik, buat larutan gula menyebar ke permukaan prisma dan jangan sampai terbentuk gelembung kemudian prisma ditutup.
5. Baca hasil pengukuran kadar gula pada refraktometer [55].
3.3.3.2 Analisis Densitas
1. Alat piknometer yang digunakan untuk mengukur densitas bioetanol dikeringkan ke dalam oven pada temperatur 100 oC selama 10 menit kemudian didinginkan sampai suhu kamar.
2. Ditimbang piknometer kosong dengan menggunakan neraca analitis kemudian dicatat massanya.
3. Diisi piknometer dengan aquades kemudian ditimbang dengan neraca analitis dan dicatat massanya. Dicatat suhu aquades pada saat pengukuran. 4. Piknometer dikeringkan di dalam oven pada temperatur 100 oC selama 10
menit lalu didinginkan sampai suhu kamar. 5. Dimasukkan sampel distilat ke dalam.
6. Ditimbang piknometer yang berisi sampel distilat dengan menggunakan neraca analitis dan dicatat massanya.
7. Dihitung densitas distilat dengan rumus :
ρ1/ m1 = ρ2/ m2
Dimana:
ρ1 = densitas air
m1 = massa (piknometer berisi air – piknometer kosong)
ρ2 = densitas distilat
3.3.3.3 Analisis Spesific Gravity dan API Gravity
Specific gravity dan API gravity adalah suatu pernyataan yang menyatakan densitas (kerapatan) atau berat per satuan volume dari suatu bahan. Hubungan antara specific gravity (sg) dan API gravity (G) adalah sebagai berikut:
, sg ,
Besarnya harga dari API gravity berkisar dari 0-100, sedangkan specific gravity merupakan harga relatif dari densitas suatu bahan terhadap air. Hubungan antara densitas dan specific gravity adalah sebagai berikut:
S densi as
kg
densi as air kg
3.3.3.4 Analisis Nilai Kalor
Nilai densitas, spesific gravity dan API gravity kemudian digunakan untuk menghitung nilai kalor dengan persamaan:
, ,
3.3.3.5 Analisis Kadar Bioetanol dengan Metode Densitas
Analisa kadar bioetanol dilakukan dengan metode densitas dengan cara berikut:
1. Nilai densitas yang diperoleh sebelumnya dicocokkan pada tabel 3.1
berikut.
2. Kadar etanol dihitung dengan menginterpolasi data densitas (berat jenis) dan kadar etanol pada suhu 30 oC pada tabel 3.1.
6
3.3.3.6 Analisis Bioetanol Dengan Reaksi Oksidasi Kalium Dikromat (K2Cr2O7)
Analisis kualitatif bioetanol dilakukan dengan metode reaksi oksidasi dengan langkah sebagai berikut:
1. Persiapan bahan dan alat yang ingin digunakan pada saat analisis.
2. Dimasukkan ke dalam tabung reaksi 2 ml K2Cr2O7 2% dan tambahkan 5
tetes H2SO4 pekat.
3. Tabung reaksi digoyangkan hingga larutan homogen.
4. Ditambahkan 1 ml sampel bioetanol ke dalam tabung reaksi yang telah homogen.
5. Diamati perubahan yang terjadi.
3.4 FLOWCHART PENELITIAN
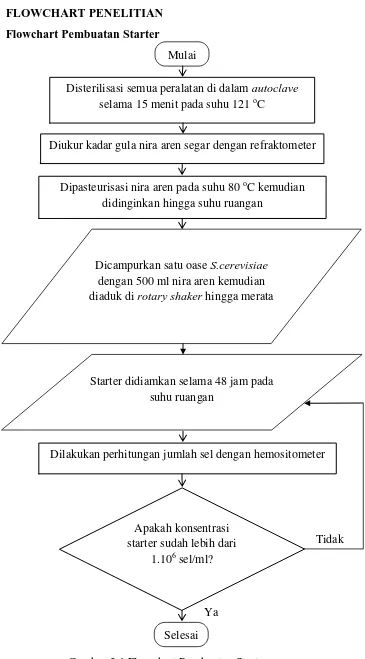
3.4.1 Flowchart Pembuatan Starter
Gambar 3.1 Flowchart Pembuatan Starter Dicampurkan satu oase S.cerevisiae
dengan 500 ml nira aren kemudian diaduk di rotary shaker hingga merata
Ya
Tidak Dilakukan perhitungan jumlah sel dengan hemositometer
Dipasteurisasi nira aren pada suhu 80 oC kemudian didinginkan hingga suhu ruangan
Mulai
Selesai
Disterilisasi semua peralatan di dalam autoclave
selama 15 menit pada suhu 121 oC
Apakah konsentrasi starter sudah lebih dari
1.106 sel/ml?
Starter didiamkan selama 48 jam pada suhu ruangan
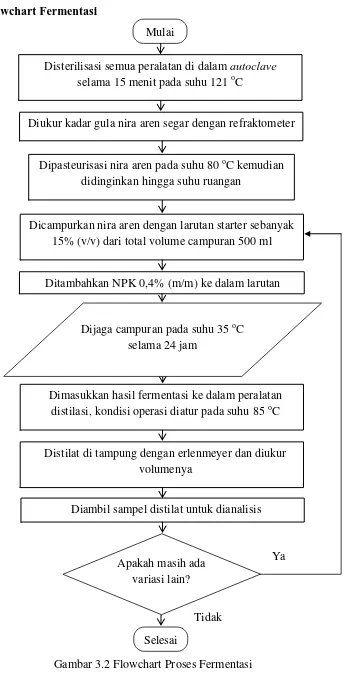
3.4.2 Flowchart Fermentasi
Gambar 3.2 Flowchart Proses Fermentasi
Diukur kadar gula nira aren segar dengan refraktometer
Dicampurkan nira aren dengan larutan starter sebanyak 15% (v/v) dari total volume campuran 500 ml
Mulai
Selesai
Disterilisasi semua peralatan di dalam autoclave
selama 15 menit pada suhu 121 oC
Ditambahkan NPK 0,4% (m/m) ke dalam larutan
Dimasukkan hasil fermentasi ke dalam peralatan distilasi, kondisi operasi diatur pada suhu 85 oC
Distilat di tampung dengan erlenmeyer dan diukur volumenya
Diambil sampel distilat untuk dianalisis
Apakah masih ada variasi lain?
Ya
Tidak Dijaga campuran pada suhu 35 oC
selama 24 jam
BAB IV
HASIL DAN PEMBAHASAN
4.1 HASIL ANALISIS KADAR GULA NIRA AREN
Penelitian ini dilakukan dengan menggunakan bahan baku berupa nira aren (Arenga pinnata Merr) yang diperoleh dari kecamatan Namorambe, Sumatera Utara, Indonesia. Hasil pengukuran dengan menggunakan refraktometer diperoleh kandungan gula nira aren sebesar 11% brix. Brix adalah zat padat kering yang terlarut dalam suatu larutan yang dihitung sebagai sukrosa. Selain itu brix juga didefinisikan sebagai persentase massa sukrosa yang terkandung di dalam massa larutan sukrosa [58]. Berdasarkan Tangkuman et al [11] yang menyatakan bahwa nira aren mengandung kadar gula berkisar 6-16%.
4.2 KARAKTERISASI FTIR (FOURIER TRANSFORM INFRA RED) ETANOL
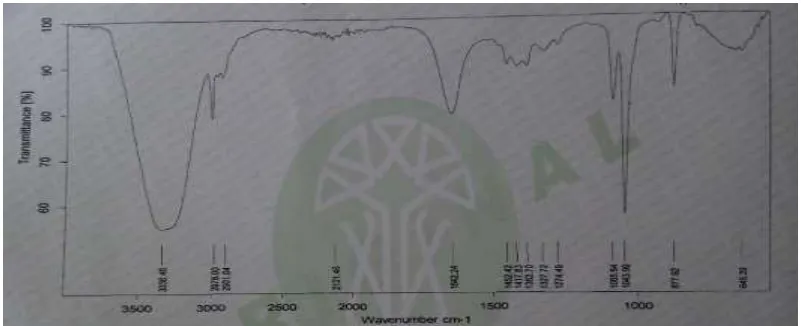
Karakterisasi FTIR (Fourier Transform Infra Red) etanol dari nira aren dilakukan untuk mengidentifikasi gugus fungsi dari senyawa etanol. Karakteristik FTIR etanol dapat dilihat pada Gambar 4.1 di bawah ini.
Gambar 4.1 Spektrum FTIR (Fourier Transform Infra Red) Etanol Dari Nira Aren
Keterangan analisa gugus fungsi [59]:
- 3336,46 cm-1 : ikatan pada -OH
- 2978,00 cm-1 : ikatan pada alkana C-H
- 1642,24 cm-1 : ikatan pada amida N-H
- 1085,54 : ikatan pada C-OH
- 1043,99 cm-1 : ikatan pada C-OH
Data spektrum etanol dengan mencermati puncak serapan gelombang yang diperlihatkan dapat dianalisis bahwa pada serapan 3336,46 cm-1 terdapat serapan
yang kuat dan melebar, Serapan yang melebar menunjukkan adanya interaksi antara molekul elektronegatif O dengan positif H yang membentuk ikatan hidrogen [60]. Hal ini menunjukkan adanya gugus –OH dalam sampel. Serapan kecil pada 2978,00 cm-1 menunjukkan adanya ikatan alkana (C-H) yang kuat. Pada serapan 1043,99 cm-1 terdapat ikatan C-OH. Maka dari hasil analisis FTIR dapat disimpulkan bahwa sampel uji yang merupakan produk dari penelitian ini adalah etanol.
Namun dari hasil analisis FTIR bioetanol masih terdapat beberapa gugus fungsi yang lain diantaranya adanya serapan pada 1642,24 cm-1 menunjukkan adanya ikatan antara nitrogen dan hidrogen (N-H). Serta pada 877,92 cm-1 menunjukkan adanya ikatan aromatik. Hal ini disebabkan karena adanya kandungan senyawa lain selain gula seperti abu, protein dan lemak pada nira [13] yang terurai pada saat pemanasaan saat distilasi kemudian ikut menguap bersama etanol sehingga terdapat beberapa gugus lain pada kandungan bioetanol yang diperoleh.
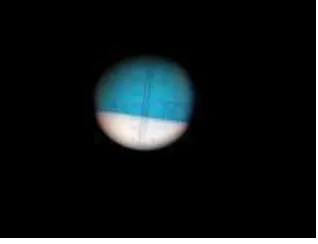
4.3 HASIL ANALISIS ETANOL DENGAN REAKSI OKSIDASI KALIUM DIKROMAT (K2Cr2O7)
Analisis reaksi oksidasi dengan kalium dikromat (K2Cr2O7) dilakukan untuk
mengidentifikasi kandungan etanol yang terdapat pada distilat yang diperoleh dari proses fermentasi nira aren. Dari hasil analisis diperoleh perubahan warna larutan dari jingga menjadi hijau kebiruan sesuai dengan gambar di bawah ini.
Gambar 4.2 Perubahan Warna Pada Oksidasi Etanol Dengan K2Cr2O7
antara etanol dengan kalium dikromat dalam suasana asam [61]. Persamaan reaksi di bawah ini [62] :
Cr2O72- + 14H+ + 6e 2Cr3+ + 7H2O
3C2H5OH 3CH3CHO + 6H+ + 6e +
3C2H5OH + Cr2O72- + 8H+ 2Cr3+ + 3CH3CHO + 7H2O
Reaksi ini ditandai berubahnya warna kalium dikromat yang mula-mula berwarna jingga menjadi hijau kebiruan [61]. Hal ini dikarenakan alkohol mengalami oksidasi sedangkan Cr6+ di dalam K2Cr2O7 tereduksi menjadi Cr3+.
Maka dari hasil analisis dapat disimpulkan bahwa distilat mengandung etanol yang diharapkan.
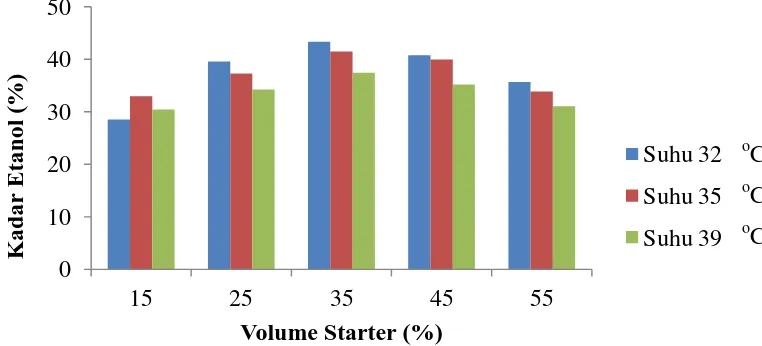
4.4 PENGARUH SUHU DAN VOLUME STARTER TERHADAP KADAR ETANOL
Hubungan antara volume starter dan suhu terhadap kadar bioetanol yang
dihasilkan dapat dilihat pada gambar 4.1. Kadar etanol yang dihasilkan dianalisis berdasarkan tabel konversi berat jenis-kadar etanol [63]. Profil kadar etanol yang
dihasilkan dilihat setelah 24 jam proses fermentasi dan telah melalui tahap distilasi.
Gambar 4.3 Grafik Pengaruh Suhu dan Volume Starter Terhadap Kadar Etanol
Gambar 4.3 menunjukkan bahwa perolehan kadar bioetanol mengalami peningkatan di awal kemudian mengalami penurunan selama proses fermentasi, sehingga grafik membentuk parabola. Hal ini menyatakan bahwa suhu dan volume starter sangat mempengaruhi proses fermentasi untuk membentuk etanol
Dalam penelitian ini diperoleh kadar etanol tertinggi sebesar 43,3165 % pada perlakuan suhu 32 oC dengan penambahan volume stater sebesar 35 %.
Sedangkan kadar etanol terendah diperoleh pada perlakuan suhu 32 oC dengan penambahan volume starter 15 % sebesar 28,5568 %. Hal ini telah sesuai dengan teori yang menyatakan bahwa volume inokulum merupakan variabel yang paling berpengaruh dalam menghasilkan alkohol, semakin besar volume inokulum, semakin besar pula konsentrasi alkohol yang didapat. Hal ini dikarenakan fase lag dipengaruhi oleh volume inokulum. Semakin besar volume inokulum maka semakin pendek fase lag yang terjadi, sehingga cepat mencapai fase log atau fase eksponensial [65]. Selain itu Agbobo et al [66] menyatakan bahwa penambahan inokulum dengan konsentrasi rendah menyebabkan laju fermentasi menjadi lambat, tetapi dapat menghasilkan etanol yang lebih tinggi karena setelah sel memperbanyak diri, sel akan mengkonversi gula menjadi etanol secara perlahan. Namun Mukhtar [67] menjelaskan bahwa inokulasi yeast yang telalu tinggi menyebabkan proses melemah lebih cepat dan menurunkan viabilitas sel setelah fase pertumbuhan. Kondisi pertumbuhan dan metabolisme pada populasi sel yang tinggi tidak diharapkan karena mengganggu akses nutrisi, keterbatasan ruang dan interaksi antar sel. Hal ini terlihat dari grafik yang terus meningkat kemudian menurun dengan jumlah starter semakin tinggi.
Selain volume starter, suhu juga sangat mempengaruhi kadar bioetanol yang
dihasikan. Gambar 4.3 menunjukkan kadar bioetanol yang dihasilkan pada suhu 32 oC lebih tinggi dibandingkan 35 oC dan 39 oC. mikroba memiliki kriteria pertumbuhan berbeda-beda. Menurut Stewart [68] pembentukan etanol akan meningkat di atas suhu 30 oC. Sedangkan Saccharomyces cerevisiae akan tumbuh antara suhu 5 oC dan 40 oC namun pertumbuhannya maksimum pada temperatur optimum yang umumnya berkisar 25- 35 oC. Khak et al [69] menyatakan
4.5 PENGARUH SUHU DAN VOLUME STARTER TERHADAP YIELD ETANOL
Hubungan antara volume starter dan suhu terhadap yield etanol yang dihasilkan dapat dilihat pada gambar 4.4. Profil yield etanol yang dihasilkan dilihat setelah 24 jam proses fermentasi dan telah melalui tahap distilasi.
Gambar 4.4 Grafik Pengaruh Suhu dan Volume Starter Terhadap Yield Etanol Gambar 4.4 menunjukkan bahwa yield etanol yang dihasilkan mengalami peningkatan di awal kemudian mengalami penurunan seiring bertambahnya
volume starter.
Dalam penelitian ini dihasilkan yield etanol tertinggi sebesar 38,1430 % pada perlakuan suhu 32 oC dengan penambahan volume starter 35 %. Sedangkan perolehan yield etanol terendah sebesar 15,5667 % pada perlakuan suhu 32 oC dengan penambahan volume starter 15 %. Yield etanol berbanding lurus terhadap konsentrasi etanol yang dihasilkan. Kenaikan konsentrasi etanol akan meningkatkan nilai yield etanol. Hal ini menunjukkan semakin tinggi nilai yield maka semakin efisien proses fermentasi tersebut [21].
Wardani dan Pertiwi [70] menyatakan bahwa pada konsentrasi sumber gula yang lebih tinggi dibutuhkan inokulum yang lebih banyak untuk mengkonversi gula menjadi etanol .Tian et al [71] melaporkan bahwa peningkatan sel ragi/inokulum pada titik tertentu untuk fermentasi menghasilkan efisiensi produksi bioetanol yang lebih tinggi.
Gambar 4.4 memperlihatkan bahwa peningkatan suhu pada proses fermentasi tidak menunjukkan nila yield yang semakin tinggi. Disisi lain Fahrizal et al [10] menyatakan bahwa peningkatan suhu akan meningkatkan perolehan kadar etanol. Dimana kadar etanol berbanding lurus terhadap nilai yield. Hal ini menunjukkan bahwa suhu dan volume starter sangat mempengaruhi pertumbuhan
Saccharomyces cerevisiae dalam melakukan proses fermentasi. Pada kondisi optimum, peningkatan suhu akan meningkatkan kecepatan pertumbuhan mikroba, maka jumlah sel akan semakin banyak [68]. Jumlah populasi sel yang semakin tinggi tidak diharapkan dalam proses fermentasi karena akan mengakibatkan keterbatasan ruang dan interasksi antar sel sehingga terjadi kemunduran dalam perolehan etanol [67].
Yield etanol sebesar 38,1430% dimanfaatkan untuk pembentukan etanol sedangkan sisanya 61,8570% dimanfaatkan untuk proses lain, seperti untuk mempertahankan metabolisme sel, untuk pembentukan biomassa atau asam piruvat yang terbentuk pada proses glikolisis belum mampu sepenuhnya dirubah menjadi etanol oleh Saccharomyces cerevisiae [64]. Yield etanol yang rendah dapat disebabkan karena adanya hambatan pembentukan dalam konsentrasi tinggi dalam waktu yang terbatas, selain itu penguapan lambat dari etanol atau kehilangan etanol saat distilasi menyebabkan penurunan konsentrasi etanol [44].
4.6 PERBANDINGAN STANDAR BAKU MUTU BIOETANOL
Untuk membandingkan larutan bioetanol yang diperoleh dari penelitian ini dengan standar etanol nabati seharusnya dapat ditunjukkan oleh tabel 4.2 berikut.
Tabel 4.1 Standar Etanol Nabati [56]
No. Parameter Satuan Mutu Standar Bioetanol
Etanol g/ml Maks. 0,7890 0,9206-0,9500
Belum
5. Reaksi
dengan Api - Mudah Terbakar Tidak Terbakar
Belum hasil dari penelitian ini telah memenuhi standar etanol nabati. Sedangkan untuk kelayakan sebagai bahan baku alternatif, Badan Standar Nasional (BSN) telah menetapkan standar baku mutu bioetanol secara umum seperti tabel 4.2 berikut ini.
Tabel 4.2 Syarat Mutu Bioetanol Bahan Bakar [72]
No. Parameter Satuan Mutu Standar Bioetanol
Bioetanol dari Nira Aren
(Hasil Penelitian) Keterangan
1. Kadar
Bioetanol yang dihasilkan pada penelitian ini belum memenuhi standar bioetanol bahan bakar yang telah ditentukan, hal ini disebabkan oleh beberapa faktor diantaranya:
1. Tertimbunnya produk serta terbentuknya flok akibat dari akumulasi jumlah mikroba pada proses fermentasi.
BAB V
KESIMPULAN DAN SARAN
5.1 KESIMPULAN
Adapun kesimpulan yang diperoleh dari penelitian ini adalah:
1. Kadar etanol yang tertinggi diperoleh sebesar 43,3165 % pada perlakuan suhu 32 oC dengan penambahan volume starter 35 %.
2. Yield etanol tertinggi dihasilkan sebesar 38,1430 % pada perlakuan suhu 32
o
C dengan penambahan volume starter 35 %.
5.2 SARAN
Saran yang dapat diberikan untuk penelitian selanjutnya adalah :
1. Sebaiknya dilakukan distilasi bertingkat atau penambahan senyawa anhidrat untuk meningkatkan kemurnian bioetanol.
2. Sebaiknya dilakukan perhitungan jumlah sel setelah proses fermentasi. 3. Sebaiknya dilakukan analisis lain untuk menganalisis etanol yang diperoleh,
BAB II
TINJAUAN PUSTAKA
2.1BIOETANOL
Bioetanol merupakan etanol yang dibuat dari tanaman [24]. Etanol dapat dibuat dari bahan-bahan pertanian diantaranya bahan-bahan yang mengandung turunan gula, mengandung pati dan mengandung selulosa melalui proses fermentasi [25]. Fermentasi merupakan salah satu cara untuk mengkonversi karbohidrat menjadi etanol dengan bantuan mikroorganisme [26].
Etanol disebut juga etil alkohol dengan rumus kimia C2H5OH merupakan
cairan kimia yang tak berwarna dengan karakteristik lainnya yaitu mudah terbakar, mudah menguap, tidak karsinogenik dan jika terjadi pencemaran tidak memberikan efek yang buruk terhadap lingkungan secara signifikan [27]. Etanol dikategorikan menjadi 2 kelompok utama yaitu etanol 95-96 % v/v disebut etanol hidrat digunakan untuk desinfektan, pelarut serta dijadikan minuman yang berkualitas tinggi dan etanol >99,5 % disebut Ethanol Fuel Grade dan digunakan sebagai bahan bakar [24]. Bioetanol 97 % belum dapat dikatakan FGE namun dapat dijadikan bahan bakar mesin, serta bioetanol 95-99 % dapat dijadikan sebagai bahan substitusi bensin atau premium dengan rasio bensin-bioetanol
90:10 dan dapat menghemat bahan bakar sebesar 12,5-29 % dibandingkan dengan menggunakan bensin murni [28].
Tabel 2.1 Sifat Fisika dan Sifat Kimia Etanol [31]
Sifat Fisika dan Sifat Kimia Nilai
Berat molekul, g/mol Titik beku, oC Titik didi normal, oC
Densitas, g/ml
Viskositas (20 oC), mPas (Cp) Panas penguapan normal, J/g Panas pembakaran pada 25 oC, J/g
Panas jenis pada 25 oC, J (g oC) Nilai oktan
Wujud pada suhu kamar Dicampur dengan natrium minuman alami yang manis dan transparan. Nira diperoleh dengan menekan ganggang dari tanaman aren tersebut. Kemudian puncak dari tangkai diiris sekitar 1-5 mm selama proses penyadapan. Pipa bambu digunakan untuk mengumpulkan getah/nira [32]. Tangkai dapat diiris setiap hari dan disadap sekali atau dua kali setiap hari selama periode aliran getah [14].
Nira yang transparan memiliki kandungan gula 100-144 g/kg dengan pH 7,0-7,4 [33]. Getah atau nira yang dikumpulkan dari pohon tanaman aren mengandung sekitar 10-12 % total gula yang terdiri dari sukrosa, lebih sedikit gula tereduksi, mineral lain dan vitamin [32]. Menurut Pontoh [13] nira segar megandung gula 13,9-14,9%, abu 0,04%, protein 0,2% dan kadar lemak 0,02%.Nira mengandung sukrosa yang melimpah dan sisi kutubnya merupakan rantai asam amino khususnya asparagin dan glutamin [34].
4 jam terpapar suhu lingkungan, nira akan terfermentasi menjadi minuman beralkohol yang disebut tuak [32].
Nira adalah salah satu produk tanaman aren (Arenga pinnata Merr) yang bernilai ekonomis [35]. Dimana aren (Arenga pinnata Merr) dapat ditemukan tumbuh liar di hutan primer dan sekunder di Asia tenggara. Aren dapat tumbuh tinggi mencapai 12 meter dan memiliki batang yang tebal, berserat dan berbulu yang ditutupi daun lebat berwarna putih dibagian bawah. Keseluruhan aren tertutup oleh serat hitam yang disebut ijuk [36].
2.3FERMENTASI
Fermentasi merupakan perubahan kimiawi dari senyawa-senyawa organik oleh enzim yang dihasilkan oleh mikroorganisme. Mikroorganisme yang berperan dalam proses fermentasi ini terutama dari golongan khamir (yeast), kapang (fungi) dan bakteri [37].
Reaksi fermentasi glukosa menjadi bioetanol ditunjukkan oleh persamaan reaksi di bawah ini:
C6H12O6 2C2H5OH + 2CO2 [38]
Faktor-faktor yang mempengaruhi hasil fermentasi antara lain : 1. Nutrisi
Merupakan bahan baku yang mengandung nutrien seperti karbohidrat yang
menjadi sumber karbon dan nutrien lain seperti protein. Nutrien-nutrien ini berfungsi sebagai penghasil energi bagi mikroba untuk menghasilkan produk pada proses fermentasi.
2. Suhu
Suhu akan mempengaruhi lamanya fermentasi. Suhu akan disesuaikan dengan kriteria mikroba yang digunakan. Jika suhu terlalu tinggi akan menyebabkan mikroba mati sehingga proses fermentasi tidak akan berlangsung, sedangkan jika suhu terlalu rendah maka fermentasi akan berlangsung lambat [39].
3. Derajat Keasaman (pH)
kapang pada pH 3-7. Dengan mengontrol pH dapat meminimalkan kontaminan [40].
4. Oksigen
Oksigen secara tidak langsung mempengaruhi fermentasi. Secara aerob maka mikroba akan menghidrolisi gula menjadi air dan CO2, tetapi pada kondisi
anaerob gula akan diubah menjadi alkohol dan CO2.
5. Mikroba
Dalam fermentasi alkohol biasanya digunakan khamir karena khamir mampu mengkonversi gula menjadi alkohol karena adanya enzim zimase [39]. Ada beberapa jenis khamir yang digunakan seperti Saccharomyces cerevisiae [41],
dry yeast [42], G. thermoglucosidasius [43], dan sebagainya.
2.4SACCHAROMYCES CEREVISIAE
Mikroorganisme yang paling banyak digunakan untuk memproduksi bioetanol adalah ragi, khususnya Saccharomyces cerevisiae. Saccharomyces cerevisiae
sering dipilih untuk produksi etanol karena sangat baik dalam melakukan fermentasi dan kemampuannya untuk tumbuh dengan cepat dibawah kondisi anaerobik dan toleransi yang tinggi terhadap etanol [44].
Saccharomyces cerevisiae banyak diaplikasikan pada bioteknologi karena memiliki fitur penting yaitu genomik DNA nya tidak mengandung intron, urutan
genom yang telah ditentukan dan teknologi fermentasi cukup berbeda [45].
Salah satu media untuk pertumbuhan mikroorganisme adalah nira. Nira aren dapat mengalami fermentasi secara alami karena dari asalnya nira aren telah membawa sel ragi yaitu Saccharomyces tuac, Dengan itu Saccharomyces sangat aktif dalam mensintesa gula (glukosa) sehingga menghasilkan alkohol dan CO2
[46].
2.5PUPUK MAJEMUK (NPK)
N, P, dan K merupakan unsur hara essensial bagi tanaman. Penyerapan salah satu unsur ke dalam tubuh tanaman dipengaruhi oleh adanya kecukupan unsur
hara lainnya, misalnya nitrogen meningkatkan penyerapan posfor, sedangkan kalium yang tidak tersedia dalam jumlah cukup juga mengakibatkan efisiensi nitrogen dan posfor menjadi rendah [48]. Keuntungan pupuk NPK adalah:
1. Dapat dipergunakan dengan memperhitungkan kandungan zat hara sama dengan pupuk tunggal.
2. Apabila tidak ada pupuk tunggal dapat diatasi dengan pupuk majemuk. 3. Penggunaannya sangat sederhana.
4. Pengangkutan dan penyimpanan pupuk ini menghemat waktu, ruangan dan biaya.
5. Pupuk majemuk ini hampir seluruhnya larut dalam air, sehingga unsur hara yang dikandungnya dapat segera diserap dan digunakan oleh tanaman dengan efektif [47].
Pemberian pupuk ini bertujuan untuk menjaga ketersediaan nutrisi tanaman agar tetap seimbang selama proses pertumbuhannya serta dapat merangsang pertumbuhan tanaman [49]. Pemupukan NPK majemuk merupakan pemberian unsur hara pada tanaman yang efisien dibanding dengan pemupukan tunggal. Tergolong murah dibanding dengan pupuk tunggal [50], mudah dan cepat tersedia [49].
2.6POTENSI EKONOMI BIOETANOL DARI NIRA AREN
Indonesia memiliki potensi tanaman aren yang cukup besar. Sentra
pertanaman aren meliputi 14 provinsi dengan perkiraan total areal seluas 60.482 ha. Menurut Puslitbang Perkebunan Indonesia [51] Jumlah tanaman aren setiap hektar rata-rata 156 pohon. Kalau yang berproduksi 50% dari populasi, maka produksi nira 210.600 liter/ha/tahun dan rata-rata setiap 10 liter nira dapat menghasilkan 3,5 liter etanol.
yang sederhana. Perlu diketahui harga bahan baku yang digunakan dalam pembuatan bioetanol yang juga mempengaruhi harga jual bioetanol. Berikut harga
komersial bahan baku nira aren dan harga jual bioetanol. Harga nira aren = Rp. 13.333,-/liter Harga bioetanol = Rp. 35.750,-/liter
Terlihat perbedaan harga jual bahan baku dan bioetanol yang cukup tinggi tanpa mengaitkan biaya produksi. Maka perlu dilakukan penelitian untuk ini agar dapat meningkatkan nilai ekonomi dari nira aren tersebut.
BAB I
PENDAHULUAN
1.1LATAR BELAKANG
Sumber energi utama yang digunakan saat ini berasal dari bahan bakar konvensional [1]. Bahkan di negara-negara berkembang, termasuk Indonesia, konsumsi energi yang berasal dari bahan tak terbarukan mencapai 90 % dari total energi yang digunakan. Yang mana sumber bahan bakarnya diimpor dari negara lain [2].
Sektor transportasi mengkonsumsi energi paling besar, yakni 27% dari total kebutuhan energi dunia [3] Hal ini menyebabkan tekanan pada pasokan minyak, emisi CO2 ke atmosfer dan mendorong terjadinya perubahan iklim [2].
Untuk mengatasi krisis energi dunia, telah banyak dilakukan usaha diversifikasi sumber energi seperti pemanfaatan limbah pertanian, hasil perkebunan dan kehutanan, serta pengembangan alternatif lain seperti biobriket yang digunakan untuk kebutuhan rumah tangga, biodiesel yang digunakan sebagai bahan campuran diesel maupun gasohol yang merupakan campuran bioetanol dan bensin [1].
Bioetanol (C2H5OH) adalah cairan biokimia yang merupakan produk hasil
proses fermentasi gula dari karbohidrat dengan bantuan mikroorganisme [4] dan memiliki sifat seperti minyak premium [1]. Bioetanol menjadi perhatian dunia dewasa ini karena potensinya yang besar sebagai alternatif bahan bakar terbarukan untuk mengantikan bahan bakar fosil [5], memiliki manfaat besar dalam bidang ekonomi, ramah lingkungan [1], dan merupakan teknologi biofuel yang paling efisien untuk menurunkan emisi gas rumah kaca secara signifikan [5].
memulai proses fermentasi sehingga dapat mempersingkat tahapan produksi etanol [11]. Hal ini berbeda jika bahan baku berasal dari pati dan selulosa, dimana
pati harus melalui proses hidrolisis untuk masuk ke tahapan fermentasi gula sedangkan selulosa harus dikonversi terlebih dahulu untuk mendapatkan gula dengan bantuan mineral asam [12].
Aren (Arenga pinnata Merr) merupakan tanaman dengan produk utamanya adalah nira aren [13]. Produksi nira aren dapat mencapai 10-12 liter nira/pohon/hari [14] dengan kandungan total gula dalam nira aren berkisar 6-16 % sehingga sangat berpotensi untuk dijadikan sumber bahan baku dalam pembuatan etanol [11]. Selain itu tanamen aren mudah untuk dibudidayakan karena daya adaptasinya yang tinggi terhadap berbagai kondisi lahan termasuk lahan kritis dan kondisi agroklimat serta dapat berperan sebagai tanaman konservasi tanah dan air [15]. Oleh karena itu, produktivitas bioetanol yang dapat dihasilkan oleh tanaman aren mencapai 20.160 liter/ha/tahun dan angka ini sangat tinggi dibandingkan sumber bahan baku lainnya seperti ubi kayu, tebu, sagu dan gandum manis [16].
Beberapa penelitian yang telah dilakukan tentang pembuatan bietanol dari bahan baku dan penggunaan mikroorganisme Saccharomyces cerevisiae dapat dilihat pada table 1.1.
Metode fermentasi dengan bantuan mikroba adalah metode yang paling umum digunakan untuk proses pembuatan bietanol dari biomassa [17]. Pembuatan
bioetanol dengan proses fermentasi dapat dilakukan hanya dengan bahan baku yang mengandung gula [18]. Beberapa penelitian menggunakan beberapa jenis mikroorganisme untuk memproduksi bioetanol, seperti E. mundtii QU 25 NITE BP-965 [19], Saccharomyces cerevisiae Y-2034 dan Pachysolan tannophilus Y-2460 [20] dan Saccharomyces cerevisiae sebagai biokatalis tunggal [21].
Saccharomyces cerevisiae digunakan untuk memecah glukosa dalam proses fermentasi [22] untuk menghasilkan kadar etanol yang tinggi [23].
Tabel 1.1 Penelitian yang Telah Dilakukan Tentang Pembuatan Bioetanol dari Berbagai Bahan Baku dan Penggunaan Mikroorganisme
Saccharomyces cerevisiae
No Nama Tahun Judul Penelitian Katalis Variabel Hasil
1 Fahrizal et al 2013
The Effect of Temperature and Length of Fermentation on
Bioethanol Production from Arenga Plant (Arenga pinnata MERR)
-
Variabel tetap : Tanpa penambahan nutrisi
Variabel berubah : waktu fermentasi (72, 96, 120, 144, 168) jam, temperatur (27
o
Fresh Oil Palm Frond Juice as a Renewable, Food, Non-Cellulosic and Complete Medium For Direct Bioethanol Production
Saccharom yces cerevisiae
Variabel tetap : kecepatan pengadukan 150 rpm, suhu 30 oC
Variabel berubah : bahan baku (OPF, sugarcane), waktu (24, 48)
Yield bioetanol:
Influence of Nutrient Addition on The Bioethanol Yield From Oil Palm Trunk Sap Fermented by
Saccharomyces cerevisiae
Saccharom yces cerevisiae
Variabel tetap : suhu reaksi 32 oC, kecepatan pengadukan 170 rpm, pH 6, jumlah penambahan nutrisi 0,2% berat
Tabel 1.1 Penelitian yang Telah Dilakukan Tentang Pembuatan Bioetanol dari Berbagai Bahan Baku dan Penggunaan Mikroorganisme
Saccharomyces cerevisiae (Lanjutan)
No Nama Tahun Judul Penelitian Katalis Variabel Hasil
4 Kismurtono 2012
Fed Batch Alcoholic Fermentation of Palm Juice (Arenga pinnata Merr) : Influence of The Feeding Rate on Yeast, Yield and Productivity
Saccharomy ces
cerevisiae
Variabel tetap : waktu fermentasi 24 jam
Variabel berubah : proses treatment (p1,p2,p3,p4)
Bioethanol Production From Thick Juice as Intermediate of Sugar Beet Processing
Saccharomy ces
cerevisiae
Variabel tetap : waktu reaksi 72 jam, kecepatan pengadukan 200 rpm, suhu 30
o
C
Variabel berubah: konsentrasi total gula (5,10,15,20,25% w/w)
Production of Bioethanol and Associated by-Products From Potato Starch Residue Stream by
1.2PERUMUSAN MASALAH
Adapun perumusan masalah dalam penelitian ini adalah bagaimana pengaruh
suhu dan volume starter terhadap kadar dan yield bioetanol yang dihasilkan dalam proses fermentasi nira aren (Arenga pinnata Merr).
1.3TUJUAN PENELITIAN
Penelitian ini bertujuan untuk:
1. Mempelajari hubungan suhu dan volume starter terhadap kadar bioetanol hasil proses fermentasi nira aren.
2. Mempelajari hubungan suhu dan volume starter terhadap yield bioetanol hasil proses fermentasi nira aren.
1.4 MANFAAT PENELITIAN
Manfaat dari penelitian yang dilakukan adalah :
1. Memberikan informasi mengenai pengaruh suhu dan volume starter pada proses fermentasi nira aren.
2. Mendapatkan data percobaan yang diperlukan untuk merancang dan membangun unit pembuatan bioetanol dari nira aren untuk skala yang lebih besar (scale up).
3. Memberikan informasi kepada masyarakat tentang bagaimana kualitas bioetanol yang dihasilkan dari proses fermentasi nira aren sekaligus meningkatkan nilai ekonomis dari nira aren tersebut.
1.5 RUANG LINGKUP PENELITIAN
Penelitian ini dilakukan di Laboratorium Mikrobiologi Teknik Departemen Teknik Kimia, Fakultas Teknik Universitas Sumatera Utara, Jl. Almamater USU Medan, Indonesia.
Variabel-variabel yang dilakukan dalam penelitian ini adalah : Variabel tetap :
1. Waktu fermentasi = 24 jam [21]
2. Nutrisi = NPK 0,4% (m/m) [21]
Variabel berubah :
1. Suhu = 32 oC [10]
35 oC 39 oC
2. Volume Starter = 15%
25% [21]
35% 45% 55%
Adapun analisis yang akan dilakukan di dalam penelitian ini adalah analisis
Fourier Transform Infra Red (FTIR), oksidasi dengan kalium dikromat (K2Cr2O7), pengukuran volume bioetanol, perhitungan densitas, kadar bioetanol,
ABSTRAK
Penelitian ini bertujuan untuk mengetahui pengaruh suhu dan volume starter terhadap kadar dan yield bioetanol yang dihasilkan dari nira Aren (Arenga pinnata
Merr). Biokatalis yang digunakan adalah Saccharomyces cerevisiae. Variabel-variabel yang diamati antara lain suhu dan volume starter pada proses fermentasi secara anaerobik. Penelitian ini diawali dengan persiapan pembuatan starter kemudian dilanjutkan dengan proses fermentasi. Hasil fermentasi kemudian didistilasi pada temperatur 85 oC. Hasil penelitian menunjukkan bahwa pada suhu rendah dengan penambahan volume starter maka kadar dan yield etanol yang dihasilkan akan semakin tinggi hingga mencapai titik maksimum, yang diperoleh pada suhu 32 oC dan volume starter 35% sebesar 43,3165 % (v/v) dan 38,1430 %. Jika melebihi titik tersebut maka perubahan suhu dan penambahan volume starter akan menurunkan kadar dan yield etanol yang dihasilkan.
ABSTRACT
This research studies about determine the effect of temperature and volume of starter on yield and concentration of bioethanol produced from nira Aren (Arenga pinnata Merr). Biocatalyst used was Saccharomyces cerevisiae. The experimental variables were temperature and volume of starter doing anaerobic fermentation process. The experiment started with preparation of a starter followed by fermentation process. The product obtained from distillation process at temperature of 85 ° C. It can be conclude that high ethanol yield and concentration obtained at low temperature with the addition of the starter, it will produce the higher content and yield of ethanol until it reaches the maximum point, obtained on the condition at a temperature of 32 ° C and 35% starter amounted to 43.3165% (v / v) and 38.1430%. If it exceed that point, the changes of temperature and the addition of starter will decrease the concentration and yield of ethanol produced.
PENGARUH SUHU DAN VOLUME STARTER
DALAM PEMBUATAN BIOETANOL DARI
NIRA AREN (ARENGA PINNATA MERR)
SKRIPSI
Oleh
GUSTI HANDAYANI
110405007
DEPARTEMEN TEKNIK KIMIA
FAKULTAS TEKNIK
PENGARUH SUHU DAN VOLUME STARTER
DALAM PEMBUATAN BIOETANOL DARI
NIRA AREN (ARENGA PINNATA MERR)
SKRIPSI
Oleh
GUSTI HANDAYANI
110405007
SKRIPSI INI DIAJUKAN UNTUK MELENGKAPI SEBAGIAN
PERSYARATAN MENJADI SARJANA TEKNIK
DEPARTEMEN TEKNIK KIMIA
FAKULTAS TEKNIK
PRAKATA
Puji dan syukur penulis panjatkan kepada Tuhan Yang Maha Esa atas berkat dan karunia-Nya sehingga skripsi ini dapat diselesaikan. Tulisan ini merupakan
Skripsi dengan judul “Pengaruh Suhu dan Volume Starter Dalam Pembuatan Bioetanol Dari Nira Aren (Arenga Pinnata Merr)”, berdasarkan hasil penelitian yang penulis lakukan di Departemen Teknik Kimia Fakultas Teknik Universitas Sumatera Utara. Skripsi ini merupakan salah satu syarat untuk mendapatkan gelar sarjana teknik.
Hasil penelitian ini ditujukan untuk memanfaatkan nira segar untuk menghasilkan bioetanol melalui proses fermentasi. Tujuannya adalah untuk meningkatkan nilai ekonomi dari nira aren yang berpotensi untuk dijadikan bahan bakar nabati karena
memiliki kandungan gula yang tinggi. Oleh karena itu, penulis berpikir untuk melakukan penelitian ini untuk dapat menghasilkan yield etanol terbaik dengan kondisi yang berbeda.
Selama melakukan penelitian sampai penulisan skripsi ini penulis banyak mendapatkan bantuan dari berbagai pihak, untuk itu penulis mengucapkan terima kasih dan penghargaan sebesar-besarnya kepada:
1. Ir. Netti Herlina, M.T. selaku Dosen Pembimbing yang telah membimbing penulis dari penentuan judul, penelitian dan penyusunan laporan.
2. Ir. Renita Manurung, M.Sc. selaku Koordinator Penelitian dan Skripsi. 3. Dr. Eng. Irvan, M.Si. sebagai Ketua Departemen Teknik Kimia USU. 4. Dr. Ir. Fatimah, MT selaku Sekretaris Departemen Teknik Kimia USU. 5. Dr. Ir. Iriany, M.Si. selaku Dosen Penguji I.
6. Dr. Maya Sarah, S.T.,M.T. selaku dosen penguji II.
7. Seluruh staf Dosen Teknik Kimia USU, yang telah mendidik dan membagikan ilmu kepada penulis.
9. Rekan mahasiswa Teknik Kimia USU, terutama kepada seluruh angkatan 2011 yang telah membantu dan mendukung penulis hingga menyelesaikan
skripsi ini.
Penulis menyadari bahwa skripsi ini masih jauh dari sempurna oleh karena itu penulis mengharapkan saran dan masukan demi kesempurnaan skripsi ini. Semoga skripsi ini memberikan manfaat bagi pengembangan ilmu pengetahuan.
Medan, 2016
Penulis
DEDIKASI
Penulis mendedikasikan skripsi ini kepada kedua orang tua penulis.
Abdul Luis Yusnani
RIWAYAT HIDUP PENULIS
Nama: Gusti Handayani NIM: 110405007
Tempat/Tgl. Lahir: Tg. Balai Karimun, 12 Agustus 1992 Nama orang tua: Abdul Luis
Alamat orang tua:
Padang Pariaman, Sumatera Barat
Asal Sekolah
SD Negeri 001 Batam, tahun 1999-2005
SMP Negeri 3 Batam, tahun 2005-2008
SMA Negeri 1 Batam, tahun 2008-2011
Pengalaman Organisasi/ Kerja:
1. Pengurus Himpunan Mahasiswa Teknik Kimia (HIMATEK) periode 2014-2015
2. Pengurus Covalen Study Group (CSG) periode 2013-2014
3. Kerja Praktek di PT Ecogreen Oleochemicals Batam Tahun 2014
Artikel yang telah dipublikasikan dalam Jurnal/Pertemuan Ilmiah:
1. Jurnal Teknik Kimia (Pengaruh Suhu dan Volume Starter dalam Pembuatan Bioetanol
dari Nira Aren (Arenga Pinnata Merr) Beasiswa yang Diperoleh:
1. PPA 2011/2012
2. Beasiswa KEPRI 2012/1013
ABSTRAK
Penelitian ini bertujuan untuk mengetahui pengaruh suhu dan volume starter terhadap kadar dan yield bioetanol yang dihasilkan dari nira Aren (Arenga pinnata
Merr). Biokatalis yang digunakan adalah Saccharomyces cerevisiae. Variabel-variabel yang diamati antara lain suhu dan volume starter pada proses fermentasi secara anaerobik. Penelitian ini diawali dengan persiapan pembuatan starter kemudian dilanjutkan dengan proses fermentasi. Hasil fermentasi kemudian didistilasi pada temperatur 85 oC. Hasil penelitian menunjukkan bahwa pada suhu rendah dengan penambahan volume starter maka kadar dan yield etanol yang dihasilkan akan semakin tinggi hingga mencapai titik maksimum, yang diperoleh pada suhu 32 oC dan volume starter 35% sebesar 43,3165 % (v/v) dan 38,1430 %. Jika melebihi titik tersebut maka perubahan suhu dan penambahan volume starter akan menurunkan kadar dan yield etanol yang dihasilkan.
ABSTRACT
This research studies about determine the effect of temperature and volume of starter on yield and concentration of bioethanol produced from nira Aren (Arenga pinnata Merr). Biocatalyst used was Saccharomyces cerevisiae. The experimental variables were temperature and volume of starter doing anaerobic fermentation process. The experiment started with preparation of a starter followed by fermentation process. The product obtained from distillation process at temperature of 85 ° C. It can be conclude that high ethanol yield and concentration obtained at low temperature with the addition of the starter, it will produce the higher content and yield of ethanol until it reaches the maximum point, obtained on the condition at a temperature of 32 ° C and 35% starter amounted to 43.3165% (v / v) and 38.1430%. If it exceed that point, the changes of temperature and the addition of starter will decrease the concentration and yield of ethanol produced.
DAFTAR ISI
DAFTAR GAMBAR xii
DAFTAR TABEL
1.2PERUMUSAN MASALAH 5
1.3TUJUAN PENELITIAN 5
1.4MANFAAT PENELITIAN 5
1.5RUANG LINGKUP PENELITIAN 5
BAB II TINJAUAN PUSTAKA 7
2.1BIOETANOL 7
2.2NIRA AREN 8
2.3FERMENTASI 9
2.4SACCHAROMYCES CEREVISIAE 10 2.5PUPUK MAJEMUK (NPK)
2.6POTENSI EKONOMI BIOETANOL DARI NIRA AREN
10 11
BAB III METODOLOGI PENELITIAN 13
3.1LOKASI PENELITIAN 13
3.2BAHAN DAN PERALATAN 13
3.2.2Peralatan 13
3.3PROSEDUR PENELITIAN 14
3.3.1Prosedur Pembuatan Starter 14
3.3.2Prosedur Fermentasi 3.3.3Prosedur Analisis
3.3.3.1 Analisis Kadar Gula Nira Segar Dengan Refraktometer
3.3.3.2 Analisis Densitas
3.3.3.3 Analisis Spesific Gravity dan API Gravity 3.3.3.4 Analisis Nilai Kalor
3.3.3.5 Analisis Kadar Bioetanol dengan Metode Densitas 3.3.3.6 Analisis Oksidasi K2Cr2O7 Terhadap Bioetanol
14
3.4FLOWCHART PENELITIAN 18
3.4.1Flowchart Pembuatan Starter 3.4.2Flowchart Fermentasi
BAB IV HASIL DAN PEMBAHASAN
4.1HASIL ANALISIS KADAR GULA NIRA AREN
4.2KARAKTERISASI FTIR (FOURIER TRANSFORM INFRA RED) ETANOL
4.3HASIL ANALISIS ETANOL DENGAN REAKSI OKSIDASI
KALIUM DIKROMAT (K2Cr2O7)
4.4PENGARUH SUHU DAN VOLUME STARTER TERHADAP KADAR ETANOL
4.5PENGARUH SUHU DAN VOLUME STARTER TERHADAP
YIELD ETANOL
4.6PERBANDINGAN STANDAR BAKU MUTU BIOETANOL BAB V KESIMPULAN DAN SARAN
5.1KESIMPULAN
DAFTAR GAMBAR
Halaman Gambar 3.1 Flowchart Pembuatan Starter
Gambar 3.2 Flowchart Proses Fermentasi
Gambar 4.1 Spektrum FTIR(Fourier Transform Infra Red) Etanol Dari Nira Aren
Gambar 4.2 Perubahan Warna Pada Oksidasi Etanol Dengan K2Cr2O7
Gambar 4.3 Grafik Pengaruh Suhu dan Volume Starter Terhadap Kadar Etanol
Gambar 4.4 Grafik Pengaruh Suhu dan Volume Starter Terhadap Yield Etanol
Gambar L3.1 Nira Segar
Gambar L3.2 Hasil Pembacaan Refraktometer untuk Kadar Gula
Nira Segar
Gambar L3.3 Proses Fermentasi a. Saccharomyces cerevisiae b.Starter c. Hasil Fermentasi
Gambar L3.4 Proses Distilasi
Gambar L3.5 Foto Analisis Oksidasi K2Cr2O7 Terhadap Bioetanol
a. Kalium Dikromat b. Kalium Dikromat + Etanol
18 19
20
21
22
24
40
40
41 41
DAFTAR TABEL
Halaman Tabel 1.1 Penelitian yang Telah Dilakukan Tentang Pembuatan
Bioetanol dari Berbagai Bahan Baku dan Penggunaan Mikroorganisme Saccharomyces cerevisiae
Tabel 2.1 Sifat Fisika dan Sifat Kimia Etanol Tabel 3.1 Konversi Berat Jenis - Kadar Etanol Tabel 4.1 Standar Etanol Nabati
Tabel 4.2 Syarat Mutu Bioetanol Bahan Bakar Tabel L1.1 Hasil Analisis Perolehan Bioetanol
DAFTAR LAMPIRAN
Halaman Lampiran 1 Data Percobaan
Lampiran 2 Contoh Perhitungan 2.1 Densitas Bioetanol
2.2 Kadar Bioetanol Berdasarkan Densitas 2.3 Yield Bioetanol
2.4 Specific Gravity dan API Gravity Bioetanol 2.5 Nilai Kalor Bioetanol
2.6 Analisis Ekonomi Lampiran 3 Dokumentasi Penelitian
3.1 Foto Bahan Baku Nira Segar
3.2 Foto Analisis Kadar Gula Nira Segar Dengan Refraktometer
3.3 Foto Proses Fermentasi 3.4 Foto Proses Distilasi
3.5 Foto Analisis Oksidasi K2Cr2O7 Terhadap Bioetanol
35 36 36 36 37 37 38 38 40 40
40
DAFTAR SINGKATAN
API American Petroleum Institute
FTIR Fourier Transform Infra Red
GC Gas Chromatography
HPLC High Performance Liquid Chromatography
NK Nilai Kalor
NPK Nitrogen Posfor Kalium


![Tabel 3.1 Konversi Berat Jenis - Kadar Etanol [56]](https://thumb-ap.123doks.com/thumbv2/123dok/877708.594836/19.595.147.516.610.750/tabel-konversi-berat-jenis-kadar-etanol.webp)