TESIS
PEMBUATAN DAN EVALUASI SEDIAAN
GASTRORETENTIF ANTASIDA DARI FILM ALGINAT
KITOSAN
Oleh:
MARIADI
NIM 117014012
PROGRAM STUDI MAGISTER FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PEMBUATAN DAN EVALUASI SEDIAAN
GASTRORETENTIF ANTASIDA DARI FILM
ALGINAT-KITOSAN
TESIS
Diajukan sebagai salah satu syarat untuk memperoleh gelar Magister Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
Oleh:
MARIADI
NIM 117014012
PROGRAM STUDI MAGISTER FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
LEMBAR PERSETUJUAN TESIS
PEMBUATAN DAN EVALUASI SEDIAAN
GASTRORETENTIF ANTASIDA DARI FILM
ALGINAT-KITOSAN
Oleh: MARIADI NIM 117014012
Medan, Agustus 2014 Menyetujui:
Komisi Pembimbing, Komisi Penguji,
Prof. Dr. Karsono, Apt. Prof. Dr. Urip Harahap, Apt. NIP 195409091982011001 NIP 195301011983031004
Prof. Dr. Hakim Bangun, Apt. Dr. Kasmirul Ramlan Sinaga, M.S., Apt. NIP 195201171980031002 NIP 195504241983031003
Prof. Dr. Karsono, Apt. NIP 195409091982011001
Prof. Dr. Hakim Bangun, Apt. NIP 195201171980031002
Mengetahui: Disahkan Oleh:
Ketua Program Studi, Dekan,
PENGESAHAN TESIS
Nama Mahasiswa : Mariadi Nomor Induk Mahasiswa : 117014012
Program Studi : Magister Farmasi
Judul Tesis : Pembuatan Dan Evaluasi Sediaan Gastroretentif Antasida Dari Film Alginat-Kitosan
Telah diuji dan dinyatakan LULUS di depan Tim Penguji pada hari Rabu tanggal dua puluh tujuh bulan Agustus tahun dua ribu empat belas.
Mengesahkan :
Tim Penguji Tesis
Ketua Tim Penguji Tesis : Prof. Dr. Karsono, Apt.
Anggota Tim Penguji Tesis : Prof. Dr. Hakim Bangun, Apt.
: Prof. Dr. Urip Harahap, Apt.
SURAT PERNYATAAN
Saya yang bertanda tangan dibawah ini:
Nama Mahasiswa : Mariadi
Nomor Induk Mahasiswa : 117014012
Program Studi : Magister Farmasi
Judul Tesis : Pembuatan dan Evaluasi Sediaan Gastroretentif Antasida dari Film Alginat-Kitosan
Dengan ini menyatakan bahwa tesis yang saya buat adalah asli karya saya sendiri, bukan plagiat dan apabila dikemudian hari diketahui tesis saya tersebut plagiat karena kesalahan saya sendiri maka saya bersedia diberi sanksi apapun oleh Program Studi Magister Farmasi Fakultas Farmasi USU. Saya tidak akan menuntut pihak manapun atas perbuatan saya tersebut.
Demikianlah surat pernyataan ini saya perbuat dengan sebenarnya dan dalam keadaan sehat.
Medan, Agustus 2014
Yang membuat pernyataan,
Mariadi
KATA PENGANTAR
Puji dan syukur kepada Allah SWT atas segala nikmat yang tak terhingga sehingga penulis bisa menyelesaikan penelitian dan penulisan tesis dengan judul Pembuatan dan Evaluasi Sediaan Gastroretentif Antasida dari Film Alginat-Kitosan, sebagai salah satu syarat untuk mencapai gelar Magister Farmasi pada Fakultas Farmasi Universitas Sumatera Utara. Selama menyelesaikan penelitian dan tesis ini penulis telah banyak mendapatkan bantuan dan dorongan dari berbagai pihak, baik moril maupun materil. Untuk itu penulis ingin menghaturkan penghargaan dan terimakasih yang tiada terhingga kepada:
1. Rektor Universitas Sumatera Utara, Bapak Prof. Dr. dr. Syahril Pasaribu, DTMH&H., M.Sc., (CTM)., Sp.A(K).
2. Dekan Fakultas Farmasi Universitas Sumatera Utara, Bapak Prof. Dr. Sumadio Hadisahputra, Apt., yang telah menyediakan fasilitas dan kesempatan bagi penulis menjadi mahasiswa Program Studi Magister Farmasi Fakultas Farmasi.
3. Ketua Program Studi Magister Farmasi Fakultas Farmasi Universitas Sumatera Utara, Bapak Prof. Dr. Karsono, Apt., yang telah menyediakan fasilitas bagi penulis selama menjadi mahasiswa Program Studi Magister Farmasi Fakultas Farmasi.
4. Bapak Prof. Dr. Karsono, Apt., dan Bapak Prof. Dr. Hakim Bangun, Apt., selaku Pembimbing yang tiada hentinya membimbing, mengarahkan, memberikan dorongan dan semangat dengan penuh kesabaran sehingga penulis terpacu untuk menyelesaikan penelitian dan penyelesaian tesis ini.
5. Bapak Prof. Dr. Hakim Bangun, Apt., sebagai Ketua Peneliti Hibah Pasca Sarjana yang mendapatkan dana untuk penelitian ini yang berasal dari DIPA Universitas Sumatera Utara tahun 2014.
7. Bapak Drs. David Sinurat, M.Si., Apt., Kepala Laboratorium Farmasi Fisik beserta staf.
8. Bapak Prof. Dr. rer.nat. Effendi De Lux Putra, S.U., Apt., Koordinator Laboratorium Penelitian Fakultas Farmasi USU beserta staf.
9. Bapak Dr. Darwin Yunus, M.S., Kepala Laboratorium Terpadu Universitas Sumatera Utara beserta staf.
Penulis juga mengucapkan terima kasih dan penghargaan yang tiada hentinya kepada istri tercinta Nurhidayah, Ayahanda Ali Akbar dan Ibunda Erniati, serta Bapak mertua M. Usman dan Ibunda Marimar, yang tiada hentinya berkorban dengan tulus ikhlas dan memberi dukungan dan motivasi bagi kesuksesan penulis, serta kepada saudaraku Marli Effendi, Mardison, Sofyan Sofany, Syafrianto dan Siti Nazly. Serta kepada teman-teman seperjuangan yang sudah banyak membantu Vonna, Denny, Fitri, Heny, Yade, Erik, Ali, Fredy, Putri, Lasni, kak Ade, dan buat semua pihak yang tidak dapat penulis sebutkan satu per satu yang telah banyak membantu dalam penelitian tesis ini. Kiranya Allah SWT memberikan balasan yang berlipat ganda atas kebaikan dan bantuan yang telah diberikan kepada penulis.
Penulis menyadari bahwa tesis ini masih jauh dari kesempurnaan, sehingga penulis mengharapkan kritik dan saran yang bersifat membangun. Akhir kata semoga tulisan ini dapat menjadi sumbangan yang berarti bagi ilmu pengetahuan khususnya bidang farmasi.
Medan, Agustus 2014 Penulis,
PEMBUATAN DAN EVALUASI SEDIAAN GASTRORETENTIF ANTASIDA DARI FILM ALGINAT-KITOSAN
ABSTRAK
Sediaan antasida konvensional memiliki durasi kerja yang singkat sekitar 2-3 jam karena proses pengosongan lambung. Bentuk sediaan gastroretentif antasida diperlukan karena penyembuhan penyakit asam lambung terjadi bila selama 24 jam pH rata-rata dijaga di atas 3 – 4.
Tujuan dari penelitian ini adalah untuk membuat suatu formula gastroretentif antasida menggunakan basis film alginat-kitosan yang mampu menetralisir asam lambung untuk waktu yang lebih lama.
Sediaan film gastroretentif antasida dibuat menggunakan alginat, kitosan dan gliserin dalam rasio yang berbeda-beda. Campuran dari alginat, kitosan dan gliserin yang mengandung antasida diratakan di atas objek gelas (2 cm x 5 cm) dan dikeringkan pada temperatur ruangan. Sifat pembentangan (unfolding) dan keutuhan (integrity) dari film di evaluasi menggunakan alat disolusi USP. Profil netralisasi ditentukan melalui simulasi sekresi asam lambung. Simulasi dilakukan dengan meneteskan 10 ml/jam larutan HCl 0,1 N ke dalam 30 ml larutan HCl 0,1 N yang mengandung film antasida. Sifat mukoadhesif diuji menggunakan mukosa lambung tikus dengan tensiometer DuNoy, dan sifat pengembangan dalam larutan HCl 0,1 N ditentukan berdasarkan pertambahan luas dan berat film.
Hasil menunjukkan bahwa film yang mengandung 1,5 g larutan alginat 4%; 2 g larutan kitosan 4%; 4 tetes gliserin; dan 300 mg serbuk Al(OH)3 memberikan karakteristik yang baik sebagai sistem penyampaian obat gastroretentif. Waktu pembentangan film adalah 5 - 10 menit, film masih tetap utuh selama 7 jam. Pada simulasi sekresi asam lambung, mempertahankan pH pada pH 3 - 3,5 sekitar 6 jam. Nilai mukoadhesif dari film adalah 107,47 ± 7,38 dyne/cm dan index swelling
Hasil penelitian menunjukkan bahwa film alginat-kitosan adalah potensial untuk diaplikasikan sebagai suatu
adalah 111,30 %.
sistem penyampaian obat gastroretentif antasida.
FORMULATION AND EVALUATION OF
GASTRORETENTIVE ANTACID
ALGINATE-CHITOSAN FILM
USING
ABSTRACT
The conventional antacid dosage forms have a short duration of action for about 2-3 hours due to gastric emptying process. A gastroretentive dosage form of antacid is needed since the healing of gastric ulcers occurs when gastric pH is kept above 3 - 4 during 24 hours.
The aim of this study was to formulate a gastroretentive film of antacid using alginate-chitosan based which is able to neutralize gastric acid for longer time.
The gastroretentive films of antacid were prepared using alginate, chitosan and glycerin in various ratio. The mixtures of alginate, chitosan and glycerin containing antacid were then flattened on a glass object (2 cm x 5 cm) and allowed to dry at room temperature. Unfolding and integrity behaviors of the films were evaluated using the USP dissolution tester. Neutralization profile was determined by simulating gastric acid secretion. The simulation was carried out by droping 10 ml/h of 0.1 N HCl solution to 30 ml of 0.1 N HCl solution containing film of antacid. Mucoadhesive property was tested using rats stomach by DuNoy tensiometer, and swelling properties in 0.1 HCl solution was determined based on the increase of film size.
The results showed that film containing 1.5 g of 4% alginate solution, 2 g of 4% chitosan solution, 4 drops of glycerin and 300 mg of Al(OH)3
The result indicates that alginate-chitosan film is potential to apply as a gastroretentive drug delivery system of antacid.
gave good characteristics as a gastroretentive drug delivery system. The unfolding time of the film was 5 - 10 minutes, the film was intact for about 7 hours. On simulating gastric acid secretion, the maintenence pH was found at pH 3 - 3.5 was about 6 hours. The mucoadhesive value of the film was 107.47 ± 7.38 dyne/cm and the swelling index was 111.30%.
DAFTAR ISI
Halaman
JUDUL ... i
LEMBAR PENGESAHAN ... iii
PENGESAHAN TESIS ... iv
SURAT PERNYATAAN ... v
KATA PENGANTAR ... vi
ABSTRAK ... ix
ABSTRACT ... x
DAFTAR ISI ... xi
DAFTAR GAMBAR ... xiii
DAFTAR LAMPIRAN ... xv
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 7
1.3 Hipotesis ... 8
1.4 Tujuan Penelitian ... 8
1.5 Manfaat Penelitian ... 9
1.6 Kerangka Pikir Penelitian ... 10
BAB II TINJAUAN PUSTAKA ... 11
2.1 Ulkus ... 11
2.2 Antasida ... 15
2.3 Gastroretentive Drugs Delivery System (GDDS) ... 17
2.5 Kitosan ... 25
2.6 Interaksi antara alginat dengan kitosan ... 26
BAB III METODE PENELITIAN ... 27
3.1 Alat dan Bahan ... 27
3.2 Pembuatan Pereaksi ... 28
3.3 Pembuatan Sediaan Film Alginat-Kitosan ... 28
3.4 Uji Variasi Ketebelan dan Berat Film ... 29
3.5 Uji Sifat Pembentangan (Unfolding behaviour) in vitro ... 29
3.6 Uji Integritas (keutuhan) Sediaan Film ... 30
3.7 Penentuan Profil Netralisasi HCl 0,1 N oleh Sediaan Film Alginat-Kitosan Secara in vitro ... 31
3.8 Uji pelepasan Ion Aluminium secara in vitro ... 32
3.9 Uji Sifat Pengembangan ... 37
3.10 Uji Bioadhesif secara in vitro ... 37
3.11 Scanning Electron Microscopy (SEM) ... 39
BAB IV HASIL DAN PEMBAHASAN ... 40
4.1 Sediaan Film Alginat-Kitosan ... 40
4.2 Sifat Pembentangan film (Unfolding behaviour) ... 43
4.3 Keutuhan film (Integrity properties) ... 47
4.4 Profil Netralisasi secara in vitro ... 49
4.6 Sifat Bioadhesif secara in vitro ... 65
4.7 Pelepasan Ion Aluminium ... 66
4.8 Scanning Electron Microscopy (SEM) ... 69
BAB V KESIMPULAN DAN SARAN ... 72
DAFTAR GAMBAR
Halaman
Gambar 1.1 Diagram kerangka pikir penelitian ... 10
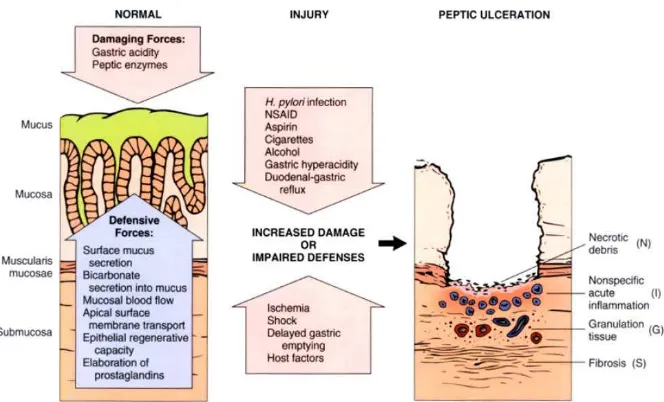
Gambar 2.1.Faktor-faktor penyebab ulkus ... 14
Gambar 2.2 GDDS dengan sistem pengembangan dan pembesaran ... 19
Gambar 2.3 GDDS dengan sistem bio/muko-adhesif ... 20
Gambar 2.4 GDDS dengan sistem floating ... 21
Gambar 2.5 GDDS dengan sistem berdensitas tinggi (High Density Systems) ... 22
Gambar 2. 6 Struktur Kimia Alginat ... 25
Gambar 2.7 Struktur Kimia Kitosan ... 26
Gambar 2. 8 Reaksi antara Alginat dan Kitosan ... 26
Gambar 3.1 Ilustrasi sediaan gastrorentif antasida film alginat-kitosan ... 30
Gambar 3.2 Netralisasi Asam ... 32
Bagan Rancangan Alat untuk Menentukan Profil Gambar 3.3 Bagan Rancangan Alat Uji Bioadhesif dengan Modivikasi Tensiometer ... 38
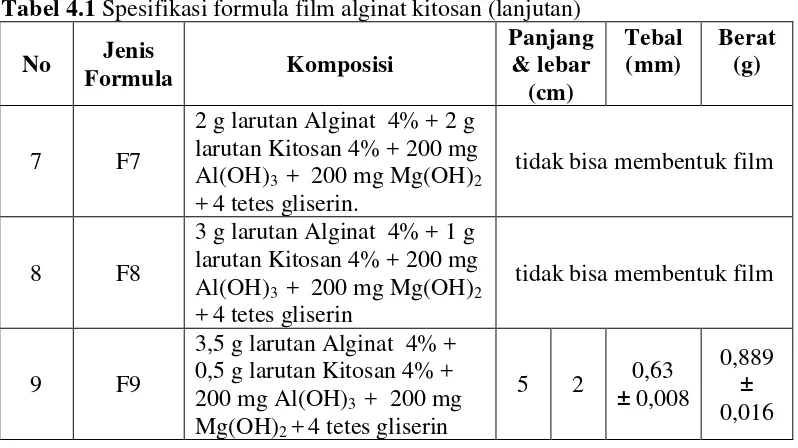
Gambar 4.1 Sediaan F4, F7, dan F8 yang tidak bisa membentuk film ... 41
Gambar 4.2 Sediaan F1, F2, F3, F5, F6 dan F9 yang bisa membentuk Film ... 42
Gambar 4.4 Sediaan film alginat yang mengandung antasida
(tidak bisa membentang) dalam medium asam ... 46 Gambar 4.5 Integritas/keutuhan sediaan film F6 ... 48 Gambar 4.6 Grafik Profil perubahan pH air versus waktuoleh
serbuk Al(OH)3, Mg(OH)2 Al(OH)
dan kombinasi
3 dan Mg(OH)2 ... 50 Gambar 4.7Grafik Profil serbuk Al(OH)3, Mg(OH)2
Al(OH)
, dan Kombinasi
3 dan Mg(OH)2 dalam 30 ml HCl 0,1 N ... 51 Gambar 4.8Profil netralisasi HCl 0,1 N oleh serbuk Al(OH)3
Mg(OH)
, 2 dan kombinasi Al(OH)3 dan Mg(OH)2
dalam simulasi sekresi asam lambung ... 53 Gambar 4.9 Grafik profil netralisasi HCl 0,1 N oleh sediaan film dalam
simulasi sekresi asam(penambahan HCl 0,1 N 10 ml/jam) ... 56 Gambar 4.10 Profil Netralisasi HCl 0,1 N oleh Sediaan F6
dalam simulasi sekresi asam lambung
berbanding serbuk antasida ... 59 Gambar 4.11Grafik profil netralisasi sediaan F6 dalam berbagai
Pendekatan ... 61 Gambar 4.12Grafik daya pengembangan sediaan film (A) Pendekatan
luas, dan (B) pendekatan berat ... 63 Gambar 4.13 Contoh daya pengembangan sediaan film alginat kitosan ... 64 Gambar 4.14 Grafik kurva kalibrasi aluminium ... 66 Gambar 4.15 Kurva % kumulatif pelepasan aluminium sediaan F6
(A)dan profil netralisasi sediaan F6 (B) ... 68
Gambar 4.16 Ilustrasi pelepasan ion aluminium melalui reaksi
DAFTAR LAMPIRAN
Halaman
Lampiran1. Perhitungan Laju Infus HCl 0,1 N pada Penentuan Profil
Netralisasi dalam Simulasi Sekresi Asam ... 77
Lampiran 2. Data Spesifikasi film alginat kitosan yang mengandung Al(OH)3, Mg(OH)2 dan kombinasi Al(OH)3 dan Mg(OH)2 ... 78
Lampiran 3. Data Sifat Pembentangan (Unfolding behaviour) ... 81
Lampiran 4. Data Sifat Integritas film ... 83
Lampiran 5. Data Hasil Pengukuran Profil Netralisasi Serbuk Al(OH)3, Mg(OH)2 dan kombinasi Al(OH)3 dan Mg(OH) dalam 30 ml Air ... 84
2 Lampiran 6. Data Pengukuran Profil Netralisasi 30 ml HCl 0,1 N oleh Serbuk Al(OH)3, Mg(OH)2 kombinasi Al(OH) dan 3 dan Mg(OH)2 ... 85
Lampiran 7. Data Hasil Pengukuran Profil Netralisasi HCl 0,1 N oleh Serbuk Al(OH)3, Mg(OH)2 dan kombinasi Al(OH) dan Mg(OH) 3 2 dalam Simulasi Sekresi Asam Lambung ... 86
Lampiran 8. Data Hasil Pengukuran Profil Netralisasi HCl 0,1 N oleh Sediaan Film dalam Simulasi Sekresi Asam Lambung ... 88
Lampiran 9. Data Profil Netralisasi HCl 0,1 N oleh Sediaan F6 dalam Simulasi Sekresi Asam dengan tanpa akumulasi penambahan larutan HCl 0,1 N ... 90
Lampiran 10. Data Profil Netralisasi 30 ml HCl 0,1 N oleh Sediaan F6 (tanpa penambahan Infus HCl 0,1 N 10 ml/jam) ... 91
Lampiran 11. Data Pengukuran Profil Netralisasi Sediaan F6 dalam Air ... 92
Lampiran 12. Data Pengukuran Sifat Pengembangan (swelling) Sediaan Film ... 93
Lampiran 13. Data Pengukuran Sifat Bioadhesif secara in vitro ... 95
Lampiran 14. Data Pengukuran Kurva Kalibrasi Aluminium ... 96
Lampiran 15. Data Perhitungan Persamaan Regresi Aluminium ... 97
Lampiran 17. Data Pelepasan ion Alumium (Al) dari Sediaan Film ... 102 Lampiran 18. Contoh Perhitungan pelepasan logam aluminium
dalam sediaan film ... 106 Lampiran 19. Gambar Alat Spektrofotometer Serapan Atom ... 105 Lampiran 20. Gambar Rangkaian Alat Uji Profil Netralisasi ... 108
Lampiran 21. Gambar Alat Scanning Electron Microscopy (SEM) ... 109
PEMBUATAN DAN EVALUASI SEDIAAN GASTRORETENTIF ANTASIDA DARI FILM ALGINAT-KITOSAN
ABSTRAK
Sediaan antasida konvensional memiliki durasi kerja yang singkat sekitar 2-3 jam karena proses pengosongan lambung. Bentuk sediaan gastroretentif antasida diperlukan karena penyembuhan penyakit asam lambung terjadi bila selama 24 jam pH rata-rata dijaga di atas 3 – 4.
Tujuan dari penelitian ini adalah untuk membuat suatu formula gastroretentif antasida menggunakan basis film alginat-kitosan yang mampu menetralisir asam lambung untuk waktu yang lebih lama.
Sediaan film gastroretentif antasida dibuat menggunakan alginat, kitosan dan gliserin dalam rasio yang berbeda-beda. Campuran dari alginat, kitosan dan gliserin yang mengandung antasida diratakan di atas objek gelas (2 cm x 5 cm) dan dikeringkan pada temperatur ruangan. Sifat pembentangan (unfolding) dan keutuhan (integrity) dari film di evaluasi menggunakan alat disolusi USP. Profil netralisasi ditentukan melalui simulasi sekresi asam lambung. Simulasi dilakukan dengan meneteskan 10 ml/jam larutan HCl 0,1 N ke dalam 30 ml larutan HCl 0,1 N yang mengandung film antasida. Sifat mukoadhesif diuji menggunakan mukosa lambung tikus dengan tensiometer DuNoy, dan sifat pengembangan dalam larutan HCl 0,1 N ditentukan berdasarkan pertambahan luas dan berat film.
Hasil menunjukkan bahwa film yang mengandung 1,5 g larutan alginat 4%; 2 g larutan kitosan 4%; 4 tetes gliserin; dan 300 mg serbuk Al(OH)3 memberikan karakteristik yang baik sebagai sistem penyampaian obat gastroretentif. Waktu pembentangan film adalah 5 - 10 menit, film masih tetap utuh selama 7 jam. Pada simulasi sekresi asam lambung, mempertahankan pH pada pH 3 - 3,5 sekitar 6 jam. Nilai mukoadhesif dari film adalah 107,47 ± 7,38 dyne/cm dan index swelling
Hasil penelitian menunjukkan bahwa film alginat-kitosan adalah potensial untuk diaplikasikan sebagai suatu
adalah 111,30 %.
sistem penyampaian obat gastroretentif antasida.
FORMULATION AND EVALUATION OF
GASTRORETENTIVE ANTACID
ALGINATE-CHITOSAN FILM
USING
ABSTRACT
The conventional antacid dosage forms have a short duration of action for about 2-3 hours due to gastric emptying process. A gastroretentive dosage form of antacid is needed since the healing of gastric ulcers occurs when gastric pH is kept above 3 - 4 during 24 hours.
The aim of this study was to formulate a gastroretentive film of antacid using alginate-chitosan based which is able to neutralize gastric acid for longer time.
The gastroretentive films of antacid were prepared using alginate, chitosan and glycerin in various ratio. The mixtures of alginate, chitosan and glycerin containing antacid were then flattened on a glass object (2 cm x 5 cm) and allowed to dry at room temperature. Unfolding and integrity behaviors of the films were evaluated using the USP dissolution tester. Neutralization profile was determined by simulating gastric acid secretion. The simulation was carried out by droping 10 ml/h of 0.1 N HCl solution to 30 ml of 0.1 N HCl solution containing film of antacid. Mucoadhesive property was tested using rats stomach by DuNoy tensiometer, and swelling properties in 0.1 HCl solution was determined based on the increase of film size.
The results showed that film containing 1.5 g of 4% alginate solution, 2 g of 4% chitosan solution, 4 drops of glycerin and 300 mg of Al(OH)3
The result indicates that alginate-chitosan film is potential to apply as a gastroretentive drug delivery system of antacid.
gave good characteristics as a gastroretentive drug delivery system. The unfolding time of the film was 5 - 10 minutes, the film was intact for about 7 hours. On simulating gastric acid secretion, the maintenence pH was found at pH 3 - 3.5 was about 6 hours. The mucoadhesive value of the film was 107.47 ± 7.38 dyne/cm and the swelling index was 111.30%.
BAB I
PENDAHULUAN
1.1Latar Belakang
Penyakit utama dari lambung dan duodenum adalah, gastritis (radang
lambung), ulkus lambung (gastric ulcer), duodenitis (radang usus) dan ulkus
duodenum (duodenal ulcer), yang semuanya dalam beberapa cara berkaitan
dengan cedera yang dimediasi oleh asam (Gregory, 2000
Patofisiologi dari penyakit ulkus dapat digambarkan sebagai
ketidakseimbangan antara faktor-faktor pertahanan mukosa (bikarbonat, mukus,
prostaglandin, NO, peptida-peptida dan faktor-faktor pertumbuhan) dengan
injurious factors (misalnya: asam dan pepsin). Kondisi ).
produksi mukus yang
terlalu sedikit atau sekresi asam yang terlalu banyak dalam lambung akan
menyebabkan erosi di lapisan mukosa lambung. Berbagai kondisi dapat
menyebabkan gangguan ini. Bakteri H. pylory dan agen eksogen seperti obat
anti-inflamasi non steroid berinteraksi secara kompleks dalam menyebabkan ulkus.
Aspirin adalah asam, yang secara langsung mengganggu atau mengikis lapisan
mukosa lambung (Wallace, 2011; Corwin, 2008).
Dalam kondisi normal, pH lambung adalah sekitar 1,2 - 1,8. Pada siang
hari, makanan yang merangsang sekresi asam juga menetralisirnya dan menjaga
pH lambung sekitar 3 - 5. Namun, ketika perut kosong, sekitar 2 - 3 jam setelah
makan, pH kembali turun, dan penderita ulkus cenderung untuk mengalami rasa
sakit yang hilang dengan makan atau minum antasida. Rasa nyeri yang dimediasi
asam terjadi ketika pH lambung berada di bawah 2 (Gregory, 2000; Perigard,
Suatu ciri penting dari sekresi asam basal adalah rithme hariannya
(circadian rhythm), bahwa sekresi asam tinggi antara jam 22.00 sampai tengah
malam dan rendah pada jam 04.00 sampai jam 08.00 pagi. Inilah yang menjadi
alasan pasien cenderung untuk bangun sekitar tengah malam dengan dispepsia dan
nyeri ulu hati (heartburn). Ini menunjukkan bahwa pH lambung cenderung turun
menjadi 1 atau 2, karena sekresi asam relatif tinggi dan tidak dinetralkan oleh
makanan (Gregory, 2000; Tolman, 2000
Penggunaan antasida pada penyakit tukak lambung berdasarkan
kemampuannya menetralkan asam lambung dan ).
mencegah konversi pepsinogen
menjadi pepsin. Pepsinogen merupakan prekursor yang diubah menjadi pepsin
aktif dengan HCl bebas dan oleh proses autokatalitik. Pepsin adalah enzim
proteolitik yang diperkirakan memediasi cedera jaringan atau degradasi mukus
dan mukosa pada penyakit ulkus (Tolman, 2000).
Ada perbedaan pada jenis antasida dalam hal kapasitas netralisasi, durasi
kerja, dan efek samping. Penyebab kurang efektifnya pengobatan dengan sediaan
antasida konvensional dapat terjadi karena frekuensi pengobatan tidak adekuat,
pemilihan sediaan tidak tepat, dan sediaan antasida konvensional durasi kerjanya
singkat. Dalam kondisi perut kosong antasida mempunyai waktu tinggal di
lambung sekitar 30 menit. Jika diberikan ketika makanan di lambung, aksi
penyangga akan berlangsung selama 2 jam dan tambahan dosis 3 jam setelah
makan akan memperpanjang waktu penyangga 1 jam (Wallace, 2011; Tolman,
2000
Masa tinggal obat antasida konvensional yang singkat di lambung
menyebabkan ).
sel-sel parietal untuk periode waktu yang lama. Antasida ideal adalah yang
memiliki kapasitas penetralan yang besar, memiliki durasi kerja yang panjang,
memberikan aksi mempertahankan pH (buffering action) terus menerus dan tidak
menyebabkan efek lokal maupun sistemik yang merugikan (Tolman, 2000).
Penyembuhan penyakit asam lambung terjadi bila pH rata-rata 24 jam
dijaga di atas 3 - 4. pH tersebut dapat ditingkatkan dengan baik oleh penetral asam
(antasida) atau penghambat sekresi lambung (antagonis H2-reseptor atau inhibitor
pompa proton) (Tolman, 2000
Penyampaian obat dengan sistem gastroretentif (Gastroretentive Drug
Delivery Systems/GDDS) merupakan suatu solusi untuk memperpanjang masa
tinggal obat di lambung dan mengatasi durasi kerja antasida konvensional yang
singkat. Sistim gastroretentif ).
adalah sebuah pendekatan untuk memperpanjang
waktu tinggal obat di lambung, menargetkan pelepasan spesifik
Perpanjangan waktu tinggal dalam lambung dari sediaan obat dapat
meningkatkan bioavailabilitas, mengontrol lamanya pelepasan obat. Disamping
itu juga akan bermanfaat bagi kerja lokal obat di bagian atas saluran pencernaan
terutama untuk pengobatan ulkus peptik (Nayak, et al., 2010).
ke lambung dan
melepaskan obatnya secara terus menerus dan terkontrol dalam waktu yang lebih
lama, sehingga akan bermanfaat untuk meningkatkan efikasi dari obat (Nayak, et
al., 2010).
Beberapa contoh desain dan pengembangan dari sistem gastroretentif
meliputi; sistem penyampaian obat mukoadhesif yang melekat pada permukaan
mukosa; sistem pengembangan (swelling) yaitu sediaan ketika kontak dengan
pilorus sehingga sediaan tetap berada dalam lambung untuk beberapa waktu
tertentu; sistem pengapungan (floating system) yaitu sistem penyampaian dengan
menggunakan sediaan dengan densitas rendah sehingga dapat mengapung dan
bertahan dalam lambung untuk beberapa waktu, dan selanjutnya sediaan dengan
densitas tinggi yang ditahan pada dasar lambung (Ami, et al., 2012; Nayak, et al.,
2010).
Beberapa penelitian telah menjelaskan tentang penggunaan
alginat-kitosan dalam formulasi pelepasan obat terkontrol, sediaan film dan sediaan
gastroretentif, seperti formulasi mikropartikel alginat-kitosan sebagai
mukoadhesif yang mengandung prednisolon untuk pelepasan terkontrol (Wittaya,
et al., 2006), sediaan floating dan mukoadhesif dari bead alginat-kitosan yang
mengandung amoksisilin sebagai gastroretentif mampu memperpanjang pelepasan
obat selama lebih dari 6 jam dalam lambung (Sahasathian, et al., 2010). Evaluasi
fisika-kimia film alginat/kitosan yang mengandung natamycin sebagai agen
antimikroba
Selanjutnya suatu sediaan antasida dengan masa tinggal yang
diperpanjang di lambung (Antacid Compositions With Prolonged Gastric
Residence Time) telah ditemukan dan dipatentkan oleh Spickett, et al., (1994), (Silvaa, et al., 2005), dan Lilian, et al, (2011), membuat campuran
film kitosan kationik dengan ekstrak protein quinoa anionik yang dapat digunakan
sebagai edibel film untuk tujuan pengemasan dalam industri makanan.
produk antasida ini meliputi campuran 10-70 % vesikel lipid dengan partikulat
base yang mengandung antasida dalam bentuk koloid, suspensi, atau produk
kering. Fase lipid dibentuk dari gliserol monostearat (GMS), kolesterol, dan cetyl
negatif, dan tween 60 sebagai surfakatan yang menunjukkan bahwa pada waktu
enam jam sebagian besar dari vesikel lipid masih dipertahankan
Sediaan antasida dengan durasi diperpanjang (Extended duration antacid
product) juga telah dipatentkan oleh Wallach, et al., (1996).
di lambung.
Penemuan ini
meliputi sediaan padat oral dua fase dengan aktivitas antasida yang diperpanjang.
Fase internal terdiri dari campuran serbuk yang mengandung bahan aktif antasida
dan bahan tambahan yang dapat diterima (acceptable) secara farmasetika dan
fase eksternal mengandung suatu zat hidrofobik organik, seperti: ester dari
gliserol dengan asam palmitat atau stearat, polialkena dihidroksilasi dan
emulsifier
non-Sementara sediaan gastroretentif bentuk matriks film dengan
menggunakan
ionik.
HPMC dan eudragit sebagai polimer dan dibutil ftalat sebagai
plastisizer menunjukkan bahwa sediaan film mampu bertahan dalam lambung
hingga 6 ± 0,5 jam dalam kondisi puasa dan 8 jam dalam keadaan makan (
Alginat merupakan suatu polisakarida yang dihasilkan dari ganggang coklat
(Phaeophyceae) dan bakteri. Alginat adalah kopolimer anionik linier yang terdiri
dari residu asam β-D-manuronat dan asam α-L-guluronat dalam ikatan 1,4.
Kelebihan yang paling penting dari natrium alginat sebagai matriks untuk
formulasi pelepasan terkontrol adalah karena sifatnya yang biodegradabel dan
biokompatibel (Sachan, et al., 2009).
Sathish,
et al., 2013).
Kitosan merupakan derivat kitin adalah biopolimer kedua terbanyak yang
terdapat di alam sesudah sellulosa. Terdapat pada hewan khususnya
lemah, bersifat basa lemah dengan pKa dari residu D-glukosamine kira-kita 6,2 -
7,0 dan oleh karena itu tidak larut dalam pH netral dan alkali tetapi larut dalam
asam encer membentuk gel. Kitosan bersifat non toksik, membentuk film (film
former), biokompatibel, biodegradable
Berdasarkan pemaparan di atas, peneliti tertarik untuk merancang suatu
sediaan antasida model baru dengan sistem penyampaian obat gastroretentif,
dengan bentuk sediaan berupa film yang digulung, kemudian dimasukkan ke
dalam cangkang kapsul, dan saat kapsul hancur di lambung, film akan
membentang kembali, sehingga
dan bersifat mukoadhesif. Mekanisme
kerja mukoadhesif terjadi melalui interaksi ionik antara gugus amino kitosan yang
bermuatan positif dengan muatan negatif asam sialat yang terdapat dalam mukus.
Selain itu, polimer hidrofilik ini menarik cairan dari lapisan gel mukus yang
terdapat pada permukaan epitel dan akan mengembang dalam suasana asam (Felt,
et al., 1998; Yogeshkumar, et al., 2013).
memperpanjang waktu tinggal obat di lambung,
Kitosan dan alginat adalah polimer yang digunakan untuk formulasi
sediaan gastroretentif berbentuk film dalam penelitian ini, serta gliserin sebagai
plastisizer. Kedua polisakarida bermuatan berlawanan ini akan membentuk
kompleks polielektrolit yang memiliki karakteristik menarik untuk aplikasi
pelepasan terkontrol (Yan, et al., 2001).
dan melepaskan obatnya secara terus menerus dan terkontrol dalam waktu yang
lebih lama.
Sifat-sifat dan kemampuan kitosan membentuk film, bersifat mukoadhesif,
alginat yang mengontrol pelepasan obat dan bertahan di lambung sebagai sediaan
gastroretentif.
Magnesium hidroksida dan aluminium hidroksida dalam penelitian ini
adalah sebagai model obat. Magnesium hidroksida memiliki aksi yang cepat
dalam penetralan asam, yang juga bersifat pencahar dan dapat menyebabkan
diare. Aluminium hidroksida memiliki tindakan yang relatif lebih lambat dan
cenderung menyebabkan sembelit. Kombinasi senyawa magnesium dan
aluminium dapat digunakan untuk saling meminimalkan efek samping,
Penelitian ini meliputi pembuatan sediaan film alginat-kitosan yang
mengandung Al(OH)
kombinasi
ini banyak dipilih oleh para ahli (Neal, 2002; Wallace, 2011).
3, Mg(OH)2 dan kombinasi Al(OH)3 dan Mg(OH)2
1.2 Perumusan Masalah
, evaluasi
dan karakterisasi sediaan, serta uji in vitro.
1. Apakah Al(OH)3, Mg(OH)2 dan kombinasi Al(OH)3 dan Mg(OH)2
2. Apakah bentuk sediaan gastroretentif film alginat-kitosan yang
mengandung Al(OH)
dapat
diformulasi dalam bentuk film alginat-kitosan sebagai sediaan
Gastroretentive Drugs Delivery System (GDDS)?
3, Mg(OH)2 dan kombinasi Al(OH)3 dan Mg(OH)2
sebagai antasida mampu mempertahankan pH 3 sampai 4 dalam waktu
yang lebih lama dibandingkan sediaan konvesional yang diuji secara in
1.3Hipotesis
1. Alginat-kitosan merupakan suatu polimer yang dapat berinterakasi
membentuk kompleks polielektrolit yang dapat diaplikasikan terhadap
Al(OH)3, Mg(OH)2 dan kombinasi Al(OH)3 dan Mg(OH)2
2. Sediaan GDDS dari film alginat-kitosan yang mengandung Al(OH) sebagai suatu
sediaan film yang bertahan lebih lama dalam lambung/GDDS.
3,
Mg(OH)2 dan kombinasi Al(OH)3 dan Mg(OH)2
1.4 Tujuan Penelitian
sebagai antasida yang
dilipat dan dimasukkan dalam kapsul mempunyai sifat elastis dan akan
membentang kembali ketika kapsul hancur di lambung sehingga mencegah
obat melewati pilorus, ditambah lagi dengan kitosan yang bersifat
mukoadhesif serta mengembang dalam suasana asam akan lebih
membantu sediaan tertahan di lambung dan menjaga pH 3 - 4 dalam waktu
yang lebih lama dibandingkan sediaan konvensional yang diuji secara in
vitro.
1. Untuk membuat formula film alginat-kitosan yang dapat diformulasikan
dengan Al(OH)3, Mg(OH)2 dan kombinasi Al(OH)3 dan Mg(OH)2
2. Untuk mengetahui kemampuan sediaan gastroretentif film alginat-kitosan
yang mengandung Al(OH)
sebagai
suatu sediaan antasida dalam bentuk film yang mampu bertahan lebih lama
dalam lambung/GDDS.
3, Mg(OH)2 dan kombinasi Al(OH)3 dan
Mg(OH)2 tertahan di lambung dan menjaga pH antara 3 - 4 dalam durasi
yang lebih lama dibandingkan sediaan konvensional yang diuji secara in
1.5Manfaat Penelitian
Penelitian ini memberikan informasi dan kontribusi dalam pengembangan
Sistem Penyampaian Obat/Drug Delivery System (DDS) terutama dalam teknologi
sediaan obat-obat yang tertahan di lambung (Gastroretentive Drugs Delivery
System (GDDS). Sediaan GDDS dapat mengontrol lamanya pelepasan obat dalam
1.6Kerangka Pikir Penelitian
Kerangka pikir penelitian dapat dilihat pada Gambar 1.1.
Variabel Bebas Variabel Terikat Parameter
Gambar 1.1 Diagram kerangka pikir penelitian
Profil Netralisasi HCL 0,1 N secara
in vitro
Pelepasan ion logam dari sediaan film
secara in vitro Sifat Bioadhesif Meliputi:
- Variasi tebal & berat film
- Sifat pembentangan (Unfolding
behaviour) - Keutuhan film
(Integrity properties) - SEM Efektivitas Sediaan Film Alginat-Al(OH)3 Film Alginat- Mg(OH)2 Film Kitosan-Al(OH)3 Film Kitosan- Mg(OH)2 Film Alginat-Al(OH)3 dan Mg(OH)2 Film Kitosan-Al(OH)3 dan Mg(OH)2 Film Alginat- Kitosan-Al(OH)3 dan
Mg(OH)2 Formulasi Gastroretentif film Alginat-Kitosan yang mengandung Antasida (Al(OH)3, Mg(OH)2, dan kombinasi Al(OH)3, dan Mg(OH)2)
Karakteristik Sediaan
Sifat Pengembangan (swellingproperties) Durasi Kerja
BAB II
TINJAUAN PUSTAKA
2.1Ulkus
Ulkus peptikum merupakan istilah yang mengacu pada erosi lapisan
mukosa di mana saja di saluran pencernaan, namun biasanya mengacu pada erosi
di lambung atau duodenum. Ada dua penyebab utama ulkus: terlalu sedikit
produksi mukus atau terlalu banyak asam yang diproduksi dalam lambung atau
dikirim ke usus
2.1.1 Faktor-faktor yang mempengaruhi produksi mukus
(Corwin, 2008).
Ulkus umumnya berkembang ketika sel-sel mukosa usus tidak
menghasilkan mukus yang cukup untuk melindungi terhadap pencernaan asam.
Penyebab penurunan produksi mukus dapat mencakup apa saja yang menurunkan
aliran darah ke usus, menyebabkan hipoksia lapisan mukosa dan cedera atau
kematian sel-sel yang memproduksi mukus. Jenis ulkus ini disebut ulkus iskemik.
Penurunan aliran darah terjadi dengan semua jenis shock. Suatu jenis tertentu dari
ulkus iskemik yang berkembang setelah luka bakar parah disebut ulkus Curling
(Corwin, 2008).
Penyebab utama penurunan produksi mukus berhubungan dengan infeksi
bakteri H. pylori. H. pylori menginfeksi sel-sel yang mensekresi mukus lambung
dan duodenum, sehingga mengurangi kemampuan mereka untuk menghasilkan
mukus. Sekitar 90% dari pasien yang memiliki ulkus duodenum dan 70% dari
pasien yang memiliki ulkus lambung disebabkan infeksi H. pylori. Penurunan
produksi mukus dalam duodenum juga dapat terjadi sebagai akibat dari
Aktivitas mereka dihambat oleh stimulasi simpatis, stimulasi simpatis meningkat
dengan stres kronis. Sehingga menjadi suatu rangkaian antara stres kronis dan
pengembangan ulkus
2.1.2 Dampak kelebihan produksi asam di lambung
(Corwin, 2008).
Secara fisiologis produksi asam di lambung diperlukan untuk aktivasi
enzim pencernaan lambung. Asam klorida (HCl) yang diproduksi oleh sel-sel
parietal sebagai respon terhadap makanan tertentu, obat-obatan, hormon
(termasuk gastrin), histamin, dan stimulasi parasimpatis. Makanan dan
obat-obatan seperti kafein dan alkohol merangsang sel-sel parietal untuk menghasilkan
asam. Beberapa individu mungkin over-reaktif dalam respon parietal mereka
untuk zat atau makanan, atau mereka mungkin memiliki lebih banyak sel parietal
dari normal dan karena itu melepaskan asam berlebih (Corwin, 2008).
Ada dua jenis sekresi asam, sekresi asam yang distimulasi (acid
secretion stimulated) dan sekresi asam basal (acid secretion basal). Sekresi asam
melalui stimulasi terjadi sebagai respon terhadap penglihatan, penciuman, dan
konsumsi makanan. Hal ini diatur terutama oleh hormon gastrin, yang dilepaskan
dari antrum lambung sebagai respon terhadap peningkatan pH (misalnya saat
makan). Ketika konsumsi makanan berhenti, pH di lambung turun, dan sekresi
gastrin berhenti, menyebabkan sekresi asam berkurang. Dengan cara ini makan
mengatur rangsangan sekresi asam (Gregory, 2000).
Selain itu, sekresi gastrin dirangsang oleh pelepasan peptida yang
melepaskan gastrin dari saraf pleksus submukosa sebagai akibat dari stimulasi
parasimpatis. Karena gastrin merangsang produksi asam, apapun yang
Contoh utama dari kondisi ini disebut sindrom Zollinger-Ellison, penyakit yang
ditandai dengan tumor sel endokrin yang mensekresi gastrin. Penyebab lain
kelebihan asam mencakup stimulasi vagus yang berlebihan pada sel-sel parietal
yang terlihat setelah cedera otak parah atau trauma. Ulkus yang berkembang
dalam keadaan ini disebut ulkus Cushing. Stimulasi vagus yang berlebihan selama
stres psikologis juga dapat menyebabkan kelebihan produksi HCl (Corwin,
2008).
Sekresi asam basal terjadi terus menerus dan independen dari rangsangan
eksternal (tidak dipengaruhi oleh ransangan dari luar). Hal ini dimediasi terutama
oleh asetilkolin, neurotransmitter dari saraf vagus. Suatu karakterisitk penting dari
sekresi asam basal adalah ritme hariannya (circadian rhythm), bahwa sekresi
asam rendah di siang hari namun relatif tinggi di malam hari, umumnya
memuncak antara jam 22.00 dan tengah malam. Baik sekresi asam yang
dirangsang gastrin dan asetilkolin, terutama dengan merangsang sel-sel
enterochromatin (ECL) di bagian bodi lambung. Sel ECL akan melepaskan
histamin yang merangsang sel-sel parietal yang berdekatan untuk mensekresikan
asam. Jalur akhir yang umum dari sekresi asam adalah pompa proton H+, K+
ATPase yang menukar ion hidrogen dengan ion kalium (Gregory, 2000; Tolman,
2000).
Pada umumnya, ulkus terjadi setiap kali ada peningkatan sekresi asam
atau penurunan ketahanan mukosa, seperti terlihat pada Gambar 2.1. Sebaliknya,
penyakit asam lambung dapat ditangani dengan baik dengan menurunkan asam
atau meningkatkan ketahanan mukosa. pH tersebut dapat ditingkatkan dengan
H2-reseptor atau inhibitor pompa proton). Ketahanan mukosa dapat ditingkatkan
dengan analog prostaglandin (Tolman, 2000).
Peningkatan aliran asam ke duodenum dapat menyebabkan ulkus
duodenum. Gerakan yang terlalu cepat dari isi lambung ke duodenum dapat
membanjiri lapisan mukus pelindung duodenum. Hal ini terjadi pada iritasi
lambung oleh makanan tertentu atau mikroorganisme, serta oleh kelebihan sekresi
[image:32.595.156.488.271.472.2]gastrin (Corwin, 2008).
Gambar 2.1.Faktor-faktor penyebab ulkus (Liu dan Crawford, 2005)
2.1.3 Cairan lambung (Gastric Juice)
Cairan lambung (Gastric juice) adalah campuran heterogen dari cairan
jernih, flocculent, dan mukus jernih. Konstituen utama dari cairan lambung
(gastric juice) adalah asam hidroklorida, protease lambung (pepsin dan
gastricsin), faktor hematopoietic (faktor intrinsik dan pengikat vitamin B12),
hormon lambung, dan mucosubstance (aminopolysaccharides, mucopolyuronides,
mucoids, dan mucoproteins). Protease lambung yang utama adalah pepsin dan
gastricsin, pepsinogen adalah prekursor yang diubah menjadi pepsin aktif oleh
Pengujian fungsi lambung biasanya dilakukan pada sampel asam lambung
yang dikumpulkan melalui intubasi langsung (direct intubation) ke dalam
lambung. Kandungan lambung dalam puasa (normal, 20 – 30 ml) dan sekresi
lambung tersebut dikumpulkan dalam keadaan basal, atau setelah stimulasi oleh
pemberian oral kafein-benzoat atau alkohol, atau pemberian histamin parenteral,
insulin, atau hormon pentagastrin. Sampel dikumpulkan melalui aspirasi terus
menerus dan dianalisis untuk keasaman dan aktivitas protease lambung pada
berbagai interval waktu (Dressman, 1998; Perigard, 2000).
Keasaman dapat ditentukan dengan pengukuran pH secara sederhana dan
konversi ke mEq H+ atau dengan titrasi asam lambung. Asam lambung yang
keluar (basal acid output ) adalah sekitar 1 mEq/jam pada kondisi normal dan 2
sampai 4 mEq pada pasien ulkus duodenum. Puncak keluaran asam (peak acid
output/PAO) setelah stimulasi histamin adalah 10 sampai 20 mEq/jam dalam
normal dan 40 sampai 50 mEq/jam dalam ulkus duodenum, PAO setelah stimulasi
pentagastrik mirip dengan histamin (Perigard, 2000
2. 2 Antasida
).
Antasida digunakan secara luas untuk menghilangkan rasa panas/nyeri ulu
hati (heartburn) dan dispepsia (keluhan pada perut bagian atas seperti kembung,
cepat kenyang/sebah, mual, atau bersendawa yang dipicu oleh makanan), serta
berbagai macam gejala GI nonspesifik. Peran utama antasida dalam penanganan
gangguan asam lambung adalah menghilangkan rasa sakit.
Antasida biasanya digunakan dalam kombinasi. Perbedaan dalam
campuran menjelaskan perbedaan relatif dalam kapasitas netralisasi dan efek
efektivitas antasida tersebut. Untuk tujuan praktis, bagaimanapun, keberhasilan
diperoleh dengan meningkatkan pH lambung menjadi 3,5 atau lebih besar. Hal ini
dicapai dengan mudah oleh antasida modern (Tolman, 2000).
Mekanisme kerja antasida bersifat kompleks. Mekanisme yang
diusulkan adalah pencegahan difusi balik ion hidrogen di mukosa GI. Umumnya
diterima bahwa meningkatkan pH lambung sekitar 4 mencegah stres ulkus, yang
diduga diperantarai oleh difusi asam kembali. Tindakan lain antasida adalah untuk
mencegah konversi pepsinogen lambung menjadi pepsin bentuk aktif. Ini adalah
enzim proteolitik diperkirakan memediasi cedera jaringan pada penyakit ulkus.
Pepsinogen mengalami inaktivasi ireversibel pada pH 5. Dengan demikian
mungkin diperlukan untuk meningkatkan pH sampai 5 untuk mencapai manfaat
maksimal dari antasida. Antasida juga dapat meningkatkan sitoproteksi di
lambung, memberikan manfaat terapeutik dengan menonaktifkan garam empedu,
yang diperkirakan refluks dari duodenum ke lambung dan memainkan beberapa
peran dalam penyakit asam lambung (Tolman, 2000
2.2.1 Kapasitas penetralan asam dan efektivitas relatif antasida
).
Antasida konvensional (sediaan antasida dengan pelepasan segera)
dibandingkan secara kuantitatif dalam hal ”Kapasitas Penetralan Asam” (
acid-neutralizing capacity/ANC), didefinisikan sebagai jumlah miliekuivalen asam
klorida yang diperlukan untuk mempertahankan 1 ml suspensi antasida pada pH 3
selama 2 jam secara in vitro (Tolman, 2000).
Efektivitas relatif dari sediaan antasida konvensional dinyatakan sebagai
miliekuivalen kapasitas penetralan asam (didefinisikan sebagai jumlah
sesuai dengan persyaratan FDA, antasida harus memiliki kapasitas netralisasi
minimal 5 mEq per dosis (Wallace, 2000).
Untuk ulkus tanpa komplikasi, antasida diberikan secara oral 1 dan 3
jam setelah makan dan sebelum tidur. Rejimen ini, memberikan - 120 mEq dari
kombinasi Mg-Al per dosis, mungkin hampir sama efektifnya dengan dosis
konvensional dengan antagonis reseptor H2. Untuk gejala berat atau refluks tidak
terkontrol, antasida dapat diberikan sesering setiap 30 - 60 menit (Wallace, 2000).
Secara umum, antasida diberikan dalam bentuk suspensi karena ini
mungkin memiliki kapasitas netralisasi lebih besar dari bentuk bubuk atau sediaan
tablet. Jika tablet yang digunakan, mereka harus benar-benar dikunyah untuk efek
maksimum, namun antasida dibersihkan dari perut kosong dalam 30 menit,
dengan adanya makanan cukup untuk meningkatan pH lambung sampai 5 selama
1 jam dan untuk memperpanjang efek netralisasi antasida selama 2 - 3 jam
(Wallace, 2000
2.3Gastroretentive Drugs Delivery System (GDDS)
).
Kandidat obat yang sesuai untuk sediaan yang tertahan di lambung atau
gastroretentif (Garg dan Gupta, 2008; Swetha, et al., 2012):
a. Obat-obat untuk aksi lokal dalam lambung misalnya: misoprostol, antasida,
dan antibiotik yang digunakan untuk mengobati infeksi Helicobacter pylori.
b. Obat-obat yang kelarutan rendah dalam pH alkalis misalnya: furosemida,
diazepam, verapamil, dan klordiazepoksida.
c. Obat-obat yang terutama diabsorbsi dalam lambung atau bagian atas dari
d. Obat-obat yang mempunyai rentang absorpsi sempit dalam saluran
pencernaan misalnya: siklosporin, metotreksat, levodopa, dan riboflavin.
e. Obat-obat yang diabsorbsi cepat dari saluran pencernaan misalnya:
metronidazol, dan tetrasikilin.
f. Obat-obat yang tidak stabil dan terdegradasi didalam kolon misalnya
ranitidin, metronidazol, dan metformin HCl.
g. Obat-obat yang mengganggu mikroba kolon misalnya antibiotik untuk
Helicobacter pylori.
Kelebihan sediaan gastroretentif (Swetha, et al., 2012):
a. Digunakan untuk aksi lokal dalam lambung.
b. Dalam pengobatan dari penyakit ulkus peptikum.
c. Digunakan untuk penghantaran obat-obat dengan rentang absorbsi yang
sempit.
d. Mengurangi frekuensi pemberian.
e. Meningkatkan bioavailabilitas obat.
f. Digunakan untuk obat-obat yang tidak stabil di dalam cairan usus.
g. Digunakan untuk menahan penghantaran obat.
h. Digunakan untuk mempertahankan konsentrasi obat sistemik dalam rentang
terapeutik.
Kekurangan sediaan gastroretentif (Swetha, et al., 2012):
a.Memerlukan jumlah yang cukup besar cairan lambung, bagi sistem untuk
mengapung dan bekerja efisien.
b.Tidak cocok untuk obat-obat dengan masalah stabilitas dan kelarutan dalam
2.3.1 Jenis-jenis Gastroretentif
Pendekatan untuk sistem penghantaran obat tertahan di lambung secara
umum terdiri dari:
1. Sistem pengembangan dan pembesaran (swelling and expandable system).
Ini merupakan bentuk sediaan yang setelah ditelan, dalam lambung
mengembang pada taraf tertentu yang mencegah mereka keluar dari pilorus,
seperti terlihat pada Gambar 2.2. Akibatnya, bentuk sediaan masih dipertahankan
dalam lambung untuk jangka waktu yang panjang. Formulasi tersebut dirancang
untuk tertahan di lambung (gastric retention) dan pelepasan obat dikontrol dalam
[image:37.595.214.347.360.463.2]rongga lambung (Kumar, 2012).
Gambar 2.2 GDDS dengan sistem pengembangan dan pembesaran (Kumar, 2012)
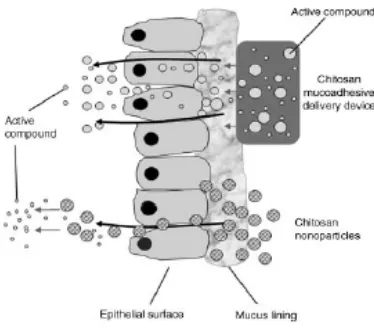
2. Sistem bioadhesif (bioadhesive systems).
Sistem bioadhesif digunakan sebagai perangkat penyampaian obat untuk
meningkatkan absorpsi di tempat spesifik (site specific) dalam lambung.
Pendekatan ini melibatkan penggunaan polimer bioadhesif, yang dapat menempel
pada permukaan epitel di lambung. Beberapa eksipien yang paling menjanjikan
yang telah umum digunakan di sistem ini meliputi polycarbophil, karbopol,
kitosan dan gliadin (Kumar, 2012). Sistem bio/muko-adhesif dapat dilihat pada
Gambar 2.3 GDDS dengan sistem bio/muko-adhesif (Al-Qadi, et al., 2012)
Mekanisme bioadhesif/mukoadhesif untuk berikatan antara polimer
dengan permukaan mukus/epitel dapat dibagi menjadi tiga kategori:
a.Adhesi yang dimediasi oleh Hidrasi
Polimer hidrofilik tertentu memiliki kecenderungan untuk menyerap
sejumlah besar air dan menjadi lengket, sehingga memperoleh sifat bioadhesif.
Gastroretensi yang diperpanjang dari sistem pengiriman bio/muko-adhesi
selanjutnya dikendalikan oleh laju disolusi polimer.
b.Adhesi yang dimediasi oleh ikatan
Adhesi polimer pada mukus/permukaan sel epitel melibatkan berbagai
mekanisme ikatan. Ikatan fisik atau mekanik dapat dihasilkan dari deposisi dan
masuknya bahan perekat di celah-celah mukosa tersebut. Ikatan kimia sekunder,
berkontribusi terhadap sifat bioadhesif, seperti interaksi van der Walls dan
interaksi ikatan hidrogen. Gugus fungsional hidrofilik yang bertanggung jawab
untuk membentuk ikatan hidrogen adalah hidroksil (-OH) dan gugus karboksilat
c.Adhesi yang dimediasi oleh reseptor
Polimer tertentu memiliki kemampuan untuk mengikat reseptor spesifik
pada permukaan sel. Peristiwa yang dimediasi reseptor berfungsi sebagai
pendekatan potensial dalam bio/muco-adhesi, sehingga meningkatkan retensi
lambung dari bentuk sediaan (Kumar, 2012).
3.Sistem pengapungan (floating systems)
Sistem ini memiliki kerapatan massa yang kurang dari cairan lambung
sehingga mengapung di lambung tanpa mempengaruhi tingkat pengosongan
lambung untuk jangka waktu lama, obat dilepaskan perlahan pada tingkat yang
diinginkan dari sistem. Setelah pelepasan obat, sistem residual dikosongkan dari
lambung. Sistem floating dapat dibagi ke dalam sistem effervescent dan
non-effervescent (Kumar, 2012). Sistem floating dapat dilihat pada Gambar 2.4.
Gambar 2.4 GDDS dengan sistem floating (Kumar, 2012)
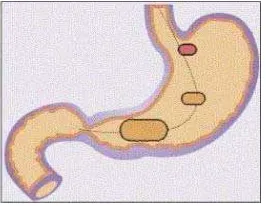
4.Sistem berdensitas tinggi (high density systems)
Sedimentasi telah digunakan sebagai mekanisme retensi untuk pelet yang
cukup kecil untuk disimpan dalam lipatan lambung dekat daerah pilorus, yang
merupakan bagian dari organ dengan posisi terendah dalam postur tegak. Pelet
padat (sekitar 3 g/cm-3) terjebak dalam lipatan juga cenderung untuk menahan
gerakan peristaltik dari dinding lambung, seperti terlihat pada Gambar 2.5. Waktu
transit GI dapat diperpanjang rata-rata 5,8 - 25 jam, tergantung pada kepadatan
seng oksida, titanium dioksida dan serbuk besi. Bahan-bahan ini meningkatkan
kepadatan hingga 1,5 - 2,4g/cm-3 (Kumar, 2012).
Gambar 2.5 GDDS dengan sistem berdensitas tinggi (High Density Systems) (Kumar, 2012)
2.3.2 Penelitian terdahulu tentang GDDS dan sediaan gastroretentif di pasaran
Penelitian terdahulu telah menjelaskan tentang sistem penyampaian
obat-obat yang tertahan di lambung (Gastroretentive Drugs Delivery
System/GDDS), diantaranya sebagai berikut:
a. Sediaan gastroretentif dengan pembawa
- Formulasi
alginat-kitosan:
mikropartikel alginat-kitosan sebagai mukoadhesif yang
mengandung prednisolon untuk pelepasan terkontrol (
-Wittaya, et al., 2006).
Sediaan floating dan mukoadhesif dari bead alginat-kitosan yang mengandung
amoksisilin sebagai gastroretentif mampu memperpanjang pelepasan obat
selama lebih dari 6 jam dalam lambung (
- Sediaan mikrobead dari campuran natrium alginat dengan natrium NaCMC
dan disalut enterik dengan kitosan untuk tujuan pelepasan terkontrol dari
amoksisilin di dalam lambung (Angadi, et al., 2012).
Sahasathian, et al., 2010).
- Pengembangan jenis baru dari floating beads inner berpori. Bead dibuat
dengan tetesan larutan busa ke dalam larutan CaCl2, larutan busa terdiri dari
berbagai gelembung mikro dengan poloxamer 188 sebagai agen pembusa, dan
b. Sediaan gastroretentif dari bahan lainnya:
- Nayak, et al., (2012), pembuatan sistem keseimbangan hidrodinamis
ofloksasin menggunakan laktosa, HPMC K4M, PVP K 30, dan parafin cair,
yang dapat meningkatkan waktu tinggal dalam lambung, dan memungkinkan
dapat melepaskan obat maksimal di lokasi penyerapan untuk meningkatkan
bioavailabilitas oral.
c. Sediaan gastroretentif antasida:
- Sediaan antasida dengan masa tinggal yang diperpanjang di lambung
(Antacid Compositions With Prolonged Gastric Residence Time) telah
ditemukan dan dipatentkan oleh Spickett, et al., (1994 ). Sediaan ini memiliki
fase internal antasida yang padat (serbuk, tablet) dan dikelilingi oleh
excipient dengan fase eksternal padat yang mengandung suatu substansi
hidrofobik seperti ester dari gliserol dengan asam palmitat atau stearat,
polialkena hidroksilasi dan emulsifier non-ionik.
- Sediaan antasida dengan durasi diperpanjang (Extended duration antacid
product) juga dipatentkan oleh Wallach, et al., (1996), merupakan suatu
produk antasida yang memiliki masa tinggal diperpanjang dalam lambung
dan sistem pencernaan bagian atas. Produk antasida ini memuat campuran 10
- 70% nonfosfolipid dalam bentuk vesikel lipid. Penelitian ini menunjukkan
bahwa selama enam jam dari sediaan masih dipertahankan dalam lambung.
d. Sediaan gastroretentif dengan bentuk film.
- Sediaan gastroretentif bentuk matriks film dengan menggunakan HPMC dan
bahwa sediaan film mampu bertahan dalam lambung hingga 6 ± 0,5 jam
dalam kondisi puasa dan 8 jam dalam keadaan makan (
Sediaan gastroretentif di pasaran
Sathish, et al., 2013).
Berkembangnya bentuk sediaan gastroretentif merupakan suatu upaya
dalam memaksimalkan teknologi sistem penyampaian obat, terutama dalam
teknologi penyampaian obat-obat untuk tujuan lokal dan spesifik di lambung
dengan pelepasan lambat (sustained release). Beberapa contoh sediaan
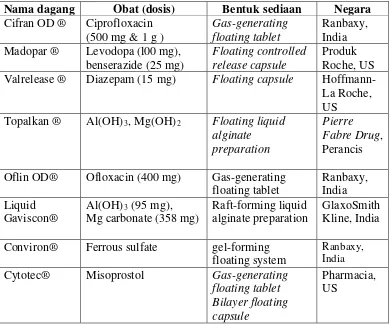
[image:42.595.121.511.332.658.2]gastroretentif yang ada di pasaran, dapat dilihat pada Tabel 2.1 di bawah.
Tabel 2.1 Produk-produk sediaan gastroretentif yang tersedia di pasaran
Nama dagang Obat (dosis) Bentuk sediaan Negara
Cifran OD ® Ciprofloxacin (500 mg & 1 g )
Gas-generating floating tablet
Ranbaxy, India Madopar ® Levodopa (l00 mg),
benserazide (25 mg)
Floating controlled release capsule
Produk Roche, US Valrelease ® Diazepam (15 mg) Floating capsule
Hoffmann-La Roche, US
Topalkan ® Al(OH)3, Mg(OH) Floating liquid alginate preparation
2 Pierre
Fabre Drug, Perancis
Oflin OD® Ofloxacin (400 mg) Gas-generating floating tablet Ranbaxy, India Liquid Gaviscon® Al(OH)3
Mg carbonate (358 mg)
(95 mg), Raft-forming liquid alginate preparation
GlaxoSmith Kline, India
Conviron® Ferrous sulfate gel-forming
floating system
Ranbaxy, India
Cytotec® Misoprostol Gas-generating
floating tablet Bilayer floating capsule Pharmacia, US
2.4Natrium alginat
Natrium alginat merupakan produk pemurnian karbohidrat yang
diekstraksi dari alga coklat (Phaeophyceae) dengan menggunakan basa lemah
(Grasdalen, et al., 1979). Alginat ini diperoleh dari spesies Macrocystis pyrifera,
Laminaria, Ascophyllum dan Sargassum. Alginat merupakan bahan yang non
toksik, non alergi (biokompatibel) dan biodegradabel (Rehm, 2009).
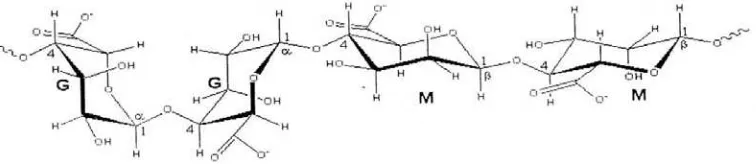
Asam alginat adalah kopolimer biner yang terdiri dari residu
β-D-mannuronat (M) dan α-L-asam guluronat (G) yang tersusun dalam blok-blok yang
membentuk rantai linear. Kedua unit tersebut berikatan pada atom C1 dan C4
dengan susunan homopolimer dari masing-masing residu (MM dan GG) dan suatu
blok heteropolimer dari dua residu (MG) (Thom, et al., 1981). Struktur alginat
dapat dilihat pada Gambar 2.6.
Gambar 2. 6 Struktur Kimia Alginat (Thom, et al., 1981)
2.5 Kitosan
Kitosan merupakan aminopolisakarida hasil deasetilasi dari kitin, kitosan
terdapat dalam cangkang crustacea seperti udang, lobster dan kepiting. Kitosan
menunjukkan sifat polimer biomedis seperti nontoksik, biokompatibel dan
biodegradabel (Felt, et al., 1998). Kitosan merupakan biopolimer yang linear,
tidak bercabang, polimer yang dibangun dari monomer-monomer glukosamin dan
N-asetilglukosamin yang terikat pada pola β-(1-4). Struktur kimia dari kitosan
[image:43.595.124.502.419.501.2]Gambar 2 .7 Struktur Kimia Kitosan (Felt, et al., 1998)
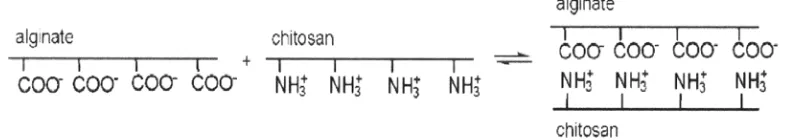
2.6Interaksi antara alginat dengan kitosan
Alginat yang merupakan polianionik dan kitosan yang merupakan
polikationik dapat berinteraksi melalui gugus asam karboksilat dari alginat dan
gugus amino dari kitosan membentuk kompleks polielektrolit dari muatan mereka
yang berlawanan seperti yang ditunjukkan pada Gambar 2.8.
Kompleks polielektrolit yang terbentuk diharapkan dapat memberikan
aplikasi farmasetika yang lebih baik karena keunikan struktur dan sifatnya
(Takahashi, et al., 1990).
[image:44.595.119.512.447.517.2]BAB III
METODE PENELITIAN
Penelitian ini dilakukan secara eksperimental yang meliputi pembuatan
sediaan film alginat-kitosan yang mengandung Al(OH)3, Mg(OH)2, dan
kombinasi Al(OH)3 dan Mg(OH)2
3.1 Alat dan Bahan
, evaluasi dan karakterisasi sediaan, dan uji in
vitro. Penelitian ini dilakukan di Laboratorium Farmasi Fisik Fakultas Farmasi
USU, Laboratorium Penelitian Fakultas Farmasi USU dan Laboratorium Terpadu
LIDA USU.
3.1.1 Alat
Alat-alat yang digunakan pada penelitian ini adalah neraca listrik (Boeco),
alat-alat gelas, magnetic stirrer, pelat kaca, rangkaian alat infus, statif dan klem,
lumpang, stamper, penangas air, lemari asam, desikator, pH meter (Hanna), hot plate,
Spektrofotometer Serapan Atom Hitachi (Z-2000), dan Scanning Electron
Microscopy (SEM).
3.1.2 Bahan
Bahan-bahan yang digunakan pada penelitian ini adalah, kitosan (Wako
Pure Chemical Industries, Ltd Japan), natrium alginat 500~600 (Wako Pure
Chemical Industries, Ltd. Japan), gliserin (Merck), cangkang kapsul 00 (PT.
Bratachem), magnesium hidroksida (Mg(OH)2, dan aluminium hidroksida
(Al(OH)3. Pereaksi yang digunakan: asam klorida (HCl) 98%, asam asetat 98%,
aluminium 1000 ppm. Semua pereaksi yang digunakan dalam penelitian ini
berkualitas pro analisa keluaran E.Merck.
3.2 Pembuatan Pereaksi
1. Larutan kitosan 4% (b/v).
Ditimbang 4 gram serbuk kitosan, kemudian dilarutkan dalam 100 ml asam
asetat 1%.
2. Larutan alginat 4% (b/v).
Ditimbang 4 gram serbuk natrium alginat (500-600), kemudian ditaburkan
dalam 100 ml air suling, diaduk sampai homogen, dibiarkan mengembang
selama 24 jam
3. Larutan HNO3
Larutan HNO
5 N (v/v)
3
4. Larutan HCl 0,1 N
65 % sebanyak 346,5 ml diencerkan dengan air suling hingga
1000 ml (Ditjen POM, 1979).
Larutan asam klorida (p) sebanyak 8,3 ml diencerkan dengan air suling sampai
1000 ml
3.3 Pembuatan Sediaan Film Alginat-Kitosan
Ditimbang larutan kitosan, larutan alginat, serbuk Al(OH)3 dan serbuk
Mg(OH)2 sesuai dengan formula yang terdapat padaTabel 3.1. Disiapkan cetakan
film dari objek gelas yang telah dilumasi dengan silikon. Kemudian serbuk
Al(OH)3 dan larutan kitosan digerus dalam lumpang sampai homogen,
ditambahkan serbuk Mg(OH)2 dan larutan alginat digerus sampai homogen,
ditambahkan gliserin dan dihomogenkan. Setelah itu campuran diratakan di atas
yang datar dan dikeringkan pada suhu kamar selama 48 jam. Film yang sudah
kering dilepas dari objek gelas secara hati-hati dan disimpan dalam desikator,
yang selanjutnya siap untuk dimasukkan ke dalam kapsul ukuran 00 dengan cara
digulung.
Tabel 3.1 Formula sediaan film alginat-kitosan yang mengandung antasida
No Jenis Formula
Pembawa Zat Aktif
Gliserin Alginat
(lart. 4%)
Chitosan (lart. 4%)
Al(OH) Mg(OH)
3
2
1 F1 2,5 g - 300 mg - 2 tts
2 F2 2,5 g - 300 mg 2 tts
3 F3 - 2,5 g 300 mg - 2 tts
4 F4 - 2,5 g - 300 mg 2 tts
5 F5 1 g 2 g 300 mg - 4 tts
6 F6 1,5 g 2 g 300 mg - 4 tts
7 F7 2 g 2 g 200 mg 200 mg 4 tts
8 F8 3 g 1 g 200 mg 200 mg 4 tts
9 F9 3,5 g 0,5 g 200 mg 200 mg 4 tts
3.4 Uji Variasi Ketebalan dan Berat Film
Ketebalan film diukur dengan menggunakan jangka sorong mikro meter.
Pengukuran dilakukan pada 5 posisi yang berbeda dari permukaan film dan
dihitung nilai rata-rata. Sedangkan untuk berat, ditimbang berat film untuk setiap
formulasi dalam tiga kali ulangan, dan dihitung nilai rata-ratanya.
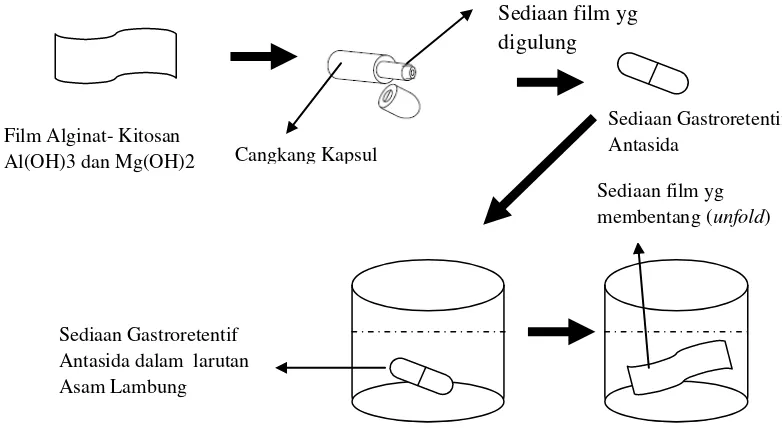
3.5 Uji Sifat Pembentangan (Unfolding behaviour) Sediaan Film secara in vitro
Uji sifat pembentangan film (Unfolding) dilakukan untuk melihat
elastisitas dan kemampuan membentang kembali dari sediaan film yang
dimasukkan ke dalam kapsul setelah digulung ketika kapsul telah hancur dalam
lambung, seperti ilustrasi pada Gambar 3.1. Uji sifat pembentangan dilakukan
menggunakan alat disolusi dalam 900 ml asam klorida pH 1,2 pada 37ºC ± 0,5ºC
Pada waktu 0, 5, 10, 15, 30, 60, 120, 360 dan 720 menit diamati sifat
pembentangan dari sediaan film. Setiap formula dilakukan tiga kali ulangan, dan
[image:48.595.119.510.181.398.2]dihitung standart deviasi rata-rata.
Gambar 3.1 Ilustrasi sediaan gastrortentif antasida film alginat-kitosan
3.6 Uji Integritas (keutuhan) Sediaan Film
Uji integritas sediaan film dilakukan untuk mengukur berapa lama
sediaan film tetap utuh dalam lambung. Keutuhan film dilihat dari ketahanan dan
tidak hancurnya sediaan film dalam rentang waktu yang diamati. Uji integritas
dilakukan menggunakan alat disolusi metode basket dalam 900 ml asam klorida
pH 1,2 pada 37ºC ± 0,5ºC dengan putaran 100 rpm.
Pada waktu 0, 30, 60, 120, 360 dan 720 menit diamati keutuhan dari
sediaan film. Setiap formula dilakukan tiga kali ulangan, dan dihitung standart
deviasi rata-rata.
Cangkang Kapsul
Sediaan Gastroretentif Antasida
Film Alginat- Kitosan Al(OH)3 dan Mg(OH)2
Sediaan film yg digulung
Sediaan Gastroretentif Antasida dalam larutan Asam Lambung
3.7Penentuan Profil Netralisasi HCl 0,1 N oleh Sediaan Film Alginat-Kitosan dalam Simulasi Sekresi Asam Lambung secara in vitro
Belum ada metode dalam literatur, text book ataupun jurnal untuk
menentukan profil netralisasi terhadap sekresi asam di lambung secara in vitro.
Metode dalam penelitian ini dirancang berdasarkan kondisi fisiologis lambung,
yaitunya kandungan asam lambung dalam puasa (normal) sekitar 20 - 30 ml, asam
lambung yang keluar (basal acid output ) adalah sekitar 1 mEq/jam
Pengukuran profil netralisasi terhadap asam
pada kondisi
normal (Dressman, 1998; Perigard, 2000).
ditentukan dengan
pengukuran pH secara sederhana. Pengukuran ini bertujuan untuk melihat
kemampuan sediaan film dalam mempertahankan pH 3 - 4 dan menetralisir
penambahan/asam klorida yang keluar berkesinambungan dari sel-sel parietal
untuk periode waktu yang lebih lama.
3.7.1 Persiapan Rancangan Alat
Alat untuk uji dirakit secara lokal dengan rancangan alat terdiri dari
rangkaian wadah gelas 250 ml yang dilengkapi dengan pengatur suhu (37 ± 0,5
o
C) dan pengaduk (100 rpm). Wadah gelas ini akan dihubungkan dengan
serangkaian selang alat infus yang berisi larutan HCl 0.1 N. Dari rangkaian alat
infus ini akan mensuplai HCl 0,1 N ke dalam wadah gelas 250 ml yang dapat
diatur laju pelepasannya. Wadah gelas berfungsi sebagai tempat alat uji
sampel/sediaan, seperti pada Gambar 3.2. Gambar Rangkaian Alat Uji Profil
Gambar 3.2Bagan Rancangan Alat untuk menentukan Profil Netralisasi Asam
Laju pelepasan HCl 0,1 N di sini menggambarkan kondisi fisiologis
pengeluaran asam lambung, pada kondisi normal sekitar 1 mEq/jam setara dengan
10 ml/jam HCl 0,1N atau dalam praktik sekitar 10 tetes/menit HCl 0,1N dengan
menggunakan infus tetes mikro (60 tetes/ml). Perhitungan laju tetesan infus HCl
0,1 N untuk uji profil netralisasi asam dapat dilihat pada Lampiran 1.
3.7.2 Penentuan Profil Netralisasi Serbuk Al(OH)3, Mg(OH)2 dan Kombinasi Al(OH)3 dan Mg(OH)2
3.7.2.1 Penentuan Profil perubahan pH air versus waktu oleh serbuk Al(OH)3, Mg(OH)2 dan kombinasi Al(OH)3 dan Mg(OH)
Dipipet 30 ml akuades ke dalam wadah sampel, kemudian diatur suhu
medium 37 ± 0,5
2
o
C. Diatur setingan laju tetesan air ke dalam wadah sampel 10
tetes/menit (infus tetes mikro: 60 tetes/ml). Kemudian diukur pH medium dengan
pH meter (sebagai pH awal). Dimasukkan serbuk antasida (Al(OH)3, Mg(OH)2,
dan kombinasi (Al(OH)3 dan Mg(OH)2) ke dalam wadah sampel dan secara
tetes/menit. Kemudian diukur perubahan pH larutan pada 15, 30, 60, 120, 180,
240, 300, 360, 420, 480, 540, 600, 660, dan 720 menit dengan pH meter.
3.7.2.2 Penentuan Profil Netralisasi 30 ml HCl 0,1 N oleh Serbuk Al(OH)3, Mg(OH)2 dan kombinasi Al(OH)3 dan Mg(OH)2
Dipipet 30ml asam klorida 0.1 N ke dalam wadah sampel, kemudian
diatur suhu medium 37 ± 0,5oC. Kemudian diukur pH medium dengan pH meter
(sebagai pH awal). Dimasukkan serbuk antasida (Al(OH)3, Mg(OH)2, dan
kombinasi (Al(OH)3 dan Mg(OH)2) ke dalam wadah sampel dan secara
bersamaan diaduk dengan kecepatan 100 rpm dan laju tetesan HCl 0,1 N dalam
kondisi off. Kemudian diukur perubahan pH larutan pada 15, 30, 60, 120, 180,
240, 300, 360, 420, 480, 540, 600, 660, dan 720 menit dengan pH meter.
3.7.2.3Penentuan Profil Netralisasi HCl 0,1 N oleh serbuk Al(OH)3, Mg(OH)2 dan kombinasi Al(OH)3 dan Mg(OH)2 dalam simulasi sekresi asam lambung (penambahan HCl 0,1 N 10 ml/jam)
Dipipet 30 ml asam klorida 0.1 N ke dalam wadah sampel, kemudian
diatur suhu medium 37 ± 0,5oC. Diatur setingan laju tetesan larutan HCl 0,1 N ke
dalam wadah sampel 10 tetes/menit (infus tetes mikro: 60 tetes/ml). Kemudian
diukur pH medium dengan pH meter (sebagai pH awal). Dimasukkan serbuk
antasida (Al(OH)3, Mg(OH)2, dan kombinasi (Al(OH)3 dan Mg(OH)2) ke dalam
wadah sampel dan secara bersamaan diaduk dengan kecepatan 100 rpm dan
diaktifkan laju tetesan HCl 0,1 N 10 tetes/menit. Kemudian diukur dan dicatat
perubahan pH larutan pada 15, 30, 60, 120, 180, 240, 300, 360, 420, 480, 540,
600, 660, dan 720 menit dengan pH meter. Selanjutnya setiap 2 jam berikutnya
3.7.3 Penentuan Profil Netralisasi Sediaan Film Alginat-Kitosan
3.7.3.1 Penentuan Profil Netralisasi Sediaan Film Alginat-Kitosan dalam Air
Dipipet 30 ml akuades ke dalam wadah sampel, kemudian diatur suhu
medium 37 ± 0,5o
3.7.3.2 Penentuan Profil Netralisasi HCl 0,1 N oleh Sediaan Film Alginat-Kitosan dalam Simulasi Sekresi Asam Lambung (penambahan HCl 0,1 N 10 ml/jam)
C. Diatur setingan laju tetesan air ke dalam wadah sampel 10
tetes/menit (infus tetes mikro: 60 tetes/ml). Kemudian diukur pH medium dengan
pH meter (sebagai pH awal). Dimasukkan kapsul yang mengandung sediaan film
ke dalam wadah sampel dan secara bersamaan diaduk dengan kecepatan 100 rpm
dan diaktifkan laju tetesan air 10 tetes/menit. Kemudian diukur perubahan pH
larutan pada 15, 30, 60, 120, 180, 240, 300, 360, 420, 480, 540, 600, 660, dan 720
menit dengan pH meter.
Dipipet 30 ml asam klorida 0.1 N ke dalam wadah sampel, kemudian
diatur suhu medium 37 ± 0,5oC. Diatur setingan laju tetesan larutan HCl 0,1 N ke
dalam wadah sampel 10 tetes/menit (infus tetes mikro: 60 tetes/ml). Kemudian
diukur pH medium dengan pH meter (sebagai pH awal). Dimasukkan kapsul yang
mengandung sediaan film ke dalam wadah sampel dan secara bersamaan diaduk
dengan kecepatan 100 rpm dan diaktifkan laju tetesan HCl 0,1 N 10 tetes/menit.
Kemudian diukur dan dicatat perubahan pH larutan pada 15, 30, 60, 120, 180,
240, 300, 360, 420, 480, 540, 600, 660, dan 720 menit dengan pH meter.
Selanjutnya setiap 2 jam berikutnya dipipet 20 ml larutan dan dikeluarkan dari