PEMANFAATAN ASAP CAIR TEMPURUNG KELAPA SEBAGAI BAHAN PENGAWET IKAN TERI NASI (Stolephorus
commersonii, Lac.) SEGAR UNTUK TUJUAN TRANSPORTASI
Oleh :
Harun Al Rasyid (F34063508)
2010
FAKULTAS TEKNOLOGI PERTANIAN INSTITUT PERTANIAN BOGOR
PEMANFAATAN ASAP CAIR TEMPURUNG KELAPA SEBAGAI BAHAN PENGAWET IKAN TERI NASI (Stolephorus
commersonii, Lac.) SEGAR UNTUK TUJUAN TRANSPORTASI
SKRIPSI
Sebagai Salah Satu Syarat Untuk Mendapatkan Gelar SARJANA TEKNOLOGI PERTANIAN Pada Departemen Teknologi Industri Pertanian
Fakultas Teknologi Pertanian Institut Pertanian Bogor
Oleh Harun Al Rasyid
F34063508
2010
FAKULTAS TEKNOLOGI PERTANIAN INSTITUT PERTANIAN BOGOR
Judul skripsi : Pemanfaatan Asap Cair Tempurung Kelapa Sebagai Bahan Pengawet Ikan Teri Nasi (Stolephorus Commersonii, Lac.) Segar Untuk Tujuan Transportasi
Nama : Harun Al Rasyid NIM : F34063508
Menyetujui,
Pembimbing I Pembimbing II
Dr. Tatit K. Bunasor, MSc. Dr. Ir. Sapta Raharja, DEA.
NIP. 19480107 197301 2001 NIP. 19631026 199002 1001
Mengetahui, Ketua Departemen Teknologi Industri Pertanian
Prof. Dr. Ir. Nastiti S. Indrasti
NIP. 19621009 198903 2001
Harun Al Rasid F34063508. Pemanfaatan Asap Cair Tempurung Kelapa Sebagai Bahan Pengawet Ikan Teri Nasi (Stolephorus Commersonii, Lac.) Segar Untuk Tujuan Transportasi. Dibawah bimbingan Tatit. K. Bunasor dan Sapta Raharja. 2010.
RINGKASAN
Asap cair merupakan suatu campuran dispersi asap dalam air yang dihasilkan dengan cara destilasi kering bahan baku pengasap seperti kayu, lalu dilanjutkan dengan proses kondensasi. Asap cair berasal dari bahan alami yaitu pembakaran hemiselulosa, selulosa, dan lignin dari kayu-kayu keras sehingga menghasilkan senyawa yang memiliki efek desinfektan, dan antioksidan seperti senyawa asam dan turunannya, alkohol, fenol, aldehid, karbonil, keton, dan piridin. Pemanfaatan asap cair mencakup industri makanan sebagai pengawet, bioinsektisida, dan desinfektan.
Pengangkutan merupakan salah satu proses yang penting dalam penanganan pasca panen. Penanganan ikan yang kurang baik dan tepat selama transportasi (jangka waktu lebih dari 7 hari) akan mempengaruhi kualitas ikan, baik sifat fisik atau kimia pada ikan. Penggunaan es sebagai pengawet ikan memiliki beberapa kelemahan, diantaranya bersifat kamba, jika mencair menambah berat beban angkutan, dan mengurangi sifat tekstur daging ikan. Adanya kelemahan tersebut mendorong penggunaan asap cair sebagai bahan pengawet selama penanganan transportasi.
Penelitian ini bertujuan mengetahui lama jangka waktu pengawetan terhadap ikan teri nasi segar menggunakan asap cair tempurung kelapa selama 9 hari waktu penyimpanan, serta pengaruh penggunaan asap cair sebagai pengawet terhadap sifat fisik dan kimia ikan teri nasi. Pada penelitian ini sebelumnya dilakukan analisa proksimat pada ikan teri nasi segar dan analisis asap cair. Setelah analisis awal, dilakukan proses perendaman dalam asap cair. Faktor-faktor dalam rancangan penelitian ini terdiri atas, (a) konsentrasi asap cair yang digunakan dengan 2 taraf yakni : a1 = 20%, a2 = 30 % dan (b) lama perendaman
dalam asap cair dengan 3 taraf, yakni : b1 = 15 menit, b2 = 30 menit dan b3 = 45
dilanjutkan dengan penyimpanan pada suhu kamar selama 9 hari, diamati tiap 2 hari (hari ke- 1, 3,5, 7 , dan 9). Selama penyimpanan dilakukan pengamatan terhadap kadar air, kadar protein dan uji Total Plate Counts (TPC), kapang dan khamir.
Harun Al Rasid F34063508. Utilization of Coconut Shell Liquid Smoke as Preservative for Fresh Rice Anchovy Fish ( Stolephorus Commersonii, Lac.) For Transportation Purpose. Supervised by Tatit. K. Bunasor and Sapta Raharja. 2010.
SUMMARY
Liquid smoke is a smokes that disperse in water resulted by dry pyrolisation of raw smoked material (such as wood), and next step is processed by condensation. Liquid smoke derive from natural material which is burning of hemicellulose, cellulose, and lignin of hardwoods, with the result that compound has disinfectant and antioxidan effect, like acid compound and derivative compound, alcohol, phenol, aldehyde, carbonil, keton, and piridin. The utilization of liquid Smoke includes the food industry as preservative, bioinsectisida, and disinfectant.
Transportation is one of important process in post-harvest handling. Handling fish unappropriately during the transportation (a period of more than 7 days) will be affect the quality of fish either physically or chemically. The use of ice as fish preservative has some weaknesses, among others requiring a lot of spaces, if the ice melts it will gain the transport burden, and lessen the fish flesh texture. Due to the weaknesses, it encourages the utilization of liquid smoke as preservative during handling the transportation.
The aims of research to find out the long term preservation of fresh rice anchovy fish by using coconut shells liquid smoke for 9 days of storage times, as well as finding out the effect of using liquid smoke as preservative toward the physical and chemical characteristic of fresh rice anchovy fish. At the beginning this research ws carried out by proximate analysis on fresh rice anchovy fish and liquid smoke analysis and also analyzed liquid smoke. After doing both analysis, then is continued by soaking process in liquid smoke. The factors in this observational design consist of, (a ) liquid smoke concentration that utilized by 2 levels namely: a 1 = 20%, a 2 = 30 %, and (b) soaking long times in liquid smoke
with 3 levels, namely: b 1 = 15 minutes, b 2 = 30 minutes and b 3 = 45 minutes.
storaging at the room temperature for 9 days and observed every 2 days (1st day, 3,5, 7, and 9). During the storage, it was observed on water contents, protein rate and Total Plate Counts (TPC) test, mould and khamir.
The result of the research showed that the coconut shells liquid smoke which utilized has good quality with criteria, specific chemical component dominant as phenol broadly area percent 21,55 %, pH 3,29, acid contents 37 %, and phenol content 38 %. Nutrient composition of fresh rice anchovy fish, which is water content 80,39 %, ash rate 3,25 %, fat rate 2,45 %, and protein rate 13,74 %. Based on ANOVA test, it was obtained the best result on liquid smoke concentration 30 % soaking long times 45 minutes which is 0,68 % of phenol content. The preservation process through soaking liquid smoke of fresh rice anchovy fish (Stolephorus commersonii, Lac.), it can keep its freshness until the 9th day. It can be seen from the observation result on protein rate which approaches to assess early protein rate (13,74 %) which is 13,17 %. and microorganism amount that stills at under safe zona according to SNI 02-2725-1992 (BSN, 02-2725-1992), which is totaled microbe 7 x 10² colonies / grams and full scale moulds and khamir 2 x 10² colonies / grams.
SURAT PERNYATAAN
Saya yang bertandatangan di bawah ini menyatakan dengan sebenar-benarnya bahwa skripsi dengan judul “ Pemanfaatan Asap Cair Tempurung Kelapa Sebagai Bahan Pengawet Ikan Teri Nasi (Stolephorus Commersonii, Lac.) Segar Untuk Tujuan Transportasi.” adalah hasil karya asli saya sendiri dengan arahan dosen pembimbing, kecuali dengan jelas ditunjukkan rujukannya.
Bogor, Oktober 2010
Yang Membuat Pernyataan
Harun Al Rasyid
RIWAYAT HIDUP
Penulis yang bernama Harun Al Rasyid dilahirkan di Sumenep pada 19 Maret 1988. Penulis adalah putra keempat dari pasangan Bapak H. Moh Sidqie Dafir dan Ibu Samahah. Riwayat pendidikan penulis dimulai dari Taman Kanak-Kanak Pondok Pesantren Tegal Al-Amien Prenduan Sumenep Madura pada tahun 1994. Selanjutnya, penulis melanjutkan pendidikan di SD Pragaan Laok I pada 1995-2000, SLTPN 2 Pamekasan 2000-2003, dan SMAN 1 Pamekasan 2003-2006. Penulis melanjutkan studinya di perguruan tinggi IPB melalui USMI (Undangan Seleksi Masuk IPB) pada 2006.
Selama menjalani studi di IPB penulis aktif di organisasi BEM Fateta IPB Departermen Polkastrat 2008, FBI Fateta Divisi Syiar 2008, dan DKM Alhurriyah IPB 2007. Selain itu, penulis juga aktif dalam kegiatan mengajar tingkat SD, SMP, dan SMA di Bimbingan Belajar Primagama 2009 dan Nurul Fikri 2010.
KATA PENGANTAR
Segala puji bagi Allah yang menciptakan akal, penglihatan, pendengaran sehingga penulis diberikan kemudahan dalam menyelesaikan sebuah karya ilmiah yang berjudul “Pemanfaatan Asap Cair Tempurung Kelapa Sebagai Bahan Pengawet Ikan Teri Nasi (Stolephorus Commersonii, Lac.) Untuk Tujuan Transportasi” ini. Sudah seharusnya orang yang beriman dan berilmu senantiasa berpikir dan menuliskan apa yang disaksikannya atas penciptaan langit dan bumi. Sebagaimana firman Allah surat Al-A’limran ayat 190-191:
“Sesungguhnya dalam penciptaan langit dan bumi, dan silih bergantinya malam dan siang terdapat tanda-tanda bagi orang-orang yang berakal, (yaitu) orang-orang yang mengingat Allah sambil berdiri atau duduk atau dalam keadan berbaring dan mereka memikirkan tentang penciptaan langit dan bumi (seraya berkata): "Ya Tuhan Kami, Tiadalah Engkau menciptakan ini dengan sia-sia, Maha suci Engkau, Maka peliharalah Kami dari siksa neraka”.
Selain itu, penulis menyadari bahwa karya tulis ini berhasil dengan dukungan dan bantuan semua pihak baik secara moril maupun spiritual. Oleh karena itu, dalam kesempatan ini penulis mengucapkan banyak terima kasih kepada :
1. Dr. Tatit K. Bunasor, MSc sebagai dosen pembimbing I atas bimbingan dan arahannya dalam bidang akademik selama masa studi di IPB, khususnya selama pelaksanaan kegiatan penelitian dan penulisan tugas akhir (skripsi).
2. Dr. Sapta Raharja, DEA sebagai dosen pembimbing II yang telah memberikan banyak masukan serta saran selama penulis melaksanakan penelitian dan penulisan skripsi.
3. Dr. Ir. Mulyorini Rahayuningsih, M.Si sebagai dosen penguji yang telah memberikan masukan serta saran dalam penulisan tugas akhir (skripsi). 4. Keluarga tercinta : Ayahanda Moh. Sidqie Dafir, Ibunda Samahah,
memberikan dukungan spiritual, semangat, dan kasih sayangnya kepada penulis sehingga penulis dapat menyelesaikan studi di IPB dengan lancar.. 5. Keluarga besar “Rumah Tercinta”, Agroindustrialist Mounteners, teman-
TIN 43 jaya, khususnya Eko Prames Swara, Cucu Rina Purwaningrum, dan Sidik Ardhi Irawan yang telah memberikan saran kritik, dukungan dan semangat kepada penulis untuk menyelesaikan skripsi ini.
6. Seluruh Staf laboratorium Teknologi Industri Pertanian, khususnya Bapak Edi Sumantri dan Ibu Egnawati Sari yang telah memberikan bantuan moril sehingga penulis dimudahkan dalam menyelesaikan penelitian.
7. Seluruh pihak yang turut membantu suksesnya kegiatan serta penyusunan laporan tugas akhir ini.
Dalam pelaksanaan penelitian ataupun dalam penyusunan laporan skripsi ini, penulis menyadari bahwa masih banyak terdapat kekurangan. Penulis menerima segala masukan yang bermanfaat terutama untuk kegiatan penelitian di masa yang akan datang.
Demikianlah laporan skripsi ini dibuat, semoga berkenan, dan dapat digunakan sebagaimana mestinya.
Bogor, Oktober 2010
i
DAFTAR ISI
Hal
DAFTAR ISI……….i
DAFTAR TABEL………...iii
DAFTAR GAMBAR………..iv
DAFTAR LAMPIRAN………v
I. PENDAHULUAN………...1
A. LATAR BELAKANG ... 1
B. TUJUAN ... 2
II. TINJAUAN PUSTAKA………3
A. ASAP CAIR ... 3
B. KOMPONEN ASAP CAIR TEMPURUNG KELAPA ... 4
C. KEAMANAN PANGAN ASAP CAIR TEMPURUNG KELAPA ... 6
D. PENGAWETAN DENGAN ASAP CAIR ... 7
E. AKTIVITAS ANTIMIKROBA ASAP CAIR ... 9
F. PEMURNIAN ASAP CAIR DENGAN DESTILASI ... 10
G. IKAN TERI NASI (Stolephorus commersonii, Lac.) ... 10
G. TRANSPORTASI………13
III. METODOLOGI PENELITIAN………...14
A. BAHAN DAN ALAT ... 14
1. Bahan………..14
2. Alat………..14
B. METODE PENELITIAN ... 14
1. Penelitian pendahuluan………...14
ii
IV. HASIL DAN PEMBAHASAN………..17
A. ANALISIS ASAP CAIR TEMPURUNG KELAPA ... 17
1. Komponen spesifik pada asap cair………..17
2. Nilai pH………...18
3. Kadar asam………..19
4. Kadar fenol………..21
B. ANALISIS IKAN TERI NASI (Stolephorus commersonii, Lac.) SEGAR ... 22
C. PROSES PERENDAMAN (ANALISIS KADAR FENOL) ... 24
D. ANALISIS SELAMA PENYIMPANAN SUHU RUANG………27
1. Analisis kadar air………..27
2. Analisis mikrobiologi………..29
3. Analisis kadar protein……….33
V. KESIMPULAN DAN SARAN………...36
A. KESIMPULAN…………...36
B. SARAN…………...36
DAFTAR PUSTAKA………....37
LAMPIRAN………...43
iii
DAFTAR TABEL
Hal
Tabel 1. Komposisi kimia tempurung kelapa………...4
Tabel 2. Klasifikasi tingkat toksisitas zat kimia berdasarkan nilai LD50…………7
Tabel 3. Komposisi kimia ikan teri segar………...12
Tabel 4. Senyawa dominan asap cair hasil deteksi GC-MS………...17
Tabel 5. Hasil analisa proksimat ikan teri nasi………...22
Tabel 6. Hasil analisa proksimat Hardinsyah dan Briawan (1990)………23
Tabel 7. Hasil uji jumlah total mikroba awal ikan teri nasi ………..24
Tabel 8. Nilai rata-rata kadar fenol ikan teri setelah direndam dalam asap cair…25 Tabel 9. Nilai rata-rata kadar air selama penyimpanan………..27
Tabel10.Nilai rata-rata TPC ikan teri nasi selama penyimpanan………...30
Tabel11. Nilai rata-rata jumlah kapang dan khamir selama penyimpanan………32
iv
DAFTAR GAMBAR
Hal Gambar 1. Diagram alir metode penelitian………16
Gambar 2. Histogram senyawa dominan asap cair tempurung kelapa…………..18
Gambar 3. Formulasi produksi asam asetat………...20
Gambar 4. Histogram hasil uji kandungan gizi ikan teri nasi………63
Gambar 5. Nilai rata-rata kadar fenol setelah direndam dalam asap cair………..63
Gambar 6. Histogram nilai rata-rata kadar air selama penyimpanan……….64
Gambar 7. Histogram nilai rata-rata total bakteri selama penyimpanan…………64
Gambar 8. Histogram nilai rata-rata kapang dan khamir selama penyimpanan…65
Gambar 9. Histogram nilai rata-rata kadar protein selama penyimpanan………..65
Gambar10.Gambar ikan teri nasi segar………..66
v
DAFTAR LAMPIRAN
Hal
Lampiran 1. Prosedur analisis asap cair tempurung kelapa………...44
Lampiran 2. Prosedur analisis proksimat dan uji kesegaran ikan teri nasi………46
Lampiran 3. Hasil lengkap senyawa dominan asap cair GC-MS………..49
Lampiran 4. Penentuan kadar asam dan kadar fenol……….55
Lampiran 5. Uji ANOVA dan Uji Lanjut beda nyata jujur………...56
Lampiran 6. Data standar fenol……….58
Lampiran 7. Data mentah kadar fenol proses perendaman………...59
Lampiran 8. Data mentah kadar air selama penyimpanan………....61
Lampiran 9. Data mentah kadar protein selama penyimpanan……….62
Lampiran10. Histogram nilai gizi dan nilai rata-rata kadar fenol………..63
Lampiran11. Histogram nilai rata-rata kadar air dan total bakteri……….64
Lampiran12. Histogram nilia total kapang, khamir dan kadar air……….65
I. PENDAHULUAN
A. LATAR BELAKANG
Kelapa sawit merupakan tanaman komoditas perkebunan yang cukup
penting di Indonesia dan masih memiliki prospek pengembangan yang cukup
cerah. Komoditas kelapa sawit, baik berupa bahan mentah maupun hasil
olahannya, menduduki peringkat ketiga penyumbang devisa nonmigas terbesar
bagi Indonesia setelah karet dan kopi.
Salah satu produk olahan kelapa sawit yang terpenting adalah minyak.
Realisasi produksi minyak sawit mentah (Crude Palm Oil/CPO) pada 2009 mencapai 21.5 juta ton menjadikan Indonesia sebagai produsen pertama terbesar
di dunia dengan ekspor mencapai 16 juta ton. Menurut Daud J. Dharsono, seorang
direktur utama salah satu perusahaan besar di Indonesia yang bergerak dibidang
agronomi memprediksi, produksi CPO nasional tahun 2010 dapat mencapai 22.5
juta ton. Menurutnya, dari 22.5 juta ton tersebut sekitar 17 juta ton akan diekspor
ke berbagai negara, sedangkan untuk konsumsi dalam negeri hanya 7.5 ton, yang
sebagian besar diproduksi dalam bentuk minyak goreng. Faktor yang mendorong
peningkatan volume produksi tersebut adalah bertambahnya luas areal perkebunan
kelapa sawit dan besarnya kebutuhan bahan baku untuk produk turunan CPO
(Pelita, 2010).
Minyak sawit memiliki sejarah yang panjang sebagai bahan pangan yang
aman untuk dikonsumsi manusia. Berbagai kegunaan atau aplikasi CPO (crude palm oil) dari minyak kelapa sawit antara lain adalah sebagai bahan dasar untuk minyak goreng, lemaknya sebagai bahan shortening (pelunak atau perenyah makanan), dan sebagai bahan dasar dalam pembuatan produk margarin (Kosasih
dan Harsono, 1991). CPO dapat pula diolah menjadi minyak sawit merah (MSM)
yang kaya akan karotenoid, yaitu melalui serangkaian proses pemurnian, tanpa
proses penghilangan pigmen (bleaching), kemudian difraksinasi dan diambil fraksi cairnya (olein).
MSM memiliki nilai gizi yang baik akibat tingginya kandungan karotenoid
di dalamnya yang berkisar antara 500-700 µg/g dan lebih dari 80% dalam bentuk
α, β, γ- karoten (Choo et al., 1989). Komponen ini memiliki banyak kegunaan
bagi kesehatan manusia antara lain sebagai komponen vitamin, senyawa
antikanker, mencegah penuaan dini, penyakit kardiovaskuler, dan kegunaan
lainnya. Selain jumlah karoten yang tinggi, minyak sawit merah juga mengandung
senyawa tokoferol berkisar antara 600-1000 µg/g (Muchtadi, 1992). Kandungan
karoten pada minyak sawit merah dapat dieksploitasi untuk produk minyak kaya
karoten atau konsentrat karoten. Produk karoten banyak digunakan pada produk
pangan sebagai sumber vitamin A maupun sebagai zat warna.
Meskipun karoten mempunyai banyak aktivitas yang penting bagi
kesehatan, senyawa ini memiliki sifat yang sensitif terhadap cahaya dan oksigen
(Nawar, 1996). Oleh karena itu diperlukan upaya untuk melindungi senyawa
tersebut dari lingkungan sekitarnya yang dapat menyebabkan terjadinya reaksi
oksidasi. Salah satu upaya yang dapat dilakukan adalah dengan cara
melindunginya dalam matriks polimer yang disebut dengan proses
mikroenkapsulasi.
Mikroenkapsulasi adalah suatu proses dimana bahan-bahan inti yang
berbentuk cair atau padat dilapisi dengan film tipis dari suatu bahan pengkapsul
khusus (Young et al., 1993). Teknologi enkapsulasi telah berkembang dan digunakan diberbagai industri farmasi, kimia, kosmetik, pangan, dan percetakan.
Produk pangan seperti, lemak dan minyak, komponen flavor dan oleoresin, vitamin,
mineral, pewarna dan enzim telah menggunakan teknologi ini (Madene et al., 2006). Oleh karena itu, proses mikroenkapsulasi MSM ini diharapkan dapat menghasilkan
produk berupa bubuk kering dengan kandungan karoten tinggi dan stabilitas yang
jauh lebih baik dibandingkan dengan penyimpanan dalam bentuk cair.
Teknik mikroenkapsulasi yang dipilih adalah teknik spray drying. Ciri khas dari penggunaan alat spray dryer adalah siklus pengeringannya yang cepat, retensi dalam ruang pengering singkat dan produk akhir siap dikemas ketika selesai
proses (Heldman et al., 1981). Efektivitas mikroenkapsulasi dengan teknik spray drying sangat tergantung pada bahan penyalut yang digunakan.
Bahan penyalut yang digunakan pada penelitian ini adalah kombinasi
antara maltodekstrin dan natrium kaseinat. Maltodekstrin (MD) merupakan
produk hidrolisat pati yang dapat memberikan stabilitas terhadap oksigen yang
baik untuk enkapsulasi minyak tetapi memiliki kapasitas dan stabilitas
emulsifikasi yang lemah dan retensi minyak yang rendah (Kenyon, 1995). Untuk
itu biasanya maltodekstrin dikombinasikan dengan bahan lain seperti gum arab,
protein, atau pati termodifikasi lainnya untuk keperluan stabilitas emulsi (Kenyon
dan Anderson, 1988). Natrium kaseinat (NaCas) merupakan suatu senyawa
protein yang potensial jika digunakan sebagai bahan penyalut. Menurut Dalgleish
(2001), kasein bersifat hidrofolik dan hidrofobik menjadikan kasein baik sebagai
bahan pengemulsi, mampu bertindak sebagai surfaktan karena dapat membentuk
lapisan penstabil yang meluas di sekeliling droplet emulsi. Pengkombinasian
kedua bahan penyalut ini didasarkan atas sifat-sifat bahan penyalut tersebut yang
tidak memiliki kemampuan sempurna jika digunakan secara tunggal.
Pada beberapa kasus, bahan penyalut yang mengandung protein dan
karbohidrat menghasilkan produk dengan daya alir dan karakteristik rehidrasi
yang baik. Peningkatan stabilitas oksidasi juga terjadi pada minyak yang
dienkapsulasi dalam matriks protein-karbohidrat (Lin et al., 1995).
Maltodekstrin memiliki harga yang cukup murah dan banyak tersedia di
pasaran. Sementara itu, harga natrium kaseinat cukup mahal dan ketersediaannya
di pasaran cukup jarang. Oleh karena itu, penggunaan bahan-bahan
pengenkapsulasi ini sangat perlu untuk dikombinasikan secara efektif.
Produk mikroenkapsulat MSM ini dapat digunakan sebagai food ingredient, yaitu sebagai sumber provitamin A yang dapat digunakan pada proses fortifikasi
produk pangan. Selain itu, produk ini dapat juga dimanfaatkan sebagai pewarna
alami kuning. Sifatnya yang larut air sangat memudahkan aplikasi pada berbagai
produk pangan seperti minuman ringan, ice cream, desserts, permen, sup, produk daging, dan lain-lain.
B. TUJUAN PENELITIAN
Penelitian ini bertujuan untuk mendapatkan formula mikroenkapsulat
MSM yang optimum dengan kombinasi konsentrasi dari bahan penyalut
maltodekstrin dan natrium kaseinat sehingga dapat mempertahankan karoten
dalam MSM dengan stabilitas yang tinggi menggunakan teknik spray drying.
4 II. TINJAUAN PUSTAKA
A. MINYAK KELAPA SAWIT
Minyak kelapa sawit berasal dari ekstraksi buah tanaman kelapa sawit.
Kelapa sawit menghasilkan dua macam minyak, yaitu minyak inti sawit (Palm
Kernel Oil) yang diperoleh dari inti kelapa sawit dan minyak sawit kasar (Crude
Palm Oil) yang diperoleh dari serabut (mesokarp) kelapa sawit (Ketaren, 1986).
Buah kelapa sawit yang digunakan untuk menghasilkan minyak adalah bagian
luar dari daging buah yang dipanaskan menggunakan uap agar enzim lipolitiknya
inaktif, selanjutnya ditekan dan diperas sehingga menghasilkan minyak sawit
kasar (CPO). CPO yang didapatkan mempunyai tingkat warna merah yang tinggi
akibat adanya karoten. Buah sawit dapat dilihat pada Gambar 1.
Gambar 1. Buah sawit (Lim, 2002)
CPO memiliki sifat-sifat yang berbeda dengan minyak inti sawit, yaitu
minyak sawit kasar bersifat setengah padat pada suhu ruang dan memiliki pigmen
karotenoid yang berwarna jingga-kemerahan sedangkan minyak inti sawit bersifat
cair pada suhu ruang dan tidak mengandung karotenoid (Muchtadi, 1992).
Perbedaaan ini disebabkan oleh perbedaan jenis dan jumlah rantai asam lemak
yang membentuk trigliserida dalam kedua minyak tersebut (Ong et al., 1990).
Minyak sawit memiliki dua komponen asam lemak yang terbesar, yaitu
asam palmitat dan asam oleat. Asam palmitat (C16:0) merupakan asam lemak
jenuh rantai panjang yang memiliki titik cair (melting point) yang tinggi, yaitu
64°C. Kandungan asam palmitat yang tinggi ini membuat minyak sawit lebih
tahan terhadap oksidasi (ketengikan) dibanding jenis minyak lain. Asam oleat
(C18:1) merupakan asam lemak tidak jenuh rantai panjang dengan panjang rantai
C18 dan memiliki satu ikatan rangkap. Titik cair asam oleat lebih rendah dibanding
5 asam palmitat, yaitu 14°C (Ketaren, 1986). Komposisi asam lemak pada minyak
sawit dapat dilihat pada Tabel 1.
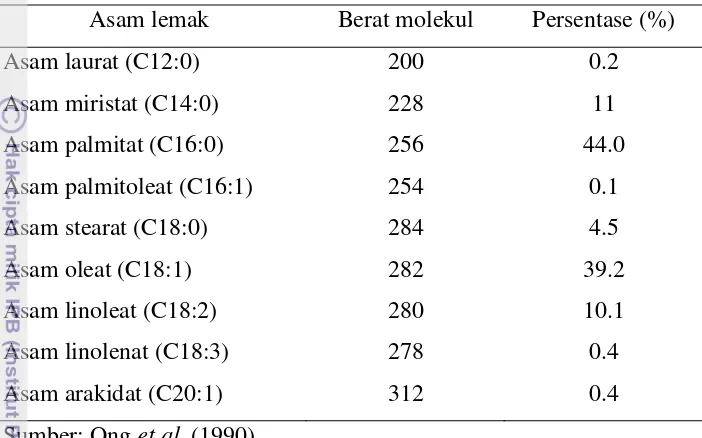
Tabel 1. Komposisi asam lemak pada minyak sawit
Asam lemak Berat molekul Persentase (%)
Asam laurat (C12:0) 200 0.2
Asam miristat (C14:0) 228 11
Asam palmitat (C16:0) 256 44.0
Asam palmitoleat (C16:1) 254 0.1
Asam stearat (C18:0) 284 4.5
Asam oleat (C18:1) 282 39.2
Asam linoleat (C18:2) 280 10.1
Asam linolenat (C18:3) 278 0.4
Asam arakidat (C20:1) 312 0.4
Sumber: Ong et al. (1990)
Selain mengandung asam-asam lemak, CPO juga mengandung lebih
kurang 1% komponen minor yang terdiri dari karotenoid, tokoferol, tokotrienol,
sterol, fosfolipid, glikolipid, terpen, gugus hidrokarbon alifatik, dan kotoran.
Komponen terbesar dari karotenoid yang terdapat dalam CPO adalah β-karoten
(56%) dan α-karoten (35%) (Gee, 2007). Komposisi komponen-komponen minor
dalam CPO secara lebih rinci dapat dilihat pada Tabel 2.
Pada umumnya, pemanfaatan minyak sawit masih didominasi untuk
produk pangan. Sekitar 90% minyak sawit digunakan untuk produk-produk
pangan seperti minyak goreng, minyak salad, margarin, shortening, vanaspati, dan
sebagainya, sedangkan sisanya (10%) digunakan untuk produk-produk nonpangan
6 Tabel 2. Komponen minor dalam CPO
Komponen minor Kandungan (ppm)
Karotenoid 500-700
Tokoferol dan tokotrienol 600-1000
Sterol 326-627
Fosfolipid 5-130
Triterpen alkohol 40-80
Metil sterol 40-80
Squalen 200-500
Dolikol dan poliprenol 81
Hidrokarbon
Non-terpenoid hidrokarbon
Ubiquinon
50
30-50
10-80
Sumber: Gee (2007)
B. MINYAK SAWIT MERAH
Minyak sawit fraksi cair (olein) merupakan hasil fraksinasi minyak kelapa
sawit yang berwarna jingga kemerahan yang disebut minyak sawit merah (MSM).
Minyak kelapa sawit berbentuk semi solid pada suhu 30°C tetapi dengan melalui
proses fraksinasi, minyak kelapa sawit dapat terpisah menjadi dua fraksi, yaitu
fraksi padat yang disebut stearin dan fraksi cair yang disebut olein dengan rasio
3:7 (Ong et al., 1990). Kandungan karetonoid dalam fraksi olein dapat meningkat
10-20% (Choo et al., 1989). Kandungan karotenoid pada berbagai fraksi minyak
sawit dapat dilihat pada Tabel 3.
Tabel 3. Kandungan karotenoid pada berbagai fraksi minyak sawit
Fraksi minyak sawit Kandungan karotenoid (ppm)
CPO (Crude Palm Oil) 630-700
Crude Palm Olein 680-760
Crude Palm Stearin 380-540
Residual Oil from Fibre 4000-6000
Second-pressed Oil 1800-2400
7 Secara umum, pembuatan MSM hampir serupa dengan produksi minyak
goreng, yaitu melalui serangkaian proses pemurnian CPO (Argha, 2008). Proses
pemurnian CPO ini biasanya terdiri dari tahap degumming, neutralizing,
bleaching, dan deodorizing (Anderson, 1996). Pada proses pemurnian CPO
terkadang satu atau lebih dari tahapan proses tersebut tidak perlu dilakukan,
tergantung dari tujuan jenis minyak yang diinginkan. Untuk mendapatkan MSM,
proses bleaching tidak dilakukan dengan maksud untuk mempertahankan karoten
secara maksimal (Riyadi, 2009).
Proses degumming dilakukan untuk memisahkan getah atau lendir yang
terdapat pada CPO tanpa mereduksi asam lemak bebas yang ada (Hodgson, 1996).
Kemudian dilakukan proses netralisasi (deasidifikasi), yaitu proses penetralan
asam lemak bebas dalam CPO menggunakan suatu alkali (Anderson, 1996).
Degumming perlu dilakukan sebelum proses netralisasi, sebab sabun yang
terbentuk dari hasil reaksi asam lemak bebas dengan alkali pada proses netralisasi
akan menyerap gum (getah atau lendir) sehingga menghambat proses pemisahan
sabun dari minyak (Ketaren, 2005). Widarta (2008) melakukan proses degumming
dengan memanaskan CPO hingga suhu 80°C, kemudian ditambahkan larutan
asam fosfat 85% sebanyak 0.15% dari berat CPO sambil diaduk perlahan (56 rpm)
selama 15 menit. Setelah proses degumming, didapatkan kondisi optimum untuk
proses deasidifikasi, yaitu pada suhu 61 ± 2°C selama 26 menit dengan
penambahan larutan NaOH konsentrasi 16°Be. Dari tahap ini didapatkanlah
NRPO (neutralized red palm oil).
Selanjutnya NRPO yang dihasilkan kembali diproses untuk
menghilangkan komponen volatil yang menimbulkan bau pada minyak
(Anderson, 1996). Penelitian yang dilakukan oleh Riyadi (2009) mendapatkan
hasil bahwa proses deodorisasi NRPO yang optimum dilakukan dengan
menghomogenisasikan NRPO dalam tangki deodorizer selama 10 menit pada
suhu 46 ± 2°C kemudian dipanaskan dalam kondisi vakum hingga suhu 140°C
selama 1 jam dan laju alir N2 dijaga konstan pada 20 L/jam. Lalu dilakukan
pendinginan sampai suhu 60°C pada kondisi vakum, maka dihasilkanlah NDRPO
8 NDRPO yang telah diperoleh masih mengandung fraksi olein dan fraksi
stearin. Oleh karena itu diperlukan proses pemisahan fraksi cair dan padatan agar
diperoleh MSM yang diinginkan. Pemisahan dilakukan dengan cara peningkatan
suhu sampai 50°C dan penurunan suhu secara perlahan-lahan hingga tercapai suhu
kamar sambil diagitasi. Pada suhu kamar terjadi kristalisasi fraksi stearin sehingga
fraksi olein yang masih bersifat cair dapat diperoleh dengan penyaringan vakum
(Weiss, 1983).
Proses pengolahan minyak sawit kaya karotenoid, yaitu MSM mulai
dikembangkan sejak tahun 1990-an, sejalan dengan semakin disadarinya peran
penting karotenoid bagi kesehatan manusia. Menurut Muchtadi (1992), berbeda
dengan minyak sawit, minyak sawit merah tidak dianjurkan untuk digunakan
sebagi minyak goreng, karoten yang terkandung di dalamnya mudah rusak pada
suhu tinggi. Minyak ini lebih dianjurkan untuk digunakan sebagai minyak makan
dalam menumis sayur, minyak salad, dan bahan fortifikan.
C. KAROTENOID
Karotenoid merupakan kelompok pigmen yang berwarna kuning, jingga,
merah jingga yang larut dalam minyak serta tersebar luas di alam (Meyer, 1982).
Karotenoid secara umum dideskripsikan sebagai struktur alifatik, alifatik-alisiklik,
atau aromatik yang terdiri dari lima karbon unit isoprena, umumnya delapan,
dimana kedua gugus metil yang dekat pada molekul pusat terletak pada posisi C-1
dan C-6, sedangkan gugus metil lainnya terletak pada posisi C-1 dan C-5. Definisi
lainnya, yaitu satu seri ikatan ganda terkonjugasi yang membentuk sistem
kromofor (Klaui dan Bauernfeind, 1981). Struktur isoprena dapat dilihat pada
Gambar 2.
Gambar 2. Struktur isoprena (Evens, 2008)
Menurut Nawar (1996), karotenoid adalah pigmen yang hanya dapat
9 stabil pada kondisi alaminya namun menjadi labil jika diekstrak atau dipanaskan.
Pigmen ini juga sensitif terhadap cahaya dan oksigen. Oksidasi pigmen ini dipicu
oleh adanya hidroperoksida hasil oksidasi lemak yang mengakibatkan terjadinya
diskolorasi (bleaching).
Berdasarkan unsur-unsur penyusunnya, karotenoid dibagi menjadi dua
golongan utama, yaitu 1) golongan karoten yang tersusun dari unsur-unsur atom C
dan H, seperti α-karoten, β-karoten, γ-karoten, dan likopen, 2) golongan
oksikaroten atau xantofil yang tersusun oleh unsur-unsur C, H, dan OH seperti
lutein, violasantin, neosamtin, zeasantin, kriptosantin, kapsantin, dan torulahordin
(Nawar, 1996). Berdasarkan fungsinya karotenoid dapat dibagi atas dua golongan,
yaitu yang bersifat nutrisi aktif seperti β-karoten dan non nutrisi aktif seperti
fukosantin, neosantin, dan violasantin. (Klaui dan Bauernfeind, 1981). Struktur
kimia beberapa karoten dapat dilihat pada Gambar 3.
Gambar 3. Struktur kimia beberapa karotenoid (Barbosa-Filhoet al., 2008)
Komponen karotenoid larut dalam pelarut non polar seperti heksana dan
10 alkohol (Gross, 1991). Menurut Meyer (1982) karotenoid memiliki beberapa sifat
fisika dan kimia antara lain larut dalam minyak dan tidak larut dalam air, larut
dalam kloroform, benzena, karbon disulfida, dan petroleum eter, tidak larut dalam
etanol dan methanol dingin, tahan terhadap panas apabila dalam keadaan vakum,
peka terhadap oksidasi, autooksidasi, dan cahaya, mempunyai ciri khas absorpsi
cahaya.
CPO merupakan sumber alami yang kaya akan karotenoid dan tokotrienol.
Karotenoid (500-700 ppm) bertanggung jawab terhadap karakteristik warna jingga
kemerahan dari CPO (Gee, 2007). Kadar karotenoid tersebut bervariasi
bergantung tingkat kematangan dan genotip dari buah. Secara umum minyak yang
berasal dari buah sawit yang berwarna merah lebih banyak mengandung
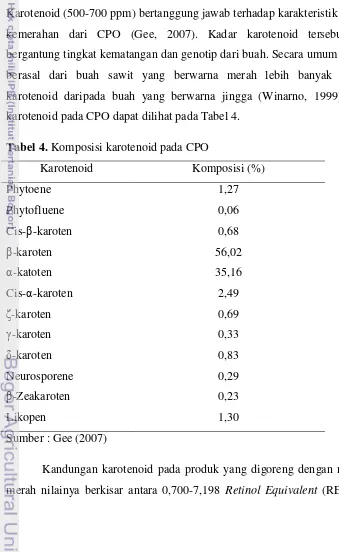
karotenoid daripada buah yang berwarna jingga (Winarno, 1999). Komposisi
karotenoid pada CPO dapat dilihat pada Tabel 4.
Tabel 4. Komposisi karotenoid pada CPO
Karotenoid Komposisi (%)
Phytoene 1,27
Phytofluene 0,06
Cis-β-karoten 0,68
β-karoten 56,02
α-katoten 35,16
Cis-α-karoten 2,49
ζ-karoten 0,69
γ-karoten 0,33
δ-karoten 0,83
Neurosporene 0,29
β-Zeakaroten 0,23
Likopen 1,30
Sumber : Gee (2007)
Kandungan karotenoid pada produk yang digoreng dengan minyak sawit
11 Nilai ini sangat kecil bila dibandingkan dengan kebutuhan vitamin A per hari per
orang, yaitu sebesar 350-600 RE vitamin A (Nurdini, 1997).
Manfaat kesehatan dan nutrisi dari kandungan karotenoid dalam minyak
sawit merah telah diteliti oleh banyak ahli. Beberapa contohnya adalah mencegah
atau memperbaiki kondisi kekurangan vitamin A, menjadi agen pelindung pada
beberapa penyakit kulit akibat cahaya (Mathews-Roth, 1981), dan mengurangi
resiko kanker paru-paru (Kitts, 1996).
D. MIKROENKAPSULASI
Mikroenkapsulasi adalah suatu teknik dimana komponen aktif yang
berbentuk padat, cair, atau gas dibungkus dengan suatu bahan penyalut yang
berfungsi untuk melindungi komponen aktif tersebut dari lingkungan sekitarnya
(Dubey et al., 2009). Komponen aktif yang disalut disebut sebagai bahan inti,
sedangkan bahan yang menyelimuti bahan inti disebut dinding, film pelindung
atau, pengkapsul yang berguna melindungi inti dari kerusakan dan melepas inti
pada kondisi yang diinginkan (Young et al., 1993). Teknik ini telah banyak
digunakan pada berbagai bidang dari bidang kimia dan farmasi sampai pada
bidang kosmetik dan percetakan. Oleh karena itu, minat dunia akan teknologi
mikroenkapsulasi berkembang pesat (Dubey et al., 2009).
Menurut Madene et al. (2006), ukuran mikrokapsul dapat berkisar antara
1-2000 µm yang bergantung pada metode mikroenkapsulasi yang digunakan.
Begitu juga dengan Gharsallaoui et al. (2007) dan Dubey et al. (2009)
menyatakan bahwa diameter rata-rata dari mikroenkapsulat berada pada kisaran
satu hingga ribuan mikrometer (beberapa millimeter).
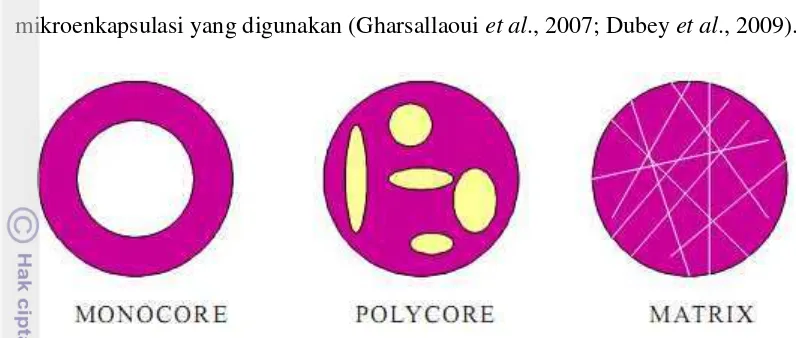
Berdasarkan morfologinya, mikroenkapsulat dapat diklasifikasikan ke
dalam tiga kategori dasar, yaitu monocore, polycore, dan matrix seperti yang
dapat dilihat pada Gambar 4. Mikroenkapsulat monocore mempunyai sebuah
ruang berongga di dalam kapsul. Mikroenkapsulat polycore mempunyai sejumlah
ruang di dalam kapsul dengan ukuran yang berbeda-beda. Mikroenkapsulat jenis
matrix mempunyai komponen aktif terintegrasi di dalam matriks bahan
12 terbentuk bergantung pada jenis bahan inti, jenis bahan pengkapsul dan metode
mikroenkapsulasi yang digunakan (Gharsallaoui et al., 2007; Dubey et al., 2009).
Gambar 4. Morfologi dari berbagai tipe mikroenkapsul (Dubey et al., 2009).
Bakan (1973) mengemukakan bahwa proses mikroenkapsulasi secara
umum melalui tiga tahap dalam suatu pengadukan yang sinambung, yaitu:
a. Bentuk tiga fase kimia yang belum saling bercampur, yaitu fase pembawa
(air), fase material inti yang akan dilapisi dan fase pengkapsul,
b. Penempelan bahan pengkapsul pada permukaan bahan inti. Umumnya tahapan
ini terjadi karena bahan pengkapsul diadsorbsikan pada antar permukaan yang
terbentuk antara materi inti dan bahan cair,
c. Pemadatan pelapis untuk membentuk mikroenkapsul yang biasanya terjadi
akibat adanya panas.
Menurut Dubey et al. (2009), terdapat banyak metode untuk proses
mikroenkapsulasi yang telah dilaporkan tetapi secara umum metode-metode
tersebut dapat dikelompokan ke dalam dua kategori utama, yaitu metode kimia
dan metode fisik/mekanik. Yang termasuk dalam metode kimia antara lain
polimerisasi suspensi, polimerisasi emulsi, dispersi, dan polikondensasi
permukaan. Sedangkan menurut Gouin (2004), yang termasuk dalam metode
fisik/mekanik antara lain spray drying, spray chilling/cooling, extrusion coating,
fluidized bed coating, liposome entrapment, coacervation, inclusion
complexation, centrifugal extrusion, rotational suspension separation, dan
lain-lain.
Keberhasilan suatu mikroenkapsulasi dan sifat mikroenkapsul yang
dihasilkan dipengaruhi oleh parameter-parameter penting, di antaranya (Deasy,
13 a. Bahan inti yang disalut, yaitu berwujud padat atau cair ; sifat fisikokimia
seperti kelarutan, hidrofobik atau hidrofilik, stabilitas terhadap suhu, dan pH,
b. Bahan pengkapsul yang digunakan,
c. Medium mikroenkapsulasi yang digunakan (pelarut air atau bukan air),
d. Prinsip proses mikroenkapsulasi yang digunakan (fisika atau kimia),
e. Tahapan proses mikroenkapsulasi (tunggal atau bertahap),
f. Struktur dinding mikroenkapsul (tunggal atau berlapis).
Berdasarkan penelitian yang dilakukan oleh Hogan et al. (2001),
mikroenkapsulasi minyak kedelai dengan rasio natrium kaseinat:karbohidrat
sebesar ≥1:19 memberikan karakteristik mikroenkapsulasi terbaik. Hal ini
disebabkan oleh pembentukan mikroenkapsulat yang bergantung pada rasio
core/wall dan rasio antar bahan penyalut yang digunakan Penelitian lain yang
dilakukan oleh Dian et al. (1996), menyatakan bahwa kombinasi
maltodekstrin:natium kaseinat dengan rasio 4:1 telah memberikan hasil
mikroenkapsulat yang lebih baik dibanding kombinasi maltodekstrin:gum akasia
untuk bahan inti berbasis minyak sawit.
Bahan-bahan penyalut yang digunakan untuk keperluan mikroenkapsulasi
telah dipilih untuk memastikan bahwa bahan-bahan inti di dalamnya tidak akan
dipengaruhi oleh lingkungannya. Beberapa alasan penting dilakukannya
enkapsulasi antara lain konversi bahan cair menjadi padatan yang memiliki
kemampuan mengalir, meningkatkan stabilitas (melindungi bahan inti dari
oksidasi/deaktivasi akibat bereaksi dengan lingkungan), menutupi bau, rasa, dan
aktivitas bahan inti, mengontrol pelepasan dari komponen aktif (memelihara atau
menunda pelepasan, dan menargetkan waktu/kondisi pelepasan bahan inti (Dubey
et al., 2009).
E. BAHAN PENYALUT
Pada proses mikroenkapsulasi, terdapat dua bahan yang terlibat di
dalamnya, yaitu inti dan penyalut. Inti adalah zat yang akan disalut. Zat ini
umumnya berbentuk padat, gas, atau cair yang mempunyai sifat permukaan
hidrofil atau hidrofob (Dubey et al., 2009). Beta karoten dari minyak sawit merah
14 Penyalut adalah zat yang digunakan untuk menyelaputi inti dengan tujuan
tertentu. Menurut Gharsallaoui et al. (2007), struktur dinding dari bahan penyalut
dirancang untuk melindungi bahan inti dari faktor-faktor yang dapat menyebabkan
kerusakan, mencegah terjadinya interaksi antara bahan inti dengan komponen lain,
membatasi kehilangan komponen volatil, dan juga mengontrol atau menjaga
pelepasan bahan inti pada kondisi yang diinginkan. Bahan penyalut untuk proses
mikroenkapsulasi pada industri pangan dapat dilihat pada Tabel 5.
Tabel 5. Bahan penyalut untuk proses mikroenkapsulasi pada industri pangan
Kelas Jenis
Karbohidrat
polimer
Pati dan turunannya, selulosa dan turunannya, gum arab,
gum karaya, mesquit gum, galaktomanan, pektin, karagenan,
alginat, xantan, gelan, dekstran, kitosan
Protein Gluten, isolat protein, kasein, whey protein, gelatin
Lemak Asam lemak/alkohol, gliserida, wax fosfolipid
Bahan anorganik Tripolifosfat, silikat, aluminium oksida
Lainnya Polyvinylpyrrolidone (PVP), parafin, shellac
Sumber: Wandrey et al. (2010)
Karbohidrat seperti pati, maltodekstrin, sirup jagung padat, dan gum
akasia telah banyak digunakan sebagai bahan pengkapsul. Bahan-bahan ini
memiliki banyak sifat yang diinginkan sebagai pengenkapsulasi seperti viskositas
yang rendah pada kadar padatan yang tinggi dan kelarutan yang baik. Namun,
bahan-bahan ini juga memiliki kekurangan fungsi interfasial sehingga perlu
digabungkan dengan bahan pengenkapsul lain seperti protein susu (Hogan, 2001).
Penelitian terhadap penggunaan campuran protein dengan karbohidrat
telah banyak dilakukan diantaranya penggunaan gum arab, isolat protein kedelai,
whey protein isolat, dan natrium kaseinat untuk minyak jeruk (Kim et al., 1996),
dan penggunaan campuran whey protein isolat dan maltodekstrin untuk lemak
susu (Young, et al., 1993). Hasil penelitian menunjukan bahwa bahan penyalut
dari jenis protein maupun kombinasi protein dengan polisakarida adalah lebih
Pada beberap
apa kasus, bahan penyalut yang mengandun
hasilkan produk dengan daya alir dan karakte
ngkatan stabilitas oksidasi juga terjadi pada
matriks protein-karbohidrat (Lin et al., 1995).
hao dan Whistler (1994), pati dapat berint
ponen lain seperti protein membentuk granula
. Granula ini dapat membawa sejumlah kom
yak dan flavor untuk mengontrol pelepasann
trin (MD)
ktrin [(C6H12O5)nH2O] didefinisikan sebagai pr
sakarida tidak manis) dengan panjang rantai
ukosa. Maltodekstrin secara teori diproduksi de
ggunakan enzim α-amilase atau asam (Kenned
terdiri dari unit α-D-glukosa yang dihubungka
4) dan biasanya diklasifikasikan menur
E).
dari DE adalah kandungan gula pereduksi ya
kstrosa dalam basis kering. Semakin tinggi ni
pula kandungan gula pereduksinya. DE maltode
20 (Kennedy et al., 1995). Gambar struktur ma
mbar 5.
ambar 5. Struktur maltodekstrin (Anonim, 2010)
15
hubungkan oleh ikatan
16 Dua tipe maltodekstrin yang digunakan secara komersial, yaitu
maltodekstrin yang mempunyai kisaran nilai DE 10-14 dan DE 15-19.
Maltodekstrin dengan DE rendah akan cenderung teretrogradasi dalam larutan
sedangkan yang DE tinggi akan membentuk larutan dengan viskositas rendah
dan dapat meningkatkan rasa manis (Kennedy et al., 1995).
Variasi kelarutan dari maltodekstrin tergantung pada nilai DE dan
metode hidrolisisnya. Pada nilai DE yang sama, produk hidrolisis dengan
enzim biasanya mengandung sakarida berbobot molekul tinggi yang lebih
rendah dan lebih mudah larut dalam air dibandingkan dengan produk
hidrolisis dengan asam. Maltodekstrin dengan DE rendah cenderung rendah
dalam menyerap air di atmosfer (Kennedy et al., 1995).
Maltodekstrin memiliki sifat tidak manis, berwarna putih, dan tidak
berbau. Hal ini membuat maltodekstrin mampu digunakan dalam berbagai
aplikasi produk yang luas. Maltodekstrin biasanya digunakan untuk bahan
yang sulit untuk dikeringkan seperti jus buah, perisa, dan pemanis
(Reineccius, 1988) dan untuk mengurangi masalah ketebalan dan
penggumpalan selama penyimpanan, dengan demikian meningkatkan
stabilitas produk (Bhandari et al., 1993).
Maltodekstrin tidak memiliki kemampuan sebenarnya dalam
emulsifikasi (lipofil atau hidrofil). Maltodektrin tersusun dari unit glukosa dan
tidak efektif untuk menstabilkan minyak dalam larutan berviskositas.
Maltodekstrin memberikan stabilitas terhadap oksigen yang baik untuk
enkapsulasi minyak tetapi memiliki kapasitas dan stabilitas emulsifikasi yang
lemah dan retensi minyak yang rendah (Kenyon, 1995). Untuk itu biasanya
maltodekstrin dikombinasikan dengan bahan lain seperti gum arab, protein,
atau pati termodifikasi lainnya untuk keperluan stabilitas emulsi (Kenyon dan
Anderson, 1988).
2. Natrium Kaseinat (NaCas)
Natrium kaseinat merupakan suatu senyawa protein yang potensial jika
digunakan sebagai bahan penyalut. Sebagai senyawa protein, natrium kaseinat
memiliki rantai samping hidrofilik dan hidrofobik (Dalgleish, 2001), kurang
17 (Pedersen et al., 1998). Sifat-sifat inilah yang menyebabkan kasein baik
sebagai bahan pengemulsi, mampu bertindak sebagai surfaktan dengan
membentuk lapisan penstabil yang meluas disekeliling droplet emulsi dan
mudah diaplikasikan pada proses spray drying.
Menurut Fox (1986), natrium kaseinat dapat bertahan dalam air hingga
suhu pemanasan 1400C selama >60 menit pada pH 6.7. Hal ini disebabkan oleh kurangnya struktur sekunder dan tersier serta lebih banyak mengandung
struktur kompleks kuartener dari protein.
Morr (1986) menyatakan bahwa kemampuan fungsional kaseinat
mencakup beberapa fungsi seperti water-fat binding, agen pengental (viscosity
dan gelation), agen pembentuk busa (whipping dan foaming), emulsifikasi,
dan agen pembentuk tekstur. Kaseinat memiliki aktivitas permukaan emulsi
yang tinggi dibanding dengan whey protein dan karakteristik sebagai surfaktan
yang sangat baik, kemungkinan besar disebabkan oleh konformasi molekul
ampifilik dari komponen-komponen dalam kasein yang menghasilkan sifat
hidrofilik dan hidrofobik pada permukaan air-minyak.
Banyak penelitian yang telah menelaah penggunaan natrium kaseinat
sebagai bahan pengkapsul yang dikombinasikan dengan bahan lain. Misalnya
pada penelitian mikroenkapsulasi minyak cumi-cumi, stabilitas terhadap
oksidasi dan suhu yang diperoleh cukup baik dengan peningkatan efektifitas
enkapsulasi (Lin et al., 1995).
F. SPRAY DRYING
Menurut Gouin (2004), enkapsulasi menggunakan teknik spray drying
telah digunakan dalam industri pangan sejak tahun 1950an untuk memberikan
perlindungan bagi minyak flavor melawan degradasi atau oksidasi. Spray dryer
digunakan untuk mengeringkan suatu larutan, campuran atau produk cair lainnya
menjadi bentuk bubuk atau powder pada kadar air mendekati kesetimbangan
dengan kondisi udara pada tempat produk keluar (Wirakartakusumah et al., 1989).
Ciri khas dari penggunaan alat spray dryer ini adalah siklus
18 akhir siap dikemas ketika selesai proses (Heldman et al., 1981). Gambar 6
menunjukkan contoh alat spray dryer skala laboratorium.
Keterangan:
A: larutan/suspensi yang akan dikeringkan B: udara atomisasi
1: udara pengering masuk 2: pemanasan udara pengering 3: atomisasi larutan/suspensi 4: tabung pengeringan
5: bagian antara tabung pengeringan dan siklon 6: siklon
7: udara pengering keluar 8: wadah penampung produk
Gambar 6. Spray dryer skala laboratorium (Anonim, 2010)
Menurut Masters (1979), teknik spray drying terdiri dari empat tahap
proses, yaitu atomisasi bahan sehingga dapat membentuk semprotan sehalus
mungkin, kontak antara bahan dengan udara pengering, evaporasi, dan pemisahan
bubuk kering dengan aliran udara yang membawanya.
Fungsi utama atomisasi adalah untuk menghasilkan droplet yang
berukuran kecil, sehingga luas permukaan menjadi lebih besar yang
mengakibatkan proses penguapan akan lebih cepat. Di samping itu, atomizer
bertindak sebagai alat pengatur kecepatan aliran produk pada proses pengeringan.
Atomizer mendistribusikan cairan pada aliran udara dengan cara yang relatif
seragam dan menghasilkan droplet dengan ukuran tertentu sesuai dengan yang
diinginkan (Heldman et al., 1981).
Evaporasi terjadi karena adanya kontak antara droplet dengan udara
pengering, sehingga terjadi transfer panas dari udara pengering ke droplet dan air
yang terdapat dalam droplet akan menguap. Transfer panas tersebut digunakan
sebagai panas laten selama evaporasi. Evaporasi terjadi pada masing-masing
droplet yang bersinggungan dengan udara pengering. Kecepatan evaporasi
dipengaruhi oleh komposisi bahan, terutama kandungan total padatan. Semakin
19 Partikel kering yang dihasilkan dipisahkan dari udara dan dikumpulkan oleh
siklon atau filters. Pemisahan dapat dilakukan secara langsung maupun bertahap
tergantung pada desain alat (Heldman et al., 1981).
Suhu pengeringan tergantung dari produk yang dikeringkan, suhu
pengeringan dapat mempengaruhi mikroenkapsulat. Suhu inlet yang tinggi
digunakan untuk meningkatkan aliran penguapan dari membran semipermeabel
pada permukaan droplet. Peningkatan suhu outlet dapat menurunkan kadar air
produk pada kondisi aliran udara dan input panas yang konstan (Masters, 1979).
Rentang suhu inlet dan outlet yang umumnya aman digunakan dan menghasilkan
retensi yang baik secara berurutan adalah 160-210°C dan >100°C (Reinnecius,
1988).
Efektivitas mikroenkapsulasi dengan metode spray drying sangat
tergantung pada bahan penyalut yang digunakan. Hal ini akan mempengaruhi
stabilitas emulsi sebelum pengeringan, kemampuan mengalir, kestabilan mekanik,
dan umur simpan setelah pengeringan. Bahan penyalut tersebut kelarutannya
harus tinggi, memiliki kemampuan mengemulsi, mampu membentuk film, dan
juga memberikan viskositas yang rendah pada konsentrasi yang tinggi
(Reinnecius, 1988).
Keuntungan penggunaan metode ini adalah produk akan kering tanpa
bersinggungan dengan logam panas, suhu produk relatif rendah, walaupun
pengeringan dilakukan pada suhu yang relatif tinggi, penguapan berlangsung
sangat cepat karena luasnya permukaan bahan, produk yang dihasilkan berupa
bubuk, sehingga memudahkan dalam penanganan dan pengangkutan (Masters,
1979). Keuntungan lain dari metode spray drying adalah biaya operasinya rendah,
banyaknya pilihan untuk bahan penyalut yang dapat digunakan, mampu
memproduksi kapsul dalam waktu yang singkat, mutu dan stabilitas kapsul tinggi,
ukuran kapsul yang dihasilkan kecil, dan produksi skala besar dapat dilakukan
20 III. METODOLOGI PENELITIAN
A. BAHAN DAN ALAT
1. Bahan
Bahan baku utama yang digunakan dalam penelitian adalah NDRPO
(neutralized and deodorized red palm oil) yang diperoleh dari hasil
deodorisasi NRPO (neutralized red palm oil) menjadi NDRPO yang telah
dilakukan oleh Riyadi (2009). Bahan baku lain yang digunakan antara lain
maltodekstrin dengan DE 10-15 merk Hi-Cap 100 yang diperoleh dari PT
Menara Sumber Daya Indonesia dan natrium kaseinat dengan kadar protein
87.82% yang diperoleh dari Naarden Agro Products BV, Holland.
Bahan-bahan untuk analisis kimia yang digunakan adalah heksana (p.a dan teknis),
kertas saring Whatman no. 42, aquades, dan aluminium foil.
2. Alat
Alat-alat yang digunakan dalam penelitian adalah mini homogenizer
Armfield L4R, spray dryer Buchi 190, UV-VIS spectrophotometer UV-2450,
Konica Minolta chromameter CR-300, seperangkat alat soxhlet, penyaring
vakum,lampu UV, oven, desikator,timbangan analitik, cawan aluminium, hot
plate, termometer, sudip, dan beberapa alat gelas.
B. METODE PENELITIAN
1. Karakterisasi Bahan Baku
Bahan baku yang akan dikarakterisasi NDRPO dan maltodekstrin
sebagai bahan penyalut. Tahap ini dilakukan untuk mengetahui kualitas awal
bahan baku yang digunakan dan membandingkannya dengan syarat mutu yang
ditetapkan dalam SNI atau sumber lain yang menetapkan spesifikasi mutu
bahan baku yang digunakan.
Fraksinasi NDRPO pada suhu ruang dilakukan sebelum karakterisasi
bahan. Mula-mula NDRPO dipanaskan menggunakan oven pengering sambil
diaduk dalam suatu panci stainless steel hingga mencapai suhu ±50°C selama
21 ruang dengan kondisi tertutup sampai terjadi pemisahan fraksi padat (stearin)
dan fraksi cair (olein). Fraksi olein yang telah terpisah diambil dan
dipindahkan ke dalam wadah tertutup yang kedap udara dan cahaya, maka
diperolehlah MSM sebagai bahan baku utama.
MSM yang telah didapat lalu dikarakterisasi meliputi analisis kadar
air, metode hot plate (AOCS, 1993) dan total karoten, metode
spektrofotometri (PORIM, 2005). Untuk maltodekstrin juga dilakukan
karakterisasi, yaitu analisis kadar air, metode oven (AOAC, 1995) dan analisis
DE (dextrose equivalent), yang terdiri dari dua tahap, meliputi analisis kadar
gula pereduksi, metode Park-Johnson (Takeda et al., 1993) serta analisis kadar
karbohidrat total, metode fenol-sulfat (Dubois et al., 1959).
2. Penentuan Formula Emulsi untuk Pembuatan Mikroenkapsulat MSM
Tahap ini bertujuan untuk menentukan kombinasi konsentrasi bahan
penyalut yang akan digunakan dan jumlah minyak yang masih dapat
ditambahkan pada kombinasi bahan penyalut maltodekstrin-natrium kaseinat
sehingga masih membentuk emulsi yang stabil. Maltodekstrin yang memiliki
ketahanan oksidasi yang baik dan dapat menurunkan viskositas emulsi
dikombinasikan dengan proporsi penggunaan yang lebih besar dibanding
dengan proporsi penggunaan natrium kaseinat yang memiliki sifat emulsifier
yang tinggi.
Jumlah minyak yang digunakan, yaitu 100% dan 200% dari total
bahan penyalut. Kombinasi proporsi maltodekstrin:natrium kaseinat yang
diujikan, yaitu 1:1, 2:1, 3:1, 4:1, dan 5:1 sedangkan konsentrasi bahan
penyalut yang digunakan adalah 30% dalam larutan.
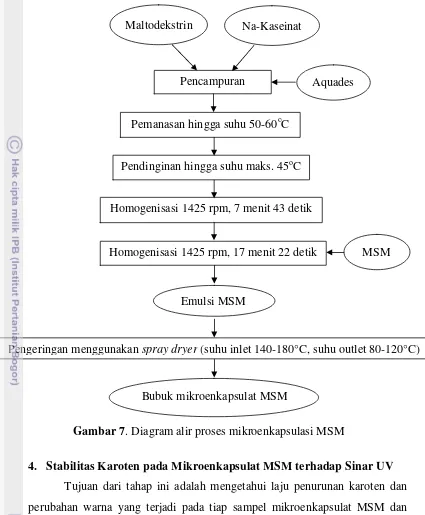
Mekanisme pembuatan emulsi MSM mengacu pada penelitian yang
telah dilakukan oleh Simanjuntak (2007) dengan memodifikasi waktu
homogenisasi bahan. Proses pembuatan emulsi MSM dapat dilihat pada
Gambar 7. Emulsi MSM yang mempunyai stabilitas 100% yang didasarkan
pada pengujian stabilitas emulsi, akan diproses lebih lanjut pada tahap
22 Pengujian stabilitas emulsi (Montesqrit, 2007) dilakukan dengan cara
mendiamkan emulsi selama 2 jam dalam gelas piala yang berdimensi sama
setelah dihomogenisasi kemudian dihitung persentase pemisahannya setelah
waktu penyimpanan tersebut, dengan asumsi bahwa sistem emulsi yang
sempurna bernilai 100%, seperti yang disajikan dengan rumus:
Stabilitas (%) = x 100%
Keterangan: a = volume keseluruhan
b = volume pemisahan
3. Produksi dan Karakterisasi Mikroenkapsulat MSM
Tahap ini bertujuan untuk mendapatkan bubuk mikroenkapsulat MSM
yang kaya karoten dan mengetahui pengaruh konsentrasi bahan penyalut
terhadap karakteristik mikroenkapsulat MSM sehingga formula optimum
dapat ditetapkan. Setelah diperoleh formula emulsi yang kestabilannya 100%,
maka diproduksilah bubuk mikroenkapsulat MSM dengan mengeringkan
emulsi menggunakan spray dryer. Produk yang dihasilkan kemudian dihitung
rendemennya berdasarkan perbandingan berat mikroenkapsulat yang
dihasilkan oleh spray dryer dengan total padatan bahan emulsi (bahan
penyalut dan MSM). Penghitungan rendemen dilakukan untuk mengetahui
pengaruh perbedaan proporsi bahan penyalut terhadap jumlah produk yang
dapat dihasilkan. Gambar 7 menunjukkan proses pembuatan mikroenkapsulat
MSM.
Pada tahap ini juga dilakukan karakterisasi mikroenkapsulat MSM dari
semua formula yang telah ditentukan. Karakterisasi produk tersebut antara lain
analisis kadar air (AOAC,1995), total karoten (PORIM, 2005), kadar minyak
tak terkapsulkan (Shahidi, 1997), kelarutan (Fardiaz et al., 1992), warna
23 Gambar 7. Diagram alir proses mikroenkapsulasi MSM
4. Stabilitas Karoten pada Mikroenkapsulat MSM terhadap Sinar UV
Tujuan dari tahap ini adalah mengetahui laju penurunan karoten dan
perubahan warna yang terjadi pada tiap sampel mikroenkapsulat MSM dan
membandingkannya dengan MSM yang tak terkapsulkan sehingga dapat
diketahui keefektifan perlakuan pengkapsulan dari mikroenkapsulat MSM itu
sendiri. Perlakuan pemaparan sinar UV pada mikroenkapsulat MSM
dilakukan dalam lemari tertutup yang telah dipasangi lampu UV seperti dapat
dilihat pada Gambar 8.
Pada tahap ini MSM yang tak terkapsulkan dan mikroenkapsulat MSM
yang telah diproduksi disinari dengan lampu UV selama rentang waktu
tertentu. Kedua jenis sampel dengan bobot yang sama ditempatkan pada MSM Pencampuran Aquades
Maltodekstrin
Emulsi MSM
Pengeringan menggunakan spray dryer (suhu inlet 140-180°C, suhu outlet 80-120°C)
Bubuk mikroenkapsulat MSM Homogenisasi 1425 rpm, 17 menit 22 detik
Pemanasan hingga suhu 50-60oC
Pendinginan hingga suhu maks. 45oC
24 loyang aluminium (22 cm x 22 cm x 3 cm) dan dimasukkan ke dalam lemari
tertutup yang telah dipasangi lampu UV. Kemudian sampel-sampel tersebut
dipapar UV selama 1, 2, 3, 4, dan 5 jam dan dilakukan pengadukan setiap 30
menit agar paparan sinar UV dapat merata diseluruh permukaan sampel.
Penentuan waktu papar didasarkan pada penelitian yang telah dilakukan oleh
Novia (2009). Sampel yang telah dipapar UV kemudian dianalisis total
karoten (PORIM, 2005), dan warna (Hutching, 1999).
Gambar 8. Tempat pemaparan sinar UV pada mikroenkapsulat MSM
5. Pemilihan Formula Optimum Mikroenkapsulat MSM
Pemilihan formula mikroenkapsulat MSM terbaik pada penelitian ini
didasarkan pada hasil analisis produk mikroenkapsulat MSM. Prioritas utama
pemilihan formula terbaik adalah hasil karakterisasi produk, meliputi kadar
total karoten, kadar minyak tak terkapsulkan, nilai kelarutan, dan derajat
warna kuning (nilai b) dari bubuk serta larutan mikroenkapsulat MSM.
Sedangkan prioritas selanjutnya ditentukan oleh uji stabilitas karoten baik laju
penurunan total karoten maupun total perubahan warna, dan terakhir adalah
hasil analisis kadar air produk. Tabel 6 menunjukkan bobot nilai untuk
masing-masing parameter analisis produk mikroenkapsulat MSM berdasarkan
urutan prioritasnya. Parameter dengan bobot nilai yang lebih besar dianggap
lebih penting setelah disesuaikan dengan aplikasi penggunaan produk dan
25 Tabel 6. Bobot nilai masing-masing parameter analisis produk
mikroenkapsulat MSM
Parameter analisis Bobot nilai
Kadar total karoten 8
Kadar minyak tak terkapsulkan 7
Kelarutan 6
Warna larutan 5
Warna bubuk 4
Laju penurunan total karoten 3
Total perubahan warna 2
Kadar air 1
Setelah dilakukan pemberian bobot untuk parameter analisis,
selanjutnya dilakukan pemberian skor (1 sampai dengan 5) untuk tiap formula
mikroenkapsulat MSM yang terpilih. Skor yang lebih tinggi diberikan pada
formula dengan hasil analisis yang lebih baik untuk tiap parameter analisisnya
dan disesuaikan pula dengan hasil uji statistik yang telah dilakukan. Formula
yang berada pada subset yang sama pada hasil uji Duncan, berarti akan
memiliki skor yang sama. Formula yang memiliki total skor tertinggi dari
hasil perkalian antara bobot nilai parameter analisis dengan skor tiap formula
adalah formula optimum yang dihasilkan.
C. ANALISIS
1. Rendemen Mikroenkapsulat
Rendemen mikroenkapsulat MSM dihitung dengan cara
membandingkan berat miroenkapsulat yang dihasilkan dengan berat padatan
(bahan penyalut dan minyak) dalam emulsi MSM, seperti pada rumus berikut:
Rendemen mkroenkapsulat (%) = x 100%
2. Kadar Air, Metode Hot Plate (AOCS, 1993)
Analisis ini digunakan untuk mengukur kadar air MSM. Sampel
26 dikeringkan dan diketahui bobotnya. Kemudian sampel dan gelas piala
dipanaskan di atas hot plate, sambil diaduk beberapa kali untuk menghindari
sampel yang memercik, lalu gelas piala ditutup menggunakan gelas arloji.
Kondensasi dari uap air yang menempel pada gelas arloji mengindikasikan
titik akhir dari analisis ini. Suhu sampel yang dipanaskan tidak boleh lebih
dari 130°C. Setelah mencapai titik akhir, sampel dipanaskan hingga titik awal
terbentuknya asap tetapi jangan terlalu panas. Sampel didinginkan sampai
suhu ruang dalam desikator lalu timbang. Kadar air sampel dapat dihitung
dengan menggunakan rumus sebagai berikut :
Kadar air basis basah (g/100 g bahan basah) = x 100 %
Kadar air basis kering (g/100 g bahan basah) = x 100 %
Keterangan : W = bobot contoh sebelum dikeringkan (g)
W1 = bobot contoh + gelas piala kering kosong (g)
W2 = bobot gelas piala kosong (g)
3. Kadar Air, Metode Oven (AOAC, 1995)
Sampel sejumlah 3-5 gram ditimbang dan dimasukkan dalam cawan
yang telah dikeringkan dan diketahui bobotnya. Kemudian sampel dan cawan
dikeringkan dalam oven bersuhu 105°C selama 6 jam. Cawan didinginkan dan
ditimbang, kemudian dikeringkan kembali sampai diperoleh bobot tetap.
Kadar air sampel dapat dihitung dengan menggunakan rumus sebagai berikut :
Kadar air basis basah (g/100 g bahan basah) = x 100 %
Kadar air basis kering (g/100 g bahan basah) = x 100 %
Keterangan : W = bobot contoh sebelum dikeringkan (g)
W1 = bobot contoh + cawan kering kosong (g)
W2 = bobot cawan kosong (g)
4. Total Karoten, Metode Spektrofotometri (PORIM, 2005)
Sebanyak 0,1 gram sampel dilarutkan dengan heksana dalam labu ukur
27 Selanjutnya absorbansi diukur dengan spektrofotometer pada panjang
gelombang 446 nm. Kadar karoten (mg/kg) dihitung dengan rumus:
Karoten (mg/kg) = ! " ## Keterangan : W = bobot sampel yang dianalisis (g)
As = absorbansi sampel
5. Dextrose Equivalent (DE)
Nilai DE (dalam persen) diperoleh dari perbandingan kadar gula
pereduksi dengan kadar total gula atau karbohidrat dalam sampel dikali 100.
Nilai DE = $
$ % & x 100
a. Persiapan Sampel
Sebanyak 1 g sampel dilarutkan dalam 100 ml etanol (sedikit demi
sedikit) kemudian larutan sampel distirer dan disentrifus 4000 rpm selama
10 menit. Pati disaring dan dimasukkan ke dalam desikator selama
semalam (sampai kering). Pati dimortar dan diambil 40 mg, kemudian
ditambahkan 20 ml air dan diautoclave 1 jam suhu 105°C, lalu didinginkan
pada suhu kamar. Setelah itu, pati disentrifuse dan diencerkan 40 kali.
b. Kadar Gula Pereduksi, Metode Park-Johnson (Takeda et al., 1993) Sampel sebanyak 1 ml ditambahkan 0.5 ml larutan buffer sodium
karbonat-sodium hidrogen karbonat (4.8 g Na2CO3, 9.2 g NaHCO3 dan
0.65 g KCN yang dilarutkan dalam aquades 1 L) dan ditambahkan 0.5 ml
potasium fericianida 0.1% (b/v). Campuran larutan tersebut dipanaskan
selama 15 menit dalam air mendidih dan didinginkan dalam air mengalir
selama 10 menit. Larutan tersebut ditambahkan 2.5 ml larutan feric
ammonium sulfat (3 g (NH4)Fe(SO3)42H2O di dalam 1 L larutan 50 mM
H2SO4). Selanjutnya divorteks dan didiamkan selama 20 menit pada suhu
ruang dan dibaca pada panjang gelombang 715 nm dengan menggunakan
28 Pembuatan kurva standar dilakukan dengan cara sama seperti untuk
sampel tetapi sampel diganti dengan glukosa dengan konsentrasi 2, 4, 6, 8
dan 10 ppm.
c. Kadar Karbohidrat Total, Metode Fenol-Sulfat (Dubois et al., 1959)
Sampel sebanyak 0.5 ml dimasukkan ke dalam tabung reaksi.
Selanjutnya ditambahkan 0.5 ml fenol 5% dan divorteks. Sebanyak 2.5 ml
larutan H2SO4 pekat ditambahkan dengan cara menuangkan secara tegak
lurus permukaan larutan (asam sulfat harus dikeluarkan dengan cepat dari
pipet, hati-hati karena reaksi panas). Kemudian larutan divorteks dan
disimpan pada suhu kamar selama 20 menit. Sebelum diukur larutan
divorteks kembali, kemudian ukur pada panjang gelombang 490 nm
dengan menggunakan spektrofotometer.
Pembuatan kurva standar dilakukan dengan cara sama seperti
untuk sampel tetapi sampel diganti dengan glukosa dengan konsentrasi 20,
40, 60, 80, dan 100 ppm.
6. Kadar Minyak Tak Terkapsulkan, Metode Ekstraksi (Shahidi dan
Wanasundara, 1997)
Labu lemak dikeringkan dalam oven 105-110oC sampai benar-benar kering lalu didinginkan dalam desikator. Setelah dingin labu lemak ditimbang.
Sampel ditimbang dalam erlenmeyer sebanyak ± 1-3 gram berat kering.
Sampel kemudian dicuci dengan menggunakan heksana sebanyak ± 20 ml
selama ± 1 menit. Sampel kemudian disaring menggunakan kertas saring ke
dalam labu lemak yang telah diketahui beratnya (Wl1). Pencucian diulang
sampai 3 kali. Heksana yang ada dalam labu lemak didestilasi dan kemudian
dikeringkan dalam oven selama 1 jam. Labu lemak kemudian didinginkan
dalam desikator. Setelah mencapai suhu ruang, labu lemak (Wl2) ditimbang.
Adapun kadar lemak yang tidak terkapsulkan dihitung dengan rumus berikut :
Kadar lemak yang tidak terkapsulkan (%) = Wl2-Wl1