UJI KANDUNGAN FOSFAT SEBAGAI P2O5 DALAM BERBAGAI MEREK PUPUK FOSFAT KOMERSIAL
SECARA SPEKTROFOTOMETRI
SKRIPSI
Diajukan untuk melengkapi tugas dan memenuhi syarat mencapai gelar Sarjana
DESMI SIANTURI 040802040
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATERA UTARA
PERSETUJUAN
Judul : UJI KANDUNGAN FOSFAT SEBAGAI P2O5 DALAM BERBAGAI MEREK PUPUK FOSFAT KOMERSIAL SECARA SPEKTROFOTOMETRI
Kategori : SKRIPSI
Nama : DESMI SIANTURI
NIM : 040802040
Program Studi : SARJANA ( S1 ) Departemen : KIMIA
Fakultas : MATEMATIKA DAN ILMU PENGETAHUAN ALAM
(FMIPA) UNIVERSITAS SUMATERA UTARA Disetujui di Medan, Desember 2008
Komisi Pembimbing :
Pembimbing II Pembimbing I
Drs. Chairuddin, MSc Drs. Usman Rasyid NIP.131 653 992 NIP. 130 422 446
Diketahui / disetujui oleh
Departemen Kimia FMIPA USU Ketua,
PERNYATAAN
UJI KANDUNGAN FOSFAT SEBAGAI P2O5 DALAM BERBAGAI MEREK PUPUK FOSFAT KOMERSIAL
SECARA SPEKTROFOTOMETRI
SKRIPSI
Saya mengakui bahwa skripsi ini adalah hasil kerja saya sendiri, kecuali beberapa kutipan dan ringkasan yang masing-masing disebutkan sumbernya.
Medan, Desember 2008
PENGHARGAAN
Puji dan syukur penulis panjatkan kehadirat Allah Bapa Yang Maha Kuasa, karena atas berkat kasih dan karunia-Nya penulis dapat menyelesaikan skripsi ini dengan baik.
Pada kesempatan ini penulis mengucapkan terima kasih kepada bapak saya tercinta Ramses Sianturi dan mama saya tercinta Nurliana Gultom serta saudara/i ku (Riduan, Elfrina, Septu Iwanri, Juliati dan Fernando) untuk doa, dukungan dan kasihnya. Saya juga berterimakasih kepada Bapak Drs. Usman Rasyid selaku Dosen Pembimbing 1 dan Bapak Drs. Chairuddin, MSc selaku Dosen Pembimbing 2 yang telah meluangkan waktunya untuk memberikan bimbingan, arahan, dan saran kepada penulis selama melakukan penelitian dan penyusunan skripsi ini, dan kepada Bapak Prof. Dr. Harlem Marpaung selaku Kepala Laboratorium Kimia Analitik FMIPA USU yang telah memberikan saran-saran kepada penulis. Ucapan terima kasih juga saya tujukan kepada Ketua dan Sekretaris Departemen Kimia FMIPA USU yaitu Ibu Rumondang Bulan Nst, MS dan Bapak Drs. Firman Sebayang, MS, Dekan dan Pembantu Dekan FMIPA USU, seluruh dosen dan staff Departemen Kimia FMIPA USU , dan kepada dosen wali saya Bapak Prof. Dr. Zul Alfian, MSc selaku dosen wali saya yang telah meluangkan waktunya untuk memberikan bimbingan selama penulis mengikuti perkuliahan di FMIPA USU. Kepada rekan rekan mahasiswa/i Departemen Kimia khususnya stambuk 2004 yang telah memberikan dukungan dan perhatian kepada penulis serta kepada rekan-rekan asisten pusat penelitian Sumber Daya Alam dan Lingkungan Sumatera Utara yang turut membantu dalam menyelesaikan skripsi ini.
ABSTRAK
Telah dilakukan uji kandungan fosfat sebagai P2O5 dalam berbagai merek pupuk
fosfat komersial. Pengambilan sampel dilakukan secara acak dari beberapa toko pupuk di kota Medan. Penentuan fosfat dilakukan dengan metode spektrofotometri menggunakan pereaksi molibdem-asam askorbat yang menghasilkan senyawa kompleks fosfomolibdat berwarna biru dan diukur absorbansinya pada panjang gelombang 880 nm. Pengujian kandungan P2O5 dilakukan untuk mengetahui
kesesuaian kandungan yang tercantum pada kemasan dengan hasil analisis. P2O5 yang
larut dalam asam sitrat 2 % dan P2O5 yang larut dalam air juga ditentukan untuk
DETERMINATION OF PHOSPHATE AS P2O5 IN COMMERCIAL PHOSPHATE FERTILIZERS WITH SPECTROFOTOMETRY
ABSTRACT
Determination of Phosphate as P2O5 in commercial phosphate fertilizers has been
carried out. The samples of phosphate fertilizers were taken randomly from several fertilizers shop in Medan. Phosphate was determined by spectrophotometric method using molybdenum-citric acid reagent to produce phosphomolybdenum blue complex and measured at wave length 880 nm. Determination P2O5 was purposed to know
suitable P2O5 in pack with yield analysis. Citrate soluble P2O5 and water soluble P2O5
DAFTAR ISI
1.8. Metode analisis fosfat 5 Bab 2 : TINJAUAN PUSTAKA 6
2.1. Fosfor 6
2.2. Pupuk 9
2.3. Prinsip produksi pupuk fosfat 10 2.4. Pupuk majemuk yang mengandung fosfat 12 2.5. Klasifikasi fosfor 13
2.6. Metode analisa kuantitatif fosfat 14
3.3.8. Pengukuran pH sampel dalam air 21 3.4. Bagan Penelitian 22
4.1. Hasil penelitian dan pembahasan 23
Bab 5 : KESIMPULAN DAN SARAN 27
5.1. Kesimpulan 27
5.2. Saran 27
DAFTAR LAMPIRAN
Halaman 1. Analisis kuantitatif fosfor sebagai % P2O5 30
1.1. Menentukan persamaan garis regresi kurva kalibrasi 30
1.2. Perhitungan koefisien korelasi 31
1.3. Perhitungan standar deviasi 31
1.4. Penentuan batas deteksi 32
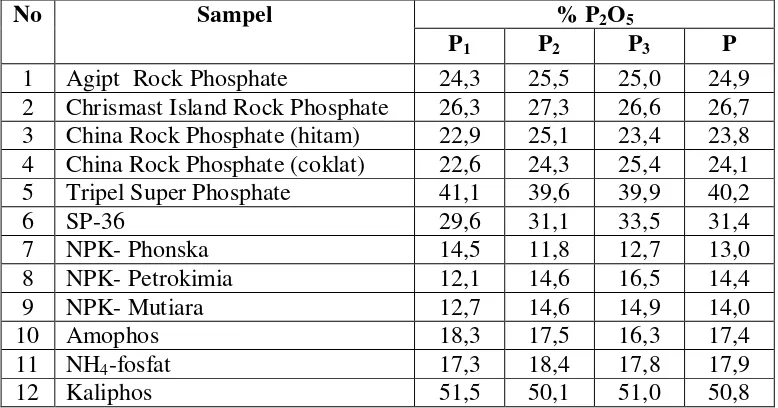
1.5. Penentuan % P2O5 dalam sampel 33
1.6. Penentuan % kadar air dalam sampel 34
1.7. Penentuan persentase P2O5 yang larut dalam asam sitrat 2 % dan air 34
DAFTAR TABEL
Halaman
Tabel 4.1. Data penentuan waktu tunggu (operating time) 23
Tabel 4.2. Data penentuan panjang gelombang maksimum P2O5 24
Tabel 4.3. Hasil pengujian beberapa parameter terhadap sampel pupuk fosfat 25
Tabel 4.4. Data absorbansi larutan standar 36
Tabel 4.5. Data absorbansi penentuan P2O5 total pada λ = 880 nm 36
Tabel 4.6. Data absorbansi penentuan P2O5 yang larut dalam asam sitrat 37
2 % pada λ = 880 nm
Tabel 4.7. Data absorbansi penentuan P2O5 yang larut dalam air pada λ = 880 nm 37
Tabel 4.8. Hasil perhitungan P2O5 total 38
Tabel 4.9. Hasil perhitungan P2O5 yang larut dalam asam sitrat 2 % 38
Tabel 4.10. Hasil perhitungan P2O5 yang larut dalam air 39
Tabel 4.11. Data penentuan % kadar air 39
Tabel 4.12. Persentase P2O5 larut dalam asam sitrat 2 % dan air atas dasar berat 40
DAFTAR GAMBAR
Halaman Gambar 1. Kurva kalibrasi larutan standar P2O5 24
Gambar 2. Kurva penentuan panjang gelombang maksimum P2O5 41
ABSTRAK
Telah dilakukan uji kandungan fosfat sebagai P2O5 dalam berbagai merek pupuk
fosfat komersial. Pengambilan sampel dilakukan secara acak dari beberapa toko pupuk di kota Medan. Penentuan fosfat dilakukan dengan metode spektrofotometri menggunakan pereaksi molibdem-asam askorbat yang menghasilkan senyawa kompleks fosfomolibdat berwarna biru dan diukur absorbansinya pada panjang gelombang 880 nm. Pengujian kandungan P2O5 dilakukan untuk mengetahui
kesesuaian kandungan yang tercantum pada kemasan dengan hasil analisis. P2O5 yang
larut dalam asam sitrat 2 % dan P2O5 yang larut dalam air juga ditentukan untuk
DETERMINATION OF PHOSPHATE AS P2O5 IN COMMERCIAL PHOSPHATE FERTILIZERS WITH SPECTROFOTOMETRY
ABSTRACT
Determination of Phosphate as P2O5 in commercial phosphate fertilizers has been
carried out. The samples of phosphate fertilizers were taken randomly from several fertilizers shop in Medan. Phosphate was determined by spectrophotometric method using molybdenum-citric acid reagent to produce phosphomolybdenum blue complex and measured at wave length 880 nm. Determination P2O5 was purposed to know
suitable P2O5 in pack with yield analysis. Citrate soluble P2O5 and water soluble P2O5
BAB 1
PENDAHULUAN
1.1. Latar belakang
Fosfat adalah salah satu unsur hara makro yang essensial dalam budidaya tanaman. Tujuan dari pemupukan adalah menambah ketersediaan unsur hara dalam tanah atau untuk menggantinya karena sebagian dari unsur tersebut diangkut keluar dari lahan pertanian bersama hasil panen. Dalam intensifikasi pertanian, penggunaan pupuk terutama pupuk kimia menjadi suatu keharusan karena pengurangan unsur-unsur hara dari lahan juga semakin intensif. Kalau dalam pertanian konvensional sawah, misalnya hanya ditanami sekali dalam setahun dengan produktifitas 2 sampai 3 ton gabah perhektar, dalam pertanian intensif musim tanam sampai 3 kali setahun dengan produktifitas mencapai 7 sampai 12 ton perhektar. Dengan demikian, pemupukan merupakan faktor yang sangat menentukan keberhasilan intensifikasi pertanian.
Pupuk fosfat dibuat dari bahan baku batuan fosfat antara lain Fluoroapatite Ca10(PO4)6F2 yang mengandung 30 - 32 % P2O5. Karena batuan fosfat yang dapat
ditambang misalnya skala komersial hampir tidak ada, maka kebutuhan pupuk fosfat di negeri kita sepenuhnya bergantung pada supply dari luar negeri, baik sebagai bahan baku (Rock Phosphate) atau sebagai bahan jadi seperti TSP (Triple Super Phosphate), SP-36 (Superphosphate) dan lain- lain.
rekayasa (buatan pabrik) mendominasi penggunaan pupuk fosfat dalam bidang pertanian dan perkebunan Karena harganya yang mahal dan tingginya permintaan pada musim tanam, seringkali beredar pupuk yang dipalsukan dimana persentase kandungan P2O5-nya tidak sesuai dengan yang tercantum dalam kemasan. Kecuali
diperiksa di laboratorium, umumnya petani sulit untuk membedakan antara yang asli dengan yang dipalsukan sehingga selalu menjadi korban.
Pupuk fosfat hasil rekayasa dapat dikelompokkan atas (1) pupuk tunggal, hanya mengandung hara fosfat seperti TSP (46 % P2O5), SP-36 (36 % P2O5) dan (2)
sebagai pupuk majemuk, terdapat bersama unsur hara lain misalnya Nitrogen dan Kalium, seperti NPK 15 : 15 : 15 dan lain-lain.
Pemalsuan pupuk terjadi dalam rantai distribusi sebelum sampai ke konsumen dan hal ini sering terjadi saat mulai musim tanam disertai kelangkaan pupuk di pasar. Apalagi untuk jenis pupuk tertentu pemalsuan lebih mudah dilakukan dibanding dengan cara menganalisis apakah pupuk tersebut asli atau palsu. Pemalsuan mungkin dilakukan dengan mencampur bahan yang serupa tapi harganya jauh lebih murah misalnya menggunakan tanah liat untuk mencampur TSP, SP-36 atau menggunakan NaCl untuk mencampur KCl. Kedua bahan pencampur ini ( NaCl dan tanah liat) sangat mudah diperoleh dan dengan harga yang lebih murah dari pupuk yang akan dipalsukan. Antara KCl dan KCl yang telah dicampur dengan NaCl hampir tidak dapat dibedakan, kecuali dilakukan analisis di laboratorium. Karena cara memalsukan relatif mudah dan murah sebaliknya membedakan yang asli terhadap yang palsu relatif sulit bagi petani, maka mereka akan selalu menjadi korban yang tak berdaya bagi orang-orang yang ingin memetik keuntungan dengan cara yang mudah. Kerugian bagi petani bukan hanya sekedar uang yang hilang untuk membeli pupuk palsu tetapi lebih jauh lagi mungkin akan menghadapi gagal panen karena lahan yang ditanami tidak mengandung hara yang cukup untuk pertumbuhan dan produktifitas tanaman. Ditengah harga sarana produksi pertanian (bibit, pupuk, obat-obatan) yang membumbung tinggi harus dilakukan sesuatu untuk melindungi petani. Berdasarkan uraian-uraian diatas, saya sangat tertarik untuk meneliti tentang kandungan P2O5
Apakah ada kesesuaian antara kandungan P2O5 hasil analisis dengan kandungan yang
terdapat pada kemasannya dan apakah ada keselarasan antara kandungan P2O5 total
terhadap bagian yang mudah larut dalam asam sitrat 2 % dan bagian yang dapat larut dalam air sebagai indikator ketersediaan unsur tersebut bagi tanaman.
1.3. Pembatasan masalah
Penelitian ini hanya dibatasi pada uji kandungan fosfat sebagai P2O5 dalam pupuk
fosfat komersial berbagai merek yang berdasarkan penampilannya sukar dibedakan antara yang asli terhadap yang dipalsukan.
1.4. Tujuan penelitian
Adapun yang menjadi tujuan dari penelitian ini adalah :
1. Untuk mengetahui kesesuaian kandungan fosfat total sebagai P2O5 hasil analisis
dengan kandungan P2O5 yang terdapat dalam kemasan.
2. Untuk mengetahui konsistensi antara P2O5 total terhadap P2O5 yang larut dalam air
dan asam sitrat 2 % karena pupuk fosfat yang mudah larut mempunyai nilai ekonomis lebih tinggi daripada pupuk fosfat yang sukar larut sehingga efektifitasnya tidak semata mata ditentukan oleh P2O5 total
1.5. Manfaat penelitian
Hasil penelitian ini diharapkan dapat dipergunakan sebagai sumber informasi yang berguna tentang kandungan fosfat dalam bentuk P2O5 yang sesuai dengan standar
yang diperbolehkan dalam pembuatan pupuk fosfat komersial
Penelitian ini dilakuka n di Laboratorium Kimia Analitik Fakultas Matematika dan Ilmu Pengetahuan Alam (FMIPA) Universitas Sumatera Utara serta Pusat Penelitian Sumber Daya Alam dan Lingkungan, Universitas Sumatera Utara.
1.7. Metodologi penelitian
Sampel pupuk fosfat yang diteliti dibagi kedalam 3 kategori yaitu (1) batuan fosfat yang telah digiling halus, (2) pupuk fosfat tunggal (TSP dan SP-36) dan (3) pupuk majemuk yang mengandung fosfat seperti tercantum dalam daftar berikut :
No Pupuk Kategori % P2O5 Produsen / Distributor
1 ARP Tepung Batu fosfat 28 – 30 % CV. Bitama Jaya 2 CIRP Tepung Batu fosfat 30 – 32 % CV. Rolimex Indonesia 3 CRP (coklat) Tepung Batu fosfat 32 % China
4 CRP (hitam) Tepung Batu fosfat 32 % China
5 TSP Tunggal 46 % PT. Meroke Tetap Jaya
6 SP-36 Tunggal 36 % PT. Petrokimia Gresik
7 NPK- Phonska Majemuk 15 % PT. Santani Sejahtera 8 NPK- Petrokimia Majemuk 15 % PT. Petrokimia Gresik 9 NPK- Mutiara Majemuk 16 % PT. Meroke Tetap Jaya 10 Amophos Majemuk 20 % PT. Meroke Tetap Jaya 11 NH4- fosfat Majemuk 20 % PT. Petrokimia Gresik
12 Kaliphos Majemuk 51 % PT. Meroke Tetap Jaya
Sampel tersebut diperoleh dari berbagai toko pupuk di kota Medan dan sekitarnya serta merupakan jenis pupuk fosfat yang paling banyak digunakan petani. Keterangan : ARP : Agipt Rock Phosphate
CIRP : Chrismast Island Rock Phosphate
CRP : China Rock Phosphate
TSP : Tripel Super Phosphate
Kandungan fosfat sebagai P2O5 dalam setiap sampel ditentukan sebagai P2O5 total,
P2O5 larut dalam 2 % asam sitrat dan P2O5 yang dapat larut dalam air. Analisis fosfat
BAB 2
TINJAUAN PUSTAKA
2.1. Fosfor
Fosfor merupakan salah satu nutrisi utama yang sangat penting dalam pertumbuhan tanaman. Fosfor tidak terdapat secara bebas di alam. Fosfor ditemukan sebagai fosfat dalam beberapa mineral, tanaman dan merupakan unsur pokok dari protoplasma. Fosfor terdapat dalam air sebagai ortofosfat. Sumber fosfor alami dalam air berasal dari pelepasan mineral-meneral dan biji-bijian (Bausch, 1974).
Fosfat terdapat dalam tiga bentuk yaitu H2PO4-, HPO42-, dan PO43-. Fosfat
umumnya diserap oleh tanaman dalam bentuk ion ortofosfat primer H2PO4- atau
ortofosfat sekunder HPO42- sedangkan PO43- lebih sulit diserap oleh tanaman. Bentuk
yang paling dominan dari ketiga fosfat tersebut dalam tanah bergantung pada pH tanah (Engelstad, 1997). Pada pH lebih rendah, tanaman lebih banyak menyerap ion ortofosfat primer, dan pada pH yang lebih tinggi ion ortofosfat sekunder yang lebih banyak diserap oleh tanaman (Hanafiah, 2005).
Ortofosfat merupakan bentuk fosfat yang dapat dimanfaatkan secara langsung oleh tanaman, sedangkan polifosfat harus terlebih dahulu mengalami hidrolisis membentuk ortofosfat sebelum dimanfaatkan sebagai sumber fosfor. Reaksi ionisasi asam ortofosfat adalah sebagai berikut :
H3PO4 ↔ H+ + H2PO4
-H2PO4 - ↔ H+ + HPO4
HPO42 - ↔ H+ + PO4
nilai pH. Perubahan polifosfat meenjadi ortofosfat pada air limbah yang mengandung bakteri berlangsung lebih cepat dibandingkan dengan perubahan yang terjadi pada air bersih (Effendi, 2003).
Sumber fosfat yang dalam tanah sebagai fosfat mineral yaitu batu kapur fosfat, sisa-sisa tanaman dan bahan organik lainnya. Perubahan fosfor organik menjadi fosfor anorganik dilakukan oleh mikroorganisme. Selain itu, penyerapan fosfor juga dilakukan oleh liat dan silikat (Isnaini, 2006).
Fosfat anorganik maupun organik terdapat dalam tanah. Bentuk anorganiknya adalah senyawa Ca, Fe, Al, dan F. Fosfor organik mengandung senyawa yang berasal dari tanaman dan mikroorganisme dan tersusun dari asam nukleat, fosfolipid, dan fitin (Rao, 1994). Bentuk fosfor anorganik tanah lebih sedikit dan sukar larut. Walaupun terdapat CO2 didalam tanah tetapi menetralisasi fosfat tetap sukar, sehingga dengan
demikian P yang tersedia dalam tanah relatif rendah. Fosfor tersedia didalam tanah dapat diartikan sebagai P- tanah yang dapat diekstraksikan atau larut dalam air dan asam sitrat. P- organik dengan proses dekomposisi akan menjadi bentuk anorganik.
Pengaruh CO2 terhadap fosfor tanah adalah sebagai berikut :
Ca3(PO4)2 + 4 H2O + 4 CO2 → Ca(H2PO4)2 + 2 Ca(HCO3)2
P- tidak larut P larut dalam air
Biasanya fosfor dijumpai dalam jumlah yang banyak dalam biji, walaupun ia juga terdapat dalam semua bagian tanaman. Fosfor sebagian besar berasal dari pelapukan batuan mineral alami, sisanya berasal dari pelapukan bahan organik. Walaupun sumber fosfor didalam tanah mineral cukup banyak, tanaman masih bisa mengalami kekurangan fosfor. Pasalnya, sebagian besar fosfor terikat secara kimia oleh unsur lain sehingga menjadi senyawa yang sangat sukar larut dalam air. Mungkin hanya 1 % fosfor yang dapat dimanfaatkan oleh tanaman.
fosfat yang sukar larut dalam air sehingga tidak dapat digunakan oleh tanaman. Pada tanah ber pH tinggi, fosfor akan bereaksi dengan ion kalsium. Reaksi ini membentuk ion kalsium fosfat yang sifatnya sukar larut dan tidak dapat digunakan oleh tanaman. Dengan demikian, tanpa memperhatikan pH tanah, pemupukan fosfor tidak akan berpengaruh bagi pertumbuhan tanaman.
Selain pH, faktor lain yang menentukan pasokan fosfor pada tanaman adalah sebagai berikut :
a. Aerasi
Ketersediaan oksigen di dalam tanah (aerasi) diperlukan untuk meningkatkan pasokan fosfor lewat proses perombakan bahan organik oleh mikroorganisme tanah. Pada tanah padat atau tergenang air, penyerapan fosfor dan unsur- unsur lainnya akan terganggu.
b. Temperatur
Secara langsung temperatur kamar dapat meningkatkan atau menurunkan ketersediaan fosfor. Pada temperatur yang relatif hangat, ketersediaan fosfor akan meningkat karena proses perombakan bahan organik juga meningkat. Ketersediaan fosfor menipis di daerah yang bersuhu rendah.
c. Bahan organik
Sebagian besar fosfor yang mudah larut diambil oleh mikroorganisme tanah untuk pertumbuhannya. Fosfor ini akhirnya diubah menjadi humus. Karena itu, untuk menyediakan cukup fosfor, kondisi tanah yang menguntungkan bagi perkembangan mikroorganisme tanah perlu dipertahankan.
d. Unsur hara lain
Tercukupinya jumlah unsur hara lain dapat meningkatkan penyerapan fosfor. Ammonium yang berasal dari nitrogen dapat meningkatkan penyerapan fosfor. Kekurangan unsur hara mikro dapat menghambat respon tanaman terhadap pemupukan fosfor.
dimanfaatkan oleh tanaman. Fosfor terdapat pada seluruh sel hidup tanaman. Beberapa fungsi fosfor adalah membentuk asam nukleat (DNA dan RNA), menyimpan serta memindahkan energi Adenusin Tri Phosphate (ATP) dan Adenosin Di Phosphate (ADP) merangsang pembelahan sel, dan membantu proses Asimilasi serta respirasi . Fosfor berperan aktif dalam mentransfer energi didalam sel baik sel tanaman maupun hewan.
Pemupukan fosfor dapat merangsang pertumbuhan awal bibit tanaman. Fosfor merangsang pembentukan bunga, buah, dan biji. Bahkan mampu mempercepat pemasakan buah dan membuat biji menjadi lebih bernas. Pemupukan fosfor sangat diperlukan oleh tanaman yang tumbuh di daerah dingin, tanaman dengan perkembangan akar yang lambat atau terhambat, dan tanaman yang seluruh bagiannya dipanen.
Jika terjadi kekurangan fosfor, tanaman menunjukkan gejala pertumbuhan sebagai berikut :
a. Lambat dan kerdil
b. Perkembangan akar terhambat
c. Gejala pada daun sangat beragam, beberapa tanaman menunjukkan warna hijau tua mengkilap yang tidak normal.
d. Pematangan buah terhambat
e. Perkembangan bentuk dan warna buah buruk f. Biji berkembang secara tidak normal (Novizan, 2002).
2.2. Pupuk
Adapun tujuan pemupukan adalah :
a. Menambah zat hara dalam tanah sehingga kebutuhan makanan bagi tanaman dapat tercukupi.
b. Memperbaiki struktur tanah yaitu merubah zat zat yang semula tidak mudah diserap menjadi lebih mudah diserap oleh tanaman.
Secara umum dapat dikatakan bahwa manfaat pupuk adalah menyediakan unsur hara yang kurang atau bahkan tidak tersedia di tanah untuk mendukung pertumbuhan tanaman. Kandungan unsur dalam pupuk juga akan menghasilkan warna pupuk yang berlainan. Ada pupuk yang berwarna hitam karena banyak mengandung humus atau gambut, ada pupuk yang berwarna abu– abu, seperti pupuk TSP, karena diambil dari batuan fosfat yang berwarna demikian, dan ada pula pupuk yang berwarna putih bersih, seperti urea sebagai hasil dari proses kimia unsur nitrogen (Sutedjo, 2002).
2.3. Prinsip produksi pupuk fosfat
Pupuk superfosfat ; terbuat dari fosfat alam yang dicampur dengan asam belerang. Pupuk superfosfat berbentuk bubuk yang berwarna abu abu dengan kandungan fosfat antara 14–20 %. Sifatnya mudah larut dalam air dan agak sedikit higroskopis. Pupuk ini juga mampu mengikat amoniak. Pupuk superfosfat buatan ini ada dalam dua bentuk yaitu Double Superfosfat (DS) dan Triple Superfosfat (TSP).
Superfosfat merupakan pupuk yang dapat bereaksi dengan cepat. Hal ini disebabkan oleh mudah larutnya kalsium fosfat asam primer. Di dalam pabrik superfosfat, kalsium fosfat alam diolah dengan asam sulfat menjadi kalsium fosfat primer, Reaksinya berlangsung sebagai berikut :
Ca3(PO4)2 + 2 H2SO4 → Ca(H2PO4)2 + 2 CaSO4
Kalsium fosfat asam primer gips
Ca(H2PO4)2 + Ca(HCO3)2 → 2 CaHPO4 + 2 H2O + 2 CO2↑
2 CaHPO4 + 2 H2O + 2CO2 → Ca3(PO4)2 + 2 H2O + 2 CO2↑
Dengan cara inilah kalsium fosfat yang tidak larut mengendap di dalam tanah dalam bentuk yang sangat halus. Karena sangat halusnya, maka sangat mudah
ditransformasi dengan asam karbonat dan asam lainnya menjadi kalsium fosfat asam primer yang mudah diserap (Rinsema,1993) .
Jenis pupuk SP-36 ini muncul sebagai akibat sulitnya mendapatkan kandungan dasar pupuk TSP yang masih harus diimpor. Oleh karena itu, kadar fosfat pada SP- 36 jauh lebih rendah dari TSP (Marsono, 2001). Kandungan pupuk SP-36 adalah P2O5
total : 36 %; P2O5 tersedia : 34 % ; P2O5 larut air : 30 %. Pupuk ini terbuat dari fosfat
alam dan sulfat. Berbentuk butiran dan berwarna abu abu. Sifatnya agak sulit larut didalam air dan bereaksi lambat sehingga selalu digunakan sebagai pupuk dasar. Reaksi kimianya tergolong netral, tidak higroskopis, dan tidak bersifat membakar (Novizan, 2002).
Pupuk SP-36 mempunyai keunggulan yaitu :
a. Kandungan hara fosfor dalam bentuk P2O5 tinggi yaitu sebesar 36 %.
b. Bersifat netral sehingga tidak mempengaruhi kemasaman tanah.
c. Tidak mudah menghisap air, sehingga dapat disimpan cukup lama dalam kondisi penyimpanan yang baik.
d. Dapat dicampur dengan pupuk urea atau pupuk ZA pada saat penggunaan
TSP adalah pupuk superfosfat yang didatangkan dari Amerika Serikat pengganti pupuk DS dari Belanda. Pupuk P ini memiliki sifat dan warna yang sama dengan pupuk DS, kecuali bentuknya butiran dan granuler. Pada dasarnya, TSP merupakan peningkatan dari pupuk superfosfat yang lebih dahulu muncul pasaran. Bahan dasar utama TSP adalah asam fosfat dan kalsium.
[
Ca3(PO4)2]
3 .CaF2 + 12H3PO4 + 9H2O → 9Ca(H2PO4)2 + CaF2(Follet, 1981)
Pupuk TSP akan diikat oleh tanah dengan cukup kuat dan relative kurang tercuci. Kandungan P dalam bentuk P2O5 pada TSP adalah 46 %. TSP merupakan
pupuk fosfat terbaik. Kandungan P paling tinggi dan mudah larut, tetapi memerlukan biaya tinggi untuk membuatnya.
2.4. Pupuk Majemuk yang mengandung fosfat
Ammonium fosfat ; dihasilkan dari hasil reaksi antara amonia dengan asam fosfat atau pencampuran fosfor dengan asam sulfat. Ada beberapa jenis pupuk ammonium fosfat yang banyak digunakan, diantaranya Monoammonium Phosphate (MAP),
Diammonium Phosphate (DAP) dan Ammonium Phosphate-Sulfate.
MAP diperoleh dari hasil reaksi antara amonia dengan asam fosfat serta mengandung 12 % N dan 61 % P2O5,
NH3 + H3PO4 → NH4H2PO4
Monoammonium Phosphate (MAP)
Dalam Diammonium Phosphate (DAP) terkandung 21 % N dan 53 % P2O5
2NH3 + H3PO4 → (NH4)2HPO4
Diammonium Phosphate (DAP)
Amonia juga dapat direaksikan dengan cara mencampurkan fosfor dengan asam sulfat yang menghasilkan ammonium phosphate-sulfate yang terdiri dari 16 % N dan 20 % P2O5.
4H3PO4 + xH2SO4 + (4 + 2x)NH3 →4NH4H2PO4.x(NH4)2SO4
Ammonium Phosphate-Sulfate
Bahan utama pupuk amophos adalah monoammonium fosfat. Bentuknya berupa butiran dan berwarna abu-abu muda. Ada dua macam pupuk amophos, yaitu amophos A yang mengandung N 11 % dan P2O5 48% serta amophos B yang
mengandung N 16,5 % dan P2O5 20 %. Kedua macam pupuk ini larut dalam air dan
tidak higroskopis.
Pupuk NPK dibuat melalui proses industri berteknologi tinggi sehingga dihasilkan butiran yang homogen. Setiap butir pupuk Phonska mengandung tiga macam unsur hara utama yaitu Nitrogen (N), Fosfor (P), Kalium (K) yang diperkaya dengan unsur hara belerang (S) dalam bentuk larut air, sehingga mudah diserap akar tanaman Pupuk NPK merupakan pupuk majemuk cepat tersedia yang paling dikenal saat ini. Bentuk pupuk NPK yang beredar di pasaran adalah pengembangan dari bentuk-bentuk NPK lama yang kadarnya masih rendah. Kadar NPK yang banyak beredar adalah 15-15-15, 16-16-16 dan 8-20-15. Kadar lain yang tidak terlalu umum beredar adalah 6-12-15, 12-12-12, atau 20-20-20.
NPK Mutiara adalah pupuk NPK produk BASF dengan kadar 16-16-16. Pupuk ini berbentuk butiran berwarna abu-abu dan agak higroskopis. Dalam pemasarannya pupuk ini dikemas dalam ukuran 1 kg dan 5 kg. Pupuk yang diimpor dari Norwegia ini termasuk diminati banyak orang (Marsono, 2004).
2.5. Klasifikasi fosfor
Kelarutan fosfor didalam fosfat pembawa yang berbeda akan bervariasi. Kelarutan pupuk fosfat dalam air tidak selalu menjadi kriteria yang terbaik dalam ketersediaan unsur ini pada tanaman. Penentuan fosfor tidaklah mudah ketika ketersediaan unsur- unsur pupuk ditentukan dengan cepat dalam sampel. Metode kimia yang telah dikembangkan dimana penilaian yang cukup baik adalah larut dalam air, ketersediaan, dan kandungan fosfor total dari pupuk.
pertama kali diekstraksi dengan air, kemudian endapannya disaring, dan fosfor yang terkandung dalam filtrat ditentukan. Kandungan fosfor dari filtrat ditentukan dan dinyatakan sebagai persentase berat total sampel. Ini mewakili fraksi sampel yang larut dalam air.
Fosfor yang larut dalam sitrat. Residu tersebut ditambahkan larutan ammonium sitrat 1 N, kemudian diekstraksi. Kandungan fosfor dari filtrat ditentukan dan dinyatakan sebagai persentase berat total sampel, ini dinamakan fosfor yang larut dalam sitrat.
Fosfor tersedia. Jumlah fosfor yang larut dalam air dan larut dalam asam sitrat 2 % mewakili taksiran yang tersedia untuk tanaman.
Fosfor total. Fosfor total dapat ditentukan secara langsung tanpa langkah – langkah yang digambarkan (Tisdale, 1975). Reaksi penentuan fosfat adalah sebagai berikut :
H3PO4 + 12 H2MoO4 → H3P
[
Mo12O40]
+ 10 H2OBiru molibdem
Mo (VI) → Mo (V)
( Hansen, 1981)
2.6.Metode Analisis Kuantitatif fosfat
Ada beberapa metode analisis kuantitatif fosfat, yaitu : 1. Metode asam askorbat
sederhana, cepat dan akurat. Akan tetapi reagen yang digunakan kurang stabil (Benhart, 1954).
2. Metode SnCl2( Deniges methods)
SnCl2 merupakan salah satu pereduksi yang mempunyai kesensitifan besar,
tetapi pereaksi ini kurang stabil dan harus digunakan dalam keadaan baru (Abbott, 1963). Dalam metode ini, SnCl2 bereaksi dengan ammonium molibdat membentuk
kompleks berwarna biru yang mengabsorpsi maksimum cahaya pada panjang gelombang 690 nm. Kepekatan warna yang dihasilkan tergantung pada proporsi reagen yang ditambahkan, temperatur dan waktu reaksi. Metode ini terganggu oleh silikat dan arsenit (positif) sedangkan arsenat, fluorida, thorium, bismut, sulfida, tiosianat (negatif). Warna yang terbentuk lebih stabil dibandingkan dengan metode asam askorbat.
3. Metode Vanadat
Fosfat bereaksi dengan vanadat membentuk senyawa kompleks berwarna kuning. Pencampuran pereaksi vanadat dan molibdat harus dilakukan beberapa hari sebelum digunakan karena sangat cenderung untuk mengendap. Bahan bahan organik yang turut tercampur harus terlebih dahulu dihilangkan agar tidak mengganggu warna yang dihasilkan menggunakan pereaksi pengoksidasi (The tintometer, 1967). Warna kompleks fosfovanadomolibdat lebih stabil dibandingkan warna kompleks biru-molibde m.
4. Metode hidroquinon – molibdat
Salah satu pereduksi yang paling klasik adalah hidroquinon yang pada saat sekarang ini kurang dianggap penting., namun masih digunakan dalam Association of
Official analytical Chemistry (AOAC). Pada metode ini ammonium molibdat
direaksikan dengan larutan fosfat membentuk ammonium fosfomolibdat berwarna kuning, kemudian direduksi dengan hidroquinon. Waktu tunggu untuk pembentukan warna maksimum adalah selama 5 menit.
Metol (β-methylamino phenol sulphate) salah satu pereduksi yang cukup stabil dengan harga yang murah. Dalam metode ini, bila sampel mengandung NO3- lebih
dari 1 mg boleh digunakan Comparator, dan jika lebih dari 3 mg harus menggunakan pereaksi Neshler. Metode ini 500 kali kurang sensitif terhadap silika dibanding fosfat. Selain itu reaksi arsenit dan fosfat akan memberi warna yang hampir sama sehingga arsenit perlu dihilangkan dengan penambahan H2S, diikuti penyaringan dan
penguapan. Komponen lain seperti gula, laktat, citrat, tartarat, oksalat dan garam-garam organik lainnya akan menekan intensitas warna yang dihasilkan sehingga semua komponen tersebut juga harus dihilangkan terlebih dahulu .
6. Metode amino-naftol-asam sulfonat
Metode ini didasarkan atas modifikasi dari Fisk dan prosedur Subbarow. Fosfat anorganik direaksikan dengan ammonium molibdat, selanjutnya direduksi dengan amino-naftol-asam sulfonat sehingga dihasilkan kompleks berwarna biru (The tintometer, 1967). Metode ini pada umumnya kurang sensitif. Waktu reaksi yang diperlukan untuk pengembangan warna adalah 15 menit (Snell, 1948).
7. Metode Valin Vanadomolibdat Tablet
Metode ini telah disederhanakan dengan menggunakan pereaksi dalam bentuk
tablet. Sama halnya seperti vanadat, kompleks yang dihasilkan berwarna kuning (The tintometer, 1967)
BAB 3
3.1. Alat – alat
- Alat - alat gelas - Termometer 100 oC - Pengaduk bermagnit
- Lempeng pemanas berpengaduk PMC - Kertas saring Whatman No. 41
- Neraca analitis Mettler pm 400
- Oven pengering Fisher Scientific - Spekrofotometer SP 300 Optima
- pH-meter Hanna Instrumen
- Cawan porselin
3.2. Bahan – bahan
- Kalium dihidrogen fosfat p.a E’Merk
- Asam sulfat p.a E’Merk
- Asam nitrat p.a E’Merk
- Ammonium molibdat p.a E’Merk - Asam askorbat p.a E’Merk - Kalium antimonil tartarat p.a E’merk - Asam sitrat p.a E’Merk - Akuades
3.3. Prosedur penelitian
A. Larutan ammonium molibdat 4 %
Ditimbang sebanyak 2 gram (NH4)6Mo7O24.4H2O, dimasukkan kedalam gelas
beaker, dilarutkan dengan akuades secukupnya, dimasukkan dalam labu takar 50 mL, diencerkan dengan akuades hingga garis tanda dan dihomogenkan.
B. Larutan H2SO4 5 N
Dipipet sebanyak 14 mL H2SO4 (p), dimasukkan dalam labu takar 100 mL
yang berisi 50 mL akuades, diencerkan dengan akuades hingga garis tanda dan dihomogenkan.
C. Larutan Kalium antimonil tartarat
Ditimbang sebanyak 0,105 gram K(SbO)C4H4O6.1/2H2O, dimasukkan dalam
gelas beaker, dilarutkan dengan akuades, dimasukkan dalam labu takar 50 mL, diencerkan dengan akuades hingga garis tanda dan dihomogenkan.
D. Larutan asam askorbat 0,1 M
Ditimbang sebanyak 0,880 gram C6H8O6, dimasukkan dalam gelas beaker,
dilarutkan dengan akuades, dimasukkan dalam labu takar 50 mL, diencerkan dengan akuades hingga garis tanda dan dihomogenkan.
E. Pembuatan pereaksi campuran pengkompleks
Dipipet sebanyak 50 mL H2SO4 5 N kedalam labu takar 100 mL, kemudian
ditambahkan berturut-turut 5 mL larutan kalium antimonil tartarat, 15 mL larutan ammonium molibdat, 30 mL asam askorbat 0,1 M dan dihomogenkan.
F. Larutan asam sitrat 2 %
Ditimbang sebanyak 5 gram C6H8O7.H2O, dimasukkan dalam gelas beaker,
dilarutkan dengan akuades, dimasukkan dalam labu takar 250 mL, diencerkan dengan akuades hingga garis tanda dan dihomogenkan.
G. Larutan standar P2O5 500 mg/L
Sebanyak 0,958 gram KH2PO4 yang telah dikeringkan dalam oven pada suhu
dengan akuades hingga garis tanda dan dihomogenkan. Dari larutan ini dibuat larutan 50 dan 5 mg/L. Larutan standar P2O5 untuk pembuatan kurva kalibrasi digunakan
konsentrasi P2O5 0,4; 0,8; 1,2; 1,6; 2,0 dan 2,4 mg/L yang dibuat dengan
mengencerkan larutan 5 mg/L P2O5.
3.3.2. Preparasi sampel
A. Untuk analisis P2O5 total
Sampel pupuk dihaluskan dengan lumpang, diayak dan dikeringkan dalam oven pada suhu 105 oC selama 2 jam, sebanyak 0,2 gram sampel pupuk kering dimasukkan dalam gelas beaker 100 mL, ditambahkan 2 mL H2SO4(p); 1,5 mL
HNO3(p) dan akuades secukupnya, selanjutnya dipanaskan hingga timbul asap putih,
didinginkan, disaring dengan kertas saring Whatman No.41, filtrat dimasukkan dalam labu takar 100 mL dan diencerkan dengan akuades hingga garis tanda dan dikocok hingga homogen.
B. Untuk analisis P2O5 yang larut dalam asam sitrat 2 %
Sebanyak 0,2 gram sampel yang telah dikeringkan ditambahkan dengan 30 mL larutan C6H8O7.H2O 2 % dalam gelas beaker 100 mL, diaduk dengan magnetikstirer
selama 45 menit, kemudian disaring, filtrat ditampung dalam labu takar 100 mL, kemudian diencerkan hingga garis tanda dan dihomogenkan.
C. Untuk analisis P2O5 yang larut dalam air
Sebanyak 0,2 gram sampel kering dilarutkan dengan akuades dalam gelas beaker 100 mL, diaduk dengan magnetikstrirer selama 45 menit, setelah itu disaring, filtrat ditampung kedalam labu takar 100 mL, diencerkan hingga garis tanda, kemudian dihomogenkan (SNI 02-3769-1995).
3.3.3. Penentuan waktu tunggu (Operating time)
absorbansinya pada λ = 880 nm., prosedur yang sama dilakukan untuk variasi waktu 10; 15; 20; dan 25 menit.
3.3.4. Penentuan panjang gelombang maksimum larutan standar P2O5
Sebanyak 10 mL larutan standar P2O5 1,2 mg/L dipipet ke dalam tabung
reaksi, ditambahkan 1,5 mL pereaksi campuran, dibiarkan selama 15 menit, diukur absorbansinya pada λ = 860-900 nm.
3.3.5. Pembuatan kurva kalibrasi larutan standar
Sebanyak 10 mL larutan standar P2O5 0,4 mg/L dipipet ke dalam tabung
reaksi, ditambahkan 1,5 mL pereaksi campuran, dibiarkan selama 15 menit, diukur absorbansinya pada λ= 880 nm, prosedur yang sama dilakukan terhadap larutan standar 0,4 ; 0,8 ; 1,2 ; 1,6 ; 2,0 dan 2,4 mg/L, pengukuran diulang sebanyak 3 kali dan dibuat kurva kalibrasi.
3.3.6. Analisis sampel secara spektrofotometri
Sebanyak 10 mL larutan sampel dipipet ke dalam tabung reaksi, ditambahkan 1,5 mL pereaksi campuran, dibiarkan selama 15 menit, diukur absorbansinya pada
λ = 880 nm, perlakuan yang sama dilakukan terhadap P2O5 yang dapat larut dalam
asam sitrat 2 % dan P2O5 yang larut dalam air.
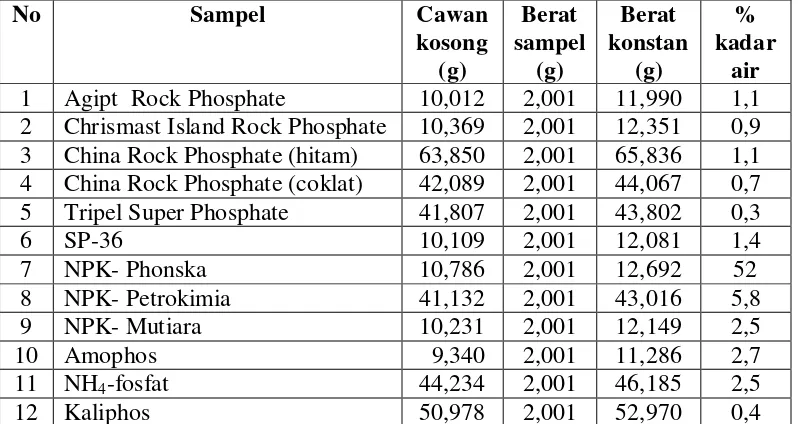
3.3.7. Penentuan % kadar air sampel
Ditimbang cawan kosong dengan neraca analitis, ditambahkan 2 gram sampel, dikeringkan dalam oven pada suhu 105 oC selama 2 jam, didinginkan dalam desikator selama 2 jam atau lebih, ditimbang beratnya, dilakukan hal yang sama sampai diperoleh berat yang konstan.
Sebanyak 0,3 gram sampel dimasukkan dalam gelas beaker, ditambahkan 40 mL akuades, dikocok dengan magnetikstirer, disaring, lalu diukur pH-nya menggunakan pH-meter.
3.4. Bagan penelitian
Digiling halus, kemudian diayak
Dikeringkan dalam oven pada suhu Dilarutkan dengan air 105 oC selama 2 jam
Diukur pHnya dengan pH-meter
Ditimbang sebanyak 0,2 gram dan dimasukkan dalam gelas beaker
Dilarutkan * dan disaring dengan menggunakan kertas saring Whatman No. 41
Dipipet sebanyak 10 mL dan dimasukkan kedalam tabung reaksi
Ditambahkan 1,5 mL pereaksi campuran
Dibiarkan selama 15 menit
Diukur absorbansinya pada λ= 880 nm
* Catatan : 1. Penentuan P2O5 total, dilarutkan dengan H2SO4 dan HNO3 pekat
2. Penentuan P2O5 larut dalam asam sitrat 2%, digunakan asam sitrat 2%
3. Penentuan P2O5 larut dalam air, digunakan akuades
Residu
Larutan berwarna biru
Kandungan P2O5
Sampel halus
pH
Sampel kering Kadar air
BAB 4
HASIL DAN PEMBAHASAN
4.1. Hasil penelitian dan pembahasan
Waktu tunggu (operating time) dan panjang gelombang maksimum
Senyawa fosfomolibdat sebagai senyawa kompleks berwarna kuning akan menjadi berwarna biru setelah direduksi asam askorbat, pada pengukuran spektrofotometri perlu ditentukan waktu tunggu (operating time) yaitu pada saat mana suatu larutan berwarna mencapai intensitas warna yang optimal sebelum diukur absorbansinya. Berdasarkan pengukuran absorbansi yang dilakukan dengan variasi waktu tunggu 5 sampai 25 menit sehingga diperoleh absorbansi maksimum dengan waktu tunggu 15 menit (Tabel 4.1). Pengukuran absorbansi sebelum dan sesudah 15 menit mengurangi kepekaan pengukuran karena absorbansi yang diperoleh lebih kecil.
Tabel 4. 1. Data penentuan waktu tunggu (operating time)
Waktu (menit) Absorbansi
5 0,124
10 0,126
15 0,127
20 0,123
25 0,121
Menurut literatur kompleks fosfomolibdat berwarna biru mempunyai absorbansi maksimum pada λ= 880 nm. Dari hasil penelitian yang dilakukan dengan variasi panjang gelombang mulai 860-900 nm (Tabel 4.2) menunjukkan adanya kesesuaian antara teori dengan data yang diperoleh sehingga metode pengukuran selanjutnya dilakukan pada λ= 880 nm.
maksimum P2O5
Untuk menghitung kandungan P2O5 dalam sampel berdasarkan nilai
absorbansi diperlukan kurva kalibrasi dari hubungan antara absorbansi yang terukur terhadap konsentrasi P2O5. Pengukuran absorbansi larutan seri standar P2O5 dibuat
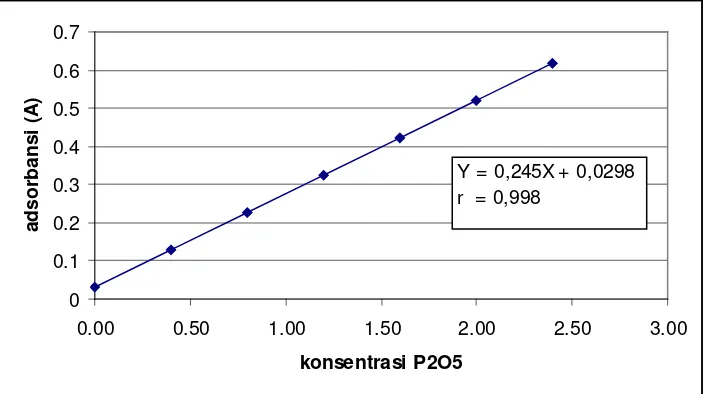
dengan kisaran konsentrasi 0,4 mg/L sampai 2,4 mg/L tercantum pada Tabel 3 pada lampiran. Persamaan garis kurva kalibrasi dapat dihitung dari persamaan garis regresi. Dari hasil perhitungan diperoleh persamaan garis regresi Y = 0,245X + 0,0298 yang ditunjukkan pada Gambar 1.
0.00 0.50 1.00 1.50 2.00 2.50 3.00
konsentrasi P2O5
Gambar 1. Kurva Kalibrasi Larutan Standar P2O5
Dari hasil perhitungan diperoleh bahwa harga koefisien korelasinya sebesar 0,998. Hal ini menyatakan adanya hubungan linear atau korelasi positif antara konsentrasi P2O5 dengan absorbansi.
Batas deteksi dari pengukuran P2O5 yang diperoleh dari hasil perhitungan
dalam penelitian ini adalah 0,0624 mg/L. Hal ini menunjukkan batas pengukuran spektrofotometer untuk fosfat dalam sampel hanya dapat dilakukan jika konsentrasi fosfat diatas 0,0624 mg/L.
Kandungan P2O5 dalam sampel
Di dalam penelitian ini diperoleh bahwa kadar fosfor sebagai P2O5 di dalam
setiap sampel sesuai dengan yang terdapat dalam kemasannya. Hal itu menunjukkan bahwa % P2O5 yang terdapat dalam sampel telah memenuhi Standar Nasional
Indonesia (SNI) tentang pupuk.
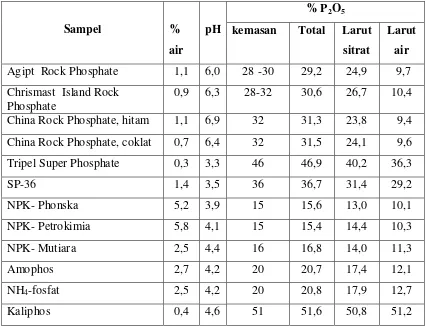
Tabel 4.3. Hasil pengujian beberapa parameter terhadap sampel pupuk fosfat
Berdasarkan uji pH yang dilakukan pada tiap sampel pupuk fosfat dengan cara melarutkan sampel dalam air dan ditentukan pH-nya menggunakan pH-meter dapat dikategorikan kedalam 3 kelompok yaitu : (1) batuan fosfat yang terdiri dari Agift Rock Phosphate, Chrismast Island Rock Phosphate, China Rock Phosphate (hitam) dan China Rock Phosphate (coklat) memiliki pH antara 6,0 sampai 6,9. (2) Pupuk tunggal (SP-36 dan Tripel Super Phosphate) mempunyai pH 3,3 sampai 3,5 dan (3) Pupuk majemuk yang terdiri atas NPK-Phonska, NPK-Petrokimia, NPK-Mutiara, Amophos, NH4-fosfat dan Kaliphos mempunyai pH sekitar 3,9 sampai 4,6. Hal ini
menyatakan bahwa tiap pupuk mempunyai tingkat keasaman yang berbeda-beda dalam air.
Kadar air
Menurut ketentuan SNI 02-3769-1995 kadar air dalam pupuk adalah < 5 %. Berdasarkan hasil penelitian yang telah dilakukan terhadap tiap sampel pupuk diperoleh kadar air yang memenuhi ketentuan SNI kecuali Phonska dan NPK-Petrokimia yang telah melewati batas maksimal kandungan air dengan kadar air 5,2 % dan 5,8 %. Hal ini disebabkan karena kedua jenis pupuk tersebut mempunyai sifat yang agak higroskopis.
KESIMPULAN DAN SARAN
5.1. Kesimpulan
1. Dari hasil penelitian ini diperoleh bahwa kandungan P2O5 total sampel pupuk yang
diambil secara acak dari berbagai toko di kota Medan sesuai dengan % P2O5 total
yang terdapat dalam kemasannya sehingga dapat dinyatakan bahwa pupuk tersebut bebas dari pemalsuan.
2. Dari hasil penelitian ini juga diperoleh bahwa % P2O5 yang larut dalam asam sitrat
2 % dan yang larut dalam air sebanding dengan kandungan P2O5 total-nya.
Kecuali Rock Phosphate, lebih kecil dari 50 % dari fosfat dalam sampel tersebut larut dalam air. Hal ini berarti respon penggunaannya pada tanaman lebih cepat dibanding pupuk lainnya.
5.2. Saran
Untuk peneliti selanjutnya diperlukan cara-cara identifikasi yang cepat dan lebih murah terhadap pupuk yang dipalsukan sehingga pemakai lebih mudah untuk mengenalinya.
Abbott, D.C., Emsden, G.E., Harris, J.R., 1963. Short Paper A Method for Determining Ortophospahate in Water. London : Department of Scientific and Industrial Research.
Bausch, Lomb. 1974. Analytical Systems Division. New York : Rochester.
Bernhart, D.N., Wreath, A.R., 1954. Analytical Chemistry. Volume 27. Chicago : Research Laboratories
Effendi, H., 2003. Telaah Kualitas Air. Yogyakarta : Penerbit Kanisius.
Engelstad, O.P., 1997. Teknologi Dan Penggunaan Pupuk. Edisi Ketiga. Yogyakarta : Gadjah Mada University Press.
Follett, R.H., Murphy, L.S., Donahue, R.L., 1981. Fertilizers and Soil Amendments. New Jersey : Prentice hall Inc.
Hanafiah, K.A., 2005. Dasar - dasar Ilmu Tanah. Jakarta : PT. Raja Grafindo Persada.
Hansen, E.H., Ruziska, J., 1981. Flow Injection Analysis. Volume 62. New York : John Wiley and Sons.
Http://www.sumenep.go.id . Diakses tanggal 20 Mei 2008
Isnaini,M., 2006. Pertanian Organik. Cetakan I. Yogyakarta : Penerbit Kreasi Wacana.
Jones, U.S., 1982. Fertilizers and Soil Fertility, Second Edition. Virginia : Reston Publishing Company.
Marsono, Sigit, P., 2001. Pupuk Akar Jenis & Aplikasi. Jakarta. : Penerbit Swadaya. Marsono, Lingga, P., 2004. Petunjuk Penggunaan Pupuk. Jakarta : Penerbit Swadaya. Novizan, 2002. Petunjuk Pemupukan Yang Efektif. Jakarta : PT. Agro Media Pustaka. Rao, N.S.S., 1994. Mikroorganisme Tanah dan Pertumbuhan Tanaman. Edisi Kedua.
Jakarta : UI Press.
Rinsema, W.J.,1993. Pupuk dan Cara Pemupukan. Jakarta : PT. Bhratara Niaga Media.
Rosmarkam, A., Yuwono, N.W., 2002. Ilmu Kesuburan Tanah. Yogyakarta : Penerbit Kanisius.
SNI 02-3769-1995. Diakses tanggal 26 November 2008
Sutedjo, M.M., 2002. Pupuk dan Cara Pemupukan. Jakarta : Penerbit Rineka Cipta. The Tintometer Ltd. 1967. Colorimetric Chemical Analytical Methods. England : Salisbury.
Tisdale, S.L., Nelson, W.L., 1975. Soil Fertility and Fertilizers. New York : Mac Millan Publishing Co Inc.
1.1. Menentukan Persamaan Garis Regresi Kurva Kalibrasi
Setelah diperoleh hasil pengukuran absorbansi dari larutan standar fosfat maka absorbansi dialurkan terhadap konsentrasi larutan standar untuk mendapatkan kurva kalibrasi berupa garis linier. Selanjutnya persamaan garis regresi kurva kalibrasi dihitung menggunakan metode Least square sebagai berikut :
No Xi Yi Xi – X Yi – Y ( Xi – X )2 ( Yi – Y )2 (Xi –X) (Yi – Y)
Persamaan garis regresi untuk kurva kalibrasi dapat ditentukan dari persamaan : Y = aX + b
Dimana : a = slope
b = intersep
Nilai a dapat ditentukan dengan :
(
)(
)
a =
Nilai b diperoleh melalui substitusi nilai a ke dalam persamaan berikut :
: Y= aX + b b = Y - aX
= 0,3728 – ( 0,2450 )( 1,4 ) = 0,3728 – 0,343
= 0,0298
Maka persamaan gari regresi yang diperoleh adalah :
Y = 0,2450X + 0,0298
1.2. Perhitungan Koefisien Kolerasi
Kofisien kolerasi (r) dari persamaan kurva kalibrasi dapat ditunjukkan sebagai berikut :
Dengan mensubstitusikan nilai konsentrasi larutan standar (Xi) ke persamaan garis
regresi maka diperoleh nilai Y yang baru (Ŷ), seperti yang tercantum pada tabel :
No Xi Yi Ŷ ( Xi )2 |Yi – Ŷ| ( Yi – Ŷ )2
(
)
Batas deteksi dapat dihitung dengan persamaan :
3 Sb = Y – Yb
Y = 3 Sb + Yb
Dimana :
Y = sinyal pada batas kadar deteksi Sb = standar deviasi
Yb = Intersep kurva kalibrasi
Persamaan kurva kalibrasi : Y = 0,2450X + 0,0298 , dimana Yb = 0,0298 dan
x
Sy = 0,0086
Maka dengan mensubstitusi Yb dan Sb pada persamaan Y = 3 Sb + Yb diperoleh nilai batas deteksi :
Y = 3 Sb + Yb
= 3 ( 0,0051 ) + 0,0298 = 0,0153 + 0,0298 = 0,0451
0,0451 = 0,2450X + 0,0298
Jadi batas deteksi pangukuran fosfat untuk penelitian ini adalah 0,0624 mg/L.
1. 5. Penentuan % P2O5 pada Sampel
Kadar P2O5 dalam sampel dapat ditentukan dengan menggunakan metode kurva
kalibrasi dengan mensubstitusi nilai Y (absorbansi) yang diperoleh dari pengukuran absorbansi terhadap persamaan garis regresi dari kurva kalibrasi.
Untuk Agipt Rock Phosphate
Pengukuran I Y1 = 0,308
Dengan mensubstitusi Y terhadap persamaan garis regresi beri Y = 0,2450X + 0,0298, maka diperoleh :
Sehingga % P2O5 dapat ditentukan dengan cara mensubstitusi nilai X pada persamaan
pengukuran % P2O5 larut dalam asam sitrat 2 % ditunjukkan pada Tabel 4.9
sedangkan % P2O5 yang larut dalam air ditunjukkan pada Tabel 4.10 (setiap
pengukuran % P2O5 masing - masing dilakukan sebanyak 3 kali ulangan).
1.6. Penentuan % kadar air dalam sampel
Kadar air dalam sampel dapat ditentukan sebagai berikut :
% kadar air =
berat awal = berat cawan kosong + berat sampel berat akhir = berat konstan
Untuk data hasil pengukuran % kadar air sampel seluruhnya ditunjukkan pada Tabel 4.11 pada lampiran.
1.7. Penentuan Persentase P2O5 yang larut dalam asam sitrat 2% dan air atas dasar berat P2O5 dalam sampel
Persentase P2O5 yang larut dalam asam sitrat 2 % dan air dapat ditentukan sebagai
% P2O5 = 2 , 29
9 , 24
x 100 %
= 85 %
Untuk data hasil perhitungan % P2O5 yang larut dalam asam sitrat 2 % dan air dapat
ditunjukkan pada Tabel 4.12 pada lampiran
Konsentrasi P2O5 (mg / L) Absorbansi
0,4 0,118
0,8 0,228
1,2 0,327
1,6 0,441
2,0 0,512
2,4 0,611
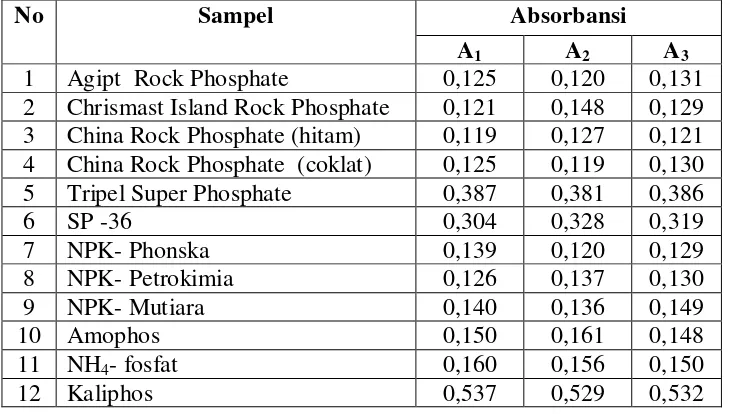
Tabel 4.5. Data absorbansi penentuan P2O5 total pada λ = 880 nm
No Sampel Absorbansi
A1 A2 A3
1 Agipt Rock Phosphate 0,308 0,320 0,325 2 Chrismast Island Rock Phosphate 0,330 0,339 0,321 3 China Rock Phosphate (hitam) 0,338 0,330 0,345 4 China Rock Phosphate (coklat) 0,336 0,334 0,349 5 Tripel Super Phosphate 0,502 0,481 0,488
6 SP -36 0,403 0,388 0,380
7 NPK- Phonska 0,184 0,188 0,175
8 NPK- Petrokimia 0,188 0,177 0,180
9 NPK- Mutiara 0,189 0,195 0,201
10 Amophos 0,240 0,228 0,231
11 NH4- fosfat 0,248 0,230 0,226
12 Kaliphos 0,541 0,530 0,539
No Sampel Absorbansi
Tabel 4.7. Data absorbansi penentuan P2O5 yang larut dalam air pada λ = 880 nm
No Sampel % P2O5
Tabel 4. 9. Hasil perhitungan P2O5 yang larut dalam asam sitrat 2 %
No Sampel % P2O5
No Sampel % P2O5
Tabel 4.11. Data penentuan % kadar air
No Sampel Cawan
No Sampel % P2O5 Total Larut
sitrat 2 %
Larut air 1 Agipt Rock Phosphate 29,2 85,2 33,2 2 Chrismast Island Rock Phosphate 30,6 87,2 34,9 3 China Rock Phosphate (hitam) 31,3 76,0 30,0 4 China Rock Phosphate (coklat) 31,5 76,5 30,4 5 Tripel Super Phosphate 46,9 85,7 77,3
6 SP-36 36,7 85,5 79,5
7 NPK- Phonska 15,6 83,3 64,7
8 NPK- Petrokimia 15,4 93,5 66,8
9 NPK- Mutiara 16,8 83,3 67,2
10 Amophos 20,7 84,0 58,4
11 NH4-fosfat 20,8 86,0 61,0
12 Kaliphos 51,6 98,4 99,2
850 860 870 880 890 900 910