SKRIPSI
UPAYA PENINGKATAN DERAJAT DEASETILASI PADA KITOSAN CANGKANG KERANG KAMPAK (Atrina pectinata) MELALUI
PROSES DEASETILASI KITIN SECARA BERTAHAP
PROGRAM STUDI BUDIDAYA PERAIRAN
Oleh :
PINTA PURBOWATI
SURABAYA – JAWA TIMUR
FAKULTAS PERIKANAN DAN KELAUTAN UNIVERSITAS AIRLANGGA
RINGKASAN
Pinta Purbowati. Upaya Peningkatan Derajat Deasetilasi Pada Kitosan Cangkang Kerang Kampak (Atrina pectinata) Melalui Proses Deasetilasi Kitin Secara Bertahap. Dosen Pembimbing Dr. Laksmi Sulmartiwi, S.Pi., MP. dan Kustiawan Tri Pursetyo, S.Pi., M.Vet.
Saat ini banyak dilakukan penelitian mengenai pemanfaatan limbah dari kerang sehingga bermanfaat menjadi sumberdaya lain yang berbasis zero waste salah satunya menjadi kitosan. Kitosan merupakan turunan kitin yang terbentuk dari hasil ekstraksi rangka luar udang, kerang, atau rajungan melalui proses deasetilasi atau penghilangan gugus asetil yang menyisakan gugus amina bebas (Atmadja, 2014). Manfaat kitin dan kitosan di berbagai bidang industri moderen cukup banyak, diantaranya dalam industri farmasi, biokimia, bioteknologi, biomedikal, pangan, gizi, kertas, tekstil, pertanian, kosmetik, membran dan kesehatan (Sulistiyoningrum dkk., 2013).
industri kosmetika dan biomedis sedikitnya 80% dan 90 (Tsugita, 1997 dalam Yulina, 2011).
Penelitian ini bertujuan untuk mengetahui adanya pengaruh proses deasetilasi kitin secara bertahap terhadap derajat deasetilasi kitosan dari limbah cangkang kerang kampak (Atrina pectinata). Metode penelitian yang digunakan dalam penelitian ini adalah metode eksperimental dan dianalisis data secara statistik. Parameter utama pada penelitian ini adalah derajat deasetilasi kitosan.
SUMMARY
Pinta Purbowati. Effort To Increase Degree Of Deacetylation On Chitosan From Kampak Shell (Atrina Pectinata) With Multistage Deacetylation Process Of Chitin. Academic Advisor Dr. Laksmi Sulmartiwi, S.Pi., MP. dan Kustiawan Tri Pursetyo, S.Pi., M.Vet.
Research of the utilization fishery waste of shells that benefit into other resource-based on zero waste become chitosan. Chitosan is a derivative of chitin are formed from the exoskeleton extraction of shrimp, scallops or crab through the process of deacetylation or removal of acetyl groups which leaves a amine group (Atmadja, 2014). Benefits of chitin and chitosan in various industry quite a lot, including in the pharmaceutical industry, biochemistry, biotechnology, biomedical, food, nutrition, paper, textile, agriculture, cosmetics, and medical membrane (Sulistiyoningrum et al. 2013).
Quality of chitosan influenced by deacetylation degree which is one of the most important chemical characteristics. Deacetylation degree give affect in application of chitosan, due to the value of amina chain and used to differentiate between chitin and chitosan (Mastuti, 2005). Degree deacetylation of chitosan determined by several factors such as NaOH concentration, temperature and time process. In addition, multistage deacetylation process of chitin can affect degree deacetylation value of chitosan (Prasetyo, 2004 in Bahri et al. 2015). Degree deacetylation of chitosan minimum in food industry is 70%, while cosmetics industry and biomedical are 80% and 90% (Tsugita, 1997 in Yulina, 2011).
were analyzed statistically. The main parameters of this research is degree of deacetylation on chitosan.
KATA PENGANTAR
Bismillahirrahmanirrahim. Puji syukur kehadirat Allah SWT atas limpahan rahmat, taufiq, ridho dan hidayah-Nya, sehingga penulis dapat menyelesaikan skripsi tentangUpaya Peningkatan Derajat Deasetilasi Pada Kitosan Cangkang Kerang Kampak (Atrina pectinata) Melalui Proses Deasetilasi Kitin Secara Bertahap. Skripsi ini disusun sebagai salah satu persyaratan untuk memperoleh gelar Sarjana Perikanan pada Program Studi Budidaya Perairan, Fakultas Perikanan dan Kelautan Universitas Airlangga Surabaya.
Penulis menyadari bahwa laporan skripsi ini masih belum sempurna, sehingga kritik dan saran yang membangun sangat penulis harapkan demi perbaikan dan kesempurnaan Karya Ilmiah ini. Akhirnya penulis berharap semoga Karya Ilmiah ini bermanfaat dan dapat memberikan informasi kepada semua pihak, khususnya bagi mahasiswa Program Studi Budidaya Perairan, Fakultas Perikanan dan Kelautan Universitas Airlangga Surabaya guna kemajuan serta perkembangan ilmu dan teknologi dalam bidang perikanan, terutama bidang teknologi industri hasil perikanan
Surabaya, 15Agustus 2016
UCAPAN TERIMA KASIH
Pada kesempatan kali ini, dengan penuh rasa hormat dan kasih penulis mengucapkan terima kasih kepada:
1. Ibu Dr. Mirni Lamid, drh., MP. Dekan Fakultas Perikanan dan Kelautan Universitas Airlangga.
2. Bapak Boedi Setya Rahardja, Ir., MP. Dosen Wali yang telah memberikan saran, bimbingan, arahan, nasehat dan motivasi yang membangun.
3. Ibu Dr. Laksmi Sulmartiwi, S.Pi., MP. Dosen Pembimbing Utama dan Bapak Kustiawan Tri Pursetyo, S.Pi., M.Vet. DosenPembimbing Serta yang telah memberikan bimbingan, arahan, masukan, dan perbaikan sejak penyusunan usulan penelitian hingga penyelesaian Skripsi ini.
4. Agustono, Ir., M.Kes., Rahayu Kusdarwati, Ir., M.Kes., dan Muhammad Arief, Ir., M.Kes. Dosen Penguji yang telah memberikan banyak masukan, kritik dan saran untuk penyempurnaan Skripsi ini.
5. Semua dosen dan staf kependidikan Sub Bagian Akademik Fakultas Perikanan dan Kelautan Universitas Airlangga yang telah membantu dalam pelayanan administrasi dan perijinan.
6. Ayahanda Purbo Supiyono, dan Ibunda Anggarwati, serta kakak tersayang Dias Anggardi Perbowo atas segala dukungan materi dan moral yang selalu menyertai serta nasehat yang menjadi penguat dalam studi untuk selalu berjuang.
8. Faisal Aziz, atas semangat, doa serta berbagai bantuan yang tak terukur selama ini.
9. Rekan-rekan Barracuda angkatan 2012 jurusan Budidaya Perairan maupun Teknologi Industri Hasil Perikanan, serta senior FPK Mardiah Rahma Umami, Hana Lidiana, Mustika Alifa, Rinca Purnamawati, Nadia Fitrianti, Ervita Eka Rosawati, dan Dina Ningrum yang telah memberikan dukungan hingga koreksi dalam pelaksanaan maupun penyelesaian Skripsi.
DAFTAR ISI
2.1Klasifikasi dan Morfologi Kerang Kampak (A. pectinata) ... 5
2.2Habitat dan Penyebaran Kerang Kampak (A. pectinata) ... 6
2.3Kandungan Kimia Cangkang Kerang ... 7
2.4Kitin dan Kitosan ... 7
2.5Pembuatan Kitosan... 10
2.6Derajat Deasetilasi ... 11
2.7Mutu Kitosan ... 11
III. KONSEPTUAL PENELITIAN DAN HIPOTESIS ... 13
3.2Hipotesis ... 14
4.3.1 Rancangan Penelitian ... 16
4.4Pelaksanaan Penelitian ... 17
4.4.1 Persiapan Bahan Baku ... 17
4.4.2 Pembuatan Kitosan ... 18
4.4.3 Pengujian Karakteristik Kitosan ... 21
1. Rendemen ... 21
4.4.4 Parameter Pengamatan ... 24
4.5 Analisis Data ... 24
V. HASIL DAN PEMBAHASAN ... 25
DAFTAR TABEL
Tabel
Halaman
DAFTAR GAMBAR
Gambar
Halaman
1. Morfologi Kerang Kampak ... 5
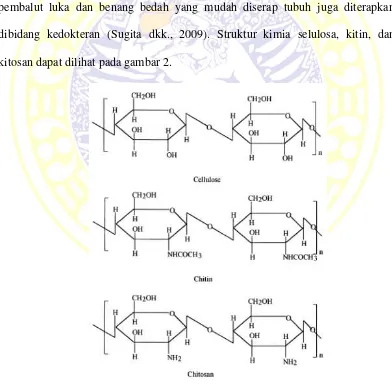
2. Struktur Kimia Selulosa, Kitin, dan Kitosan ... 9
3. Kerangka Konseptual ... 15
4. Diagram Alir Penelitian ... 20
5. Kitosan dengan proses deasetilasi kitin sebanyak 1 tahap, 2 tahap dan 3 tahap ... 25
6. Grafik rendemen kitosan dengan tahap proses deasetilasi kitin yang berbeda ... 26
7. Grafik derajat deasetilasi kitosan dengan tahap proses deasetilasi kitin yang berbeda ... 27
8. Grafik kelarutan kitosan dengan tahap proses deasetilasi kitin yang berbeda ... 28
9. Grafik kadar abu kitosan dengan tahap proses deasetilasi kitin yang berbeda ... 28
DAFTAR LAMPIRAN
Lampiran
Halaman
1. Data Rendemen Kitosan Cangkang Kerang Kampak (A. pectinata) ... 42
2. Data Derajat Deasetilasi Kitosan Cangkang Kerang Kampak (A. pectinata) ... 43
3. Data Kelarutan Kitosan Cangkang Kerang Kampak (A. pectinata) ... 44
4. Data Kadar Abu Kitosan Cangkang Kerang Kampak (A. pectinata) ... 45
5. Data Kadar Air Kitosan Cangkang Kerang Kampak (A. pectinata) ... 46
6. Data Statistik Hasil Pengujian Rendemen ... 47
7. Data Statistik Hasil Pengujian Derajat Deasetilasi ... 48
8. Data Statistik Hasil Pengujian Kelarutan ... 49
9. Data Statistik Hasil Pengujian Kadar Abu ... 50
10. Data Statistik Hasil Pengujian Kadar Air ... 51
11. Bahan Penelitian ... 52
I PENDAHULUAN
1.1Latar Belakang
Indonesia sebagai negara kepulauan mempunyai potensi yang besar pada sumberdaya kekerangan (Arifin dan Setyono, 1992). Sektor perikanan sampai saat ini masih melakukan eksplorasi pada hasil laut yaitu tuna, udang, rumput laut, dan berbagai jenis moluska yang diminati untuk dikembangkan. Salah satu contoh moluska adalah kerang yang merupakan hasil perikanan yang melimpah di daerah tropis dan sumber protein hewani yang baik dan murah bagi masyarakat. Kerang dapat pula dikembangkan menjadi salah satu produk ekspor yang dapat diandalkan (Chairunisah, 2011). Berdasarkan data ekspor hasil perikanan Indonesia pada tahun 2003 dan 2004, untuk komoditas koral dan kulit kerang dihasilkan sekitar 3.208 ton dan 2.752 ton. Limbah padat berupa cangkang kerang ini diantaranya merupakan sisa dari industri pengolahan kerang segar, selama ini kerang hasil tangkapan nelayan hanya dimanfaatkan daging atau otot aduktornya saja sementara cangkangnya dibuang dan menjadi limbah (Agustini dkk., 2011). Salah satu contoh jenis kerang yang termasuk dalam Classis Bivalvia adalah kerang kampak atau yang disebut kerang manuk.
Kerang kampak (Atrina pectinata) didistribusikan secara luas di sepanjang wilayah Indo-Pasifik Barat, Afrika, Malaysia, Selandia Baru, dan Jepang. Kerang A. pectinata menarik bagi dunia perikanan karena merupakan sumber makanan
cangkang kerang hanya sebagai limbah. Cangkang kerang merupakan bahan baku penghasil kitin dan kitosan. Jumlah kandungan kitin pada cangkang kerang berkisar 14 – 35% (Margonof, 2003 dalam Sinardi dkk., 2013). Kitin adalah biopolimer melimpah di alam yang menduduki peringkat kedua setelah selulosa. Kitin bersifat non-toxic (tidak beracun) dan biodegradable, serta dapat mengalami proses deasetilasi menghasilkan kitosan (Puspitasari, 2007).
Kitosan merupakan turunan kitin yang terbentuk dari hasil ekstraksi rangka luar udang, kerang, atau rajungan melalui proses deasetilasi atau penghilangan gugus asetil yang menyisakan gugus amina bebas (Atmadja, 2014). Hasil penelitian kitosan pada cangkang kerang bulu oleh (Hastuti dan Tulus, 2015) diperoleh derajat deasetilasi sebesar 80,6%, sedangkan kitosan pada cangkang kerang simping oleh (Sulistiyoningrum dkk., 2013) diperoleh derajat deasetilasi sebesar 69,11%, dan kitosan pada cangkang kerang darah oleh (Bahri dkk., 2015) diperoleh derajat deasetilasi sebesar 69,72%. Kualitas kitosan dapat diketahui dari derajat deasetilasinya. Derajat deasetilasi mempengaruhi dalam aplikasi kitosan, karena menentukan muatan gugus amina bebas serta digunakan dalam membedakan antara kitin dan kitosan (Mastuti, 2005). Menurut Bahri dkk. (2015), kitosan tidak dapat larut dalam larutan netral atau basa tetapi larut dalam asam-asam organik, sedangkan kitin tidak larut dalam air, asam-asam encer, ataupun pelarut organik namun sebagian larut dalam LiCl2 atau dimetilasetamida (Sugita dkk.,
(Sulistiyoningrum dkk., 2013). Derajat deasetilasi kitosan minimal untuk industri pangan adalah 70%, industri kosmetika dan biomedis sedikitnya 80 dan 90% (Tsugita, 1997 dalam Yulina, 2011).
Mutu kitosan dipengaruhi oleh derajat deasetilasi yang merupakan salah satu karakteristik kimia yang paling penting. Derajat deasetilasi kitosan ditentukan oleh beberapa faktor yaitu konsentrasi NaOH, suhu dan lama proses deasetilasinya (Prasetyo, 2004 dalam Bahri dkk., 2015). Selain itu, tahapan deasetilasi kitin juga menentukan nilai derajat deasetilasi yang diperoleh (Bahri dkk., 2015)
Dari latar belakang berikut, dilakukan penelitian peningkatan derajat deasetilasi pada kitosan limbah cangkang kerang kampak (Atrina pectinata) melalui proses deasetilasi kitin secara bertahap.
1.3 PerumusanMasalah
Apakah proses deasetilasi kitin secara bertahap dapat memberikan pengaruh terhadap derajat deasetilasi kitosan limbah cangkang kerang kampak (Atrina pectinata)?
1.4 Tujuan
1.5 Manfaat
II TINJAUAN PUSTAKA
2.1 Klasifikasi dan Morfologi Kerang Kampak (Atrina pectinata)
Menurut Hayward et al. (1990) klasifikasi Atrina pectinata adalah sebagai berikut:
Filum : Mollusca Kelas : Bivalvia Subkelas : Pteromorphia Ordo : Mytilidae Famili : Pinnidae Genus : Atrina
Spesies : Atrina pectinata
Gambar 1. Morfologi Kerang Kampak (Sumber: Kuijver, 2015)
Atrina pectinata atau kerang kampak termasuk anggota familia pinnidae yang
kecoklatan, dan sangat tipis pada bagian periostracum. Bagian posterior cangkang kerang bertekstur kasar atau berambut, terdiri atas relief konsentris yang kurang jelas, kaki mengalami reduksi atau tidak ada (Dura, 1997). Morfologi kerang kampak terdapat pada Gambar 1.
Kedua keping cangkang kerang dihubungkan oleh hinge ligamen, yakni semacam pita elastis dari bahan organik seperti zat tanduk. Kedua bagian dalam cangkang tersebut ditautkan oleh sepasang otot aduktor yang serupa, yakni pada bagian anterior dan posterior. Otot aduktor berguna untuk membuka dan menutup cangkang. Bila otot aduktor berelaksasi maka hinge ligamen berkerut dan kedua cangkang akan terbuka. Sebaliknya, cangkang akan menutup apabila otot aduktor berkontraksi (Niswari, 2004).
Menurut Barnes (1974), susunan cangkang kerang terdiri dari tiga lapisan yaitu, periostracum (lapisan terluar) yang terdiri dari protein, lostracum (lapisan tengah) yaitu lapisan prismatik paling tebal yang tersusun dari lapisan kalsium, dan hypostracum (lapisan dalam) yang terdiri dari lembaran-lembaran cochiolin dan kalsium karbonat yang umumnya tipis dan mengkilat, lapisan ini biasanya disebut nacre.
2.2 Habitat dan Penyebaran Kerang Kampak (Atrina pectinata)
Kerang kampak (Atrina pectinata) merupakan spesies Benua Asia yang didistribusikan secara luas di sepanjang wilayah Indo-Pasifik Barat, Afrika, Malaysia, Selandia Baru, Jepang dan Indonesia (An et al., 2012). Moluska kerang mytilidae sangat potensial dibudidayakan di perairan-perairan pantai utara Jawa dan pantai timur Sumatera (LON LIPI, 1987 dalam Niswari, 2004).
2.3 Kandungan Kimia Cangkang Kerang
Cangkang kerang memiliki kandungan kalsium dan fosfor yang tinggi. Pada cangkang kerang diduga bersumber dari lapisan kalsium karbonat (CaCO3) yang
melindungi tubuh kerang sehingga tekstur kerang sangat padat (Paus, 2014). Selain itu, terdapat banyak kulit atau cangkang biota laut yang mengandung kitin. Kandungan kitin terbanyak terdapat pada cangkang kepiting yaitu mencapai 50%-60%, cangkang udang mencapai 42%-57%, dan cangkang cumi-cumi dan kerang masing-masing 40% dan 14%-35% (Margonof, 2003 dalam Sinardi dkk., 2013).
2.4 Kitin dan Kitosan
Monomer kitin adalah 2-asetamida-2-deoksi-D-Glukosa (N-asetil glukosamin) dengan rumus molekul (C8H13NO5)n (Horton, 2002). Kitin secara
alami tidak memiliki tingkat asetilasi yang lengkap, Kitin biasanya mempunyai derajat deasetilasi kurang dari 10% (Hartati dkk., 2002). Penggunaan kitin dibatasi oleh sifat-sifat yang tidak larut dan sulit dipisahkan dengan bahan lain yang terikat terutama protein, sehingga untuk pemanfaatannya kitin perlu diubah terlebih dahulu menjadi kitosan (Hendri, 2008). Menurut Sahara (2011) kitin dapat dimanfaatkan dengan dicampurkan pada pakan ternak, sedangkan dalam Rusdianto (2010) senyawa kitin memiliki kemampuan untuk menurunkan logam berat berupa Kadmium (Cd) dan Seng (Zn) pada limbah cair pabrik tekstil.
Kitosan merupakan turunan dari kitin dengan struktur [β-(1-4)amina -2-deoksi-Dglukosa] dengan rumus molekul (C6H11NO4)n (Sugita dkk., 2009).
Kitosan berbentuk padatan amorf bewarna putih dengan struktur kristal tetap dari bentuk awal kitin murni. Kitosan mempunyai rantai yang lebih pendek daripada rantai kitin (Wardaniati dan Setyaningsih, 2009). Menurut Bahri dkk. (2015), kitosan tidak dapat larut dalam larutan netral atau basa tetapi larut dalam asam-asam organik. (Widodo, 2006 dalam Azhar dkk., 2010) mengungkapkan bahwa pelarut kitosan yang baik adalah asam asetat. Sifat biologi kitosan yang menguntungkan yaitu alami, (biodegradable) mudah diuraikan oleh mikroba, biokompatibel yang artinya sebagai polimer alami sifatnya tidak mempunyai efek samping, dan tidak beracun (Muzzarelli, 1996).
diteliti dan dikembangkan. Kitosan digunakan secara luas di industri makanan, kosmetik, kesehatan, farmasi dan pertanian serta pada pengolahan air limbah. Sebagai contoh, di industri pangan, kitosan dapat digunakan sebagai suspensi padat, pengawet, penstabil warna, penstabil makanan, bahan pengisi, pembentuk gel, dan tambahan pakan hewan ternak (Shahidi et al., 1999). Selain itu, manfaat kitosan dibidang pertanian adalah sebagai pestisida, herbisida, virusida tanaman, deasidifikasi buah-buahan, sayuran, dan penjernih sari buah. Fungsi kitosan sebagai antimikroba, antijamur, bahan pembuat lensa kontak, aditif kosmetik, pembalut luka dan benang bedah yang mudah diserap tubuh juga diterapkan dibidang kedokteran (Sugita dkk., 2009). Struktur kimia selulosa, kitin, dan kitosan dapat dilihat pada gambar 2.
2.5 Pembuatan Kitosan
Cangkang kerang mengandung senyawa kimia yang disebut kitin dengan rumus molekul (C8H13NO5)n, kitin diperoleh melalui proses deproteinasi dan
demineralisasi. Penghilangan protein pada proses deproteinasi bertujuan untuk menghilangkan protein yang terikat dalam matriks kulit (Sugita dkk., 2009). Di dalam kerangka luar hewan bercangkang mengandung kitin yang berikatan langsung dengan kalsium karbonat (CaCO3) dan protein. Protein yang terikat di
dalam cangkang bisa mencapai kisaran antara 30-40% dari senyawa organik totalnya, tergantung pada jenis spesiesnya (Cho et al., 1998). Deproteinasi merupakan reaksi hidrolisis pada kitin dalam suasana basa dengan menggunakan larutan NaOH 5% pada suhu kamar selama semalam atau suhu 90 oC selama 1 jam, dan hasil deproteinasi kemudian dinetralisasi menggunakan aquades (Shaji et al., 2010).
Setelah deproteinasi, selanjutnya dilakukan tahap demineralisasi yaitu menghilangkan mineral atau senyawa anorganik yang ada pada limbah cangkang kerang. Mineral utama paling banyak pada cangkang kerang adalah CaCO3 dan
kalsium fosfat Ca3(PO4)2 (Priyambodo, 2009). Proses demineralisasi dilakukan
dengan menambahkan HCl 1N dengan perbandingan bobot bahan dan volume pengekstrak 1:7 (b/v) dan dipanaskan pada suhu 90 oC selama 1 jam (Suptijah, 2004).
yang terbentuk dicuci menggunakan aquades hingga netral (Muzzarelli dan Rochetti, 1985). Waktu deasetilasi yang panjang dengan suhu yang tinggi akan menyebabkan terjadinya penurunan rendemen (Sugita dkk., 2009).
2.6 Derajat Deasetilasi
Derajat deasetilasi merupakan suatu parameter mutu kitosan yang menunjukkan persentase gugus asetil yang dapat dihilangkan dari rendemen kitin maupun kitosan. Semakin tinggi derajat deasetilasi kitosan, maka gugus asetil kitosan semakin rendah sehingga interaksi antar ion dan ikatan hidrogennya akan semakin kuat (Knoor, 1982). Pelepasan gugus asetil dari kitosan menyebabkan kitosan bermuatan positif yang mampu mengikat senyawa bermuatan negatif, seperti protein, anion polisakarida membentuk ion netral (Suhartono, 1989 dalam Rochima 2007).
2.7 Mutu Kitosan
Dalam menentukan kualitas kitosan yang digunakan, perlu dilakukan standar mutu kitosan berdasarkan (BSN, 2013). Kemurnian kitosan dapat dilihat dari nilai derajat deasetilasinya. Semakin tinggi derajat deasetilasi, jumlah gugus amina (NH2) pada rantai molekul kitosan akan tinggi sehingga kitosan semakin murni.
Tabel 1. Karakteristik kitosan
Jenis Uji Satuan Persyaratan 1 Bentuk partikel - Serpihan sampai serbuk
2 Warna - Coklat muda sampai putih
3 Fisika
- Benda asing - Negatif
4 Kimia
- Derajat deasetilasi % Min 75
- pH - 7-8
- Kadar abu % Maks 5
- Kadar air % Maks 12
III KONSEPTUAL PENELITIAN DAN HIPOTESIS
3.1 Kerangka Konseptual
Kerang kampak merupakan hasil perikanan yang melimpah di daerah tropis dan sumber protein hewani yang baik dan murah bagi masyarakat. Selama ini sebagian besar kerang hasil tangkapan nelayan hanya dimanfaatkan daging atau otot aduktornya saja sementara cangkangnya dibuang dan menjadi limbah (Agustini dkk., 2011). Limbah ini jika dibiarkan terus menumpuk tanpa adanya penanganan khusus maka akan menimbulkan pencemaran dan estetika lingkungan terganggu.
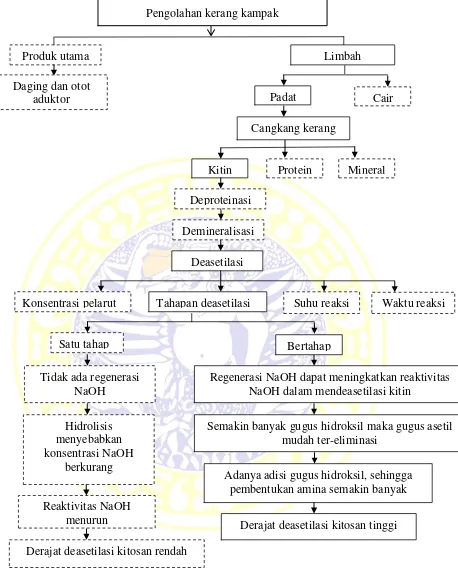
berlangsung, konsentrasi larutan NaOH makin lama semakin berkurang yang menyebabkan reaktivitasnya semakin menurun hingga semakin kurang efektif sebagai agen deasetilasi. Dengan melakukan regenerasi larutan NaOH, maka reaktivitas NaOH untuk mendeasetilasi kitin kembali efektif.
Berdasarkan paparan diatas maka dilakukan penelitian pembuatan kitosan limbah cangkang kerang kampak (Atrina pectinata) melalui proses deasetilasi kitin secara bertahap untuk mendapatkan derajat deasetilasi yang tinggi. Gambar kerangka konseptual dapat dilihat pada Gambar 3.
3.2 Hipotesis
Gambar 3. Kerangka Konseptual
Konsentrasi pelarut Tahapan deasetilasi Suhu reaksi
IV METODOLOGI PENELITIAN
4.1 Tempat dan Waktu
Penelitian ini telah dilaksanakan pada bulan April – Juni 2016. Proses pembuatan kitosan dan pengujian derajat deasetilasi dilakukan di Laboratorium Pendidikan Fakultas Perikanan dan Kelautan Universitas Airlangga Surabaya.
4.2 Materi Penelitian
4.2.1 Alat Penelitian
Peralatan yang digunakan dalam penelitian ini meliputi seperangkat alat gelas pyrek, hot plate, thermometer, magnetic stirrer, timbangan analitik, kertas saring, pH indikator, spektrofotometer UV-Vis dan oven.
4.2.2 Bahan Penelitian
Bahan-bahan yang digunakan pada penelitian ini adalah cangkang kerang kampak yang diperoleh di pesisir Pantai Kenjeran Surabaya, NaOH, HCl 37%, CH3COOH, dan aquades.
4.3 Metode Penelitian
4.3.1 Rancangan Penelitian
Rancangan penelitian yang digunakan adalah Rancangan Acak Lengkap (RAL). Penelitian ini dirancang dengan tiga perlakuan yang diulang sebanyak enam kali ulangan sehingga terdapat delapan belas satuan percobaan, yaitu: A1,
A2, A3, A4, A5, A6, B1, B2, B3, B4, B5, B6, C1, C2, C3, C4, C5, C6. Perlakuan pada
penelitian ini diadopsi dari pernyataan Bahri dkk. (2015), bahwa untuk menghasilkan kitosan dengan derajat deasetilasi yang tinggi sebaiknya dilakukan tahapan pada proses deasetilasi kitin. Model perlakuan yang diberikan adalah sebagai berikut:
Perlakuan A : Deasetilasi kitin selama 1 x 3 jam (deasetilasi satu tahap) Perlakuan B : Deasetilasi kitin selama 2 x 1,5 jam (deasetilasi dua tahap) Perlakuan C : Deasetilasi kitin selama 3 x 1 jam (deasetilasi tiga tahap) Penelitian ini mengandung beberapa variabel, antara lain:
Variabel bebas : Jumlah tahapan proses deasetilasi kitin. Variabel tergantung : Derajat deasetilasi.
Variabel kontrol : Pelarut yang digunakan selama proses pembuatan kitosan dan suhu.
4.4. Pelaksanaan Penelitian
4.4.1 Persiapan Bahan Baku
penggilingan dan diayak dengan pengayakan ukuran ≤100 mesh, selanjutnya
cangkang kerang kampak disimpan ke dalam kantong plastik.
4.4.2 Pembuatan Kitosan
Prosedur pembuatan kitosan dari limbah cangkang kerang kampak dilakukan melalui beberapa proses antara lain deproteinasi, demineralisasi, dan deasetilasi mengacu pada prosedur penelitian yang dilakukan oleh Bahri dkk. (2015) dari limbah kulit cangkang kerang darah dengan metode deasetilasi bertahap. Pembuatan kitosan metode Bahri dkk. (2015) diawali dengan tahap preparasi bahan. Pada tahap ini bahan baku yang akan digunakan dicuci menggunakan air mengalir hingga tidak ada kotoran dan sisa daging yang menempel pada permukaan cangkang. Setelah kering, cangkang digiling dan diayak hingga diperoleh serbuk dengan ukuran ≤100 mesh.
Proses selanjutnya, yaitu isolasi kitin dari serbuk cangkang kerang dilakukan melalui proses deproteinasi menggunakan larutan NaOH 4% dengan perbandingan 1 : 10 (b/v) pada temperatur 80 oC selama 1 jam, serbuk cangkang kerang hasil deproteinasi disaring dan dicuci menggunakan aquades hingga netral kemudian dikeringkan dengan oven temperatur 50 oC selama 24 jam. Kitin hasil deproteinasi kemudian dilakukan proses demineralisasi menggunakan HCl 1 M dengan perbandingan 1 : 15 (b/v) pada temperatur kamar selama 3 jam, serbuk kitin disaring dan dicuci menggunakan aquades hingga netral kemudian dikeringkan dengan oven temperatur 50 oC selama 24 jam.
4.4.3 Pengujian Karakteristik Kitosan
Kitosan yang dihasilkan kemudian dilakukan pengujian karakteristik untuk mengetahui perlakuan mana yang mendapatkan hasil terbaik. Pengujian dan prosedur yang dilakukan adalah sebagai berikut :
1. Rendemen
Rendemen diperoleh dari perbandingan antara berat kering kitosan cangkang kerang kampak yang dihasilkan dengan berat bahan baku cangkang kerang (Zahiruddin et al., 2008). Besarnya rendemen dapat dihitung dengan metode AOAC sebagai berikut :
Rendemen (%) =
x 100% 2. Derajat Deasetilasi
3. Kelarutan Kitosan
Analisis kelarutan kitosan menurut Agustina dkk. (2015) dilakukan dengan melarutkan kitosan dalam asam asetat dengan konsentrasi 2% dengan perbandingan 1:100 (g/ml), lalu difiltrasi. Persentase kelarutan kitosan ditunjukkan dengan kitosan yang tersisa dibandingkan dengan kitosan awal.
Kelarutan (%) =
x 100%
4. Kadar Abu
Kadar abu kitosan dihitung berdasarkan metode (BSN, 2006a), yaitu cawan porselen dibersihkan dan dikeringkan di dalam tungku pengabuan bersuhu 550oC selama 1 malam, kemudian turunkan suhu pengabuan hingga suhu 40oC lalu didinginkan selama 30 menit di dalam desikator dan ditimbang hingga didapatkan berat tetap (A). Sampel kitosan sebanyak 2 g dimasukkan ke dalam cawan porselen. Selanjutnya pindahkan ke tungku pengabuan dan naikkan temperatur secara bertahap sampai suhu 550oC selama 8 jam sampai diperoleh abu berwarna putih, kemudian turunkan suhu pengabuan hingga suhu 40oC lalu didinginkan selama 30 menit di dalam desikator dan ditimbang hingga didapatkan berat tetap (B). Nilai kadar abu tersebut merupakan nilai rerata dari dua sampel yang sama. Kadar abu dihitung dengan rumus (BSN, 2006a) :
Kadar abu (%) =
x 100%
Keterangan :
5. Kadar Air
Pengujian kadar air kitosan mengacu pada metode BSN (2006b). Metode yang digunakan dalam penentuan kadar air adalah metode gravimetri. Berikut langkah yang dilakukan dalam pengujian kadar air :
Cawan kosong dimasukkan terlebih dahulu ke dalam oven minimal 2 jam dengan suhu 105°C. Cawan kosong yang telah dimasukkan ke dalam oven dipindahkan ke dalam desikator sekitar 30 menit sampai mencapai suhu ruang lalu bobot cawan kosong ditimbang (A). Sampel kitin sebanyak ± 2 g dimasukkan dalam cawan kosong dan ditimbang (B). Cawan yang telah diisi sampel dimasukkan ke dalam oven dengan suhu 105°C selama 16 jam – 24 jam. Setelah cawan di oven, cawan dipindahkan dengan menggunakan cruss tang ke dalam desikator selama 30 menit setelah itu ditimbang (C) dan dilakukan perhitungan dengan rumus sebagai berikut :
adar air ( ) 100 Keterangan :
A = Berat cawan kosong dinyatakan dalam g
B = Berat cawan + sampel awal, dinyatakan dalam g C = Berat cawan + sampel kering, dinyatakan dalam g
6. Analisis Struktur
4.4.4 Parameter Pengamatan
Parameter utama yang diamati pada penelitian ini adalah kadar rendemen, derajat deasetilasi, kelarutan kitosan, kadar air, dan kadar abu. Sedangkan parameter pendukung yang diamati pada penelitian ini adalah pH dan warna dari produk kitosan yang dihasilkan.
4.5 Analisis Data
V HASIL DAN PEMBAHASAN
5.1 Hasil Penelitian
Karakterisasi kitosan yang dilakukan meliputi pH, warna, bentuk, rendemen, derajat deasetilasi, kelarutan, kadar abu dan kadar air. Hasil penelitian ini menunjukan kitosan dengan proses deasetilasi kitin secara bertahap memiliki karakteristik yang tidak jauh berbeda. Penampakan fisik kitosan dengan perlakuan proses deasetilasi kitin 1 tahap, 2 tahap dan 3 tahap memiliki warna cenderung putih. kitosan pada tiap perlakuan berbentuk serbuk halus dan tidak berbau serta pada masing-masing perlakuan memiliki pH netral. Adapun kitosan yang dihasilkan pada masing-masing perlakuan dapat dilihat pada Gambar 5.
Gambar 5. Kitosan dengan proses deasetilasi kitin sebanyak (A) 1 tahap, (B) 2 tahap dan (C) 3 tahap.
C
B
5.1.1 Rendemen Kitosan
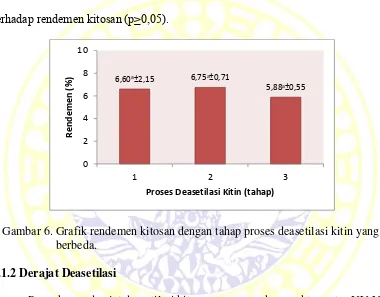
Nilai rendemen kitosan yang dihasilkan pada penelitian ini berkisar antara 5,88% – 6,60%. Rendemen kitosan ini didapat dari presentase berat awal cangkang kerang dibandingkan berat akhir kitosan. Penyajian data rendemen kitosan dapat dilihat pada Gambar 6. Berdasarkan hasil analisis sidik ragam menunjukkan bahwa proses deasetilasi kitin secara bertahap tidak berbeda nyata terhadap rendemen kitosan (p≥0,05).
Gambar 6. Grafik rendemen kitosan dengan tahap proses deasetilasi kitin yang berbeda.
5.1.2 Derajat Deasetilasi
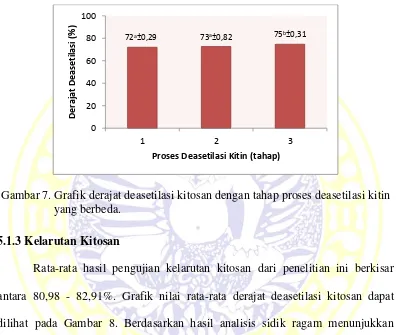
Pengukuran derajat deasetilasi kitosan menggunakan spektrometer UV-Vis dengan panjang gelombang 201 nm pada masing-masing perlakuan dengan proses deasetilasi kitin sebanyak (A) 1 tahap, (B) 2 tahap dan (C) 3 tahap berturut-turut adalah 72 ; 73 dan 75. Grafik nilai rata-rata derajat deasetilasi kitosan dapat dilihat pada Gambar 7.
Berdasarkan hasil analisis sidik ragam menunjukkan bahwa proses deasetilasi kitin secara bertahap berbeda nyata terhadap derajat deasetilasi kitosan
(p≤0,05). Selain itu, hasil uji lanjut Duncan menunjukkan bahwa derajat
deasetilasi tertinggi terdapat pada perlakuan proses deasetilasi kitin 3 tahap dengan nilai derajat deasetilasi 75 namun tidak berbeda nyata dengan perlakuan 1 tahap maupun 2 tahap.
Gambar 7. Grafik derajat deasetilasi kitosan dengan tahap proses deasetilasi kitin yang berbeda.
5.1.3 Kelarutan Kitosan
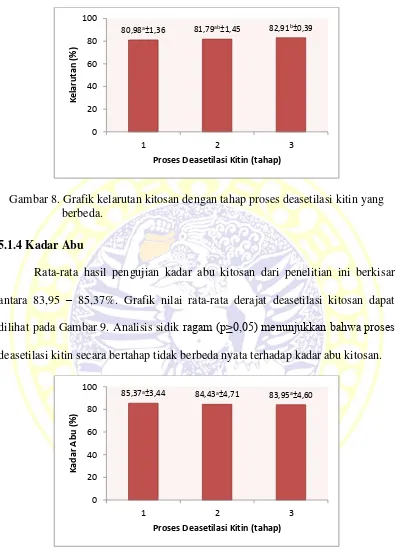
Rata-rata hasil pengujian kelarutan kitosan dari penelitian ini berkisar antara 80,98 - 82,91%. Grafik nilai rata-rata derajat deasetilasi kitosan dapat dilihat pada Gambar 8. Berdasarkan hasil analisis sidik ragam menunjukkan bahwa proses deasetilasi kitin secara bertahap berbeda nyata terhadap kelarutan kitosan (p≤0,05). Selain itu, hasil uji lanjut Duncan menunjukkan bahwa kelarutan
tertinggi terdapat pada perlakuan proses deasetilasi kitin 3 tahap dengan nilai kelarutan 82,91% namun tidak berbeda nyata dengan perlakuan deasetilasi kitin 2 tahap dan berbeda nyata dengan perlakuan deasetilasi kitin 1 tahap.
Gambar 8. Grafik kelarutan kitosan dengan tahap proses deasetilasi kitin yang berbeda.
5.1.4 Kadar Abu
Rata-rata hasil pengujian kadar abu kitosan dari penelitian ini berkisar antara 83,95 – 85,37%. Grafik nilai rata-rata derajat deasetilasi kitosan dapat dilihat pada Gambar 9. Analisis sidik ragam (p≥0,05) menunjukkan bahwa proses deasetilasi kitin secara bertahap tidak berbeda nyata terhadap kadar abu kitosan.
5.1.5 Kadar Air
Air merupakan komponen utama dalam bahan makanan. Rata-rata hasil pengujian kadar air kitosan dari penelitian ini berkisar antara 0,52% – 0,75%. Grafik nilai rata-rata derajat deasetilasi kitosan dapat dilihat pada Gambar 10. Secara hasil analisis sidik ragam (p≥0,05) menunjukkan bahwa perlakuan proses deasetilasi kitin secara bertahap tidak berbeda nyata pada nilai kadar air kitosan.
Gambar 10. Grafik kadar air kitosan dengan tahap proses deasetilasi kitin yang berbeda.
5.1.6 Analisis Struktur
Kitosan yang diperoleh dari hasil ekstraksi dianalisis secara kualitatif dengan menggunakan spektrofotometer FTIR untuk mengetahui gugus fungsi utama pada molekul kitosan. Pengujian FTIR ini dapat digunakan untuk mengidentifikasi suatu senyawa yang belum diketahui, karena spektrum yang dihasilkan spesifik untuk senyawa tersebut. Hasil FTIR kitosan cangkang kerang kampak menunjukkan pola serapan pada panjang gelombang 3383,29 cm-1. Hasil FTIR kitosan cangkang kerang kampak ditunjukkan pada Lampiran 1.
5.2 Pembahasan
Hasil rendemen kitosan yang dihasilkan pada masing-masing perlakuan mengalami penurunan dari berat bahan baku awal yang diduga dipengaruhi oleh proses pembuatan kitosan. Kitosan merupakan produk yang melalui proses demineralisasi, deproteinasi dan deasetilasi sehingga komponen mineral atau bahan anorganik lainnya dan protein pada bahan baku cangkang kerang banyak yang terlarut dalam larutan HCl maupun NaOH serta mengakibatkan berat akhir kitosan yang lebih rendah daripada berat cangkang kerang utuh (Priyambodo, 2009).
Serbuk cangkang kerang yang telah dipreparasi harus mengalami proses demineralisasi yang merupakan tahapan awal untuk mendapatkan kitosan. Proses demineralisasi berpengaruh terhadap rendemen kitosan yaitu sesuai pernyataan dalam Mahmoud et al. (2005) bahwa selain pengaruh konsentrasi pelarut yang tinggi, waktu perendaman cangkang kerang di dalam larutan HCl akan mempengaruhi penurunan kadar mineral pada proses pembuatan kitosan. Semakin lama waktu perendaman, maka akan menghasilkan semakin sedikit rendemen kitosan. Pada proses demineralisasi, terjadi proses penghilangan mineral utama yang terdapat pada cangkang kerang seperti kalsium karbonat (CaCO3) dan fosfor
menggunakan pelarut HCl. Penambahan larutan HCl akan bereaksi dengan mineral tersebut sehingga terbentuk garam-garam yang dapat larut dalam pelarut sehingga mudah dihilangkan dan akan terbentuk gas CO2 yang dapat terpisah dari
terlebih dahulu dan bertujuan untuk memutuskan ikatan antara protein dan kitin dengan cara menambahkan pelarut NaOH. Melalui tahap deproteinasi, protein yang terekstrak adalah dalam bentuk Na-proteinat, dimana ion Na+ akan mengikat ujung rantai protein yang bermuatan negatif sehingga akan larut dengan pelarut natrium hidroksida (Rochima, 2007). Tahapan terakhir untuk mendapatkan kitosan disebut dengan proses deasetilasi. Pada proses tersebut, gugus asetil (-NHCOCH3) pada kitin dihilangkan agar menjadi gugus amina. Proses deasetilasi
kitin secara bertahap tidak memberikan pengaruh terhadap rendemen kitosan. Mengacu pada penelitian (Puspawati dan Simpen, 2004) bahwa pengaruh dari konsentrasi pelarut pada rendemen kitosan terjadi karena reaksi adisi gugus OH -pada struktur gugus kitin yang mengakibatkan struktur gugus kitin menjadi semakin mengembang dan terbuka, seiring dengan kenaikan konsentrasi NaOH yang digunakan. Tingkat pembukaan struktur gugus kitin yang semakin tinggi menyebabkan jumlah gugus amina yang terbentuk semakin banyak, sedangkan menurut Suptijah (2004) menyatakan bahwa tinggi rendahnya rendemen kitosan yang didapatkan dipengaruhi oleh lamanya proses reaksi dan suhu reaksi.
Hasil analisis yang disajikan pada Lampiran 8, diketahui bahwa proses deasetilasi kitin secara bertahap berbeda nyata (p≤0,05) pada derajat deasetilasi
tahap maupun 2 tahap yaitu sebesar 75, sehingga semakin banyak penambahan NaOH mengakibatkan semakin banyak pula gugus hidroksil yang tersedia untuk terjadinya proses hidrolisis, sehingga memperbesar kemungkinan terjadinya eliminasi pada gugus asetil yang disebabkan tejadinya adisi oleh hidroksil, sehingga pembentukan amina juga semakin banyak (Bahri, 2015). Adanya tahapan proses deasetilasi yang sesuai dapat meningkatkan derajat deasetilasi produk kitosan yang dihasilkan, dimana setiap tahapannya dilakukan regenerasi larutan NaOH yang baru. Hal ini sesuai dengan pernyataan Junaidi dkk. (2009) bahwa selama regenerasi NaOH secara signifikan dapat meningkatkan efektivitas proses deasetilasi. Selama reaksi hidrolisis berlangsung, konsentrasi larutan NaOH makin lama semakin berkurang yang menyebabkan reaktivitasnya semakin menurun hingga semakin kurang efektif sebagai agen deasetilasi. Dengan melakukan regenerasi larutan NaOH, maka reaktivitas NaOH untuk mendeasetilasi kitin kembali efektif. Menurut BSN (2006) derajat deasetilasi kitosan minimal untuk industri adalah 75, sedangkan menurut Sugita dkk. (2009) derajat deasetilasi kitosan minimal untuk industri pangan yaitu 70, oleh karena itu kitosan yang dihasilkan dalam penelitian ini dapat dimanfaatkan dalam bidang industri non pangan karena masih memiliki nilai kadar abu yang tinggi, contohnya sebagai bioremediasi limbah cair, chelating agent yang dapat menyerap logam berat perairan dan sebagai pupuk tanaman karena tingginya kandungan kapur yang dapat menyuburkan tanaman.
Hasil peningkatan kelarutan berbanding lurus dengan peningkatan derajat deasetilasi. Hal ini dikarenakan gugus asetil pada kitin yang dipotong oleh gugus hidroksil pada proses deasetilasi yang akan menyisakan gugus amina. Ion H+ pada gugus amina menjadikan kitosan mudah berinteraksi dengan asam asetat melalui ikatan hidrogen. Gugus amina dari kitosan akan terprotonasi membentuk gugus amina kationik (NH3+). Kation dalam kitosan tersebut jika bereaksi dengan polimer anionik akan membentuk kompleks elektrolit (Sanford, 1989). Sifat kitosan hanya dapat larut dalam asam organik, seperti asam asetat, asam format, asam sitrat kecuali kitosan yang telah disubstitusi maka dapat larut pada air (Dunn et al., 1997). Kelarutan kitosan dalam larutan asam asetat dapat dipengaruhi oleh
lamanya perendaman dalam larutan NaOH dan konsentrasi pelarut NaOH (Rochima, 2007). Pada proses deasetilasi kitin 3 tahap terjadi regenerasi larutan NaOH yang akan menstabilkan kapasitas rasio pelarut dan konsentrasi NaOH sehingga proses pemutusan gugus asetil dapat berlangsung secara maksimal yang akan meningkatkan jumlah gugus amina yang dihasilkan dalam reaksi deasetilasi dibandingkan dengan perlakuan tanpa adanya regenerasi NaOH.
(Margonof, 2003 dalam Sinardi dkk., 2013) bahwa kandungan kitin kerang hanya sebesar 14-35%. Hal itu dapat dilihat pada saat proses demineralisasi dengan penambahan HCl menimbulkan gelembung udara (CO2) yang cukup banyak
(Nurjannah dkk., 2016). Kadar abu ini diketahui dari sampel yang tidak terabukan. Berdasarkan analisis statistik menunjukkan bahwa proses deasetilasi kitin secara bertahap tidak memberikan pengaruh nyata (p≥0,05) terhadap kadar abu kitosan. Besarnya kadar abu yang terkandung memperlihatkan proses demineralisasi yang kurang sempurna dan mineral-mineral yang terkandung dalam sampel belum semuanya hilang. Faktor yang mempengaruhi efektifitas kadar abu adalah konsentrasi pelarut dan lamanya waktu pengadukan (Hastuti dan Tulus, 2015). Pada proses demineralisasi, asam dapat terjerat dan berdifusi secara lambat dalam kisi-kisi kristal atau berasosiasi dengan asam amino bebas dan residu protein, sehingga dapat menimbulkan kerusakan (pemutusan rantai) selama pengeringan. Kerusakan ini dapat dicegah dengan pencucian hingga pH netral (Johnson and Peniston, 1982 dalam Sugita, 2009).
Penentuan kadar air memperlihatkan jumlah kandungan air dalam kitosan. Kadar air dalam kitosan diketahui dari banyaknya air yang menguap setelah pemanasan. Berdasarkan Lampiran 10, dapat dilihat bahwa proses deasetilasi kitin secara bertahap tidak berbeda nyata (p≥0,05) terhadap kadar air kitosan. Menurut
diketahui bahwa kitosan cangkang kerang kampak memiliki kadar air yang relatif sedikit sehingga dapat diabaikan. Pada penelitian kali ini dihasilkan kitosan dengan warna putih, menurut Harianingsih (2010) bahwa warna itu sendiri tergantung pada jenis raw materialnya dan secara umum warna tidak memengaruhi sifat fungsional kitosan. Selain itu, kitosan cangkang kerang kampak juga memiliki pH netral. Hal ini dikarenakan kitosan akan dapat mengikat ion lebih mudah dengan kondisi pH yang netral (Agusnar dan Noviary, 2013). Popury et al., (2009) menyatakan bahwa apabila pada pH asam terjadi tolakan elektrostatik antara –NH3+ kitosan dengan kation bahan pelarut. Sementara pada
kondisi yang terlalu basa, gugus OH- pada lingkungan akan mengubah struktur kitosan.
Pengujian spektrofotometer FTIR (Fourier Transform Infra Red) berguna untuk mengetahui gugus fungsi utama yang terdapat pada kitosan. Hasil dari pengujian ini adalah kitosan menunjukkan pola serapan pada panjang gelombang 3383,29 cm-1 yang menunjukkan gugus fungsi OH dan NH2. Gugus hidroksil dan
VI SIMPULAN DAN SARAN
6.1 Simpulan
Proses deasetilasi kitin secara bertahap memberikan pengaruh terhadap derajat deasetilasi kitosan yang dihasilkan. Adanya regenerasi NaOH pada tiap tahapan dapat meningkatkan derajat deasetilasi dan kelarutan.
6.2 Saran
DAFTAR PUSTAKA
Agusnar., H dan H. Noviary. 2013. Preparasi Dan Karakterisasi Kitosan Dari Cangkang Belangkas (Tachypleus gigas) Yang Diikat Silang Dengan Modifikasi Genipin. Prosiding Seminar Nasional Sains dan Teknologi Nuklir PTNBR-BATAN.
Agustina, S., dan Y. Kurniasih. 2013. Pembuatan Kitosan dari Cangkang Udang dan Aplikasinya Sebagai Adsorben Untuk Menurunkan Kadar Logam Cu. Prosiding Seminar Nasional MIPA (Vol. 3, No. 1).
Agustina, S., I. Swantara dan I.N. Suartha. 2015. Isolasi Kitin, Karakterisasi, dan Sintesis Kitosan dari Kulit Udang. Journal of Chemistry, 9(2).
Agustini, T. W., A. S. Fahmi., I. Widowati., dan A. Sarwono. 2011. Pemanfaatan limbah cangkang kerang simping (Amusium pleuronectes) dalam pembuatan cookies kaya kalsium. Jurnal Pengolahan Hasil Perikanan Indonesia, 14(1).
An, H. S., J. W. Lee and C. M. Dong. 2012. Population genetic structure of Korean pen shell (Atrina pectinata) in Korea inferred from microsatellite marker analysis. Genes & Genomics, 34(6), 681-688. Arifin, Z., Setyono. 1992. Potensi sumberdaya kekerangan dan prospek
pengembangannya di Maluku. Prosiding Lokakarya Ilmiah Potensi Sumberdaya Perikanan Maluku, No. 8. Balitbang Perikanan Budidaya Pantai, Maros : 77–86.
Atmadja, F. 2014. Pengaruh Kitosan Kulit Pupa Ulat Sutera Sebagai Pengganti Formalin Terhadap Daya Simpan Tahu. Skripsi. Fakultas Ekologi Manusia, Institut Pertanian Bogor. Bogor. 7 hal.
Azhar, M., J. Effendi., E. Syafyeni., R. M. Lesi dan S. Novalina. 2010. Pengaruh Konsentrasi NaOH dan KOH terhadap Derajad Deasetilasi Kitin dari Limbah Kulit Udang. Jurnal Riset Kimia. Vol 1.
Badan Standardisasi Nasional. 2006a. Penentuan Kadar Abu pada Produk Perikanan. SNI 01-2354.1-2006. BSN. Jakarta. 8 hal.
Badan Standardisasi Nasional. 2006b. Penentuan Kadar Air Produk Perikanan. SNI 01-2354.2-2006. BSN. Jakarta 12 hal.
Bahri, S., E. A. Rahim dan S. Syarifuddin. 2015. Derajat Deasetilasi Kitosan dari Cangkang Kerang Darah dengan Penambahan NaOH Secara Bertahap. Jurnal Riset Kimia. 1(1).
Barnes, R.D. 1974. Invertebrate Zoology, 3rd ed. W.B. Saunders Co. Philadelphia. London.
Chairunisah. 2011. Karakteristik Asam Amino Daging Kerang Tahu (Meretrix meretrix), Kerang Salju (Pholas dactylus), dan Keong Macan (Babylonia spirata). Skripsi. Fakultas Perikanan dan Ilmu Kelautan, Institut Pertanian Bogor. Bogor. 1 hal.
Cho, Y. I., H. K. No and S. P. Meyers. 1998. Physicochemical Characteristics and Functional Properties of Various Commercial Chitin and Chitosan Products. Journal of Agricultural and Food Chemistry 46 (7, Februari) : 3839-3843 (accessed online from url http : //pubs.acs.org/).
Dura, 1997. Studi Komunitas Bivalvia di Daerah Interdal Pantai Krakal Gunung Kidul. Skipsi Fakultas Biologi. Universitas Atma Jaya. Yogyakarta. 8 hal. DunnET, GrandmaisonEW, GoosenMFA. 1997. Applications and properties of
chitosan. Di dalam: Goosen MFA (ed.). Applications of Chitin and Chitosan. Technomic PubBasel p 3-30.
Harianingsih. 2010. Pemanfaatan Limbah Cangkang Kepiting Menjadi Kitosan Sebagai Bahan Pelapis (Coater) Pada Buah Stroberi. Tesis. Program Magister Teknik Kimia. Universitas Diponegoro. Semarang. 9 hal.
Hartati, F. K., T. Susanto dan S. Rakhmadiono. 2002. Faktor-Faktor Yang Berpengaruh Terhadap Tahap Deproteinasi Menggunakan Enzim Protease Dalam Kitin Dari Cangkang Rajungan (Portunus Pelagicus). Biosain 2. 68-77.
Hastuti, B., dan N. Tulus. 2015. Sintesis Kitosan Dari Cangkang Kerang Bulu (Anadara inflata) Sebagai Adsorben Ion Cu 2+. Seminar Nasional Kimia dan Pendidikan Kimia VII. 11 hal.
Hayward, P.J., G. D. Wigham and N. Yonow. 1990. Mollusca I: Polyplacophora, Scaphopoda, and Gastropoda. In: The Marine Fauna of the British Isles and North-West Europe. (ed. P.J. Hayward & J.S. Ryland). Clarendon Press, Oxford: 628-730. www. species-identification.org. 30 Januari 2016. 1 hal.
Horton, R.H., L. A. Moran., R. S. Ochs., J. D. Rawn and K. G. Scrimgeour. 2002. Principles of Biochemistry. Third edition. New York: Prentice-Hall,Inc. Junaidi, A. B., I. Kartini., dan B. Rusdiarso. 2009. Preparasi Kitosan Melalui
Deasetilasi Kitin Secara Bertahap dan Sifat Fisikokimianya. Indonesian Journal of Chemistry, 9(3), 369-372.
Khan T.A, K.K Peh, Hung S.C. 2002. Reporting Degree of Deacetylation Values of Chitosan : the Influence Analitycal Methods, J Pharm Pharmacent Sci. Knorr D. 1982. Function properties of chitin and chitosan. Jurnal Food Science.
47(36)
Kuijver, M. J., S.S Ingalsuo dan R.H. de Bruyne. 2015. Mollusca of the North Sea. www. species-identification.org. 13 Januari 2016. 1 hal.
Kumar, M.N.V. 2000. A Review Of Chitin and Chitosan Applications. Reactive and Functional Polymers 56 : 1-27.
Kusriningrum, R. S. 2012. Perancangan Percobaan. Airlangga University Press. Surabaya. Hal 43.
Kusumaningsih, T., A. Masykur dan U. Arief. 2004. Pembuatan Kitosan dari Kitin Cangkang Bekicot (Achatina fulica). Biofarmasi, 2(2), 64-68. Liu, D., Y. Wei., P. Yao and L. Jiang. 2006. Determination of the degree of
acetylation of chitosan by UV spectrophotometry using dual standards. Carbohydrate research, 341(6), 782-785.
Manurung, M. 2011. Potensi Khitin/Khitosan dari Kulit Udang sebagai Biokoagulan Penjernih Air. Journal of Chemistry, 5(2).
Mastuti, W. 2005. Pengaruh Konsentrasi NaOH dan Suhu pada Proses Deasetilasi Khitin dari Kulit Udang. Jurnal Teknik Kimia. 4(1). pp. 21-25.
Muzzarelli, R. A. 1996. Chitosan-based dietary foods. Carbohydrate Polymers,29(4), 309-316.
Muzzarelli, R. A. and R. Rocchetti. 1985. Determination of the Degree of Acetylation of Chitosans by First Derivative Ultraviolet Spectrophotometry. Carbohydrate Polymers, 5(6), 461-472.
Nurjannah, A., D. Darmanto., and I. Wijayanti. 2016. Optimization Making Glucosamine Hydrochloride (HCl GlcN) of Crab Shell Waste through Chemical Hydrolysis. Jurnal Pengolahan Hasil Perikanan Indonesia, 19(1), 26-35.
Paus, S. P. 2014. Pengaruh Suhu dan Lama Pengeringan Terhadap Karakteristik Kimia Tepung Cangkang Kijing Lokal (Pilsbryoconcha sp). Tesis. Universitas Negeri Gorontalo. 14 hal.
Popury, S. R. Y. Vijaya., V. M. Boddu., and K. Abburi. 2009. Adsorptive Removal of Copper and Nickel Ions from Water Using Chitosan Coated PVC Beads. Bioresource Technol. 100:194-199.
Priyambodo, E. 2009. Pengaruh Konsentrasi Kitosan dari Cangkang Udang Terhadap Efisiensi Penjerapan Logam Berat. Skripsi. Fakultas Matematika dan Ilmu Pengetahuan Alam. Universitas Negeri Yogyakarta. Yogyakarta. 45 hal.
Puspawati, N. M., dan I. N. Simpen. 2010. Optimasi deasetilasi khitin dari kulit udang dan cangkang kepiting limbah restoran seafood menjadi khitosan melalui variasi konsentrasi NaOH. Journal of Chemistry, 4(1).
Rifai, D. N. R. 2007. Isolasi dan Identifikasi Kitin, Kitosan dari Cangkang Hewan Mimi (Horseshoe Crab) Menggunakan Spektrofotometri Inframerah. Skripsi. Fakultas Sains dan Teknologi. Universitas Islam Negeri Malang. Malang. 4 hal.
Rochima, E. 2007. Karakterisasi Kitin dan Kitosan Asal Limbah Rajungan Cirebon Jawa Barat. Jurnal Pengolahan Hasil Perikanan Indonesia, 10(1).
Rusdianto, P. R. 2010. Pemanfaatan Kitin Udang Untuk Menurunkan Kadar admium ( d) dan Seng (Zn) Pada Limbah air Pabrik Tekstil “X” di Yogyakarta. Skripsi. Program Studi Biologi. Fakultas Teknobiologi. Universitas Atma Jaya Yogyakarta. Yogyakarta. 2 hal.
Sahara, E. 2011. Penggunaan kepala udang sebagai sumber pigmen dan kitin dalam pakan ternak. Jurnal Agribisnis dan Industri Peternakan. 1(1), 31-35.
Sandford, P. 1989. Chitosan: Commercial uses and potential applications. Di dalam: Skjak -Braek G, Anthon sen T, Sandford P (eds.). Chitin and Chitosan: Sources, Chemistry, Biochemistry, Physical Properties and Application. London:Elsevier.
Manajemen Sumberdaya Perairan. Fakultas Perikanan dan Ilmu Kelautan. Institut Pertanian Bogor. Bogor. 88 hal.
Shahidi, F., J. K. V. Arachchi and Y. J. Jeon. 1999. Food applications of chitin and chitosans. Trends in food science & technology, 10(2), 37-51.
Shaji, J., V. Jain and S. Lodha. 2010. Chitosan: A novel pharmaceutical excipient. International Journal of Pharmaceutical and Applied Sciences, 1, 1.
Sinardi., P. Soewandi dan S. Notodarmojo. 2013. Pembuatan Karakteristik dan Aplikasi Kitosan dari Cangkang Kerang Hijau (Mytulus Virdis Linneaus) Sebagai Koagulan Penjernih Air. Konferensi Nasional Teknik Sipil. Universitas Sebelas Maret. Solo. 33 hal.
Sugita, P., T. Wukirsari., A. Sjahriza dan D. Wahyono. 2009. Kitosan: Sumber Biomaterial Masa Depan. Bogor: Penerbit IPB Press. 50 hal.
Sulistiyoningrum, R. S., J. Suprijanto dan A. Sabdono. 2013. Aktivitas Anti Bakteri Kitosan dari Cangkang Kerang Simping Pada Kondisi Lingkungan Yang Berbeda: Kajian Pemanfaatan Limbah Kerang Simping (Amusium sp.). Journal of Marine Research, 2(4), 111-117. Suptijah, P. 2004. Tingkatan Kualitas Kitosan Hasil Modifikasi Proses
Produksi. Jurnal Pengolahan Hasil Perikanan Indonesia, 7(1).
Wardaniati, R. A dan S. Setyaningsih. 2009. Pembuatan Chitosan Dari Kulit Udang dan Aplikasinya Untuk Pengawetan Bakso. Prosiding Penelitian. Jurusan Teknik Kimia. Fakultas Teknik. Universitas Diponegoro. Semarang. 15 hal.
Yulina, I. K. 2011. Aktivitas Antibakteri Kitosan Berdasarkan Perbedaan Derajat Deasetilasi dan Bobot Molekul. Sekolah Pascasarjana Institut Pertanian Bogor. Bogor. 78 hal.
Lampiran 7. Data Statistik Hasil Pengujian Rendemen
Lampiran 8. Data Statistik Hasil Pengujian Derajat Deasetilasi
Descriptive Statistics
ANOVA
Means for groups in homogeneous subsets are displayed.
Lampiran 9. Data Statistik Hasil Pengujian Kelarutan
Lampiran 10. Data Statistik Hasil
2 tahap 6 84,4333 4,71577 9,1850 ,25265
Lampiran 11. Data Statistik Hasil Pengujian Kadar Air
1 tahap 6 ,6883 ,29816 1,0833 ,13125
2 tahap 6 ,7533 ,52102 1,1000 ,22163
3 tahap 6 ,5167 ,18715 1,0050 ,09354
Total 18 ,6528 ,35615 1,0628 ,15461
ANOVA
kadar_air
Sum of Squares df Mean Square F Sig.
Between Groups ,179 2 ,090 ,681 ,521
Within Groups 1,977 15 ,132
Total 2,156 17
kadar_air
Duncan
perlakuan N Subset for
alpha = 0.05
1
3 tahap 6 1,0050
1 tahap 6 1,0833
2 tahap 6 1,1000
Sig. ,340
Means for groups in homogeneous subsets are displayed.
Lampiran 8. Alat Penelitian
Heat Stirer Magnetic bar
Beaker Glass pH Indikator
Thermometer Timbangan Analitik
Lampiran 9. Bahan Penelitian
NaOH
HCl
Asam Asetat Aquades