APLIKASI ELEKTROKOAGULASI PASANGAN ELEKTRODA
BESI UNTUK PENGOLAHAN AIR DENGAN SISTEM KONTINYU
APPLICATION OF ELECTROCOAGULATON IRON
ELECTRODE PAIRS FOR WATER TREATMENT WITH
CONTINUOUS SYSTEM
Andri Lukismanto* dan Abdu Fadli Assomadi** Jurusan Teknik Lingkungan-FTSP-ITS
*email: andri_l@enviro.its.ac.id **email: assomadi@its.ac.id
Abstrak
Telah dilakukan percobaan elektrokoagulasi pada outlet bak prasedimentasi PDAM Karang Pilang I dengan kekeruhan antara 100 – 130 NTU, menggunakan sistem yaitu batch dan kontinyu.kuat arus dan waktu kontak terbaik pada sistem batch digunakan sebagai dasar dalam sistem kontinyu yaitu dengan menggunakan kuat arus sebesar 2 A dengan waktu kontak yaitu 15menit ;16,7menit ;20menit;25menit ;33,3menit. Berdasar percobaan yang telah dilakukan didapatkan hasil yang terbaik yaitu pada waktu kontak 33,3menit untuk efisiensi penurunan kekeruhan sebesar 64% dan pada debit 20menit untuk penurunan warna sebesar 65,87%. Analisa biaya yang dilakukan pada proses ini adalah sebesar Rp 140,96 untuk elektrokoagulasi dan sebesar Rp 220 apabila kita menggunakan koagulan kimia dengan jumlah besi yang terlarut sebesar 6,128 gr setiap 196 L air yang diolah.
Kata kunci : Pengolahan Air, Elektrokoagulasi, Besi, Kontinyu
Abstract
In this electrocoagulation experiments using water samples originated from the outlet basin taps prasedimentasi PDAM Karang Pilang I , which has a turbidity of 100-130 NTU, then performed the analysis on the two systems are batch and continuous. The best results on the batch system is used as the basis in determining the continuous system is by using the current of 2 A with a discharge of 15, 16,7 , 20, 25, 33,3min. Based experiments have been carried out which showed the best results in discharge of 33min for turbidity reduction efficiency of 64% and on discharge of 20min for color reduction of 65.87%. Cost analysis conducted in this process is Rp 140.96 electrocoagulation process and Rp 220 if we use a chemical coagulant to the amount of dissolved iron at 6.128 grams per 196 liters of water were processed.
1. PENDAHULUAN 1.1. Latar Belakang
Ketersediaan air bersih di daerah kota merupakan hal yang vital untuk menunjang keberlangsungan aktifitas manusia sehari – hari, tidak dapat dipungkiri bahwa semakin berkembangnya zaman akan terjadi peningkatan jumlah penduduk dan akhirnya meningkat pula kebutuhan akan air bersih. Perusahaan Daerah Air Minum (PDAM) Surabaya adalah salah satu pemasok air minum ke masyarakat yang mengambil air baku dari sungai dimana harus sesuai dengan baku mutu sebagai air baku air minum. Dalam upaya penjernihan air baku, PDAM Surabaya menggunakan koagulan kimia yang tidak sedikit, penggunaan bahan kimia misalnya koagulan yang berlebih akan terjadi terjadi peningkatan biaya operasional Untuk menanggulangi biaya yang dikeluarkan diperlukan alternatif penganti tawas dan pastinya lebih efisien yaitu dengan Teknologi Elektrokoagulasi sebagai pengganti proses koagulasi – flokulasi yang sudah ada.
Adanya permasalahan diatas maka diperlukan suatu teknologi pengganti kebutuhan koagulan kimia yang semakin meningkat yaitu dengan metode elektrokoagulasi yaitu dengan mengalirkan arus ke suatu lempeng elektroda sehingga dapat menghasilkan ion – ion yang dapat bertindak seperti koagulan yang dapat mengikat pengotor dalam air baku
1.2. Perumusan Masalah
Dari latar belakang masalah di atas, dapat dirumuskan beberapa permasalahan, sebagai berikut: 1. Hubungan antara waktu kontak dan kuat arus terhadap efisiensi penurunan warna dan
kekeruhan dengan menggunakan elektroda Besi (Fe) pada sistem batch.
2. Hubungan antara waktu kontak dan kuat arus terhadap efisiensi penurunan warna dan kekeruhan dengan menggunakan elektroda Besi (Fe) pada sistem kontinyu.
3. Berapa jumlah besi yang terlarut dan perbandingan biaya yang diperlukan untuk proses elektrokoagulasi dibandingkan dengan penggunaan koagulan kimia.
Tujuan dari penelitian ini adalah:
1. Menentukan waktu kontak dan kuat arus terhadap efisiensi penurunan warna dan kekeruhan terbaik dengan menggunakan elektroda Besi (Fe) pada sistem batch.
2. Menentukan pengaruh waktu kontak dan kuat arus pada elektroda terhadap efisiensi penurunan warna dan kekeruhan terbaik dengan menggunakan elektroda Besi (Fe) pada sistem kontinyu.
3. Menghitung jumlah besi yang terlarut dan perbandingan biaya yang diperlukan untuk proses elektrokoagulasi dibandingkan dengan penggunaan koagulan kimia. (FeCl3)
1.4. Teori
Proses elektrokoagulasi merupakan gabungan dari proses elektrokimia dan proses koagulasi-flokulasi. Sel elektrokimia adalah sel yang menghasilkan transfer bentuk energi listrik menjadi energi kimia atau sebaliknya, melalui saling interaksi antara arus listrik dan reaksi redoks. Kajian-kajian yang mempelajari perubahan kimia oleh sebab adanya transfer elektron disebut elektrokimia (Santoso et al., 2000) dan Proses koagulasi dengan menggunakan koagulan yaitu suatu proses destabilisasi dan penggabungan dari partikel-partikel koloid dan halus yang tersuspensi dengan menggunakan bahan koagulan. Koagulan yang banyak digunakan adalah kapur, tawas, dan kaporit. Pertimbangan pemberiannya adalah karena garam-garam Ca, Fe, dll yang bersifat tidak larut dalam air akan mengendap bila bertemu dengan sisa-sisa basa (Kusnaedi, 1995).
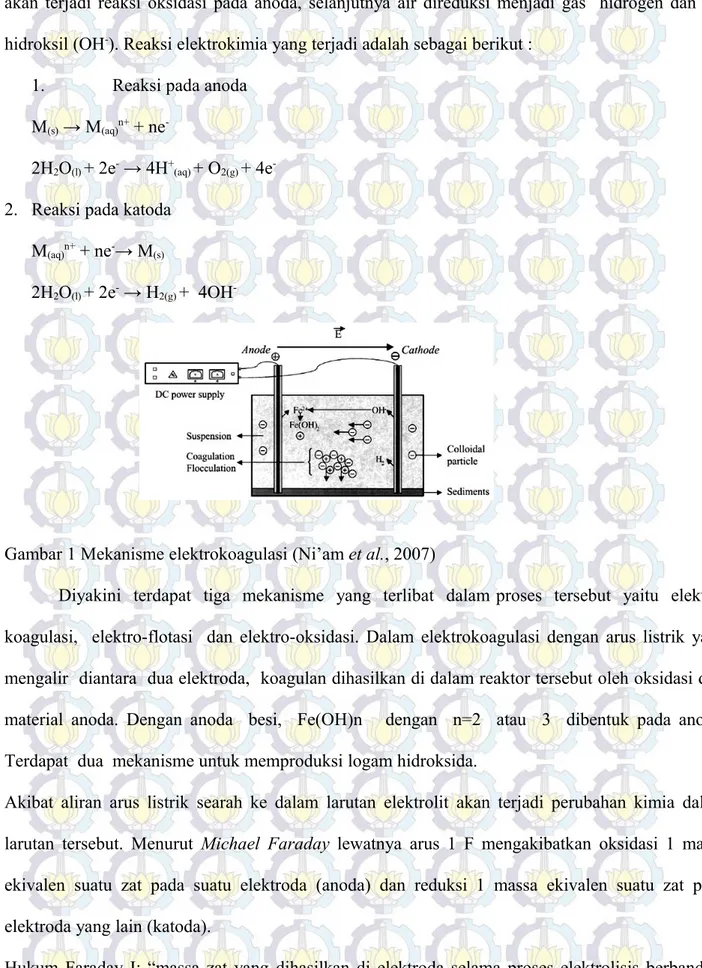
Teknik elektrokoagulasi menggunakan arus searah (Direct Current) yang menyebabkan ion dari anoda yang dikorbankan menyisihkan kontaminan melalui reaksi kimia dan pengendapan atau dengan mengikat partikel koloid kemudian menyisihkannya melalui flotasi. pH, jenis dan konsentrasi polutan, ukuran dan posisi gelembung, stabilitas flok dan kecepatan pengendapan, semua itu dipengaruhi oleh proses elektrokoagulasi. Mekanisme dari elektrokoagulasi dapat dilihat pada Gambar 1. Ketika anoda dan katoda sudah dihubungkan dengan sumber arus dari luar, maka
akan terjadi reaksi oksidasi pada anoda, selanjutnya air direduksi menjadi gas hidrogen dan ion hidroksil (OH-). Reaksi elektrokimia yang terjadi adalah sebagai berikut :
1. Reaksi pada anoda M(s) → M(aq)n+ + ne
2H2O(l) + 2e- → 4H+(aq) + O2(g) + 4e -2. Reaksi pada katoda
M(aq)n+ + ne-→ M(s)
2H2O(l) + 2e- → H2(g) + 4OH
-Gambar 1 Mekanisme elektrokoagulasi (Ni’am et al., 2007)
Diyakini terdapat tiga mekanisme yang terlibat dalam proses tersebut yaitu elektro-koagulasi, elektro-flotasi dan elektro-oksidasi. Dalam elektrokoagulasi dengan arus listrik yang mengalir diantara dua elektroda, koagulan dihasilkan di dalam reaktor tersebut oleh oksidasi dari material anoda. Dengan anoda besi, Fe(OH)n dengan n=2 atau 3 dibentuk pada anoda. Terdapat dua mekanisme untuk memproduksi logam hidroksida.
Akibat aliran arus listrik searah ke dalam larutan elektrolit akan terjadi perubahan kimia dalam larutan tersebut. Menurut Michael Faraday lewatnya arus 1 F mengakibatkan oksidasi 1 massa ekivalen suatu zat pada suatu elektroda (anoda) dan reduksi 1 massa ekivalen suatu zat pada elektroda yang lain (katoda).
Hukum Faraday I: “massa zat yang dihasilkan di elektroda selama proses elektrolisis berbanding lurus dengan banyaknya mol elektron (kuantitas kelistrikan) yang diberikan ke elektroda”.
w ~ Q
w = massa zat yang diendapkan (g).
• w ~ I.t
Q = jumlah arus listrik = muatan listrik (C) w = e.I.t = gek.I.t = = Ar.I.t
F n. F
e = tetapan = (gek : F)
I = kuat arus listrik (A).
gek = massa ekivalen zat (gek). t = waktu (dt).
n = valensi ion.
Ar = massa atom relatif.
F = bilangan faraday = 96 500 C.
Massa ekivalen = massa zat yang sebanding dengan 1 mol elektron = 6,02 x 1023 ē. 1 gek ~ 1 mol ē
2. METODOLOGI
Pada penelitian ini dilakukan analisa terhadap kemampuan elektroda dari plat Besi (Fe) sebagai anoda dan katoda dalam menurunkan kekeruhan dan warna dengan menggunakan metode elektrokoagulasi. Ada dua tahapan dalam analisa ini yaitu Percobaan Pendahuluan (sistem Batch) dan Percobaan Lanjutan (Sistem Kontinyu). Percobaan pendahuluan dilakukan terhadap variasi waktu kontak dan kuat arus yang digunakan dalam metode batch untuk mengetahui besarnya pengaruh waktu kontak dan kuat arus terhadap efisiensi penurunan kekeruhan dan warna yang terbaik, Kuat arus yang dipakai adalah 1,2 A; 0,9A; 0,6 A; dan 1,2 A, serta waktu yang dipakai adalah 120 ,60, 40 dan 30 detik.
Percobaan Lanjutan (Sistem Kontinyu) dilakukan dengan aliran kontinyu dengan menggunakan elektroda Besi (Fe) sebagai anoda dan katoda dengan menggunakan variasi debit yang merupakan hasil dari waktu kontak terbaik.dari percobaan pendahuluan sehingga didapatkan debit dan kuat arus yag terbaik dalam analisa ini. Pada penelitian ini juga dilakukan perbandingan tehadap karakteristik fisik flok yang dihasilkan dengan metode elektrokoagulasi dan dengan penggunaan bahan kimia
3. HASIL DAN PEMBAHASAN
Pada penelitian elektrokoagulasi ini dilakukan dua percobaan yaitu percobaan pendahuluan yang dilakukan dengan sistem batch dan percobaan lanjutan dengan sistem kontinyu
3.1 Percobaan Pendahuluan
Percobaan pendahuluan dilakukan dengan Sistem Batch yaitu menggunakan air sampel yang diambil dari outlet PDAM Karangpilang I dengan karakteristik kekeruhan sebesar 100 – 130 NTU dan range pH antara 6 – 8 kemudian dianalisa dalam wadah berukuran 1000 ml dimana sampel diberi aliran arus dan waktu kontak sesuai dengan yang ditentukan. Pada saat arus mengalir dilakukan pengadukan dengan menggunakan magnetik stirrer dengan kecepatan 200 rpm dan 50 rpm sebagai proses pengadukan cepat dan pengadukan lambat. Pengambilan sampel dalam percobaan pendahuluan dilakukan sebelum operasi dan setelah proses sedimentasi selama 15 menit. Percobaan pendahuluan bertujuan mendapatkan kuat arus dan waktu kontak terbaik kemudian diagunakan pada sistem kontinyu. Parameter yang digunakan adalah kekeruhan, pH, warna, dan Daya Hantar Listrik (DHL).
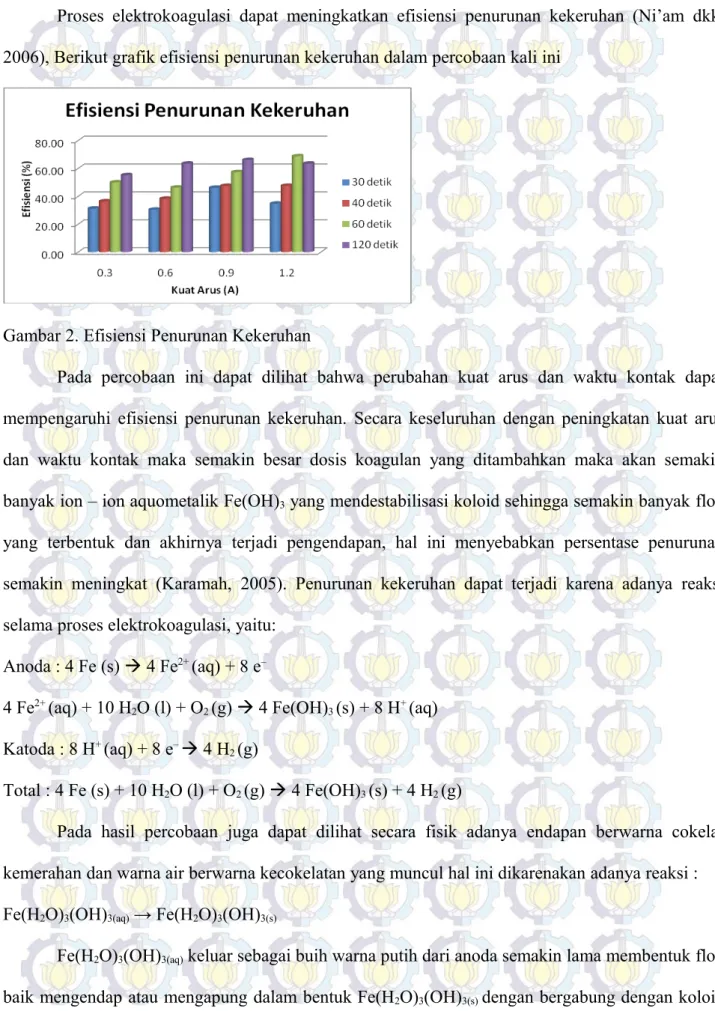
Proses elektrokoagulasi dapat meningkatkan efisiensi penurunan kekeruhan (Ni’am dkk, 2006), Berikut grafik efisiensi penurunan kekeruhan dalam percobaan kali ini
Gambar 2. Efisiensi Penurunan Kekeruhan
Pada percobaan ini dapat dilihat bahwa perubahan kuat arus dan waktu kontak dapat mempengaruhi efisiensi penurunan kekeruhan. Secara keseluruhan dengan peningkatan kuat arus dan waktu kontak maka semakin besar dosis koagulan yang ditambahkan maka akan semakin banyak ion – ion aquometalik Fe(OH)3 yang mendestabilisasi koloid sehingga semakin banyak flok yang terbentuk dan akhirnya terjadi pengendapan, hal ini menyebabkan persentase penurunan semakin meningkat (Karamah, 2005). Penurunan kekeruhan dapat terjadi karena adanya reaksi selama proses elektrokoagulasi, yaitu:
Anoda : 4 Fe (s) 4 Fe2+ (aq) + 8 e–
4 Fe2+ (aq) + 10 H2O (l) + O2 (g) 4 Fe(OH)3 (s) + 8 H+ (aq) Katoda : 8 H+ (aq) + 8 e– 4 H2 (g)
Total : 4 Fe (s) + 10 H2O (l) + O2 (g) 4 Fe(OH)3 (s) + 4 H2 (g)
Pada hasil percobaan juga dapat dilihat secara fisik adanya endapan berwarna cokelat kemerahan dan warna air berwarna kecokelatan yang muncul hal ini dikarenakan adanya reaksi : Fe(H2O)3(OH)3(aq) → Fe(H2O)3(OH)3(s)
Fe(H2O)3(OH)3(aq) keluar sebagai buih warna putih dari anoda semakin lama membentuk flok baik mengendap atau mengapung dalam bentuk Fe(H2O)3(OH)3(s) dengan bergabung dengan koloid
sehingga warna putih berubah menjadi warna cokelat kemerahan. Secara bersamaan timbul Warna kuning diakibatkan oleh lepasnya Fe2+ dimana larut dalam air.
Pada percobaan ini didapatkan efisiensi terbesar penurunan sebesar 68,75% yaitu pada sampel yang mengalami perlakuan dengan kuat arus 1,2 Ampere dan waktu kontak 60 detik yaitu dari kekeruhan awal sebesar 128 NTU menjadi 40 NTU. Ternyata pada kondisi terbaik ini masih belum memenuhi kriteria kekeruhan yang masuk ke filter yaitu sebesar kurang dari 5 NTU. Hal ini kemungkinan dikarenakan waktu untuk proses sedimentasi yang kurang karena waktu pengendapan untuk koagulan dari garam Fe adalah 1 jam (Aguiler dkk dalam Karamah, 2006) sehingga masih banyak flok – flok yang belum turun untuk mengendap.
3.1.2. Analisa perubahan pH
pH sampel dapat mempengaruhi kelarutan dari suatu koagulan. Semakin mudah larut suatu koagulan, maka semakin mudah terbentuknya ion aquometalik yang akhirnya semakin cepatnya partikel koloid ternetralisasi membentuk flok. Apabila reaksi tidak berada pada pH optimal maka ion aquometalik semakin sulit terbentuk, yang akhirnya mengurangi jumlah partikel koloid yang dapat ternetralisasi membentuk flok. Pembentukan gas Hidrogen (H2) pada katoda selama proses elektrokoagulasi juga terjadi seiring dengan lepasnya ion OH- ke dalam larutan. Berikut tabel perubahan pH pada percobaan ini
Tabel 1 Perubahan nilai pH pada Percobaan Pendahuluan
(A) pHo pHt ∆pH pHo pHt ∆pH pHo pHt ∆pH pHo pHt ∆pH 0.3 7.0 8 7.2 0 0.12 6.5 0 7.1 0 0.60 7.0 0 7.2 0 0.20 7.1 5 7.4 1 0.26 0.6 7.0 6 7.2 9 0.23 6.8 0 7.3 5 0.55 7.3 0 7.4 0 0.10 7.4 0 7.5 0 0.10 0.9 7.5 0 7.7 0 0.20 7.3 5 7.4 0 0.05 7.4 0 7.4 7 0.07 7.5 0 8.1 6 0.66 1.2 7.8 0 8.1 0 0.30 8.0 5 7.5 0 -0.55 7.1 5 6.3 0 -0.85 7.9 0 7.1 7 -0.73
Telah dijelaskan pada teori sebelumnya bahwa terjadi dua mekanisme yang mungkin terjadi pada proses elektrokoagulasi sehingga berpengaruh pada perubahan pH yang terjadi. Pada saat kuat arus antara 0,3 – 0,9 Ampere terjadi kenaikan kenaikan nilai pH, hal ini disebabkan karena katoda memproduksi ion hidroksi (OH-) secara berlebih (Babu et al., 2007), seiring dengan pertambahan waktu proses elektrolisa (listrik dinyalakan dalam air) maka pH akan meningkat, dengan adanya peningkatan pH ini maka dapat diketahui bahwa proses koagulasi berjalan, dengan reaksi yaitu Pada Anoda : Fe Fe2+ + 2 e -Fe 2+ + 2 OH- Fe(OH)2 Pada Katoda : 2 H2O + 2 e- H2 + 2 OH -Reaksi Keseluruhan : Fe2+ + 2 H2O + O2 Fe(OH)2 + H2
Jika kondisi air sampel mempunyai pH lebih besar dari 6 maka ion aquometalic Fe(OH)2 akan secara mudah teroksidasi menjadi ferric hydroxide (Fe(OH)3) oleh oksigen terlarut dan membentuk flok yang sangat tidak terlarut dengan reaksi sebagai berikut :
Secara umum memang terjadi kenaikan pH tetapi pada percobaan berikutnya terjadi penurunan pH hal ini dikarenakan produksi ion H+ pada saat proses elektrokoagulasi yaitu pada reaksi Pada Anoda : 4 Fe 4 Fe 2+ + 8 e -4 Fe 2+ + 10 H2O + O2 4 Fe(OH)3 + 8 H+ Pada Katoda : 8 H+ + 8e- 4 H2 Reaksi Keseluruhan : 4 Fe 2+ + 10 H2O + O2 4 Fe(OH)3 + 4 H2
Alasan dilakukan pengukuran pH adalah dengan adanya perubahan nilai pH maka dapat dipastikan bahwa proses elektrokimia / elektrolisis telah berjalan, sehingga elektrokoagulasi dapat dilihat atau dikontrol dari terbentuknya gelembung – gelembung yang muncul dan perubahan nilai pH.
3.1.3. Analisa Perubahan Warna
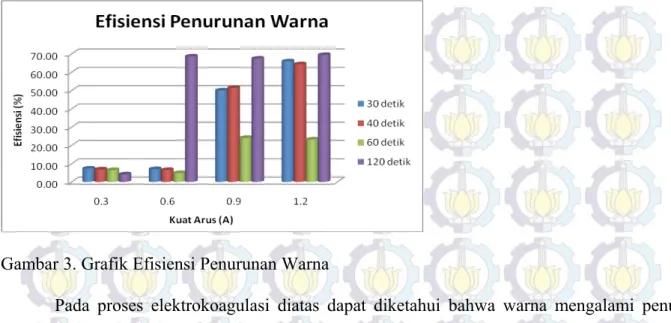
Parameter warna merupakan hal yang penting dalam air karena mempengaruhi estetika dalam hal penggunaannya sehingga sesungguhnya proses koagulasi dan flokulasi yang dilaksanakan pada air berwarna tidak lain adalah melaksanakan proses adsorpsi dengan bantuan penambahan bahan kimia .Berikut grafik efisiensi penuruna warna yang terjadi dalam proses ini.
Gambar 3. Grafik Efisiensi Penurunan Warna
Pada proses elektrokoagulasi diatas dapat diketahui bahwa warna mengalami penurunan. Penurunan warna disebabkan oleh proses adsorbsi, dimana substansi molekul meninggalkan larutan dan bergabung pada permukaan zat padat (koagulan) dari proses elektrokoagulasi. Proses adsorbsi disini berfungsi untuk menyisihkan senyawa-senyawa aromatik dan senyawa organik terlarut. Berdasarkan data di atas dapat diketahui bahwa terjadi penurunan warna pada sampel air seiring dengan penurunan kekeruhan pada sampel air dengan penurunan terbesar terjadi pada saat air sampel dialiri arus sebesar 1,2 Ampere dengan waktu 120 detik. Terdapat permasalahan yaitu timbulnya warna kuning kecokelatan akibat adanya pada air setelah proses elektrokoagulasi tetapi masih memenuhi baku mutu Permenkes No. 907 Tahun 2002 yaitu kurang dari 15 TCU.
Pada analisa warna terdapat kekurangan yaitu analisa warna dilakukan dengan standar PtCo seharusnya dilakukan analisa terhadap warna yang diakibatkan oleh Fe2+ sehingga dapat diketahui hasil warna setelah proses elektrokoagulasi dengan menggunakan logam Besi dimana berwarna kuning. Maka dibuatlah kurva kalibrasi besi untuk dibandingkan dengan kurva kalibrasi standar PtCo didapatkan pada tabel berikut.
Tabel 2. Perbandingan nilai kalibrasi
PtCo Fe
R 0,999 0,994
Y 0,005x 0,019x + 0,023
(hasil pengamatan)
3.1.4. Perubahan Nilai Daya Hantar Listrik (DHL)
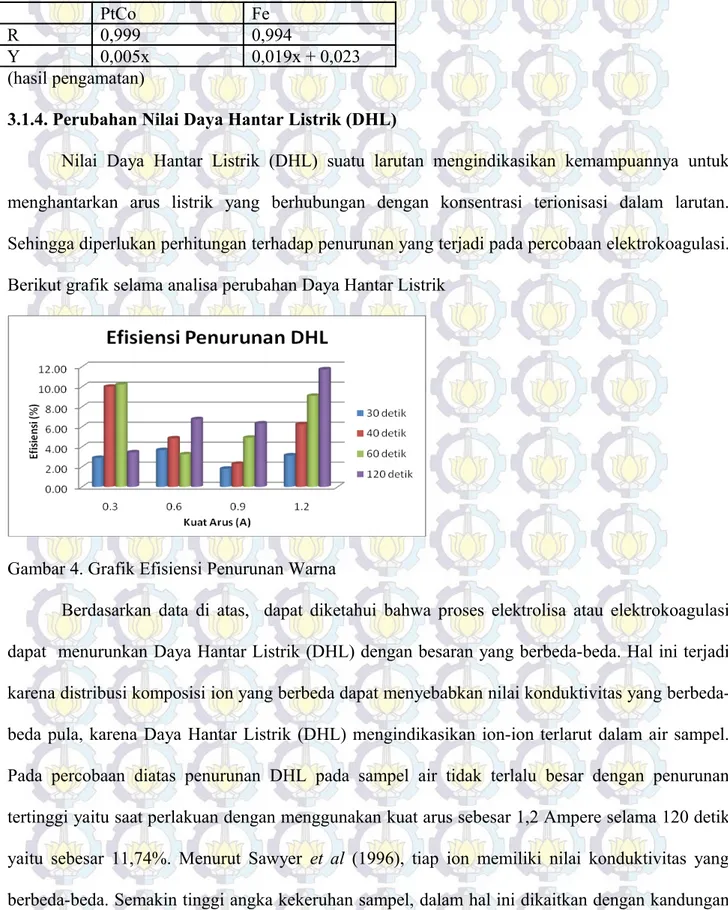
Nilai Daya Hantar Listrik (DHL) suatu larutan mengindikasikan kemampuannya untuk menghantarkan arus listrik yang berhubungan dengan konsentrasi terionisasi dalam larutan. Sehingga diperlukan perhitungan terhadap penurunan yang terjadi pada percobaan elektrokoagulasi. Berikut grafik selama analisa perubahan Daya Hantar Listrik
Gambar 4. Grafik Efisiensi Penurunan Warna
Berdasarkan data di atas, dapat diketahui bahwa proses elektrolisa atau elektrokoagulasi dapat menurunkan Daya Hantar Listrik (DHL) dengan besaran yang berbeda-beda. Hal ini terjadi karena distribusi komposisi ion yang berbeda dapat menyebabkan nilai konduktivitas yang berbeda-beda pula, karena Daya Hantar Listrik (DHL) mengindikasikan ion-ion terlarut dalam air sampel. Pada percobaan diatas penurunan DHL pada sampel air tidak terlalu besar dengan penurunan tertinggi yaitu saat perlakuan dengan menggunakan kuat arus sebesar 1,2 Ampere selama 120 detik yaitu sebesar 11,74%. Menurut Sawyer et al (1996), tiap ion memiliki nilai konduktivitas yang berbeda-beda. Semakin tinggi angka kekeruhan sampel, dalam hal ini dikaitkan dengan kandungan zat padat terlarut yang terdapat dalam sampel, maka semakin tinggi pula nilai DHLnya. Menurut
Alaerts dan Sumestri (1984), angka DHL seimbang dengan jumlah zat padat terlarut (garam terlarut). Nilai DHL tinggi pada larutan dengan jumlah zat padat terlarut yang tinggi pula. Pada proses elektrokogulasi, semakin lama waktu operasi sehingga dosis yang dikeluarkan semakin meningkat akan meningkatkan efisiensi penurunan nilai TDS (Karamah, 2006)
Nilai DHL diperlukan dikarenakan diperlukan pergerakan ion dari katoda ke anoda sehingga proses ini dapat berjalan, penurunan nilai DHL dapat diindikasikan dengan penurunan kuat arus pada saat proses elektrokoagulasi berlangsung.
3.2. Percobaan Lanjutan (Sistem Kontinyu)
Percobaan Lanjutan dilakukan dengan pada reaktor kontinyu yaitu menggunakan air sampel dari outlen PDAM Karangpilang I dianalisa dengan mengalirkan air sampel tersebut pada sebuah reaktor dengan variasi kuat arus dan waktu terbaik yang didapatkan dari percobaan pendahuluan, hasil yang didapatkan yaitu pada kuat arus 120 Ampere dan waktu kontak 60 detik.
3.2.1. Penentuan Kebutuhan Kuat Arus dan Debit yang Digunakan pada Reaktor Kontinyu Pada reaktor kontinyu, reaktor elektrokoagulasi-flokulasi-sedimentasi menjadi satu rangkaian. Pada percobaan lanjutan menggunakan elektroda besi dengan dimensi 300 mm x 50 mm x 5 mm dengan jumlah total 10 buah yang dipasang pararel.
Perhitungan :
Berdasar dari percobaan pendahuluan, diperoleh data berikut :
• Kuat Arus sebesar 1,2 Ampere
• Waktu kontak 60 detik
• Volume air 1liter
• Sehingga dapat diartikan bahwa debit pada percobaan pendahuluan yaitu 1 liter / menit
Pada reaktor kontinyu, volume ruangan elektrokoagulasi sebesar 25 liter.Sehingga dibutuhkan arus sebesar :
25 x 1,2 Ampere = 30 Ampere
Jadi dibutuhkan arus sebesar 30 Ampere dengan debit 25 liter / menit. Pada percobaan kali ini peralatan yang ada mempunyai nilai arus maksimum yaitu sebesar 2 Ampere sehingga debit kontak yang dibutuhkan sebesar
menit liter / 66 , 1 2 30 t liter/meni 25 = ⋅ = Ampere Ampere Q
Semakin lama waktu proses elektrokoagulasi maka pembetukan H2 dan OH- semakin banyak sehingga semakin banyak pula jumlah kompleks yang mengikat polutan dan jumlah gas hidrogen. Dengan demikian jumlah polutan dalam larutan akan semakin berkurang (Putero. S.H. dkk, 2008). Oleh karena itu berdasarkan hasil perhitungan di atas diperoleh besar kuat arus yang dibutuhkan untuk percobaan kontinyu sebesar 2A dengan debit yaitu 1,66 dm3/liter sehingga dilakukan variasi debit yaitu sebesar 1,66 l/menit ; 1,5 l/menit ; 1,25 l/menit ; 1 l/menit dan 0,75 l/menit atau apabila dikonversi ke waktu kontak adalah sebesar 15 , 16,7 , 20 , 25 , 33,3 menit. 3.2.2. Analisa Perubahan Kekeruhan, pH, warna, dan Daya Hantar Listrik
Seperti halnya pada percobaan pendahhuluan, Percobaan Lanjutan juga menganalisa perubahan yang terjadi pada Kekeruhan, pH, warna, dan Daya Hantar Listrik pada air sampel sehingga didapatkan pada tebel berikut ini
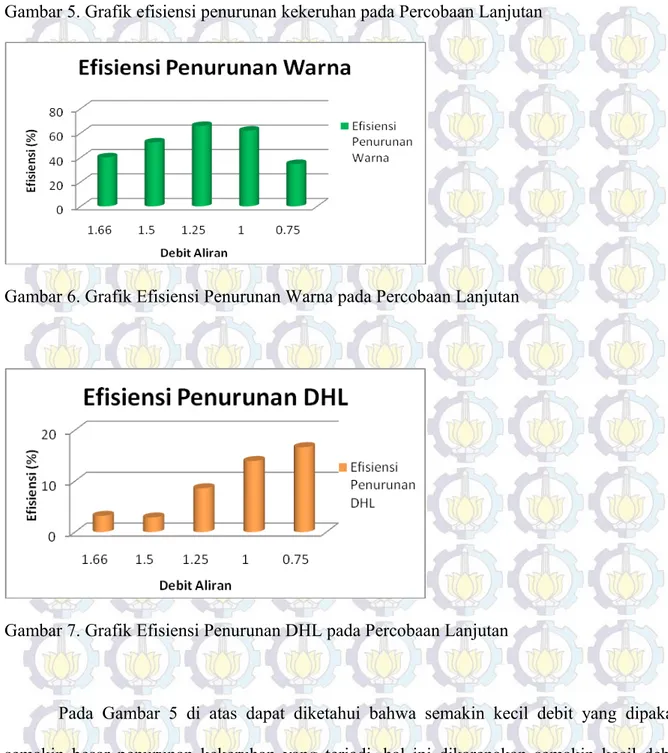
Gambar 5. Grafik efisiensi penurunan kekeruhan pada Percobaan Lanjutan
Gambar 6. Grafik Efisiensi Penurunan Warna pada Percobaan Lanjutan
Gambar 7. Grafik Efisiensi Penurunan DHL pada Percobaan Lanjutan
Pada Gambar 5 di atas dapat diketahui bahwa semakin kecil debit yang dipakai maka semakin besar penurunan kekeruhan yang terjadi, hal ini dikarenakan semakin kecil debit maka waktu kontak antara elektroda yang dialiri arus listrik dengan air semakin lama sehingga banyak terjadi pengikatan antara Fe3+ terhadap partikel sehingga terbentuk flok yang semakin banyak berwarna cokelat. Jadi efisiensi penurunan kekeruhan terbesar pada percobaan kali ini berada pada debit kontak sebesar 0,75 liter / menit yaitu sebesar 64 %.
Pada Gambar 6 dapat diketahui bahwa terjadi penurunan warna sejalan dengan penurunan debit yang masuk ke reaktor kontinyu. Warna yang timbul ternyata masih sesuai dengan
PERMENKES No. 907 Tahun 2002. Jadi, penurunan warna terbesar berada pada waktu kontak sebesar 1,25 liter / menit yaitu sebesar 65,87% untuk standar PtCo
Berdasarkan Gambar 7 di atas dapat diketahui bahwa Daya Hantar Listrik (DHL) pada sampel air mengalami penurunan seiring dengan berkurangnya debit air yang masuk dalam reaktor dengan penurunan terbesar terjadi pada debit 0,75 liter / menit yaitu sebesar 16,67 %
Selain adanya perubahan kekeruhan , warna dan daya hantar listrik juga terjadi perubahan nilai pH pada proses elektrokoagulasi, perubahan ini ditampilkan dalam tabel berikut
Tabel 3 . Penurunan Nilai pH sampel air debit (liter/menit) pHo pHf ∆ Ph 1.66 7.6 7.4 -0.2 1.5 7.6 7.3 -0.3 1.25 7.62 7.22 -0.4 1 7.6 7.3 -0.3 0.75 7.85 7.62 -0.23
Pada percobaan kontinyu dapat dilihat bahwa pH cenderung tetap atau tidak mengalami perubahan karena pada dasarnya penurunan 0,2 – 0,4 pada pH tidak terlalu berpengaruh pada hasil elektrokoagulasi. penurunan pH hal ini dikarenakan produksi ion H+ pada saat proses elektrokoagulasi yaitu pada reaksi
Pada Anoda: 4 Fe 4 Fe 2+ + 8 e -4 Fe 2+ + 10 H2O + O2 4 Fe(OH)3 + 8 H+ Pada Katoda : 8 H+ + 8e- 4 H2 Reaksi Keseluruhan : 4 Fe 2+ + 10 H2O + O2 4 Fe(OH)3 + 4 H2
3.3. Analisa Berat Plat Besi
Untuk mengetahui berat plat Besi (Fe) yang melarut atau melepaskan ionnya dapat dihitung dari masa logam Besi yang larut dengan cara perhitungan secara teoritis, yaitu sebagai berikut: Berdasarkan dari kondisi yang optimal maka didapatkan debit air yang digunakan adalah sebesar 0,75 liter / menit, dengan volume reaktor sebesar 196 L maka waktu kontak adalah selama
t = V = 196 Liter = 4,4, jam Q 0,75 L/menit
Berdasarkan hasil perhitungan secara teoritis
Apabila tanpa diperhitungkan densitas bahan, menggunakan hukum Faraday . Arus yang mengalir pada setiap rangkaian paralel sebesar 2 A, berat atom Besi = 56 , n (jumlah ekivalen elektron yang terlibat) = 3, maka jumlah masa yang teroksidasi atau terlarut sebesar:
nxF Ixtxa m= 96500 3 56 ) 3600 4 , 4 ( 2 x x x Ax = =6,128 gr
jadi pada percobaan kontinyu dengan penurunan sebesar 64%, elektroda besi yang meluruh sebesar 6,128 gr
3.4. BIAYA OPERASIONAL 3.4.1 Proses Elektrokoagulasi
Untuk menghitung biaya pengolahan elektrokoagulasi, diberikan batasan-batasan sebagai berikut. 1. Biaya operasional adalah biaya pengoperasian instalasi listrik rumah tangga sesuai dengan
golongan tarif yang ditetapkan PLN.
2. Perhitungan biaya pengoperasian tidak termasuk biaya beban listrik sesuai golongan tarif yang ditetapkan PLN.
4. Biaya dihitung untuk penurunan kekeruhan tertinggi dari hasil percobaan yaitu pada tingkat 64%.
Untuk penurunan kekeruhan pada prosentase 64%, alat elektrokoagulasi dioperasikan pada : 1. Jarak antara elektrode 1,5 cm
2. Arus listrik 2 Ampere 3. Jumlah elektrode 10 buah 4. Lama air dalam bak 4,4 jam Volume air yang dihasilkan 196 liter,
Daya listrik yang digunakan dalam satuan Kilo Watt Hour (KWh) adalah : P = V.I.h/1000
Dimana :
P = daya listrik (KWh) V = Potensial listrik (volt) I = Arus Listrik (ampere) H = waktu (jam)
Biaya Litrik Rp 1200 / kwh
Tegangan (V) yang dikeluarkan untuk pengoperasian alat pada I = 2 Ampere adalah 9 Volt. Waktu operasi selama 4,4 jam adalah :
P = 9 x 2 x 4,4/1000 = 0,0792 KWh
Biaya listrik untuk menghasilkan 196 liter air adalah biaya pemakaian KWh (Rp/KWh) dikalikan dengan besarnya daya listrik yang digunakan.
Biaya listrik = Rp 1200 x 0,0792 = Rp 95
jadi apabila dipakai terus menerus selama 24 jam, maka biaya yang dibutuhkan tiap hari adalah sebesar Rp 95,00 x 24/4,4 = Rp 520,00
Besi yang telarut pada saat proses elektrokoagulasi adalah
6,128 gr dengan harga besi Rp. 7500,00 / kg , sehingga biaya yang dikeluarkan sebesar 0,006128 kg x Rp. 15.000 = Rp 45,96
Jadi total biaya yang dikeluarkan sebesar
Rp 95 + Rp 45,96 = 140,96 tiap 196 air yang terolah
3.4.2. Proses Koagulasi dengan Koagulan Kimia (FeCl3)
Pada perhitungan biaya operasional yaitu dihitung jumlah FeCl3 yang diperlukan untuk mengolah air sebanyak yang telah dilakukan dalam elektrokoagulasi yaitu sebanyak 196 Liter. Maka dosis yang diperlukan adalah dengan menghitung dari kuat arus optimum yaitu sebesar 1,2 Ampere jadi :
nxF IxtxMr w= w = 1,2 A x 60 detik x 162,5 3 x 96500 w = 0,040 gr
w = 40 mg dalam 1 liter air sampel jadi diperlukan dosis 40 mg/l
Dari data datas dapat dihitung kebutuhan FeCl3 adalah sebagai berikut dengan harga tiap kg sebesar Rp.25.000,00
FeCl3 (kg) = 40 mg / liter. x 196 Liter = 0,007840 kg Jadi biaya yang diperlukan
Biaya (Rp) = 0,007840 kg x Rp.25.000,00 = Rp. 196.,00
Biaya listrik pada saat jartest adalah menggunakan alat dengan daya sebesar 200 watt dengan waktu 1 menit koagulasi dan 5 menit flokulasi
= 200 watt x 0,1 jam = 20 wh / 1000 = 0,02 kwh
Biaya listrik 0,02 x Rp. 1200 = 24 rupiah
Total biaya yang diperlukan adalah Rp 196 + Rp 24 = Rp 220
4. Kesimpulan dan Saran 4.1 Kesimpulan
Berdasarkan hasil percobaan elektrokoagulasi baik pada percobaan pendahuluan maupun percobaan lanjutan dapat diketahui bahwa :
1 Pada percobaan pendahuluan pada sistem batch didapatkan :
nilai efisiensi penurunan kekeruhan terbesar adalah 68,75% yang terjadi pada saat air sampel diberi arus listrik sebesar 1,2 Ampere dengan waktu kontak selama 60 detik
nilai efisiensi penurunan warna terbesar adalah 69,37 % yang terjadi pada saat air sampel diberi arus listrik sebesar 1,2 Ampere dengan waktu kontak selama 120 detik.
2 Pada percobaan lanjutan pada sistem kontinyu didapatkan :
nilai efisiensi penurunan kekeruhan terbesar adalah 64 % yang terjadi pada saat air sampel diberi arus listrik sebesar 2 Ampere dengan waktu kontak 33menit
nilai efisiensi penurunan warna terbesar adalah 65,87 % yang terjadi pada saat air sampel diberi arus listrik sebesar 2 Ampere dengan waktu kontak 20menit
Pada Proses elektrokoagulasi sebesar Rp 140,96 dan apabila menggunakan koagulan kimia sebesar Rp 220 tiap 196 liter air yang terolah atau 36% lebih murah dengan menggunakan proses elektrokoagulasi
Berat besi yang terlarut sebesar 6,128 gr tiap 196 liter air yang terolah 4.2. Saran
1. Perlu dilakukan analisa kadar Fe dalam air hasil elektrokoagulasi apakah masih memenuhi baku mutu Permenkes 907 tahun 2002
2. Warna kuning yang muncul, masih mengganggu estetika sehingga diperlukan pengolahan lanjutan untuk mereduksi warna
DAFTAR KEPUSTAKAAN
Alaerts, G., dan Sumestri S. 1984. Metode Penelitian Air. Surabaya : Usaha Nasional
Karamah, E. F., dan Bismo, S.. 2006.” Pengaruh Dosis Koagulan PAC Dan Surfaktan SLS Terhadap Kinerja Proses Pengolahan Limbah Cair Yang Mengandung Logam Besi(Fe), Tembaga (Cu), Dan Nikel (Ni) Dengan Flotasi Ozon”. Departemen Teknik Kimia, Fakultas Teknik Universitas Indonesia. Kampus UI Depok
Karamah, E. F., dan Kostiano, F. G,. 2005.”Perbandingan Pralakuan Koagulasi dengan menggunakan FeSO4.7H2O dan Al2(SO4)3.18H2O Terhadap Kinerja Membran Mikrofiltrasi
Polypropilene Hollow Fiber”. Prosiding Seminar Nasional Teknologi Proses Kimia VII
2005. ISSN 1410-9891
Kusnaedi, 1995. Mengolah Air Gambut dan Air Kotor untuk Air Minum. Penebar Swadaya Ni’am, M. F., Othman, F., Sohaili, J., dan Fauzia, Z.. 2006.“Combined Magnetic Field
and Electrocoagulation Process for Suspended Solid Removal from Wastewater”. Proceedings of the 1st International Conference on Natural Resources Engineering
& Technology 2006. Putrajaya, Malaysia
Ni’am, M. F., Othman, F., Sohaili, J., dan Fauzia, Z.. 2006. “ Enhancing Suspended Solids Removal From Wastewater Using Fe Electrodes”. Malaysian Journal of Civil Engineering 18(2) : 139-148
Sawyer, C dan Perry L.M. 1994. Chemistry For Environmental Engineering 3rd Edition. New York : McGraw Hill, Book Company,