MELALUI REAKSI TRANSESTERIFIKASI
SKRIPSI
EKA MARGARETHA LUMBANTORUAN 170822014
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATERA UTARA
MEDAN 2019
SINTESIS ESTER SELULOSA STEARAT DARI SELULOSA JERAMI PADI (Oriza Sativa L) DENGAN METIL STEARAT
MELALUI REAKSI TRANSESTERIFIKASI
SKRIPSI
Diajukan untuk melengkapi tugas dan memenuhi syarat mencapai gelar Sarjana Sains
EKA MARGARETHA LUMBANTORUAN 170822014
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATERA UTARA
MEDAN 2019
PERNYATAAN ORISINALITAS
SINTESIS ESTER SELULOSA STEARAT DARI SELULOSA JERAMI PADI (Oriza Sativa L) DENGAN METIL STEARAT
MELALUI REAKSI TRANSESTERIFIKASI
SKRIPSI
Saya menyatakan bahwa skripsi ini adalah hasil karya saya sendiri, kecuali beberapa kutipan dan ringkasan yang masing-masing disebutkan sumbernya.
Medan, Desember 2019
Eka Margaretha Lumbantoruan 170822014
PENGESAHAN SKRIPSI
Judul : SINTESIS ESTER SELULOSA STEARAT DARI
SELULOSA JERAMI PADI (Oriza Sativa L.) DENGAN METIL STEARAT MELALUI REAKSI
TRANSESTERIFIKASI
Kategori : Skripsi
Nama : Eka Margaretha Lumbantoruan
Nomor Induk Mahasiswa : 170822014 Program Studi : Sarjana Kimia
Fakultas : Matematika dan Ilmu Pengetahuan Alam Universitas Sumatera Utara
Disetujui di Medan, Desember 2019
Diketahui Oleh
Departemen Kimia FMIPA USU Pembimbing Ketua,
Dr. Cut Fatimah Zuhra, M.Si. Dr. Adil Ginting, M.Sc
NIP : 197405051999032001 NIDK : 8882190018
SINTESIS ESTER SELULOSA STEARAT DARI SELULOSA JERAMI PADI (Oriza Sativa L) DENGAN METIL STEARAT
MELALUI REAKSI TRANSESTERIFIKASI
ABSTRAK
Selulosa stearat telah disintesis melalui reaksi transesterifikasi antara α- selulosa hasil isolasi dari jerami padi (Oriza Sativa L) dengan metil stearat. Dimana sintesis metil stearat dilakukan dengan mereaksikan metanol dan asam stearat dengan bantuan katalis H2SO4(p). Terbentukya metil stearat didukung oleh data spektrum FT- IR dengan puncak vibrasi bilangan gelombang 2917,14 cm-1 menunjukkan gugus C- H stretching, 1739,35 cm-1 menunjukkan gugus C=O, 1173,09 cm-1 menunjukkan gugus C-O-C. Sintesis selulosa stearat dilakukan dengan cara refluks selama 4 jam menggunakan pelarut metanol dengan variasi katalis Na2CO3 10, 15, 20, 25, dan 30 mg dengan variasi terbaik ditentukan berdasarkan uji derajat substitusi yaitu dengan katalis Na2CO3 30 mg sebesar 1,299. Hasil sintesis yaitu selulosa stearat diuji gugus fungsi dengan spektroskopi FT-IR dan morfologi permukaan menggunakan SEM.
Terbentuknya selulosa stearat didukung oleh spektrum FT-IR pada bilangan gelombang 3448,72 cm-1 menunjukkan gugus O-H, 2916,37 cm-1 menunjukkan gugus C-H Streching, 1743,65 cm-1 menunjukkan gugus C=O, 1465,90 cm-1 menunjukkan gugus C-H bending, 1172,72 menunjukkan gugus C-O-C dan 725,23 cm-1 menunjukkan gugus (CH2)n>4. Hasil analisis morfologi permukaan menggunakan SEM menunjukkan bahwa permukaan selulosa stearat tampak homogen, lebih teratur dan memiliki rongga-rongga yang lebih rapat daripada selulosa sebelum dimodifikasi.
Kata kunci: Metil Stearat, Selulosa, Selulosa Stearat, Transesterifikasi
SYNTHESIS ESTER CELLULOSA STEARATE FROM RICE STRAW CELLULOSA (Oriza Sativa L) WITH METHYL STEARATE THROUGH
THE TRANSESTERIFICATION REACTION
ABSTRACT
Stearate cellulose is synthesized by a transesterification reaction between α- cellulose that has been created via an isolation of rice straw (Oriza Sativa L) and methyl stearate. Where the synthesis of methyl stearic is done by reacting methanol and stearic acid with the help of a catalyst H2SO4(p). The forming of methyl stearate is supported by FT-IR data spectrum with the vibrational peak of the wave number 2917.14 cm-1 showing the C-H stretching , 1739.35 cm-1 showing the C = O, 1173.09 cm-1 showing the C-O-C. Synthesis of stearate cellulose was carried out by reflux for 4 hours using a methanol solvent with a catalyst variation of 10, 15, 20, 25, and 30 mg and the best variations is determined according to the degree of substitution test with a 30 mg catalyst variation of 1.299. The results of the synthesis of stearate cellulose that is tested by functional groups with FT-IR spectroscopy and surface morphology using SEM. The formation of the stearate cellulose is supported by FT-IR spectrum at the number of vibrational peaks in the region of wave number 3448.72 cm-1 shows the O-H group, 2916,37 cm-1 shows the C-H group, 1743.65 cm-1 shows the C = O group , 1465.90 cm-1 shows C-H bending group, 1172.72 shows the C-O-C group. The results of surface morphological analysis using SEM showed that the surface of stearate cellulose looks homogeneous, more organized and had larger pores than cellulose before it was modified.
Keywords: Celulosa, Metil Stearate, Stearate Celulosa Transesterifikasi,
PENGHARGAAN
Puji dan syukur penulis panjatkan kepada Tuhan Yang Maha Esa, atas segala kasih karunia dan berkatNya sehingga penulis dapat menyelesaikan penyusunan skripsi ini dengan judul “Sintesis Ester Selulosa Stearat dari Selulosa Jerami Padi (Oriza Sativa L) dengan Metil Stearat Melalui Reaksi Transesterifikasi”.
Terimakasih penulis sampaikan kepada Bapak Dr. Adil Ginting, M.Sc selaku dosen pembimbing yang telah meluangkan waktunya serta tulus dan sabar dalam membimbing dan memberikan arahan dan saran sehingga skripsi ini dapat terselesaikan. Terimakasih penulis sampaikan kepada Ibu Dr. Cut Fatimah Zuhra, M.Si selaku ketua program studi Kimia FMIPA USU Medan dan Ibu Dr.Sovia Lenny, S.Si, M.Si selaku sekretaris program studi kimia dan Koordinator Kimia Ekstensi Bapak Firman Sebayang, MS FMIPA USU, Medan, Dekan dan Wakil Dekan FMIPA USU, seluruh staff dan dosen program studi Kimia FMIPA USU, dan pegawai.
Secara khusus penulis mengucapkan terimakasih kepada orang tua terkasih Drs. B. Lumbantoruan dan M. Tampubolon, Amd dan juga kepada oppung Br Marbun, tante terkhusus tante Erda Tampubolon serta adik-adik penulis (Mawar, Eni, Markus) dan seluruh keluarga yang telah banyak memberikan dukungan doa, moril, materil, dan kasih sayang yang tak terhingga, penulis juga mengucapkan terimakasih kepada abang penulis Zulfanri Lumbantoruan yang turut membimbing, mengajari, dan memberi dukungan sehingga akhirnya penulis dapat menyelesaikan pendidikan.
Penulis juga mengucapkan terimakasih kepada sahabat-sahabat (Betria Hutapea, Adi Siagian, Ricky Butar Butar, kak Sry Sihotang, Bona Silitonga) teman TIS (kak Hillary, Debora, Made) serta NHKBP P.Bulan, dan seluruh Asisten Laboratorium Kimia Organik yang telah memberikan bantuan, semangat dan motivasi kepada penulis.
Akhir kata penulis berharap semoga skripsi ini dapat bermanfaat bagi penelitian dan kemajuan ilmu pengetahuan.
Medan, November 2019
Eka Margaretha Lumbantoruan
DAFTAR ISI
Halaman
PENGESAHAN SKRIPSI i
ABSTRAK ii
ABSTRACT iii
PENGHARGAAN iv
DAFTAR ISI v
DAFTAR TABEL viii
DAFTAR GAMBAR ix DAFTAR LAMPIRAN x DAFTAR SINGKATAN xi BAB 1 PENDAHULUAN 1.1 Latar Belakang 1 1.2 Permasalahan 3 1.3 Tujuan Penelitian 3 1.4 Pembatasan Masalah 3 1.5 Manfaat Penelitian 3 1.6 Lokasi Penelitian 3
1.7 Metodologi Penelitian 4
BAB 2 TINJAUAN PUSTAKA 2.1 Padi (Oryza sativa L) 5 2.2 Selulosa 8 2.3 Turunan Selulosa 11
2.4 Asam Lemak 17
2.5 Asam Stearat 18
2.6 Transesterifikasi 20
BAB 3 METODE PENELITIAN 3.1 Tempat dan Waktu 23
3.2 Alat dan Bahan 23
3.2.1 Alat 23
3.2.2 Bahan 24
3.3 Prosedur Penelitian 25
3.3.1 Pembuatan HNO 3,5 % 25
3.3.2 Pembuatan NaOH 2 % 25
3.3.3 Pembuatan NaOH 17,5 % 25
3.3.4 Pembuatan NaOCl 1,75 % 25
3.3.5 Pembuatan H2O2 10 % 25
3.3.6 Preparasi sampel 25
3.3.7 Isolasi Selulosa dari Jerami Padi 25
3.3.8 Pembuatan Metil Ester Stearat 26
3.3.9 Sintesis Ester Selulosa Stearat 26
3.3.10 Penentuan Derajat Substitusi (DS) 27
3.4 Bagan Penelitian 28
3.4.1Preparasi Sampel 28
3.4.2 Isolasi α-Selulosa dari Jerami Padi 29
3.4.3 Pembuatan Metil Ester Stearat 30
3.4.4 Sintesis Selulosa Stearat 31
BAB 4 HASIL DAN PEMBAHASAN 4.1 Isolasi α-Selulosa dari Jerami Padi (Oriza Sativa L) 32
4.2 Analisa Pembuatan Metil Ester Stearat 34
4.3 Analisa Sintesis Selulosa Stearat 35
4.4 Penentuan Derajat Substitusi 37
4.5 Analisa Morfologi Permukaan dengan SEM (Scanning Electron Microscopic) 38
BAB 5 KESIMPULAN DAN SARAN 5.1 Kesimpulan 40
5.2 Saran 40
DAFTAR PUSTAKA 41
LAMPIRAN 45
DAFTAR TABEL
Nomor Judul Halaman Tabel
2.1 Kandungan Pada Jerami Padi (Oriza Sativa L) 7 2.2 Asam Lemak Yang Umum Sebagai Ester Dalam
Tumbuhan atau Hewan. 18
4.4 Hasil Penentuan Derajat Substitusi Selulosa Stearat 37
DAFTAR GAMBAR
Nomor Judul Halaman
Gambar
2.1 Foto Tanaman Padi 5
2.2 Foto Jerami Padi 6
2.3 Struktur Selulosa 9
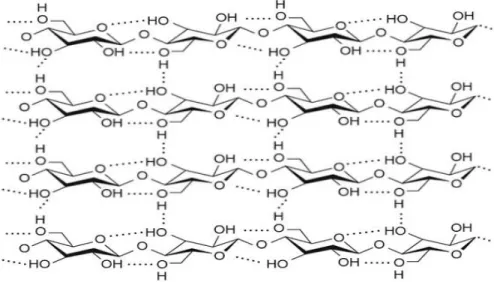
2.4 Ikatan Hidrogen Intramolekul dan Intermolekul Pada Selulosa 9
2.5 Reaksi Pembentukan Selulosa Format 12
2.6 Struktur Selulosa Sulfat 13
2.7 Struktur Selulosa Nitrat 14
2.8 Reaksi Pembentukan Selulosa Karbamat 14 2.9 Reaksi Pembentukan Selulosa Xantogenat 15
2.10 Struktur Asam Stearat 15
2.11 Reaksi Pembentukan Alkoholisis 21
2.12 Reaksi Pembentukan Asidolisis 21
2.13 Reaksi Pembentukan Metil Ester 22
4.1 Spektrum FT-IR α-Selulosa 35
4.2 Reaksi Pembentukan Metil Stearat 34
4.3 Spektrum FT-IR Metil Stearat 34
4.4 Mekanisme Reaksi Selulosa Stearat 35
4.5 Spektrum FT-IR Selulosa Stearat 36
4.6 Perbandingan Spektrum FT-IR Selulosa dan Selulosa Stearat 36 4.7 Hasil Morfologi Permukaan dengan SEM Selulosa 38 4.8 Hasil Morfologi Permukaan dengan SEM Selulosa Stearat 39
DAFTAR LAMPIRAN
Nomor Judul Halaman
Lampiran
1 Perhitungan Pembuatan Pereaksi 46
2 Perhitungan Derajat Substitusi 47
3 Foto Proses Pembuatan α-Selulosa 48
4 Foto Hasil Selulosa Stearat 49
5 Hasil Morfologi Permukaan SEM α-Selulosa
dan Selulosa Stearat 50
DAFTAR SINGKATAN
DS = Derajat Substitusi
FT-IR = Fourier Transform-Infra Red
SEM = Scanning Electron Microscopic
BAB 1 PENDAHULUAN
1.1 Latar Belakang
Jerami merupakan limbah pertanian terbesar serta belum sepenuhnya dimanfaatkan karena adanya faktor teknis dan ekonomis. Pada sebagian petani, jerami sering digunakan sebagai mulsa pada saat menanam palawija. Hanya sebagian kecil petani menggunakan jerami padi sebagai pakan ternak alternatif di kala musim kering karena sulitnya mendapatkan hijauan. Di lain pihak jerami padi sebagai limbah pertanian, sering menjadi permasalahan bagi petani, sehingga sering di bakar untuk mengatasi masalah tersebut. Menurut Badan Pusat Statistik, produksi padi nasional mencapai 71,29 juta ton pertahun pada tahun 2011. Sedangkan produksi jerami padi dapat mencapai 12 - 15 ton per hektar per panen, bervariasi tergantung pada lokasi dan jenis varietas tanaman padi yang digunakan (Berita Resmi Statistik, 2013). Jerami padi merupakan biomassa yang secara kimia dan merupakan senyawa berlignoselulosa. Komponen terbesar penyusun jerami padi adalah selulosa (35- 50%), hemiselulosa (20-35%) dan lignin (10-25%) dan zat lain penyusun jerami padi (Saha, 2004).
Selulosa merupakan bahan organik yang paling banyak terdapat dialam karena merupakan komponen utama dinding sel tanaman tingkat tinggi. Selulosa tidak hanya merupakan polisakarida struktural ekstra selular yang paling banyak dijumpai pada dunia tumbuhan, tetapi juga merupakan senyawa yang paling banyak diantara semua biomolekul pada tumbuhan atau hewan. Karena selulosa merupakan homopolisakarida liniar tidak bercabang, terdiri 10.000 atau lebih unit D-glukosa (Lehninger, 1998). Selulosa tersusun atas gugus β-D-glukopiranosil yang berikatan melalui ikatan glikosidik β 1,4 (Estiati, dkk.2015). Selulosa yang diberi nama pada awal abad ke-19 oleh seorang ilmuwan perancis, Anselme Payen adalah biopolimer terbarukan yang paling melimpah di bumi (Chen, 2014). Selulosa mempunyai rumus empirik (C6H10O5)n (Rowe, dkk.,2009). Molekul selulosa berbentuk linier dan kuat untuk membentuk ikatan hidrogen intramolekul dan intermolekul. Ketersediaan selulosa dalam jumlah besar akan membentuk serat yang kuat, tidak larut dalam air, tidak larut dalam pelarut organik, dan berwarna putih (Fengel dan Wagener, 1995).
Studi mengenai serat selulosa tumbuhan untuk berbagai aplikasi secara luas telah dilakukan karena sifatnya yang berkelanjutan, alami dan ramah lingkungan.
Proses yang mudah, biaya murah, konsumsi energi rendah, bobot yang ringan, kekuatan spesifik yang baik, tidak berbahaya bagi lingkungan serta dapat diperbaharui dan di daur ulang menghasilkan minat yang besar dikalangan peneliti dibanding dengan serat sintesis konvensional (Saurabh et al, 2016).
Untuk meningkatkan nilai gunanya, para peneliti menggunakan sifat dasar kimia selulosa yang memiliki permukaan reaktif dari gugus hidroksil sebagai cara untuk modifikasi kimia agar mencapai sifat permukaan yang berbeda (Yakubu et al, 2011).
Asam lemak adalah asam karboksilat yang gugus alkilnya adalah rantai hidrokarbon, yang mempunyai atom C panjang dan tidak bercabang (Fessenden,1999). Asam lemak rantai panjang dapat diperoleh dari minyak nabati, salah satunya asam stearat. Asam stearat sering disebut octadecanoic acid C18H36O2 dengan komposisinya C 75.99%, H 12.76%, O 11.25%. Asam stearat diperoleh dengan memperlakukan lemak hewan dengan air pada tekanan tinggi dan suhu, mengarah pada hidrolisis dari trigliserida. Hal ini juga dapat diperoleh dari hidrogenasi beberapa tak jenuh minyak nabati ( Anonim,1976).
Ada beberapa modifikasi selulosa yaitu seperti eterifiksasi (Hong, 2013), asetilasi (Cetin et al, 2009), esterifikasi (Spinella et al, 2015) dan transesterifikasi.
Transesterifikasi adalah reaksi pembentukan ester dari suatu senyawa ester lain melalui pertukaran gugus alkil dari ester yang bereaksi dengan suatu alkohol. Reaksi transesterifikasi dapat dikatalisis oleh asam maupun basa (Asthasari, 2008). Reaksi ini berjalan sangat lambat sehingga diperlukan katalis untuk mempercepat reaksi agar dapat digunakan secara komersial. Penggunaan katalis hanya mempercepat terjadinya kesetimbangan tetapi tidak dapat menggeser posisi kesetimbangan .
Iswiyarto, dkk (2009) melakukan penelitian pengaruh temperatur pada sintesis ester asam lemak selulosa (FACE) menggunakan katalis Na2CO3. Dalam penelitian ini dijelaskan bahwa katalis Na2CO3 digunakan untuk menghasilkan polimer ester asam lemak selulosa (FACE) yang dengan nilai derajat transesterifikasi
yang tinggi, karena semakin banyak gugus hidroksi dari selulosa yang tersubtitusi dari gugus ester dari Metil ester asam lemak (FAME).
Berdasarkan uraian diatas, peneliti tertarik untuk meneliti lebih lanjut tentang selulosa dari jerami padi yang berpotensi untuk dimodifikasi melalui reaksi transesterifikasi dengan metil ester stearat, sehingga selulosa memiliki sifat yang lebih baik.
1.2 Permasalahan
1. Bagaimana mensintesis selulosa stearat dari selulosa jerami padi dengan metil stearat melalui reaksi transesterifikasi sehingga menghasilkan selulosa stearat?
2. Bagaimana karakteristik ester selulosa stearat?
1.3 Tujuan Penelitian
1. Untuk mensintesis selulosa stearat dari selulosa jerami padi dengan metil stearat melalui reaksi transesterifikasi sehingga menghasilkan selulosa stearat?
2. Untuk menentukan karakteristik ester selulosa stearat.
1.4 Pembatasan Masalah
1. Selulosa yang digunakan adalah selulosa hasil isolasi dari jerami padi.
2. Sintesis selulosa stearat dengan mereaksikan selulosa dari jerami padi dengan metil stearat dengan variasi katalis 10 mg sampai 30 mg.
1.5 Manfaat Penelitian
Penelitian ini diharapkan dapat memberikan informasi mengenai bagaimana cara mensintesis ester selulosa stearat dari bahan baku selulosa jerami padi dengan metil stearat serta memberikan informasi mengenai bagaimana karakteristik sifat ester selulosa stearat yang diteliti.
1.6 Lokasi Penelitian
Penelitian ini dilakukan di laboratorium Kimia Organik FMIPA USU.
Analisis secara Spektrofometer FT-IR (Fourier Transform-Infra Red) di Laboratorium Kimia Organik FMIPA UGM dan Laboratorium Kimia Organik FMIPA UNP dan analisis Morfologi Permukaan dengan SEM (Scanning Electron Miscroscopic) dilakukan dilaboratorium Puslabfor Bareskrim Polri.
1.7 Metodologi Percobaan
Penelitian ini dilakukan melalui eksperimen di laboratorium, dimana α - selulosa yang dihasilkan diperoleh dari hasil isolasi jerami padi (Oriza Sativa L) kemudian dianalisa dengan spektroskopi FT-IR. Metil stearat yang diperoleh yaitu dari hasil esterifikasi asam stearat dan metanol dengan katalis asam yaitu H2SO4(p) kemudian dianalisa dengan spektroskopi FT-IR. Selanjutnya sintesis selulosa stearat dilakukan dengan mereaksikan selulosa dengan metil stearat dengan variasi katalis Na2CO3 yaitu dari 10 mg, 15mg, 20 mg, 25 mg, dan 30 mg.
Kemudian selulosa stearat yang diperoleh di uji dengan derajat substitusi dimana derajat substitusi tertinggi dikarakterisasi dengan spektroskopi FT-IR dan uji morfologi permukaan (SEM).
BAB 2
TINJAUAN PUSTAKA
2.1 Padi (Oryza sativa L)
Padi (Oryza sativa L) merupakan tanaman penghasil beras yang menjadi sumber karbohidrat utama bagi masyarakat Indonesia (Petriella, 2016). Meskipun sebagai bahan makanan pokok padi dapat digantikan/disubstitusi oleh makanan lainnya, namun padi memiliki nilai tersendiri bagi orang yang biasa makan nasi dan tidak dapat dengan mudah digantikan oleh bahan makanan lainnya (Aak, 1990).
Padi merupakan tumbuhan monocotyl yang tumbuh di daerah tropis.
Produksi padi dunia menempati urutan ketiga dari semua serelia setelah jagung dan gandum. Namun, padi merupakan sumber karbohidrat utama bagi mayoritaspenduduk dunia. Di Indonesia, pada tahun 2008, produksi padi menembus angka 60 juta ton.
Klasifikasi tanaman padi menurut Utama (2015):
Divisi : Spermathophyta Kelas : Monokotiledon Ordo : Poales
Famili : Poaceae Genus : Oryza
Spesies : Oryza sativa L.
Gambar 2.1 Foto tanaman padi
Padi adalah salah satu bahan makanan yang mengandung gizi dan penguat yang cukup bagi tubuh manusia, sebab di dalamnya terkandung bahan-bahan yang mudah diubah menjadi energi. Oleh karena itu, padi disebut juga makanan energi (Aak, 1990).
Tanaman padi tersusun atas akar, batang, daun, dan bunga. Tipe perakaran tanaman padi yaitu serabutyang terdiri atas akar seminal dan akar adventif. Akar serabut terletak pada kedalaman tanah 20-30 cm. Akar-akar serabut muncul dari batang, akar berkembang pesat saatbatang mulai membentuk anakan. Bentuk batang tanaman padi bulat dan berongga (jerami). Pada batang utama membentuk rumpun (Nurmala, 1998).
Gambar 2.2. Foto Jerami Padi
Jerami padi merupakan limbah hasil samping dari pertanian padi.
Pemanfaatan jerami padi selama ini hanya sebatas untuk pakan ternak, dibakar untuk dijadikan kompos, serta digunakan sebagai media pengembangan jamur merang.
Jerami padi adalah bagian batang tumbuh yang telah dipanen bulir-bulir buah bersama atau tidak dengan tangkainya dikurangi dengan akar dan bagian batang yang tertinggal. Jerami adalah hasil samping usaha pertanian berupa tangkai dan batang tanaman serealia yang telah kering, setelah biji-bijiannya dipisahkan. Massa jerami kurang lebih setara dengan massa biji-bijian yang dipanen. Jerami memiliki banyak fungsi, di antaranya sebagai bahan bakar, pakan ternak, alas atau lantai kandang,
pengemas bahan pertanian (misal telur), bahan bangunan (atap, dinding, lantai), mulsa, dan kerajinan tangan. Jerami umumnya dikumpulkan dalam bentuk gulungan, diikat, maupun ditekan (Komar, 1984).
Jerami padi merupakan bagian dari batang padi tanpa akar yang tertinggal setelah diambil butir buahnya. Peningkatan produksi padi juga diiringi peningkatan limbah jerami padi. Banyaknya jerami padi yang belum dimanfaatkan secara optimal mendorong ara peneliti mengembankan potensi jerami apdi menjadi sesuatu yang mempunyai nilai ekonomi tinggi.
Berikut beberapa kandungan pada jerami padi (Oriza Sativa L) pada tabel 2.1, sebagai berikut :
Kandungan Jerami Padi Berat (%)
Serat Kasar 32,56
Protein Kasar 3,2
Lemak 1,33
NDF 64,34
ADF 46,40
Selulosa 40,80
Hemiselulosa 26,62
Lignin 5,78
Sumber : Fatmawati, (2005)
Kandungan selulosa yang cukup besar, mengakibatkan proses perombakan bahan organik secara alami membutuhkan waktu relatif lambat (Djuarnani, 2004).
Selain kandungan nutrisi yang sangat rendah, jerami padi juga termasukpakan hijauan yang sulit dicerna. Selain karena kandungan serat kasarnya tinggi sekali.
Daya serat yang rendah itu terutama disebabkan oleh struktur jaringan jerami yang sudah tua. Jaringan-jaringan pada jerami telah mengalami proseslignifikasi (pengerasan) sehingga terbentuk lignoselulosa dan lignohemiselulosa (Santoz, E, 2013).
2.2 Selulosa
Selulosa merupakan salah satu senyawa organik yang paling melimpah di alam tetapi proses dekomposisinya lama. Selulosa bersifat dapat diperbaharui, mudah terurai, tidak beracun dan juga merupakan polimer karbohidrat yang tersusun atas ß- D glukopiranosa dan terdiri dari tiga gugus hidroksi per anhidro glukosa menjadikan selulosa memiliki derajat fungsionalitas yang tinggi (Coffey et al, 1995). Selulosa mempunyai rumus empirik (C6H10O5)n dengan n hingga 1500 dan berat molekul hingga 243.000 (Rowe, dkk. 2009).
Selulosa merupakan komponen utama penyusun dinding sel tanaman.
Kandungan selulosa pada dinding sel tanaman tingkat tinggi sekitar 35-50% dari berat kering tanaman (Lynd et al,2002). Bangun dasar selulosa berupa suatu selobiosa yaitu dimer dari glukosa. Rantai panjang selulosa terhubung secara bersama melalui ikatan hidrogen dan gaya van der Waals (Perez et al, 2002).
Selulosa merupakan bahan berberat molekul tinggi, rantai linier, homopolimer dan bersifat tidak larut dalam air, Selulosa tidak mudah didegradasi secara kimia maupun mekanis. Dialam, biasanya selulosa berasosiasi dengan polisakarida lain seperti hemiselulosa atau lignin yang membentuk kerangka utama dinding sel tumbuhan (Holtzapple et al, 1993). Adanya lignin serta hemiselulosa disekeliling selulosa merupakan hambatan utama untuk menghidrolisis selulosa (Sjostrom, 1995).
Unit penyusun selulosa adalah selobiosa karena unit keterulangan dalam molekul selulosa adalah 2 unit gula (D-glukosa). Selulosa adalah senyawa yang tidak larut di dalam air dan ditemukan pada dinding sel tumbuhan terutama pada tangkai, batang, dahan, dan semua bagian berkayu dari jaringan tumbuhan. Selulosa merupakan polisakarida structural yang berfungsi untuk memberikan perlindungan, bentuk, dan penyangga terhadap sel, dan jaringan (Lehninger, 1988).
Selulosa cenderung membentuk mikrofibril melalui ikatan inter dan intra molekuler. Mikrofibril selulosa terdiri dari dua tipe yaitu kristalin dan amorf (Anindyawati, 2010). Mikrofibril membentuk fibril – fibril dan akhirnya serat-serat selulosa. Sebagai akibat dari struktur yang berserat dan ikatan hidrogen yang kuat,
selulosa mempunyai kekuatan tarik yang tinggi dan tidak larut dalam kebanyakan pelarut (Atalla, 1987). Selulosa adalah polisakarida yang paling melimpah di alam.
Senyawa ini memiliki bobot molekul yang tinggi, strukturnya teratur berupa polimer linier dengan unit ulangan β-D-glukopiranosa, karena keteraturan strukturnya selulosa adalah polimer yang nisbi, murah dengan sifat fisik dan kimia yang istimewa (Suminar, 1990).
Reaktivitas dalam selulosa bergantung pada strukturnya. Untuk memodifikasi struktur selulosa, ikatan hidrogen harus dihancurkan dengan cara pembengkakan atau pemutusan. Bagian yang reaktif pada selulosa dapat diderivatisasi adalah ketiga gugus hidroksil, yaitu pada C-2, C-3, dan C-6. Gugus hidroksil pada C-6 adalah hidroksil primer, yang mempunyai posisi yang paling reaktif untuk reaksi esterifikasi, sementara C-2 adalah lebih asam dibandingkan kedua gugus hidroksil sekunder dan merupakan sisi yang lebuh reaktif untuk esterifikasi. Selulosa memiliki afinitas yang kuat terhadap dirinya sendiri dan bahan yang mengandung hidroksil.
Berdasarkan pada gugus fungsi hidroksil yang dominan, maka selulosa bersifat reaktif dengan air. Selulosa sangat stabil dalam berbagai pelarut dan hanya dapat dihansurkan dengan adanya asam kuat atau system pelarut dengan ikatan hydrogen yang kuat, biasanya basa amina. Sifat termal selulosa yaitu temperatur transisi gelas selulosa dengan kisaran 200-2300C (Goring, 1963).
Berikut adalah struktur dari selulosa dapat dilihat pada gambar 2.3.
Gambar 2.3. Struktur Selulosa
Selulosa bukan merupakan jenis karbohidrat pereduksi, jika di hidrolisis dalam suasana asam akan menghasilkan banyak molekul D-glukosa. Didalam molekul selulosa, monomer-monomernya tersusun secara linier, sedangkan diantara pita-pita satuan polimernya tersusun secara parallel. Oleh karena itu di antara pita- pita satuan polimernya tersebut terdapat banyak jembatan hidrogen intermolekul dan intramolekuler yang menyebabkan selulosa mempunyai struktur yang massif/kompak dan merupakan struktur dasar sel-sel tumbuhan (Riswiyanto, 2009).
Gambar 2.4 Ikatan Hidrogen Intramolekul dan Intermolekul pada Selulosa Material selulosa memiliki derajat polimerisasi (DP) yang berbeda-beda tergantung dari sumber dan perlakuannya. Selulosa serbuk (yang didapatkan dari selulosa pulp melalui penggilingan dan fraksinasi) memiliki DP 100-300. Selulosa dari dinding sekunder kapas memiliki DP 20.000 dan selulosa terregenerasi memiliki DP 200-500 (Wertz, 2010).
Berdasarkan derajat polimerisasi dan kelarutan dalam senyawa natrium hidroksida (NaOH) 17,5% selulosa dapat dibedakan menjadi 3 jenis yaitu :
1. Alfa selulosa (α-selulosa) adalah selulosa berantai panjang, tidak larut dalam NaOH 17,5% atau larutan basa kuat dengan derajat polimerisasi 600-1500. Alfa selulosa (α-selulosa) digunakan sebagai penduga atau penentu tingkat kemurnian selulosa. α-selulosa merupakan kualitas selulosa yang paling tinggi (murni). Dengan derajat kemurnian α diatas 92% memenuhi syarat untuk bahan baku pada industri
kertas dan sandang/kain. Semakin tinggi kadar alfa selulosa, maka semakin baik mutu bahannya (Nuringtyas, 2010).
2. Beta Selulosa (β-Selulosa) adalah selulosa berantai pendek, larut dalam NaOH 17,5% atau basa kuat dengan derajat polimerisasi 15-90, dan dapat mengendap bila dinetralkan (Nuringtyas, 2010).
3. Gamma selulosa (γ-Selulosa) adalah selulosa berantai pendek yang larut dalam NaOH 17,5% atau basa kuat dengan derajat polimerisasinya kurang dari 15.
Selulosa merupakan polimer rantai lurus. Tidak seperti pati, selulosa tidak mengalami pemelintiran atau percabangan dan molekul selulosa membentuk konformasi batang panjang, yang dibantu oleh konformasi ekuatorial dari residu glukosa. Gugus hidroksi yang terdapat pada unit glukosa dari satu rantai mengalami ikatan hidrogen dengan molekul oksigen dari rantai yang sama atau rantai tetangga, yang menahan rantai-rantai secara kuat bersisian dan membentuk mikrofibril dengan daya kuat tarik yang tinggi (Kalia, 2011).
2.3 Turunan Selulosa
Selulosa telah menjadi material yang banyak digunakan dalam berbagai aplikasi. Salah satunya dalam industri kertas, di mana selulosa diolah secara konvensional. Walaupun kertas menjadi produk utama dari selulosa, tidak berarti membatasi penggunaan selulosa untuk kegunaan lain. Selulosa dapat dimodifikasi secara kimia untuk menciptakan turunan yang lebih luas dimana dapat digunakan dalam sektor industri. Turunan ini dapat dijadikan sebagai agen coating, laminating, film optis, juga sebagai adsorben. Turunan selulosa juga dapat dijumpai sebagai bahan aditif dari bahan bangunan, farmasi, makanan serta produk-produk kosmetik (Ganstrom, 2009).
Turunan selulosa terbagi dua berdasarkan reaksi pembentukannya, sebagai berikut :
1. Esterifikasi Selulosa
Modifikasi ester selulosa dengan asam organik dan asam anorganik membentuk turunan selulosa bersifat kovalen pertama kali disintesis dalam laboratorium.
Selulosa nitrat, selulosa asetat dan selulosa xantogenat telah diproduksi dalam skala industri pada pertengahan abad yang lalu dan saat ini telah mencakup lebih dari 90%
total produksi selulosa. Menurut Sjostrom (1995), esterifikasi selulosa dibagi 2 yaitu : ester asam organik dan ester asam anorganik. Ester asam organik adalah selulosa format dan selulosa asetat sedangkan ester asam anorganik mencakup selulosa sulfat, selulosa nitrat, selulosa xantogenat, selulosa karbamat.
a. Selulosa Format
Selulosa format memiliki sifat yang tidak stabil dengan Derajat Subtitusi 2,0- 2,5. Jika dipanaskan didalam air pada suhu 1100C dapat terjadi dekomposisi antara selulosa dan asam format.
Gambar 2.5 Reaksi Pembentukan Selulosa Format
b. Selulosa Sulfat
Selulosa sulfat dapat dibentuk melalui beberapa tahap berikut :
1. Sulfonasi gugus hidroksi biasanya dimulai dalam sebuah sistem heterogen.
2. Sulfonasi gugus hidroksi yang bebas sebagian membentuk ester selulosa atau eter selulosa dimana substituent primer bertindak sebagai gugus pelindung.
3. Sulfonasi oleh pertukaran tempat gugusester atau eter dengan makromolekul.
Sebagian besar asam sulfat, asam sulfit, atau asam klorosulfonat dapat digunakan sebagai agen sulfonasi, yang juga dapat dikombinasikan dengan pelarut inert seperti alcohol. Secara umum reaksi pembentukan selulosa sulfat dapat ditunjukkan oleh reaksi berikut :
Gambar 2.6 Struktur Selulosa Sulfat c. Selulosa Nitrat
Menurut derajat nitrasi, selulosa nitrat (Rsel– O _NO2) larut dalam alkohol, ester atau keton jernih. Larutan-larutan ini digunakan untuk menentukan viskositas dan distribusi derajat polimerisasi. Selulosa nitrat biasanya dipakai untuk memproduksi kapas sintesis, larutan nitro, bahan peledak, dan sebagai bahan pelembut untuk pembuatan bahan-bahan sintesis (Muladi, 2013).
Selulosa nitrat merupakan turunan selulosa pertama yang diproduksi dalam skala industry untuk pembuatan kain sutera sintetik. Ini bias dibentuk melalui reaksi antara polimer dengan HNO3 berdasarkan reaksi :
Produksi selulosa nitrat masih didasarkan pada reaksi kesetimbangan heterogen antara selulosa dan system nitrasi yang disebutkan diatas.
Gambar 2.7. Struktur Selulosa Nitrat
d. Selulosa Karbamat
Pada reaksi ini digunakan katalis berupa garam metal, biasanya digunakan zink sulfat, pada suhu sekitar 1400. Selulosa karbamat dengan derajat subtitusi 0,2 – 0,3 dapat larut dalam larutan NaOH.
e. Selulosa Xantogenat
Selulosa Xantogenat larut dalam air karena bersifat polielektrolit. Selulosa Xantogenat dan garamnya tidak memiliki penggunaan secara teknis, tetapi bahan dasar untuk memproduksi sutera buatan (untuk tekstil) dan rayon (serta ban) (Muladi, 2013). Reaksi pembentukan Selulosa Xantogenat sebagai berikut :
Gambar 2.9. Reaksi Pembentukan Selulosa Xantogenat
f. Selulosa Asetat
Selulosa Asetat merupakan salah satu ester selulosa yang penting, selulosa dapat diasetilasi dengan asetat anhidrida dengan adanya asam sulfat glacial sebagai katalisator menghasilkan diasetat dan triasetat.
Oligosakarida yang terasetilasi terbentuk didalam degradasi asetilitik selulosa. Hal ini dapat dipisahkan dengan kromatografi kedalam asetat selubiosa, selotriosa, selotetraosa, selopentaosa, dan seloheksaosa dan diidentifikasi sebagai bentuk-bentuk Kristal.
2. Eterifikasi Selulosa
Eterifikasi selulosa merupakan turunan selulosa komersial yang sangat penting dan menjadi proses yang banyak diteliti dibandingkan dengan ester selulosa.
Eter selulosa dapat dibuat dengan mereaksikan selulosa alkali dengan jumlah pereaksi yang meliputi alkil halida atau aril halida, alkena oksida dan senyawa- senyawa tidak jenuh yang diaktifkan oleh gugus-gugus penarik elektron (Sjostrom, 1995).
Karbosimetil selulosa (CMC) adalah salah satu contoh dari eterifikasi selulosa. Karbosimetil selulosa merupakan senyawa turunan selulosa yang paling penting, yang memiliki kepentingan sangat besar diindustri dan kehidupan kita sehari hari. Salah satu fungsi dari karbosimetil selulosa adalah sebagai pengental, stabilisator, sebagai pengemulsi, pembentuk gel, dan beberapa hal yang dapat meratakan penyebaran antibiotik (Winarno, 1984). Senyawa CMC memiliki tekstur yang linier, berantai panjang, tidak larut dalam air, dan polisakarida anionik yang diturunkan dari selulosa (Hong, 2013).
Senyawa eter dan ester selulosa secara komersial diproduksi dalam kondisi reaksi heterogen menggunakan asam dan asam anhidrat sebagai reagent. Dengan kata lain, jalur utama dari sintesis eter adalah sintesis eter Williamson. Kelemahan dari reaksi heterogen ialah laju reaksi yang relative lambat dan tidak adanya sifat regioselektif dari suatu reaksi, sehingga aksesibilitas dari gugus hidroksil bebas dari selulosa menjadi factor penentu terhadap selektivitas dan juga terhadap derajat substitusi. Lebih jelasnya, ketika reaksi berlangsung dalam larutan homogen, maka sifat regioselektivitas dari reaksi ditentukan oleh perbedaan kereaktifan gugus
hidroksil bebeas yang dimiliki molekul selulosa, bukan dari sisi aksesibilitasnya.
Sebagai tambahan terhadap kemampuan mengontrol selektivitas dalam reaksi, nilai substitusi dapat disesuaikn mulai dari turunan senyawa dengan derajat substitusi rendah hingga turunan senyawa dengan derajat substittusi yang lebih tinggi. Oleh sebab itu, material yang dihasilkan dari turunan selulosa dapat disesuaikan sesuai alur yang kita kehendaki (Klemm, 1998).
Selulosa tidak dapat digunakan sebagai bahan makanan oleh tubuh, namun selulosa yang terdapat sebagai serat-serat tumbuhan, sayuran atau buah-buahan, berguna untuk memperlancar pencernaan makanan. Adanya serat-serat dalam saluran pencernaan, gerak peristaltik ditingkatkan dan dengan demikian memperlancar proses pencernaan dan dapat mencengah konstipasi. Tentu saja jumlah serat yang terdapat dalam bahan makanan tidak boleh terlalu banyak (Poedjiadi, 2006).
Ester Selulosa banyak digunakan sebagai serat dan plastik, sedangkan eter selulosa sebagai pengikat dan bahan tambahan untuk mortir khusus atau kimia khusus untuk bangunan dan konstruksi stabilisator viskositas pada cat, makanan, produk farmasetik dan lain-lain. Selulosa juga merupakan bahan dasar pembuatan kertas. Seratnya mempunyai durabilitas yang tinggi ( Zugenmaier, 2008). Turunan selulosa telah digunakan secara luas dalam farmasi seperti etil selulosa, metil selulosa, karboksimetil selulosa, dan dalam bentuk lainnya. Penggunaan bentuk- bentuk selulosa dalam sediaan disebabkan sifatnya yang inert dan biokompatibilitas yang sangat baik pada manusia (Jackson, dkk. 2011).
2.4 Asam Lemak
Asam lemak terdiri atas unsur-unsur seperti karbon, hidrogen dan oksigen yang tersusun sebagai rangka rantai karbon linier dengan beragam panjang rantai dan mempunyai sebuah gugus karboksil pada salah satu ujung rantainya. Asam-asam lemak dapat berupa saturated (tidak memiliki ikatan rangkap), monounsaturated (memiliki sebuah ikatan rangkap), atau polyunsaturated (memiliki dua atau lebih ikatan rangkap) (Chow, 2008).
Asam lemak berasal dari hewan maupun tumbuhan. Rantai karbon yang jenuh atau yang tidak jenuh dan terdiriatas 4 sampai 24 buah atom karbon. Rantai karbon jenuh merupakan rantai karbon yang tidak mengandung ikatan rangkap, sedangkan rantai karbon tidak jenuh merupakan rantai karbon yang mengandung ikatan rangkap. Pada umumnya asam lemak mempunyai jumlah atom karbon genap (Poejdiadi, 1994).
Asam lemak merupakan organik yang terdiri atas rantai hidrokarbon lurus yang pada satu ujungnya mempunyai gugus hidroksil (COOH) dan pada ujung lainnya memiliki gugus metil (CH3) (Almatsier, 2006). Asam lemak yang mempunyai berat molekul yang paling besar di dalam molekul gliserida juga merupakan bagian yang reaktif. Asam lemak yang menyusun lemak masih dibedakan antara asam lemak yang jenuh dan tak jenuh. Asam lemak jenuh yang banyak pemakaiannya antara lain adalah asam laurat (C12), asam miristat (C14), asam stearat (C18). Asam lemak jenuh tidak menunjukkan kenaikan yang teratur di dalam titik cairnya dengan kenaikan panjang rantainya (Sastrohamidjojo, 2009). Panjang rantai karbon mempengaruhi titik cair. Pada asam lemak jenuh, titik cair akan semakin meningkat dengan semakin panjangnya rantai karbon. Pada asam lemak tak jenuh, titik cairnya, akan semakin menurun dengan bertambahnya ikatan rangkap, sehingga asam lemak jenuh mempunyai titik cair yang lebih tinggi dibandingkan dengan asam lemak tak jenuh dengan jumlah atom karbon yang sama (Seager dan Slabough, 1994).
Berikut beberapa asam lemak yang umum sebagai ester dalam tumbuhan atau hewan dapat dilihat pada tabel 2.3.
Nama Rumus Asam Lemak Jenuh
Asam Butirat C3H7COOH Asam Laurat C11H23COOH Asam Palmitat C15H31COOH Asam Stearat C17H35COOH
Asam Lemak Tak Jenuh
Asam Oleat C17H33COOH Asam Linoleat C17H31COOH Asam Linolenat C17H29COOH Sumber : (Poedjiadi, 1994)
Asam lemak yang berantai pendek dapat larut dalam air, semakin panjang rantai asam-asam lemak maka kelarutannya didalam air semakin berkurang. Asam lemak ditentukan dengan panjang rantai karbon dimana semakin panjang rantai karbon, maka titik cair asam lemak semakin tinggi dan ditentukan juga dengan ketidakjenuhannya, dimana semakin tinggi derajat ketidakjenuhan asam lemak, maka titik cairnya semakin rendah, serta asam lemak yang berstruktur trans mempunyai titik cair yang lebih tinggi daripada yang berstruktur cis (Ketaren, 2005).
2.5 Asam Stearat
Asam stearat merupakan asam lemak jenuh karena tidak ada ikatan rangkap antara karbon bertetangga, ini berarti bahwa rantai hidrokarbon fleksibel dan dapat berputar menjadi siklis atau lurus dan menjadi rantai zig-zag yang panjang (Winarno, 1992).
Gambar 2.10. Struktur Asam Stearat
Asam stearat (nama sistematis, asam oktadekanoat, CH3(CH2)16COOH) merupakan asam lemak berantai panjang dengan 18 atom karbon tanpa adanya ikatan rangkap. Meskipun asam stearat diklasifikasikan sebagai asam lemak jenuh, baik dari segi biokimia maupun kegunaan nutrisi serta rekomendasi diet, data yang telah dikumpulkan selama 50 tahun terakhir menunjukkan bahwa asam stearat sangat unik diantara asam-asam lemak jenuh dalam makanan. Tidak seperti asam lemak jenuh rantai panjang lainnya (palmitat, miristat, dan laurat), yang mana dapat meningkatkan level kolesterol dalam darah, namun asam stearat menunjukkan efek netral pada total darah serta mempunyai level kolesterol LDL yang rendah (Beef Facts, 2007)
Asam stearat memiliki titik leleh 69.6ºC dan titik didih 240 ºC. Titik leleh dan titik didih asam stearat relatif lebih tinggi dibandingkan dengan asam lemak jenuh yang memiliki atom karbon lebih sedikit. Asam stearat memiliki berbagai kegunaan seperti sebagai komposisi tambahan dalam makanan, kosmetik, dan produk industri. Kegunaan lain asam stearat adalah mencegah oksidasi. Senyawa ini biasanya digunakan untuk melapisi serbuk logam seperti besi dan aluminium yang digunakan dalam kembang api, sehingga memungkinkannya disimpan dalam waktu lama (Swern , 1979).
Asam lemak ini merupakan asam lemak jenuh, wujudnya padat pada suhu ruang. Asam stearat diproses dengan memperlakukan lemak hewan dengan air pada suhu dan tekanan tinggi. Asam ini dapat pula diperoleh dari hidrogenasi minyak nabati. Dalam bidang industri asam stearat dipakai sebagai bahan pembuatan lilin, sabun, plastik, kosmetika, dan untuk melunakkan karet (Anonim , 2010).
2.6 Transesterifikasi
Reaksi transesterifikasi merupakan reaksi antara trigliserida yang banyak terdapat pada minyak nabati atau lemak hewani dengan alkohol untuk menghasilkan metil ester dan gliserol. Alkohol yang biasanya digunakan adalah metanol karena sifatnya yang mudah bereaksi dan harga yang terjangkau sehingga disebut juga reaksi metanolisis.
Reaksi transesterifikasi berperan dalam membentuk ester amilosa dan selulosa pada kondisi homogen. Reaksi transesterifikasi merupakan reaksi kesetimbangan yang biasanya dilakukan secara sederhana dengan mencampurkan reaktan-reaktan. Reaksi ini berjalan dengan lambat sehingga diperlukan katalis untuk mempercepat reaksi agar dapat digunakan secara komersial. Penggunaan katalis hanya mempercepat terjadinya kesetimbangan tetapi tidak dapat menggeser posisi kesetimbangan. Asam kuat dan basa kuat banyak digunakan sebagai katalis. Untuk meningkatkan konversi reaksi, perlu diperhatikan beberapa aspek seperti perubahan konsentrasi pereaksi maupun hasil reaksi, volume, tekanan dan temperatur. Reaksi transesterifikasi banyak dikenal secara komersial dalam reaksi organik industri.
Dalam reaksi ini, suatu ester dikonversi menjadi ester lain dengan mempertukarkan gugus asam atau gugus alkoholik. Apabila transesterifikasi mempertukarkan gugus alkoholik, maka disebut reaksi alkoholisis. Dalam alkoholisis, alcohol diberikan berlebih untuk memperoleh yield yang tinggi dari ester yang diinginkan. Akhir-akhir ini, produksi alkil ester, secara khusus metil ester, dari minyak tumbuhan (seperti minyak kelapa sawit, minyak jarak pagar) menjadi sangat popular dalam proses pembuatan biodiesel dari bahan baku terbarukan.
Transesterifikasi dibagi dalam tiga jenis reaksi yaitu :
1. Interesterifikasi yaitu pembentukan ester dari ester dengan ester
2. Alkoholisis yaitu reaksi suatu ester dengan alkohol untuk membentuk suatu ester baru, dimana reaksinya biasanya lambat namun dapat dipercepat dengan bantuan suatu katalis yang bias dipergunakan adalah suatu asam anorganik seperti HCl dan H2SO4.
Gambar 2.11. Reaksi Pembentukan Alkoholisis
3. Asidolisis yaitu reaksi pembentukan suatu ester antara ester dengan ester lain.
Disini terjadi pertukaran gugus alkil pada ester dengan atom hidrogen dari asam yang digunakan. Katalis yang digunakan akan menyebabkan terjadinya abstraksi proton yang kemudian diikuti dengan pengikatan alkil dari ester oleh ion enolat yang terbentuk.
Gambar 2.12 Reaksi Pembentukan Asidolisis (Frank, 2004)
Reaksi transesterifikasi sangat sensitif terhadap air. Kehadiran air akan menyebabkan terjadinya reaksi penyabunan. Karena alasan tersebut, reaksi transesterfikasi harus dilangsungkan menggunakan alkohol absolut serta asam pekat atau basa dalam bentuk Kristal sebagai katalis.
Ester asam lemak dialam terdapat dalam bentuk ester antara gliserol dengan asam lemak ataupun terkadang ada gugus hidroksilnya yang teresterkan tidak dengan asam lemak tetapi dengan posfat seperti pada posfolipid. Disamping itu, ada juga ester antara asam lemak dengan alkoholnya yang membentuk monoester seperti terdapat pada minyak jojoba. Ester asam lemak sering dimodifikasi baik untuk bahan makan maupun untuk bahan surfaktan, aditif, detergen dan lain sebagainya.
Reaksi transesterifikasi menggunakan katalis heterogen memiliki parameter penting untuk diperhatikan sebagai temperature, luasdari muatan katalis, perbandingan mol antarametanol dengan minyak dan waktu reaksi (Viswanathan, 2005). Reaksi transesterifikasi meliputi pengubahan lemak/minyak menjadi senyawa
metil ester. Umumnya pada reaksi transesterifikasi diperlukan adanya katalis berdasarkan reaksi di bawah ini :
Gambar 2.13 Reaksi Pembentukan Metil Ester
BAB 3
METODE PENELITIAN
3.1 Waktu dan Tempat
Penelitian ini dilaksanakan dari bulan Maret 2019 hingga Oktober 2019.
Penelitian ini dilakukan di Laboratorium Kimia Organik FMIPA USU. Analisis Spektroskopi Fourier Transform - Infra Red (FT-IR) dilakukan di Laboratorium Kimia Organik UGM dan Laboratorium Kimia Organik Universitas Negeri Padang dan Analisa Morfologi Permukaan dengan SEM (Scanning Electron microscopic) dilakukan di Laboratorium Puslabfor Bareskrim Polri.
3.2 Alat dan Bahan 3.2.1 Alat
- Labu takar 1000 mL Pyrex
- Beaker glass 2000 mL Pyrex
- Gelas ukur 100 mL Pyrex
- Indikator pH universal Sartorius
- Hotplate Stirrer Fishous
- Neraca Analitis Metler PM 480
- Termometer 1100C Fisher
- Magnetic Bar - Oven - Blender
- Cawan porselen Pyrex
- Labu leher tiga 500 mL Pyrex
- Labu Rotary 100 mL Heidolph
- Rotary evaporator Heidolph
- Statif dan Klem - Desikator
- Kertas saring biasa
- Kondensor Pyrex
- Corong penetes Pyrex - Buret
- Erlenmeyer 250mL Pyrex
- Plastik dan Karet - Pipet tetes
- Spektoskopi FT-IR Agilent Technologies
- Scanning Electron Microscopic JSM-35C Shumandju
3.2.2 Bahan - Jerami Padi - Aquadest
- HNO3 3,5% p.a E’Merck
- NaOH 2% p.a E’Merck
- NaOH17,5% p.a E’Merck
- Na2SO3 2%
- NaOCl 1,75%
- H2O2 p.a E’Merck
- Asam Stearat
- Metanol p.a E’Merck
- Benzen p.a E’Merck
- H2SO4(p) p.a E’Merck
- n-heksan p.a E’Merck
- Na2SO4 p.a E’Merck
- Indikator Phenoftalein - KOH 0.5 M
- HCl 0.5 M - Etanol 75%
- Na2CO3
3.3 Prosedur Penelitian 3.3.1. Pembuatan HNO3 3,5%
Sebanyak 53,8 ml HNO3 65%, lalu diencerkan dengan aquadest dalam labu takar 1L hingga garis akhir batas, kemudian dihomongenkan.
3.3.2. Pembuatan NaOH 2 %
Ditimbang sebanyak 20 gram NaOH pellet, dilarutkan dengan aquadest pada labu takar 1L, kemudian dihomogenkan.
3.3.3. Pembuatan NaOH 17,5 %
Ditimbang sebanyak 87,5 gram NaOH pellet, kemudian dilarutkan dengan aquadest dalam labu takar 500 ml hingga garis batas, kemudian dihomogenkan 3.3.4. PembuatanNaOCl 1,75 %
Sebanyak 72,91 ml larutan NaOCl 12 %, kemudian diencerkan dengan aquadest dalam labu takar 500 ml hingga garis batas, kemudian dihomogenkan.
3.3.5. Pembuatan H2O2 10 %
Sebanyak 167 ml H2O2 30% diencerkan dengan aquadest dalam labu takar 500 ml hingga garis batas, kemudian dihomogenkan.
3.3.6. Preparasi Sampel
Terlebih dahulu jerami padi dibersihkan. Kemudian dipotong kecil-kecil, lalu di keringkan, setelah kering dihaluskan dengan menggunakan blender sampai menjadi serbuk.
3.3.7. Isolasi Selulosa dari Jerami Padi
Sebanyak 75 gram serbuk jerami padi dimasukkan kedalam beaker glass, kemudian ditambahkan 1 liter HNO3 3,5 %, lalu dipanaskan pada suhu 900C selama 2 jam sambil diaduk menggunakan stirer diatas hotplate. Kemudian disaring dan dicuci residu hingga pH netral. Setelah pH netral ditambahkan 375 ml NaOH 2 % dan 375 ml Na2SO3 2 %, kemudian dipanaskan pada suhu 500C selama satu jam sambil diaduk, lalu disaring dan dicuci residu hingga pH netral. Setelah netral diputihkan dengan 500 ml NaOCl 1,75%, lalu dipanaskan pada suhu 700C selama 30 menit sambil diaduk diatas hotplate. Kemudian disaring dan dicuci residu hingga
filtrat pH netral. Kemudian ditambahkan dengan 500 ml NaOH 17,5% untuk melarutkan beta dan gamma selulosa, lalu dipanaskan pada suhu 800C selama 30 menit sambil diaduk diatas hotplate. Kemudian disaring dan dicuci residu sampai pH netral. Setelah netral ditambahkan dengan 250 ml H2O2 10%. Lalu dipanaskan pada suhu 600C selama 15 menit sambil diaduk diatas hotplate. Kemudian disaring dan dicuci dengan aquadest hingga pH netral. Dan dihasilkan alfa selulosa basah, lalu alfa selulosa basah di keringkan dalam oven pada suhu 600C, sehingga dihasilkan alfa selulosa kering. Selanjutnya dianalisa dengan FT-IR dan SEM.
3.3.8. Pembuatan Metil Stearat
Sebanyak 50 gram asam stearat dimasukkan kedalam labu leher tiga 500 ml.
Kemudian ditambahkan 30 ml metanol dan 75 ml benzen, kemudian ditambahkan katalis H2SO4(p) sebanyak 1,5 ml dan direfluks selama 5 jam dengan suhu 70-800C.
Setelah campuran dingin kemudian di rotarievaporator untuk menghilangkan kelebihan metanol dan pelarut. Kemudian di ekstraksi dengan 75 ml n-heksan dan dicuci dengan 25 ml aquadest sebanyak dua kali. Lalu akan terbentuk dua lapisan dimana lapisan atas ditambahkan dengan Na2SO4 anhidrous untuk menghilangkan kandungan air sisa. Kemudian dirotarievaporator untuk menghilangkan kadar n-heksan. Sehingga diperoleh metil ester stearat. Selanjutnya dikarateristik dengan FT-IR.
3.3.9. Sintesis Selulosa Stearat (Ismiyarto, 2009)
Sintesis selulosa stearat dilakukan dengan memasukkan 1 gram selulosa, 10 ml metil stearat, 10 mg Na2CO3 dan 50 ml pelarut metanol ke dalam labu leher tiga.
Campuran diaduk dengan magnetik sterer selama 1 jam diatas hotplate. Campuran dipanaskan pada temperatur 130oC selama 4 jam. Selulosa stearat yang dihasilkan disaring dan dicuci dengan metanol p.a kemudian dioven pada suhu 400C.
Dilakukan percobaan yang sama dengan katalis 15 mg, 20 mg, 25 mg, 30 mg Na2CO3. selanjutnya, diuji dengan Derajat Substitusi, di analisis dengan spektroskopi FT-IR dan analisa SEM.
3.3.10. Penentuan Derajat Substitusi (Wurzburg 1978 dalam Singh 2004)
Sebanyak 0,1 gram selulosa stearat dimasukkan dalam gelas erlenmeyer 250 ml ditambahkan 50 ml etanol 75%. Selulosa stearat kemudian diaduk dengan suhu 500C selama 30 menit dan didinginkan. Setelah dingin, sampel ditambahkan dengan 40 ml KOH 0,5 M. Kelebihan alkali kemudian dititrasi dengan HCl 0,5 M menggunakan indikator PP. Blanko dibuat menggunakan selulosa yang belum di asetilasi.
Acetyl % = ( )
3.4. Bangan Penelitian 3.4.1 Preparasi Sampel
3.4.2 Isolasi α-selulosa dari jerami padi (Oriza Sativa L)
3.4.3 Pembuatan Metil Stearat
3.4.4 Sintesis Selulosa Stearat
BAB 4
HASIL DAN PEMBAHASAN
4.1. Isolasi α-Selulosa dari Jerami Padi (Oriza Sativa L)
α-Selulosa yang digunakan pada penelitian ini adalah hasil isolasi dari jerami padi (Oriza Sativa L) yang berasal dari Desa Hutabayu Raja. Selulosa yang dianalisis dari hasil isolasi jerami padi sebanyak 75 gram melalui beberapa tahap sesuai metode penelitian sebelumnya. α-selulosa yang diperoleh dari 75 g hasil isolasi jerami padi sebanyak 15,43 gram (20,57% dari berat awal).
Tahap pertama adalah prehidrolisis yaitu penghilangan zat-zat ekstraktif dengan menggunakan HNO3 3,5%. Tahap kedua adalah delignifikasi yaitu memisahkan selulosa dari lignin atau senyawa- senyawa lain dengan menggunakan NaOH 2 % pada suhu 500C sehingga lignin dapat larut. Larutnya lignin pada temperature tersebut disebabkan karena molekul lignin terdegradasi oleh nukleofil basa kuat (OH). Pada proses delignifikasi selulosa yang dihasilkan berwarna kuning sehingga perlu dilakukan proses pemutihan (bleaching) dengan menggunakan NaOCl sebagai reagen pemutih yang bertujuan untuk menghilangkan sisa-sisa lignin yang menempel. Ion hipoklorit (ClO-) merupakan oksidator kuat yang dapat memecahkan ikatan karbon-karbon pada lignin dan akan lebih menyerang lignin dibandingkan selulosa karena molekul-molekul lignin banyak mengandung gugus kromofor (ikatan rangkap konjugasi) yang kaya elektron. Kemudian dilakukan penghilangan β-selulosa dan γ-selulosa dengan melarutkan residu dalam NaOH 17,5%, dimana α-selulosa akan mengendap sedangkan β-selulosa dan γ-selulosa akan larut sehingga diperolehlah α –selulosa yang berwarna putih kekuningan. Kemudian dilakukan pemucatan dengan H2O2 10 % untuk menghilangkan pigmen yang melekat pada selulosa. Hasil isolasi α-selulosa dapat dilihat pada Gambar 4.1.
Gambar 4.1. Hasil Isolasi α-selulosa
α-Selulosa yang dihasilkan diuji dengan Spektroskopi FT-IR memberikan spektrum dengan puncak vibrasi pada daerah bilangan gelombang 3441.01 cm-1 menunjukkan gugus –OH, 2893,22 cm-1 menunjukkan gugus C-H stretching, 1373,32 cm-1 menunjukkan C-H bending, 1635,64 merupakan vibrasi starching gugus C=O yang berada diujung rantai selulosa ; 1064,71 cm-1 merupakan vibrasi starching gugus C-O-C yang merupakan ikatan antara C1-C5 dan ikatan β-1,4- glikosidik. Dapat dilihat pada gambar 4.2.
Gambar 4.2 Spektrum FT-IR α-selulosa
4.2 Analisis Pembuatan Metil Ester Stearat
Metil stearat diperoleh dari hasil reaksi esterifikasi antara metanol dan asam stearat dengan menggunakan katalis asam yaitu H2SO4(p) pada suhu 70-800C. Maka akan dihasilkan Metil Stearat sebanyak 55 ml dan berwarna bening. Reaksi Esterifikasi Metanol dan Asam Stearat dapat dilihat pada gambar 4.3.
Gambar 4.3. Reaksi Pembentukan Metil Stearat
Hasil yang diperoleh dianalisa dengan Spektroskopis FT-IR dengan puncak- puncak vibrasi pada daerah bilangan gelombang 2917,14 cm-1 menunjukkan gugus C-H stretching, 1739,35 cm-1 menunjukkan gugus C=O, 1366,39 cm-1 menunjukkan C-H bending, 1173,09 cm-1 menunjukkan gugus C-O-C. Dapat dilihat pada gambar 4.4.
Gambar 4.4 Spektrum FT-IR Metil Stearat
4.3 Analisa Sintesis Selulosa Stearat
Selulosa stearat merupakan hasil reaksi transesterifikasi antara α-selulosa dari jerami padi dengan metil stearat dengan bantuan katalis Na2CO3. Direfluks selama 4 jam. Selulosa stearat yang dihasilkan disaring dan dicuci dengan methanol p.a kemudian dioven pada suhu 40oC. Berikut merupakan foto hasil selulosa stearat dapat dilihat pada gambar 4.5.
Gambar 4.5 Foto Hasil Selulosa Stearat
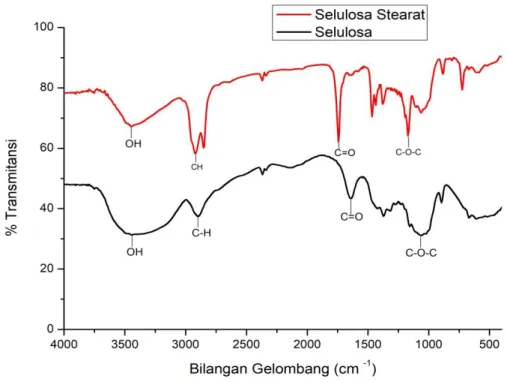
Gambar 4.6 Spektrum FT-IR Selulosa Stearat
Hasil spektroskopi FT-IR yang dilakukan memberikan spektrum dengan puncak-puncak vibrasi pada daerah bilangan gelombang 3448,72 cm-1 menunjukkan gugus O-H, 2916,37 cm-1 menunjukkan gugus C-H streching, 1743,65 cm-1 menunjukkan gugus C=O, 1465,90 cm-1 menunjukkan gugus C-H bending, 1172,72 cm-1 menunjukkan gugus C-O-C dan bilangan gelombang 725,23 cm-1 menunjukkan gugus (CH2)n>4.
Berikut merupakan perbandingan spektrum FT-IR α-Selulosa dan Selulosa Stearat.
Gambar 4.7 Perbandingan Spektrum FT-IR Selulosa dan Selulosa Stearat
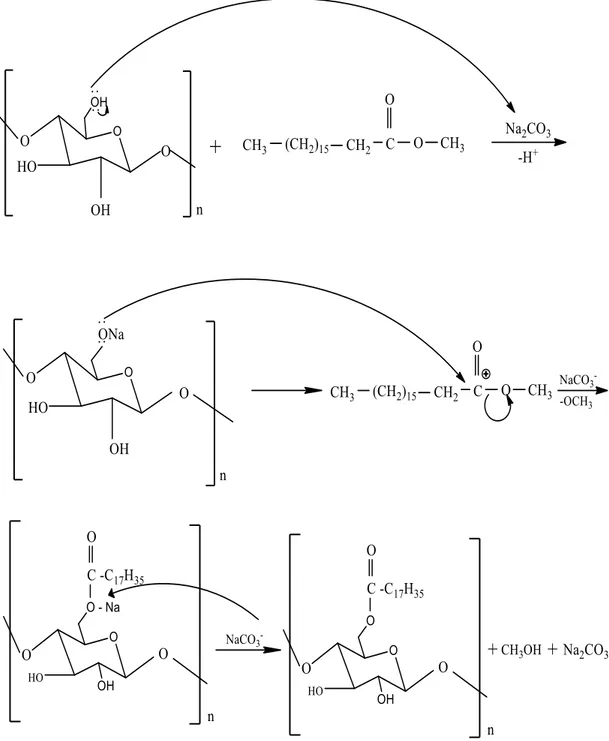
Gambar 4.8 Mekanisme Reaksi Selulosa Stearat
4.4 Penentuan Derajat Substitusi
Hasil penelitian Derajat Substitusi yang ditentukan secara titrasi (tabel 4.4) Tabel 4.4 Hasil Penentuan Derajat Substitusi Selulosa Stearat
Katalis Na2CO3 (mg) DS 10 0,898 15 0,778 20 0,664 25 1,025 30 1,299
Derajat Substitusi merupakan jumlah rata-rata gugus per anhidroglukosa yang disubstitusikan oleh gugus lain. Pada penelitian ini nilai DS yang paling tinggi yaitu 1.299 berasal dari selulosa stearat dengan variasi katalis 30 mg Na2CO3. Dimana hal ini menunjukkan banyaknya gugus ester yang tersubstitusi ke gugus OH pada selulosa, semakin besar nilai derajat substitusi memungkinkan semakin banyaknya gugus yang tersubstitusi. Apabila gugus yang menggantikan berupa satu gugus anhidroksil pada setiap unit anhidroglukosa diesterifikasi dengan satu buah gugus asetil, nilai DS sebesar 1. Apabila terdapat tiga buah gugus hidroksil yang diesterifikasi, maka nilai DS sebesar 3 (Wurzburg, 1989).
4.5 Analisa Morfologi Permukaan dengan SEM (Scanning Electron Microscopic) Analisa morfologi permukaan SEM dilakukan untuk melihat morfologi dari senyawa hasil modifikasi selulosa yang diperoleh. Dari analisa ini akan menunjukkan gambaran seberapa baik interaksi reagensia yang digunakan dalam modifikasi selulosa. Dalam penelitian ini analisa morfologi permukaan SEM dilakukan pada selulosa hasil isolasi dari jerami padi dengan perbesaran 1000 kali dan 2000 kali.
Adapun hasil SEM dari selulosa hasil isolasi dari jerami padi dapat kita lihat pada gambar 4.9, menunjukkan morfologi permukaan yang tampak homogen, halus dan memiliki rongga-rongga besar serta permukaan serat kecil.
(a) (b)
Gambar 4.10 Hasil SEM dari Selulosa (a) Perbesaran 1000 kali, (b) Perbesaran 2000 Kali.
(a) (b)
Gambar 4.11 Hasil SEM dari Selulosa Stearat (a) Perbesaran 1000 kali, (b) Perbesaran 2000 kali.
Adapun hasil SEM dari selulosa stearat hasil reaksi antara selulosa dengan metil stearat ditunjukkan pada gambar 4.9. Dari gambar menunjukkan morfologi permukaan pada perbesaran 1000 kali dan 2000 kali tampak lebih homogen, lebih teratur dan memiliki rongga-rongga yang lebih rapat daripada selulosa sebelum dimodifikasi. Hal ini terjadi perubahan morfologi permukaan yang menandakan bahwa telah terjadi reaksi antara gugus OH pada atom C2 selulosa dengan gugus karbonil dari metil stearat.
BAB 5
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Berdasarkan hasil penelitian yang telah dilakukan, dapat diambil kesimpulan sebagai berikut:
1. Selulosa stearat merupakan hasil sintesis antara α-selulosa dengan hasil metil stearate dengan bantuan katalis Na2CO3 sehingga menghasilkan Selulosa stearat. Dimana selulosa stearat dianalisa oleh data spektroskopi FT-IR yaitu dengan munculnya gugus O-H, gugus C-H stetching gugus C=O, gugus C-Hbending, gugus C-O-C dan gugus (CH2)n>4.
2. Karakterisasi dari selulosa stearat yaitu berdasarkan analisi FT-IR didapat puncak vibrasi pada daerah bilangan gelombang 3448,72 cm-1 menunjukkan gugus O-H, 2916,37 cm-1 menunjukkan gugus C-H streching, 1743,65 cm-1 menunjukkan gugus C=O, 1465,90 cm-1 menunjukkan gugus C-H bending, 1172,72 cm-1 menunjukkan gugus C- O-C, 725,23 cm-1 menunjukkan gugus (CH2)n>4. Berdasarkan hasil SEM permukaan pada perbesaran 1000 kali, dan 2000 kali tampak lebih homogen, lebih teratur dan memiliki rongga-rongga yang lebih rapat daripada selulosa sebelum dimodifikasi.
5.2 Saran
1. Diharapkan kepada peneliti selanjutnya agar dapat menlanjutkan penelitian ini dengan menggantikan sumber asam lemak yang digunakan.
2. Diharapkan kepada peneliti selanjutnya agar dapat melanjutkan penelitian ini dengan mengaplikasikannya.
DAFTAR PUSTAKA
Aak, 1990. Budidaya Tanaman Padi. Yogyakarta : Kanisius.
Almatsier, Sunita. 2006. Prinsip Dasar Ilmu Gizi. Jakarta : Gramedia.
Attala, R.H. 1987. Stucture of Cellulose, Characterization of The Solid States. ACS Symposium Series. No. 340. Washinton.
Anonim,1976. The Merck Index. Ninth Edition. An Encyclopedia of Chemical and Dugs, Merck and Co.Inc, Rahway. N.Y.USA.
Anonim. 2010. Tekno Pangan dan Agroindustri. Volume I, Nomor 1-12. Departemen Teknologi Pangan dan Gizi, Fakultas Teknologi Pertanian. Institut Pertanian Bogor.
Anindyawati, Trisanti. 2010. Potensi Selulase Dalam Mendegradasi Lignoselulosa Limbah Pertanian Untuk Pupuk Organik. Jurnal Vol. 45, No. 2. Cibinong : Lipi.
Anggorodi. 1979. Ilmu Makanan Ternak Umum. PT Gramedia. Jakarta.
Asthasari, R. 2008. Kajian Pembuatan Biodisel dari Minyak Jelantah Dengan Menggunakan Katalis Abu Tandan Kosong Kelapa Sawit. Skripsi. Fakultas Teknologi Pertanian. IPB. Bogor.
Badan Pusat Statistik, 2013. Berita Resmi Statistik dari Bahan Pusat Statistik Tentang Keadaan Ketenagakerjaan.
Beef Facts, 2007. Stearic Acid : A Unique Saturated Fat. USA. National Cattlemen’s Beef Association.
Bono, A., Ying, P.H., Yan, F.Y., Muci, C.L., Sarbatly, R., Krishnaiah, D. 2009.
Synthesis and Characterization of Charboximetyl Cellulose from Palm Kernel Cake. American Eurasian Network for Scientific Information, Vol 3 No. 1:5- 11.
Casey, P., James. 1960,Pulp and Paper, Chemistry and Chemical Technology, Vol.
1. Second Ed. Intercine Publishing, New York.
Chen, 2014.DegradationStudies On Plant Cellulose and Bacterial Cellulose FT_IR and SEM. [Thesis]. Birmingham : University Of Birmingham.
Chow, C.K. 2008. Fatty Acids In Foods and Their Implications. 3rd Ed. Boca Raton.
CRC Press.
Coffey, D., Bell D., and Handerson, A., 1995. Celuloce and Cellulose Derivate. New York : John Wiley & Son.
Davidek, J.J,. Valisel and Pokorny. 1990. Chemical Changes During Food Processing Development. In Food Science 21. Elsevier.
Djuarnani. 2004. Cara Cepat Membuat Kompos. PT. agromedia Pustaka. Jakarta.
Estiati T, Dwi RP, Widyastuti E, 2015. Komponen Minor dan Bahan Tambahan Pangan. Bumi Aksara. Jakarta.
Fatmawati. 2005. Tingkat serangan hama utama padi pada dua musim yang berbeda di Sulawesi Selatan. Di dalam: Seminar dan Pertemuan Tahunan XXI PEI.
Makassar. PFI Komda Sulawesi Selatan dan Dinas Perkebunan Pemerintah Provinsi Sulawesi Selatan.
Fessenden, J. 1999. Kimia Organik. Edisi ketiga. Jilid 1. Penerbit Erlangga. Jakarta Gandhi, N.N. 1997. Application Of Lipase. J. Am. Oil Chem. Soc.74,6.
Goring, D. 1963. Thermal Softening ofLignin. Pulp and Paper Magazine of Canada.
64 (12) : T517-T527.
Granstrom M, 2009. Cellulose Derivate : Synthesis, Properties and Aplications.
Helsinki University Publishing House. Helsinki.
Holtzapple, K.M. 1993. Cellulose : Encyclopedia of Food Science, Food Technology and Nutrition. Academic Press. London
Hong, K.M. 2013. Preparation and Characterization of Carboxymethyl Cellulose from Sugarcane Bagasse. (S). Departement of Chemical Science. Faculty of Science. University Tunku Abdul Rahman. Malaysia
Iswiyarto, S,. N. 2009. Pengaruh Temperatur Pada Sintesis Ester Asam Lemak Selulosa (FACE) Menggunakan Katalis Na2CO3. FMIPA. Universitas Diponegoro. Semarang.
Jackson, J.K., Letchford, K., Wasserman, B.Z., Ye. L., Hamad, W.Y., dan Burt, H.M. 2011. The Use Of Nanocrystalline Cellulose For The Binding and Controlled Release Of Drugs. International Journal Of Nanomedicine. 6 : 321-330.
Kalia S, 2011. Cellulose Fibers: Bio- and Nano- Polymer Composites. Springer- Verlag. London.
Ketaren S, 2005. Minyak dan Lemak Pangan. Ui-Press. Jakarta