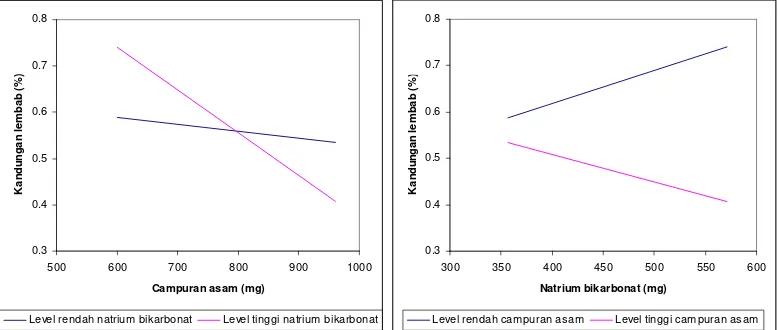
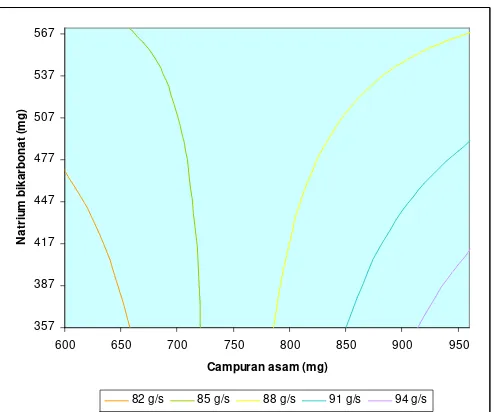
Optimasi campuran natrium sitrat-asam fumarat dan natrium bikarbonat sebagai eksipien dalam pembuatan granul effervescent ekstrak rimpang temulawak [Curcuma xanthorrhiza Roxb.] secara granulasi basah dengan metode desain faktorial - USD Repository
Teks penuh
Gambar

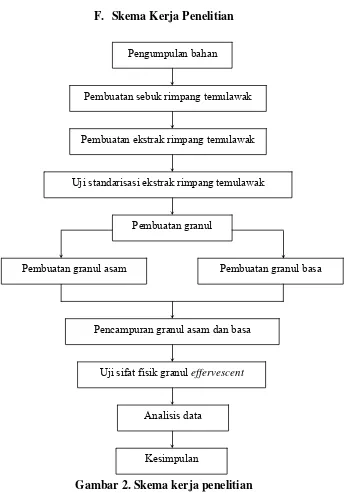
Garis besar
Dokumen terkait
(1) Untuk pelaksanaan Anggaran Belanja Pembangunan, Departemen/ Lembaga Pemerintah Non Departemen/instansi vertikal di daerah mengisi Daftar Isian Proyek atau dokumen lain
Perjanjian Kerja Bersama yang selanjutnya disingkat PKB adalah perjanjian yang diselenggarakan oleh Serikat Pekerja / Serikat Buruh hasil perundingan antara
Penyelidikan endapan bitumen padat di daerah Meulaboh merupakan kegiatan survey pendahuluan dimaksudkan untuk mempelajari keadaan geologi, khususnya mengenai sebaran dan
Setelah jumlah minimum sampel didapatkan, maka jumlah sampel untuk tiap jenis kendaraan dilakukan dengan menghitung proporsi besarnya jumlah kendaraan tersebut yang lewat
Apabila dana subsidi yang diklaim ke Bank oleh Lini 4 lebih rendah dari alokasi subsidi pemerintah yang disalurkan ke Bank (misalnya karena petani tidak menebus semua jatah
Pembatasan penggunaan hak kemerdekaan atau kebebasan menyatakan pendapat di muka umum sebagai implementasi dari pelaksanaan hak asasi manusia telah diatur secara
Bagaimana membuat sistem trading otomatis menggunakan analisis teknikal dengan acuan candlestick digabungkan dengan metode Martingale menggunakan bahasa pemrograman
Karena pembahasan tema ini sangat menarik, maka ada empat pertanyaan penting yang perlu diberikan jawabannya dalam tulisan ini, yaitu; Apa faktor pendukung