BAB 2
TINJAUAN PUSTAKA
2.1. Antithrombin
AT adalah molekul protein kecil yang menginaktifasi beberapa
sistem koagulasi. AT adalah glikoprotein dengan berat molekul 58 kDa
yang diproduksi oleh hati dan sel endotel, terdiri dari 432 asam amino,
berisi tiga ikatan disulfida. α-antithrombin adalah bentuk dominan dari
antithrombin ditemukan 90% dalam plasma darah. Sedangkan
β-antithrombin ditemukan kira-kira 10% dalam plasma darah. 3,5,6,14,15
Mekanismenya memblok pembekuan darah dengan menonaktifkan
protein "trombin". Oleh karena itu, disebut "anti-thrombin". Sementara
antithrombin III adalah nama asli yang diberikan untuk protein ini, nama
yang benar sekarang ini hanya antithrombin, dengan menghilangkan
angka "III". Nama-nama lain dan singkatan dari antithrombin ialah
antithrombin III, AT, AT III, dan heparin kofaktor I. 5
Beberapa perbedaan aktifitas AT pada plasma telah dilaporkan
pertama kali pada pertengahan abad 20, disebutkan klasifikasi dari AT I -
IV. AT I mengacu pada penyerapan trombin ke fibrin setelah trombin
mengaktifkan fibrinogen. AT II mengacu pada kofaktor dalam plasma,
yang bersama-sama dengan heparin mengganggu interaksi
menonaktifkan trombin. AT IV mengacu pada antithrombin yang diaktifkan
selama dan segera setelah pembekuan darah. Kemudian setelah
mempertunjukkan berbagai macam aktivitas AT ini, fungsi sebenarnya
adalah dari satu molekul AT III, yang namanya telah dipendekkan hanya
“antithrombin” ditetapkan pada “Meeting of the International Society on
Thrombosis and Haemostasis” tahun 1993. 5,14
2.1.1. Fisiologi dan Biokimia Antithrombin
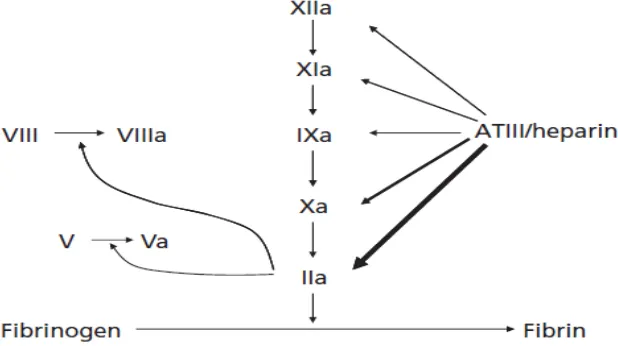
AT adalah serin protease inhibitor, antikoagulan alami yang
menghambat thrombin (IIa), faktor Xa dan juga menghambat faktor IXa,
XIa, XIIa, kallikrein dan plasmin. Konsentrasi AT pada plasma normal
adalah 150 µg/ml dan waktu paruh plasma sekitar 2 - 3 hari. 4,5,16,17,18
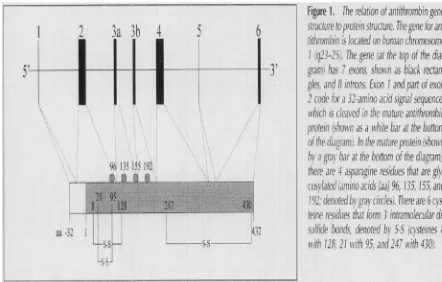
Pengkodean gen AT terletak pada kromosom 1 (q23-25) dan
berbagai mutasi telah diidentifikasi pada individu dengan defisiensi AT dan
Gambar 2.1. Struktur Gen Antithrombin 5
2.1.2. Aktivitas Antithrombin
AT melindungi dari koagulasi darah yang terlalu banyak. Jika kadar
AT rendah, darah seseorang akan memiliki kecenderungan untuk
koagulasi lebih mudah. Jika kadar AT terlalu tinggi, seseorang dapat
secara teoritis memiliki kecenderungan pendarahan. Namun peningkatan
kadar AT tampaknya tidak menyebabkan perdarahan atau tidak memiliki
signifikansi klinis. 5,18,19
Aktivitas endogen AT sangat dipotensiasi oleh keberadaan
proteoglikan yang bersifat asam seperti heparin. Zat ini terikat dengan
tempat kationik spesifik pada AT dengan menginduksi perubahan bentuk
dan meningkatkan pengikatannya pada trombin disamping substrat
lainnya. 6,20
Ada juga beberapa kondisi dimana AT seseorang menurun, tetapi
kadarnya kembali normal setelah kondisi sembuh. Jika kadar AT diukur
pada saat terjadi koagulasi akut atau saat diberikan heparin, kadarnya
akan menurun untuk sementara. Namun kadar AT biasanya kembali
normal setelah pasien pulih (dalam beberapa hari - minggu) atau ketika
heparin dihentikan. Ini penting diketahui untuk menghindari diagnosis
yang salah "defisiensi AT " jika ditemukan kadar AT yang rendah. 21
2.1.3. Kompleks trombin-antithrombin (TAT) dan pengaruhnya terhadap pemeriksaan kadar aktivitas Antithrombin (AT)
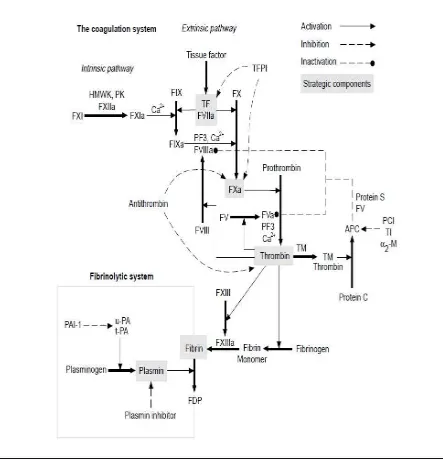
Jika terjadi aktivasi koagulasi maka akan terbentuk trombin dari
protrombin dengan melepaskan fragmen protrombin 1 dan 2 (F 1.2).
Trombin akan diikat oleh antithrombin sehingga terbentuk kompleks
trombin-antithrombin (TAT). Trombin juga akan mengubah fibrinogen
menjadi fibrin monomer dengan melepaskan fibrinopeptida A dan B (FPA
dan FPB). Fibrin monomer akan mengalami polimerisasi membentuk fibrin
polimer yang selanjutnya oleh pengaruh F XIII akan terjadi ikatan silang
sehingga terbentuk croos-linked fibrin. Kemudian plasmin akan memecah
cross-linked fibrin menghasilkan D-dimer. Oleh karena itu parameter yang
dapat dipakai sebagai petanda aktivasi koagulasi adalah F1.2, TAT, fibrin
monomer, FPA dan D-dimer. 19
Selanjutnya untuk mencari faktor risiko trombus/fibrin formation
salah satu pemeriksaan yang perlu dilakukan adalah pemeriksaan
aktivitas AT. AT berperan penting dalam pengaturan dan pencegahan
pembentukan fibrin yang berlebihan dengan menghambat sirkulasi
trombin.
Pada kadar AT yang diperiksa secara imunologi (AT antigen)
kadarnya normal, bisa saja pada pemeriksaan aktivitas AT (AT fungsional)
menunjukkan aktivitas AT yang rendah. Maka yang terpenting untuk
2.1.4. Pengukuran Kadar Aktivitas Antithrombin
AT plasma dapat diukur baik secara imunologi (AT antigen) atau
fungsional (AT activity). Pada uji fungsional ditetapkan aktivitas AT
dengan metode Chromogenic menggunakan anti - Xa. 5,18,19,23,24
2.1.5. Defisiensi Antithrombin
Defisiensi AT dapat terjadi secara bawaan maupun didapat.
Defisiensi AT menyebabkan faktor koagulasi yang aktif tidak dinetralkan
sehingga kecenderungan trombosis meningkat. Defisiensi AT dapat
digolongkan atas 2 tipe yaitu tipe I dan Tipe II. Tipe I ditandai dengan
kadar AT yang rendah, sedang tipe II ditandai dengan kadar AT yang
normal tetapi aktivitasnya rendah. 5,6,17,19,23,25,26
Nilai normal AT fungsional / AT activity : 27
• Prematur infant : 26 – 61 %
• Full-term infant : 44 – 76 %
• After 6 month : 80 – 120 %
Defisiensi AT bawaan diturunkan secara autosomal dominan, pada
individu yang heterozigot kadarnya 25 – 50% dari orang normal. Frekuensi
defisiensi AT heterozigot pada pasien trombosis sekitar 2,5-4%,
sedangkan pada populasi sehat sekitar 0,05-1,0%. Resiko trombosis pada
individu dengan defisiensi AT heterozigot 5 kali lipat lebih tinggi dari pada
individu dengan AT normal. Pada umumnya, individu dengan defisiensi
muda kurang dari 40 tahun, sering kali tanpa faktor lingkungan sebagai
pencetus dan kadang-kadang di tempat yang tidak biasa seperti di sinus
serebri, vena abdomen atau vena dalam lengan. Individu ini juga
cenderung mengalami trombosis berulang dan sering mempunyai riwayat
trombosis dalam keluarga. 5,19,23,25
Defisiensi AT didapat dijumpai pada sirosis hati, sindroma nefrotik,
pemakaian pil kontrasepsi, setelah trombosis yang luas dan setelah
pengobatan dengan heparin dosis tinggi. AT disintesis dihati sehingga
pada sirosis hati produksinya menurun. Pada sindroma nefrotik terjadi
kehilangan AT melalui urin karena kebocoran membran glomeruli. Pada
pemakai pil kontrasepsi yang mengandung estrogen terjadi penurunan
aktivitas AT yang bersifat reversibel. Mekanisme terjadinya hal ini belum
diketahui dengan jelas. Setelah trombosis yang luas, AT banyak terpakai
untuk menetralkan faktor-faktor yang aktif, sehingga aktivitasnya
berkurang.Demikian pula setelah pengobatan dengan heparin dosis tinggi,
AT banyak terpakai karena heparin tidak dapat bekerja tanpa AT.
5,17,19,21,27
Obat –obat yang meningkatkan kadar AT : anabolic steroids, androgens,
oral kontrasepsi (yang mengandung progesteron) dan sodium warfarin.
Obat-obat yang menurunkan kadar AT : fibrinolitik, heparin, oral
2.2. Intervensi Koroner Perkutan (IKP)
IKP telah dikenalkan lebih dari 20 tahun yang lalu. IKP adalah suatu
teknik untuk menghilangkan trombus dan melebarkan pembuluh darah
koroner yang menyempit dengan memakai kateter balon dan sering kali
dilakukan pemasangan stent. Tindakan ini dapat menghilangkan
penyumbatan dengan segera, sehingga aliran darah dapat menjadi
normal kembali, sehingga kerusakan otot jantung dapat dihindari. Angka
keberhasilan dari arteri dilatasi dengan tindakan IKP > 90 % pada lesi
yang tunggal. 9,10
Pada pasien PJK stabil, tindakan IKP dilakukan hanya pada pasien
dengan adanya keluhan dan tanda-tanda iskemik akibat penyempitan
pembuluh darah koroner. Pada penelitian-penelitian awal dijumpai
manfaat yang lebih kecil terhadap survival pasien yang dilakukan IKP
tanpa stent dibandingkan dengan operasi pintas koroner. Tetapi dengan
adanya stent dan stent bersalut obat (DES-Drugs Eluting Stent) serta
tersedianya obat-obatan ajuvan maka tindakan IKP saat ini menghasilkan
manfaat yang lebih besar dibandingkan operasi pintas koroner. 7
Pada NSTEMI dan angina pektoris tak stabil (APTS) tindakan
intervensi koroner perkutan bertujuan mengurangi kejadian morbiditas dan
mortalitas koroner di belakang hari.7
IKP primer pada STEMI didefinisikan sebagai tindakan intervensi
setelah onset nyeri dada, tanpa sebelumnya diberi trombolitik atau terapi
lain untuk menghancurkan penyumbatan tersebut.7
Adapun prosedur melakukan tindakan IKP terdiri dari beberapa
langkah. Pertama melakukan akses perkutan. Dalam proses ini arteri
femoralis harus diidentifikasi lebih dahulu (atau yang lebih jarang bisa
menggunakan arteri radialis atau arteri brachialis pada lengan) dengan
menggunakan suatu alat yang disebut jarum pembuka. Setelah jarum
sudah masuk, sheath introducer diletakkan pada jalan pembuka untuk
mempertahankan arteri tetap terbuka dan mengontrol perdarahan. Melalui
sheath introducer ini, guiding catheter dimasukkan. Ujung guiding catheter
ditempatkan pada ujung arteri koroner. Dengan guiding catheter, penanda
radio opak diinjeksikan ke arteri koroner, hingga kondisi dan lokasi
kelainan dapat diketahui. Selama visualisasi sinar X, ahli jantung
memperkirakan ukuran arteri koroner dan memilih ukuran balon kateter
serta guide wire coronary yang sesuai. Guiding wire coronary adalah
sebuah selang yang sangat tipis dengan ujung radio opak yang fleksibel
yang kemudian dimasukkan melalui guiding cathether mencapai arteri
koroner. Dengan visualisasi langsung, ahli jantung memandu kabel
mencapai tempat terjadinya blokade. Ujung kabel kemudian dilewatkan
menembus blokade. Setelah kabel berhasil melewati stenosis, balon
kateter dilekatkan dibelakang kabel. Angioplasti kateter kemudian
didorong kedepan sampai balon berada di dalam blokade. Kemudian baru
dan menekan arteri sehingga mengembang. Jika stent ada pada balon,
maka stent diimplantkan atau ditinggalkan pada tubuh untuk mendukung
arteri dari dalam agar tetap mengembang.
Prosedur melakukan IKP ini dapat menyebabkan pengaruh
terhadap cederanya arteri akibat gesekan pada endothelium sewaktu
kateter diarahkan secara retrograd melalui pembuluh darah. Gesekan ini
mungkin dapat mencetuskan nidus terbentuknya trombus baru. Trombus
pada intrakoronaria merupakan salah satu kemungkinan yang dapat
timbul di belakang hari pasca prosedur IKP.10
Terjadinya trombus dapat melalui 3 tahap: (1) paparan sirkulasi
darah terhadap permukaan yang bersifat trombogenik seperti kerusakan
endothelium vaskular akibat ruptur plaque atherosklerotik; (2) terjadi
rangkaian peristiwa yang berhubungan dengan platelet lebih lanjut
meliputi adhesi, aktifasi dan agregasi bersama-sama dengan pengeluaran
substrat yang akan memacu timbulnya agregasi kembali; (3) terjadi
pemacuan mekanisme anti pembekuan. 28
Akibat gesekan IKP pada permukaan endothelium, maka
endothelium akan melepaskan dan mengaktifasi trombin yang terkandung
didalamnya. Aktifasi trombin merupakan resiko besar untuk terjadinya
komplikasi pembentukan trombus baru dan stenosis berulang setelah
tindakan IKP. Hal ini sering terjadi pada IKP yang dilakukan umumnya
pada pasien yang mengalami angina pektoris tidak stabil (unstable
Antikoagulan selama IKP dibutuhkan untuk meminimalisasi resiko
dari komplikasi trombosis setelah tindakan IKP. Antikoagulan yang secara
umum dikenal adalah Unfractionated heparin (UFH). UFH adalah indirect
antithrombotic activity, mempunyai fungsi sebagai kofaktor untuk AT,
meningkatkan aktivitas molekul 1000 kali lipat. Pemeriksaan AT dengan
darah vena dimulai sebelum dan sesudah tindakan IKP. Pemeriksaan
dilakukan dengan metode chromogenic menggunakan anti-Xa.
20,23,24,30,31,32,33,34,35
2.2.1. Stent Bersalut Obat (Drugs Eluting Stent-DES) 7
Stent bersalut obat (drugs eluting stent) merupakan salah satu hal
yang sangat penting dalam perkembangan kardiologi intervensi, karena
DES dapat mengurangi angka restenosis. Tetapi DES ini lebih mahal
daripada stent biasa sehingga penggunaannya di negara berkembang
masih terbatas. Saat ini harga DES empat kali lebih mahal dari stent
biasa.
Beragam cara pelepasan obat dari berbagai bahan (platform stent)
dengan atau tanpa polimer yang dikandungnya giat dipelajari saat ini.
Berbagai penelitian untuk menilai efek anti proliferasi dan anti inflamasi
dari sirolismus, paclitaxel tacrolimus, everolimus, ABT-578, biolismus, dan
obat-obat lain seperti dexamethasone, 17-betaestradiol, batimastat,
actinomycin D. methotrexat, angiopeptin, tyrosinkinase inhibitors,
obat-obat anti proliferasi di atas tidaklah sama menunjukkan efek dalam
mencegah restenosis.
2.2.2. Indikasi DES 7
Keadaan-keadaan di mana dijumpai peningkatan risiko terjadinya
restenosis sehingga dibutuhkan penggunaan DES, yakni:
- small vessel (pembuluh darah kecil)
- chronic total occlusions (oklusi total kronik)
- bifurcational (percabangan)
- ostial lesion (lesi pangkal)
- by pass stenosis (penyumbatan pembuluh by pass)
- insulin dependent diabetes melitus (DM tipe 1)
- multivessel disease (pembuluh darah banyak terlibat)
- unprotected left main stenosis (oklusi cabang utama kiri)
- instent restenosis (oklusi pada tempat stent)
2.2.3. Perbandingan IKP dan CABG 36
Data yang dikumpulkan selama arteriografi koroner membantu
dokter menentukan apakah pasien sebaiknya dipertimbangkan untuk IKP
atau CABG untuk meningkatkan aliran darah arteri.
IKP dapat memberikan hasil yang optimal pada pasien yang dipilih
dengan hati-hati. Dengan panduan X-ray, sebuah kawat dimasukkan dari
menyusuri kawat untuk mencapai segmen yang menyempit. Balon
kemudian dikembangkan untuk menekan arteri agar terbuka dan sebuah
stent penahan besi kemudian disisipkan.
Bedah CABG dilakukan untuk mengurangi angina pada pasien
yang telah gagal dengan terapi obat-obatan dan bukan kandidat yang baik
untuk IKP. Bedah CABG ideal untuk pasien-pasien dengan penyempitan
multipel pada cabang arteri koroner yang berbeda seperti sering terlihat
pada pasien dengan diabetes. Bedah CABG telah memperlihatkan
peningkatan harapan hidup jangka panjang pada pasien-pasien dengan
penyempitan signifikan arteri koroner utama kiri dan pada pasien-pasien
dengan penyempitan signifikan arteri multipel khususnya pada
pasien-pasien dengan penurunan fungsi pompa otot jantung.
Studi yang sedang berlangsung membandingkan hasil terapi IKP
versus bypass (CABG) pada pasien yang merupakan calon prosedur
keduanya. Kedua prosedur sangat efektif mengurangi gejala angina,
mencegah serangan jantung dan mengurangi kematian. Banyak penelitian
memperlihatkan manfaat yang sama atau sedikit menguntungkan CABG
(terutama pada diabetes berat) meskipun data penelitian terbaru
mengevaluasi dua prosedur menggunakan teknik terbaru (sebagai contoh
stent terbaru dan CABG tanpa pompa) masih sedang dikumpulkan.
Pilihan terbaik untuk pasien individu dibuat oleh kardiolog, ahli bedah dan
2.3. Obat Antitrombotik : Unfractionated Heparin (UFH) Group obat antitrombotik termasuk indirect thrombin inhibitor (UFH
atau low molecular-weight heparin / LMWH) dan direct thrombin inhibitor
(Hirudin, Bivalirudin, Dabigatran etexilate, Ximelagatran dan
Argatroban).37
Telah lebih dari 40 tahun UFH digunakan sebagai terapi standar
untuk pengobatan awal trombosis vena. Di samping itu terapi UFH juga
cukup efektif untuk mencegah dan mengobati emboli paru, sebagai terapi
awal unstable angina serta infark miokard akut. UFH juga digunakan untuk
mengobati penderita operasi jantung dengan cara by pass -CABG,
operasi pembuluh darah dan prosedur IKP. Pada umumnya UFH
diberikan untuk keadaan dimana tidak dapat diberikan antikoagulan oral.22
2.3.1. Metabolisme dan Mekanisme kerja UFH
UFH merupakan mukopolisakarida dengan panjang rantai
berbeda-beda sehingga berat molekulnya bervariasi antara 5000 sampai 30.000
dalton, dengan berat molekul rata-rata 15.000 dalton, yang kira-kira terdiri
dari 45-50 rantai polisakarida. UFH diisolasi dan dimurnikan dari paru sapi
atau mukosa usus babi. Aktifasi antikoagulan dan clearance UFH
tergantung juga dari panjang molekulnya. Makin besar berat molekulnya,
makin cepat dibersihkan dari sirkulasi. 19,20,22,35
UFH ditemukan pada tahun 1916 oleh Mc Lean. Penelitian
Brinkhous dan kawan-kawan menunjukkan bahwa efek antikoagulan UFH
membutuhkan kofaktor yang terdapat dalam plasma yang disebut AT,
sehingga AT disebut kofaktor UFH. Efek antikoagulan UFH menurun pada
kondisi defisiensi AT baik herediter maupun didapat. Bahkan pada kadar
AT yang sangat rendah dapat menyebabkan heparin resisten.19,20,32,33,34,38
UFH mempunyai waktu paruh 30 menit – 2 jam tergantung dosis
pemberian. Efek antikoagulan segera timbul pada pemberian suntikan
bolus IV dengan dosis terapi, dan terjadi kira-kira 20-30 menit setelah
suntikan subkutan. Sebagian UFH akan mengalami degradasi di hati oleh
heparinase dan sebagian lagi diekskresi dalam bentuk utuh melalui ginjal.
UFH keluar melalui urin dalam waktu 5-9 jam setelah penyuntikan. Pasien
dengan kelainan hati atau ginjal lebih sensitif terhadap UFH karena waktu
paruh UFH menjadi lebih panjang. UFH juga diserap otot, lemak dan
limfe.22
UFH mempunyai berat molekul yang cukup besar sehingga tidak
bisa melewati membran, tidak bisa diserap usus dan tidak dapat melewati
plasenta. Dengan demikian UFH hanya dapat diberikan secara intra vena
atau subkutan. Pada pemberian UFH, hanya sepertiga dari dosis UFH
yang diberikan yang akan berikatan dengan AT. Trombin dan enzim
koagulasi lain mempunyai gugus aktif berupa serine protease. Gugus ini
akan diinaktifasi oleh arginine-reactive site pada AT. UFH akan berikatan
dengan gugus lisin pada AT. Akibat ikatan ini AT berubah dari inhibitor
kompleks AT-heparin juga menginaktifasi faktor koagulasi lain, yaitu faktor
Xa, IXa, XIa dan XIIa.19,35,36,37
2.3.2. Dosis dan lama pemberian UFH
Berbagai penelitian telah banyak dilakukan untuk mendapatkan
cara pemberian, dosis optimal dan lamanya pemberian UFH yang efektif
untuk pengobatan dan pencegahan trombosis. 38
Studi terakhir mendapatkan bahwa lama pemberian UFH dapat
dikurangi dari 10 hari menjadi 5 hari, apabila pemberiannya
dikombinasikan dengan antikoagulan oral. 22,38
Dosis pemberian UFH diberikan dengan dosis inisial 5000 U bolus
IV, kemudian dilanjutkan dengan drip 1000 U/jam, dosis ini harus selalu di
evaluasi dan disesuaikan untuk mendapatkan nilai aPTT 1,5 – 2,5 kontrol
(46 -70 detik), aPTT ini diperiksa setiap 4–6 jam. 22,38
Alternatif lain pemberian UFH adalah diberikan 5000 unit secara
subkutan setiap 8-12 jam, dengan catatan besarnya dosis yang diberikan
harus disesuaikan dengan pemeriksaan aPTT, nilai aPTT tetap
dipertahankan 1,5-2,5 kontrol. 2,22,35
2.3.3. Komplikasi pemberian UFH
Respon antikoagulan dari UFH berbeda pada tiap-tiap individu
karena obat ini berikatan secara nonspesifik dengan plasma dan protein
sel. Efek samping meliputi perdarahan, trombositopenia dan osteoporosis.
sekitar 3-5%. Resiko perdarahan akan meningkat pada pasien dengan
faktor resiko, seperti : usia (wanita >60 tahun, pria >70 tahun), operasi
yang lama, peningkatan kreatinin serum, stroke perdarahan, penyakit
ulkus peptikum, hipertensi, riwayat kelainan perdarahan dan aPTT >2 kali
nilai normal. Trombositopenia pada pasien pasca bedah frekuensinya
mencapai 5% bahkan pada pasien bedah jantung sampai 50%,
sedangkan pada pasien non bedah frekuensinya sekitar 3,5%.
Pada pemberian UFH berkepanjangan dapat juga menyebabkan
osteoporosis. Radiografi membuktikan terdapat penurunan densitas tulang
kira-kira 15% pada wanita yang mendapat pengobatan jangka panjang
selama kehamilan dan 2% mengalami fraktur vertebra yang simptomatik.
Pada penelitian lain dilaporkan, bahwa pemakaian UFH selama 3 bulan
menyebabkan osteoporosis pada 2-3% pasien.19,20,22,39,40
2.4. Kerangka Konsep
Kriteria Inklusi Kriteria Eksklusi
IKP
(Intervensi Koroner Perkutan)
Pasien IKP Primer Pasien IKP Elektif
Pemeriksaan Antithrombin