PERILAKU DISOLUSI KETOPROFEN TERSALUT
RANGKAP DALAM GEL KITOSAN-GOM GUAR DENGAN
ALGINAT
YUNIA ANGGI SETYANI
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
BOGOR
2009
ABSTRAK
YUNIA ANGGI SETYANI. Perilaku Disolusi Ketoprofen Tersalut Rangkap Gel Kitosan-Gom Guar dengan Alginat. Dibimbing oleh PURWANTININGSIH SUGITA dan BAMBANG SRIJANTO.
Modifikasi gel kitosan oleh hidrokoloid gom guar dengan penaut silang glutaraldehida berpotensi sebagai penyalut dalam sistem pengantaran sediaan obat mikrokapsul. Laju pelepasannya pada medium lambung dan usus telah dipelajari melalui uji disolusi. Hasil disolusi ketoprofen tersalut kitosan-gom guar sebelumnya menunjukan bahwa mikrokapsul hancur pada pH lambung sehingga pelepasan obat menjadi tidak terkendali. Penyalutan ganda ketoprofen dengan kitosan-gom guar dengan alginat untuk memperbaiki pelepasan ketoprofen telah dilakukan dalam penelitian ini. Sejumlah ragam
konsentrasi alginat dan larutan CaCl2 digunakan untuk optimasi kinerja penyalut. Hasil
uji disolusi ketoprofen menunjukkan pengaruh waktu terhadap pelepasan ketoprofen melalui model kinetika pelepasan obat. Pada medium asam sebagian besar formula penyalutan mengikuti model Korsmeyer-Peppas, sedangkan pada medium basa semua formula penyalutan mengikuti model Korsmeyer-Peppas. Mekanisme pelepasan obat dalam penelitian ini adalah secara difusi.
ABSTRACT
YUNIA ANGGI SETYANI. Dissolution Behavior of Ketoprofen Double Coated by Chitosan-Gum Guar Gel with Alginate Supervised by PURWANTININGSIH SUGITA and BAMBANG SRIJANTO.
Modification of chitosan gel by guar gum hydrocoloid with glutaraldehyde cross-link is capable to coat drug as microcapsule. The release rate in gastric medium and intestinal has been studied by dissolution test. Dissolution result of chitosan-gum guar coated ketoprofen previously showed that the microcapsule shaterred at gastric pH so that the drug release was not restrained. Double coating of ketoprofen by chitosan-gum guar with alginate in order to improve ketoprofen release has been done in this research. A number
of concentration levels of alginate and CaCl2 solutions were applied for optimation of
coat performance. Test dissolution result of ketoprofen showed time effect to ketoprofen release through kinetic models of drugs release. In acid medium, a large part of coating formulas followed Korsmeyer-Peppas model, while all coating formulas followed Korsmeyer-Peppas model in alkaline medium. The mechanism of drugs release in this research is diffusion.
PERILAKU DISOLUSI KETOPROFEN TERSALUT
RANGKAP DALAM GEL KITOSAN-GOM GUAR DENGAN
ALGINAT
YUNIA ANGGI SETYANI
Skripsi
sebagai salah satu syarat memperoleh gelar Sarjana Sains pada
Departemen Kimia
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
BOGOR
2009
Judul : Perilaku Disolusi Ketoprofen Tersalut Rangkap dalam Gel Kitosan-Gom Guar dengan Alginat.
Nama : Yunia Anggi Setyani NIM : G44204075
Disetujui
Pembimbing I, Pembimbing II,
Dr. Purwantiningsih Sugita, MS Ir. Bambang Srijanto
NIP 131 779 513 NIP 680 003 303
Diketahui
Dekan Fakultas Matematika dan Ilmu Pengetahuan Alam Institut Pertanian Bogor,
Dr. drh. Hasim DEA
NIP 131 578 806
PRAKATA
Puji syukur Penulis panjatkan kepada Allah SWT atas segala berkat yang memampukan Penulis menyelesaikan karya ilmiah ini. Penelitian ini dilaksanakan pada bulan Febuari hingga November 2008 di Laboratorium Kimia Organik, Laboratorium Bersama Departemen Kimia Fakultas Matematika dan Ilmu Pengetahuan Alam IPB, serta di Laboratorium Teknologi Farmasi dan Medika Puspitek, Serpong.
Penulis mengucapkan terima kasih kepada orang tua dan keluarga atas dukungan, dorongan, kasih sayang, doanya selama penulis menyelesaikan studi ini. Selain itu, penulis juga mengucapkan terima kasih kepada Ibu Dr. Purwantiningsih Sugita, MS dan Bapak Ir. Bambang Srijanto selaku pembimbing yang senantiasa memberikan arahan, motivasi, dan menyempatkan waktu untuk berdiskusi selama penelitian ini; kepada Ibu Tetty Kemala, Bapak M.Si, Drs. Ahmad Sjahriza, Budi Arifin, S.Si, Tuti Wukirsari, S.Si, dan Ibu Dini atas segala arahan, motivasi, dan diskusi-diskusi yang sangat berharga selama Penulis menjalani penelitian ini; serta kepada Papa dan Mama yang selama ini telah berjuang keras agar Penulis bisa tetap sekolah sampai akhirnya dapat menyusun karya ilmiah ini.
Penulis juga mengucapkan terima kasih kepada Bapak Sabur, Ibu Yenni Karmila, dan Ibu Siti Robiah atas segala fasilitas dan masukan yang diberikan, kepada Ibu Idah, Mas Julham, dan Mas Ending atas bantuannya selama penelitian di Laboratorium Teknologi Farmasi dan Medika Puspitek Serpong. Penulis juga mengucapkan terima kasih kepada teman-teman peneliti di Laboratorium Kimia Organik (Dedi, Feby, Andre, Bekti, Adi, Panji, Miqdad, Asnel, Ade Erika, Yuyun, Kak Robi, Kak Mamet, Mba Yuniar, Mba Rian, dan Mba Titik), teman-teman Bisma, serta teman-teman kimia 41 (Nindy, Asti, Budi) atas semangat dan motivasinya kepada Penulis, atas kerja sama dan keceriaan yang terjalin.
Pada kesempatan ini, Penulis juga mengucapkan terima kasih kepada Hibah Kompetensi Internal Departemen Kimia atas nama Dr. Purwantiningsih Sugita, M.Si sebagai sumber dana penelitian ini.
Akhir kata, semoga karya ilmiah ini dapat bermanfaat.
Bogor, Januari 2009
RIWAYAT HIDUP
Penulis dilahirkan di Jakarta pada tanggal 16 Juni 1985 sebagai anak pertama dari dua bersaudara dari ayah Djoko Setyo Atmodjo dan ibu Siti Sukaesih.
Penulis menyelesaikan studi dari SMU Negeri 42 Jakarta pada tahun 2003. Pada tahun 2004, penulis lulus seleksi masuk Institut Pertanian Bogor melalui jalur Seleksi Penerimaan Mahasiswa Baru pada Departemen Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam.
Selama mengikuti perkuliahan, Penulis menjadi asisten praktikum Kimia Tingkat Persiapan Bersama pada tahun ajaran 2005/2006, Kimia Organik pada tahun ajaran 2005/2006 dan 2006/2007, Kimia Organik D3 dan Kimia Polimer pada tahun ajaran 2007/2008, serta Kimia Bahan Alam dan Kimia Pangan D3 Analisis Kimia pada tahun ajaran 2008/2009. Pada bulan Juli-Agustus 2007, Penulis melaksanakan Praktik Lapangan di Pusat Penelitian dan Pengembangan Gizi dan Makanan Bogor.
DAFTAR ISI
Halaman
DAFTAR TABEL………... viii
DAFTAR GAMBAR……….. viii
DAFTAR LAMPIRAN………... ix
PENDAHULUAN………... 1
TINJAUAN PUSTAKA Kitosan dan Modifikasinya……….... 2
Alginat………... 3
Ketoprofen………. 4
Mikroenkapsulasi………... 4
Uji Disolusi... 5
Kinetika Pelepasan Obat...…….…... 5
BAHAN DAN LINGKUP KERJA Bahan dan Alat……….……….. 6
Pembentukan Mikrokapsul………... 6
Efisiensi Enkapsulasi …………...………. 7
Uji Disolusi Secara In Vitro ………...………... 7
Pencirian Mikrokapsul... 7
HASIL DAN PEMBAHASAN Pembentukan Mikrokapsul………... 7
Pelepasan Obat ... 8
Kinetika Pelepasan Obat... 9
Analisis Morfologi Mikrokapsul...………... 10
SIMPULAN DAN SARAN Simpulan………... 12
Saran………... 12
DAFTAR PUSTAKA………. 12
DAFTAR TABEL
Halaman
1 Spesifikasi kitosan niaga Anonim (1987) dalam Jamaludin (1994)... 2
2 Kinetika disolusi melalui pendekatan orde reaksi dan model kinetika... 9
3 Ukuran mikrokapsul... 11
DAFTAR GAMBAR
Halaman 1 Unit struktur kitin (R = NHCOCH3 ) (a) dan kitosan (R : NN2) (b)... 22 Struktur hidrogel kitosan: (a) ikatan silang kitosan-kitosan, (b) jaringan polimer hibrida, (c) jaringan semi-IPN, dan (d) kitosan berikatan silang ionik... 2
3 Pengaruh waktu terhadap pelepasan ketoprofen rerata pada medium disolusi pH 1.2 ( ) dan pH 7.4 ( )... 3
4 Foto SEM permukaan mikrokpasul ketoprofen hasil disolusi pada pH 1.2 saat menit ke-90 pada perbesaran 2000x... 3
5 Struktur berulang alginat... 3
6 Kompleks alginat dengan kitosan………... 3
7 Struktur ketoprofen………... 4
8 Klasifikasi mikrokapsul menurut morfologi………. 4
9 Alat uji disolusi Hansen paddle (USP dissolution)………... 5
10 Gel mikrokapsul saat berada dalam larutan alginat (a), mikrkapsul setelah penyaringan (b), dan mikrokapsul setelah pengerinagn suhu 400C (c)………… 7
11 Gel mikrokapsul saat berada di dalam larutan alginat 1% (a), 2% (b), dan 3% (c)... 8
12 Pengaruh waktu terhadap pelepasan ketoprofen pada medium asam ( ) dan basa ( ) dari mikrokapsul kitosan-gom guar dengan konsentrasi. alginat dan CaCl2 berturut-turut 3% dan 0.15 M... 9 13 Kurva regresi model Korsmeyer-Peppas pada medium pH 1.2 untuk formula alginat 3% dan CaCl2 0.15 M... 10 14 Kurva regresi model Korsmeyer-Peppas pada medium pH 7.4 untuk formula alginat 3% dan CaCl2 0.15 M... 10 15 Persentase pelepasan maksimum ketoprofen berdasarkan perhitungan dan penelitian dalam medium asam (a) dan basa (b)... 10 16 Mikrokapsul kitosan-gom guar dengan konsentrasi alginat 1 (a), 2 (b), dan 3% (b/v) (c) (mikroskop fotosetero dengan perbesaran 11.25 kali, serta mikrokapsul kosong dengan konsentrasi alginat 2% (d) (kamera digital)... 10
17 Foto SEM permukaan mikrokapsul tanpa (a) dan dengan penambahan
ketoprofen (b) dengan perbesaran 50 kali... 11
18 Foto SEM permukaan mikrokapsul kitosan-gom guar dengan alginat dengan perbesaran 1500 kali... 11
19 Foto SEM permukaan mikrokapsul ketoprofen sebelum disolusi (a), setelah disolusi asam (b), dan setelah disolusi basa (c) dengan perbesaran 1000 kali (inset serpihan alginat yang hancur)... 12
DAFTAR LAMPIRAN
Halaman 1 Diagram alir penelitian…... 172 Penetuan kadar air kitosan dan mikrokapsul... 18
3 Penentuan kadar abu kitosan... 18
4 Penentuan bobot molekul kitosan... 19
5 Penentuan derajat deasetilasi kitosan... 20
6 Preparasi bahan-bahan yang digunakan... 21
7 Efisiensi enkapsulasi ketoprofen dalam mikrokapsul kitosan-gom guar dengan alginat... 22
8 Hasil analisis data persentase pelepasan berdasarkan uji statistik... 23
9 Konsentrasi rerata ketoprofen yang terlepas dari mikrolapsul pada waktu t... 24
10 Bobot rerata ketoprofen yang terlepas dari mikrokapsul pada waktu t... 25
11 Persentase rerata ketoprofen yang terlepas dari mikrokapsul pada waktu t... 26
12 Bobot rerata ketoprofen yang masih terdapat dalam mikrokapsul pada waktu t (At)... 27 13 Persentase rerata ketoprofen yang tertinggal di dalam mikrokapsul pada waktu t... 28 14 Kinetika Disolusi ketoprofen pada medium asam (pH 1.2)... 29
15 Kinetika Disolusi ketoprofen pada medium basa (pH 7.4)... 32
16 Ukuran mikrokapsul... 34
17 Spektrum ketoprofen pada berbagai panjang gelombang dalam larutan NaOH 0.1M (a), dalam medium disolusi bufer klorida pH 1.2 (b), dan dalam medium disolusi bufer fosfat pH 7.4 dengan spektrofotometer UV... 35 18 Deret standar ketoprofen penentu konsetrasi ketoprofen dalam ekstrak NaOH 0.1M mikrokapsul dan uji diolusi dalam medium asam dan basa... 36
O R OH CH2OH O R OH CH2OH O O O n PENDAHULUAN
Ketoprofen merupakan zat aktif yang banyak digunakan dalam obat antiradang, analgesik (penghilang rasa nyeri), dan antipiretik (penurun panas). Namun, waktu paruh eliminasinya, yaitu 1.5—2 jam, sehingga harus sering dikonsumsi. Di sisi lain, bila obat tersebut terakumulasi sampai dosis > 300 mg di dalam tubuh, maka dapat terjadi pendarahan lambung (AMA 1991). Salah satu cara untuk mengatasi kelemahan tersebut ialah dengan menyalut ketoprofen dalam mikrokapsul sebagai suatu sistem pengantaran obat yang terkendali.
Kitosan merupakan salah satu biopolimer yang telah digunakan dalam mikroenkapsulasi ketoprofen (Yamada et al. 2001). Namun, gel kitosan bersifat rapuh sehingga perlu dimodifikasi. Modifikasi yang pernah dilakukan ialah dengan penambahan poli(vinil alkohol) (PVA) sebagai bahan saling tembus (IPN) dan glutaraldehida sebagai penaut silang (Wang et al. 2004). Modifikasi lainnya berupa penambahan hidrokoloid alami sebagai IPN, yaitu gom guar (Sugita et al. 2006a), alginat (Sugita et al. 2006c; Cardenas et al. 2003), karboksimetilselulosa (Sugita etal. 2006b), dan gom xantan (Sugita et al. 2007a). Modifikasi ini meningkatkan kekuatan mekanik gel dan mempercepat pembentukan gel.
Salah satu hasil modifikasi gel kitosan yang sifat reologinya telah dioptimumkan untuk pengantaran obat ialah gel kitosan-gom guar (Sugita et al. 2006a) dan gel kitosan-CMC (Sugita et al. 2006c). Mikrokapsul gel tersebut telah diuji efektivitasnya sebagai penyalut ketoprofen: gel kitosan-gom guar oleh Sugita et al. (2007b) dan Setyowati (2008), sedangkan gel kitosan-CMC oleh Yundhana (2008).
Kinerja membran kitosan-gom guar telah dilakukan oleh Nata et al. (2007) melalui uji difusi. Pemodelan ini memberikan gambaran bahwa mekanisme pelepasan ketoprofen dari membran kitosan-gom guar diawali dengan proses pembengkakan (swelling) membran saat membran kontak dengan cairan, selanjutnya pembukaan pori sehingga obat terlepas. Hasil disolusi ketoprofen tersalut kitosan-gom guar menunjukkan bahwa gel kitosan-gom guar tidak tahan terhadap kondisi pH lambung (pH 1.2). Hasil SEM memperlihatkan bahwa mikrokapsul terurai dan hancur setelah menit ke-90 uji disolusi pada pH lambung sehingga pelepasan obat menjadi tidak terkendali. Sementara, pada pH usus, sekalipun pelepasan ketoprofen terkendali, waktu pelepasannya masih terlalu cepat, yaitu sekitar 15 menit
(Sugita et al, 2007b). Namun, uji stabilitas yang dipercepat pada ketoprofen tersalut kitosan-gom guar menunjukan usia guna yang cukup baik, yaitu mencapai 9.07 minggu dengan kondisi penyimpanan 45–50 °C dan kelembapan relatif (RH) 75±5% (Setyowati 2008). Oleh karena itu, kinerja ketoprofen tersalut kitosan-gom guar perlu diperbaiki agar laju pelepasan ketoprofen di dalam lambung dan usus menjadi terkendali dengan waktu pelepasan yang tidak terlalu cepat. Dalam penelitian ini, ketoprofen tersalut kitosan-gom guar disalut lagi dengan kompleks polielektrolit (PEC) alginat yang tahan pada pH < 3 (Parfitt 1999).
Penyalutan pertama dengan kitosan gom guar dilakukan sesuai kondisi optimum kitosan-gom guar Sugita et al. (Sugita et al.
2006b). Sementara penyalutan kedua dengan PEC alginat dilakukan dengan ragam konsentrasi alginat dan CaCl2. Uji disolusi in
vitro kitosan berpenyalut ganda ini dilakukan selama 3 jam pada pH lambung dan 6 jam pada pH usus dengan pengambilan alikuot setiap 15 menit. Kinetika difusi ketoproden melalui matriks penyalut dikaji berdasarkan koefisien determinasi (R2) dari persamaan dengan
menggunkan pendekatan orde reaksi ke-0, ke-1, Higuchi, Hixson-Crowell, dan Korsmeyer-Peppas untuk mengetahui mekanisme pelepasannya.
TINJAUAN PUSTAKA Kitosan dan Modifikasinya
Kitosan, (C6H11NO4)n, merupakan
padatan amorf hasil deasetilasi kitin (Gambar 1) (Friedli dan Schlanger 2005) dengan unit berulang utama 2-amino-2-deoksi-D-glukosa (D-glukopiranosa) yang bertautan -(1 4). Polisakarida dapat membentuk polielektrolit kationik dalam larutan asam organik maupun anorganik sehingga kitosan dapat larut di dalamnya (Sakkinen 2003).
(a) (b) Gambar 1 Unit struktur kitin (R =
NHCOCH3 ) (a) dan kitosan
Sifat kitosan bergantung pada sumber, derajat deasetilasi (DD), panjang rantai, dan bobot molekulnya. Sementara mutu kitosan ditentukan oleh nilai derajat deasetilasi, kadar abu, kadar air, dan viskositas. Spesifikasi kitosan niaga disajikan pada Tabel 1.
Tabel 1 Spesifikasi kitosan niaga Anonim (1987) dalam Jamaludin (1994) Parameter Ciri Ukuran partikel Serpihan sampai bubuk Kadar air (%) ≤10 Kadar abu (%) ≤2 Derajat deasetilasi (%) 70−95* Warna larutan tidak berwarna Viskositas (cps): Rendah < 200 Medium 200−799 Tinggi 800−2000 Sangat tinggi > 2000 * Sakkinen (2003)
Larutan kitosan pada batas konsentrasi tertentu dalam larutan asam asetat 1% dapat membentuk gel (Khan et al. 2002). Gel kitosan tersebut dapat menahan air dalam strukturnya sehingga disebut hidrogel yang dapat membentuk formasi tiga dimensi (Wang et al. 2004). Hidrogel dapat dibedakan menjadi 2 berdasarkan proses pembentukannya, yaitu hidrogel kimia dan fisika. Hidrogel kimia melibatkan tautan-silang tak dapat balik melalui ikatan kovalen, sedangkan hidrogel fisika melibatkan tautan-silang ionik yang dapat balik (Stevens 2001 dan Berger et al. 2004).
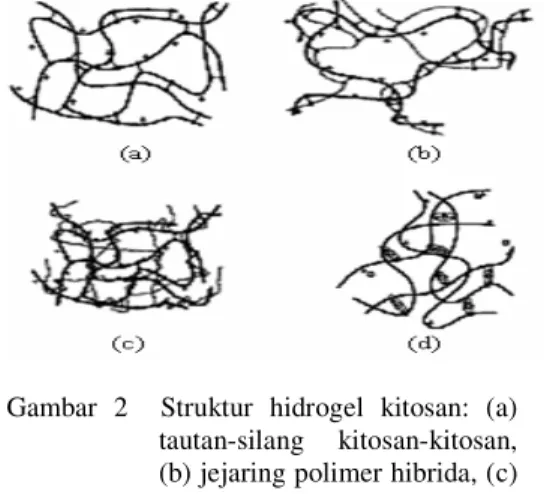
Kitosan termasuk hidrogel kimia. Tautan-silang kovalen dalam hidrogel kitosan dapat dibedakan menjadi 4 bagian, yaitu (a) tautan-silang kitosan-kitosan, (b) jejaring polimer hibrida (hybrid polymer network [HPN]), (c) jejaring polimer saling-tembus tanggung atau utuh (semi IPN atau full-IPN), dan (d) kitosan bertautan silang ionik (Gambar 2). Sifat tautan-silang hidrogel terutama bergantung pada bobot jenis tautan-silang (mol agen penaut-silang terhadap pengulangan mol unit polimer).
Gambar 2 Struktur hidrogel kitosan: (a) tautan-silang kitosan-kitosan, (b) jejaring polimer hibrida, (c) jejaring semi-IPN, dan (d) kitosan bertautan silang ionik (Berger et al. 2004).
Gel kitosan bersifat rapuh sehingga perlu dimodifikasi. Modifikasi yang pernah dilakukan, ialah dengan penambahan gom guar untuk obat antiradang (Kshirsagar 2000) dan penambahan CMC untuk obat antiperadangan indometasin (Tiyaboonchai & Ritthidej 2003; Yundhana 2008). Sugita et al. (2006a) telah memperoleh kondisi optimum pembentukan gel kitosan-gom guar sebagai sistem pengantaran obat, yaitu pada kitosan 2.5% (b/v), glutaraldehida 4.86% (v/v), dan gom guar 0.33% (b/v). Nata et al.
(2007) menggunakan komposisi kitosan-gom guar dengan komposisi kitosan yang berbeda dengan Sugita et al. (2006a), lebih rendah konsentrasi kitosannya (1.5% (b/v)), karena bobot molekul kitosan yang lebih tinggi, telah menunjukkan potensi membran tersebut sebagai sistem pengantaran obat terkendali. Membran membengkak ketika terjadi kontak antara membran dan cairan yang berdifusi, yang diikuti dengan pembukaan pori.
Setyowati (2008) telah melaporkan bahwa membran ini memiliki efisiensi mikroenkapsulasi sebesar 86.78% dan stabil ketika disimpan pada suhu 45–50 °C dengan kelembapan relatif (RH) (75±5)%. Namun, uji disolusi yang dilakukan oleh Sugita et al.
(2007) menunjukkan ketahanan mikrokapsul yang sangat buruk pada kondisi pH lambung. Mikrokapsul telah hancur seluruhnya pada menit ke-90 (Gambar 3). Kinerja mikroenkapsulasi pada medium usus lebih baik, namun pelepasan ketoprofen masih terlalu cepat (Gambar 4).
Gambar 3 Foto SEM permukaan mikrokapsul ketoprofen hasil disolusi pada pH 1.2 saat menit ke-90 pada perbesaran. 0 2 0 4 0 6 0 8 0 0 1 5 3 0 4 5 6 0 7 5 9 0 1 0 5 Wa kt u ( me n i t )
Gambar 3 Pengaruh waktu terhadap pelepasan ketoprofen rerata pada medium disolusi pH 1.2 ( ) dan pH 7.4 ( ).
Alginat
Alginat tergolong salah satu contoh hidrokoloid alami yang dapat berinteraksi ionik dengan kitosan. Alginat merupakan kopolimer rantai lurus dari residu asam -(1 4)-D-manuronat (M) dan asam -(1 4)-L-guluronat (G) yang membentuk blok homopolimer M atau G dan blok heteropolimer MG (Gambar 5) (Cardenas et al. 2003).
Gambar 5 Struktur berulang alginat (George dan Abraham 2006).
Garam alginat larut dalam air, tetapi mengendap dan membentuk gel pada pH kurang dari 3 (Parfitt 1999). Alginat dapat membentuk gel (formasi egg-box), film, manik
(beads), pelet, mikropartikel, nanopartikel (Ferreira et al. 2007). Oleh karena itu, gel alginat dapat digunakan sebagai bahan penyalut (UI-Ain et al. 2003).
Gel alginat terbentuk jika ditambahkan kation divalen (misalnya ion kalsium) (Cardenas et al. 2003) yang berfungsi berfungsi sebagai penaut silang antarmolekul alginat.
Laju pembentukan gel alginat bergantung pada ion yang ditambahkan (Mg2+ << Ca2+ <
Sr2+ < Ba2+). Jika penambahan kation
divalen dikendalikan, gel akan dihasilkan (Chaplin 2005).
Alginat dapat digunakan untuk memperbaiki struktur dasar kitosan yang mudah hancur dalam lingkungan asam lambung, melalui interaksi alginat-kitosan dengan membentuk PEC, sehingga melindungi zat aktif dalam obat yang dikonsumsi secara oral (Cardenas et al. 2003, Ferreira 2007). PEC dibentuk dengan mereaksikan 2 polielektrolit dengan muatan berbeda dan banyak mengandung air sehingga terbentuk jejaring tautan-silang secara ionik (Tarirai 2005). Jejaring silang alginat-kitosan memerlukan ion Ca2+ untuk
meningkatkan kekuatan mekaniknya (Gambar 6) (Friedli dan Schlanger 2005).
Gambar 6 Kompleks alginat dengan kitosan (Friedli dan Schlanger 2005). Alginat telah diaplikasikan sebagai penyalut hormon insulin (Timmy et al.
2002) dan sel bakteri tanpa kehilangan aktivitas (Bregni et al. 2000; Inanova et al.
2000; Ouyang et al. 2004). Contoh penggunaan lainnya ialah sebagai pengantar obat tuberkulosis (Ul-Ain et al. 2003) dan pengantar obat penglihatan (Motwani et al. 2007).
Ketoprofen
Ketoprofen, asam 2-(3-benzoilfenilpropanoat, merupakan obat antiradang nonsteroid dengan rumus molekul C16H14O3 dan bobot molekul 254.3 g mol-1.
Zat ini berupa serbuk putih atau hampir putih, tidak berbau, tidak higroskopis, serta mudah larut dalam etanol, kloroform, dan eter, tetapi tidak larut dalam air. Titik lelehnya berkisar 93–96 °C (USP 2003). Struktur ketoprofen dapat dilihat pada Gambar 7.
C O CH CH3 COH O
Gambar 7 Struktur ketoprofen. Ketoprofen merupakan zat dengan aktivitas analgesik, antiradang, dan antipiretik. Laju pelepasan ketoprofen dalam tubuh cepat, lalu dieliminasi melalui ginjal. Ketoprofen biasa digunakan dalam pengobatan artritis reumatoid, osteoartritis, dan berbagai penyakit muskuloskeletal kronis. Dosis yang umum digunakan ialah 50—100 mg, dikonsumsi dua kali sehari (Martindale 1982), sedangkan dosis oral ketoprofen bagi penderita artritis reumatoid dan osteoartritis adalah 75 mg (3 kali sehari) atau 50 mg (4 kali sehari) (AMA 1991). Mikroenkapsulasi ketoprofen dengan kitosan telah dilakukan oleh Yamada et al. (2001) dengan cara emulsifikasi.
Mikroenkapsulasi
Mikroenkapsulasi adalah teknik penyiapan bahan pengungkung (penyalut) yang disebut mikrokapsul (Yoshizawa 2004). Mikroenkapsulasi dapat melindungi bahan inti dari pengaruh lingkungan luar dan melepaskan bahan inti pada waktu dan tempat yang diinginkan. Mikrokapsul juga digunakan antara lain dalam bidang pertanian, farmasi, makanan, kosmetik, tekstil, kertas, dan cat. Mikrokapsul biasanya berukuran 5—2000 m (Kondo dan Asaji 1979).
Morfologi mikrokapsul bergantung pada metode mikroenkapsulasi yang digunakan. Berdasarkan morfologinya, mikrokapsul dapat dibagi menjadi tiga kelompok, yaitu berinti tunggal, berinti banyak, dan tipe matriks (Gambar 8).
Gambar 8 Klasifikasi mikrokapsul menurut morfologi (Yoshizawa 2004).
Mikroenkapsulasi dapat dilakukan secara kimia, fisikokimia, dan fisika. Pengeringan semprot kering dan beku, suspensi udara, penyalutan dengan panci penyalut, dan deposisi elektrostatik tergolong metode fisika., Polimerisasi antarmuka, polimerisasi in-situ, dan teknik pengerasan dalam cairan adalah contoh metode kimia, sedangkan koaservasi pemisahan fase, teknik pengeringan dalam cairan, dispersi secara leburan, dan teknik
power beds termasuk metode fisokokimia Penaut silang termasuk ke dalam pembuatan mikroenkapsulasi secara kimia. Mikroenkapsulasi dengan metode koaservasi pemisah fase membentuk kompleks koaservat yang terjadi karena kemampuan polimer kationik dan anionik yang larut air untuk berinteraksi.
Uji Disolusi
Uji disolusi merupakan suatu metode fisiko-kimia yang digunakan dalam pengembangan produk dan pengendalian mutu sediaan obat berdasarkan pengukuran parameter laju pelepasan dan melarutnya zat berkhasiat dari sediaannya. Proses disolusi diawali dengan masuknya larutan bufer ke dalam permukaan mikrokapsul sehingga mikrokapsul membengkak dan membentuk pori. Kemudian bufer berinteraksi dengan zat aktif sehingga terjadi pelarutan dan pelepasan zat aktif secara bertahap (Martin 1993). Uji disolusi ini diterapkan pada sediaan obat padat yang bertujuan mengukur dan mengetahui jumlah zat aktif yang terlarut dalam medium cair yang diketahui volumenya pada suatu waktu, suhu, dan peralatan tertentu (Siregar 1986).
Peralatan dayung Hansen (Hansen paddle) (Gambar 9) digunakan dalam uji disolusi secara in vitro. Keuntungan desain alat ini adalah kondisi hidrodinamik yang terpelihara dengan posisi yang tepat dari peletakan pengaduk dan wadah contoh (Martin 1993).
Gambar 9 Alat uji disolusi Hansen paddle
Kinetika Pelepasan Obat
Kinetika pelepasan obat dapat menggambarkan laju pelepasan obat dan model pelepasannya. Laju didefinisikan sebagai perubahan konsentrasi per satuan waktu. Laju pelepasan obat diamati dengan menggunakan parameter waktu paruh (t1/2), orde reaksi, dan
tetapan laju. Umumnya kinetika pelepasan obat terkendali mengikuti orde ke nol atau ke satu (Shoaib et al. 2006; Sarvanan et al. 2003). Reaksi orde ke nol dapat dituliskan sebagai: [A]t = [A]o – kt atau Q = kt...(1)
dengan [A]t ialah konsentrasi obat yang tersisa
di dalam sediaan obat setelah waktu t, [A]o ialah
konsentrasi obat mula-mula, Q ialah persen pelepasan, dan k ialah tetapan laju. Waktu paruh reaksi orde ke-0 dinyatakan dengan
k
t12 =
ln
2
...(2) sementara reaksi orde ke-1 dinyatakan dengan persamaan-persamaan sebagai berikut:ln [A]t = ln [A]o - kt...(3) k t
ln
2
2 1 = ...(4) (Dogra 1990; Atkins 1996).Pelepasan obat dari sediaan dapat berlangsung dengan mekanisme erosi atau difusi. Pada mekanisme erosi, sediaan terkikis sehingga obat terlepas ketika bersentuhan dengan medium. Proses ini umumnya terjadi pada sediaan obat yang berbentuk tablet. Mekanisme pelepasan obat secara erosi mengikuti hukum Fick pertama:
h C Cs DS dt dW [ − ] = ...(5) dengan dt dW
adalah laju disolusi massa, S luas permukaan penghalang, D koefisien difusi, Cs
konsentrasi obat dalam keadaan jenuh, C
konsentrasi obat dalam medium, h adalah ketebalan membran, dan t adalah waktu.
Sementara pelepasan obat secara difusi pada prinsipnya ialah terjadinya perpindahan obat melalui bahan penghalang atau matriks. Proses difusi ini umumnya terjadi pada sediaan obat yang menggunakan penyalut dan dinyatakan dengan persamaan Higuchi, yang juga dikembangkan dari hukum Fick:
2 1 2 = t ADCs dt dQ atauQ=(2DACs)12t12(6) dengan dt dQ
adalah laju pelepasan obat, A jumlah obat per satuan volume matriks, D
koefisien difusi obat melalui matriks, Cs
kelarutan dalam matriks, t waktu, dan Q jumlah obat per satuan luas yang dilepaskan dari matriks. jika nilai (2DACs)1/2 = k, maka
persamaan (6) menjadi persamaan (7).
2 1
kt
Q= ...(7) Selain dengan model Higuchi, proses pelepasan secara difusi dapat digambarkan juga melalui pendekatan model kinetika yang dikemukakan oleh Korsmeyer-Peppas dan Hixson-Crowell. Persamaan untuk model Korsmeyer-Peppas digambarkan melalui persamaan (8):
n kt
Q= ...(8)
Q adalah fraksi dari obat yang terlepas pada waktu t, k tetapan laju, dan n eksponen pelepasan. Sementara model Hixson-Crowell digambarkan melalui persamaan:
kt Qt
Qo13− 13 = ...(9)
Qt adalah jumlah obat yang terlepas pada waktu t, Q0 adalah jumlah obat awal dalam
sediaan obat, dan k adalah tetapan laju. Persamaan-persamaan di atas telah digunakan untuk menentukan kinetika pelepasan ibuprofen dari matriks tablet dengan hidroksipropil metilselulosa (HPMC) (Shoaib et al. 2006). Shoaib et al.(2006) menyatakan bahwa pelepasan ibuprofen mengikuti model Higuchi dan Korsmeyer-Peppas dengan R2 tertinggi berturut-turut
0.9994 dan 0.9942. Dalam penelitian lainnya, Kim et al. (2007) menjelaskan model pelepasan Novel Pelletizer dari pengaruh natrium alginat. Model pelepasannya mendekati model orde ke nol dan Korsmeyer-Peppas dengan nilai R2
tertinggi pada kedua model tersebut sama, yaitu 0.9988.
BAHAN DAN LINGKUP KERJA Bahan dan Alat
Bahan-bahan yang digunakan dalam penelitian ini antara lain kitosan yang dibeli dari Bratachem dengan spesifikasi nilai kadar air, kadar abu, DD, dan bobot molekul berturut-turut sebesar 7.5%, 0.11%, 74.41%, dan (2.44 × 106–6.32 × 106) g/mol
(Lampiran 1—4), glutaraldehida, gom guar, larutan bufer klorida (KCl—HCl)-air (1:2) pH 1.2, larutan bufer fosfat (KH2PO4—
NaOH)-air (1:3) pH 7.4, CaCl2, alginat,
Tween 80, dan senyawa aktif ketoprofen yang diperoleh dari PT Kalbe Farma.
Alat-alat yang digunakan di antaranya alat-alat kaca, spektrofotometer transformasi Fourier (FTIR) Bruker jenis Tensor 37, alat disolusi dayung Hansen, spektrofotometer UV-1700 PharmaSpec, mikroskop elektron susuran (SEM) Jeol-JSM-5310LV, dan analisis ukuran mikrokapsul dengan menggunakan mikroskop cahaya dan mikroskop fotostereo. Analisis FTIR dilakukan di Pusat Studi Biofarmaka (PSB) IPB, uji disolusi dan pengukuran diameter mikrokapsul di Laboratorium Farmasi dan Medikal Pusat Penelitian dan Teknologi (Puspiptek) Serpong dan Laboratorium Anatomi Departemen Biologi IPB, SEM di Laboratorium Zoologi Lembaga Ilmu Pengetahuan Indonesia (LIPI) Cibinong.
Lingkup Kerja
Penelitian utama meliputi pembuatan mikrokapsul, diawali dengan pembuatan gel kitosan-gom guar dengan penaut silang glutaraldehida berdasarkan hasil optimalisasi Sugita et al. (2006a). Gel tersebut disalut rangkap dengan alginat. Selanjutnya, efisiensi mikrokapsul, uji disolusi secara in vitro dalam medium asam dan basa, pencirian mikrokapsul dengan analisis SEM, pendekatan model kinetik, analisis kadar air dan ukuran mikrokapsul dilakukan dalam penelitian ini (Lampiran 5).
Pembentukan Mirokapsul (Sugita et al. 2006a dan Friedli & Schlanger 2005)
Sebanyak 22.8 ml larutan kitosan 2.5% (b/v) dalam larutan asam asetat 1% (v/v) ditambahkan dengan 3.8 ml larutan gom-guar 0.35% sambil diaduk. Setelah itu, sebanyak 0.76 ml glutaraldehida 3.75% (v/v) ditambahkan ke dalam larutan tersebut sambil diaduk hingga homogen.
Sebanyak 0.3991 g ketoprofen dalam etanol 96% 5.0 ml dicampurkan ke dalam larutan kitosan-gom guar tersebut sehingga nisbah bobot kitosan-ketoprofen 2:1. Setelah itu, 5 ml Tween-80 2% ditambahkan sambil diaduk pada suhu kamar (Sugita et al. 2006a).
Mikrokapsul dengan meneteskan campuran kitosan-gom guar ke dalam larutan alginat dengan ragam konsentrasi 1, 2, dan 3% (b/v). Kemudian mikrokapsul disaring dan dicuci dengan larutan CaCl2 dengan ragam konsentrasi
0.05, 0.10, dan 0.15 M. Mikrokapsul ketoprofen yang tersalut kitosan-gom guar dan alginat dikeringkan dalam oven 40 ºC selama 3 jam.
Efisiensi Enkapsulasi (Varma 2007)
Sebanyak 50 mg mikrokapsul dari setiap varian dilumatkan, lalu ketoprofen diekstraksi
dengan 80 ml larutan NaOH 0.1 M selama 5 menit. Ekstrak disaring dan ditambahkan NaOH hingga 100 ml. Konsentrasi ketoprofen yang terekstraksi dari mikrokapsul diukur menggunakan spektrofotometer UV pada panjang gelombang 257 nm. Absorbans yang diperoleh digunakan untuk menentukan konsentrasi ketoprofen dengan bantuan kurva standar.
Uji Disolusi secara In Vitro (Depkes 1995)
Uji disolusi mikrokapsul dilakukan dengan alat disolusi tipe 2 (metode dayung Hansen). Sebanyak 500 mg mikrokapsul ditimbang dan dimasukkan ke dalam
chamber disolusi. Uji disolusi dilakukan dalam medium pH 1.2 (cairan lambung) selama 3 jam dan medium pH 7.4 (cairan usus) selama 6 jam (Depkes 1995) pada suhu (37 ± 0.5) °C dengan kecepatan pengadukan 150 rpm. Pengambilan alikuot pada disolusi asam maupun basa dilakukan setiap 15 menit dengan volume setiap kali pengambilan 15 ml. Setiap kali pengambilan alikuot, volume medium yang terambil digantikan dengan larutan medium yang baru dengan volume dan suhu yang sama. Volume medium disolusi yang digunakan sebanyak 500 ml. Konsentrasi ketoprofen dalam larutan alikuot diukur dengan alat spektrofotometer UV pada panjang gelombang 258.6 nm (untuk disolusi pada pH 1.2) dan 260 nm (untuk disolusi pada pH 7.4). Data yang diperoleh dikaji kinetikanya. Dibuat kurva hubungan antara persen pelepasan ketoprofen dan waktu disolusi, kemudian orde reaksi dan mekanisme model pelepasan ketoprofen dari matriks penyalutan ganda ditentukan model kinetik yang diujikan ialah orde ke-0, ke-1, Higuchi, Hixson-Crowell, dan Korsmeyer-Peppas.
Pencirian Mikrokapsul
Pencirian morfologi mikrokapsul dilakukan terhadap mikrokapsul kosong dan yang terisi ketoprofen serta mikrokapsul setelah disolusi di medium asam dan basa dengan menggunakan SEM. Sementara pengukuran partikel dilakukan dengan mikroskop cahaya.
HASIL DAN PEMBAHASAN Pembentukan Mikrokapsul Gel kitosan-gom guar tersalut alginat terbentuk melalui 3 jenis interaksi, yaitu interaksi kitosan dengan alginat yang
membentuk PEC; interaksi antara alginat dan Ca2+ (Friedli & Schlanger 2005); serta
tautan-silang antarkitosan oleh glutaraldehida yang menghasilkan ruang-ruang kosong. Gom guar digunakan sebagai bahan saling tembus yang akan mengisi ruang-ruang kosong yang dihasilkan dari tautan silang antarkitosan.
Penetesan larutan kitosan-gom guar ke dalam larutan alginat membentuk bulatan-bulatan kecil putih yang lama-kelamaan akan memadat dan tenggelam, ketika interaksi kedua penyalut telah berjalan sempurna. Gel mikrokapsul tersebut tidak bulat sempurna karena adanya pengaruh gravitasi bumi saat penetesan (Gambar 10). Ion Ca2+ akan
berikatan dengan alginat pada bagian residu guluronatnya dan membentuk egg-box dengan berdifusinya CaCl2 ke dalam gel kitosan-gom
guar alginat (Abraham & George 2006).
(a) (b) (c) Gambar 10 Gel mikrokapsul saat berada dalam
larutan alginat (a), mikrokapsul setelah penyaringan (b), dan mikrokapsul setelah pengeringan suhu 40 oC (c).
Konsentrasi alginat dan CaCl2 berpengaruh
pada sifat gel yang dihasilkan. Pada formula dengan konsentrasi alginat 1% (b/v), gel tidak stabil dan mudah pecah. Hal tersebut diduga karena gaya adhesi kitosan-gom guar dengan alginat 1% (b/v) lebih kecil dibandingkan dengan gaya kohesi larutan alginat. Selain itu, jumlah air bebas disekitar mikrokapsul lebih banyak karena jumlah hidrokoloid alginat yang digunakan lebih sedikit pada alginat 1% (b/v). dibandingkan dengan alginat 2 dan 3% (b/v) sehingga cenderung membengkak gel mikrokapsul. Gel dengan konsentrasi alginat 2 dan 3% (b/v) lebih bulat serta tidak rapuh karena ikatan PEC-nya semakin kuat. Sebagaimana ditunjukan pada gambar 11, Gel dalam larutan alginat cenderung bergerombol karena adanya ikatan hidrogen antarmolekul alginat pada lapisan luar gel mikrokapsul.
(a) (b) (c) Gambar 11 Gel mikrokapsul saat berada di
dalam larutan alginat 1 % (a), 2 % (b), dan 3 % (c).
Kadar air mikrokapsul berkisar 13.91-25.84% (Lampiran 2). Kadar air yang lebih dari 10% menyebabkan mikrokapsul mudah ditumbuhi mikroorganisme. Tingginya kadar air mikrokapsul kitosan-gom guar dengan alginat dikarenakan gom guar memiliki kemampuan yang tinggi dalam menyerap air (Sugita et al. 2006a).
Pelelpasan Obat
Laju pelepasan ketoprofen dari matriks kitosan-gom guar alginat dalam medium asam (bufer pH 1.2) dan basa (bufer pH 7.4) diperlihatkan pada (Lampiran 6—10). Pada kedua medium tersebut, kinerja pelepasan ketoprofen yang tersalut rangkap, baik pada medium asam maupun basa, lebih baik jika dibandingkan dengan pelepasan ketoprofen yang hanya tersalut kitosan-gom guar (Gambar 3). Persentase pelepasan ketoprofen dalam medium asam dan basa berbeda nyata dengan <0.0001 (Lampiran 11). Hal ini ditunjukkan dengan persentase pelepasan ketoprofen di medium asam terjadi secara perlahan dengan kisaran 1.46—12.97%.
Keberadaan penyalut kedua (PEC alginat) secara nyata telah memperkuat jejaring matriks mikrokapsul sehingga pelepasan ketoprofen dalam asam menjadi terkendali. Ketika matriks mikrokapsul kontak dengan bufer asam, cairan merembes ke dalam matriks melalui pori-pori matriks, sehingga matriks mengembang dan melarutkan kitosan (Tan et al. 2003). Akibatnya gugus imina terhidrolisis sehingga rantai kitosan terurai dan larutan menjadi kekuningan pada menit ke-15. Sementara matriks alginat tetap utuh.
Persentase pelepasan ketoprofen di medium asam paling besar terjadi pada formula B dengan konsentrasi alginat 1% (b/v) dan CaCl2 0.1 M. Hal tersebut
dikarenakan tautan-silang yang lebih lemah antara alginat dan ion Ca2+ sebagai lapisan
terluar matriks. Konsentrasi alginat dan CaCl2 memengaruhi pelepasan mikrokapsul
pelepasan ketoprofen pada mikrokapsul yang menggunakan alginat 1, 2, dan 3% (b/v) berturut-turut ialah 11.51—37.58, 3.45—54.97, dan 6.61—42.80%. Pelepasan ketoprofen pada alginat 1% (b/v) dipengaruhi oleh penyalutan ketoprofen yang tidak sempurna sehingga pelepasannya kecil. Hal ini dikarenakan terbentuknya gel kitosan-gom guar alginat yang mengungkung ketoprofen tidak stabil. Kecilnya pelepasan pada formula dengan alginat 3% (b/v) dibandingkan dengan alginat 2% menunjukkan bahwa penyalutan yang semakin kuat. Hal tersebut mendukung pernyataan Tan
et al. (2003) yang menyatakan bahwa konsentrasi alginat yang lebih tinggi akan menghasilkan mikrokapsul yang tidak berpori sehingga ketoprofen sulit lepas. Selain itu, Sutriyo et al. (2005) juga mengemukakan hal yang sama, yaitu tebalnya lapisan gel akan menyebabkan senyawa aktif semakin sulit terlepas.
Berdasarkan persentase pelepasan ketoprofen dalam medium asam dan basa, mikrokapsul yang memiliki profil terbaik ialah formula I (alginat 3% (b/v) dan CaCl2 0.15M)
dengan nilai efisiensinya sebesar 30.10 % (Lampiran 12). Formula tersebut memiliki persentase pelepasan maksimum di medium asam dan di medium basa dan berturut-turut 6.03% dan 43.55%. Konstentrasi ketoprofen di dalam medium tersebut berturut-turut 5.5868 dan 131.0734 mg/L. Konsentrasi terapi minimum ketoprofen yang diinginkan sebesar 15−25 mg/l. Namun, pada penelitian ini konsentrasi ketoprofen setimbang 100—120 mg/l sehingga telah melebihi konsentrasi terapi minimum. Profil pelepasan ketoprofen pada formula tersebut dapat dilihat pada Gambar 12.
Pada Gambar tersebut terlihat bahwa dalam medium asam, persentase pelepasan relatif tetap seiring dengan lamanya waktu disolusi. Sementara dalam medium basa, pelepasan ketoprofen mencapai maksimum pada menit ke-210, selanjutnya cenderung stabil dan menurun. Hal ini terjadi karena kesetimbangan antara cairan bufer dan cairan dalam matriks serta terjadinya pengenceran akibat pengambilan cuplikan. 0 20 40 60 80 100 120 140 0 60 120 180 300 360 Menit ke-K o n se n tr as i k et o p ro fe n ( p p m )
Gambar 12 Pengaruh waktu terhadap pelepasan ketoprofen pada medium asam ( ) dan basa ( ) dari mikrokapsul kitosan-gom guar dengan konsentrasi. alginat dan CaCl2 berturut-turut 3% dan
0.15 M.
Kinetika Pelepasan Obat
Pelepasan ketoprofen dalam mikrokapsul mengikuti mekanisme difusi (Shoaib 2006). Model kinetika pelepasan baik dalam medium asam maupun medium basa ditentukan dengan melihat nilai koefisien determinasi (R2), tertinggi dari
diperoleh dari kurva hubungan antara persentase pelepasan ketoprofen dan waktu melalui pendekatan kinetika persamaan orde ke nol (Q terhadap t), orde ke satu (ln Qt terhadap t), model Higuchi (Q terhadap t1/2)
model Hixson-Crowell (Qt1/3 tehadap t) , dan
model Korsmeyer-Peppas (log Q terhadap log t). Hasil perhitungan R2 ditampilkan
pada Tabel 2.
Berdasarkan data uji disolusi medium asam, Formula A, B, C, D, E, dan I mengikuti model Korsmeyer-Peppas. Sementara formula F, G, dan H mengikuti model Higuchi (Tabel 2). Formula terbaik I memilki koefisien determinasi sebesar 0.6603 dengan persamaan garis Log Q = 0.2745 log t + 0.1683 (Gambar 13). Berdasarkan persamaan (7) dapat diperoleh nilai tetapan laju reaksi, k sebesar 1.47 menit-n dengan eksponen pelepasan, n,
sebesar 0.2745. Pelepasan ketoprofen dalam medium asam pada formula I, nilai n antara 0.28—0.35 sehingga menunjukkan mekanisme pelepasan ketoprofen mengikuti difusi Fickian.
Persentase pelepasan di dalam medium asam sebesar 7.32% selama 3 jam. Hal ini membuktikan bahwa model Korsmeyer-Peppas dapat mewakili laju pelepasan ketoprofen yang sebenarnya (Gambar 15).
y = 0.6284x + 0.1062 R2 = 0.9198 0 0.2 0.4 0.6 0.8 1 1.2 1.4 1.6 1.8 0 0.5 1 1.5 2 2.5 3 log t lo g [ x] y = 0.2745x + 0.1683 R2 = 0.6603 0 0.1 0.2 0.3 0.4 0.5 0.6 0.7 0.8 0.9 0 0.5 1 log t 1.5 2 2.5 lo g [ x]
a nilai koefisien determinasi tertinggi Keterangan : A : alginat 1 %, CaCl2 0.05 M
B : alginat 1 %, CaCl2 0.10 M C : alginat 1 %, CaCl2 0.15 M D : alginat 2 %, CaCl2 0.05 M E : alginat 2 %, CaCl2 0.10 M
Gambar 13 Kurva regresi model Korsmeyer-Peppas pada medium pH 1.2 untuk formula alginat 3% (b/v) dan CaCl2
0.15 M.
Pelepasan ketoprofen pada medium basa untuk semua formula mengikuti model Korsmeyer-Peppas. Formula terbaik I memilki koefisien determinasi sebesar 0.9198 dengan persamaan garis log Q = 0.6284 log t + 0.1062 (Gambar 14). Formula I memiliki R2 tertinggi
dibandingkan dengan formula lainnya dengan
F : alginat 2%, CaCl20.10 M G : alginat 3%, CaCl2 0.05 M H : alginat 3%, CaCl2 0.15 M I : alginat 3%, CaCl2 0.15 M
nilai n sebesar 0.6284 (n = 0.51---0.7) sehingga menunjukkan bahwa mekanisme pelepasan ketoprofen secara difusi Anomalous (non-Fickian).
Persentase pelepasan ketoprofen di dalam medium asam sebesar 44.92 % selama 6 jam. Hal ini membuktikan bahwa model Korsmeyer-Peppas dapat mewakili laju pelepasan ketoprofen yang sebenarnya (Gambar 15).
Gambar 14 Kurva regresi model Korsmeyer- Peppas pada medium pH 7.4 untuk formula alginat 3% (b/v) dan CaCl2 0.15 M.
Medium asam
Formula Orde ke-0 Orde ke-1 Higuchi Hixson-Crowell Korsmeyer-Peppas R2 k (menit )-1 R2 k (menit )-1 R2 k (menit )-1/2 R2 k (menit )-1/3 R2 k (menit )-n n A 0.8138 0.0242 0.8139 0.0003 0.8399 0.4388 0.8139 0.0004 0.886a 0.889 0.3921 B 0.8896 0.0441 0.896 0.0005 0.9615 0.8189 0.8939 0.0007 0.978a 1.845 0.3832 C 0.3359 0.0098 0.2755 0.001 0.4367 0.1995 0.2783 0.0015 0.5639a 1.744 0.2262 D 0.8383 0.0096 0.8395 0.0001 0.903 0.17736 0.8391 0.0002 0.9261a 0.633 0.3173 E 0.8292 0.0218 0.8251 0.0005 0.8381 0.3917 0.8265 0.0007 0.8556a 0.699 0.4001 F 0.8551 0.043 0.8948 0.0004 0.902a 0.6424 0.8944 0.0006 0.8702 1.044 0.4173 G 0.9125 0.0403 0.9154 0.0004 0.9458a 0.7334 0.9145 0.0007 0.171 6.674 0.02 H 0.878 0.0145 0.8491 0.0002 0.8873a 0.2608 0.8777 0.0002 0.876 0.4369 0.4111 I 7x10-7 16.05 0.1649 0.0001 5x10-7 0.0002 4x10-7 1x10-5 0.6603a 1.473 0.2745 Medium basa
Formula Orde ke-0 Orde ke-1 Higuchi Hixson-Crowell Korsmeyer-Peppas R2 k (menit )-1 R2 k (menit )-1 R2 k (menit )-1/2 R2 k (menit )-1/3 R2 k (menit )-n n A 0.0781 0.0148 0.0527 0.0001 0.2938 0.5697 0.0676 0.0002 0.8184 1.1393 0.4726 B 0.0991 0.0295 0.0676 0.0003 0.3347 1.0785 0.0777 0.0005 0.8504a 1.1534 0.5796 C 0.0693 0.0145 0.0527 0.0001 0.0693 0.8718 0.058 0.0002 0.8173a 1.1429 0.4788 D 0.1918 0.0211 0.1784 0.0002 0.3042 0.0044 0.1829 0.0003 0.8742a 1.1048 0.4744 E 0.0923 0.0309 0.0584 0.0003 0.3225 1.1485 0.0691 0.0005 0.85a 1.1553 0.5908 F 0.2798 0.0713 0.1632 0.0008 0.4358 1.4738 0.1796 0.0011 0.898a 1.1397 0.6644 G 0.1692 0.0461 0.1283 0.0005 0.4509 0.7057 0.1419 0.0008 0.8768a 1.1475 0.6237 H 0.1791 0.0223 0.2202 0.0003 0.6424 1.6924 0.1587 0.0003 0.9198a 1.1153 0.4971 I 0.3512 0.0628 0.3353 0.0008 0.0178 0.1345 0.0002 1x10-5 0.9198a 1.112 0.6284
0 2 4 6 8 10 12 14 16 A B C D E F G H I Formula % p el ep as an
hasil penelitian hasil perhitungan
0 10 20 30 40 50 60 1 2 3 4 5 6 7 8 9 Formula % p el ep as an
hasil penelit ian hasil perhitungan
Berdasarkan hasil perhitungan dengan menggunakan persamaan model kinetika Korsmeyer-Peppas, persentase pelepasan maksimum ketoprofen di medium asam lebih kecil dibandingkan dengan di medium basa. Hal ini sejalan dengan pernyataan sebelumnya yang menyatakan bahwa pelepasan di asam lebih rendah. Laju pelepasan ketoprofen berdasarkan perhitungan serupa dengan laju pelepasan ketoprofen berdasarkan dengan penelitian (Gambar 15).
(a)
(b)
Gambar 15 Persentase pelepasan maksimum ketoprofen berdasarkan perhitungan dan penelitian dalam medium asam (a) dan basa (b).
Analisis Morfologi Mikrokapsul
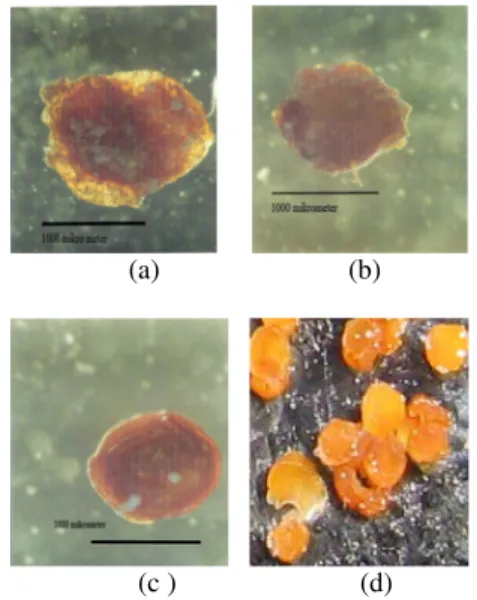
Mikrokapsul ketoprofen (Gambar 16a, 16b, dan 16c) berwarna cokelat kekuningan yang diakibatkan oleh warna kitosan. Sementara mikrokapsul kosong terlihat kuning dan lebih transparan (Gambar 16d). Warna kuning tersebut berasal dari warna kitosan yang merupakan komponen terbesar mikrokapsul.
Gambar 16 juga menunjukkan bahwa ukuran mikrokapsul bergantung pada konsentrasi alginat dan CaCl2 yang digunakan.
Semakin tinggi konsentrasi alginat dan CaCl2
maka ukuran mikrokapsul semakin kecil karena ikatan yang terjadi semakin kuat. Hal tersebut didukung dengan data ukuran mikrokapsul setiap variasi menunjukkan bahwa mikrokapsul
dengan konsentrasi alginat 3% memilki ukuran mikrokapsul yang lebih kecil dibandingkan dengan alginat 1% dan alginat 2% (Tabel 3), data lengkapnya terdapat pada Lampiran 15.
(a) (b)
(c ) (d)
Gambar 16 Mikrokapsul kitosan-gom guar dengan konsentrasi alginat 1 (a), 2 (b), dan 3% (b/v) (c) (mikroskop foto stereo dengan perbesaran 11.25 kali, serta mikrokapsul kosong dengan konsentrasi alginat 2% (d) (kamera digital).
Tabel 3 Ukuran Mikrokapsul
Variasi Ukuran mikrokapsul ( m) Alginat 1%, CaCl2 0.05M 1075-2000 Alginat 1%, CaCl2 0.10M 1025-1975 Alginat 1%, CaCl2 0.15M 1125-2000 Alginat 2%, CaCl2 0.05M 775-1200 Alginat 2%, CaCl2 0.10M 700-1335 Alginat 2%, CaCl2 0.15M 625-1475 Alginat 3%, CaCl2 0.05M 725-1225 Alginat 3%, CaCl2 0.10M 725-1400 Alginat 3%, CaCl2 0.15M 750-1125
Berdasarkan hasil scoring, formula I dengan konsentrasi alginat 3% dan CaCl2
0.15 M menghasilkan mikrokapsul terbaik. Hasil pengamatan SEM terhadap formula tersebut menunjukkan bahwa mirokapsul kosong (Gambar 17a) dibandingkan dengan mikrokapsul ketoprofen tidak keriput dan lebih halus (Gambar 17b). Hal ini
disebabkan oleh telah terisinya ruang kosong di dalam mikrokapsul oleh ketoprofen.
(a)
(b)
Gambar 17 Foto SEM permukaan mikrokapsul tanpa (a) dan dengan penambahan ketoprofen (b) dengan perbesaran 50 kali.
Foto SEM terhadap mikrokapsul ketoprofen yang sama dengan perbesaran yang lebih tinggi menunjukkan adanya retakan yang dangkal di permukaan mikrokapsul (Gambar 18). Hal ini diakibatkan proses pengeringan mikrokapsul. Selain itu, terlihat serpihan halus di permukaan mikrokapsul yang diduga merupakan hasil tautan silang alginat dengan Ca2+.
Gambar 18 Foto SEM permukaan mikrokapsul kitosan-gom guar dengan alginat dengan perbesaran 1500 kali. Setelah disolusi asam maupun basa, mikrokapsul terlihat masih utuh dan disertai dengan pembengkakan ukuran. Akan tetapi, pembengkakan dalam medium asam lebih besar daripada dalam medium basa. Dalam medium asam, larutan dari medium akan mengalami penetrasi ke dalam mikrokapsul sehingga kitosan yang merupakan komponen utama mikrokapsul mengembang bahkan sebagian larut. Hal ini juga ditunjukkan dengan terjadinya perubahan warna medium asam menjadi kekuning-kuningan setelah disolusi asam. Namun, hal tersebut tidak terjadi pada
medium basa karena sifat dasar kitosan yang tidak larut dalam suasana basa.
Pengamatan foto SEM terhadap morfologi mikrokapsul setelah 180 menit disolusi asam memperlihatkan bahwa permukaan mikrokapsul tidak jauh berbeda dengan permukaan sebelum disolusi (Gambar 19a dan b). Hal tersebut dikarenakan lapisan terluar mikrokapsul, yaitu alginat tertaut silang Ca2+, tidak banyak
terpengaruh oleh pH asam. Lapisan alginat terlihat mengembang sebagai akibat desakan dari pembengkakan matriks kitosan-gom guar. Namun, lapisan tipis alginat tidak kuat menahan sehingga sebagian terlihat hancur sebagai serpihan di permukaan mikrokapsul.
(a)
(b)
(c)
Gambar 19 Foto SEM permukaan mikrokapsul ketoprofen sebelum disolusi (a), setelah disolusi asam (b), dan setelah disolusi basa (c) dengan perbesaran 1000 kali (inset serpihan alginat yang hancur). Gambar 19c memperlihatkan bahwa lapisan alginat telah hancur setelah disolusi basa karena tidak mirip dengan permukaan
sebelum disolusi. Hal ini didukung dengan pernyataan Ivanova et al. (2000) yang menyatakan bahwa bufer basa dapat merusak ikatan silang alginat-Ca2+ sehingga alginat
larut. Jadi, foto SEM tersebut merupakan permukaan dari matriks kitosan-gom guar. Disebabkan oleh lapisan alginat telah hancur, ketoprofen dapat dengan lebih mudah terlepas dari matriks kitosan-gom guar ketika kontak dengan medium basa. Pelepasan tersebut didukung dengan banyaknya lekukan sehingga luas permukaan yang kontak dengan medium juga lebih besar.
SIMPULAN DAN SARAN Simpulan
Pengaruh waktu terhadap pelepasan ketoprofen dalam medium asam untuk formula A, B, C, D, E, dan I mengikuti pendekatan model Korsmeyer-Peppas. Sementara formula F, G, dan H mengikuti model Higuchi. Pada medium basa, semua formula mengikuti model Korsmeyer-Peppas. Dari pendekatan kinetika ini, mekanisme pelepasannya melalui cara difusi.
Saran
Penelitian lebih lanjut mikroenkapsulasi perlu dilakukkan teknik pembuatan mikrokapsul yang lain dengan menggunakan
spray gun pada formula yang paling baik sehingga ukuran mikrokapsul lebih kecil. Penelitian selanjutnya perlu dilakukkan analisis transmisi mikroskop elektron (TEM) untuk melihat ketebalan mikrokapsul. Selain itu, modifikasi formula untuk penyalutan dengan kitosan-gom guar alginat perlu dilakukan agar matriks yang diperoleh dapat tahan asam lebih lama dan obat dapat keluar terkendali di medium basa. Selain itu, memperhatikan faktor pengenceran dalam uji disolusi. Pengujian disolusi dilakukan secara seri (dari lambung langsung ke usus), serta uji disolusi ketoprofen ketoprofen dilakukkan secara in vivo agar pengaruh pelepasan obat dapat diketahui secara pasti di dalam tubuh.
DAFTAR PUSTAKA
[AMA] American Medical Association. 1991.
Drug Evaluations. Ed ke-8.
[AOAC] Association of Official Analytical Chemists. 1999. Official methods of analysis of AOAC International. 5th Revisoin. Volume 2. Cunnif P, (Editor). Maryland: AOAC International.
Atkins PW. 1996. Kimia Fisik Jilid 2. Ed ke-4. Kartohadiprodjo, penerjemah; P.W. Indarto, editor. Jakarta: Erlangga. Terjemahan dari: Physical Chemistry. Bregni C et al. 2000. Alginate microspheres
of Bacillus substilis. Ars Pharm
41:245-248.
Berger J et al. 2004. Structure and interactions in covalently and ionically crosslinked chitosan hydrogels for biomedical applications.
Eur J Pharm Biopharm 57:193-194. Cardenas A, Monal WA, Goycoolea FM,
Ciapara IH, Peniche C. 2003. Diffusion through membranes of the polyelectrolyte complex of chitosan and alginate. Macromol Biosci 3:535-539.
Chaplin M. 2005. Alginate. London South Bank University. [terhubung berkala]. Http://chem.skku.ac.kr/~wkpark/tutor/ mirror/www.martin.chaplin.btinter.net .co.uk/hygua.html.
[Depkes] Departemen Kesehatan RI. 1995.
Farmakope Indonesia. Ed. ke-4. Jakarta: Depatemen Kesehatan RI. Dogra S, Dogra SK. 1990. Kimia Fisik dan
Soal-Soal. Mansyur U, Penerjemah. Jakarta: UI-Press.
Ferreira D et al. 2007. Alginate/chitosan nanoparticles are effective for oral insulin delivery. Pharmaceutical Res
24: 2198 —2206.
Friedli AC, Schlanger IR. 2005. Demonstrating encapsulation and release: A new take on alginate complexation and the nylon rope trick. J Chem Educ 82:1017-1020. George M, Abraham TE. 2006. Polyionic
hydrocolloids for the intestinal delivery of protein drugs: Alginate and chitosan — A review. Controlled Release 114:1–14.
Ivanova E, Chipeva V, Inanova I, Dousset X, Poncelet D. 2000. Encapsulation of lactic acid bacteria in calcium alginate
beads for bacteriocin production. J Cult Collections 3:53-58.
Jamaludin MA. 1994. Isolasi dan pencirian kitosan limbah udang windu (Penaeus monodon fabricus) dan afinitasnya terhadap ion logam Pb2+, Cr6+, dan Ni2+
[skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Kshirsagar NA. 2000. Drug delivery system.
Indian J Pharmacol 32:54-61.
Khan TA, Peh KK, Ch’ng HS. 2002. Reporting degree of deacetylation values of chitosan: The influence of analytical methods. J Pharm Pharmaceut Sci
5:205-212.
Kondo, Asaji. 1979. Microcapsule Processing & Technology. New York: Marcel Dekker.
Martin A. 1993. Physical Pharmacy. Ed. ke-4. Philadelphia: Lea & Febiger.
Martindale. 1982. The extra Pharmacopeia. Ed ke-28. London: The Pharmaceutical Pr. Min-Soo, Jeong-Soo, dan Sung-Joo H. 2007.
The effect of sodium alginate on physical and dissolution properties of surelease-matrix pellets prepares by a Novel Pelletizer. Chem Pharm Bull
55:1631—1634.
Motwani SK et al. 2007. Chitosan-sodium alginate nanoparticles as submicroscopic reservoir for ocular delivery: Formulation, optimization, and in vitro
characterization. Eur J Pharm Biophr am.
NataF, Sugita P, Sjachriza A, Arfin B. 2007. Diffusion behavior of ketoprofen through chitosan-guar gum gel membranes. Di dalam: Prosiding Seminar International Conference and Workshop on Basic Science and Applied Science: Improving Link Basic Science and Applied Science, Surabaya, 6−7 Agu 2007. Surabaya: Unair-RUG-KNAW-UTM, hlm.
Ouyang W et al. 2004. Artificial cell microcapsule for oral delivery of live bacterial cell for theraphy: Design,
preparation, and in-vitro
characterization. J Pharm Pharmaceut Sci 7:315-324.
Parfitt K, editor. 1999. Martindale: The Complete Drug Reference. Vol ke-2. Ed ke-32. London: Pharmaceutical Pr. Sakkinen M. 2003. Biopharmaceutical evaluation of microcrystalline chitosan as release-rate-controlling hydrophilic polymer in granules for gastro-retentive drug delivery [disertasi]. Helsinki: Department of Pharmacy, University of Helsinki. Sarvanan M et al. 2007. Hydroxypropyl
methylcellulose based cephalexin extended release tablets: Influence of tablet formulation, hardness and storage on in vitro release kinetics.
Chem Pharm Bull 51(8):978-983. Setyowati EV. 2008. Stabilitas obat anti
peradangan ketoprofen tersalut gel kitosan-gom guar [skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Siregar, Charles JP. 1986. Beberapa Aspek Pokok Pengujian Mutu Perbekalan Farmasi. Jakarta: Pusat Pemeriksaan Obat dan Makanan Nasional.
Shoaib MH et al. 2006. Evaluation of drug release kinetics from ibuprofen matrix tablets using HPMC. J. Pharm. Sci
19: 119-124.
Stevens MP. 2001. Kimia Polimer. Sopyan I, Penerjemah. Jakarta: Pradnya Paramita. Terjemahan dari: Polymer Chemistry: An Introduction.
Sugita P, Sjahriza A, Lestari SI. 2006a. Sintesis dan optimalisasi gel kitosan-gom guar. J Nature 9:32-36.
Sugita P, Sjahriza A, Rachmanita. 2006b. Sintesis dan optimalisasi gel kitosan-karboksimetilselulosa. Di dalam: Arifin B, Wukirsari T, Gunawan S, Wahyuni WT, editor. Prosiding Seminar Nasional Himpunan Kimia Indonesia. Bogor, 12 Sep 2006. Bogor: Departemen Kimia IPB-HKI Cabnag Banten. 437-443.
Sugita P, Sjahriza A, Wahyono D. 2006c. Sintesis dan optimalisasi gel kitosan-alginat. J Sains Teknol 8:133-137. Sugita P, Sjahriza A, Utomo DW. 2007a.
Optimization synthesis chitosan-xanthan gum gel for metal adsorption. Prosiding 1st International Conference on
Chemical Science MAT/33-4.
Sugita P, Srijanto B, Amelia F, Arifin B, Wukirsari T. 2007b. Perilaku disolusi ketoprofen tersalut gel kitosan-gom guar.
JSChem, in press.
Sutriyo, Joshita D, Indah R. 2005. Perbandingan pelepasan propranonol hidroklorida dari matriks kitosan, etil selulosa, dan hidroksipropil metil selulosa. Maj Ilmu Kefarmasian 2: 145-153.
Tarbojevich M, Cosani A. 1996. Molecular weight determination of chitin and chitosan. Di dalam: Muzarelli RAA, Peter MG, Editor. 1997. Chitin Handbook. Ancona: European Chitin Society 85-108.
Tarirai C. 2005. Cross-linked chitosan matrix system for sustained drug release [tesis]. Tshware: Faculty of Health Science, Tshwane University of Technology. Tian-Wei, Hu B, Xian-Hua, Zhang M. 2003.
Release behaviour of Ketoprofen from chitosan/alginate microcapsules. J Bioactive and Compatible Polymer. Vol 18: 207.
Timmy et al. 2002. Betacyclodextrin complexed insulin loaded alginate microsphere oral delivery system. Trend Biomater Arti Organs 15:48-53.
Tiyaboonchai W, Ritthidej GC. 2003. Development of indomethacin sustained release microcapsules using chitosan-carboxymethylcellulose complex coacervation. Songklanakarin J Sci Technol 25:245-254.
Ul-Ain Q, Sharma S, Khuller GK, Grag SK. 2003. Alginate-bassed oral delivery system for tuberculosis pharmacokinetics and therapeutics effects. J Antimico rb Chemothera 51:931-938.
[USP] United States Pharmacopoeia. 2003.
US Pharmacopeia 2003. Maryland: The United States Pharmacopeial Convention.
Varma
MVK,
Hermamalini K. 2007. Comparative studies on the dissolutiom profile of flubriprofen from coated and uncoated alginate microspheres. Pharmacology 2:187-202.Wang T, Turhan M, Gunasekaram S. 2004. Selected properties of pH-sensitive, biodegradable chitosan-poly(vinyl alcohol) hydrogel. Polym Int 53:911-918
Yamada T, Onishi H, Machida Y. 2001. In vitro and in vivo evaluation of sustained release chitosan-coated ketoprofen microparticles. Yakugaku Zasshi 121:239-245.
Yoshizawa H. 2004. Trends in microencapsulation reseach. KONA
20. [terhubung berkala]. http.// www.kona.or.jp/search/22_023.pdf [22 Sep 2005].
Yundhana Y. 2008. Perilaku disolusi ketoprofen tersalut gel kitosan-CMC. [skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Lampiran 1 Penentuan kadar air kitosan dan mikrokapsul (AOAC 1999)
Penentuan kadar air kitosan dilakukan dengan metode gravimetri. Sebanyak
±
1.0000 g kitosan dimasukkan ke dalam cawan porselen yang telah diketahui bobotnya, kemudian cawan beserta isinya dimasukkan ke dalam oven dengan suhu 105 oC selama 3 jam. Setelah itu,dimasukkan ke dalam desikator dan ditimbang. Kadar air kitin/kitosan dihitung dengan persamaan
Kadar air = bobot sampel awal – bobot sample kering x 100% bobot sampel awal
Lampiran 2 Analisis Kadar Abu kitosan (AOAC 1999)
Penentuan kadar abu kitosan dilakukan dengan metode gravimetri. Cawan porselen dibersihkan dan dimasukkan ke dalam tanur untuk menghilangkan sisa-sisa kotoran yang menempel dalam cawan, kemudian didinginkan dalam desikator dan ditimbang. Sebanyak ± 0.5000 g kitosan dimasukkan ke dalam cawan tersebut dan dibakar dalam tanur pengabuan dengan suhu 600oC sampai diperoleh abu berwarna putih. Setelah itu, cawan beserta isinya dimasukkan ke
dalam desikator dan ditimbang. Kadar abu kitosan dihitung dengan persamaan
Kadar abu = bobot abu x 100% bobot sampel
Data hasil pengukuran kadar air dan kadar abu kitosan Kadar air dan kadar abu kitosan
Ulangan ke- Sampel Kadar air (%) Kadar abu (%) 1 Kitosan 1 7.76 0.08 2 Kitosan 2 7.31 0.14 3 Kitosan 3 7.43 0.12 Rerata 7.50 0.11 Data hasil pengukuran kadar air mikrokapsul
Perlakuan Kadar air % Alginat CaCl2 (M) 3% 0.15 13.91 3% 0.10 17.43 3% 0.05 24.79 2% 0.15 25.84 2% 0.10 18.14 2% 0.05 16.24 1% 0.15 23.36 1% 0.10 14.73 1% 0.05 14.48
Lampiran 3 Penentuan Bobot Molekul Kitosan (Tarbojevich & Cosani 1996)
Bobot molekul kitosan ditentukan dengan menggunakan metode viskometer. Sebanyak kira-kira 0.1000 g kitosan dilarutkan dalam 100 mL asam asetat 0.5 M, kemudian diambil sebanyak 5 ml dan dimasukkan ke dalam viskometer Ostwald-Cannon-Fenske untuk ditentukan waktu alirnya. Pengukuran juga dilakukan untuk beberapa konsentrasi kitosan dan waktu alir dibaca sebanyak tiga kali pengulangan dengan tiga titik pengambilan.
Contoh perhitungan :
Waktu alir larutan kitosan Sampel 1 Konsentrasi Waktu (detik) Rerata
0.00 62.93 63.01 62.90 63.19 0.02 66.75 66.61 66.54 66.55 0.04 71.46 71.52 71.56 71.55 0.06 76.92 77.09 77.24 77.10 0.08 82.39 82.53 82.68 82.52 0.10 87.96 87.93 88.07 87.77
Kemudian dibuat kurva hubungan antara ηsp/c dengan c sehingga diperoleh persamaan:
lnηsp/c =ln [η] + k’ [η]2 c
y a b x
Kurva pene ntuan bobot m olek ul sam pel 1
y = 3.9429x + 1.0255 R2 = 0.8712 0 0.5 1 1.5 0 0.02 0.04 0.06 0.08 0.1 0.12 k onsentrasi ln ( n sp /c )
Hubungan konsentrasi larutan kitosan (%) dengan ln ln ηsp /C Bobot molekul kitosan dihitung dengan menggunakan persamaan Mark-Houwink: Viskositas relatif ηr = η/ηo≅t/to Viskositas spesifik ηsp =ηr -1 Viskositas intrinsik [η] = (ηsp/c)c=0 η = KMα dengan K = 3.5 x 10-4 mL/g α = 0.76
t0 = waktu alir pelarut
η = viskositas zat
η0 = viskositas pelarut
M = bobot molekul zat
Dengan menggunakan mode regresi linear diperoleh persamaan: ln ηsp/c =ln [η]+k’[η]2c sama dengan y = 3.9429 x + 1.0255
untuk rumus [η] = KMα, maka 3.9429 = 3.5 × 10-4 × M0.76
sehingga diperoleh M = 63.1553 x 105 g/mol
Kisaran bobot molekul kitosan adalah (24.3894 x 105 - 63.1553 x 105) g/mol
Lampiran 4 Penentuan derajat deasetilasi kitosan (Khan et al. 2002)
Penentuan derajat deasetilasi kitosan, digunakan FTIR. Kitosan yang diperoleh dibuat pelet dengan KBr 1%, kemudian dilakukan penyusuran pada daerah frekuensi antara 4000 cm-1
dan 400 cm-1. Derajat deasetilasi ditentukan dengan metode garis dasar.
Puncak tertinggi dicatat dan diukur dari garis dasar yang dipilih. Nilai absorbans dapat dihitung dengan menggunakan rumus
P
P
A
=
log
0P0= % transmitans pada garis dasar
P = % transmitans pada puncak minimum
Kitin yang terdeasetilasi sempurna (100%) memiliki nilai A1655 = 1.33. Dengan membandingkan
absorbans pada bilangan gelombang 1655 cm-1 (serapan pita amida I) dengan absorbans pada
bilangan gelombang 3450 cm-1 (serapan gugus hidroksil), % derajat deasetilasi dapat dihitung
dengan persamaan
%
100
33
.
1
1
1
%
3450 1655×
×
−
=
A
A
DD
Spektrum FTIR dan derajat deasetilasi kitin dan kitosan
Spektrum FTIR kitosan Derajat deasetilasi kitosan dicari dengan rumus:
A = log
P Po
dimana: Po = % transmitansi pada garis dasar
P = % transmitansi pada puncak minimum
A = absorbansi % DD = 1 –
1
100
%
33 , 1 3450 1655×
×
A Adimana: A1655 = absorbansi pada bilangan gelombang 1655 cm -1 (serapan pita amida)
A3450 = absorbansi pada bilangan gelombang 3450 cm -1 (serapan gugus hidroksil)
A1655 = log
8105
.
1
5615
.
7
= 0.6208 A3450 = log1597
.
0
65
.
10
= 1.8239 % DD = − ) 33 , 1 1 8239 . 1 6208 . 0 ( 1 x x 100 % = 74.41 %Lampiran 5 Diagram alir penelitian
Larutan Ketoprofen dalam etanol
Pembuatan campuran kitosan-gom guar, kitosan 1.75 % (b/v) dalam asam asetat 1% (b/b), gom guar 0.35% (b/v), dan glutaraldehida 3.75% (v/v)
Larutan ketoprofen tersalut kitosan-gom guar dengan alginat
0.5 ml Tween 80 2%
Penyalutan Rangkap
Larutan ketoprofen tersalut kitosan-gom guar dimasukan ke dalam
syiringe 23 G, lalu diteteskan ke dalam larutan alginat dengan konsentrasi 1, 2, dan 3% (b/v) , disaring, selanjutnya dicelupan ke dalam larutan CaCl2 dengan konsentrasi 0.05, 0.1, dan 0.15% (b/v)
Pencirian mikrokapsul dengan mikroskop elektron
Kadar air mikrokapsul
R2 terbesar
Pengeringan di dalam oven dengan suhu 40ºC
Presetase ketoprofen yang tersalut persatuan bobot mikrokapsul
% pelepasan sedikit dalam medium asam selama 3 jam dan terbanyak
selama 6 jam
Scoring parameter Ekstraksi dengan NaOH 0.1M dan diukur dengan UV pada 257
nm
Produk mikrokapsul
Uji Disolusi Secara In Vitro
(konsentrasi ketoprofen diukur dengan spektrofotometer UV 258,5 nm untuk cairan lambung dan 260.5 nm untuk cairan