BAB I BAB I
FUNGSIONALISASI DAN INTERKONVERSI FUNGSIONALISASI DAN INTERKONVERSI
GUGUS FUNGSI GUGUS FUNGSI
Salah satu aspek penting dalam sintesis adalah memasukkan gugus fungsi Salah satu aspek penting dalam sintesis adalah memasukkan gugus fungsi kedalam suatu molekul dan interkonversi gugus fungsi. Molekul target terkadang kedalam suatu molekul dan interkonversi gugus fungsi. Molekul target terkadang mengandung gugus fungsi yang sulit pada posisi tertentu, sehingga gugus fungsi mengandung gugus fungsi yang sulit pada posisi tertentu, sehingga gugus fungsi tersebut harus disiapkan dari awal. Gugus fungsi yang disiapkan bisa dalam bentuk tersebut harus disiapkan dari awal. Gugus fungsi yang disiapkan bisa dalam bentuk sudah jadi maupun dalam bentuk gugus fungsi tertentu yang kemudian diubah selama sudah jadi maupun dalam bentuk gugus fungsi tertentu yang kemudian diubah selama proses
proses sintesis sintesis menjadi menjadi bentuk bentuk yang yang diinginkan diinginkan melalui melalui serangkaian serangkaian interkonversiinterkonversi gugus fungsi.
gugus fungsi.
1.1 FUNGSIONALISASI ALKANA 1.1 FUNGSIONALISASI ALKANA
Sudah dikenal luas bahwa alkana tidak reaktif terhadap reagen elektrofilik dan Sudah dikenal luas bahwa alkana tidak reaktif terhadap reagen elektrofilik dan nukleofilik. Alkana dapat mengalami halogenasi melalui mekanisme reaksi radikal. nukleofilik. Alkana dapat mengalami halogenasi melalui mekanisme reaksi radikal. Namun,
Namun, reaksi inreaksi ini tidak i tidak banybanyak membantu ak membantu karena reaksi karena reaksi radikal sulradikal sulit dit dikontrol. ikontrol. ReaksiReaksi brominasi
brominasi lebih lebih selektif selektif dibandingkan reaksi dibandingkan reaksi klorinasi klorinasi karena karena kereaktifan kereaktifan BrBr •• lebihlebih
rendah. 2-bromo-2-metilpropana secara eksklusif terbentuk bila
rendah. 2-bromo-2-metilpropana secara eksklusif terbentuk bila isobutana direaksikanisobutana direaksikan dengan gas bromin pada temperatur 300
dengan gas bromin pada temperatur 30000 C, sedangkan reaksinya dengan gas klorin C, sedangkan reaksinya dengan gas klorin akan menghasilkan campuran 1-kloro dan 2-kloro-2-metilpropana dengan rasio 2 : 1, akan menghasilkan campuran 1-kloro dan 2-kloro-2-metilpropana dengan rasio 2 : 1, seperti terlihat pada persamaan reaksi berikut :
seperti terlihat pada persamaan reaksi berikut :
Skema 1.1 Skema 1.1 CH CH33 CC CH CH33 H H CH CH33 CH CH33 CC CH CH33 Br Br CH CH33 CH CH33 CC CH CH33 Cl Cl CH CH33 CH CH33 CC CH CH22 H H CH CH33 Cl Cl + + Br Br 22 Cl Cl22 300 30000 300 30000
1.2 FUNGSIONALISASI ALKENA 1.2 FUNGSIONALISASI ALKENA
Tidak seperti alkana, alkena memiliki dua sisi aktif dapat dimanfaatkan dalam Tidak seperti alkana, alkena memiliki dua sisi aktif dapat dimanfaatkan dalam proses fungsionalisasi
proses fungsionalisasi dengan tingkat dengan tingkat spesifikasi spesifikasi yang tinggi. yang tinggi. Fungsionalisasi alkenaFungsionalisasi alkena dapat terjadi pada karbon yang berikatan rangkap (C = C) dan pada karbon tetangga dapat terjadi pada karbon yang berikatan rangkap (C = C) dan pada karbon tetangga dari karbon berikatan rangkap (posisi allilik).
dari karbon berikatan rangkap (posisi allilik).
Reaksi kimia alkena dengan suatu elektrofil yang terjadi pada karbon ikatan Reaksi kimia alkena dengan suatu elektrofil yang terjadi pada karbon ikatan rangkap telah menjadi perhatian sejak lama. Ikatan rangkap alkena dapat diubah rangkap telah menjadi perhatian sejak lama. Ikatan rangkap alkena dapat diubah menjadi epoksida, diol, atau asam karboksilat melalui proses oksidasi tergantung jenis menjadi epoksida, diol, atau asam karboksilat melalui proses oksidasi tergantung jenis oksidator yang digunakan. Selain itu, ikatan rangkap alkena dapat diaddisi oksidator yang digunakan. Selain itu, ikatan rangkap alkena dapat diaddisi menghasilkan berbagai macam produk seperti alkana, alkohol, alkilhalida, halohidrin menghasilkan berbagai macam produk seperti alkana, alkohol, alkilhalida, halohidrin dan sebagainya. Produk addisinya-pun memiliki keragaman sesuai dengan mekanisme dan sebagainya. Produk addisinya-pun memiliki keragaman sesuai dengan mekanisme yang dilalui. Addisi alkena ada yang melalui mekanisme karbokation, karbokation yang dilalui. Addisi alkena ada yang melalui mekanisme karbokation, karbokation berjembatan,
berjembatan, radikal, radikal, dan dan addisi addisi yang yang berlangsung berlangsung serempak. serempak. Mekanisme Mekanisme reaksireaksi alkena ini telah dibahas pada materi kuliah Kimia Organik I, dan skema reaksinya alkena ini telah dibahas pada materi kuliah Kimia Organik I, dan skema reaksinya dapat dirangkum sebagai berikut.
dapat dirangkum sebagai berikut.
Skema 1.2 Skema 1.2 CH CH33 CCHH CCHH22 Oksidasi Oksidasi CH CH33 CCOOOOHH + + CCOO22 CH CH33CH(OH)CHCH(OH)CH22OHOH CH CH33 CCHH CCHH22 O O CH CH33 CHCH22 CHCH33 Hidrogenasi katalitik Hidrogenasi katalitik X
X22 atau HXO atau HXO
CH CH33 CCHH CCHH22 X X XX CH CH33 CCHH CCHH22 O OHH XX CH CH33 CCHH CCHH33 Y Y addisi asam addisi asam lemah lemah HY / H HY / H++ Y = OH, CH
Y = OH, CH33COOCOO --addisi addisi radikal radikal HB HBr r CH CH33 CHCH22 CHCH22Br Br addisi asam addisi asam kuat (HX) kuat (HX) CH CH33 CCHH CCHH33 X X X =Cl, Br, I, X =Cl, Br, I, CF CF33COCOOO --HS HSOO44 --addisi addisi H H22O melaluiO melalui Hidoborasi Hidoborasi CH CH33 CHCH22 CHCH22OHOH
1.3 FUNGSIONALISASI ALKUNA 1.3 FUNGSIONALISASI ALKUNA
Sifat kimia alkuna lazimnya tertuju pada kereaktifannya terhadap elektrofil Sifat kimia alkuna lazimnya tertuju pada kereaktifannya terhadap elektrofil dandan kemampuannya alkuna terminal bertindak sebagai asam lemah, yang sangat berguna kemampuannya alkuna terminal bertindak sebagai asam lemah, yang sangat berguna pada
pada pembentukan pembentukan ikatan ikatan karbon-karbon. karbon-karbon. Disamping Disamping itu, itu, transformasi transformasi suatu suatu alkunaalkuna menjadi senyawa karbonil (keton) sangatlah penting dalam sintesis organik.
menjadi senyawa karbonil (keton) sangatlah penting dalam sintesis organik.
Skema 1.3 Skema 1.3
1.4 FUNGSIONALISASI HIDROKARBON AROMATIK 1.4 FUNGSIONALISASI HIDROKARBON AROMATIK
Reaksi kharakteristik dari benzena adalah reaksi substitusi elektrofilik. Reaksi Reaksi kharakteristik dari benzena adalah reaksi substitusi elektrofilik. Reaksi ini telah digunakan secara
ini telah digunakan secara luas untuk memasukkan suatu gugus fungsi kedalam cincinluas untuk memasukkan suatu gugus fungsi kedalam cincin benzena,
benzena, seperti seperti reaksi reaksi alkilasi alkilasi dan dan asilasi asilasi Friedel-Craft, Friedel-Craft, halogenasi, halogenasi, sulfonasi, sulfonasi, dandan nitrasi.
nitrasi.
Adanya gugus fungsi pada cincin benzena akan mempengaruhi reaktifitas Adanya gugus fungsi pada cincin benzena akan mempengaruhi reaktifitas cincin benzena. Gugus penarik elektron akan menurunkan reaktifitas cincin terhadap cincin benzena. Gugus penarik elektron akan menurunkan reaktifitas cincin terhadap elektrofil, bahkan bisa berubah menjadi reaktif terhadap nukleofil. Sebaliknya, gugus elektrofil, bahkan bisa berubah menjadi reaktif terhadap nukleofil. Sebaliknya, gugus pendorong el
pendorong elektron ektron akan akan meningkatkan meningkatkan reaktifitas reaktifitas cincin cincin terhadap terhadap elektrofil. elektrofil. SelainSelain mempengaruhi reaktifitas cincin terhadap elektrofil dan nukleofil, adanya substituen mempengaruhi reaktifitas cincin terhadap elektrofil dan nukleofil, adanya substituen (suatu gugus fungsi) juga akan mengarahkan reaktifitas cincin pada reaksi sela
(suatu gugus fungsi) juga akan mengarahkan reaktifitas cincin pada reaksi sela njutnya.njutnya. Oleh karena itu, jika molekul target merupakan senyawa aromatik yang mengandung Oleh karena itu, jika molekul target merupakan senyawa aromatik yang mengandung substituen lebih dari satu, urutan fungsionalisasi yang dilakukan patut dipikirkan substituen lebih dari satu, urutan fungsionalisasi yang dilakukan patut dipikirkan secara seksama. Fungsionalisasi benzena selengkapnya dirangkum pada
secara seksama. Fungsionalisasi benzena selengkapnya dirangkum pada Skema 1.4Skema 1.4
R
R CC CCHH
CH
CH33 CHCH22 CHCH33 Hidrogen
Hidrogenasi asi katalitikkatalitik
Basa Basa Br Br 22 R R CC CCHH33 O O H H22O/HO/H++ Hg HgOO CH CH33 CCHH CCHH22 B Brr BBr r R R CC CC --CH CH33 CCHH CCHH22 atau atau
Skema 1.4 Skema 1.4
Tabel 1.1
Tabel 1.1 Orientasi dan Kecepatan Reaksi Substitusi Elektrofilik pada Benzena Orientasi dan Kecepatan Reaksi Substitusi Elektrofilik pada Benzena Tersubstitusi
Tersubstitusi Substituen
Substituen Orientasi Orientasi SubstitusiSubstitusi Elektrofilik Elektrofilik Kecepatan Reaksi Kecepatan Reaksi Substitusi Relatif Substitusi Relatif terhadap Benzena terhadap Benzena Aril atau alkil
Aril atau alkil o -, p -o -, p - cepatcepat –
– OH, OH, – – OR OR o -, p -o -, p - cepatcepat –
– NH NH22,, – – NHR, NHR, – – NR NR 22 o -, p -o -, p - cepatcepat Halogen
Halogen o -, p -o -, p - sama sama / / lebih lebih lambatlambat Karbonil
Karbonil m -m - lebih lebih lambatlambat
–
– C C N N m -m - lebih lebih lambatlambat –
– NO NO22 m -m - lebih lebih lambatlambat –
– SO SO33HH m -m - lebih lebih lambatlambat –
– CF CF33 m -m - lebih lebih lambatlambat
X X22 / FeX/ FeX33 halogenasi halogenasi X X HNO HNO33 / H / H22SOSO44 nitrasi nitrasi NO NO22 RCOCl RCOCl AlCl AlCl33 Friedel-Craft Friedel-Craft COR COR reduksi reduksi CH CH22 -R -R RCl RCl AlCl AlCl33 Friedel-Craft Friedel-Craft R R D D22SOSO44 pertukaran pertukaran hidrogen hidrogen D D Ar Ar Ar Ar
.
.
SO SO33 sulfonasi sulfonasi H H22SOSO44 SO SO33HH1.5 INTERKONVERSI GUGUS FUNGSI 1.5 INTERKONVERSI GUGUS FUNGSI
Pada bahasan sebelumnya, telah dibicarakan cara memasukan suatu gugus Pada bahasan sebelumnya, telah dibicarakan cara memasukan suatu gugus fungsi pada suatu molekul. Namun terkadang gugus fungsi tertentu tidak dapat fungsi pada suatu molekul. Namun terkadang gugus fungsi tertentu tidak dapat dimasukkan secara langsung, melainkan melalui gugus fungsi tertentu yang dimasukkan secara langsung, melainkan melalui gugus fungsi tertentu yang selanjutnya diubah menjadi gugus fungsi yang diinginkan. Langkah-langkah yang selanjutnya diubah menjadi gugus fungsi yang diinginkan. Langkah-langkah yang dilakukan untuk mengubah gugus fungsi yang tersedia menjadi gugus fungsi yang dilakukan untuk mengubah gugus fungsi yang tersedia menjadi gugus fungsi yang diinginkan (sesuai dengan molekul target) disebut
diinginkan (sesuai dengan molekul target) disebut Interkonversi Gugus FungsiInterkonversi Gugus Fungsi (lazim disingkat
(lazim disingkat IGFIGF).).
1.5.1 Transformasi Gugus Hidroksil 1.5.1 Transformasi Gugus Hidroksil
Alkohol merupakan basa lemah yang mampu bertindak sebagai nukleofil. Alkohol merupakan basa lemah yang mampu bertindak sebagai nukleofil. Alkohol bereaksi dengan klorida asam atau anhidrida asam menghasilkan ester. Ion Alkohol bereaksi dengan klorida asam atau anhidrida asam menghasilkan ester. Ion alkoksida adalah nukleofil kuat yang dapat bereaksi dengan alkilhalida, sulfonat, dan alkoksida adalah nukleofil kuat yang dapat bereaksi dengan alkilhalida, sulfonat, dan sulfat membentuk eter. Pada rea
sulfat membentuk eter. Pada reaksi yang menggunakan alkilhalida sekunder dan tersierksi yang menggunakan alkilhalida sekunder dan tersier sebagai pereaksi,
sebagai pereaksi, produk subproduk substitusi akan bstitusi akan bersaing dengan ersaing dengan produk eliminasi.produk eliminasi.
Alkilhalida dapat disintesis dari alkohol menggunakan reagen tionilklorida Alkilhalida dapat disintesis dari alkohol menggunakan reagen tionilklorida untuk klorida, HBr panas atau
untuk klorida, HBr panas atau PBr PBr 33 untuk bromida, dan I untuk bromida, dan I22 atau re atau red fosfor untuk iodida.d fosfor untuk iodida. Pembuatan tersier halida memerlukan kondisi yang lunak untuk mencegah terjadinya Pembuatan tersier halida memerlukan kondisi yang lunak untuk mencegah terjadinya proses eliminasi.
proses eliminasi.
Dehidrasi alkohol menghasilkan alkena dalam kondisi asam Bronsted dan Dehidrasi alkohol menghasilkan alkena dalam kondisi asam Bronsted dan asam Lewis. Asam kuat akan menghasilkan produk eliminasi Zaytzeff lebih banyak asam Lewis. Asam kuat akan menghasilkan produk eliminasi Zaytzeff lebih banyak melalui mekanisme E
melalui mekanisme E11..
Fenol merupakan alkohol aromatik. Fenol dapat mengalami alkilasi dan
Fenol merupakan alkohol aromatik. Fenol dapat mengalami alkilasi dan asilasiasilasi melalui mekanisme yang identik dengan alkohol. Arilmetil eter lazimnya dibuat melalui mekanisme yang identik dengan alkohol. Arilmetil eter lazimnya dibuat melalui reaksi fenol dengan diazometan. Proses transformasi alkohol dan fenol melalui reaksi fenol dengan diazometan. Proses transformasi alkohol dan fenol selengkapnya terlihat pada
Skema 1.5 Skema 1.5
1.5.2 Transformasi Gugus Amino 1.5.2 Transformasi Gugus Amino
Gugus amino bersifat basa dan mampu bertindak sebagai nukleofil terhadap Gugus amino bersifat basa dan mampu bertindak sebagai nukleofil terhadap alkilhalida menghasilkan amina sekunder, tersier, dan garam amonium kuaterner. alkilhalida menghasilkan amina sekunder, tersier, dan garam amonium kuaterner. Sementara reaksinya dengan klorida asam dan anhidrida asam akan menghasilkan Sementara reaksinya dengan klorida asam dan anhidrida asam akan menghasilkan amida. Untuk amina alifatik, reaksi amina primer sedikit dimanfaatkan karena akan amida. Untuk amina alifatik, reaksi amina primer sedikit dimanfaatkan karena akan menghasilkan produk yang kompleks (campuran produk) kecuali produk eliminasi. menghasilkan produk yang kompleks (campuran produk) kecuali produk eliminasi. Sifat kimia amina selengkapnya terlihat pada
Sifat kimia amina selengkapnya terlihat pada Skema 1.6Skema 1.6
H H OHOH H H XX H H OOCCOORR H H OROR O O RCOCl RCOCl R(CO) R(CO)22OO R' R'33NN H H++ Asam Asam LewLewisis
H H++ OH OH --(RO) (RO)22SOSO22 RX RX O O H H O O ArO ArOHH (RO) (RO)22SOSO22 RX / OH RX / OH --(RO) (RO)22OO RCOCl RCOCl R' R'33NN CH CH22NN22 ArO ArORR ArO ArOCHCH33 ArO ArOCORCOR
Skema 1.6 Skema 1.6 R R NHNH22 R'Cl R'Cl ArSO ArSO22ClCl RNHCOR' RNHCOR' R'COCl R'COCl (R'CO) (R'CO)22OO RNHSO
RNHSO22 Ar Ar RXRX
RNHR' RNHR' RNR' RNR'22 RNR'RNR'33++ClCl --HONO HONO RR'NNO RR'NNO reduksi reduksi RR'NNH RR'NNH22 R'Cl R'Cl R'Cl R'Cl Ar Ar NHNH22 R RClCl Ar 'SO Ar 'SO22ClCl ArN ArNHCOHCORR (RCO) (RCO)22OO ArN
ArNHSOHSO22 Ar ' Ar '
ArN ArNHRHR ArN
ArNRR22 ArN ArNRR33++ClCl
--HONO HONO ArR ArRNNNNOO reduksi reduksi ArR ArRNNNNHH22 RCOCl RCOCl RCl RCl RCl RCl HONO HONO Senyawa
Senyawa CC-nitroso-nitroso
ArN
ArN22++HSOHSO44 --NaNO NaNO22 H H22SOSO44 PhOH PhOH OH OH --OH OH ArN ArN22 lar. berair lar. berair dipanaskan
dipanaskan ArOH ArOH H H33POPO22 ArH ArH Cu Cu22XX22 HX HX ArX [ ArX [ X = X = Cl, Cl, Br ]Br ] KI KI Ar I Ar I NaBF NaBF44 KCN KCN Cu Cu22(CN)(CN)22 OH OH --Ph PhHH Ph - Ar Ph - Ar Ar Ar - CN- CN ArN ArN22++BFBF44 --pirolisis pirolisis NaNO NaNO22 Ar - Ar - FF Ar - Ar - NONO22
1.5.3 Transformasi Senyawa Halogen 1.5.3 Transformasi Senyawa Halogen
Halogen merupakan gugus pergi yang baik pada reaksi substitusi nukleofilik. Halogen merupakan gugus pergi yang baik pada reaksi substitusi nukleofilik. Halogen juga penarik elektron yang kuat sehingga menciptakan dipol pada molekul Halogen juga penarik elektron yang kuat sehingga menciptakan dipol pada molekul terutama terhadap atom karbon terdekatnya. Oleh karena itu, alkihalida banyak terutama terhadap atom karbon terdekatnya. Oleh karena itu, alkihalida banyak dimafaatkan dalam reaksi substitusi
dimafaatkan dalam reaksi substitusi nukleofilik. Reaksi alkilhalida dengan alkohol dannukleofilik. Reaksi alkilhalida dengan alkohol dan amina telah dipelajari sejak lama. Reaksi alkilhalida sekunder akan menghasilkan amina telah dipelajari sejak lama. Reaksi alkilhalida sekunder akan menghasilkan campuran produk substitusi dan eliminasi. Sementara alkilhalida tersier hanya campuran produk substitusi dan eliminasi. Sementara alkilhalida tersier hanya menghasilkan produk eliminasi.
menghasilkan produk eliminasi.
Alkilhalida dapat dihidrolisis dengan natrium hidroksida menghasilkan Alkilhalida dapat dihidrolisis dengan natrium hidroksida menghasilkan alkohol, tetapi untuk halida sekunder dan tersier akan terjadi persaingan dengan alkohol, tetapi untuk halida sekunder dan tersier akan terjadi persaingan dengan produk
produk eliminasi. Produeliminasi. Produk ek eliminasi akan liminasi akan dominan dominan bila dbila digunakan igunakan basa kuat basa kuat dan dan pelarutpelarut nonpolar pada temperatur tinggi. Produk eliminasinya biasanya mematuhi peraturan nonpolar pada temperatur tinggi. Produk eliminasinya biasanya mematuhi peraturan Zaytzeff.
Zaytzeff.
Alkilhalida bereaksi dengan logam tertentu membentuk senyawa alkil logam. Alkilhalida bereaksi dengan logam tertentu membentuk senyawa alkil logam. Yang banyak digunakan dalam sintesis diantaranya reagen Grignard (RMgX) dan Yang banyak digunakan dalam sintesis diantaranya reagen Grignard (RMgX) dan turunan alkil-litium. Transformasi senyawa halogen terangkum pada
turunan alkil-litium. Transformasi senyawa halogen terangkum pada Skema 1.7Skema 1.7
H H ClCl H H OROR H H LiLi H H MMggCCll Li Li RS RS --RN RNHH22 eter eter Mg Mg H H SRSR OR OR --+ + H H NNHHRR + + HH NRNR H H CN CN --H H CNCN H H CC C+ C+
1.5.4 Transformasi Senyawa Nitro 1.5.4 Transformasi Senyawa Nitro
Senyawa nitro alifatik le
Senyawa nitro alifatik lebih jarang digunakan dalam sintesis bila dibandingkanbih jarang digunakan dalam sintesis bila dibandingkan dengan senyawa nitro aromatik. Senyawa nitro alifatik dapat menghasilkan
dengan senyawa nitro aromatik. Senyawa nitro alifatik dapat menghasilkan karbanionkarbanion yang stabil pada atom karbon terdekatnya. Sementara senyawa nitro aromatik sangat yang stabil pada atom karbon terdekatnya. Sementara senyawa nitro aromatik sangat berguna
berguna untuk untuk sintesis sintesis senyawa-senyawa senyawa-senyawa aromatik aromatik yang yang mengandung mengandung atom atom N N dandan senyawa lainya yang dapat dibuat melalui proses transformasi gugus fungsi dari nitro. senyawa lainya yang dapat dibuat melalui proses transformasi gugus fungsi dari nitro.
Skema 1.8 Skema 1.8
1.5.5 Transformasi Aldehid dan Keton 1.5.5 Transformasi Aldehid dan Keton
Aldehid dan keton dapat mengalami proses oksidasi dan re
Aldehid dan keton dapat mengalami proses oksidasi dan re duksi sebagai akibatduksi sebagai akibat reaktivitas karbon karbonilnya sebagai elektrofil. Dalam sintesis, seringkali dijumpai reaktivitas karbon karbonilnya sebagai elektrofil. Dalam sintesis, seringkali dijumpai reaksinya dengan alkohol pada suasana asam membentuk hemi-asetal, hemi-ketal, reaksinya dengan alkohol pada suasana asam membentuk hemi-asetal, hemi-ketal, asetal dan ketal. Reaksi ini bersifat reversibel dan banyak dimanfaatkan pada proses asetal dan ketal. Reaksi ini bersifat reversibel dan banyak dimanfaatkan pada proses melindungi gugus karbonil dalam suatu proses reaksi (kemoselektivitas). Selain melindungi gugus karbonil dalam suatu proses reaksi (kemoselektivitas). Selain alkohol, tioalkohol juga dapat digunakan pada proses ini.
alkohol, tioalkohol juga dapat digunakan pada proses ini.
Skema 1.9 Skema 1.9
H H22SOSO44
ArN
ArN++=NAr =NAr
ArN
ArNHNHNHAHAr r Z Znn NaOH NaOH CF CF33COCO33HH As As22OO33 NaOH NaOH ArN ArNOO22 berair berair ArN ArNHH22 O O -- ArN
ArN22++ ArN ArNOO
ArN ArNHOHOHH NH NH44ClCl Zn Zn K K22CRCR22OO77 Zn Zn NaOH NaOH MeOH MeOH ArN ArN = = NANAr r ArN ArNHH22 Zn Zn NaOH
NaOH berair berair
O O RO ROHH H H++ H H22OO HOHO RO RO RO RO RO RO H H++ H H22OO + ROH + ROH - ROH - ROH
1.5.6 Transformasi Asam Karboksilat
1.5.6 Transformasi Asam Karboksilat dan Turunannyadan Turunannya
Asam karboksilat bisa diubah menjadi ester melalui reaksi dengan alkohol Asam karboksilat bisa diubah menjadi ester melalui reaksi dengan alkohol yang dikatalis asam. Khusus untuk meti
yang dikatalis asam. Khusus untuk metil ester, lal ester, lazimnya digunakan diazometan. Untukzimnya digunakan diazometan. Untuk ester yang lebih kompleks, reaksi alkohol dengan halida asam dan anhidrida asam ester yang lebih kompleks, reaksi alkohol dengan halida asam dan anhidrida asam lebih sering digunakan.
lebih sering digunakan.
Halida asam biasanya dibuat melalui reaksi asam karboksilat dengan tionil Halida asam biasanya dibuat melalui reaksi asam karboksilat dengan tionil klorida, dan diubah menjadi anhidrida asam melalui reaksi dengan garam natrium dari klorida, dan diubah menjadi anhidrida asam melalui reaksi dengan garam natrium dari asam. Sementara itu, amida dapat dibuat melalui reaksi asam karboksilat dengan asam. Sementara itu, amida dapat dibuat melalui reaksi asam karboksilat dengan amonia atau reaksi amina dengan anhidrida asam, ester, dan klorida asam. Amida amonia atau reaksi amina dengan anhidrida asam, ester, dan klorida asam. Amida primer
primer dapat dapat dikonversi dikonversi menjadi menjadi nitril. nitril. Banyak Banyak lagi lagi reaksi reaksi asam asam karboksilat karboksilat dandan turunannya yang berguna. Selengkapny
turunannya yang berguna. Selengkapnya tea terangkum dalamrangkum dalam Skema 1.10Skema 1.10
Skema 1.10 Skema 1.10 RCOCl RCOCl R(CO) R(CO)22OO RCO RCO22 --RCONH RCONH22 NH NH33 NH NH33 RCO RCO22R'R' R'OH R'OH NH NH33 Na NaNN33 RCON RCON33 R'OH R'OH Panas Panas RN RNHH22 RCO RCO22HH NH NH33 Br Br 22 OH OH --P P22OO55 RCN RCN RX RX + + CNCN --RCHO RCHO H H22 Pd/BaSO Pd/BaSO44 RCOCHN RCOCHN22 CH CH22NN22 RCH RCH22COCO22HH Ag Ag22OO H H22OO RCONHR' RCONHR' R'NHR'NH22 RCO RCO22HH SOCl SOCl22 R'NH R'NH22 R'OH R'OH AgN AgNOO33 R'Cl R'Cl R'OH/H R'OH/H++ R RCOCO22CHCH33 CH CH22NN22
BAB II BAB II
PEMBENTUKAN IKATAN KARBON-KARBON PEMBENTUKAN IKATAN KARBON-KARBON
2.1 Pendekatan Sinton 2.1 Pendekatan Sinton
Teknik pendekatan yang banyak digunakan para ahli karena telah teruji Teknik pendekatan yang banyak digunakan para ahli karena telah teruji keberhasilannya adalah
keberhasilannya adalah pendekatan diskoneksipendekatan diskoneksi atau atau pendekatan sintonpendekatan sinton.. MolekulMolekul target
target ( (MTMT), yaitu molekul yang akan disintesi), yaitu molekul yang akan disintesis, dipecah menjadi unti-unit yang lebihs, dipecah menjadi unti-unit yang lebih kecil melalui serangkaian proses yang disebut
kecil melalui serangkaian proses yang disebut diskoneksidiskoneksi, hingga diperoleh, hingga diperoleh reagenreagen ((material awalmaterial awal) yang sederhana dan mudah diperoleh. Diskoneksi molekul target) yang sederhana dan mudah diperoleh. Diskoneksi molekul target manjadi sinton dipisahkan dengan tanda
manjadi sinton dipisahkan dengan tanda dan pdan proses kebalikannyroses kebalikannya (sintesis) a (sintesis) diberidiberi tanda →.
tanda →. Interkonversi Gugus Fungsi (IGF)Interkonversi Gugus Fungsi (IGF) merupakan proses pengubahan suatu merupakan proses pengubahan suatu gugus fungsional menjadi gugus yang lain melalui reaksi substitusi, addisi, eliminasi, gugus fungsional menjadi gugus yang lain melalui reaksi substitusi, addisi, eliminasi, oksidasi, dan reduksi serta operasi balik yang digunakan dalam analisis.
oksidasi, dan reduksi serta operasi balik yang digunakan dalam analisis. SintonSinton merupakan fragmen ideal, biasanya suatu
merupakan fragmen ideal, biasanya suatu kation atau anion yang dihasilkan dari kation atau anion yang dihasilkan dari prosesproses diskoneksi. Sementara
diskoneksi. Sementara ReagenReagen adalah senyawa yang digunakan dalam praktek untukadalah senyawa yang digunakan dalam praktek untuk suatu sinton.
suatu sinton.
Suatu contoh senyawa keton
Suatu contoh senyawa keton (1) (1), bila diskoneksi dilakukan pada ikatan C, bila diskoneksi dilakukan pada ikatan C33 – – CC44 maka akan diperoleh sinton akseptor (positif) dan sinton donor (negatif) yang setara maka akan diperoleh sinton akseptor (positif) dan sinton donor (negatif) yang setara dengan reagen suatu alkil halida (2) dan
dengan reagen suatu alkil halida (2) dan -keto karboksilat (3). Reagen (3) dalam-keto karboksilat (3). Reagen (3) dalam suasana basa akan membentuk karbon
suasana basa akan membentuk karbon yang bertindak sebagai nukleofil, dan akan yang bertindak sebagai nukleofil, dan akan menyerang karbon elektrofilik yang mengikat atom brom. Selanjutnya dekarboksilasi menyerang karbon elektrofilik yang mengikat atom brom. Selanjutnya dekarboksilasi dilakukan dalam suasana asam diikuti dengan pemanasan.
dilakukan dalam suasana asam diikuti dengan pemanasan.
Analisis Analisis O O OO + + _ _ O O X X CO CO22EtEt + + MT (1) MT (1) (2) (2) (3) (3)
Sintesis Sintesis
1.2 Pembentukan Ikatan Karbon-Karbon 1.2 Pembentukan Ikatan Karbon-Karbon
Sudah jelas diketahui bahwa bagian terpenting dalam sintesis organik biasanya Sudah jelas diketahui bahwa bagian terpenting dalam sintesis organik biasanya adalah pembentukan kerangka karbon yang sesuai dengan kerangka produk akhir adalah pembentukan kerangka karbon yang sesuai dengan kerangka produk akhir (molekul target). Memang pada molekul yang lebih kecil, misalnya molekul yang (molekul target). Memang pada molekul yang lebih kecil, misalnya molekul yang mengandung enam atau tujuh atom karbon mungkin kerangkanya bisa disiapkan dari mengandung enam atau tujuh atom karbon mungkin kerangkanya bisa disiapkan dari material awal, dan hanya memerlukan tahap fungsionalisasi atau interkonversi gugus material awal, dan hanya memerlukan tahap fungsionalisasi atau interkonversi gugus fungsi. Namun, saat ini sintesis molekul yang ukurannya kecil sudah relatif jarang, dan fungsi. Namun, saat ini sintesis molekul yang ukurannya kecil sudah relatif jarang, dan kalaupun masih perlu disintesis bukanlah menjadi permasalahan lagi.
kalaupun masih perlu disintesis bukanlah menjadi permasalahan lagi. Seperti yang telah disampai
Seperti yang telah disampaikan sebelumnya, sintesis organik merupakan suatukan sebelumnya, sintesis organik merupakan suatu interaksi antara atom elektrofilik dengan atom nukleofilik. Hal ini juga terjadi pada interaksi antara atom elektrofilik dengan atom nukleofilik. Hal ini juga terjadi pada pembentukan
pembentukan ikatan ikatan karbon, karbon, yang yang merupakan merupakan interaksi interaksi atom atom karbon karbon nukleofiliknukleofilik (sinton donor) dengan atom karbon elektrofilik (sinton akseptor). Pada
(sinton donor) dengan atom karbon elektrofilik (sinton akseptor). Pada Tabel 2.1Tabel 2.1 ditampilkan beberapa reagen yang dapat bertindak sebagai sinton donor dan sinton ditampilkan beberapa reagen yang dapat bertindak sebagai sinton donor dan sinton akseptor, serta jenis reaksinya.
akseptor, serta jenis reaksinya.
O O CO CO22EtEt 1. EtO 1. EtO --2. 2. Br Br O O CO CO22EtEt 1. OH 1. OH-- / H / H22OO 2. 2. HH++panaspanas MT (1) MT (1) C C + + ++ _ _ CC CC CC sinton sinton akseptor akseptor sinton sinton donor donor
Tabel 2.1
Tabel 2.1 Reaksi Pembentukan Ikatan Karbon-karbonReaksi Pembentukan Ikatan Karbon-karbon No
No Reaksi Reaksi Reagen Reagen ProdukProduk Sinton
Sinton akseptor akseptor Sinton Sinton donordonor
1 1 Sianida Sianida RR – – X X HCN HCN RR – – CN CN 2 2 Asetilida Asetilida RR – – X X R’– R’– C CCC – – M M RR – – R’R’ 3 Org 3 Organologam anologam a a RR – – X X R’ – R’ – M M RR – – R’R’ M = MgX, Li M = MgX, Li ZnX b ZnX b R’ – R’ – M M (R)(R)22CC – – R’R’ cc R’ – R’ – M M RCH(OH)CH2R’RCH(OH)CH2R’ 4
4 Organotembaga Organotembaga RR – – X X R’R’22CuLi CuLi RR – – R’R’
R’
R’22CuLiCuLi
5
5 Alkilasi Alkilasi enolat enolat RR – – X X
6
6 Kondensasi Kondensasi enolatenolat
7
7 Asilasi Asilasi Friedel-Craft Friedel-Craft PhPh – – H H 8
8 Alkilasi Alkilasi Fridel-Craft Fridel-Craft RR – – X X PhPh – – H H RR – – Ph Ph
9
9 Reaksi Reaksi Wittig Wittig PhPh33P = CR’P = CR’22 (R’)(R’)22C = C(R)C = C(R)22
10
10 Siklisasi Siklisasi Diels-AlderDiels-Alder
2.3 Pembalikan Polaritas 2.3 Pembalikan Polaritas
Pembalikan polaritas adalah proses perubahan sifat atom karbon dari sinton Pembalikan polaritas adalah proses perubahan sifat atom karbon dari sinton donor (bersifat nukleofilik) menjadi sinton akseptor (bersifat elektrofilik) atau donor (bersifat nukleofilik) menjadi sinton akseptor (bersifat elektrofilik) atau sebaliknya. Pembalikan polaritas (umpolung) sangat penting dalam sintesis senyawa sebaliknya. Pembalikan polaritas (umpolung) sangat penting dalam sintesis senyawa organik, karena sinton dari hasil diskoneksi tidak selalu tersedia reagennya secara organik, karena sinton dari hasil diskoneksi tidak selalu tersedia reagennya secara langsung, melainkan harus melalui proses pembalikan polaritas a
langsung, melainkan harus melalui proses pembalikan polaritas a tau tetau terkadang melaluirkadang melalui proses pengalihan pusat kereaktifan. Conto
proses pengalihan pusat kereaktifan. Contohnya sintesis etana dari metil iodida. Metilhnya sintesis etana dari metil iodida. Metil iodida, yang merupakan reagen dari sinton akseptor (elektrofil) dapat diubah menjadi iodida, yang merupakan reagen dari sinton akseptor (elektrofil) dapat diubah menjadi reagen dari sinton donor (nukleofil) melalui reaksi dengan logam litium.
reagen dari sinton donor (nukleofil) melalui reaksi dengan logam litium.
R R C C R R O O O O R R CH CH C C R R O O CH CH22 RR CC CHCH22 O O CH CH22RR'' CH CH22 C C R' R' OH OH CH CH22 C C R R'' O O CH CH22RR X X C C R' R' O O CH CH22 C C R' R' OH OH CH CH22 C C R R'' O O C C RR O O Cl Cl C C R' R' O O Ph Ph C C R' R' O O R R C C R R O O
Pembalikan polaritas Pembalikan polaritas
Ada
Ada beberapa cara beberapa cara yang yang dilakukan dilakukan untuk untuk proses pproses pembalikan embalikan polaritaspolaritas termasuk pengalihan pusat kereaktifan, seperti :
termasuk pengalihan pusat kereaktifan, seperti : 1.
1. Pertukaran atom heteroPertukaran atom hetero
2.
2. Memasukkan atom heteroMemasukkan atom hetero
CH CH33 + + ++ HH33CC CHCH33 sinton sinton akseptor akseptor sinton sinton donor donor CH CH33 - -MT MT sinton sinton akseptor akseptor sinton sinton donor donor CH CH33 + + CHCH33 - -+ + H H33CC II H H33CC LiLi 2 Li 2 Li ++ Li -I Li -I + + HH33CC CHCH33 H H33CC II HH33CC LiLi MT MT C C H H C C H H PPh PPh33 / / Br Br Br Br PPh PPh33 Wittig Wittig -HBr -HBr C C PPhPPh33 C C H H C C H H MgX MgX X X Mg Mg C C H H C C H H M M X X 2 M 2 M - - MXMX C C - - HH++ H H O O HS HS HS HS S S C C S S H H SS C C S S
3.
3. Addisi fragmen karbonAddisi fragmen karbon
C C C C RRCOCO33HH CC C C O O C C C C H H O O Br Br 22 - HBr - HBr C C C C Br Br O O C C C C EWG EWG H H R RSHSH R RSS H H EWG EWG H H [O [O]] - - HH++ SS EWG EWG H H O O R R O O EWG = gugus penarik
EWG = gugus penarik elektron CHO, COR, COelektron CHO, COR, CO 22R, CNR, CN
Ar Ar HH O O CN CN-- Ar Ar CNCN OH OH R R HH O O Ar Ar CC OH OH H HCC CC --CH CH H H 1. [O] 1. [O] 1. -- H 1. -- H++ Ar Ar CC O O C C - - R R RR O O MgX MgX R R OH OH R R R R OH OH22 R R H H++
kereaktifan dialihkan ke atom karbon yang lain kereaktifan dialihkan ke atom karbon yang lain *) *) *) *) *) *)
BAB III BAB III
DISKONEKSI SATU GUGUS C DISKONEKSI SATU GUGUS C
–
–
X X3.1 SENYAWA TURUNAN R 3.1 SENYAWA TURUNAN R
–
–
XXSenyawa turunan R
Senyawa turunan R – – X meliputi alkohol, eter, alkilhalida, dan sulfida. X meliputi alkohol, eter, alkilhalida, dan sulfida. Diskoneksi C
Diskoneksi C – – X dalam senyawa alifatik (R X dalam senyawa alifatik (R – – X) akan memberikan suatu nukleofil X) akan memberikan suatu nukleofil HX dan spesies karbon elektrofilik berupa alkilhalida, tosilat dan mesilat. Halida (Cl, HX dan spesies karbon elektrofilik berupa alkilhalida, tosilat dan mesilat. Halida (Cl, Br), tosilat, dan mesilat
Br), tosilat, dan mesilat merupakan gugus pergi yang baik, serta semuanya dapat dibuatmerupakan gugus pergi yang baik, serta semuanya dapat dibuat dari alkohol (
dari alkohol (Skema 3.1Skema 3.1).).
Skema 3.1 Skema 3.1
R
R XX XH + RXH + R ++ = = RBr atau RBr atau ROTROTs atau s atau ROMsROMs
ROTs = ROTs = ROMs = ROMs = R R OO SS O O O O CH CH33 R R OO SS O O O O CH CH33 R R OHOH R R OOTTss R R OOMMss R R Br Br Ts - Cl Ts - Cl Piridin Piridin Ms - Cl Ms - Cl Et Et 3 3NN PBr PBr 3 3 HBr HBr R R OOHH RR XX R' -OH R' -OH Basa Basa R R OORR'' R R SSRR'' R' -SH R' -SH Basa Basa 1. (NH 1. (NH22))22CSCS 2. OH 2. OH--/H/H22OO R R SHSH Halogen Halogen R R HHaall R R NuNu Nu Nu Eter Eter Sulfida Sulfida Tiol Tiol Alk
Alkilhilhalidaalida Turu
Turunan lainan lainn X = halida,
X = halida, OTs, OMs OTs, OMs
Senyawa (1) dapat dibuat dengan reaksi Friedel-Crafts dari benzena dan Senyawa (1) dapat dibuat dengan reaksi Friedel-Crafts dari benzena dan klorida tersier (2)
klorida tersier (2) yang bisa diperoleh dari alkohol (3).yang bisa diperoleh dari alkohol (3).
Analisis : Analisis :
Sintesis : Sintesis :
Bila molekul target memiliki dua gugus samping seperti pada se
Bila molekul target memiliki dua gugus samping seperti pada se nyawa parfumnyawa parfum “wallflower” (
“wallflower” (44), diskoneksi dilakukan berdasarkan reaktivitas kedua substituen.), diskoneksi dilakukan berdasarkan reaktivitas kedua substituen. Atom oksigen pada senyawa (
Atom oksigen pada senyawa (44) reaktif sebagai nukleofil pada reaksi SN) reaktif sebagai nukleofil pada reaksi SN22, karenanya, karenanya diskoneksi dipilih pada ikatan O
diskoneksi dipilih pada ikatan O – – CH CH33..
Analisis : Analisis : Sintesis : Sintesis : Cl Cl + + OH OH MT ( 1 ) MT ( 1 ) ( 2 )( 2 ) ( 3 )( 3 ) ( 3 ) ( 3 ) HCl pekatHCl pekat ( 2 )( 2 ) Ph - HPh - H AlCl AlCl33 MT ( 1 ) MT ( 1 ) 70 % 70 % H H33CC O O CHCH33 H H33CC O O --CH CH33 - - YY + + MT MT ( ( 4 )4 ) H H33CC OH OH (CH (CH33O)O)22SOSO22 NaOH NaOH MT MT ( ( 4 )4 ) 85 85 %%
Senyawa parfum gardenia (
Senyawa parfum gardenia (55) dapat didiskoneksi pada dua sisi, karena) dapat didiskoneksi pada dua sisi, karena keduanya melibatkan alkilhalida primer. Benzil halida lebih reaktif dibandingkan keduanya melibatkan alkilhalida primer. Benzil halida lebih reaktif dibandingkan benzil
benzil alkohol, alkohol, tetapi tetapi pemilihan pemilihan rute rute (b) (b) disebabkan disebabkan oleh oleh adanya persainadanya persaingan prodgan produkuk substitusi dan produk eliminasi pada rute (a) pada suasana basa.
substitusi dan produk eliminasi pada rute (a) pada suasana basa.
Analisis : Analisis :
Sintesis : Sintesis :
Klorbensida (
Klorbensida (66) yang merupakan suatu desinfektan (pe) yang merupakan suatu desinfektan (pembunuh kuman), dapatmbunuh kuman), dapat didiskoneksi pada sisi alkil dan sisi aril. Teta
didiskoneksi pada sisi alkil dan sisi aril. Tetapi diskoneksi pada sisi alkil pi diskoneksi pada sisi alkil lebih disukailebih disukai karena lebih mudah membuat suatu elektrofil pada karbon alkil dibandingkan pada karena lebih mudah membuat suatu elektrofil pada karbon alkil dibandingkan pada karbon aril. karbon aril. Analisis : Analisis : Sintesis : Sintesis : Ph Ph OO b b aa aa b b P Phh OOHH x x + + Ph Ph ++ HOHO X X MT ( 5 ) MT ( 5 ) HO HO basa basa -- O O P Phh CCll MT ( 5 ) MT ( 5 ) 85 % 85 % S S Cl Cl Cl Cl C - S C - S Sulfida Sulfida S S --Cl Cl Cl Cl Cl Cl + + MT ( 6 ) MT ( 6 ) SH SH Cl Cl Cl Cl + + NaOEt NaOEt EtOH EtOH MT ( 6 ) MT ( 6 )
3.2 SENY
3.2 SENYAWA TURUNAWA TURUNAN KARBONIL AN KARBONIL RR
–
–
COXCOXDiskoneksi pada senyawa turunan asam mudah dilakukan, terutama pada Diskoneksi pada senyawa turunan asam mudah dilakukan, terutama pada ikatan atom hetero dengan gugus karbonil. Diskoneksi model ini selal
ikatan atom hetero dengan gugus karbonil. Diskoneksi model ini selal u menjadi pilihanu menjadi pilihan pertama pada
pertama pada senyawa senyawa turunan turunan asam. Aasam. Asil halida (Y sil halida (Y = C= Cl) merupakan l) merupakan senyawa senyawa turunanturunan asam yang paling reaktif
asam yang paling reaktif dalam pelarut dan katalis piridalam pelarut dan katalis piridin, sehingga banyak digundin, sehingga banyak digunakanakan dalam sintesis senyawa turuanan asam yang lain. Diskoneksi dan reaktivitas turunan dalam sintesis senyawa turuanan asam yang lain. Diskoneksi dan reaktivitas turunan asam tertera pada
asam tertera pada Skema 3.2Skema 3.2
Skema 3.2 Skema 3.2
Senyawa ester (
Senyawa ester (77) baik digunakan sebagai pengusir serangga atau ) baik digunakan sebagai pengusir serangga atau pelarut untukpelarut untuk parfum. Diskoneksi pada ikatan C - O ester merupakan pilihan terbaik.
parfum. Diskoneksi pada ikatan C - O ester merupakan pilihan terbaik.
Analisis : Analisis : R R CC O O X X RR CC O O Y Y + + XHXH C - X C - X RCOOH (Asam) RCOOH (Asam) SOCl
SOCl22 atau PCl atau PCl55
Ac Ac22OO R'OH R'OH H H++ RCOCl RCOCl (RCO) (RCO)22OO RCOOR' RCOOR' R'R"NH R'R"NH RCONR'R" RCONR'R" Klorida asam Klorida asam Anhidrida Anhidrida Ester Ester Amida Amida Paling reaktif Paling reaktif Paling stabil
Paling stabil biasanya tidak dibuatbiasanya tidak dibuat secara langsung secara langsung P Phh OO PPhh O O C - O C - O ester ester P Phh OOHH PPhh O O Y Y + + MT ( 7 ) MT ( 7 )
Sintesis : Sintesis :
Suatu amida, propanil (
Suatu amida, propanil (88) banyak digunakan sebagai pembasmi tanaman) banyak digunakan sebagai pembasmi tanaman pengganggu
pengganggu (rumput dan semak) di (rumput dan semak) di sawah. Diskoneksi pada sawah. Diskoneksi pada ikatan C karbonikatan C karbonil denganil dengan atom N akan menjadi suatu amina dan klorida asam.
atom N akan menjadi suatu amina dan klorida asam.
Analisis : Analisis :
Sintesis : Sintesis :
Senyawa (
Senyawa (99) merupakan contoh yang lebih sulit, tetapi kita telah mengenal) merupakan contoh yang lebih sulit, tetapi kita telah mengenal pada
pada senyawa senyawa tersebut tersebut ada ada gugus gugus ester ester yang yang dapat dapat didiskoneksi, didiskoneksi, sehingga sehingga akaakann diperoleh suatu turunan asam yang baik dan murah, yaitu anhidrida ftalat (10).
diperoleh suatu turunan asam yang baik dan murah, yaitu anhidrida ftalat (10).
P Phh OOHH Ph-COClPh-COCl piridin piridin MT ( 7 )MT ( 7 ) HN HN O O Cl Cl Cl Cl C - N C - N amida amida NH NH22 O O Cl Cl Cl Cl ClCl + + IGF IGF reduksi reduksi NO NO22 Cl Cl Cl Cl C - N C - N nitrasi nitrasi Cl Cl Cl Cl MT ( 8 ) MT ( 8 ) Cl Cl Cl Cl HN HNOO33 H H22SOSO44 NO NO22 Cl Cl Cl Cl H H22 / / PdPd NH NH22 Cl Cl Cl Cl EtCOCl EtCOCl MT ( 8 ) MT ( 8 )
Analisis : Analisis : Sintesis : Sintesis : C - O C - O ester ester MT ( 9 ) MT ( 9 ) CO CO22HH O O PhPh O O CO CO22HH Y Y O O H HOO PPhh + + O O O O O O (10) (10) O O O O O O (10) (10) H HOO PPhh Et Et33NN MT ( 9 )MT ( 9 )
BAB IV BAB IV
DISKONEKSI DUA GUGUS C DISKONEKSI DUA GUGUS C
–
–
X X4.1 Senyawa 1,1-difungsional 4.1 Senyawa 1,1-difungsional
Seperti namanya, senyawa 1,1-difungsional memiliki dua gugus fungsi yang Seperti namanya, senyawa 1,1-difungsional memiliki dua gugus fungsi yang terletak pada satu at
terletak pada satu atom karbon. Kedua gugus fungsi ini dapat disederhanakan menjadiom karbon. Kedua gugus fungsi ini dapat disederhanakan menjadi satu gugus fungsi yang lain untuk memudahkan proses diskoneksi. Jika kedua gugus satu gugus fungsi yang lain untuk memudahkan proses diskoneksi. Jika kedua gugus fungsi mengandung atom oksigen, maka ada
fungsi mengandung atom oksigen, maka ada dua nukleofil yang dilibatkan. Sebaliknyadua nukleofil yang dilibatkan. Sebaliknya jika hanya satu
jika hanya satu gugus fungsi yang mengandung atom oksigen bagugus fungsi yang mengandung atom oksigen baik dalam bentuk OHik dalam bentuk OH (alkohol) maupun OR (eter), maka hanya satu nukleofil yang terlibat. Senyawa yang (alkohol) maupun OR (eter), maka hanya satu nukleofil yang terlibat. Senyawa yang diturunkan dari sianohidrin dan
diturunkan dari sianohidrin dan -halo eter merupakan contoh senyawa 1,1--halo eter merupakan contoh senyawa 1,1-difungsional yang memilki satu gugus fungsi dengan atom oksigen. Secara umum, difungsional yang memilki satu gugus fungsi dengan atom oksigen. Secara umum, senyawa 1,1-difungsional tertera pada
senyawa 1,1-difungsional tertera pada skema 4.1skema 4.1
Skema 4.1 Skema 4.1
Senyawa (
Senyawa (11)) yang yang merupakan parfum merupakan parfum dari daun dari daun “lilae”, mengandung “lilae”, mengandung gugusgugus
HX HX HY HY
..
..
+ + Y Y X X O O O OMeMe O OMeMe OOMeMe OO ++ MeOHMeOH
..
..
CN CN O OHH O OHH OO ++ HCNHCN + + + + ROH ROH HCl HCl + + Cl Cl O ORR O O..
..
Analisis : Analisis :
Sintesis : Sintesis :
Senyawa (
Senyawa (22) merupakan salah satu contoh senyawa yang diturunkan dari) merupakan salah satu contoh senyawa yang diturunkan dari sianohidrin. Reduksi gugus CN akan menghasilkan amina.
sianohidrin. Reduksi gugus CN akan menghasilkan amina.
Analisis : Analisis :
Sintesis : Sintesis :
Senyawa asam
Senyawa asam -amino (-amino (33) suatu analog metabolit “dopa” untuk terapi) suatu analog metabolit “dopa” untuk terapi penyakit
penyakit Parkinson, Parkinson, dapat dapat disederhanakan disederhanakan menjadi menjadi senyawa senyawa 1,1-difungsional 1,1-difungsional aminoamino sianida. Diskoneksi senyawa ini akan diperoleh suatu keton (4). Reaksi sintesis sianida. Diskoneksi senyawa ini akan diperoleh suatu keton (4). Reaksi sintesis senyawa asam
senyawa asam -amino dengan metode ini disebut Sintesis Strecker.-amino dengan metode ini disebut Sintesis Strecker.
Analisis : Analisis : 1,1-di X 1,1-di X asetal asetal + + Ph Ph OM OMee OM OMee P Phh CHOCHO 22MMeeOOHH MT ( 1 ) MT ( 1 ) P Phh CCHHOO MeOH MeOH H H ++ MT ( 1 ) MT ( 1 ) NH NH22 OH OH IIGGFF CN CN OH OH 1,1-di X 1,1-di X O O HCN HCN + + MT ( 2 ) MT ( 2 ) O O + + H H KCN KCN CNCN OH OH H H22 PtO PtO22 MT ( 2 ) MT ( 2 )
Sintesis : Sintesis :
Senyawa (
Senyawa (55) merupakan contoh senyawa) merupakan contoh senyawa -halo eter. Diskoneksi 1,1--halo eter. Diskoneksi 1,1-difungsional senyawa ini akan menghasilkan suatu alkohol (6).
difungsional senyawa ini akan menghasilkan suatu alkohol (6).
Analisis : Analisis : Sintesis : Sintesis : 4.2 Senyawa 1,2-difungsional 4.2 Senyawa 1,2-difungsional 4.2.1 Senyawa Alkohol 4.2.1 Senyawa Alkohol
Senyawa dengan atom hetero dekat atom-atom karbon seperti (7) dan (8) dapat Senyawa dengan atom hetero dekat atom-atom karbon seperti (7) dan (8) dapat dianggap sebagai suatu turunan alkohol. Diskoneksi memberi sinton (9), dimana dianggap sebagai suatu turunan alkohol. Diskoneksi memberi sinton (9), dimana reagennya adalah epoksida (10).
reagennya adalah epoksida (10).
1,1-di X 1,1-di X Strecker Strecker MT ( 3 ) MT ( 3 ) H H22NN COCO22HH HO HO HO HO ( 4 ) ( 4 ) HO HO HO HO O O 1. NH 1. NH44Cl, KCNCl, KCN 2. HCl pekat 2. HCl pekat MT ( 3 ) MT ( 3 ) ( 4 ) ( 4 ) 1,1-di X 1,1-di X O O ClCl MT ( 5 ) MT ( 5 ) MeO MeO ( 6 ) ( 6 ) OH OH MeO MeO ++ CHCH22O + HClO + HCl MT ( 5 ) MT ( 5 ) ( 6 ) ( 6 ) CHCH22O, HClO, HCl Nu Nu OCOR OCOR N Nuu --OH OH + + Nu Nu Cl Cl N Nuu OH OH OO ( 10 ) ( 10 ) ( 9 ) ( 9 ) ( 7 ) ( 7 )
Proparakaina (
Proparakaina (1111) adalah seri anestetik yang mengandung gugus ester, eter,) adalah seri anestetik yang mengandung gugus ester, eter, dan amina. Diskoneksi ikatan C
dan amina. Diskoneksi ikatan C – – O ester merupakan langkah awal yang tepat. Asam O ester merupakan langkah awal yang tepat. Asam (12) dapat dibuat dengan diskoneksi aromatik standar dan alkohol (13) adalah senyawa (12) dapat dibuat dengan diskoneksi aromatik standar dan alkohol (13) adalah senyawa 1,2-difungsional yang setara dengan suatu epoksida dan amina.
1,2-difungsional yang setara dengan suatu epoksida dan amina.
Analisis : Analisis : Sintesis : Sintesis : C - O C - O 1,2-diX 1,2-diX O O + + M MTT(( 1111 )) ((1122)) (13) (13) O O NEt NEt22 O O NH NH22 O O ester ester OH OH O O NH NH22 O O + + HO HO NEt NEt22 HNEt HNEt22 (12) (12) IGF IGF reduksi reduksi OH OH O O NO NO22 O O C - N C - N nitrasi nitrasi OH OH O O O O C - O C - O eter eter C C33HH77 CC33HH77 C C33HH77 CC33HH77 OH OH O O OH OH
Beberapa senyawa
Beberapa senyawa -kloro amina mempunyai aktivitas fisiologik seperti-kloro amina mempunyai aktivitas fisiologik seperti bersifat anti-tumor, dan
bersifat anti-tumor, dan senyawa (senyawa (1515) adalah salah satunya. Atom klor bisa diperoleh) adalah salah satunya. Atom klor bisa diperoleh dari alkohol (16). Diskoneksi C
dari alkohol (16). Diskoneksi C – – N senyawa (16) akan menghasilkan suatu epoksida N senyawa (16) akan menghasilkan suatu epoksida dan senyawa (17). Senyawa (17) merupakan ester siklik dari suatu epoksida dengan dan senyawa (17). Senyawa (17) merupakan ester siklik dari suatu epoksida dengan asam antranilat (18). asam antranilat (18). Analisis : Analisis : OH OH O O OH OH OH OH O O NO NO22 OH OH OH OH O O NO NO22 O O CC33HH77 HN HNOO33 CC33HH77 - - ClCl basa basa Cl Cl O O NO NO22 O O CC33HH77 SOCl SOCl22 ( 14 ) ( 14 ) O O + + HNEt HNEt22 ( 13 ) ( 13 ) ( 14 )( 14 ) O O N NEtEt22 O O NO NO22 O O CC33HH77 H H22 Pd, C Pd, C MT ( 11 ) MT ( 11 ) O O N N O O Cl Cl C - Cl C - Cl O O N N O O OH OH 1,2-diX 1,2-diX O O H H N N O O O O + + MT ( 15 ) MT ( 15 ) (16)(16) (17)(17) O O H H N N O O (17) (17) C - O C - O ester ester H H N N CO CO22HH OH OH 1,2-diX 1,2-diX NH NH22 CO CO22HH O O + + (18) (18)
Sintesis : Sintesis : O O berlebih berlebih (16) (16) POClPOCl33 MT ( 15 )MT ( 15 ) (18) (18)
4.2.2 Senyawa Karbonil 4.2.2 Senyawa Karbonil
Pada tingkat oksidasi yang lebih tinggi (19), sinton elektrofilik akan berupa Pada tingkat oksidasi yang lebih tinggi (19), sinton elektrofilik akan berupa kation karbonil (20), suatu spesies yang sangat tidak stabil. Reagen yang paling baik kation karbonil (20), suatu spesies yang sangat tidak stabil. Reagen yang paling baik untuk sinton ini adalah senyawa
untuk sinton ini adalah senyawa -halo karbonil.-halo karbonil.
Herbisida’2,4
Herbisida’2,4--D’ D’ ((2121) adalah salah satu pestisida yang banyak digunakan.) adalah salah satu pestisida yang banyak digunakan. Diskoneksi C
Diskoneksi C - O dan C - O dan C – – Cl aromatik akan menghasilkan material awal fenol. Cl aromatik akan menghasilkan material awal fenol.
Analisis : Analisis : Sintesis : Sintesis : 4.2 Senyawa 1,3-difungsional 4.2 Senyawa 1,3-difungsional
Senyawa 1,3-difungsional hanya dapat didiskoneksikan pada tingkat oksidasi Senyawa 1,3-difungsional hanya dapat didiskoneksikan pada tingkat oksidasi karbonil, dimana reagen dari sinton yang dihasilkan adalah senyawa karbonil
karbonil, dimana reagen dari sinton yang dihasilkan adalah senyawa karbonil ,,-tak-tak jenuh.
jenuh. Reaksi Reaksi menggunakan menggunakan reagen reagen ini ini dikenal dikenal dengan dengan reaksi reaksi Michael, Michael, dan dan efektifefektif untuk semua senyawa karbonil dan sianida serta senyawa nitro.
untuk semua senyawa karbonil dan sianida serta senyawa nitro.
Nu Nu R R O O 1,2-diX 1,2-diX Nu Nu --R R O O + + Ha Hall R R O O ( 19 ) ( 19 ) ( 20 )( 20 ) C Cll CCll O O COCO22HH 1,2-diX 1,2-diX MT ( 21 ) MT ( 21 ) C Cll CCll OH OH C - Cl C - Cl CO CO22HH Cl Cl + + Ph - OHPh - OH Ph - OH Ph - OH Cl Cl22 Fe Fe C Cll CCll OH OH 1. NaOH 1. NaOH 2. ClCH 2. ClCH22COCO22HH MT ( 21 )MT ( 21 ) Nu Nu Nu Nu --+ + R R RR RR
Reagen Grignard dari senyawa (
Reagen Grignard dari senyawa (2222) banyak digunakan dalam sintesis.) banyak digunakan dalam sintesis. Diskoneksi asetal dari (
Diskoneksi asetal dari (2222) akan memberikan senyawa) akan memberikan senyawa -bromo aldehid, dan ini -bromo aldehid, dan ini dapatdapat dibuat dari addisi Michael Br
dibuat dari addisi Michael Br – – terhadap akrolein. terhadap akrolein.
Analisis : Analisis :
Sintesis : Sintesis :
Amina tipe (
Amina tipe (2323) dapat dibuat dengan mereduksi sianida (24), yang merupakan) dapat dibuat dengan mereduksi sianida (24), yang merupakan produk reaksi Michael dari senyawa
produk reaksi Michael dari senyawa ,,-tak jenuh dari suatu sianida dengan alkohol.-tak jenuh dari suatu sianida dengan alkohol.
Analisis : Analisis : Sintesis : Sintesis : MT ( 22 ) MT ( 22 ) Br Br HH O O O O Br Br HH O O H H O O Br Br
--1,1-diX 1,1-diX asetal asetal 1,3-diX 1,3-diX H H O O HB HBr r Br Br HH O O O OHH HO HO H H++ MT ( 22 ) MT ( 22 ) R ROO NNHH22 IIGGFF reduksi reduksi RO RO CN CN M MTT ((2233)) (( 2244)) RO RO --CN CN 1,3-diX 1,3-diX ROROHH NaOMeNaOMe CN CN ( 24 ) ( 24 ) H H22 Rh, Al Rh, Al22OO33 MT ( 23 ) MT ( 23 )
BAB V BAB V
GUGUS PELINDUNG GUGUS PELINDUNG
Dalam sintesis masalah kemoselektivitas seringkali ditemukan. Misalkan, Dalam sintesis masalah kemoselektivitas seringkali ditemukan. Misalkan, molekul yang akan direaksikan mengandung dua gugus fungsi yang reaktif padahal molekul yang akan direaksikan mengandung dua gugus fungsi yang reaktif padahal kita hanya menginginkan salah satu dari kedua gugus fungsi tersebut yang bereaksi. kita hanya menginginkan salah satu dari kedua gugus fungsi tersebut yang bereaksi. Salah satu cara
Salah satu cara untuk mengatasi permasalahan ini auntuk mengatasi permasalahan ini adalah dengan menggunakan gugusdalah dengan menggunakan gugus pelindung.
pelindung. Senyawa Senyawa ketoester ketoester (1) (1) mengandung mengandung dua dua gugus gugus karbonil karbonil yang yang berbedaberbeda kereaktifannya. Gugus karbonil keton kereaktifannya lebih tinggi dibandingkan kereaktifannya. Gugus karbonil keton kereaktifannya lebih tinggi dibandingkan karbonil ester, karenanya jika senyawa tersebut direduksi akan menghasilkan alkohol karbonil ester, karenanya jika senyawa tersebut direduksi akan menghasilkan alkohol (2) bukan alkohol (3). Untuk mereduksi ester menjadi alkohol, lazimnya digunakan (2) bukan alkohol (3). Untuk mereduksi ester menjadi alkohol, lazimnya digunakan LiAlH
LiAlH44 dan NaBH dan NaBH44 sebagai re sebagai reduktor. Namun produk yang dihasilkan masih dominanduktor. Namun produk yang dihasilkan masih dominan kearah alkohol (2) karena faktor kereaktifan. Agar alkohol yang dihasilkan adalah kearah alkohol (2) karena faktor kereaktifan. Agar alkohol yang dihasilkan adalah alkohol (3), gugus karbonil keton harus dilindungi dulu (misalnya diubah menjadi alkohol (3), gugus karbonil keton harus dilindungi dulu (misalnya diubah menjadi asetal).
asetal).
Sintesis : Sintesis :
Gugus pelindung y
Gugus pelindung yang baik harus memenuhi persyaratan sebagai berikut :ang baik harus memenuhi persyaratan sebagai berikut : 1.
1. mudah dimasukkan dan mudah mudah dimasukkan dan mudah dihilangkandihilangkan 2.
2. resisten terhadap reagen yang akan menyerang gugus fungsional yang tidakresisten terhadap reagen yang akan menyerang gugus fungsional yang tidak terlindungi terlindungi CO CO22EtEt O O NaBHNaBH44 ? ? O O CO CO22EtEt OH OH OH OH (1) (1) (2) (2) (3) (3) (1) (1) H H++ COCO22EtEt O O O O LiAlHLiAlH44 OO OO OH OH HH22OO H H++ (3) (3) OH OH HO HO
Dalam sintesis (3), asetal mudah dibuat dan mudah dihilangkan, keduanya Dalam sintesis (3), asetal mudah dibuat dan mudah dihilangkan, keduanya dengan hasil yang baik, tahan rea
dengan hasil yang baik, tahan reagen seperti basa, nukleofil, dan agen pereduksi sepertigen seperti basa, nukleofil, dan agen pereduksi seperti LiAlH
LiAlH44. Pada. Pada tabel 5.1tabel 5.1 ditampilkan beberapa macam gugus pelindung yang tersediaditampilkan beberapa macam gugus pelindung yang tersedia untuk semua gugus fungsional.
untuk semua gugus fungsional.
Tabel 5.1
Tabel 5.1 Gugus-gugGugus-gugus us pelindungpelindung Gugus Gugus Gugus Gugus pelindung pelindung (GP) (GP) Penambahan
Penambahan Penghilangan Penghilangan KetahananKetahanan GP GP GP reaktif GP reaktif terhadap terhadap Aldehid Asetal Aldehid Asetal RCHO
RCHO RCH(OR’)RCH(OR’)22 R’OH, HR’OH, H++ HH++/ H/ H22O O Nukleofil,Nukleofil,
basa, reduktor basa, reduktor Elektrofil, Elektrofil, oksidator oksidator Keton
Keton Asetal Asetal (ketal)(ketal) RCOR R
RCOR R 22C(OR’)C(OR’)22 R’OH, HR’OH, H++ HH++/ H/ H22O O Nukleofil,Nukleofil,
basa, reduktor basa, reduktor Elektrofil, Elektrofil, oksidator oksidator Asam Ester Asam Ester RCO
RCO22H H RCORCO22Me Me CHCH22 N N22 HH22/katalis/katalis
Pd/C Pd/C Basa lemah, Basa lemah, elektrofil elektrofil Basa kuat, Basa kuat, nukleofil, nukleofil, reduktor reduktor RCO
RCO22Et Et EtOH/HEtOH/H++ OHOH---- /H /H22O O Basa Basa lemah,lemah,
elektrofil elektrofil Basa kuat, Basa kuat, nukleofil, nukleofil, reduktor reduktor RCO
RCO22CHCH22Ph Ph PhCHPhCH22OH/HOH/H++ HH22/katalis,/katalis,
atau HBr atau HBr Basa lemah, Basa lemah, elektrofil elektrofil Basa kuat, Basa kuat, nukleofil, nukleofil, reduktor reduktor RCO
RCO22Bu-Bu-tt HH++//t t -BuOH -BuOH HH++ Basa lemah,Basa lemah,
elektrofil elektrofil Basa kuat, Basa kuat, nukleofil, nukleofil, reduktor reduktor RCO
RCO22CHCH22CClCCl33 ClCl33CCHCCH22OHOH Zn.MeOH Zn.MeOH Basa Basa lemah,lemah,
elektrofil elektrofil Basa kuat, Basa kuat, nukleofil, nukleofil, reduktor reduktor RCO
RCO22---- basa basa asam asam nukleofil nukleofil elektrofilelektrofil
Alkohol Eter Alkohol Eter
ROH ROCH
ROH ROCH22Ph Ph PhCHPhCH22Br / basaBr / basa HH22/katalis,/katalis,
atau HBr atau HBr Basa/oksidasi, Basa/oksidasi, elektrofil elektrofil HX HX nukleofil nukleofil Asetal Asetal THP THP DHP DHP HH++/ H/ H 2
2O O Basa Basa asamasam
MEM
MEM ROCHROCH22O(CHO(CH22)OMe)OMe ZnBr ZnBr 22 Basa Basa asamasam
Ester Ester RCO
RCO22R’R’ R’COCl /piridinR’COCl /piridin NHNH33, , MeOH MeOH Basa/oksidasi,Basa/oksidasi,
elektrofil elektrofil nukleofil nukleofil Fenol eter Fenol eter ArOH
ArOH ArOMe ArOMe MeMe22SOSO44
K K 22COCO33 HI, HBr HI, HBr atau BBr atau BBr 33 Basa, Basa, elektrofil elektrofil lemah lemah Serangan Serangan elektrofil elektrofil ke cincin ke cincin Asetal Asetal ArOCH
ArOCH22OMe MeOCHOMe MeOCH33Cl Cl / / basa basa HOAc, HOAc, HH22O O Basa,Basa,
elektrofil elektrofil lemah lemah Serangan Serangan elektrofil elektrofil ke cincin ke cincin
Tabel 5.1
Tabel 5.1 (lanjutan)(lanjutan) Gugus Gugus Gugus Gugus pelindung pelindung (GP) (GP) Penambahan
Penambahan Penghilangan Penghilangan KetahananKetahanan GP GP GP reaktif GP reaktif terhadap terhadap Amina Amida Amina Amida RNH
RNH22 RNHCOR’RNHCOR’ R’OCClR’OCCl OHOH---- /H /H22O O elektrofilelektrofil
Uretan Uretan
RNHCO.OR’
RNHCO.OR’ R’OCOClR’OCOCl HH22 /katalis /katalis
atau HBr atau HBr elektrofil Basa, elektrofil Basa, nukleofil nukleofil RNHCOOBu-tt t
t -BuOCOCl -BuOCOCl HH++ elektrofil elektrofil Basa,Basa,
nukleofil nukleofil flalimida
flalimida Anhidrida Anhidrida ftalat ftalat NHNH22 NH NH22 elektrofil elektrofil Basa,Basa,
nukleofil nukleofil Tiol
Tiol RSH
RSH AcSR AcSR AcCl AcCl / / basa basa OHOH---- /H /H 2
2O O elektrofil elektrofil oksidasioksidasi
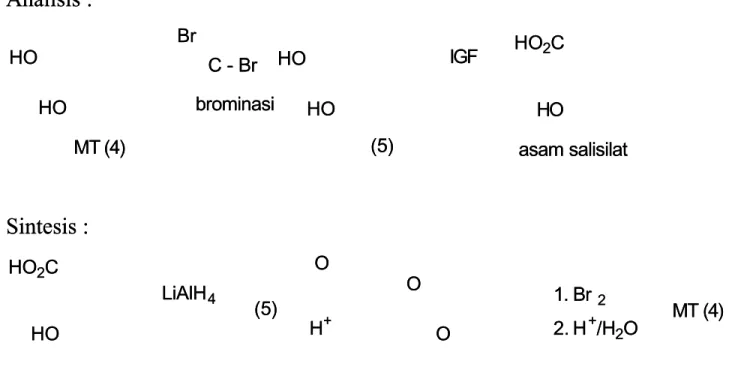
Senyawa karbonil dapat digunakan untuk melindungi diol, seperti pada Senyawa karbonil dapat digunakan untuk melindungi diol, seperti pada salbutamol (
salbutamol (44). Diskoneksi yang tepat dimulai dari ikatan C). Diskoneksi yang tepat dimulai dari ikatan C – – Br, diikuti dengan proses Br, diikuti dengan proses IGF sehingga diperoleh asam salisilat sebagai material start. Reduksi asam salisilat IGF sehingga diperoleh asam salisilat sebagai material start. Reduksi asam salisilat akan menghasilkan diol (5), dan bila langsung dilanjutkan dengan brominasi, akan menghasilkan diol (5), dan bila langsung dilanjutkan dengan brominasi, benzilalkohol
benzilalkohol akan akan teroksidasi kteroksidasi kembali. embali. Karenanya Karenanya sebelum brosebelum brominasi, diominasi, diol dilindungl dilindungii menjadi ketal dengan aseton dalam suasana asam.
menjadi ketal dengan aseton dalam suasana asam.
Analisis : Analisis :
Sintesis : Sintesis :
Gugus pelindung untuk asam karboksilat adalah vital dalam sintesis peptida. Gugus pelindung untuk asam karboksilat adalah vital dalam sintesis peptida. Bahkan
Bahkan problemanya problemanya sangat sangat jelas jelas sekalipun sekalipun hanya hanya dipeptida. dipeptida. Dipeptida Dipeptida ester ester Asp- Asp-Phe-OCH
Phe-OCH33 (6) merupakan agen pemanis, 150 kali lebih manis dari gula tebu. Hanya (6) merupakan agen pemanis, 150 kali lebih manis dari gula tebu. Hanya
HO HO HO HO HO HO HO HO H HOO HO HO22CC Br Br C - Br C - Br brominasi brominasi IIGGFF MT (4)
MT (4) (5)(5) asam salisilatasam salisilat
HO HO HO HO22CC LiAlH LiAlH44 (5) (5) H H++ O O O O O O 2. 2. HH++/H/H22OO 1. Br 1. Br 2 2 MT (4) MT (4)
material start. Tetapi, masalah utamanya adalah bagaimana kita membuat kombinasi material start. Tetapi, masalah utamanya adalah bagaimana kita membuat kombinasi dipeptida seperti yang diinginkan dan menghilangkan peluang terbentuknya dimer dipeptida seperti yang diinginkan dan menghilangkan peluang terbentuknya dimer Asp-Asp, Phe-Phe, dan produk yang salah Phe-Asp. Selain itu, juga perlu diingat Asp-Asp, Phe-Phe, dan produk yang salah Phe-Asp. Selain itu, juga perlu diingat bahwa
bahwa Asp Asp memiliki memiliki dua dua gugugugus s karboksilat. karboksilat. Dalam Dalam hal hal ini ini penggunaan penggunaan gugusgugus pelindung adalah jawaban y
pelindung adalah jawaban yang tepat.ang tepat.
Analisis : Analisis : Proteksi Asp Proteksi Asp Proteksi Phe Proteksi Phe H H N N O O Ph Ph CO CO22CHCH33 HO HO22CC H H22NN C - NC - N amida amida O O HO HO22CC H H22NN OHOH H H22NN Ph Ph CO CO22CHCH33 C - O C - O ester ester H H22NN Ph Ph CO CO22HH + + MT (6) MT (6) O O H HOO22CC N N H H OH OH O O Ph Ph O O O O HO HO22CC H H22NN OHOH O O Ph Ph O O Cl Cl (7) (7) (7) (7) PhCH PhCH22OHOH H H++ COCO22CHCH22PhPh Ph PhHH22COCO22CC N N H H O O Ph Ph O O 1. LiOH, H1. LiOH, H 2 2OO 2. H 2. H ++ Ph PhHH22COCO22CC N N H H O O Ph Ph O O (8) (8) CO CO22HH H H22NN Ph Ph CO CO22HH CH CH33OOHH SOCl SOCl22 H H22NN Ph Ph CO CO22CHCH33 (9) (9)
Sintesis : Sintesis : (8) (8) ++ C Cll CCll HO HO Cl Cl Ph PhHH22COCO22CC N N H H O O Ph Ph O O O O Cl Cl C Cll CCll (10) (10) pengaktivasi pengaktivasi (10) (10) ++ (9)(9) EtEt33NN Ph PhHH22COCO22CC N N H H O O Ph Ph O O HH N N COCO22CHCH33 Ph Ph O O H H22, , PdPd HOAc HOAc H H22OO MT (6) MT (6)
BAB VI BAB VI
DISKONEKSI DUA GUGUS : SENYAWA KARBONIL DISKONEKSI DUA GUGUS : SENYAWA KARBONIL
6.1
6.1 SENYAWA SENYAWA 1,3-DIFUNGSIONAL 1,3-DIFUNGSIONAL DAN DAN -HIDROKSI -HIDROKSI KARBONILKARBONIL
Diskoneksi langsung dari gugus senyawa ini dimungkinkan pada dua tingkat Diskoneksi langsung dari gugus senyawa ini dimungkinkan pada dua tingkat oksidasi, yaitu 1,3-dikarbonil (1) dan
oksidasi, yaitu 1,3-dikarbonil (1) dan -hidroksi karbonil (3). Diskoneksi senyawa (-hidroksi karbonil (3). Diskoneksi senyawa (1)1) merupakan kebalikan reaksi asilasi (X = OR, Cl) dari ion enolat (2). Enona (4) dapat merupakan kebalikan reaksi asilasi (X = OR, Cl) dari ion enolat (2). Enona (4) dapat dibuat melalui dehidrasi senyawa (3).
dibuat melalui dehidrasi senyawa (3).
Senyawa parfum (aroma balsamik) (
Senyawa parfum (aroma balsamik) (55) memiliki hubungan 1,3-dikarbonil, dan) memiliki hubungan 1,3-dikarbonil, dan dapat didiskoneksi menjadi enolat keton dan suatu ester. Senyawa keton (6) dalam dapat didiskoneksi menjadi enolat keton dan suatu ester. Senyawa keton (6) dalam suasana basa kuat akan berada dalam kesetimbangan dengan bentuk enolat. Serangan suasana basa kuat akan berada dalam kesetimbangan dengan bentuk enolat. Serangan ion enolat terhadap ester etil asetat diikuti dengan pengasaman akan menghasilkan ion enolat terhadap ester etil asetat diikuti dengan pengasaman akan menghasilkan senyawa target ( senyawa target (55).). O O OO O O --+ + O O 1 1 2 2 33 O O --X X O O O O OHOH + + OH OH 1 1 2 2 33 O O 1 1 2 2 33 IGF IGF + + ( 1 ) ( 1 ) ( 2 ) ( 2 ) ( 3 ) ( 3 ) ( 4 ) ( 4 ) ( 2 ) ( 2 ) ++ H H O O
Analisis : Analisis :
Sintesis : Sintesis :
Pival (
Pival (77) merupakan racun tikus dengan tiga gugus keton yang memiliki) merupakan racun tikus dengan tiga gugus keton yang memiliki hubungan 1,3 dengan yang lainnya. Dari dua diskoneksi yang mungkin, diskoneksi b hubungan 1,3 dengan yang lainnya. Dari dua diskoneksi yang mungkin, diskoneksi b lebih cepat menuntun ke material start yang tersedia.
lebih cepat menuntun ke material start yang tersedia.
Analisis : Analisis : Ph Ph O O Ph Ph O O O O --+ + O O Ph Ph O O --EtO EtO O O + + MT ( 5 ) MT ( 5 ) Ph Ph O O H H EtOEtO --Ph Ph O O --OEt OEt O O MT ( 5 ) MT ( 5 ) H H++ ( 6 ) ( 6 ) O O O O O O aa b b aa OO O O O O -- ++ EtOEtO b b CO CO22EtEt O O O O CO CO22EtEt CO CO22EtEt O O + + MT ( 7 ) MT ( 7 )
Sintesis : Sintesis :
Senyawa (
Senyawa (88) kelihatannya rumit, tetapi satu diskoneksi yang tepat) kelihatannya rumit, tetapi satu diskoneksi yang tepat menunjukkan bahwa senyawa ini terbentuk dari dua molekul material start yang sama. menunjukkan bahwa senyawa ini terbentuk dari dua molekul material start yang sama.
Analasis : Analasis :
Sintesis : Sintesis :
Senyawa (
Senyawa (99) merupakan salah satu contoh senyawa enon yang tidak) merupakan salah satu contoh senyawa enon yang tidak terkonjugasi. Dengan bantuan diskoneksi Wittig akan memberikan senyawa terkonjugasi. Dengan bantuan diskoneksi Wittig akan memberikan senyawa 1,3-dikarbonil (10), dan diskoneksinya lebih lanjut akan memberikan suatu ester (11) dan dikarbonil (10), dan diskoneksinya lebih lanjut akan memberikan suatu ester (11) dan aldehid (12) dengan kerangka molekul yang sama. Karenanya, sinte
aldehid (12) dengan kerangka molekul yang sama. Karenanya, sinte sis dapat dilakukansis dapat dilakukan dengan mereaksikan dua molekul aldehid (12) kemudian
dengan mereaksikan dua molekul aldehid (12) kemudian dioksidasi.dioksidasi.
CO CO22EtEt CO CO22EtEt O O + + Basa Basa MT ( 7 ) MT ( 7 ) --+ + HO HO O O MT ( 8 ) MT ( 8 ) 1,3-diO 1,3-diO O O O O O O basa basa MT ( 8 ) MT ( 8 )