LAPORAN
PRAKTIKUM METODE PENGUKURAN DENGAN INSTRUMEN
Oleh : Kelompok 5
Anggota : Nila Huda 1408100045
Rosidatul Mahmudah 1408100047 Nindya Ayu Yudita 1408100049 Fajri Perdana 1408100051 Bagus Ayatul Jihad 1408100053
LABORATORIUM KIMIA ANALITIK JURUSAN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM INSTITUT TEKNOLOGI SEPULUH NOPEMBER
2
Laporan Praktikum MPI Kelompok 5 ANALISA KADAR CU DENGAN INSTRUMEN1. Tujuan
a. untuk menentukan kadar Cu dalam batuan dengan metode Atomic Absorption Spectroscopy (AAS) dan X-Ray Flouresence (XRF) dan membandingkan hasil dari pengukuran tersebut
b. untuk melakukan simulasi pen.gukuran dengan potensiostat
2. Tinjauan Pustaka
2. 1Atomic Absorption Spectroscopy (AAS)
Atomic Absorption Spectroscopy (AAS) adalah suatu alat yang digunakan pada metode analisis untuk penentuan unsur-unsur logam dan metalloid yang pengukurannya berdasarkan penyerapan cahaya dengan panjang gelombang tertentu oleh atom logam dalam keadaan bebas (Skoog, 2000). Metode ini sangat tepat untuk analisis zat pada konsentrasi rendah. Teknik ini mempunyai beberapa kelebihan dibandingkan dengan metode spektroskopi emisi konvensional. Memang selain dengan metode serapan atom, unsur-unsur dengan energi eksitasi rendah dapat juga dianalisis dengan fotometri nyala, akan tetapi fotometri nyala tidak cocok untuk unsur-unsur dengan energi eksitasi tinggi. Fotometri nyala memiliki range ukur optimum pada panjang gelombang 400-800 nm, sedangkan AAS memiliki range ukur optimum pada panjang gelombang 200-300 nm (Skoog, 2000).
Metode AAS berprinsip pada absorbsi cahaya oleh atom, atom-atom menyerap cahaya tersebut pada panjang gelombang tertentu, tergantung pada sifat unsurnya. Dengan absorpsi energi, berarti memperoleh lebih banyak energi, suatu atom pada keadaan dasar dinaikan tingkat energinya ke tingkat eksitasi. Keberhasilan analisis ini tergantung pada proses eksitasi dan memperoleh garis resonansi yang tepat.
Hukum absorpsi sinar (Lambert-Beer) yang berlaku pada spektrofotometer absorpsi sinar ultraviolet (UV), sinar tampak maupun infra merah, juga berlaku pada AAS. Perbedaan analisis AAS dengan spektrofotometri molekul adalah peralatan dan bentuk spectrum absorpsinya. Setiap alat AAS terdiri atas tiga komponen yaitu:
- Unit atomisasi (atomisasi dengan nyala dan tanpa nyala) - Sumber radiasi
3
Laporan Praktikum MPI Kelompok 5 Gambar 1. Alat Atomic Absorption Spectroscopy (AAS)Unit Atomisasi
Unit Atomisasi merupakan bagian yang penting karena pada tempat ini senyawa akan dianalisa. Pada sistem pengatoman, unsur-unsur yang akan dianalisa diubah bentuknya dari bentuk ion menjadi bentuk atom bebas. Ada beberapa jenis atomisasi yang lazim digunakan pada setiap alat AAS, antara lain:
Atomisasi dengan nyala api Atomisasi dengan tungku grafit Atomisasi dengan pembentukan
hidrida
Atomisasi dengan uap dingin Atomisasi sampel padat
Sumber radiasi
Sumber radiasi merupakan sistem emisi yang diperlukan untuk menghasilkan sinar yang energinya akan diserap oleh atom bebas. Sumber radiasi haruslah bersifat sumber yang kontinyu. Seperangkat sumber yang dapat memberikan garis emisi yang tajam dari suatu unsur yang spesifik tertentu dengan menggunakan lampu pijar Hollow cathode. Lampu ini memiliki 2 elektroda, satu diantaranya berbentuk silindris dan terbuat dari unsur yang sama dengan unsur yang akan dianalisa.
Detektor
Detektor pada AAS berfungsi untuk mengukur intensitas radiasi yang diteruskan dan telah diubah menjadi energy listrik oleh fotomultiplier. Hasil pengukuran detektor dilakukan penguatan dan dicatat oleh alat pencatat yang berupa printer dan pengamat angka.
2
Laporan Praktikum MPI Kelompok 5 Apabila cahaya dengan panjang gelombang tertentu dilewatkan pada suatu sel yang mengandung atom-atom bebas yang bersangkutan maka sebagian cahaya tersebut akan diserap dan intensitas penyerapan akan berbanding lurus dengan banyaknya atom bebas logam yang berada pada sel. Hubungan antara absorbansi dengan konsentrasi diturunkan dari: Hukum Lambert: bila suatu sumber sinar monkromatik melewati medium transparan, maka intensitas sinar yang diteruskan berkurang dengan bertambahnya ketebalan medium yang mengabsorbsi. Hukum Beer: Intensitas sinar yang diteruskan berkurang secara eksponensial dengan bertambahnya konsentrasi spesi yang menyerap sinar tersebut.
Dari kedua hukum tersebut diperoleh suatu persamaan Lambert Beer:
I=Io exp -∈ b c ………… (1a) atau A = log = ∈ b c………… (1b) Dimana: Io = intensitas sumber sinar
I = intensitas sinar yang diteruskan ∈ = absortivitas molar
b = panjang medium
c = konsentrasi atom-atom yang menyerap sinar A = absorbansi (serapan)
Dari persamaan di atas, dapat disimpulkan bahwa absorbansi cahaya berbanding lurus dengan konsentrasi atom (Day & Underwood, 1989).
Metode Analisis Standar adisi
Metode analisis standar adisi dipakai secara luas karena mampu meminimalkan kesalahan yang disebabkan oleh perbedaan kondisi lingkungan (matriks) sampel dan standar. Dalam metode ini dua atau lebih sejumlah volume tertentu dari sampel dipindahkan ke dalam labu takar. Satu larutan diencerkan sampai volume tertentu kemudiaan larutan yang lain sebelum diukur absorbansinya ditambah terlebih dahulu dengan sejumlah larutan standar tertentu dan diencerkan seperti pada larutan yang pertama. Menurut hukum Lambert Beer akan berlaku hal-hal berikut:
A1 = ∈ b cx ………(2a) dan
3
Laporan Praktikum MPI Kelompok 5 Dimana: A1 = Absorbansi sampel (tanpa penambahan standar)A2 = Absorbansi sampel + standar Cx = Konsentrasi sampel
Cs = Konsentrasi larutan standar yang ditambahkan ke larutan sampel Vx = Volume sampel
Vs = Volume larutan standar yang ditambahkan ke larutan sampel Vt = Volume total (sampel + standar)
Jika persamaan (2a) dan (2b) digabung maka akan diperoleh: Cx =
Keuntungan dan kelemahan AAS
Keuntungan metode AAS dibandingkan dengan spektrofotometer biasa yaitu spesifik, batas deteksi yang rendah dari larutan yang sama bisa mengukur unsur-unsur yang berlainan, pengukurannya langsung terhadap contoh, output dapat langsung dibaca, cukup ekonomis, dapat diaplikasikan pada banyak jenis unsur, batas kadar penentuan luas (dari ppm sampai %).
Sedangkan kelemahannya yaitu pengaruh kimia dimana AAS tidak mampu menguraikan zat menjadi atom misalnya pengaruh fosfat terhadap Ca, pengaruh ionisasi yaitu bila atom tereksitasi (tidak hanya disosiasi) sehingga menimbulkan emisi pada panjang gelombang yang sama, serta pengaruh matriks misalnya pelarut.
2. 2X-Ray Flouresence (XRF)
XRF adalah alat yang digunakan untuk menganalisis kandungan unsur dalam bahan yang menggunakan metode spektrometri. Alat ini mempunyai keunggulan analisis yaitu lebih sederhana dan lebih cepat dibanding analisis dengan alat lain. Alat XRF merupakan alat uji tak merusak yang mampu menentukan kandungan unsur dalam suatu bahan padat maupun serbuk secara kualitaif dan kuantitatif dalam waktu yang relatif singkat. XRF merupakan pemancaran sinar X dari atom tereksitasi yang dihasilkan oleh tumbukan elektron berenergi tinggi, partikel-partikel lain, atau suatu berkas utama dari sinar X lain.
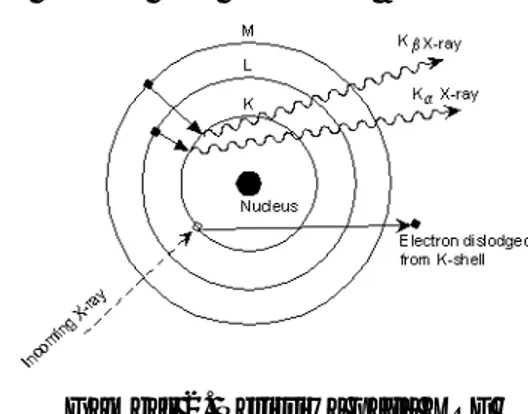
Prinsip kerja dari alat XRF yaitu tabung pembangkit sinar X menembakkan radiasi foton elektromagnetik ke material yang akan diteliti. Radiasi elektromagnetik yang dipancarkan akan berinteraksi dengan elektron yang berada di kulit K suatu unsur. Elektron
4
Laporan Praktikum MPI Kelompok 5 yang berada dikulit K akan memiliki energi kinetik yang cukup untuk melepaskan diri dari ikatan inti, sehingga elektron tersebut akan tereksitasi.Gambar 2. Peristiwa pada XRF
Metode spektrometri merupakan metode analisis suatu bahan dengan peralatan tertentu yang hasil ujinya berupa spektrum (grafik) sumbu X-Y. Pengujian menggunakan alat XRF akan diperoleh hubungan 2 parameter yaitu sumbu X (horisontal) berupa energi unsur dan sumbu Y (vertikal) berupa intensitas cacahan perdetik (cps/ count per second).
Analisis dengan menggunakan XRF dapat dilakukan dengan metode kualitatif maupun kuantitatif. Analisis unsur secara kualitatif hanya memberikan informasi kandungan unsur suatu bahan yang dinyatakan dalam intensitas dengan satuan cps (count per second). Semakin besar intensitas yang muncul, maka semakin banyak kandungan unsur tersebut dalam suatu bahan. Dalam analisis secara kuantitatif, setiap puncak dari unsur yang terkandung dalam bahan tersebut mempunyai kandungan unsur dalam jumlah yang berbeda-beda. Analisis kuantitatif dilakukan menggunakan standar pembanding yang bersertifikat dengan persyaratan untuk menentukan bahan non standar yang akan dianalisis.
5
Laporan Praktikum MPI Kelompok 5 Kelebihan dari metode XRF antara lain: akurasi yang tinggi,
dapat menentukan unsur dalam material tanpa adanya standar,
dapat menentukan kandungan mineral baik dalam bahan biologis maupun dalam tubuh secara langsung.
Kelemahan dari metode XRF antara lain:
tidak dapat mengetahui senyawa apa yang dibentuk oleh unsur-unsur yang terkandung dalam material yang akan diteliti,
tidak dapat menentukan struktur dari atom yang membentuk material itu.
2. 3Potensiostat
Potensiostat merupakan alat elektronik yang mengontrol beda potensial antara elektroda kerja dan elektroda pembanding dalam suatu sel elektrokimia yang tersusun atas tiga elektroda, yaitu elektroda kerja (working electrode), elektroda pembanding (reference electrode) dan elektroda pendukung (counter electrode). Contoh fisik potensiostat ini ditujukan pada gambar dibawah ini.
Gambar 4. Alat Potensiostat
Elektroda pembanding adalah elektroda yang potensialnya dibuat konstan sehinnga dapat digunakan sebagai pembanding terhadap perubahan yang terjadi pada elektroda kerja. Fungsi elektroda pambanding adalah sebagai penstabil beda potensial pada kerja dalam sel eletrokimia .Elektroda pembanding yang biasa digunakan adalah elektroda kalomel dan Ag/AgCl.Elektroda Ag/agCl ini dapat dibuat dengan mudah melalui elektrolisis larutan klorida menggunakan anoda perak,sehinngga membentuk lapisan elektrolit AgCl pada permukaan kawat perak (Pramasasti, 2007).
Elektroda pendukung adalah elektroda yang berperan sebagai sumber atau tempat masuknya electron sehingga arus dapat dilewatkan melalui sel. Elektroda pendukung yang biasa digunakan adalah platina (Pt) yang dapat berupa kawat lurus, kawat spiral atau cakram
6
Laporan Praktikum MPI Kelompok 5 (disk). Zat lain yang bersifat inert seperti karbon dan grafit pun dapat juga digunakan sebagai elektroda pendukung (Pramasasti, 2007).Elektroda kerja adalah elektroda tempat reaksi reduksi – oksidasi analit berlangsung. Elektroda ini umumnya terbuat dari logam, bahan semikonduktor,dan juga karbon. Elektroda logam yang sering digunakan adalah platina (Pt), emas (Au) dan perak (Ag). Sedangkan elektroda semikonduktor yang umumnya digunakan adalah silicon (Si) dan gallium (Ga). Untuk elektroda karbon terdapat beberapa jenis yaitu pasta, glassy carbon dan juga pyrolitic graphite (Pramasasti, 2007)
Penggunaan elektrolit di dalam sel elektrokimia juga merupakan hal yang penting disamping elektroda. Elektrolit berfungsi sebagai medium penghantar dimana transfer muatan terjadi melalui pergerakan ion-ion elektrolit tersebut. Larutan elektrolit yang digunakan harus menghantarkan arus listrik dan tidak mengganggu reaksi kimia yangterjadi. Elektrolit dapat berupa larutan garam atau padatan konduktor. Untuk menambah konduktivitas dari elektrolit kadang perlu ditambahkan suatu elektrolit pendukung seperti larutan garam anorganik, asam atau basa (Aurelia,2005).
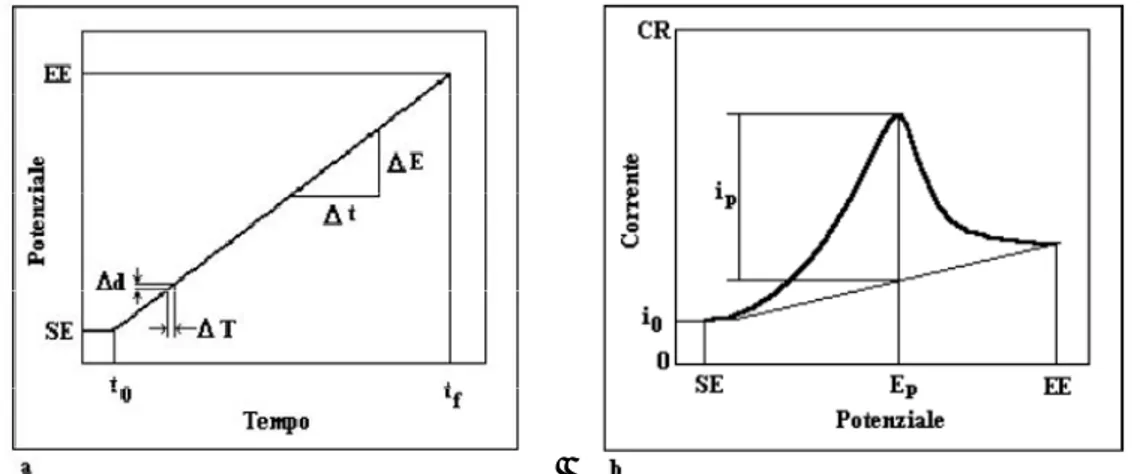
Potensial yang diterapkan pada elektroda dalam teknik voltametri ini bisa bermacam-macam, yang menghasilkan beberapa varian teknik voltametri diantaranya adalah : LSV (linear sweep voltammetry), CV (cyclic voltammetry), DPV (differensian pulse voltammetry) dan SWV (square wave voltammetry).
a. LSV (linear sweep voltammetry)
Linear sweep voltammetry adalah istilah umum untuk suatu teknik voltametri dimana potensial yang diberikan pada elektroda kerja dengan variasi waktu linier. Metode ini juga mencakup polarography, siklik voltametri rotating disc voltametri. Slope yang dihasilkan dari metode ini memiliki unit potensial (volt) per satuan waktu, dan biasanya disebut scan rate
percobaan.
b. CV (cyclic voltammetry)
Cyclic voltammetry adalah yang paling umum digunakan dalam teknik elektrokimia, dan berdasarkan pada kelinieran potensial dari kurva. Sehingga perubahan potensial sebagai fungsi linier dari waktu. Tingkat perubahan potensial dengan waktu mengarah pada scan rate. c. DPV (differensian pulse voltammetry)
Differensian pulse voltammetry diperoleh dengan menambahkan secara periodic pulse potensial (meningkatkan potensial sementara) untuk menjalankan voltase yang digunakan
7
Laporan Praktikum MPI Kelompok 5 pada LSV. Arus diukur hanya khusus untuk pulse dan diakhiri pada penerapan pulse. Perbedaan antara kedua arus diplotkan sebagai fungsi jalur potensial pada LSV.3. Metodologi 3. 1Alat dan Bahan
Peralatan yang digunakan untuk analisa Cu adalah satu set alat AAS, XRF, potensiostat, beaker gelas, labu ukur, pengaduk, mortar, kaca arloji, pengayak, dan penangas.
Bahan-bahan yang digunakan adalah sampel batuan, HNO3 pekat, aquadest, padatan
CuSO4 , kertas saring dan gas argon (Ar).
3. 2Prosedur Kerja
a. Atomic Absorption Spectroscopy (AAS) Destruksi Batuan untuk analisa AAS
Tumbuk halus sebanyak 1 gr sample batuan dengan ukuran 60 mesh dan masukkan dalam Erlenmeyer 100 mL. Tambahkan 15 mL HNO3 pekat kemudian panaskan pada suhu
90° C. ketika volume larutan tinggal 1/3 (asap coklat mulai hilang), tambahkan 25 mL aquademin / aquades lalu saring larutan. Cuci residu yang dihasilkan dengan aquades 5 mL sebanyak 3 kali. sedangkan filtrat diencerkan kembali sampai 100 mL . Larutan siap diguanakan untuk analisis.
Pembuatan Larutan Standar CuSO4
Timbang padatan CuSO4 sebanyak 7,980 gram, kemudian masukkan dalam beaker
gelas dan larutkan dengan sedikit aquades. Aduk hingga larut. Lalu masukkan larutan dalam labu ukur 50 mL, tambahkan aquades hingga tanda batas dan kocok. Larutan siap digunakan untuk analisis.
Pengukuran Absorbansi dengan AAS
Ukur absorbansi larutan sampel dengan AAS menggunakan metode standar adisi dengan larutan standar CuSO4.
run Perlakuan
1 10 mL larutan sampel
2 10 mL larutan sampel + 0,5 mL larutan standar CuSO4 1 M
3 10 mL larutan sampel + 1,0 mL larutan standar CuSO4 1 M
8
Laporan Praktikum MPI Kelompok 5 Cara mengoperasikan AAS sebagaimana dalam Lampiran 1.b. X-ray Diffraction Preparasi Sampel
Ambil beberapa bongkah batuan. Gerus sampel batuan tersebut dengan mortar besi. Kemudian lanjutkan penghalusan dengan mortar dan cawan porselin sampai halus sempurna. Ayak sampel hingga didapat ukuran butiran yang homogen. Timbang sampel yang sudah halus sebanyak 10 gram.
Analisa Sampel dengan Metode XRF
Masukkan sampel kedalam P1 (tempat sampel pada XRF) hingga tinggi sampel 1/3 dari tinggi P1. Kemudian press sampel menggunakan hydraulic press. Masukkan sampel yang sudah di-press kedalam alat XRF. Kemudian analisa dengan XRF.
c. Potensiostat
Pengukuran dengan menggunakan Potensiostat dilihat pada simulasi penggunaan alat potensiostat berikut. Pertama “on”kan tombol bagian belakang alat potensiostat. Kemudian buka aplikasi eChem dan dipilih “techniq” pada toolbal. Selanjutnya “linear sweep voltametri” dipilih dan diset potensialnya, rate, dan lengthnya. Kemudian klik pada view. Pengukuran dengan metode differensial pulse voltametri dan Cycle Voltametri dilakukan langkah yang sama. Pada saat pengukuran, 3 jenis elektroda, yaitu elektroda kerja, elektroda pembanding dan elektroda kerja dijepitkan pada penjepit yang sesuai.
4. Hasil dan Pembahasan
4. 1Atomic Absorption Spectroscopy (AAS)
Pada analisa AAS ini, sampel yang digunakan didestruksi dari batuan. Di mana pada proses destruksi, batuan yang telah digerus dilaruttkan dalam asam nitrat pekat (HNO3).
Larutan HNO3 digunakan karena larutan ini mampu melarutkan semua logam dalam sampel
batuan. Pemanasan pada suhu 90°C bertujuan untuk menguapkan pengotor yang mungkin ada dalam sampel.
Percobaan ini dilakukan dengan metode standar adisi. Metode standar adisi dilakukan dengan penambahan larutan standar berkonsentrasi tinggi dengan volume yang sedikit pada larutan sampel. Metode ini digunakan untuk meminimalisir adanya kesalahan karena
9
Laporan Praktikum MPI Kelompok 5 perbedaan matriks antara sampel dan standar. Dalam hal ini, larutan standar yang digunakan adalah CuSO4 1 M dengan volume standar 0,5 mL; 1,0 mL dan 1,5 mL.Pengukuran sampel dengan AAS diawali dengan membuka tabung gas, kompresor dan ducting terlebih dahulu. Kompresor berfungsi untuk mensuplai kebutuhan udara yang akan digunakan oleh AAS pada waktu pembakaran atom. Sedangkan ducting berfungsi untuk menyedot asap atau sisa pembakaran pada AAS, yang langsung dihubungkan pada cerobong asap bagian luar, agar asap yang dihasilkan oleh AAS tidak berbahaya bagi lingkungan sekitar.
Setelah masuk dalam program AAS, maka harus dipilih lampu yang sesuai untuk analisis sehingga energi yang diberikan lampu hanya dapat mengeksitasi logam yang ingin dianalisis. Di mana pada percobaan ini lampu yang digunakan untuk analisis Cu adalah lampu No. 4. Saat pengukuran, sampel diatomisasi dengan menggunakan nyala sehingga logam yang berada di dalam larutan akan mengalami eksitasi dari energi rendah ke energi tinggi ketika diberikan sinar dari sumber radiasi.
Berdasarkan data, diperoleh konsentrasi sampel sebagai berikut: 0,5067 M, 0,6679 M dan 0,7053 M, di mana rata-rata persen transmitan yang diperoleh pada percobaan ini adalah 0,38 %. Hal ini menunjukkan banyaknya Cu yang diabsorp pada saat analisa. Sehingga hasil analisa bisa dipertimbangkan.
4. 2X-Ray Flouresence (XRF)
Pada analisa XRF ini sampel yang dianalisa digerus terlebih dahulu, untuk memperoleh luas permukaan merata saat ditempatkan pada tempat sampel (P1). Sample yang telah dimasukkan kemudian ditutup dengan plastik dan dipres, serta tidak boleh kusut. Hal ini bertujuan agar sinar X yang ditembakkan tepat menembus sampel. Tidak semua sampel bisa dianalisa dengan XRF. Syarat-syarat sampel yang dapat dianalisa dengan XRF antara lain:
untuk sampel serbuk ukurannya < 4 mesh,
untuk sampel padatan harus datar untuk menghasilkan analisis kuantitatif yang optimal dan permukaan yang dilapisi akan meminimalisir efek penghamburan.
untuk sampel cairan tidak boleh mengandung endapan dan dalam keadaan segar ketika dianalisis. Analisis dilakukan secara cepat jika sampel mudah menguap.
Energi yang digunakan untuk analisa Cu sebesar 14 kV agar elektron pada logam Cu yang berada di kulit terdalam tereksitasi. Sedangkan filter yang digunakan adalah Ag, filter ini berguna untuk mencegah ganguan dari unsur lain.
10
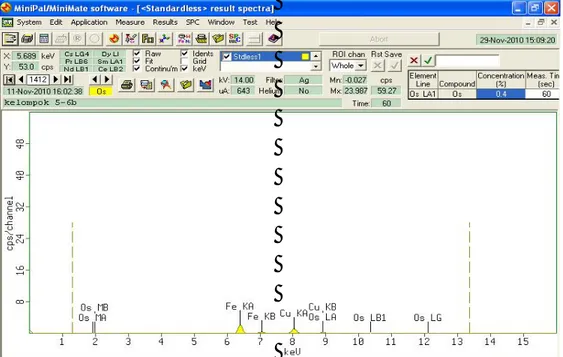
Laporan Praktikum MPI Kelompok 5 Dari analisa sampel batuan dengan alat XRF ini, menghasilkan spektra melalui aplikasi MiniPal/MiniMate Software. Gambar spektra dapat ditunjukkan sebagai berikut:Gambar 5. Spectra yang Ditunjukkan oleh Analisa Sampel 1
Berdasarkan grafik diatas dapat diketahui persentase Cu dalam sample 37%, Fe 72% dan OS 0,8%.
Gambar 6. Spektra yang Ditunjukkan oleh Analisa Sampel 2
11
Laporan Praktikum MPI Kelompok 5 4. 3PotensiostatPada simulasi dengan menggunakan potensiostat ini digunakan 3 metode, yaitu Linear Sweep Voltametri (LSV), Differensial Pulse Voltametri (DPV) dan Cycle Voltametri (CV). Karena tidak ada sample yang dianalisis, maka kita hanya dapat mengetahui grafik inputnya. Apabila ada sample yang dianalisa maka diperoleh grafik outputnya. Grafik masing-masing metode adalah sebagai berikut.
Gambar a. Grafik input dan output LSV
12
Laporan Praktikum MPI Kelompok 5 Gambar c. Grafik input dan output DPVJika dimisalkan sampel yang diuji bervolume 10 mL dengan volume standar adisi 0,5 mL; 1,0 mL dan 1,5 mL dengan arus awal diatur 80 µA dan arus akhir 100 µA, maka diperoleh konsentrasi sampel masing-masing 0,16 M; 0,267 M dan 0,343 M.
5. Kesimpulan
Konsentrasi Cu dalam sampel yang diuji dengan AAS adalah 0,5067 M, 0,6679 M dan 0,7053 M
Prosentase Cu dalam sampel yang diuji dengan XRF adalah 37 % dan 40 %
Hasil simulasi analisa dengan potensiostat diperoleh tipikal input dan output yang berbeda untuk metode yang berbeda.
Daftar Pustaka
Aurelia, Inezia. 2005. Studi Modifikasi Glassy karbon dengan Teknik Elektrodeposisi Iridium Oksida untuk Aplikasi sebagai Elektroda Sensor Arsen (III). Karya Utama Sarjana Kimia. Departemen Kimia. FMIPA-UI
Pramasasti, Sisma. 2007. Modifikasi Elektroda Emas dengan EDTA untuk Mengidentifikasi Ion Hg2+. Karya Utama Sarjana Kimia. Departemen Kimia. FMIPA-UI
Skoog, West, Holler, Crouch. 2000. Fundamental of Analytical chemistry. Thomson Brook/Cole
13
Laporan Praktikum MPI Kelompok 5 Lampiran 1Cara mengoperasikan AAS
a. Pertama-tama gas di buka terlebih dahulu, kemudian kompresor, lalu ducting, main unit, dan komputer secara berurutan.
b. Di buka program SAS (Spectrum Analyse Specialist), kemudian muncul perintah ”apakah ingin mengganti lampu katoda, jika ingin mengganti klik Yes dan jika tidak No.
c. Dipilih yes untuk masuk ke menu individual command, dimasukkan nomor lampu katoda yang dipasang ke dalam kotak dialog, kemudian diklik setup, kemudian soket lampu katoda akan berputar menuju posisi paling atas supaya lampu katoda yang baru dapat diganti atau ditambahkan dengan mudah.
d. Dipilih No jika tidak ingin mengganti lampu katoda yang baru.
e. Pada program SAS 3.0, dipilih menu select element and working mode. Dipilih unsur yang akan dianalisis dengan mengklik langsung pada symbol unsur yang diinginkan f. Jika telah selesai klik ok, kemudian muncul tampilan condition settings. Diatur parameter
yang dianalisis dengan mensetting fuel flow : 1,2 ; measurement; concentration ; number of sample : 2 ; unit concentration : ppm ; number of standard : 3 ; standard list : 1 ppm, 3 ppm, 9 ppm.
g. Diklik ok and setup, ditunggu hingga selesai warming up.
h. Diklik icon bergambar burner/ pembakar, setelah pembakar dan lampu menyala alat siap digunakan untuk mengukur logam.
i. Pada menu measurements pilih measure sample.
j. Dimasukkan blanko, didiamkan hingga garis lurus terbentuk, kemudian dipindahkan ke standar 1 ppm hingga data keluar.
k. Dimasukkan blanko untuk meluruskan kurva, diukur dengan tahapan yang sama untuk standar 3 ppm dan 9 ppm.
l. Jika data kurang baik akan ada perintah untuk pengukuran ulang, dilakukan pengukuran blanko, hingga kurva yang dihasilkan turun dan lurus.
m. Dimasukkan ke sampel 1 hingga kurva naik dan belok baru dilakukan pengukuran. n. Dimasukkan blanko kembali dan dilakukan pengukuran sampel ke 2.
o. Setelah pengukuran selesai, data dapat diperoleh dengan mengklik icon print atau pada baris menu dengan mengklik file lalu print.
14
Laporan Praktikum MPI Kelompok 5 p. Apabila pengukuran telah selesai, aspirasikan air deionisasi untuk membilas burnerselama 10 menit, api dan lampu burner dimatikan, program pada komputer dimatikan, lalu main unit AAS, kemudian kompresor, setelah itu ducting dan terakhir gas.
15
Laporan Praktikum MPI Kelompok 5 Lampiran 2Penurunan persamaan Lambert Beer untuk metode standar adisi A1 = ∈ b cx ………(2a) dan
A2 = ∈ b cx + ∈ b cs ………(2b)
Karena persamaan (2a) merupakan persamaan Lambert Beer untuk sampel tanpa standar, sedangkan persamaan (2b) merupakan persamaan Lambert Beer untuk sampel dengan standar. Maka nilai pada persamaan (2a) adalah 1. Sehingga (2a) menjadi: A1 = ∈ b cx
Dari kedua persamaan di atas, maka:
= ∈b c + ∈b c ∈b c = ∈b c + ∈b c ∈b c = ∈b ( c + c ) ∈b c c = c + c c − c = c c − c = c c ( − ) = c c = c ( − )
16
Laporan Praktikum MPI Kelompok 5 Lampiran 3Perhitungan AAS
Data Hasil absorbansi AAS :
a. 10 mL sampel A = 2,3364
b. 10 mL sampel + 0,5 mL CuSO4 1 M A = 2,4447
c. 10 mL sampel + 1,0 mL CuSO4 1 M A = 2,4420
d. 10 mL sampel + 1,5 mL CuSO4 1 M A = 2,4638
Perhitungan konsentrasi Cu
Berdasarkan hasil penurunan rumus di atas, maka konsentrasi sampel (Cx) dapat ditentukan dengan perhitungan di bawah ini:
c = c
( − )
Untuk data (a) dan (b)
c = 2,3364 . 1M . 0,5 mL
2,4447 . 10,5 mL− 2,3364 . 10 mL= 0,5067 M
Untuk data (a) dan (c)
c = 2,3364 . 1M . 1,0 mL
2,4420 . 11 mL− 2,3364 . 10 mL= 0,6679 M
Untuk data (a) dan (d)
c = 2,3364 . 1M . 1,5 mL
2,4638 . 11,5 mL− 2,3364 . 10 mL= 0,7053 M
Perhitungan Transmitan (%)
Dari data absorbansi, maka besarnya transmitan dapat dihitung dengan persamaan: A = -log T T (%) = 10 -A x 100 %
Jadi, Untuk A1; T (%) = 10 -A x 100 % = 10 -2,3364 x 100 % = 0,46 % Untuk A2; T (%) = 10 -A x 100 % = 10 -2,4447 x 100 % = 0,36 %
Untuk A3; T (%) = 10 -A x 100 % = 10 -2,4420 x 100 % = 0,36 % Untuk A4; T (%) = 10 -A x 100 % = 10 -2,4638 x 100 % = 0,34 %
17
Laporan Praktikum MPI Kelompok 5 Lampiran 4 Perhitungan Potensiostat Diketahui : Vsampel = 10 mL Vstandar = 0,5 mL, 1 mL dan 1,5 mL C standar = 1 M i1 = 80 µA i2 = 100 µA Ditanya : Cs? Penyelesaian : i1 = k. Cs Cs = 80/K ... (1) i1 = K . . ... (2) Untuk Vst = 1 mL 100 = K . . 100 = K 100 = K 100 = 1100 = 800 + K K = 1100 – 800 = 300 µA/Mmaka, nilai Cs adalah .... Cs = = µ
µ / = 0,267 M
Dengan cara yang sama,
harga Cs untuk Vst = 0,5 mL adalah 0,16 M harga Cs untuk Vst = 1,5 mL adalah 0,343 M