i TESIS
EFEKTIFITAS MEMBRAN KHITOSAN DARI KULIT UDANG GALAH (Macrobanchium rosenbergii)
UNTUK MENURUNKAN FOSFAT DALAM AIR LIMBAH LAUNDRY
NI MADE YUNARSIH
PROGRAM PASCASARJANA UNIVERSITAS UDAYANA
DENPASAR
2013
ii
EFEKTIFITAS MEMBRAN KHITOSAN DARI KULIT UDANG GALAH (Macrobanchium rosenbergii)
UNTUK MENURUNKAN FOSFAT DALAM AIR LIMBAH LAUNDRY
NI MADE YUNARSIH NIM. 1092061006
PROGRAM MAGISTER PROGRAM STUDI KIMIA TERAPAN
PROGRAM PASCASARJANA UNIVERSITAS UDAYANA
DENPASAR
2013
iii
EFEKTIFITAS MEMBRAN KHITOSAN DARI KULIT UDANG GALAH (Macrobanchium rosenbergii)
UNTUK MENURUNKAN FOSFAT DALAM AIR LIMBAH LAUNDRY
Tesis untuk Memperoleh Gelar Magister
pada Program Magister, Program studi Kimia Terapan Program Pascasarjana Universitas Udayana
NI MADE YUNARSIH NIM. 1092061006
PROGRAM MAGISTER PROGRAM STUDI KIMIA TERAPAN
PROGRAM PASCASARJANA UNIVERSITAS UDAYANA
DENPASAR
2013
iv
Lembar Pengesahan
TESIS INI TELAH DISETUJUI TANGGAL 16 September 2013
Pembimbing I Pembimbing II
Dr. Ketut Gede Dharma Putra, M.Sc Dr. Manuntun Manurung, M.S NIP. 19601007 198603 1 001 NIP. 19610525 199009 1 001
Mengetahui
Ketua Program Studi Kimia Terapan, Direktur
Program Pascasarjana Program Pascasarjana
Universitas Udayana Universitas Udayana
Prof. Dr. I Made Dira Swantara, M.Si Prof. Dr. dr. A.A. Raka Sudewi,Sp.S(K) NIP. 19540101 198603 1 001 NIP. 19590215 198510 2 001
v
Tesis Ini Telah Diuji pada Tanggal 16 September 2013
Panitia Penguji Tesis Berdasarkan SK Rektor Universitas Udayana
No: tanggal 16 September 2013
Ketua : Dr. Drs. Ketut Gede Dharma Putra, M.Sc.
Sekretaris : Dr. Drs. Manuntun Manurung, M.S.
Anggota :
1. Prof. Dr. Drs. I Made Dira Swantara, M.Si.
2. Prof. Dr. Ir. Ida Bagus Putra Manuaba, M.Phil.
3. Dr. Dra. Ni Made Suaniti, M.si.
vi
UCAPAN TERIMAKASIH
Puji syukur penulis panjatkan kehadapan Tuhan Yang Maha Esa/ Ida Sang Hyang Widhi Wasa , karena atas berkat dan rahmat-Nya tesis ini dapat diselesaikan.
Pada kesempatan ini perkenankanlah penulis mengucapkan terimakasih yang sebesar-besarnya kepada Dr. Drs. Ketut Gede Dharma Putra, M.Sc. dan Dr.
Drs. Manuntun Manurung, M.S. sebagai pembimbing I dan II yang dengan sungguh-sungguh memberikan dorongan, semangat dan bimbingan selama penulis menyelesaikan tesis ini.
Penulis juga mengucapkan terimakasih yang tulus kepada Ketua Program Studi Kimia Terapan, Program Pascasarjana Universitas Udayana yang dijabat oleh Prof. Dr. Drs. I Made Dira Swantara, M.Si. atas kesempatan dan petunjuk yang diberikan sehingga penulis bisa mengikuti dan menyelesaikan pendidikan di Program Pascasarjana Universitas Udayana. Ucapan terimakasih penulis juga disampaikan kepada Direktur Program Pascasarjana Universitas Udayana yang dijabat oleh Prof. Dr. dr. A. A. Raka Sudewi, Sp.S(K) atas kesempatan yang telah diberikan kepada penulis untuk mengikuti dan menjadi mahasiswa Program Pascasarjana Universitas Udayana. Terimakasih sepenuhnya penulis ucapkan kepada para penguji tesis yaitu Prof. Dr. Drs. I Made Dira Swantara, M.Si. Prof.
Dr. Ir. Ida Bagus Putra Manuaba, M.Phil. Dr. Dra. Ni Made Suaniti, M.si. yang telah berkenan memberikan saran, masukan dan kritikan yang bersifat membangun sehingga tesis ini menjadi lebih baik. Ucapan terimakasih juga penulis tujukan kepada semua pihak yang telah mendukung dan membantu sampai penulis dapat menyelesaikan tesis ini.
Semoga Tuhan Yang Maha Esa/ Ida Sang Hyang Widhi Wasa senantiasa memberikan rahmatnya dan menunjukkan cahaya terang dalam setiap langkah kita semua untuk memajukan ilmu pengetahuan.
Denpasar, 16 September 2013 Penulis
vii ABSTRAK
EFEKTIFITAS MEMBRAN KHITOSAN DARI KULIT UDANG GALAH (Macrobanchium rosenbergii) UNTUK MENURUNKAN FOSFAT DALAM
AIR LIMBAH LAUNDRY
Penanggulangan terhadap pencemaran air limbah yang mengandung senyawa fosfat terutama yang berasal dari air limbah laundry dapat dilakukan dengan menggunakan teknologi membran. Membran dapat dibuat dari bahan polimer alam yaitu senyawa khitosan yang diperoleh dari khitin yang terdapat di dalam kulit udang. Khitin yang diperoleh dari kulit udang galah dapat diubah menjadi khitosan melalui proses deasetilasi dengan menggunakan NaOH 50%.
Kualitas khitosan yang diperoleh pada penelitian ini ditentukan dengan FTIR diperoleh derajat deasetilasi (DD) 66.27%. Khitosan dilarutkan dalam asam asetat 1%, selanjutnya digunakan untuk membuat membran dengan variasi konsentrasi khitosan 1%, 2%, 3%, 4% dan 5%. Membran tersebut digunakan untuk menurunkan kadar foksfat larutan standar KH2PO4 10 ppm dengan waktu kontak 30, 60, 90 dan 120 menit.
Membran khitosan 3% dan waktu kontak 60 menit merupakan membran terbaik karena mampu menurunkan kadar fosfat larutan standar KH2PO4 10 ppm secara optimal. Kondisi ini diaplikasikan untuk menurunkan kadar fosfat total yang terdapat dalam air limbah laundry. Hasil pengamatan menunjukkan dapat menurunkan kadar fosfat total sampai 97.40% setelah dilakukan filtrasi empat kali dan perubahan pH larutan dari 9 menjadi 8.
Kata kunci : Derajat deasetilasi, Membran Khitosan, Fosfat.
viii ABSTRACT
THE EFFECTIVENESS OF CHITOSAN MEMBRANE MADE OF CRAYFISH SHRIMP SHELL (Macrobanchium Rosenbergii) TO REDUSE
PHOSPHATE IN WASTEWATER OF LAUNDRY
Countermeasures against pollution waste water containing phosphate compounds derived primarily from laundry wastewater can be performed using membrane technology . Membranes can be made from natural polymers are compounds derived from chitin chitosan contained in the shrimp shells. Chitin obtained from prawn shell can be converted to chitosan by deacetylation process using 50% NaOH. Quality chitosan obtained in this study was determined by FTIR obtained degree of deacetylation ( DD ) 66.27 %. Chitosan dissolved in 1%
acetic acid, then used to make membranes with various concentrations of chitosan 1%, 2%, 3%, 4% and 5%. The membrane is used to reduce levels of phosphate standard solution of KH2PO4 10 ppm with a contact time 30, 60, 90 and 120 minutes.
3 % chitosan membrane and contact time of 60 minutes is the best because the membrane is able to reduce levels of phosphate standard solution of 10 ppm KH2PO4 optimally. This condition is applied to reduce the total phosphate content contained in laundry wastewater. The results showed lower levels of phosphate can total up to 97.40 % after filtration four times and the pH of the solution changes from 9 to 8.
Keyword : degree of deacetylation, chitosan membrane, phosphate.
ix
RINGKASAN
EFEKTIFITAS MEMBRAN KHITOSAN DARI KULIT UDANG GALAH (Macrobanchium rosenbergii) UNTUK MENURUNKAN FOSFAT DALAM
AIR LIMBAH LAUNDRY
Usaha pelestarian lingkungan dan upaya menekan timbulnya dampak terhadap pencemaran lingkungan dari limbah cair yang berasal dari limbah laundry dapat dilakukan dengan menggunakan metode dari yang paling sederhana sampai penggunaan teknologi membran. Membran merupakan suatu selaput semipermaeabel yang dapat melewatkan komponen tertentu dan menahan material yang lain. Membran dapat dibuat dari bahan polimer ataupun keramik, pada penelitian ini dipilih polimer yang melimpah keberadaannya di alam seperti senyawa khitosan yang terdapat pada khitin dari kulit udang.
Penelitian ini berjudul “Efektifitas Membran Khitosan dari Kulit Udang Galah (Macrobanchium rosenbergii) untuk Menurunkan Fosfat dalam Air Limbah Laundry” bertujuan untuk mengetahui pada konsentrasi berapa khitosan sebagai membran dapat menurunkan kadar fosfat total termasuk mengetahui besarnya fluks yang dihasilkan dari membran khitosan. Senyawa khitosan dapat diperoleh dari proses deasetilasi khitin dengan basa kuat. Khitosan yang dihasilkan dari penelitian ini memiliki derajat deasetilasi (DD) 66.27% dan digunakan membuat membran dengan melarutkan khitosan dalam asam asetat 1%. Membran khitosan dibuat dalam berbagai kosentrasi khitosan mulai dari 1%, 2%, 3%, 4% dan 5%, selanjutnya dipergunakan untuk menurunkan kadar fosfat dalam larutan standar fosfat 10 ppm dengan waktu kontak 30, 60, 90 dan 120 menit.
Membran khitosan secara optimum dapat menurunkan kadar fosfat dalam larutan standar fosfat 10 ppm yaitu pada konsentrasi 3% dan waktu kontak 60 menit. Kondisi ini diaplikasikan untuk menurunkan kadar fosfat total yang terdapat pada air limbah laundry. Melalui proses penyaringan (filtrasi) bertingkat diperoleh penurunan kadar fosfat total dalam air limbah laundry mencapai 97.40%
setelah empat kali filtrasi sedangkan fluks membran optimum dengan melewatkan air pada membran khitosan diperoleh pada konsentrasi membran 3%.
x DAFTAR ISI
Halaman
SAMPUL ... i
ABSTRAK ... v
ABSTRACT ... vi
RINGKASAN ... vii
DAFTAR ISI ... viii
DAFTAR GAMBAR ... xi
DAFTAR TABEL ... xii
DAFTAR LAMPIRAN ... xiii
BAB I PENDAHULUAN 1.1 Latar Belakang ... 1
1.2 Rumusan Masalah ... 5
1.3 Tujuan Penelitian ... 5
1.4 Manfaat Penelitian ... 6
BAB II TINJAUAN PUSTAKA 2.1 Detergen ... 7
2.1.1 Fosfat ... 9
2.1.2 Pemisahan Fosfat ... 11
2.2 Pengertian Membran Secara Umum ... 11
2.2.1 Parameter Utama Proses Pemisahan Membran ... 13
2.2.2 Model Aliran Umpan pada Membran ... 16
2.3 Klasifikasi Membran ... 17
2.3.1 Membran Ultrafiltrasi ... 18
2.3.2 Mekanisme Transfort pada Membran UF ... 21
2.4 Khitin dan Khitosan ... 25
2.5 Derajat Deasetilasi ... 31
2.6 Tinjauan tentang Spektro Ultra Violet-Visible (UV-Vis) .... 32
xi
BAB III KERANGKA KONSEP DAN HIPOTESIS
3.1. Kerangka Konsep ... 35
3.2. Hipotesis ... 37
BAB IV METODE PENELITIAN 4.1 Metode Penelitian... 38
4.2 Ruang Lingkup Penelitian ... 38
4.3 Rancangan Penelitian ... 38
4.4 Tempat dan Waktu Penelitian ... 39
4.5 Bahan dan Alat Penelitian ... 39
4.5.1 Bahan Penelitian ... 39
4.5.2 Alat Penelitian ... 39
4.6 Prosedur Penelitian... 40
4.6.1 Isolasi Khitin dari Kulit Udang ... 40
4.6.1.1 Pembuatan Tepung Kulit Udang ... 40
4.6.1.2 Proses Deproteinasi ... 40
4.6.1.3 Proses Demineralisasi ... 41
4.6.1.4 Proses Depigmentasi ... 41
4.6.1.5 Uji Khitin ... 41
4.6.2 Proses Deasetilasi Khitin menjadi Khitosan ... 42
4.6.3 Pembuatan Membran Khitosan ... 42
4.6.4 Analisis Uji Tarik ... 43
4.6.5 Analisis Fosfat dalam Air Limbah Laundry dengan Spektro UV-Vis ... 43
4.6.6 Proses Pengolahan air Limbah Laundry dengan Membran Khitosan ... 43
BAB V HASIL PENELITIAN 5.1 Isolasi Khitin dari Kulit udang ... 45
5.1.1 Tepung Kulit Udang ... 45
5.1.2 Proses Deproteinasi ... 45
5.1.3 Proses Demineralisasi ... 46
xii
5.1.4 Uji Khitin ... 47
5.2 Proses Deastilasi Khitin Menjadi Khitosan... 47
5.3 Pembuatan Membran Khitosan ... 48
5.4 Analisis Uji Tarik ... 49
5.5 Pembuatan Kurva Kalibrasi dengan Larutan Standar Fosfat ... 55
5.6 Hasil Pengukuran Fluks Membran Khitosan Menggunakan Air... 55
5.7 Proses Pengolahan Air Limbah Laundry dengan Membran Khitosan ... 56
BAB VI PEMBAHASAN 6.1 Isolasi Khitin dari Kulit udang ... 58
6.1.1 Proses Deproteinasi ... 58
6.1.2 Proses Demineralisasi ... 58
6.2 Proses Deastilasi Khitin Menjadi Khitosan... 60
6.3 Pembuatan Membran Khitosan ... 61
6.4 Analisis Uji Tarik ... 62
6.5 Pembuatan Kurva Kalibrasi Standar Fosfat ... 64
6.6 Perhitungan Fluks Membran Khitosan dengan Menggunakan Air... 64
6.7 Proses Pengolahan Air Limbah Laundry dengan Membran Khitosan ... 65
BAB VII SIMPULAN DAN SARAN 7.1 Simpulan ... 69
7.2 Saran ... 69
DAFTAR PUSTAKA ... 71
LAMPIRAN ... 76
xiii
DAFTAR GAMBAR
Halamam
Gambar 2.1. Lambang Umum untuk Surfaktan ... 8
Gambar 2.2. Proses Pemisahan Membran ... 12
Gambar 2.3. Fluks sebagai Fungsi dari Waktu ... 15
Gambar 2.4. Model Proses Aliran Umpan pada Operasi Membran ... 17
Gambar 2.5. Struktur Cross-Section Membran UF Simetrik dan Asimetrik ... 20
Gambar 2.6. Konsep Dasar Pemisahan dengan Membran dan Polarisasi Konsentrasi pada Kondisi Steady-State ... 22
Gambar 2.7. Tipe Resistensi pada Membran saat Perpindahan Massa Melewati Membran dengan Driving Force Tekanan ... 25
Gambar 2.8. Struktur Senyawa Khitin ... 26
Gambar 2.9. Adisi Nukleofilik Bentuk Anion ... 29
Gambar 2.10. Transfer Proton pada Anion ... 30
Gambar 2.11. Tahap Protonasi pada Nitrogen Amida ... 30
Gambar 2.12. Tahap Pelepasan N Terprotonasi ... 31
Gambar 2.13. Mekanisme Serapan UV-Vis... 34
Gambar 3.1. Kerangka Konsep Penelitian ... 37
Gambar 5.1.a. Kulit Udang ... 45
Gambar 5.1.b. Tepung Kulit Udang ... 45
Gambar 5.2.a. Pengaduk Magnetik ... 46
Gambar 5.2.b. Khitin Kasar ... 46
Gambar 5.3. Khitin ... 46
Gambar 5.4. Khitosan ... 48
Gambar 5.5. Membran Khitosan ... 49
Gambar 6.1. Grafik Hubungan antara Tegangan dan Regangan Membran Khitosan ... 63
xiv
DAFTAR TABEL
Halaman
Tabel 2.1. Karakteristik Khitin Kulit Udang ... 27
Tabel 2.2. Karakteristik Khitosan Kulit Udang ... 29
Tabel 5.1. Hasil Karakteristik Khitin Kulit Udang ... 47
Tabel 5.2. Hasil Karakteristik Khitosan Kulit Udang ... 48
Tabel 5.3. Data Uji Tarik Membran Khitosan 1% ... 50
Tabel 5.4. Data Uji Tarik Membran Khitosan 2% ... 51
Tabel 5.5. Data Uji Tarik Membran Khitosan 3% ... 52
Tabel 5.6. Data Uji Tarik Membran Khitosan 4% ... 53
Tabel 5.7. Data Uji TarikMembran Khitosan 5% ... 54
Tabel 5.8. Absorbansi Larutan Standar Fosfat ... 55
Tabel 5.9. Fluks Membran Khitosan ... 56
Tabel 5.10. Absorbansi Permeat Larutan Standar Fosfat 10 ppm ... 56
Tabel 5.11. Karakteristik Air Limbah Laundry ... 57
Tabel 5.12. Konsentrasi Permeat Air Limbah Laundry ... 57
Tabel 6.1. Hasil Uji Tarik Membran Khitosan ... 63
Tabel 6.2. Hasil Perhitungan Fluks Membran Khitosan ... 65
Tabel 6.3. Konsentrasi Standar Fosfat 10 ppm sebelum dan setelah Perlakuan ... 67
Tabel 6.4. Konsentrasi Fosfat dalam Air Limbah Laundry sebelum dan setelah Perlakuan ... 67
xv
DAFTAR LAMPIRAN
Halaman Lampiran 1 Skema Isolasi Khitin dari Kulit Udang menjadi Khitosan ... 77 Lampiran 2 Skema Pembuatan Membran Khitosan ... 78 Lampiran 3 Uji Tarik Membran Khitosan Menggunakan Alat
Screw Test Stand ... 80 Lampiran 4 Skema Penggunaan Membran Khitosan untuk Penurunan
Kadar Fosfat dalam Larutan Standar Fosfat (Larutan
KH2PO4 10 ppm) ... 86 Lampiran 5 Skema Mekanisme Penggunaan Membran Khitosan ... 87 Lampiran 6 Perhitungan Kurva Kalibrasi Standar Fosfat ... 88 Lampiran 7 Perhitungan Konsentrasi Larutan Standar Fosfat 10 ppm
setelah di lewatkan pada Membran Khitosan berbagai
Konsentrasi dan Waktu Kontak ... 90 Lampiran 8 Perhitungan Data Statistik Absorbansi Larutan Standar
Fosfat 10 ppm setelah di lewatkan pada Membran Khitosan (1%, 2%,3%, 4% dan 5%) dan Waktu Kontak 30, 60, 90
dan 120 menit ... 92 Lampiran 9 Perhitungan Derajat Deasetilasi Senyawa Khitosan
dengan Metode Garis ... 97 Lampiran 10 Perhitungan Persentase deasetilasi khitin menjadi
Khitosan ... 98 Lampiran 10 Spektra FTIR Senyawa Khitin ... 99 Lampiran 11 Spektra FTIR Senyawa Khitosan ... 100
1 BAB I PENDAHULUAN
1.1. Latar Belakang
Air merupakan sumber kehidupan, setiap saat semua mahluk hidup memerlukan air untuk keperluan aktifitas hidupnya. Penggunaan air setiap hari semakin banyak dan dalam proses pemakaiannya dipastikan menghasilkan sisa buangan yang berupa limbah, bahkan 85% limbah masuk ke badan perairan.
Limbah cair yang di buang begitu saja ke badan perairan dalam waktu yang lama dapat menimbulkan pencemaran terhadap lingkungan. Pencemaran limbah cair bisa bersumber dari limbah industri, limbah rumah tangga, ataupun limbah yang berasal dari proses pencucian pakaian oleh jasa laundry yang selanjutnya bisa juga disebut sebagai air limbah domestik. Keputusan Menteri Negara Lingkungan Hidup Nomor 112 Tahun 2003, pasal 1 ayat 1 menyebutkan bahwa air limbah domestik adalah air limbah yang berasal dari usaha dan atau kegiatan permukiman, rumah makan, perkantoran, perniagaan, apartemen dan asrama.
Limbah cair termasuk limbah yang mempunyai sifat cair dimana komposisinya terdiri atas 99,9% air dan sisanya adalah bahan padat (Mahida, 1995). Limbah dapat berbentuk bahan tersuspensi atau lainnya dalam bentuk terlarut. Menurut Soemirat (2003), air bekas cucian, bekas kamar mandi, bekas cuci perabot dikatagorikan sebagai limbah yang mengandung detergen, sabun dan mikroorganisme. Detergen atau sabun paling banyak dipakai dalam mencuci pakaian sehari-hari. Tingkat kesibukan seseorang menyebabkan semakin banyak orang yang menggunakan jasa laundry untuk mencuci pakaian. Oleh karena itu
2
penggunaan detergen semakin banyak pula. Limbah laundry sering dibuang langsung ke saluran air (got) tanpa adanya pengolahan sebelumnya, jika terus menerus dilakukan dapat menyebabkan dampak yang merugikan bagi kelangsungan lingkungan hidup. Detergen umumnya tersusun atas tiga komponen utama terdiri atas surfaktan (sebagai bahan dasar detergen) antara 20– 30%, bahan builder (senyawa fosfat) antara 70-80%, dan bahan aditif (pemutih, pewangi) antara 2-8%. Kandungan senyawa fosfat dalam detergen cukup besar sehingga limbah dari proses pencucian mempunyai kandungan fosfat yang cukup tinggi.
Senyawa fosfat dalam air limbah dapat berupa senyawa ortofosfat, polifosfat, dan fosfat organik. Setiap senyawa tersebut terdapat dalam bentuk terlarut, tersuspensi atau terikat di dalam sel organisme dalam air. Sumber utama pencemaran fosfat yaitu 10% dari proses alamiah, 7% industri, 11% detergen, 17% pupuk pertanian, 23% limbah manusia, dan 32% limbah peternakan.
Keberadaan fosfat yang berlebihan di badan air menyebabkan suatu fenomena eutrofikasi. Air dikatakan eutrofik jika konsentrasi fosfat dalam air 35-100 μg/L.
Kondisi eutrofik, sangat memungkinkan alga dan tumbuhan air berukuran mikro tumbuh berkembang biak dengan cepat. Keadaan ini menyebabkan kualitas air menjadi menurun, karena rendahnya konsentrasi oksigen terlarut bahkan sampai batas nol, sehingga menyebabkan kematian makhluk hidup air seperti ikan dan spesies lain yang hidup di air.
Upaya penanggulangan limbah cair, metode yang digunakan diantaranya pengolahan limbah secara fisik, kimia dan biologi atau kombinasinya untuk mengatasi pencemaran. Umumnya pengolahan limbah cair secara kimia dilakukan dengan proses koagulasi-flokulasi, sedimentasi dan secara floatasi dengan
3
menggunakan udara terlarut, serta pengolahan limbah cair secara biologi yaitu proses aerob dan anaerob. Proses kimia seringkali kurang efektif dikarenakan biaya untuk pembelian bahan kimianya cukup tinggi dan umumnya pengolahan limbah dengan menggunakan bahan kimia akan menghasilkan lumpur (sludge) yang cukup banyak. Pengolahan limbah cair secara floatasi akan menggunakan energi yang cukup tinggi, sedangkan proses pengolahan secara biologi memerlukan lahan yang cukup luas. Sehingga menimbulkan pemikiran untuk mengembangkan dan memodifikasi teknologi baru untuk pengolahan limbah cair (limbah laundry) yaitu dengan teknologi membran. Membran merupakan suatu lapisan penghalang (barrier) atau pembatas selektif yang di letakkan antara dua fase bersifat semipermeabel yang dapat melewatkan komponen tertentu dan menahan komponen yang lain (Mulder, 1996).
Pemanfaatan teknologi membran merupakan teknologi yang ramah lingkungan karena tidak menimbulkan dampak yang buruk bagi lingkungan.
Teknologi membran ini dapat mengurangi senyawa organik dan anorganik yang berada dalam air tanpa menggunakan bahan kimia dalam pengoperasiannya (Wenten, 1999). Membran ultrafiltrasi adalah teknik pemisahan dengan menggunakan membran untuk menghilangkan zat terlarut dengan bobot molekul (BM) tinggi, koloid, mikroba sampai padatan tersuspensi dari air. Proses pemisahan menggunakan membran ultrafiltrasi biasanya digunakan di bidang industri dan penelitian untuk penjernihan air karena pada umumnya mempunyai ukuran pori 0.1 – 0.01 µm. Kemampuan membran ultrafiltrasi dalam merejeksi COD (Chemical Oxygen Demand) pada pengolahan limbah emulsi minyak dengan sistem aliran dead-end mencapai 90% (Zulkarnein dkk, 2004). Tingkat
4
rejeksi zat organik dengan membran ultrafiltrasi sistem aliran dead-end pada pengolahan air waduk mencapai 90% (Deniva dkk, 2004). Tingkat rejeksi COD pada pengolahan limbah cair emulsi minyak dengan membran ultratrafiltrasi yang didahului dengan proses pretreatment dengan koagulan jenis Poly Aluminium Chloride (PACl) mencapai 98,56% (Mayashanty dkk, 2004). Membran ultrafiltrasi yang sering digunakan dalam proses pengolahan air adalah membran terbuat dari selulosa asetat, polisulfon, dan poliakrilonitril (suatu polimer) yang harganya cukup mahal. Oleh karena itu diperlukan suatu bahan baku alternatif yang lebih mudah dan murah dengan memanfaatkan khitosan sebagai bahan pembuatan membran yang juga merupakan suatu polimer yang ramah lingkungan.
Khitosan pertama kali ditemukan oleh Rauget pada tahun 1859 dengan cara merefluk khitin dengan KOH pekat, dan tahun 1934 dua paten didapat oleh Rigby yaitu penemuan mengenai pengubahan khitin menjadi khitosan dan pembuatan membran dari serat khitosan. Senyawa khitin pada kulit udang diubah menjadi khitosan berpotensi sebagai bahan pembuatan membran, karena khitin merupakan polimer alam yang melimpah keberadaaanya, mempunyai karakteristik yang baik seperti dapat terbiodegradasi (mudah terurai), tak beracun dan khitin dapat diubah menjadi khitosan dengan proses yang sederhana. Khitosan mempunyai reaktifitas yang tinggi karena memiliki gugus amina bebas yang bersifat nukleofil kuat (Marganof, 2003). Adanya gugus amina bebas pada khitosan dapat membentuk ikatan hidrogen intermolekuler atau intramolekuler sehingga menyebabkan khitosan tidak larut dalam air tapi larut dalam pelarut asam lemah. Khitosan merupakan polimer alam dapat menawarkan pendekatan sebagai alat biokontrol dalam bidang pengolahan air. Menurut Liu (2003)
5
membran khitosan dapat digunakan sebagai adsorben karena khitosan dalam bentuk membran mempunyai luas permukaan yang lebih besar daripada dalam bentuk serpihan dan dapat meningkatkan kapasitas adsorpsinya. Oetomo (2004) menyatakan bahwa penggunaan khitosan sebagai adsorben dapat digunakan untuk menurunkan kadar logam Cu pada pelapisan logam sampai 98,62% dengan metode jartes, selain itu khitosan juga dapat dibentuk menjadi film tipis (Hassan dan Sulaiman, 1996). Pada penelitian ini, membran khitosan dibuat menggunakan bahan baku kulit udang, proses pembuatannya yaitu pertama dilakukan ekstraksi khitin selanjutnya diubah menjadi khitosan kemudian dibuat menjadi membran dengan melarutkan khitosan dalam asam asetat dalam berbagai konsentrasi, yang aplikasinya digunakan untuk menurunkan kadar fosfat dalam air limbah laundry.
1.2. Rumusan Masalah
Berdasarkan uraian di atas, ada beberapa masalah di dalam penelitian ini yaitu :
1. Berapakah tingkat kemurnian khitosan yang diperoleh dari khitin kulit udang yang ditandai dengan derajat deasetilasi?
2. Berapakah konsentrasi optimum khitosan sebagai membran dan pada waktu kontak optimum dapat menurunkan kadar fosfat optimum dalam air limbah laundry?
3. Berapakah fluks terbaik (jumlah volume permeat yang melewati satuan luas membran dalam waktu tertentu)?
6 1.3. Tujuan Penelitian
Tujuan penelitian ini adalah:
1. Mengetahui tingkat kemurnian khitosan yang diperoleh dari khitin kulit udang.
2. Membuat membran khitosan dan mengetahui pada konsentrasi serta waktu kontak, membran secara optimum dapat menurunkan kadar fosfat total dari limbah laundry.
3. Mengetahui fluks (jumlah volume permeat melewati permukaan membran dalam waktu optimum).
1.4. Manfaat Penelitian
Dapat memberikan informasi kepada pemangku kepentingan baik instansi atau lembaga yang bergerak dibidang pengolahan limbah tentang penggunaan khitosan sebagai membran dalam menurunkan kadar fosfat dalam air limbah laundry dan aktifitas lain yang penghasil limbah sejenis, sehingga tingkat pencemaran fosfat terhadap lingkungan dapat diturunkan.
7 BAB II
TINJAUAN PUSTAKA
2.1. Detergen
Detergen berasal dari kata detergree yang merupakan bahasa latin mempunyai arti membersihkan. Detergen merupakan penyempurnaan dari produk sabun. Kelebihannya dibandingkan sabun adalah bisa mengatasi air sadah dan larutan asam, serta harganya lebih murah. Detergen sering disebut dengan istilah detergen sintetis yang dibuat dari bahan-bahan sintetis (Zoller, 2004). Detergen umumnya terdiri atas tiga komponen yaitu, surfaktan (sebagai bahan dasar detergen LAS, ABS), bahan builders (senyawa fosfat) dan bahan aditif (pemutih dan pewangi). Komponen terbesar dari detergen yaitu bahan builders antara 70- 80%, bahan dasar sekitar 20-30%, dan bahan aditif relatif sedikit antara 2-8%.
Surfaktan (surface active agents), merupakan senyawa yang dapat menurunkan tegangan permukaan air. Molekul surfaktan mempunyai suatu ujung hidrofobik (satu rantai hidrokarbon atau lebih) dan satu ujung hidrofilik. Porsi hidrokarbon dari suatu molekul surfaktan harus mengandung 12 atom karbon atau lebih agar efektif. Molekul-molekul dan ion-ion yang diadsorbsi pada antar muka dinamakan surface aktive agent atau surfaktan. Nama lainnya adalah amfifil, yang menunjukkan bahwa molekul atau ion tersebut mempunyai affinitas tertentu terhadap baik pelarut polar maupun non polar. Hal ini tergantung dari jumlah dan sifat dari gugus-gugus polar dan non polar yang ada padanya, amfifil dapat bersifat hidrofilik (suka air), lipofilik (suka minyak) atau bersifat seimbang di
8
antara dua sifat yang ekstrim tersebut. Lambang dari surfaktan terlihat seperti Gambar 2.1.
Ekor hidrofobik kepala hidrofilik Gambar 2.1. Lambang umum untuk Surfaktan
Builder adalah suatu bahan yang dapat menambah kerja dari bahan penurun tegangan permukaan dengan cara menonaktifkan mineral penyebab kesadahan air. Builders digunakan untuk melunakkan air sadah dengan cara mengikat mineral-mineral yang terlarut, sehingga surfaktan dapat berkonsentrasi pada fungsi utamanya. Builder juga membantu menciptakan kondisi keasaman yang tepat agar proses pembersihan dapat berlangsung lebih baik serta membantu mendispersikan dan mensuspensikan kotoran yang telah lepas (Meyer, 2006).
Dalam pembuatan detergen, builder sering ditambahkan dengan maksud menambah kekuatan daya cuci dan mencegah mengendapnya kembali kotoran- kotoran yang terdapat pada pakaian yang akan dicuci. Contoh builder yang sering digunakan: Sodium Tri Poli Fosfat (STPP), Nitril Tri Acetat (NTA).
Bahan tambahan (aditif) digunakan untuk membuat produk lebih menarik, misalnya pewangi, pemutih, pelembut, pewarna, dan lain sebagainya. Bahan ini tidak berhubungan langsung dengan daya cuci detergen, bahan ini ditambahkan lebih untuk maksud komersialisasi produk. Salah satu contoh dari bahan aditif adalah Carboxyl Methyl Cellulose (CMC). Bahan ini berbentuk serbuk putih dan
9
berfungsi untuk mencegah kembalinya kotoran ke pakaian sehingga disebut antiredeposisi. Selain CMC, masih banyak macam dari bahan aditif ini, tetapi pada umumnya merupakan rahasia dari tiap-tiap perusahaan. Ini sebenarnya merupakan tantangan bagi pelaku wirausaha untuk selalu mencari bahan aditif ini sehingga produk deterjen bubuk mempunyai nilai lebih dan berdaya saing tinggi.
2.1.1. Fosfat
Menurut Hammer dan Viesman (2005) bentuk utama dari fosfor dalam limbah domestik cair adalah fosfor organik, orthofosfat (H2PO4- , HPO42-, PO43-) dan polifosfat. Orthofosfat banyak dijumpai pada air buangan yang telah tercemari pupuk. Terdapat tiga asam fosfat asam orthofosfat H3PO4, asam pirofosfat H4P2O7, dan asam metafosfat HPO3. Diantara ketiga asam fosfat tersebut yang paling stabil adalah orthofosfat. Larutan piro dan metafosfat berubah menjadi orthofosfat perlahan-lahan pada suhu biasa, dan lebih cepat dengan dididihkan.
Asam orthofosfat adalah asam berbasa-tiga, yang membentuk tiga deret garam orthofosfat primer misalnya NaH2PO4, orthofosfat sekunder Na2HPO4, orthofosfat tersier Na3PO4. Jika suatu larutan asam orthofosfat dinetralkan dengan natrium hidroksida dengan memakai metil jingga sebagai indikator, titik netral dicapai bila asam itu telah diubah menjadi fosfat primernya. Menggunakan fenolftalien sebagai indikator larutan akan bereaksi netral bila fosfat sekundernya terbentuk, dengan 3 mol alkali akan terbentuk fosfat tersier atau fosfat normalnya. NaH2PO4
bersifat netral terhadap metil jingga dan asam terhadap fenolftalien. Na2HPO4 bersifat netral terhadap fenolftalien dan basa terhadap metil jingga, Na3PO4
bersifat basa terhadap kebanyakan indikator karena hidrolisisnya yang luas (Vogel, 1985).
10
Tipe polifosfat adalah sodium hexa meta fosfat Na3(PO3)6 dan sodium pirofosfat Na4P2O7. Polifosfat berasal dari air buangan penduduk dan industri yang menggunakan detergen mengandung fosfat. Komponen fosfat dipergunakan untuk membuat detergen sebagai pembentuk buih. Sedangkan fosfat organik terdapat dalam air buangan penduduk (tinja) dan sisa makanan. Fosfat organik dapat pula terjadi dari orthofosfat yang terlarut melalui proses biologis karena baik bakteri maupun tanaman menyerap fosfat bagi pertumbuhannya. Adanya fosfat dalam air limbah dapat menghambat penguraian pada proses biologis (Saefumilah, 2006). Konsentrasi rata-rata fosfor keseluruhan sebanyak 10 mg/l berada dalam air limbah perkotaan, kira-kira 10% dibuang sebagai bahan tak terpakai selama pengendapan primer dan 10% hingga 20% lainnya digabungkan ke dalam sel-sel bakteri selama pengolahan biologis. Sisa yang 70% dari fosfor yang masuk pada umumnya dilepaskan bersama buangan instalasi sekunder .
Bila kadar fosfat pada air alam sangat rendah (<0,01 mg/l), pertumbuhan tanaman dan ganggang akan terhalang, keadaan ini dinamakan “oligotrop”.
Pembuangan limbah yang banyak mengandung fosfat ke dalam badan air dapat menyebabkan pertumbuhan lumut dan mikroalga yang berlebih yang disebut
“eutrophication”, sehingga air menjadi keruh dan berbau karena pembusukan
lumut-lumut yang mati. Pada keadaan “eutrotop” tanaman dapat menghabiskan oksigen dalam air pada malam hari atau bila tanaman tersebut mati dan dalam keadaan sedang mencerna (digest). Saat siang hari pancaran sinar matahari ke dalam air akan berkurang, sehingga proses fotosintesis yang dapat menghasilkan oksigen juga berkurang.
11 2.1.2. Pemisahan Fosfat
Pemisahan fosfat secara umum meliputi 2 langkah yaitu : a. Merubah bentuk fosfor menjadi ortofosfat yang larut.
b. Menentukan secara kolorimetris ortofosfat yang larut.
Pemisahan fosfor kedalam bentuk ortofosfat didefinisikan secara teknis dapat dipergunakan untuk tujuan interpretasi, dimana pemisahan atau penyaringan menggunakan filter membran 0,45 μm dapat dipergunakan untuk membedakan antara fosfat total dan fosfat terlarut. Fosfat yang dapat langsung diperiksa secara kolorimetris melalui perombakan secara oksidatif dengan pemanasan sampel disebut sebagai fosfor reaktif atau ortofosfat (terdapat dalam bentuk terlarut dan partikel). Hidrolisis dengan asam pada titik didih air mengubah fosfat dalam bentuk terlarut atau fosfat partikulat yang berkondensasi menjadi ortofosfat terlarut (dikenal dengan istilah fosfat terhidrolisis asam). Metode kolorimetris yang dipergunakan adalah metode asam askorbat, yaitu menggunakan ammonium molibdat dan potassium antimonil tartrat dalam media asam dengan ortofosfat untuk membentuk asam heteropoli-asam fosfomolibdat yang tereduksi menjadi molybdenum yang berwarna biru oleh asam askorbat. Warna ini sebanding dengan konsentrasi fosfat yang ditentukan dengan menggunakan spektrofotometer (Effendi, 2003).
2.2. Pengertian membran secara umum
Kata membran berasal dari bahasa Latin Membrana yang berarti potongan kain. Operasi membran dapat diartikan sebagai proses pemisahan dua atau lebih komponen dari aliran fluida melalui suatu membran. Membran memiliki ketebalan yang berbeda-beda, ada yang tebal dan ada juga yang tipis serta ada
12
yang homogen dan yang heterogen. Ditinjau dari bahannya membran terdiri atas bahan alami dan bahan sintetis. Bahan alami adalah bahan yang berasal dari alam misalnya pulp dan kapas, sedangkan bahan sintetis dibuat dari bahan kimia, misalnya polimer polisulfon, akrilik, poliakrilat.
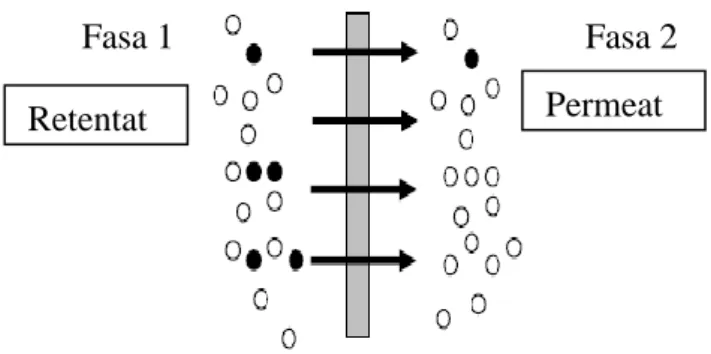
Membran berfungsi sebagai penghalang (Barrier) yang sangat selektif diantara dua fasa, hanya dapat melewatkan komponen (ion-ion) tertentu dan menahan komponen lain dari suatu aliran fluida yang dilewatkan melalui membran (Mulder, 1996). Komponen aktif membran adalah suatu senyawa bermuatan atau netral yang mampu membentuk senyawa kompleks dengan ion- ion secara reversible dan mambawanya melalui membran organik. Larutan yang mengandung komponen yang tertahan disebut retentat dan larutan yang mengalir disebut permeat. Filtrasi dengan menggunakan membran selain berfungsi sebagai sarana pemisahan juga berfungsi sebagai sarana pemekatan dan pemurnian dari suatu larutan yang dilewatkan pada membran tersebut. Proses membran melibatkan umpan (cair dan gas), dan gaya dorong (driving force) akibat perbedaan tekanan (ΔP), perbedaan konsentrasi (ΔC) dan perbedaan energi (ΔE).
Proses pemisahan dengan membran dapat diilustrasikan seperti Gambar 2.2.
Membran
Fasa 1 Fasa 2
Gaya Dorong
Gambar 2.2. Proses pemisahan membran
Retentat Permeat
13
Dalam teknologi pemisahan dengan menggunakan membran mempunyai keunggulan dibandingkan dengan teknologi pemisahan yang lain yaitu :
- pemisahan membran berdasarkan ukuran molekular sehingga beroperasi pada temperatur rendah (temperatur ambient).
- Pemakaian energi yang relatif rendah, karena biasanya pemisahan menggunakan membran tidak melibatkan perubahan fasa.
- Tidak menggunakan zat bantu kimia sehingga tidak ada tambahan produk buangan
- Bersifat modular artinya modul membran dapat discale-up dengan memperbanyak unitnya.
- Proses membran dapat mudah digabungkan dengan proses pemisahan lainnya ( hybrid processing )
2.2.1. Parameter utama proses pemisahan membran
Pada proses membran umumnya terjadi fenomena fluks berbanding terbalik dengan selektifitas. Semakin tinggi fluks seringkali berakibat menurunnya selektifitas dan sebaliknya, sedangkan hal yang diinginkan dalam proses berbasis membran adalah mengoptimasi fluks dan selektifitas.
A. Permeabilitas
Permeabilitas suatu membran merupakan ukuran kecepatan dari suatu spesi atau konstituen menembus membran. Secara kuantitas, permeabilitas membran sering dinyatakan sebagai fluks atau koefisien permeabilitas. Definisi dari fluks adalah jumlah volume permeat yang melewati satuan luas membran dalam waktu tertentu dengan adanya gaya dorong dalam hal ini berupa tekanan.
Secara umum fluks dapat dirumuskan sebagai (Mulder, 1996) :
14
………(2.1) dimana :
J = Fluks (Lt/m
2
.jam) V = Volume permeat (Lt)
A = Luas permukaan membran (m2) t = Waktu ( jam)
Laju fluks akan menurun sejalan dengan waktu pengoperasian akibat pengendapan atau pelekatan material dipermukaan membran, yang dikenal dengan istilah fouling dan scaling. Fouling dapat didefinisikan sebagai proses terbentuknya lapisan oleh material yang tidak diinginkan pada permukaan membran. Secara teknis, scaling didefinisikan sebagai akumulasi kerak (scale) akibat adanya peningkatan konsentrasi dari materi anorganik yang melewati hasil kali kelarutannya pada permukaan membran dan menyebabkan penurunan kinerja membran. Sehingga definisi fouling sudah termasuk scaling. Dalam penggunaannya, istilah fouling lebih banyak pada materi biologis dan koloid, sedangkan istilah scaling digunakan untuk pengendapan garam atau mineral anorganik.
Terjadinya fouling diawali dengan adanya polarisasi konsentrasi yaitu peningkatan konsentrasi lokal dari suatu solut pada permukaan membran, sehingga material terlarut berkumpul membentuk lapisan gel yang semakin lama menebal. Pada polarisasi konsentrasi ini, fluks mengalami penurunan karena adanya peningkatan pada tahapan hidrodinamik pada lapisan batas dan kenaikan tekanan osmotik lokal. Selain polarisasi konsentrasi, penurunan fluks dapat terjadi akibat pengaruh dari adsorpsi, pembentukkan lapisan gel (gel layer formation) dan
15
penyumbatan pada pori. Dampak langsung yang dapat diamati dan cukup signifikan yang menandai terjadinya fauling ini adalah menurunnya kinerja membran (fluks permeat menurun seiring waktu), seperti yang terlihat pada Gambar 2.3.
Gambar 2.3. Fluks sebagai fungsi dari waktu B. Selektifitas
Selektivitas suatu membran merupakan ukuran kemampuan suatu membran untuk menahan suatu spesi atau melewatkan suatu spesi tertentu.
Selektifitas membran tergantung pada interaksi antar muka dengan spesi yang akan melewatinya, ukuran spesi dan ukuran pori permukaan membran. Parameter yang digunakan untuk menggambarkan permselektifitas membran adalah koefisien rejeksi (R). Koefisien rejeksi adalah fraksi konsentrasi zat terlarut yang tidak menembus membran, dan dirumuskan sebagai berikut :
………(2.2) dimana :
R = Koefisien rejeksi (%)
Cp = Konsentrasi zat terlarut dalam permeat Cf = Konsentrasi zat terlarut dalam umpan.
16
Dengan harga R berkisar antara 0 sampai 1. Jika harga R = 1 berarti zat kontaminan ditahan oleh membran secara sempurna.
Untuk mengurangi penumpukan materi pada permukaan membran, ada dua cara yang dapat diambil, yaitu (Milisic, 1996):
a. Menjaga partikel mengenai membran, atau b. Membersihkan membran tersebut
Untuk menjaga partikel mengenai membran, ada beberapa teknik yang digunakan seperti proses filtrasi, proses koagulasi dimana upaya-upaya tersebut lazim disebut sebagai pretreatment. Sedangkan untuk membersihkan membran dapat digunakan pembersihan membran secara periodik, atau meningkatkan tegangan geser (shear stress) pada permukaan membran dimana konstituen yang telah tertahan (fouling) akan tergeser oleh turbulensi aliran sehingga tidak terjadi penumpukan partikel.
2.2.2. Model aliran umpan pada membran
Dalam operasi membran dikenal dua jenis aliran umpan, yaitu aliran cross- flow dan aliran dead-end. Secara sederhana ditunjukan pada Gambar 2.4. Pada sistem cross- flow, aliran umpan mengalir melalui suatu membran, dengan hanya sebagian saja yang melewati pori membran untuk memproduksi permeat, sedangkan aliran pelarut atau cairan pembawa akan melewati permukaan membran sehingga larutan, koloid dan padatan tersuspensi yang tertahan oleh membran akan terus terbawa menjadi aliran balik. Sedangkan pada sistem dead- end, keseluruhan dari fluida melewati membran (sebagai media filter) dan partikel
tertahan pada membran, dengan demikian fluida umpan mengalir melalui tahanan membran dan tahanan penumpukan partikel pada permukaan membran (Mallack et al., 1997).
17
Dead-end Cross-flow
retentat umpan retentat
permeat
permeat
Gambar 2.4. Model proses aliran umpan pada operasi membran
Sistem cross-flow secara teori lebih baik dari sistem dead-end dimana laju aliran retentatg tidak seluruhnya menjadi permeat, ada bagian yang lewat menjadi laju aliran balik pada sistem cross-flow.
2.3. Klasifikasi Membran
Berdasarkan struktur dan prinsif pemisahan membran dapat dibedakan menjadi 3 (tiga) jenis yaitu :
1. Membran berpori (pemisahan berdasarkan perbedaan ukuran partikel dengan ukuran pori membran)
2. Membran tidak berpori (pemisahan berdasarkan perbedaan kelarutan dan kemampuan berdifusi)
3. Membran cair (pemisahan berdasarkan sifat molekul pembawa spesifik/carrier)
Berdasarkan gradient tekanan sebagai gaya dorongnya dan pemeabilitasnya, membran dapat dibedakan menjadi 4 (empat) jenis yaitu (Mulder,1996):
a. Mikrofiltrasi (MF), Membran jenis ini memiliki ukuran pori 0.05 – 10 µm dengan tebal 10 – 200 µm, dapat dibuat dari bahan polimer maupun
18
keramik, beroperasi pada tekanan berkisar 0,1-2 Bar dan batasan permeabilitas-nya lebih besar dari 50 L/m
2
.jam.bar
b. Ultrafiltrasi (UF), Membran jenis ini memiliki ukuran pori berkisar 0.05 – 1 µm ( 1- 100 nm), dengan tebal mencapai 150 µm, dapat dibuat dari bahan keramik atau polimer, beroperasi pada tekanan antara 1-5 Bar dan batasan permeabilitas-nya adalah 10-50 L/m2.jam.bar
c. Nanofiltrasi, Membran ini memiliki ukuran pori 0.01 - 5 nm, dapat dibuat dari bahan poliamida (interfacial polymerisasi), beroperasi pada tekanan antara 5-20 bar dan batasan permeabilitas-nya mencapai 1,4 – 12 L/m
2
.jam.bar
d. Reverse Osmosis (RO), Membran jenis ini memiliki ukuran pori lebih kecil dari 2 nm, dapat terbuat dari bahan selulosa triasetat atau aromatic poliamida, beroperasi pada tekanan antara 10-100 Bar dan batasan permeabilitas-nya mencapai 0,05-1,4 L/m
2
.jam.bar.
Jenis membran yang dipakai pada penelitian ini menggunakan membran khitosan dari kulit udang, yang termasuk ke dalam membran ultrafiltrasi.
2.3.1 Membran Ultrafiltrasi
Membran ultrafiltrasi (UF) adalah teknik proses pemisahan (menggunakan) membran untuk menghilangkan berbagai zat terlarut BM (berat molekul) tinggi, aneka koloid, mikroba sampai padatan tersuspensi dari air.
Ukuran dan bentuk molekul terlarut merupakan faktor penting, batas berat molekul membran (molecular weight cut-off, MWCO) adalah ukuran dari karakteristik pemisahan dari suatu membran dalam istilah berat atom (massa), sebagai ukuran pori-pori. Membran ultrafiltrasi mempunyai ukuran pori 1-100nm
19
(1000-106 NWCO), biasanya diukur dalam satuan Dalton. Satu Dalton adalah unit massa yang besarnya sama dengan 1/12 massa atom karbon-12 (yaitu satu satuan massa atom (atomic mass unit, amu) biasanya digunakan sebagai satuan untuk mengukur batas berat molekul (MWCO) yang dapat dipisahkan oleh membran ultrafiltrasi. Teknologi pemurnian air, menggunakan membran ultrafiltrasi dengan batas berat molekul membran (MWCO) 1000 – 20000 lazim untuk penghilangan pirogen, sedangkan berat molekul membran (MWCO) 80.000- 100.000 untuk pemakaian penghilangan koloid. Tekanan sistem ultrafiltrasi biasanya rendah, 1-10 bar (70-700 kPa), maka dapat menggunakan pompa sentrifugal biasa. Membran ultrafiltrasi sehubungan dengan pemurnian air dipergunakan untuk menghilangkan koloid (penyebab fouling) dan penghilangan mikroba, pirogen.
Membran ultrafiltrasi dibuat dengan mencetak polimer selulosa acetate (CA) ataupun jenis polimer alam (kitosan) sebagai lembaran tipis. Membran khitosan mudah diperoleh karena kelarutannya yang tinggi dalam asam asetat 1%
dan membran diperoleh setelah menguapkan pelarutnya. Fluks maksimum bila membrannya anisotropik, ada lapisan tipis rapat dan berpori. Membran selulosa acetate (CA) mempunyai sifat pemisahan yang bagus namun sayangnya dapat dirusak oleh bakteri dan zat kimia, rentan pH. Membran juga dapat terbuat dari polimer polisulfon, akrilik, juga polikarbonat, PVC, poliamida, piliviniliden fluoride, kopolimer AN-VC, poliasetal, poliakrilat dan bahan lainnya.
20
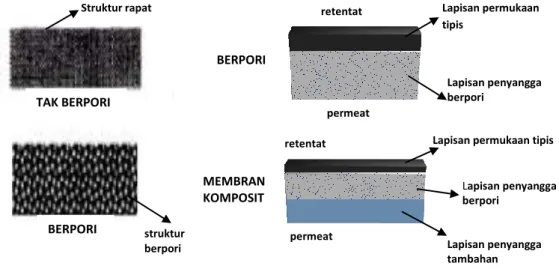
Struktur membran UF secara morfologinya dapat diklasifikasikan menjadi dua yaitu membran simetrik dan membran asimetrik, terlihat pada Gambar 2.5.
Simetrik Asimetrik
Gambar 2.5. Struktur cross-section membran UF simetrik dan asimetrik Membran simetrik (yaitu terdiri atas membran porous/berpori dan nonporous/tak berpori) ketebalannya berkisar antara 10 – 200 µm, dimana ketebalan suatu membran dapat menentukan ketahanan membran terhadap transfer massa.
Pemisahan membran berpori berdasarkan atas perbedaan ukuran partikel dengan ukuran pori membran. Membran tidak berpori (membran rapat), prinsif pemisahannya berdasarkan pada perbedaan kelarutan dan kemampuan berdifusi.
Membran asimetrik (yaitu terdiri dari membran berpori dan komposit), membran asimetrik berpori memiliki lapisan yang sangat tipis (0,1 - 1µm) pada bagian permukaannya yang berpengaruh pada fluks dan selektifitas membran. Lapisan bawah berupa lapisan penyangga berpori dengan ketebalan 50 – 150 µm merupakan penyangga mekanis. Membran komposit pada bagian atasnya memiliki pori berukuran kecil (≤ 0,1 µm) bertindak sebagai barrier (penghalang) menghasilkan fluks yang tinggi. Bagian bawah membran (lapisan
retentat Lapisan permukaan tipis
Lapisan penyangga berpori
permeat
Lapisan penyangga tambahan
Lapisan penyangga berpori
Lapisan permukaan tipis retentat
permeat BERPORI
TAK BERPORI
BERPORI
MEMBRAN KOMPOSIT Struktur rapat
struktur berpori
21
penyangga/pendukung) memiliki ukuran pori lebih besar, biasanya lapisan ini menggunakan jenis polimer yang berbeda dengan lapisan permukaan.
2.3.2. Mekanisme transfort pada membran UF
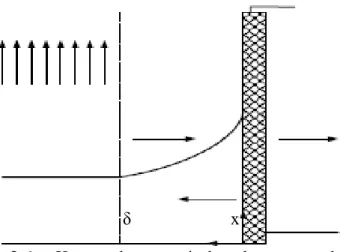
Faktor penting yang menentukan kinerja keseluruhan sistem membran ultrafiltrasi adalah tingkat transportasi zat terlarut atau partikel dalam larutan umpan terhadap membran. Seperti ditunjukkan pada Gambar 2.6, aliran tekanan yang digerakkan melintasi membran mengangkut zat terlarut ke permukaan membran. Jika membran ini sebagian atau sepenuhnya dapat menahan zat terlarut tertentu, tingkat awal dari transportasi zat terlarut terhadap membran akan lebih besar dari fluks zat terlarut melalui membran sehingga menyebabkan zat terlarut menumpuk di permukaan membran. Fenomena ini umumnya disebut sebagai polarisasi konsentrasi, yaitu akumulasi ion yang direjeksi saat proses pemisahan yang membentuk lapisan pada permukaan membrane (Wenten, 2004). Akumulasi zat terlarut pada permukaan membran menyebabkan aliran kembali berdifusi menuju larutan bulk. Kondisi steady state dicapai ketika transportasi konveksi dari zat terlarut ke membran adalah sama dengan jumlah dari aliran permeat ditambah transportasi difusi zat terlarut, yaitu:
J.C - D = J.Cp ………(2.3)
J adalah fluks permeat,
C adalah konsentrasi zat terlarut dalam arah x, D adalah koefisien difusi, dan
Cp adalah konsentrasi zat terlarut dalam permeat.
22
δ x
Gambar 2.6. Konsep dasar pemisahan dengan membran dan Polarisasi Konsentrasi pada kondisi steady-state Pada kondisi batas (boundary) jika :
x = 0 x = Cw (konsentrasi zat terlarut pada permukaan membran) x = δ x = Cb (konsentrasi zat terlarut pada larutan bulk)
Integrasi dari persamaan (2.3) menghasilkan :
ln = ………(2.4)
Jika rasio antara koefisien difusi (D) dengan batas ketebalan (δ) merupakan koefisien perpindahan massa (k) yaitu : k =
maka persamaan (2.4) menjadi :
J = k ln ………(2.5) Nilai fluks dengan total zat terlarut tertahan membentuk lapisan gel menyebabkan besar(Cp = 0) sehingga besar fluks (J) dapat dihitung dengan persamaan :
J = k ln ………(2.6)
Konsentrasi zat terlarut pada permukaan membran dapat diperoleh dengan ekstrapolasi antara fluks (J) terhadap ln Cb dan informasi yang diberikan kurang
23
akurat terutama jika larutan umpan berupa macrosolutes dengan konsentrasi Cw = Cb tidak memberikan nilai fluks nol.
Akumulasi zat terlarut atau partikel pada permukaan membran dapat mempengaruhi menyerap fluks dalam dua cara berbeda, yaitu pertama, akumulasi zat terlarut dapat menghasilkan cairan osmotik didorong mengalir kembali melintasi membran dari sisi permeat ke sisi umpan, sehingga mengurangi laju transportasi pelarut. Efek ini umumnya akan paling menonjol untuk zat terlarut kecil, yang cenderung memiliki tekanan osmotik besar misalnya, mempertahankan garam di reverse osmosis (Jonsson, 1984). Kemudian yang kedua, zat terlarut atau partikel ireversibel bisa merusak membran karena interaksi fisik maupun kimia yang spesifik antara membran dan berbagai komponen hadir dalam aliran proses, sehingga menambah ketahanan hydraulik terhadap aliran pelarut secara seri dengan yang disediakan oleh membran. Interaksi yang dapat menyebabkan penurunan fluks ini dapat dipengaruhi oleh adsorpsi, pembentukan lapisan gel, penyumbatan dari pori-pori membran. Penurunan fluks lebih lanjut juga diakibatkan oleh bahan membran itu sendiri, sifat zat terlarut, dan variabel lainnya seperti pH, kekuatan ion, suhu larutan dan operasi tekanan (Jonsson &
Tragardh, 1990). Fluks juga dapat didefinisikan sebagai :
fluks = ………(2.7)
atau fluks = ………....(2.8)
Rtotal = Rm + Rp + Ra + Rg + Rcp ………(2.9) Perbedaan tekanan osmotik, Δπ yang melintasi membran dapat menyebabkan gaya dorong (driving force) menjadi besar, sehingga memberikan transfortasi membran menjadi ΔP - ζΔπ (Zeman dan Sydney, 1996). ζ adalah
24
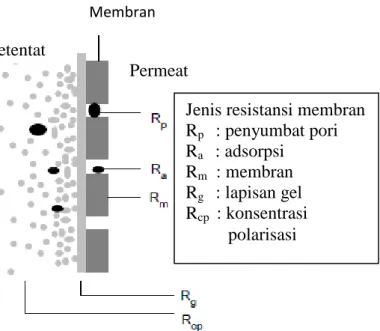
koefisien refleksi (parameter perpindahan), menunjukkan tingkat selektivitas membran. Bila ζ = 1 zat terlarut benar-benar dipertahankan dan ketika ζ = 0 itu benar-benar permeabel. Hambatan dari zat terlarut yang terakumulasi pada permukaan membran ini disebut sebagai hydraulik resistansi, Rs. Pada keadaan ideal resistensi yang berpengaruh pada membran hanya resistensi membran itu sendiri, Rm, tetapi membran memiliki batas resistensi tertentu terhadap zat terlarut maka akan terjadi akumulasi zat terlarut yang tertahan oleh membran di sekitar permukaan membran. Hal ini menyebabkan terbentuknya lapisan zat terlarut yang terkonsentrasi, sehingga menimbulkan resistensi baru terhadap proses perpindahan massa yaitu resistensi polarisasi konsentrasi, Rcp. Zat terlarut yang terkonsentrasi ini memiliki kecenderungan yang besar untuk membentuk lapisan gel dipermukaan membran dan menghasilkan resistensi lapisan gel, Rg. Pada kasus membran berpori, terdapat kemungkinan zat terlarut masuk kedalam pori membran dan menyumbat pori sehingga timbul pore blocking resistance Rp. Akhirnya, resistensi total bertambah akibat fenomena adsorpsi, Ra. Hal-hal tersebut terjadi pada semua jenis membran, baik yang berpori maupun yang tidak berpori (Mulder,1996). Jenis-jenis resistensi yang berpengaruh pada membran terlihat pada Gambar 2.7.
25
Gambar 2.7. Tipe resistensi pada membran saat perpindahan massa melewati membran dengan driving force tekanan.
2.4. Khitin dan Khitosan 2.4.1. Khitin
Senyawa khitin banyak terdapat pada kulit luar hewan Artropoda, Molusca Anellida, Crustacea (jenis udang-udangan, kepiting) dan juga terdapat pada dinding sel Fungi. Khitin merupakan biopolimer rantai panjang yang lurus tersusun dari 2000 – 3000 monomer (2-asetamida-2-deoksi-D-glukosa) yang terangkai dengan ikatan 1,4-β-glikosida. Kitin memiliki rumus molekul [C8H13NO5]n mimiliki berat molekul 1,2 x 106 Dalton. Khitin memiliki gugus asetamida (-NHCOCH3) yang merupakan polimer berunit N-asetilglukosamin.
Bentuk yang paling umum dari hkitin adalah ά-kitin, yaitu mempunyai 2 unit NN’-diasetil kitobiosa dari 2 rantai dengan susunan antiparalel (Minke dan Blackwell,1978). Sedangkan menurut Svitil, et al (1997) khitin berdasarkan susunan rantai molekulnya mempunyai 3 jenis struktur yaitu ά,β dan γ. Struktur
Membran Retentat
Permeat
Jenis resistansi membran Rp : penyumbat pori Ra : adsorpsi
Rm : membran Rg : lapisan gel Rcp : konsentrasi
polarisasi
26
ά-khitin tersusun dalam rantai yang tidak sejajar dengan ikatan sangat kuat; β- khitin tersusun dalam rantai yang sejajar (paralel ) dan γ-khitin merupakan campuran dari rantai paralel dan antiparalel. Umumnya khitin diisolasi melalui rangkaian proses produksi berbahan dasar kulit udang. Proses isolasi khitin sebagai berikut pertama, demineralisasi atau proses penghilangan mineral menggunakan asam kemudian kedua, deproteinasi atau proses penghilangan protein menggunakan basa selanjutnya yang ketiga, dekolorisasi atau proses penghilangan warna menggunakan oksidator atau pelarut organik (Rismana, 2006). Struktur senyawa khitin terdapat pada Gambar 2.8 :
Gambar 2.8 Struktur Senyawa Khitin
Khitin berbentuk serpihan dengan warna putih kekuningan, memiliki sifat tidak beracun dan mudah terurai secara hayati (biodegradable). Khitin tidak larut dalam air, larutan basa encer dan pekat, larutan asam encer dan pelarut organik.
Tetapi senyawa ini larut dalam asam mineral pekat, seperti asam klorida, asam sulfat, asam nitrat. Namun asam sulfat, asam nitrat dan asam fospat dapat merusak kitin yang menyebabkan kitin terdegradasi menjadi monomer-monomer sederhana yang lebih kecil (Bastaman, 1989). Sistem pelarut yang efektif dalam melarutkan kitin adalah campuran N,N-dimetil asetamida dan LiCl 5% terlarut (Austin, 1988).
Identifikasi adanya khitin dapat dideteksi dengan reaksi warna Van Wesslink, yaitu terdiri atas larutan I2 dalam KI yang memberikan warna coklat, kemudian
27
jika ditambahkan asam sulfat berubah warnanya menjadi violet. Perubahan warna dari coklat hingga menjadi violet menunjukkan reaksi positif adanya khitin.
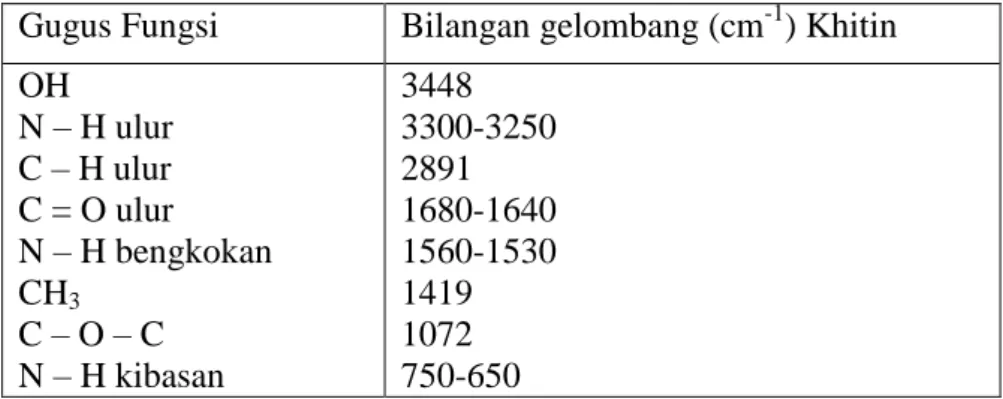
Secara kuantitatif untuk mengidentifikasi suatu senyawa khitin dengan analisis FTIR (Fourier Transform Infra Red ) . Hasil analisis gugus fungsi khitin dari kulit udang dengan FTIR dapat dilihat pada Tabel 2.1
Gugus Fungsi Bilangan gelombang (cm-1) Khitin OH
N – H ulur C – H ulur C = O ulur N – H bengkokan CH3
C – O – C N – H kibasan
3448 3300-3250 2891 1680-1640 1560-1530 1419 1072 750-650
Tabel 2.1 Karakteristik Khitin Kulit Udang (Stuart, 2003) 2.4.2. Khitosan
Khitosan adalah produk deasetilasi khitin yang merupakan polimer rantai panjang glukosamin (2-amino-2-deoksi-D-Glukosa), memiliki rumus molekul [C6H11NO4]n dengan bobot molekul 2,5x105 Dalton. Khitosan berbentuk serpihan putih kekuningan, tidak berbau dan tidak berasa. Khitosan tidak larut dalam air, larutan basa kuat, asam sulfat, pelarut-pelarut organik seperti dalam alkohol, aseton. Sifat khitosan sedikit larut dalam asam klorida maupun dalam asam nitrat, larut dalam asam asetat 1%-2%, dan mudah larut dalam asam format 0,2%-1,0%
dengan pH sekitar 4,0. Pada pH asam cenderung terjadi pengendapan dan larutan khitosan membentuk komplek polielektrolit yang bermuatan positif dengan hidrokoloid anionik menghasilkan gel. Secara biologis khitosan tidak beracun, mudah mengalami biodegradable dan polielektrolit kationik karena mempunyai gugus fungsional yaitu gugus amino selain itu terdapat juga gugus hidroksil primer dan sekunder yaitu masing-masing terikat pada atom C primer dan
28
sekunder. Adanya gugus fungsi tersebut mengakibatkan khitosan mempunyai kereaktifitasan kimia yang tinggi. Gugus fungsi amina bebas yang bersifat nukleofilik kuat yang terdapat pada khitosan menyebabkan khitosan lebih reaktif dari senyawa khitin dan memungkinkan juga untuk modifikasi kimia yang beranekaragam. Kondisi ini menyatakan bahwa khitosan termasuk salah satu material alami yang banyak memiliki manfaat mulai dari pengolahan limbah sampai untuk dunia medis. Berbeda dengan polisakarida alami lainnya seperti selulosa, alginat, agarosa, dan pektin yang memiliki sifat netral atau asam, khitosan bersifat basa karena memiliki gugus amino dalam jumlah besar pada rantai tulang punggungnya (Mak & Sun, 2008). Gugus ini dapat mengalami protonasi pada pH kurang dari 6,5, yang menjadikan khitosan polimer kationik.
Muatan positif pada khitosan kemudian dapat berikatan dengan material lain yang bermuatan negatif seperti enzim, sel, polisakarida lainnya, asam nukleat, kulit, dan rambut (Argin-Soysal, 2007).
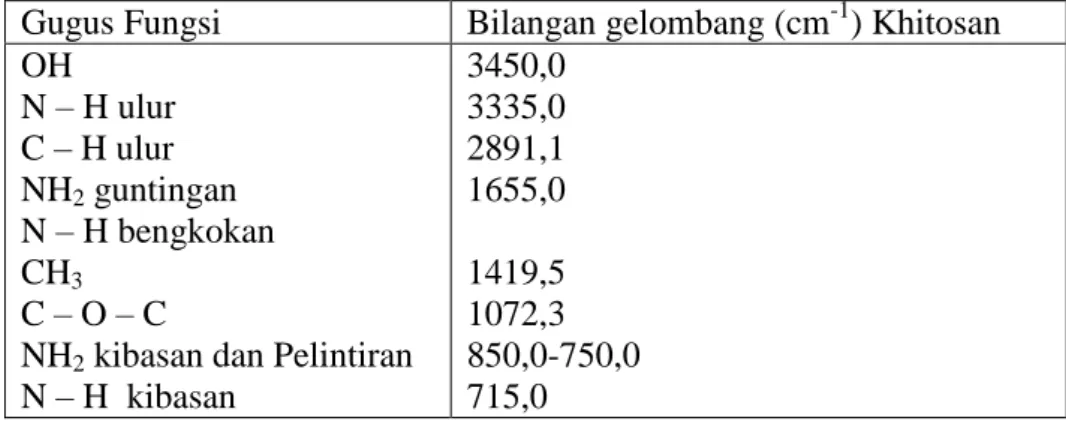
Perbedaan senyawa khitin dan khitosan adalah berdasarkan kandungan nitrogennya, bila polimer kurang dari 7% maka merupakan polimer khitin, apabila kandungan total nitrogennya lebih dari 7% maka merupakan polimer khitosan (Roberts, 1992). Hasil analisis gugus fungsi khitosan dari kulit udang dengan FTIR dapat dilihat pada Tabel 2.2.
29
Gugus Fungsi Bilangan gelombang (cm-1) Khitosan OH
N – H ulur C – H ulur NH2 guntingan N – H bengkokan CH3
C – O – C
NH2 kibasan dan Pelintiran N – H kibasan
3450,0 3335,0 2891,1 1655,0 1419,5 1072,3 850,0-750,0 715,0
Tabel 2.2 Karakteristik Khitosan Kulit Udang (Stuart, 2003)
Manfaat Kitosan di berbagai bidang industri modern cukup banyak diantaranya dalam industri farmasi, biokimia, bioteknologi, pangan, gizi, kertas, tekstil, pertanian, kosmetik, membran dan kesehatan. Pemanfaatan tersebut didasarkan atas sifat-sifatnya yang dapat digunakan sebagai bahan pengemulsi, pengkoagulasi, pengkelat termasuk memiliki sifat fisik yang khas yaitu mudah dibentuk menjadi spons, larutan, gel, pasta serat yang bermanfaat dalam aplikasinya.
Proses transformasi khitin menjadi khitosan adalah reaksi hidrolisis amida yang disertai dengan penambahan gugus hidroksil pada atom C dari gugus amida (adisi nukleofilik). Raksinya ada pada Gambar 2.9
Gambar 2.9. Adisi nukleofilik
30
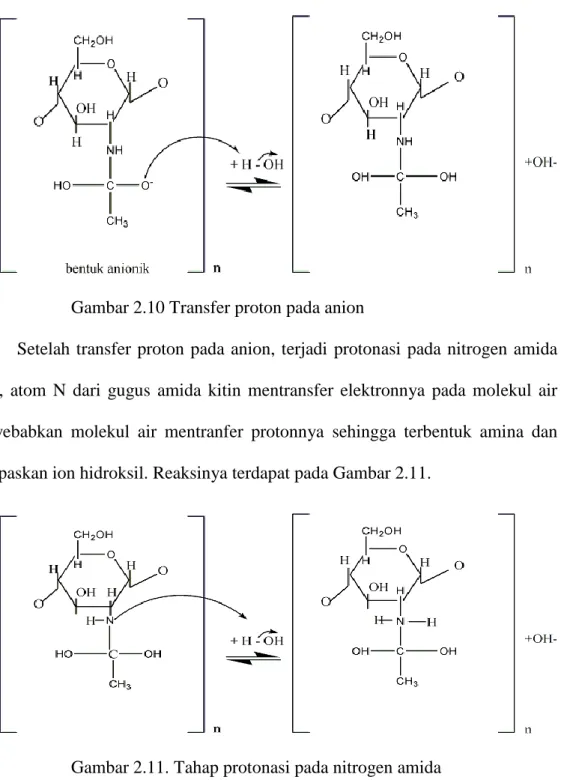
Dilanjutkan dengan transfer proton pada anion, yaitu atom O dari gugus asetil mentrasfer elektronnya pada molekul air yang ada pada proses deasetilasi, kemudian air mentransfer proton (H+) kepada atom O dari gugus asetil kitin sehingga terbentuk gugus hidroksil. Mekanisme dari reaksinya tedapat pada Gambar 2.10.
Gambar 2.10 Transfer proton pada anion
Setelah transfer proton pada anion, terjadi protonasi pada nitrogen amida yaitu, atom N dari gugus amida kitin mentransfer elektronnya pada molekul air menyebabkan molekul air mentranfer protonnya sehingga terbentuk amina dan melepaskan ion hidroksil. Reaksinya terdapat pada Gambar 2.11.
Gambar 2.11. Tahap protonasi pada nitrogen amida
31
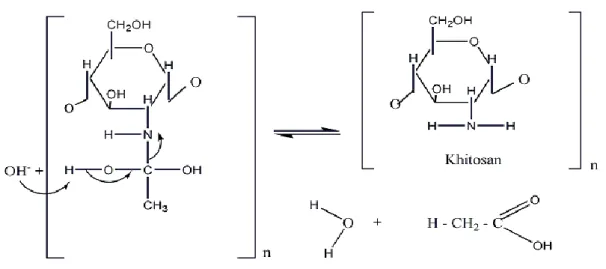
Tahap N terprotonasi, yaitu gugus hidroksil yang dilepaskan mentransfer elektronnya ke atom H dari gugus asetil kemudian atom H tersebut akan mentransfer elektronnya ke atom O serta atom O mentransfer elektronnya ke atom N yang terprotonasi sehingga ikatan dari gugus asetil terputus membentuk molekul air, molekul asam asetat dan molekul khitosan. Mekanisme reaksinya dapat dilihat pada Gambar 2.12
Gambar 2.12. Tahap pelepasan N terprotonasi 2.5.Derajat Deasetilasi
Khitin yang direaksikan dengan alkali dapat mengalami hidrolisis dari gugus asetamida kepada gugus amino (Kurita 2006). Proses hidrolisis ini selalu menggunakan NaOH dan KOH pada suhu tinggi. Hidrolisis dengan alkali dapat mengalami penurunan berat molekul, jika reaksi berlangsung lama. Oleh sebab itu dalam hidrolisis perlu dilakukan pemanasan dan khitosan yang dihasilkan tergantung dari konsentrasi alkali yang digunakan. Kemurnian khitosan dapat diketahui dari Derajat Deasetilasi (DD) diperoleh dan melarut dengan baik dalam asam asetat 1%. Sifat kelarutan ini disebabkan oleh deasetilasi dalam larutan alkali.
32
Metode FTIR (Fourier Transform Infra Red ) dapat digunakan untuk mengetahui Derajat Deasetilasi (DD) khitosan. Untuk menentukan DD digunakan metode garis oleh Moore dan Robert, seperti ditunjukkan dalam persamaan 2.10.
A1588 1
DD = 1 - x x 100% ………..(2.10) A3410 1,32
Keterangan rumus :
A = log = absorbansi
A1588 = Absorbansi pada panjang gelombang 1588 cm-1 untuk serapan gugus amida/asetamida (CH
3CONH-)
A3410 = Absorbansi pada panjang gelombang 3410 cm-1 untuk serapan gugus hidroksil (OH-)
2.6.Tinjauan tentang Spektrofotometer Ultra Violet (UV-Vis)
Hubungan antara radiasi yang diserap dan konsentrasi spesies penyerap dinyatakan oleh hukum Lambert-Beer. Dalam hukum Lambert Beer dinyatakan bahwa absorbansi berbanding langsung dengan konsentrasi. Rumusan Hukum Lambert Beer dapat dijelaskan sebagai berikut: bila suatu medium penyerap dibagi menjadi lapisan-lapisan imajiner yang tebalnya sama dan berkas sinar radiasi diarahkan melewati medium tersebut, maka setiap lapisan akan menyerap bagian yang sama dari radiasi. Absorpsi dapat dijabarkan secara matematis sebagai berikut:
= -k. C. db .…………...………...(2.11)
33
ln
= -k. C. db ……….………...………...(2.12)
log = . b. C atau ....…....……….………..(2.13)
log
=
-ε. b. C ….…...………….. ……..……..………..(2.14) C adalah konsentrasi larutan dalam molar. Jika konsentrasi larutan dalam bentuk gram/liter maka rumus 2.14. menjadi:log
= -a. b. C ………...(2.15)
log disebut optical density (OD) atau absorbansi (A), sedangkan It/I0 disebut dengan transmitans yang merupakan proporsi radiasi yang diteruskan. Bila T dikalikan dengan 100% disebut sebagai persen transmitans. Hubungan absorbansi dengan transmitan ditunjukkan pada persamaan (2.16).
A = log T = log =- ε. b.C ………….………....(2.16) Dengan ketentuan:
I0 : intensitas radiasi yang dilewatkan It : intensitas radiasi yang diserap
a : koefisien aktivitas (bila satuan kadar adalah gram/liter) ε : koefisien aktivasi molar (bila satuan kadarnya adalah molar) C : konsentrasi
A : absorbansi
b : panjang sampel /tebal kuvet
Spektrum absorpsi UV-Vis umumnya dinyatakan sebagai aluran grafik absorbansi sebagai ordinat dan panjang gelombang sebagai absis. Spektrum
34
serapan UV-Vis berasal dari transisi elektronik, tingkat energi elektronik terbagi- bagi menjadi tingkat energi vibrasi, rotasi dan translasi. Instrumentasi dari spektrofotometer dapat berupa susunan alat-alat, seperti sumber radiasi, monokromator, wadah sampel, detektor, penguat/amplifier, dan rekorder.
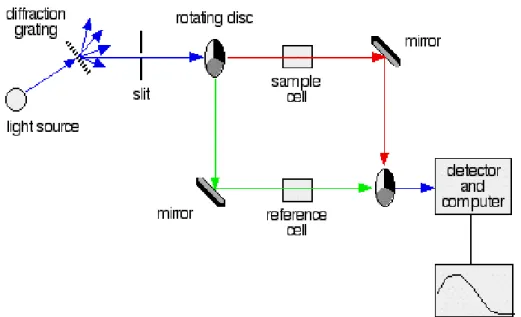
Spektrum ultraviolet pada senyawa tertentu biasanya diperoleh dengan melewatkan cahaya pada panjang gelombang tertentu (cahaya monokrom) melalui larutan encer senyawa tersebut dalam pelarut yang tidak menyerap misalnya, air, etanol, dan heksana (Khopkar, 2003). Fraksi dari radiasi yang diteruskan atau ditransmisikan oleh larutan disebut transmitan. Rangkaian sistem kerja alat UV- Vis terdapat pada Gambar 2.13.
Gambar 2.13. Mekanisme serapan UV-Vis