KIMIA.STUDENTJOURNAL, Vol. , No. , , pp. -. UNIVERSITAS BRAWIJAYA MALANG Received, , Accepted, , Published online, .
SINTESIS ANILIN
Pretty Septiana, Ningrum Arrochmah, Della Afriyana, Shofiatul Hanani, Dr. Elvina Dhiaul Iftitah, S.Si., M.Si, M. Abdi Baihaqi
Jurusan Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas Brawijaya Jl. Veteran Malang 65154
Tel : +62-341-575838, Fax : +62-341-575835 Email :[email protected]
ABSTRAK
Anilin merupakan senyawa organik dengan rumus kimia C6H5NH2 yang tersusun dari
gugus fenil dan terikat pada gugus amino. Umunya anilin digunakan sebagai bahan dasar zat warna dan karet sintesis. Sintesis anilin dapat dilakukan dengan cara reduksi nitrobenzena dengan serbuk besi dan direaksikan dengan HCl. Melalui tahap refluks, larutan kemudian ditambahkan NaOH dan selanjutnya melalui tahap destilasi uap untuk menghasilkan destilat berupa fasa air dan fasa organik yaitu anilin. Destilat yang terbentuk dilakukan proses salting out yakni dengan menambahkan NaCl agar kelarutan anilin dalam air berkurang kemudian dipisahkan antara dua fasa yang berbeda. Anilin yang diperoleh berwarna kuning kecoklatan dengan massa sebesar 6.43gram dan volume 6.4mL. Densitas anilin yang diperoleh sebesar 1.005 gram/mL dan presentase rendemen sebesar 63.5%.
Kata kunci: Anilin, refluks, destilasi uap
ABSTRACT
Aniline is an organic compound with the chemical formula C6H5NH2 composed of a
phenyl group and bonded to the amino group. Aniline generally used as a basic ingredient of dyes and synthetic rubber. Aniline synthesis can be able by reduction of nitrobenzene with iron powder and reacted with HCl. Through reflux phase, NaOH solution was then added and further through steam distillation stage to produce a distillate in the form of aqueous phase and an organic phase that is aniline. Distillate formed salting process is carried out by adding NaCl so that the solubility of aniline in reduced water is then separated between two distinct phases. The colour of aniline is brownish yellow with mass is 6,43gram and volume is 6.4mL. Density of aniline is 1.005gram/mL and the percentage yield is 63.5%.
PENDAHULUAN
Anilin merupakan bahan kimia yang dapat dibuat dari beberapa macam cara dan bahan serta dapat digunakan untuk membuat produk kimia, dalam era industrialisasi ini anilin
mempunyai peranan penting yaitu digunakan sebagai zat pewarna dan karet sintesis[1]. Karena
pentingnya anilin dalam pemanfaatannya oleh karena itu melalui penelitian sintesis anilin akan diketahui proses dan metode sintesis anilin dengan benar sehingga praktikan dapat mengaplikasikannya dengan baik dalam laboratorium. Tujuan dari penelitian sintesis anilin adalah mengetahui reaksi redoks dalam reaksi senyawa organik dan mempraktekkan prinsip
salting out dalam sintesis.
Sintesis adalah proses reaksi kimia dimana suatu senyawa bereaksi dengan senyawa lainnya dan membentuk suatu senyawa tertentu. Reaksi umumnya yang terjadi A+ B C. Senyawa yang menjadi penyusun terjadinya reaksi bisa dua, tiga, empat atau lima senyawa. Reaksi sintesis merupakan reaksi yang paling sering terjadi. Pada intinya sintesis merupakan
proses reaksi antara senyawa lain sehingga membentuk produk senyawa yang baru[2].
Anilin pertama disintesis pada abad 19 tetapi baru berguna dan menjadi penting setelah pemanfaatannya sebagai polimer. Polimer anilin dan turunannya lebih banyak digunakan karena stabilitasnya terhadap oksigen dan air. Sintesis anilin dapat dilakukan
dengan cara kimia ataupun elektrokimia[3]. Hoffman memperoleh anilin dengan mereduksi
nitrobenzene. Anilin tidak berwarna, berminyak / licin, mudah terbakar dan sedikit larut
dalam air dingin. Anilin memiliki rumus C6H5NH2 dengan struktur sebagai berikut[4].
N
H
2Gambar 1. Struktur Anilin
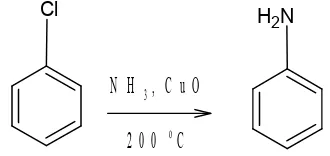
Anilin dipreparasi dengan berbagai cara yaitu reduksi nitrobenzene dengan reagen besi hidrokloric cair dan perlakuan klorobenzena dengan ammonia pada temperatur tinggi dan
F e , 3 0 % H C l
nitrobenzen anilium klorida anilin
Gambar 2. Nitrobenzen direduksi dengan Fe
Refluks adalah salah satu metode untuk mensintesis suatu senyawa organik maupun anorganik. Prinsip metode refluks adalah pelarut volatil yang digunakan akan menguap pada temperatur tinggi namun akan di dinginkan dengan kondensor sehingga akan mengembun dan
turun lagi kedalam wadah reaksi sehingga pelarut akan tetap ada selama reaksi berlangsung[6].
Prinsip kerja dari destilasi uap adalah memisahkan suatu campuran yang memiliki titik didih tinggi dengan cara mengalirkan uap kedalamnya dimana senyawa yang memiliki titik didih yang tinggi sebelum mencapai titik didihnya dimurnikan dengan menggunakan uap atau air mendidih. Penerapan dari destilasi uap adalah untuk mengekstrak beberapa produk alam seperti minyak eucalliptus, minyak sitrus dari lemon atau jeruk dan untuk ekstraksi minyak
parfum dari tumbuhan[7].
Reaksi Diels Alder merupakan reaksi sikloadisi yang bergantung pada temperatur dan mekanismenya melibatkan tumpang tindih antara orbital sigma dan orbital phi. Reaksi ini terjadi antara molekul dengan dua ikatan rangkap yang terkonjugasi (diena) dan molekul dengan satu ikatan rangkap ganda (dienofil) serta menghasilkan dua ikatan karbon-karbon
METODA PENELITIAN
Bahan dan Alat
Peralatan utama yang digunakan pada penelitian ini yaitu satu set alat refluks dan satu set alat destilasi. Peralatan analisa meliputi gelas ukur, gelas kimia, pipet tetes, pengaduk, neraca analitik, oven, corong pisah, aluminium foil, bola hisap, batu didih, termometer, tabung reaksi, dan botol semprot. Bahan yang digunakan adalah larutan nitrobenzena, serbuk
besi, larutan HCl, larutan NaOH, padatan NaCl, larutan FeCl3, dan larutan kloroform.
Prosedur
Penelitian sintesis anilin digunakan dua metode, yaitu metode refluks dan metode destilasi uap. Larutan nitrobenzena dipipet sebanyak 25mL menggunakan pipet ukur dan dimasukkan ke labu alas bulat, kemudian ditambahkan 25gram serbuk besi sehingga terbentuk gumpulan hitam. Kemudian labu alas bulat dimasukkan ke wadah yang berisi air es dan ditambahkan 50mL larutan HCl sedikit demi sedikit, setiap 5 tetes penambahan labu digoyang. Setelah penambahan 50mL larutan HCl, dimasukkan batu didih kedalam labu alas bulat dan dirangkai alat refluks kemudian direfluks selama satu jam setelah uap air pertama menetes kedalam labu alas bulat. Setelah dilakukan refluks larutan berwarna hitam kekuningan, kemudian didinginkan pada temperatur ruangan sekitar ± 10 menit atau hingga larutan dingin. Padatan NaOH ditimbang sebanyak 15gram dan dilarutkan kedalam 25mL akuades kemudian dikocok hingga seluruh NaOH larut. Setelah itu dimasukkan kedalam labu alas bulat dan dirangkai alat destilasi. Katel dihubungkan pada labu alas bulat ketika dilakukan destilasi agar terbentuk uap yang menjaga tekanan dalam labu saat temperatur tinggi. Corong pisah digunakan sebagai wadah penampung destilat yang diperoleh agar mudah saat dilakukan pemisahan fasa. Destilat yang diperoleh berwarna kuning-putih untuk fasa cair dan berwarna kuning-kecoklatan untuk fasa organik atau anilin. Destilat yang diperoleh ditambahkan padatan NaCl sebanyak 20gram agar kelarutan anilin dalam fasa cair berkurang. Larutan dikocok hingga seluruh NaCl larut dan terbentuk dua lapisan yang jelas antara fasa air dan anilin. Anilin berada di lapisan atas karena berat jenis anilin lebih ringan daripada berat jenis air. Setelah itu dipisah dan anilin yang diperoleh dihitung volume, massa, densitas dan rendemennya. Diperoleh volume anilin sebanyak 6.4mL, massa anilin 6.43gram, densitas 1.005gram/mL dan rendemen 63.6%. Dua tabung reaksi diisi kloroform dan larutan
anilin pada kloroform mampu larut dan terbentuk larutan berwarna kuning cerah, sedangkan
pada larutan FeCl3 terbentuk endapan coklat di lapisan bawah dan lapisan atas tetap tidak
berwarna, sehingga anilin tidak larut dalam larutan FeCl3.
HASIL DAN PEMBAHASAN
Berdasarkan penelitian yang telah dilakukan, pada saat larutan nitrobenzena yang berwarna kuning ditambahkan dengan serbuk besi, larutan campuran yang dihasilkan berwarna hitam. Ketika ditetesi dengan larutan HCl sebanyak 50mL muncul asap putih yang
merupakan gas H2. Ketika campuran direfluks dan warna larutan hitam. Pada saat pembuatan
larutan NaOH dengan aquades, warna larutan adalah putih dan gelas kimia terasa panas. Hal tersebut menunjukkan reaksi eksoterm (melepas panas). Pada saat dilakukan destilasi uap, dihasilkan destilat dalam corong pisah yang terdiri dari beberapa lapisan. Pada lapisan paling atas dan paling bawah, warna larutan adalah coklat. Lapisan tersebut menandakan adanya anilin. Sedangkan pada lapisan tengah berwarna kuning yang merupakan fasa air.
Ketika ditambahkan garam NaCl sebanyak 20gram dan dilakukan pengocokan, fasa organik yang semula berada pada lapisan atas dan bawah menjadi berada dibagian atas secara keseluruhan. Karena adanya pengocokan larutan didalam corong pisah, anilin menjadi terdistribusi merata dikedua fasa. Ketika didiamkan, terbentuk dua lapisan dimana lapisan atas mengandung anilin berwarna kuning kecoklatan sedangkan lapisan bawah merupakan fasa air berwarna keruh.
Massa anilin yang diperoleh sebesar 6.43gram. Volume anilin yang diperoleh adalah sebesar 6.4mL. Rendemen yang diperoleh sebesar 63.6%. Rendemen yang dihasilkan tidak 100% karena kemungkinan adanya serbuk besi yang mengalami oksidasi menjadi Fe2O3
sehingga tidak dalam bentuk murni. Sedangkan dalam proses reduksi nitrobenzena digunakan Fe murni. Hal ini menyebabakan nitrobenzena tidak sepenuhnya tereduksi. Selain itu karena adanya pengotor atau terkontaminasi zat lain sehingga menyebabkan hasil rendemen yang
diperoleh tidak sempurna. Hal lain yang menjadi penyebab adalah karena banyaknya gas H2
yang mudah menguap dapat menyebabkan nitrobenzene kurang tereduksi secara sempurna.
Reduksi
diperoleh lebih banyak. Reduktor yang digunakan apabila semakin asam pHnya (penambahan HCl semakin banyak) maka anilin yang diperoleh juga semakin banyak.
Anilin merupakan senyawa amina aromatis dengan rumus struktur C6H5NH2 yang
terdiri dari gugus fenil terikat gugus amino. Anilin tidak berwarna, berminyak, dan mengeluarkan bau menyengat dan bersifat basa. Anilin sangat sukar larut dalam air karena anilin merupakan senyawa hidrokarbon hidropobik dengan gugus amina, namun ion anilinum larut dalam air. Anilin tidak berwarna namun perlahan-lahan bisa teroksidasi karena interaksi dengan udara dan berubah warna menjadi kuning atau merah-coklat. Anilin memiliki berat
molekul 93.13gram/mol dengan titik leleh sebesar -6 C dan titik didih sebesar 184 C. Berat⁰ ⁰
jenisnya 1.03gram/cm3. Kelarutan dalam air 0,3gram/L dang titik nyala sebesar 70 C⁰ [9]. Anilin
yang diperoleh dari hasil penelitian memiliki sifat fisik berupa cairan berwarna kuning kecoklatan, berminyak dengan massa jenis sebesar 1.005gram/mL. Hasil yang diperoleh sesuai dengan teoritis. Hal ini membuktikan bahwa sebagian besar nitrobenzene telah berhasil tereduksi menjadi anilin.
Pada uji kelarutan, anilin yang diperoleh direaksikan dengan FeCl3 dan kloroform.
Pada penambahan kloroform, anilin dapat larut dan menghasilkan larutan dengan warna kuning. Sedangkan pada penambahan FeCl3, anilin tidak dapat larut dan menghasilkan
endapan berwarna coklat kehitaman. Uji kelarutan senyawa organik bertujuan untuk mengetahui kepolaran dari suatu larutan. Pelarut kloroform bersifat non polar. Anilin merupakan benzene tersubstitusi yang memiliki sifat non polar. Hal ini menyebabkan anilin
mudah larut dalam kloroform dan sukar larut dalam akuades[10]. Berdasarkan prinsip “like
dissolves likes” dimana senyawa dengan sifat non polar akan mudah larut dalam pelarut non polar, begitupun sebaliknya.
Reaksi redoks yang terjadi pada sintesis anilin adalah sebagai berikut :
Mekanisme reaksi pembentukan anilin adalah sebagai berikut :
Hasil sintesis anilin dengan mereduksi nitrobenzena dengan serbuk besi dan direaksikan menggunakan HCl diperoleh massa anilin sebesar 6.43g, volume 6.4mL, densitas 1.005g/mL dan rendemen 63.6%. Metode yang digunakan dalam sintesis ini yaitu refluks untuk mensistesis dan destilasi uap untuk memisahkan campuran dengan perbedaan titik didih yang tinggi. Anilin yang diperoleh berwarna kuning kecoklatan dan nilai densitas hasil penelitian apabila dibandingkan dengan teotiritis memiliki perbedaan yang sangat sedikit.
UCAPAN TERIMAKASIH
DAFTAR PUSTAKA
[1] Suhendra, E, 2013, Keberadaan Anilin di Sungai Citarum Akibat Penggunaan Azo pada
IndustriTekstil, Universitas Diponegoro, Semarang.
[2] Muria, 2006, Sintesis, www.ahlikimia.com, diakses tanggal 6 Mei 2016.
[3] Valle M.A, Manuel A, Euddy D, Pedro P, Fernando R, Maria B, Monica P and Juan P,
2012, Electro-Synthesis and Characterization of Aniline and o-aniside Oligomers,
International Journal of Electrochemical Science, 2552-2565.
[4] Kurniawan, 2012, Penuntun Praktikum Farmasi I, Universitas Halvaleo, Kendari.
[5] Morrison, R and Robert N.B, 2007, Organic Chemistry Sixth Eddition, Prectice Hall of
India, New Delhi.
[6] Setyani,W, 2014, Metode Refluks, www.analisakimia.com, diakses padaa 6 Mei 2016.
[7] Guenter, E, 2007, Ekstraksi Minyak Atsiri dengan Metode Distilasi Uap, UI Press, Jakarta.
[8] Mc-Murry, 2008, Organic Chemistry, Cengage Learning, Cornell University.
[9] Hadiana, Deni, 2012, Polimerisasi Anilih oleh Horseadish Peroksida dan
Karalteristiknya, www.lib.ui.ac.id, diakses pada 10 Mei 2016.