METODE PENELITIAN
3.1 Waktu dan Tempat Penelitian
Penelitian dilaksanakan pada Juli sampai September 2021 di Laboratorium Kimia, Laboratorium Teknik 1, Institut Teknologi Sumatera, dan Laboratorium Teknologi Hasil Pertanian, Politeknik Negeri Lampung.
3.2 Bahan dan Alat
Bahan utama yang digunakan untuk penelitian ini yaitu sampel buah dan keripik buah, yaitu nangka, pisang muli, dan nanas madu. Kemudian bahan yang dibutuhkan untuk pengujian yaitu, larutan H2SO4 0,255 N, NaOH (0,3 N, 0,1 N, 40%), Na2SO4 anhidrat, CuSO4, aquades, HCl (0,1 N), indikator PhenolPtalein, etanol, pelarut n-heksana, alkohol 95%, K2SO4 10%.
Alat yang diperlukan pada penelitian ini yaitu oven, desikator, hotplate (Thermo Scientific Probe Cimarec), labu Kjeldahl, neraca analitik (ketelitian 0,1 mg AND GF-300 dan 0,01 mg Chrus Pioneer), destilator (Velp Scientifica F30200140), labu lemak 250 mL (IWAKI Asahi Glass), kertas saring, kapas bebas lemak, alat soxhlet, erlenmeyer (Duran 1000 mL, IWAKI Asahi Glass 100 mL), pendingin balik (Pyrex), corong buncher, cawan crucible 25 mL (Hardenwanger), cawan logam, gelas beaker 500 mL (IWAKI Asahi Glass), batang pengaduk, kertas lakmus, alat penyaring (Jouan), Furnace (Heraceus instrument), krustang, spatula, pestel, dan mortar.
3.3 Tahapan Penelitian
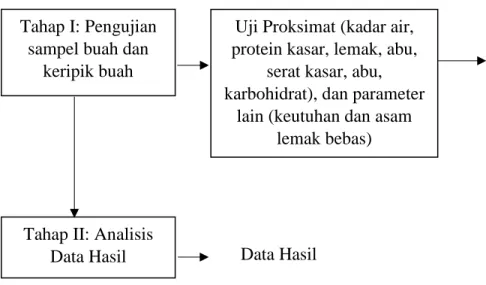
Penelitian ini dibagi menjadi dua tahap yaitu 1) pengujian sampel buah dan keripik buah, dan (2) analisis data. Diagram alir tahap penelitian ditunjukkan pada Gambar 3.1 berikut ini:
Gambar 3. 1 Tahapan Penelitian
3.4 Pengujian Sampel Buah dan Keripik Buah
Sampel buah segar yang digunakan yaitu buah pisang muli, nanas madu dan nangka. Sampel buah yang dipilih yaitu yang berumur tua. Kemudian terlebih dahulu dipisahkan dari kulit dan bijinya serta yang diambil hanya bagian daging buahnya saja. Setelah itu, buah tersebut dipotong-potong atau dicacah menjadi ukuran yang sangat kecil kemudian ditempatkan di dalam wadah yang bersih.
Pengujian yang dilakukan yaitu uji proksimat meliputi pengujian protein kasar, lemak, abu, serat kasar, dan karbohidrat pada buah segar.
Sampel keripik buah yang digunakan terdiri atas keripik pisang muli, keripik nanas madu, dan keripik nangka dalam kemasan 100 g. Sampel keripik buah dipersiapkan dengan mengambil dan membuka sebanyak satu kemasan masing-masing, kemudian dipindahkan ke wadah plastik bersih, kering, dan di seal menggunakan sealer. Pengujian dilakukan triplo, dengan mengambil masing-masing sampel keripik buah dari tiga kemasan berbeda. Pengujian yang dilakukan yaitu uji proksimat meliputi pengujian air, karbohidrat, lemak, protein kasar, serat kasar, dan abu pada buah segar dan keripik buah. Parameter lain yang diukur yaitu keutuhan, dan asam lemak bebas pada keripik buah.
Tahap I: Pengujian sampel buah dan
keripik buah
Data Hasil
Uji Proksimat (kadar air, protein kasar, lemak, abu,
serat kasar, abu, karbohidrat), dan parameter
lain (keutuhan dan asam lemak bebas)
Tahap II: Analisis Data Hasil
Pengujian
Data
Berikut ini merupakan prosedur analisis protein kasar, serat kasar, abu, asam lemak bebas, lemak, air, keutuhan, dan karbohidrat :
3.4.1 Penentuan Kadar Protein Kasar
Analisis kadar protein menggunakan metode Gunning. Metode ini bekerja berdasarkan penentuan kadar nitrogen yang akan menunjukkan jumlah protein yang juga mengikat senyawa N bukan protein seperti urea, asam nukleat, asam amino, nitrat, nitrit, amida, purin, dan pirimidin [68]. Sampel yang akan diuji dihaluskan kemudian ditimbang sebanyak 0,5-1 g lalu dimasukkan ke dalam labu Kjeldahl 100 mL. Sebanyak 1 g Na2SO4 anhidrat dan 10 mL H2SO4 kemudian ditambahkan kedalam labu Kjeldahl. Kemudian agar destruksi mudah dilakukan, ditambahkan 0,1-0,3 CuSO4 lalu dihomogenkan. Pendestruksian dilakukan di atas hotplate dalam lemari asam dengan api kecil, apabila asap sudah hilang api dibesarkan. Pemanasan berakhir apabila larutan menjadi jernih. Setelah dingin, sebanyak 100 mL dan larutan NaOH 40% ditambahkan kedalam labu Kjeldahl.
Setelah itu, dilakukan tahap destilasi. Labu Kjeldahl dipanaskan sampai ammonia menguap semua, distilat ditampung dalam erlenmeyer berisi 25 mL HCL 0,1N yang sudah diberi indikator Phenolptalein 1% sebanyak 2 tetes. Distilasi diakhiri setelah distilat tertampung sebanyak 150 mL atau setelah distilat yang keluar tak bersifat basa. Kemudian distilat dititrasi dengan larutan NaOH 0,1 N hingga berwarna merah muda [69]. Setelah itu, dilakukan penetapan blanko seperti perlakuan di atas namun tanpa menggunakan sampel. Perhitungan kadar protein dapat dilakukan dengan rumus berikut:
% N = (ml NaOH blanko-ml NaOH sampel)x N NaOH x 14,088
bobot sampel x 100
% Protein (bb) = %N x Faktor Konversi
% Protein (bk) = %kadar protein kasar (basis basah)x 100 (100-%kadar air)
3.4.2 Penentuan Kadar Serat Kasar
Analisis kadar serat kasar dilakukan dengan metode hidrolisis asam basa.
Penimbangan 2 g sampel (dibebaskan lemaknya dengan ekstraksi soxhletasi atau dengan cara diaduk atau diendapkan). Sampel dipindahkan dalam Erlenmeyer 600 mL, ditambahkan sebanyak 200 mL H2SO4 kemudian ditutup dengan pendingin balik dan didihkan selama 30 menit. Residu dipindahkan dari kertas saring kedalam erlenmeyer kembali dengan spatula, dan sisanya dibersihkan dengan NaOH mendidih (1,25 g NaOH/100mL = 0,313 N NaOH) sebanyak 200 mL sampai semua residu masuk ke dalam erlenmeyer. Residu dididihkan dengan pendingin balik sambil sesekali digoyang-goyangkan selama 30 menit. Residu kemudian disaring menggunakan kertas saring yang telah diketahui beratnya atau krus Gooch yang telah dipijarkan dan diketahui beratnya, sambil dicuci dengan larutan K2SO4 10.
Residu kemudian dicuci kembali dengan aquades mendidih dan kemudian dengan 15 mL Alkohol 95%. Kertas saring atau krus dikeringkan dengan isinya pada 110C selama 1-2 jam sampai berat konstan, lalu didinginkan dalam desikator dan ditimbang [70]. Kadar serat kasar dapat dihitung dengan rumus di bawah ini:
% Serat Kasar (bb) = B-CA x 100
% Serat Kasar (bk) = %kadar serat kasar (basis basah)x 100 (100-%kadar air)
Keterangan:
A : bobot sampel (g)
B : bobot kertas saring dan serat (g) C : bobot kertas saring (g)
3.4.3 Penentuan Kadar Abu
Analisis kadar abu dilakukan dengan metode tanur. Cawan porselen dikeringkan dalam oven selama satu jam pada suhu 105oC. Cawan porselen kemudian didinginkan dalam desikator selama 15 menit lalu ditimbang. Sebanyak 5 g sampel
tidak berasap. Cawan berisi sampel dimasukkan kedalam tanur pengabuan dengan suhu 600oC selama 1 jam. Sampel ditimbang hingga berat konstan [71].
Perhitungan:
% Kadar Abu (bb) = berat sampelberat abu x 100%
% Kadar Abu (bk) = %kadar abu (basis basah)x 100 (100-%kadar air)
Keterangan:
Berat abu : (berat abu + cawan) – berat cawan Berat sampel : berat sampel mula-mula 3.4.4 Penentuan Kadar Asam lemak Bebas
Sebanyak 5 g sampel diambil, kemudian ditempatkan ke dalam erlenmeyer. Lalu ditambahkan sebanyak 50 mL alkohol netral yang sudah dipanaskan hingga mendidih. Selanjutnya, ditambahkan sebanyak 3 tetes indikator PP. Titrasi dengan menggunakan NaOH 0,1 N sampai warna berubah menjadi merah muda dan tidak hilang selama 30 detik [72]. Kadar asam lemak bebas dihitung dengan cara:
% ALB sebagai oleat (bb) = V x 0.25 x 282 x 100 bobot ekstrak x 1000
Keterangan:
V : volume NaOH 0,1 N (mL) 0.25 : molaritas dari NaOH
282 : bobot ekuivalen dari ALB oleat 3.4.5 Penentuan Kadar Lemak
Analisis kadar lemak dilakukan dengan menggunakan metode ekstraksi soxhlet.
Labu lemak dikeringkan dalam oven, kemudian didinginkan dalam desikator lalu ditimbang (W2). Sebanyak 2 g sampel (W) dibungkus ke dalam selongsong kertas saring yang dialasi dan disumbat dengan kapas, kemudian dimasukkan ke dalam alat ekstraksi dan sokhlet yang telah dihubungkan dengan labu lemak. Refluks
lemak dengan heksana selama 4-6 jam. Pelarut yang ada dalam labu lemak didestilasi dan pelarut ditampung kembali. Labu yang berisi lemak hasil ekstraksi dipanaskan dalam oven pada suhu 105°C selama 1 jam, kemudian didinginkan dalam desikator dan ditimbang (W1) [71]. Pemanasan dan penimbangan diulangi hingga tercapai bobot konstan. Kadar lemak dapat diperoleh dengan persamaan berikut:
% Kadar lemak (bb) = W-W1
W2 x 100%
% Kadar lemak (bk) = %kadar lemak (basis basah) x 100 (100-%kadar air)
Keterangan:
W : Berat sampel (g) W1 : Berat labu lemak (g)
W2 : Berat labu lemak + ekstrak lemak (g) 3.4.6 Penentuan Kadar Air
Analisis kadar air dilakukan dengan metode thermogravimetri. Cawan alumunium kosong dikeringkan dalam oven dengan suhu 105°C selama 15 menit. Cawan diangkat dan didinginkan dalam desikator selama 20 menit. Cawan ditimbang kemudian dicatat beratnya. Mortar dan alu disiapkan kemudian sampel ditimbang seberat 1-2 g dan dimasukan kedalam cawan kering. Sampel dimasukkan kedalam oven bersuhu 100-102°C selama 6 jam. Sampel dimasukan kembali kedalam oven selama 30 menit. Setelah 30 menit, sampel didinginkan kembali kedalam desikator kemudian ditimbang. Perlakuan ini dilakukan sampai mencapai berat konstan atau selisih penimbangan kurang dari 0,003 g [71].
Perhitungan kadar air dalam bahan berdasarkan basis basah dapat di hitung dengan rumus berikut:
% Kadar air (bb) = berat awal-berat akhir
berat sampel x 100%
Sampel uji diambil dari kemasan utuh, kemudian diletakkan di atas wadah yang bersih dan kering. Kemudian ditimbang seluruh bobot keripik (W). Keripik yang patah atau tidak sempurna dipisahkan dari keripik yang utuh. Lalu ditimbang bobot keripik yang tidak sempurna tersebut (W1). Kemudian dihitung persentase keutuhan dan ketelitiannya [67].
% Keutuhan = W-W1
W x 100%
Keterangan:
W : Bobot seluruh keripik W1 : Bobot tak utuh keripik
3.4.8 Penentuan Kadar Karbohidrat
Penentuan kadar karbohidrat menggunakan metode karbohidrat total secara by difference [70].
Kadar karbohidrat (bk) = 100% – (kadar air + kadar abu + kadar protein + kadar lemak)
3.5 Analisis Data
Data yang didapatkan akan terlebih dahulu dilakukan perhitungan pada masing- masing parameter berupa kadar air, protein kasar, lemak, abu, serat kasar, dan karbohidrat pada buah segar dan keripik buah. Parameter lain yang diukur yaitu keutuhan dan asam lemak bebas pada keripik buah. Data yang diperoleh ditampilkan menggunakan tabel untuk mempermudah dalam penyajian data. Data yang ditampilkan berupa hasil rata-rata ± standar deviasi. Kemudian data hasil uji proksimat akan dianalisis dengan T-test menggunakan Microsoft Excel dan dibandingkan dengan SNI 8370:2018 [67].