ABSTRAK
DEFISIENSI G6PD SEBAGAI FAKTOR RISIKO TERHADAP HIPERBILIRUBINEMIA PADA NOENATUS BERUMUR DUA HARI DI
RSAB HARAPAN KITA, JAKARTA BARAT, TAHUN 2015
Shielda N Shidarta, 2016. Pembimbing I : Lisawati Sadeli, dr., M. Kes Pembimbing II : Cindra Paskaria, dr., M.K.M
Hiperbilirubinemia merupakan salah satu masalah paling umum yang terjadi pada neonatus. Lebih dari 80% neonatus mengalami ikterus akibat hiperbilirubinemia yang didominasi oleh bilirubin indirek. Hiperbilirubinemia dikatakan patologis ketika kadar bilirubin indirek meningkat lebih dari 7 mg/dL pada saat neonatus berusia dua sampai lima hari.
Salah satu penyebab hiperbilirubinemia patologis adalah defisiensi glucose-6-phosphate dehydrogenase (G6PD). Enzim G6PD berperan untuk menyediakan energi bagi NADPH agar dapat mempertahankan glutathione dalam bentuk terreduksi (GSH) sebagai antioksidan sehingga tidak terjadi denaturasi hemoglobin dan hemolisis akibat kerusakan membran eritrosit.
Tujuan penelitian ini untuk memperlihatkan pentingnya dilakukan skrining defisiensi G6PD pada neonatus. Penelitian ini bersifat analitik dengan desain kontrol kasus. Jumlah sampel adalah 912 responden (whole sampling) di Rumah Sakit Anak dan Bunda (RSAB) Harapan Kita, Jakarta Barat, tahun 2015, yang memenuhi kriteria inklusi dan eksklusi. Subjek penelitian adalah neonatus berumur dua hari yang diperiksa kadar bilirubin serum dan aktivitas G6PD.
Hasil uji chi-square menunjukkan bahwa defisiensi G6PD menjadi faktor risiko yang signifikan (p<0,05) terhadap terjadinya hiperbilirubinemia.
Simpulan dari penelitian ini adalah defisiensi G6PD menjadi faktor risiko hiperbilirubinemia pada neonatus berumur dua hari di RSAB Harapan Kita, Jakarta Barat, tahun 2015.
ABSTRACT
G6PD DEFICIENCY AS A RISK FACTOR FOR NEONATAL HYPERBILIRUBINEMIA AT TWO DAYS OLD IN RSAB HARAPAN KITA, WEST JAKARTA, 2015
Shielda N Shidarta, 2016. 1st advisor : Lisawati Sadeli, dr., M. Kes 2nd advisor : Cindra Paskaria, dr., M.K.M
Hyperbilirubinemia is one of the most common problems in neonates. More than 80% neonates have jaundice due to hyperbilirubinemia were dominated by indirect bilirubin. Pathological hyperbilirubinemia defines when indirect bilirubin levels increased by more than 7 mg/dL at two to five days old.
One of the pathological hyperbilirubinemia causes is glucose-6-phosphate dehydrogenase (G6PD) deficiency. The role of this enzyme is to provide energy for NADPH to maintain the reduced glutathione (GSH) form as an antioxidant to prevent hemoglobin denaturation and hemolysis because damage to the erythrocyte membrane.
The aim of the research was to show that screening for G6PD deficiency is important. This research was an analytic case-control design. The total sample was 912 respondents (whole sampling) in Rumah Sakit Anak dan Bunda (RSAB) Harapan Kita, West Jakarta, during 2015, who meet inclusion and exclusion criteria. Subjects are two days old neonates and are examined their serum bilirubin and the activity of G6PD.
Chi-square result showed that G6PD deficiency as a significant (p<0,05) risk factor on the occurance of hyperbilirubinemia.
It can be concluded that G6PD deficiency becomes a risk factor for neonatal hyperbilirubinemia at two days old in RSAB Harapan Kita, West Jakarta, during 2015.
DAFTAR ISI
1.4 Manfaat Karya Tulis Ilmiah ... 4
1.5 Landasan Teori dan Hipotesis ... 4
1.5.1 Landasan Teori ... 4
1.5.2 Hipotesis Penelitian ... 6
BAB II TINJAUAN PUSTAKA ... 7
2.1 G6PD ... 7
2.2 Fisiologi Pembentukan Bilirubin ... 10
2.3 Anatomi dan Histologi Hepar ... 12
2.4 Hiperbilirubinemia ... 13
2.5 Hiperbilirubinemia pada Neonatus ... 14
2.6.2 Ikterus Hepatik ... 18
2.6.3 Ikterus Post-Hepatik ... 19
2.7 Ikterus pada Neonatus ... 19
2.8 Kernikterus ... 20
BAB III BAHAN DAN METODE PENELITIAN ... 22
3.1 Bahan Penelitian ... 22
3.2 Populasi dan Sampel ... 22
3.3 Kriteria Penelitian Subjek ... 22
3.3.1 Kriteria Inklusi ... 22
3.3.2 Kriteria Eksklusi ... 22
3.4 Lokasi dan Waktu Penelitian ... 23
3.5 Metode Penelitian ... 23
3.5.1 Desain Penelitian ... 23
3.5.2 Data yang Diukur ... 23
3.5.3 Analisis Data ... 23
3.6 Definisi Operasional Variabel Penelitian ... 23
3.7 Prosedur Penelitian ... 24
3.8 Aspek Etik Penelitian ... 24
BAB IV HASIL PENELITIAN DAN PEMBAHASAN ... 26
4.1 Hasil Penelitian ... 26
4.1.1 Gambaran Kasus Defisiensi G6PD pada Neonatus Berumur Dua Hari di RSAB Harapan Kita, Tahun 2015 ... 26
4.1.3 Gambaran Kasus Hiperbilirubinemia pada Neonatus dengan
Defisiensi G6PD yang Berumur Dua Hari di RSAB
Harapan Kita, Tahun 2015 ... 28
4.1.4 Hasil Analisis Hubungan G6PD dengan Hiperbilirubinemia pada Neonatus Berumur Dua Hari di RSAB Harapan Kita, Tahun 2015 ... 29
4.2 Pembahasan ... 30
4.3 Uji Hipotesis ... 34
4.3.1 Hipotesis Penelitian ... 34
4.3.2 Hal-Hal yang Mendukung Penelitian ... 34
4.3.3 Hal-Hal yang Tidak Mendukung Penelitian ... 34
4.3.4 Simpulan ... 34
BAB V SIMPULAN DAN SARAN ... 35
5.1 Simpulan ... 35
5.2 Saran ... 35
DAFTAR PUSTAKA ... 36
LAMPIRAN ... 40
DAFTAR TABEL
Halaman
Tabel 2.1 Obat-Obat yang Dihindari pada Defisiensi G6PD ... 8
Tabel 2.2 Normal Bilirubin Total ... 14
Tabel 3.1 Variabel Penelitian, Definisi Operasional, dan Skala Ukur ... 24
Tabel 4.1 Gambaran Kasus Defisiensi G6PD ... 26
Tabel 4.2 Gambaran Jenis Kelamin pada Kasus Defisiensi G6PD ... 26
Tabel 4.3 Gambaran Ikterus pada Kasus Defisiensi G6PD ... 27
Tabel 4.4 Gambaran Anemia Hemolitik pada Kasus Defisiensi G6PD ... 27
Tabel 4.5 Gambaran Kasus Hiperbilirubinemia pada Neonatus ... 27
Tabel 4.6 Gambaran Kasus Hiperbilirubinemia pada Neonatus dengan Defisiensi G6PD ... 28
Tabel 4.7 Gambaran Risiko Kernikterus pada Neonatus dengan Defisiensi G6PD ... 28
DAFTAR GAMBAR
Halaman
Gambar 1.1 Mekanisme Terjadinya Hiperbilirubinemia pada
Neonatus dengan Defisiensi G6PD ... 6
Gambar 2.1 Aktivitas G6PD ... 7
Gambar 2.2 Fisiologi Pembentukan Bilirubin ... 10
Gambar 2.3 Histologi Hepar ... 13
Gambar 2.4 Nomogram Bhutani ... 15
Gambar 2.5 Patofisiologi Ikterus ... 17
DAFTAR LAMPIRAN
Halaman
Lampiran 1: Data Penelitian Neonatus Berumur Dua Hari
dengan Defisiensi G6PD di RSAB Harapan Kita,
Jakarta Barat, Tahun 2015 (Bagian 1) ... 42
Lampiran 2: Data Penelitian Neonatus Berumur Dua Hari dengan Defisiensi G6PD di RSAB Harapan Kita, Jakarta Barat, Tahun 2015 (Bagian 2) ... 43
Lampiran 3: Chi-Square dan Odd Ratio ... 44
Lampiran 4: Surat Keputusan Komisi Etik ... 46
BAB I
PENDAHULUAN
1.1 Latar Belakang
Hiperbilirubinemia merupakan keadaan bilirubin yang meningkat di dalam
darah. Peningkatan tersebut dapat terjadi pada kadar bilirubin total, bilirubin
indirek, dan/atau bilirubin direk. Hal ini dapat diketahui melalui pemeriksaan
bilirubin serum secara kuantitatif (Ambalavanan & Carlo, 2011).
Salah satu masalah paling umum yang ditemukan pada neonatus adalah
hiperbilirubinemia (Porter & Dennis, 2002). Lebih dari 80% neonatus mengalami
ikterus akibat akumulasi bilirubin pada kulit, sklera, dan membran mukosa. Oleh
karena itu, American Academy of Pediatrics (AAP) merekomendasi untuk
melakukan melakukan pemeriksaan bilirubin pada seluruh neonatus sebelum
dipulangkan dari rumah sakit (Tortora & Derrickson, 2012; Newman, 2009;
Yaworski, Van Meer, & Wong, 2002).
Ikterus umumnya terjadi akibat peningkatan kadar bilirubin indirek karena
denaturasi membran eritrosit sehingga ikterus dapat disertai dengan anemia
hemolitik (WHO Working Group, 1989). Peningkatan bilirubin indirek melebihi 7
mg/dL pada saat neonatus berumur dua sampai lima hari menunjukkan
hiperbilirubinemia patologis yang berhubungan dengan tingginya risiko
kernikterus (kerusakan otak) yang dapat menimbulkan kecacatan hingga kematian
(Ambalavanan & Carlo, 2011).
Hiperbilirubinemia patologis dapat diakibatkan oleh banyak hal, seperti
defisiensi glucose-6-phosphate dehydrogenase (G6PD), inkompabilitas ABO,
inkompabilitas rhesus (Rh), serta infeksi atau sepsis (Porter & Dennis, 2002).
Defisiensi G6PD merupakan kelainan enzim tersering pada jalur pentosa
fosfat. Kekurangan enzim ini menyebabkan degradasi heme yang lalu
menimbulkan kerusakan pada membran eritrosit akibat kurangnya GSH
Hiperbilirubinemia pada neonatus akibat defisiensi G6PD biasanya terjadi
akibat tiga faktor pencetus. Pertama, ibu hamil dan menyusui yang mengonsumsi
obat-obat tertentu, seperti antimalaria, obat kemoterapi, dan antibiotik yang
melapaskan reactive oxygen species (ROS). Kedua, ibu hamil dan menyusui yang
mengonsumsi kacang fava yang mengandung suatu oksidan yang potensial
menimbulkan stres oksidatif. Radikal bebas atau substansi oksidatif ini
ditransmisikan dari ibu ke neonatus melalui plasenta dan air susu ibu (ASI).
Ketiga, neonatus itu sendiri yang mengalami infeksi atau sepsis sehingga memicu
pembentukan ROS melalui pelepasan sitokin proinflamasi. Ketiga faktor pencetus
tersebut menimbulkan denaturasi hemoglobin yang lalu membentuk bilirubin
(Ambalavanan & Carlo, 2011; Klowak & Wong, 2008).
Dilaporkan ada 400 juta orang di seluruh dunia menderita defisiensi G6PD.
Prevalensi tertinggi terjadi di Afrika, Asia, Mediterania, dan Timur Tengah
(Frank, 2005). Daerah-daerah tersebut merupakan endemik malaria yang merujuk
pada teori bahwa pembawa gen defisiensi G6PD dimaksudkan untuk memiliki
proteksi awal terhadap infeksi malaria, terutama yang diakibatkan oleh
Plasmodium falciparum, penyebab malaria terbanyak (Frank, 2005; Greene,
1993).
Di Indonesia, prevalensi defisiensi G6PD berkisar antara 2,7%–14,2%
(Kurniawan, 2014). Sebanyak 5,2% dari 1802 neonatus ditemukan dengan
defisiensi G6PD pada penelitian di Rumah Sakit Anak dan Bunda (RSAB)
Harapan Kita tahun 2009–2011 (Elizabeth, 2012).
Defisiensi G6PD merupakan kelainan X-linked recessive, seperti pada penyakit
hemofilia dan buta warna yang diturunkan. Terdapat 300 varian menurut lokasi
alel yang akan mempengaruhi sintesis enzim G6PD (Beutler, 1994).
Sebanyak 0,7–1,6 per 1000 kelahiran dilaporkan meninggal akibat kernikterus
pada neonatus dengan defisiensi G6PD. Oleh karena itu, WHO telah
merekomendasikan untuk melakukan skrining defisiensi G6PD pada populasi di
Skrining defisiensi G6PD di Indonesia belum menjadi program skrining
neonatus. Sampai saat ini, skrining neonatus yang umumnya tersedia di Indonesia
hanya hipotiroid kongenital dengan pemeriksaan kadar thyroid-stimulating
hormone (TSH) yang dimulai sejak tahun 2000 (Rustama, 2015; Elizabeth, 2012).
Salah satu rumah sakit yang melakukan pemeriksaan G6PD pada neonatus di
Indonesia adalah RSAB Harapan Kita di Jakarta Barat, tempat penelitian ini
dilakukan. Pengambilan data diperoleh melalui rekam medis RSAB Harapan Kita
yang mencatat hasil skrining defisiensi G6PD dan pemeriksaan kadar bilirubin
serum pada neonatus berusia dua hari selama tahun 2015. Pemeriksaan G6PD di
rumah sakit tersebut dilakukan dengan uji fluorescent spot yang
direkomendasikan oleh Internal Committee for Standardization in Hematology
(ICSH) (Elizabeth, 2012).
Alasan dilakukannya pemeriksaan G6PD dan bilirubin serum pada neonatus
berusia dua hari adalah untuk memonitor laju progresivitas kadar bilirubin serum
yang memuncak pada hari ketiga sampai hari kelima. Jika didapatkan neonatus
dengan hiperbilirubinemia disertai defisiensi G6PD, kemungkinan besar
progresivitas peningkatan kadar bilirubin berjalan cepat untuk beberapa hari ke
dapan sehingga dapat diberikan penanganan light therapy yang tidak hanya
bermanfaat untuk menangani hiperbilirubinemia pada neonatus, tetapi juga
sebagai pencegahan terhadap kernikterus dengan gejala awal yang muncul pada
saat neonatus berumur dua hari (Ambalavanan & Carlo, 2011).
1.2 Identifikasi Masalah
Apakah defisiensi G6PD menjadi faktor risiko hiperbilirubinemia pada
neonatus berumur dua hari di RSAB Harapan Kita, Jakarta Barat, tahun 2015.
1.3 Maksud dan Tujuan
Sementara tujuan dari penelitian ini untuk memperlihatkan pentingnya
program skrining defisiensi G6PD pada neonatus berumur dua hari di seluruh
tempat penyedia layanan kesehatan.
1.4 Manfaat Karya Tulis Ilmiah
Manfaat Akademisi
Mengetahui peran G6PD terhadap mekanisme terjadinya hiperbilirubinemia
dan faktor-faktor yang dapat memicu timbulnya hiperbilirubinemia akibat
defisiensi G6PD.
Manfaat Praktis
Memberi pengetahuan kepada masyarakat mengenai istilah ‘bayi kuning’ yang
timbul akibat kekurangan enzim G6PD sehingga dapat menghindari hal-hal yang
dapat memperberat keadaan ‘bayi kuning’ tersebut. Langkah ini dimaksudkan
untuk mencegah timbulnya cacat permanen dan kematian pada bayi.
1.5 Landasan Teori dan Hipotesis
1.5.1 Landasan Teori
Mutasi di kromosom Xq28 menyebabkan terganggunya sintesis G6PD di
dalam eritrosit sehingga energi yang mempertahankan kadar NADPH
(nicotinamide adenine dinucleotide phosphate) menurun (Daniele, 2009).
Fungsi dari NADPH adalah menjaga GSH (glutathione terreduksi) tetap berada
dalam bentuk teroksidasi. GSH secara aktif dihasilkan oleh eritrosit sebagai
H2O2 menjadi menjadi molekul yang stabil, yakni H2O dan O2 melalui glutathione
peroxidase. NADPH kemudian mengubah kembali GSSG menjadi GSH agar
dapat melaksanakan perannya sebagai antioksidan (Kumar et al, 2010; WHO
Working Group, 1989).
Pada defisiensi G6PD, NADPH tidak cukup banyak dihasilkan sehingga GSSG
tidak diubah menjadi GSH dan hemoglobin mengalami denaturasi akibat stres
oksidatif (kerusakan yang terjadi akibat proses oksidasi yang ditimbulkan oleh
radikal bebas). Hemoglobin yang paling banyak terpengaruhi adalah hemoglobin
rantai beta (WHO Working Group, 1989). Stres oksidatif kemudian
mempengaruhi membran eritrosit sehingga terjadi hemolisis (Keohane, Smith, &
Walenga, 2016). Satu gram hemoglobin kira-kira dapat membentuk 35 miligram
bilirubin (Riley, 2014).
G6PD diekspresikan di seluruh sel, namun peranannya sangat penting di
eritrosit yang tidak memiliki mitokondria, sehingga G6PD merupakan sumber
utama dari NADPH (WHO Working Group, 1989).
Ada tiga faktor pencetus yang umum menyebabkan hiperbilirubinemia akibat
defisiensi G6PD pada neonatus, yakni ibu hamil (BUMIL) dan menyusui
(BUTEKI) yang mengonsumsi obat-obat tertentu dan kacang fava, serta neonatus
yang mengalami infeksi atau sepsis. Ketiga pencetus tersebut memicu stres
oksidatif pada eritrosit (Ambalavanan & Carlo, 2011).
Beberapa obat antimalaria, kemoterapi, antibiotik, antipiretik, analgesik, dan
antidiabetes melepaskan reactive oxygen species (ROS)—suatu radikal bebas—
saat dimetabolisme di hepar. Kacang fava (Vicia faba) mengandung divicine
sebagai suatu oksidan yang potensial menimbulkan stres oksidatif. Hemolisis
yang terjadi akibat mengonsumsi kacang fava dinamakan favism (Klowak &
Wong, 2008).
Substansi-substansi pencetus stres oksidatif itu dikonsumsi oleh ibu hamil
menjelang waktu persalinan dan melalui darah maternal ditransmisikan ke janin
melalui plasenta. Substansi tersebut dapat pula ditransmisikan melalui ASI pada
ROS juga dapat diperoleh bila neonatus mengalami infeksi—misalnya akibat
Parvovirus, Salmonella, dan virus hepatitis—seiring dengan pelepasan sitokin
proinflamasi oleh sistem imun (Klowak & Wong, 2008).
Tanpa faktor pencetus, hiperbilirubinemia dapat terjadi pada neonatus dengan
defisiensi G6PD akibat begitu rendahnya aktivitas enzim tersebut di dalam
eritrosit (<10%) (Frank, 2005).
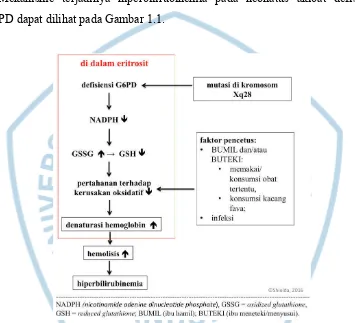
Mekanisme terjadinya hiperbilirubinemia pada neonatus akibat defisiensi
G6PD dapat dilihat pada Gambar 1.1.
Gambar 1.1 Mekanisme Terjadinya Hiperbilirubinemia pada Neonatus
dengan Defisiensi G6PD
1.5.2 Hipotesis Penelitian
Defisiensi G6PD sebagai faktor risiko terhadap hiperbilirubinemia pada
BAB V
SIMPULAN DAN SARAN
5.1 Simpulan
Berdasarkan penelitian yang telah dilakukan, maka dapat disimpulkan bahwa
defisiensi G6PD menjadi faktor risiko hiperbilirubinemia pada neonatus berumur
dua hari di RSAB Harapan Kita, Jakarta Barat, tahun 2015.
5.2 Saran
Dilakukan penelitian lebih lanjut mengenai bagaimana cara mendeteksi
neonatus dengan defisiensi G6PD pada awal kehamilan sehingga dapat dilakukan
DEFISIENSI G6PD SEBAGAI FAKTOR RISIKO
TERHADAP HIPERBILIRUBINEMIA PADA
NEONATUS BERUMUR DUA HARI
DI RSAB HARAPAN KITA, JAKARTA BARAT,
TAHUN 2015
KARYA TULIS ILMIAH
Karya Tulis Ini Dibuat sebagai Salah Satu Syarat untuk Memperoleh Gelar Sarjana Kedokteran
SHIELDA NATASHA SHIDARTA
1310144
FAKULTAS KEDOKTERAN
UNIVERSITAS KRISTEN MARANATHA
BANDUNG
KATA PENGANTAR
Puji dan syukur kepada Tuhan Yang Maha Esa karena atas rahmat dan
karunia-Nya, penulis dapat menyelesaikan Karya Tulis Ilmiah ini sebagai salah satu syarat
untuk memperoleh gelar Sarjana Kedokteran (S.Ked) di Fakultas Kedokteran
Universitas Kristen Maranatha.
Karya tulis ini dapat dirampungkan oleh penulis dengan baik, tentu tak lepas
dari dukungan dan bantuan berbagai pihak. Oleh karena itu, penulis ingin
menyampaikan terima kasih kepada:
1. Lisawati Sadeli, dr., M.Kes sebagai pembimbing utama Karya Tulis
Ilmiah yang telah memberikan waktu, arahan, nasihat, dan bimbingan
kepada penulis dalam penyusunan Karya Tulis Ilmiah ini.
2. Cindra Paskaria, dr., M.K.M sebagai pembimbing pendamping Karya
Tulis Ilmiah yang telah memberikan waktu, arahan, dan bimbingan,
terutama dalam bidang stastistika kepada penulis.
3. Setyadewi Lusyati, dr., Sp.A(K), Ph.D dari RSAB Harapan Kita yang
telah memberikan waktu, arahan, dan nasihat kepada penulis saat
pengambilan data di RSAB Harapan Kita, Jakarta Barat.
4. Para staf di bagian rekam medis di RSAB Harapan Kita yang telah
membantu peneliti dalam menyediakan tenaga dan waktu untuk
mengumpulkan sumber data penelitian.
5. Dr. Meilinah Hidayat, dr., M.Kes atas dukungannya kepada penulis.
6. Kedua orang tua penulis—Imelda Martinelli dan Shidarta—atas cinta, doa,
dukungan, dan harapan mereka yang begitu besar. Karya Tulis Ilmiah ini
juga penulis persembahkan sebagai hadiah untuk ayah penulis yang
berulang tahun tanggal 16 Oktober, “Selamat hari ulang tahun, Pi.”
7. Sahabat-sahabat penulis—Helen Sustantine, Almira Talitha, Diella,
Veronica Shinta, Cristika, Nahania Gracia, dan Maria Alfiani—yang
selalu mendukung, memberikan semangat dan doa.
penulis terima dengan senang hati. Penulis berharap Karya Tulis Ilmiah ini dapat
memberi manfaat bagi perkembangan ilmu kedokteran di kemudian hari.
Bandung, November 2016
DAFTAR PUSTAKA
AAP. 2004. Management of hyperbilirubinemia in the newborn infant 35 or more weeks of gestation. Pediatrics, 114: 297–316.
Ali et al. 2012. Icterus neonatorum in near-term and term infants. Sultan Qaboos Univ Med J, 12[2]: 153-60.
Ambalavanan N, Carlo WA. 2011. Jaundice and hyperbilirubinemia in the newborn: Kliegman RM, Stanton BF, St. Geme JW, Schor NF. (Eds.). Nelson Textbook of Pediatrics. 19th ed. Philadelphia: Saunders Elsevier. p 603–8.
__________. 2011. Kernicterus: Kliegman RM, Stanton BF, St. Geme JW, Schor NF. (Eds.). Nelson Textbook of Pediatrics. 19th ed. Philadelphia: Saunders Elsevier. p 608–12.
Arias IM. 2012. Liver function from Y to Z. J Clin Invest, 122[8]: 2763-4.
Bashore RA, Smith F, Schenker S. 1969. Placental transfer and disposition of bilirubin in the pregnant monkey. Am J Obstet Gynecol, 103: 950.
Bain BJ, Swirsky D. 2012. Erythrocyte and leucocyte cytochemistry. Practical Haematology. London: Churchill Livingstone. p 333-52.
Beutler. 1994. G6PD deficiency. Blood, 84[11]: 3613-36.
Bhutani VK, Johnson L, Sivieri EM. 1999. Predictive ability of a predischarge hour-specific serum bilirubin for subsequent significant hyperbilirubinemia in healthy term and near-term newborns. Pediatrics, 103:6-14.
Boamah LM, Balistreri WF. 2011. Manifestations of liver disease: Kliegman RM, Stanton BF, St. Geme JW, Schor NF. (Eds.). Nelson Textbook of Pediatrics. 19th ed. Philadelphia: Saunders Elsevier. p 1374-8.
Chatterjea MN, Shinde R. 2012. Textbook of medical biochemistry. 8th ed. New Delhi: Jaypee Brothers Medical Publishers (P) Ltd. p 660-1.
Daniele G. 2009. Glucose-6-phosphate dehydrogenase. http://flipper.diff.org/app/ pathways/2101. Accessed October 1, 2016.
Dennery PA, Seidman DS, Stevenson DK. 2001. Neonatal hyperbilirubinemia. N Engl J Med, 344: 581-90.
Duh SH, Cook JD. 2005. Laboratory reference range values. APP17, 17.
Estridge BH, Reynolds AP. 2012. Basic clinical laboratory techniques. 6th ed. New York: Delmar. p 609.
Frank JE. 2005. Diagnosis and management of G6PD deficiency. Am Fam Phys, 72[7]: 1277-82.
Godlewski et al. 1997. Liver development in the rat and in man during the embryonic period (Carnegie stages 11-23). Microsc Res Tech, 39[4]:314-27.
Greene LS. 1993. G6PD deficiency as protection against falciparum malaria: an epidemiologic critique of population and experimental studies. Am J Phys Anthropol, 36: 153-78.
Guillemette C. 2003. Pharmacogenomics of human UDP-glucuronosyltransferase enzymes. Pharmacogenomics J, 3: 136-58.
Hall JE. 2011. Guyton and hall textbook of medical physiology. 12th ed. Philadelphia: Saunders Elsevier. p 418-20; 840-2.
Harvey R, Ferrier D. 2011. Biochemistry. 5th ed. Philadelphia: Lippincott, Williams & Wilkins. p 282-9.
Keohane EM, Smith LJ, Walenga JM. 2016. Intrinsic defects leading to increased
erythrocyte destruction. Rodak’s Hematology: Clinical Principles and
Applications. 5th ed. Philadelphia: Saunders Elsevier. p 383-8.
Klowak J, Wong E. 2008. Glucose-6-phosphate dehydrogenase. Lancet, 371[9606]:
64-74.
Kramer LI. 1969. Advancement of dermal icterus in the jaundiced newborn. Am J Dis Child. 118[3]: 454-8.
Kremer M. 1940. The classification of jaundice. Postgrad Med J, 16[171]: 11-7.
Kumar et al. 2010. Robbins and Cotran Pathologic Basis of Disease. 8th ed. Philadelphia: Saunders Elsevier. p 20-2.
Kurniawan LB. 2014. Skrining, diagnosis, dan aspek klinis defisiensi glukosa-6-fosfat dehidrogenase (G6PD). CDK, 222[41]: 807-11.
Lang F, Lang E, Föller M. 2012. Physiology and pathophysiology of eryptosis. Tranfus Med Hemother, 39[5]: 308-14.
MIMS. 2006. Drugs to avoid in G6PD deficiency. http://www.cych.org.tw/pharm/ MIMS%20Summary%20Table-G6PD.pdf. Accessed October 1, 2016.
Muthayya NM. 2002. Human Physiology. 3rd ed. New Delhi: Jaypee Brothers Medical Publishers (P) Ltd. p 145.
Newman TB. 2009. Universal bilirubin screening, guidelines, and evidence. Pediatrics, 124[4]: 1199-21.
NIH. 2011. What is Rh incompatibility. https://www.nhlbi.nih.gov/health/health-topics/topics/rh. Accessed October 2, 2016.
NIH. 2016. UGT1A1 gene. https://ghr.nlm.nih.gov/gene/UGT1A1. Accessed October 1, 2016.
Palmer J. 2011. ABO incompability in newborns. http://www.pregnancy.com.au/ resources/topics-of-interest/postnatal/abo-incompatibility-in-newborns.shtml. Accessed November 12, 2016.
Peters AL, Van Noorden CJF. 2009. Glucose-6-phosphate dehydrogenase deficiency and malaria: cytochemical detection of heterozygous G6PD deficiency in women. J Histochem Cytochem, 57[11]: 1003-11.
Porter ML, Dennis BL. 2002. Hyperbilirubinemia in the term newborn. Am Fam Phys, 65[4]: 599-607.
Riley MR. 2014. Bilirubin metabolism. http://www.merckmanuals.com/
professional/pediatrics/perinatal-physiology/perinatal-physiology. Accessed
September 29, 2016.
Roche SP, Kobos R. 2004. Jaundice in the adult patient. Am Fam Phys, 69[2]: 299-304.
Roper D, Layton M. 2012. Investigation of the hereditary haemolytic anaemias: membrane and enzyme abnormalities. Practical Haematology. London: Churchill Livingstone. p 254-72.
Rustama D. 2015. Pentingnya skrining hipotiroid pada bayi. http://www.idai.or.id /artikel/seputar-kesehatan-anak/pentingnya-skrining-hipotiroid-pada-bayi. Accessed November 13, 2016.
Städeler G. 1864. Uber die farbstoffe der galle. Justus Liebigs Ann Chem, 132: 323-54.
Webster J, Blyth R, Nugent F. 2006. An appraisal of the use of the kramer’s scale in predicting hyperbilirubinaemia in healthy full term infants. Birth Issues, 14[3]: 83-9.
WHO Working Group. 1989. Glucose-6-phosphate dehydrogenase deficiency. Bull World Health Organ, 67[6]: 601-11.
WHO. 2006. Infant, newborn. http://www.who.int/topics/infant_newborn/en/. Accessed October 2, 2016.
Wong et al. 2009. Comparison of detection of glucose-6-phosphate dehydrogenase deficiency using fluorescent spot test, enzyme assay, and molecular method for prediction of severe neonatal hyperbilirubinaemia. Singapore Med J, 50[1]: 62-7.
Wysowski et al. 1978. Epidemic neonatal hyperbilirubinemia and use of phenolic disinfectant detergent. Pediatrics, 61[2]: 165-70.