1
Kode/ Nama Rumpun Ilmu :112/ Kimia
LAPORAN AKHIR TAHUN
PENELITIAN BERBASIS KOMPETENSI
Pengembangan Biomaterial Kolagen Hidroksiapatit Kitosan Untuk Restorasi Jaringan Tulang (Bone Graft)
TIM PENGUSUL
Prof.Dr. SARI EDI CAHYANINGRUM, M.Si (NIDN:0029127002) Dr. NUNIEK HERDYASTUTI, M.Si (NIDN:0010117004)
Tahun ke-1 dari rencana 2 tahun
UNIVERSITAS NEGERI SURABAYA OKTOBER, 2017
4 RINGKASAN
Indonesia adalah negara dengan jumlah pemakai biomaterial tertinggi, khususnya untuk pemakaian bone graft sebagai pensubstitusi penderita patah tulang dan implan gigi. Bone
graft berfungsi membantu merangsang pertumbuhan tulang pada fraktur, yaitu terputusnya
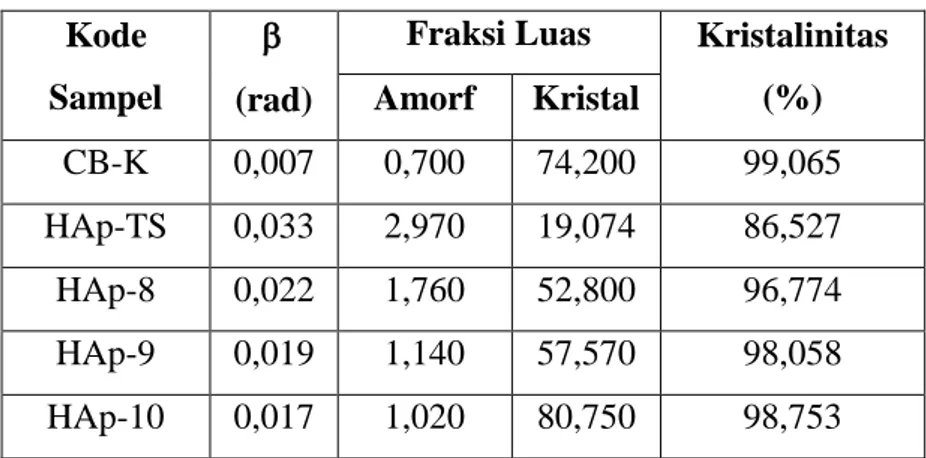
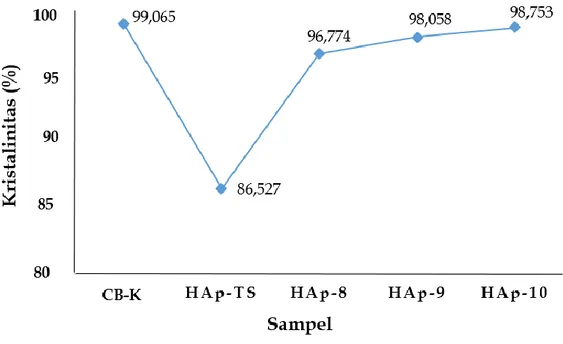
jaringan tulang dan juga biasa digunakan untuk implan gigi. Bone graft penggunaannya sangat luas, tetapi ketersediaannya belum mencukupi karena jumlah kebutuhan bone graft meningkat setiap tahunnya. Selama ini Indonesia mencukupi kebutuhan bone grfat dengan cara impor, sehingga memerlukan biaya yang mahal. Karena itulah inovasi teknologi untuk mengembangkan biomaterial ini sangat diperlukan. Beberapa peneliti mulai mengembangkan penelitian tentang sintesis bone graft, tetapi yang dilakukan adalah sintesis dengan memadukan 2 bahan baku. Perpaduan 2 bahan baku mempunyai beberapa kelemahan. Tulang manusia terdiri dari komponen anorganik dan organik. Komponen anorganik didominasi hidroksiapatit sedangkan komponen organik didominasi kolagen dan glukosamin. Berdasarkan hal tersebut pada penelitian ini bone graft disintesis dari 3 bahan baku yaitu kolagen, hidroksiapatit dan kitosan.. dengan harapan bone graft yang dihasilkan mempunyai struktur dan komposisi yang mirip tulang manusia. Tujuan jangka panjang penelitian ini adalah menghasilkan inovasi teknologi yang unggul yang memberi konstribusi mendasar bagi pengembangan sintesis biometrial untuk bidang kesehatan dengan memanfaatkan bahan dasar lokal untuk menghasilkan bone graft yang mempunyai secara struktur, dan komposisi mirip tulang alami, dapat diterima tubuh (biokompatibel), tidak beracun, menguntungkan bagi proses osteokonduktif, osteoinduksi dan osteogenesis. Selain itu juga dihasilkannya publikasi pada jurnal internasional, buku ajar dan paten. CB-K memiliki fasa CaO 94,8 %b/b dan Ca(OH)2 5,2 %b/b dengan derajat
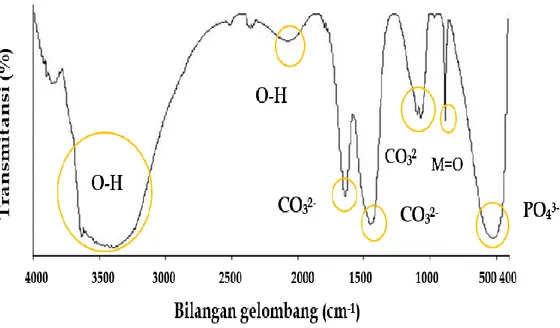
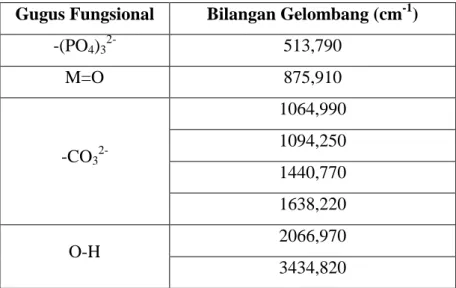
kristalinitas 99,065 %. Gugus Fungsional CB-K yaitu OH-, (PO4)32-, dan CO32-. Morfologi
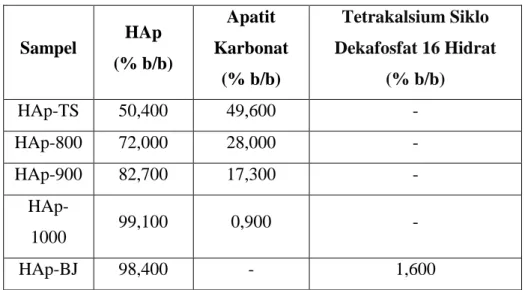
permukaan CB-K merupakan bentuk lonjong yang tidak seragam dan mengalami aglomerasi.Suhu sintering berpengaruh pada sintesis HAp untuk meningkatkan kemurnian dan kristalinitas HAp. HAp terbaik yaitu pada HAp-9 dengan fasa HAp 82,7%b/b, kristalinitas 98,058%, dan morfologi permukaan berpori tanpa aglomerasi.HAp-TS memiliki fasa HAp 50,400 %b/b dan apatit karbonat 49,600%b/b dengan kristalinitas 99,065%. HAp-8 merupakan fasa HAp 72,000 %b/b dan apatit karbonat 28,000 %b/b dengan kristalinitas 96,774%. HAp-9 merupakan fasa HAp 82,700 %b/b dan apatit karbonat 17,300%b/b dengan kristalinitas 98,058%. HAp-10 memiliki fasa HAp 99,100 %b/b dan apatit karbonat 0,900 %b/b dengan kristalinitas 98,753%. HAp memiliki bentuk bongkahan tidak beraturan dan teraglomerasi pada suhu 1000 oC. Gugus fungsional seluruh HAp adalah –OH, -(PO4)32-, dan -CO32-.Komposisi komposit mempengaruhi nilai derajat
kristalinitas dan uji tekan komposit, komposit HA/Coll/Chi 7:2:1 dengan kandungan kolagen tertinggi memiliki derajat kristalinitas paling rendah yaitu 73,41%. Karakterisasi uji tekan menunjukkan komposit HA/Coll/Chi 7:2:1 menghasilkan nilai uji tekan terendah yaitu 137,29 Kpa.Karakterisasi kimia melalui FTIR pada ketiga sampel komposit HA/Coll/Chi memiliki gugus fungsional OH-, (PO4)32-, dan CO32- yang mengindikasikan
adanya HA serta adanya pergeseran gugus C=O dan NH2 yang berasal dari kolagen dan
kitosan yang menunjukkan telah terjadi ikatan antara HA-kolagen dan kitosan. Karakterisasi XRD menujukkan munculnya fasa HA, kitosan dan kolagen pada ketiga sampel komposit. Pada tahun pertama luaran yang telah dicapai adalah artikel pada jurnal internasional bereputasi (Q3) sudah pada tahap under review, artikel pada seminar internasional ( pelaksanaan 4 Nopember 2017) dan artikel pada seminar nasional (sudah dilaksanakan), draft paten dan draft buku ajar. Pada tahun kedua penelitian yang akan dilaksanakan adalah melanjutkan karakterisasi bone graft yaitu uji kuat tekan, tarik mulur,
5
analisis permukaan, uji korosi, uji degradasi, uji in vitro dan sitotoksisitas. Filasisasi paten , buku ajar dan penulisasn artikel pada jurnal internasional
6 DAFTAR ISI HALAMAN SAMPUL 1 HALAMAN PENGESAHAN 2 RINGKASAN 3 PRAKATA 4 DAFTAR ISI 5 DAFTAR TABEL 6 DAFTAR GAMBAR 7 DAFTAR LAMPIRAN 8 BAB I PENDAHULUAN 9
BAB II TINJAUAN PUSTAKA 16
BAB III TUJUAN DAN MANFAAT 32
BAB IV METODE PENELITIAN 33
BAB V HASIL DAN LUARAN YANG DICAPAI 38
BAB VI RENCANA TAHAPAN BERIKUTNYA 74
BAB VII KESIMPULAN DAN SARAN 75
DAFTAR PUSTAKA 76
LAMPIRAN
Lampiran 1: artikel jurnal internasional dan progressnya 78 Lampiran 2: artikel seminar nasional dan sertifikat 86
Lampiran 2: artikel seminar internasional 93
Lampiran 4: draf paten 97
7
BAB I PENDAHULUAN
Saat ini penelitian pengembangan biomaterial yang berguna untuk membantu menjalankan fungsi tubuh manusia sedang banyak dilakukan terutama biomaterial yang digunakan untuk restorasi jaringan atau organ tubuh yang rusak akibat kecelakaan, penyakit bawaan atau penyakit non bawaan. Berdasarkan data di Asia, Indonesia adalah negara dengan jumlah pemakai biomaterial tertinggi, khususnya untuk pemakaian bone
graft sebagai pensubstitusi pada proses restorasi patah tulang dan implan gigi. Di RS Dr.
Soetomo Surabaya, sekitar 400 kasus operasi bedah tulang per bulan (Gunawarman, 2010). Bagian tubuh yang sering mengalami patah tulang adalah bagian panggul, dan pergelangan kaki. Bone graft berfungsi membantu merangsang pertumbuhan tulang pada fraktur, yaitu terputusnya jaringan tulang. Bone graft penggunaannya sangat luas, tetapi ketersediaannya belum mencukupi karena jumlah kebutuhan bone graft meningkat setiap tahunnya selama ini untuk mencukupi kebutuhan bone graft maka dilakukan dengan cara impor. Hal ini menyebabkan harga bone graft mahal, sehingga pengadaan bone graft sintesis berbahan dasar local Indonesia sangat diperlukan.
Bone graft dibedakan menjadi autograft, allograft, dan xenograft, sebagai pensubstitusi tulang setiap material tersebut memiliki kekurangan dan kelebihan. Autograft diambil dari bagian tubuh pasien, kelebihannya pasti cocok dan tidak ada penolakan dari tubuh pasien. Kelemahan autograft adalah sering menyebabkan komplikasi dalam penyembuhan luka, operasi tambahan, nyeri pada donor dan pasokan tulang tidak memadai untuk mengisi gap. Allograft menggunakan tulang mayat kekurangannay terkait dengan reaksi infeksi, inflamasi, dan penolakan kadang-kadang terjadi masalah dalam reaksi imunogenik dan resiko penyakit menular (AIDS dan hepatitis). Xenograft juga membawa resiko penyakit menular antar spesies (Wahl & Czernuszka, 2006) karena berasal dari tulang hewan. Keterbatasan tersebut memicu perkembangan riset di bidang biomaterial, yaitu dengan melakukan berbagai modifikasi pembuatan biomaterial sintetis. Inovasi teknologi biomaterial sintetis diharapkan menghasilkan biomaterial dimana karakter bahan diketahui secara pasti dan terkontrol.
Beberapa peneliti telah melakukan sitesis bone graft menggunakan 2 bahan baku misalnya Istifarah (2013) menggunakan tulang sotong-kitosan; Nedelcu (2013) mengkompositkan Kolagen –hidroksiapatit dn Hindawi (2014) menggunakan kitosan hidrosiapatit. Perpaduan 2 bahan baku untuk sintesis bone graft memiliki kekurangan karena produk yang dihasilkan kurang sesuai dengan struktur dan komposisi tulang alami.
8
Bone graft sintesis harus sesuai dengan syarat kesehatan yaitu bone graft yang secara struktur, dan komposisi mirip tulang alami, dapat diterima tubuh (biokompatibel), tidak beracun, menguntungkan bagi proses osteokonduktif, osteoinduksi dan osteogenesis. Osteokonduktif dan osteoinduktif merupakan syarat terpenting dari suatu biomaterial karena berhubungan dengan kemampuan mengarahkan dan mendorong formasi pertumbuhan jaringan (Wahl & Czernuska, 2006). Osteoinduktif dan osteogenesis berhubungan dengan porositasnya (Develioglu, 2005). Salah satu bahan yang sedang dikembangkan saat ini adalah hidroksiapatit. Hidroksiapatit termasuk senyawa kalsium fosfat yang memiliki sifat bioaktif dengan bioafinitas tinggi, osteokonduktif, biokompatible dan tidak beracun. Tetapi hidroksiapatit kekuatan dan kelenturannya rendah dan sangat rapuh. Oleh karena itu perlu ditambahkan material lain untuk memperbaiki kekurangan tersebut. Material yang ditambahkan harus mempunyai elastisitas yang tinggi, non toksik dan biodegradabel. Beberapa material yang sering digunakan adalah alginat, selulosa, akrilat dll. Pada penelitian ini digunakan kolagen. Kolagen dapat disintesis dari tulang cakar ayam, tulang ikan, tulang sapi dll. Pada penelitian ini digunakan tulang sapi, karena kolagen tulang sapi, merupakan kolagen tipe I, sama dengan kolagen di tulang manusia. Perpaduan kolagen dengan hidroksiapatit diharapkan menghasilkan bone graft sintesis yang mempunyai kemiripan yang sangat besar dengan tulang. Tulang manusia mempunyai komponen utama kolagen dan hidroksiapatit serta beberapa komponen yang lain (Vaccaro, 2002).
Bone graft yang potensial untuk dikembangkan selain dari kemiripan dengan tulang alami adalah bone graft berpori. Pori yang terbentuk berfungsi sebagai media pembentukan jaringan sel tulang yang tumbuh. Jaringan sel tulang baru akan tumbuh dalam pori-pori yang terbentuk sehingga dapat meningkatkan regenerasi tulang (Attaf, 2011). Pembentukan pori dapat dilakukan dengan penambahan porogen. Berbagai bahan porogen sering digunakan seperti parafin, polinaftalen, gelatin, alginat dan kitosan. Pada penelitian ini digunakan kitosan sebagai porogen. Kitosan merupakan bahan alami yang tersedia melimpah dan mudah proses isolasinya, sifatnya biodegradabel, biokompatibel dan non toksik. Inovasi teknologi penggabungan material kolagen hidroksiapatit dan kitosan sangat perlu untuk dilakukan sehingga dapat menghasilkan bone graft yang berkualitas sesuai standar kesehatan. Bone graft yang dihasilkan dapat diaplikasikan untuk memenuhi kebutuhan yang terus meningkat sehingga dapat mendukung Indonesia mandiri dibidang kesehatan.
9
Penelitian ini direncanakan untuk pelaksanaan selama 2 tahun, tujuan utamanya adalah memanfaatkan potensi bahan dasar lokal (tersedia melimpah di Indonesia) untuk menghasilkan bone graft sintesis yang berkualitas dan memenuhi syarat kesehatan yaitu bone graft yang secara struktur, dan komposisi mirip tulang alami, dapat diterima tubuh (biokompatibel), tidak beracun, menguntungkan bagi proses osteokonduktif, osteoinduksi dan osteogenesis.
Untuk mencapai tujuan tersebut maka tahapan penelitiannnya adalah pada tahun I difokuskan pada sintesis bahan baku tulang sapi, hidrosiapatit dari cangkang telur bebek dan kitosan dari cangkang udang. Masing masing bahan baku dikarakterisasi sifat fisika dan kimianya. Kemudian sintesis bone graft dilakukan dengan metode ex situ. Bone graft yang dihasilkan dikarakterisasi sifat fisikanya. Pada tahun ke-2 difokuskan pada karakterisasi bone graft secara kimia, dan aplikasi bone graft sebagai pensubstitusi dilakukan secara in vitro, uji degradasi, laju korosi dan uji sitotoksisitas.
Urgensi (keutamaan ) Penelitian
Dewasa ini, teknologi dibidang biomaterial sedang mendapat mendapat perhatian besar, karena kebutuhan yang terus meningkat. Biomaterial yang banyak dikembangkan adalah bone graft, katup buatan pada jantung, sensel sendi dan sebagainya. Selama ini bone graft diimport dengan harga yang cukup mahal, padahal kebutuhan terus meningkat. Upaya untuk mengurangi bone graft import adalah dengan membuat bone graft sintesis berbahan dasar produk local. Klasifikasi bone graft meliputi autograft, allograft, dan xenograft mempunyai beberapa keterbatasan secara medis. Keterbatasan tersebut memicu perkembangan riset di bidang biomaterial, yaitu dengan melakukan berbagai modifikasi pembuatan biomaterial sintetis. Cangkang udang, cangkang telur itik, tulang sapi yang berpotensi sebagai sumber kitosan, hidroksiapatit dan kolagen tersedia melimpah dan murah di Indonesia. Inovasi teknologi biomaterial bone graft sintetis dengan bahan dasar lokal diharapkan meningkatkan nilai ekonomis limbah dan menghasilkan biomaterial dimana karakter bahan diketahui secara pasti dan terkontrol sehingga akan mendukung kemandirian Indonesia di bidang kesehatan.
Luaran yang ditargetkan serta kontribusi pada ilmu pengetahuan
Pengembangan inovasi teknologi biomaterial berbais kolagen hidroksiapatit kitosan untuk restorasi jaringan tulang merupakan teknologi terkini dibidang kesehatan. Selama ini kebutuhan bone graft sebagai bahan pengganti jaringan tulang yang rusak meningkat setiap tahun dicukupi dengan impor, tentu saja biayanya sangat mahal. Padahal di Indonesia
10
bahan untuk sintesis bone graft sangat melimpah. Sintesis bone graft dengan bahan baku lokal akan akan membantu memenuhi kebutuhan bone graft sehingga kedepan Indonesia akan mandiri dibidang ini.Hal ini merupakan upaya peneliti untuk ambil bagian dalam penguatan Sistem Inovasi Nasional (SINas) agar Indonesia tidak tertinggal dari bangsa-bangsa lain di dunia. Inovasi yang diunggulkan peneliti adalah dengan memanfaatkan potensi alam Indonesia yaitu kitosan yang berasal dari cangkang udang yang tersedia melimpah, Hidroksiapatit dapat diisolasi dengan mudah dengan memanfaatkan bahan baku yang juga melimpah misalnya dari cangkang telur, tulang sapi, ceker ayam. Limbah tersebut dapat ditingkatkan nilai ekonomisnya sedemikian rupa sehingga sifat unggul dari material dapat terekspresikan dalam produk yang bermutu. Kolagen juga dapat diisolasi dari bahan-bahan seperti tulang sapi, kambing dll. Perpaduan ketiga bahan tersebut akan menghasilkan biomaterial yang biokompatibel, non toksik mempunyai struktur dan komposisi yang mirip dengan tulang alami asalkan disintesis pada kondisi yang sesuai. Inovasi teknologi biomaterial bone graft sintetis dengan bahan dasar lokal diharapkan meningkatkan nilai ekonomis limbah dan menghasilkan biomaterial dimana karakter bahan diketahui secara pasti dan terkontrol sehingga akan mendukung kemandirian Indonesia di bidang kesehatan. Inovasi sintesis bone graft dengan bahan lokal pada penelitian ini dilakukan dengan memadukan dua metode pengendapan basah untuk sintesis hidroksiapatit dan metode ex situ pada sintesis bone graft, inovasi ini akan menghasilkan bone graft yang mempunyai kemurnian yang tinggi, struktur dan komposisi bone graft yang dihasilkan mirip dengan tulang alami. Luaran dari kegiatan penelitian ini selain di peroleh bone graft yang sudah terkarakterisasi, juga dihasilkan publikasi pada jurnal internasional, paten dan buku ajar yang membahas tentang biomaterial.
Rencana target capaian luaran
No. Jenis Luaran Indikator Capaian
TS 1) TS 2)
1. Publikasi Ilmiah 2) Internasional accepted accepted Nasional
Terakreditasi 2. Pemakalah dalam temu
ilmiah 3)
Internasional terdaftar Sudah dilaksanakan Nasional Sudah
dilaksanakan
Sudah dilaksanakan 3. Invited speaker dalam
temu ilmiah 4)
Internasional Tidak ada Tidak ada Nasional Tidak ada Draf
11
4. Visiting Lecturer 5) internasional Tidak ada Tidak ada
5. Hak Kekayaan
Intelektual (HKI) 6)
Paten terdaftar Terdaftar Paten
sederhana
Tidak ada Tidak ada Hak cipta Tidak ada Tidak ada Merek dagang Tidak ada Tidak ada Rahasia
dagang
Tidak ada Tidak ada Desain produk
industri
Tidak ada Tidak ada Indikasi
geografis
Tidak ada Tidak ada Perlindungan
varietas tanaman
Tidak ada Tidak ada
Perlindungan topografi sirkuit terpadu
Tidak ada Tidak ada
6 Teknologi tepat guna 7) Produk Produk
7. Model/purwarupa/desain/karya seni/rekayasa social 8)
Tidak ada Tidak ada
8. Buku Ajar (ISBN) 9) Draf Sudah terbit
9. Tingkat Kesiapan teknologi 10) 2 2
Penelitian ini merupakan rangkaian penelitian yang dilakukan peneliti dalam rangka mengeksplorasi potensi kitosan sebagai sumber biomaterial masa depen. Pengembangan dari penelitian yang sudah dilakukan oleh peneliti tentang potensi kitosan dalam berbagai bidang. Penelitian Hibah bersaing (2006-2007) imobilisasi papain pada kitosan dan aplikasinya sebagai penghilang aroma langu pada susu kedelai; Penelitian Disertasi (2009) tentang pembuatan kitosan bead (speris) untuk imobilisasi papain, Hibah Stranas (2010) serta penelitian hibah Kompetensi Dikti (2011) telah menghasilkan kitosan nanopartikel yang dimanfaatkan untuk matriks imobilisasi glukosa isomerase dan kitosan nanofiber untuk imobilisasi papain. Hibah bersaing (2013-2015) yang menghasilkan kitosan alginat untuk matriks enkapsulasi obat TBC. Hasil penelitian tersebut menunjukkan bahwa kitosan tersedia melimpah, proses isolasinya mudah, bersifat non toksis, biokompatible sehingga membuka peluang untuk mengkaji potensi kitosan sebagai bahan dasar pembuatan bone graft sintesis. Selain itu, hasil penelitian juga telah dipublikasikan pada jurnal nasional maupun internasional dan menghasilkan beberapa paten.
Pada penelitian ini kitosan dikompositkan dengan material lain pada sintesis bone
12
kemampuannya sebagai pembentuk pori (porogen) (Cahyaningrum, 2014) membuka peluang bahwa bone graft yang disintesis dari perpaduan kolagen –hidroksiapatit- kitosa mpunyai karakteristik yang sama dengan jaringan tulang alami. Tulang alami merupakan komposit alami yang terdiri dari bahan organik dan inorganik, yaitu 30% bahan organik, 55% bahan inorganik dan 15% air ( Sari et al, 2008). Substansi inorganik tulang dikenal sebagai fase mineral tulang dengan komponen utamanya adalah kristal hidroksiapatit (HAP) (Schnettler et al, 2005). Bentuk bone graft dapat berupa bubuh, pipih, batangan dan kubus.
Penelitian Peter et. al,(2010) menggunakan keramik nanopartikel dengan kitosan untuk menghasilkan pensubstitusi jaringan, kombinasi ini memiliki kelemahan yaitu kurang lentur. Kombinasi kitosan/ HA yang dihasilkan Zhang et.al 2008 menghasilkan biomaterial yang mempunyai nilai modulus young yang kecil. Ragenty et. al, 2010 mengkombinasikan kolagen dan kitosan untuk menghasilkan biomaterial pensubstitusi jaringan tulang, menghasilkan biomaterial yang bagus struktur dan komposisinya mirip tulang tetapi kurang kuat. Kirubanandan, 2010 menunjukkan bahwa bone graft sintesis harus berpori untuk meningkatkan pembentukan tulang baru dan pembentukan kapiler. Strukur tulang alami mempunyai ukuran pori minimum sekitar 300μm, makroporositas yang terlalu tinggi dapat mengakibatkan hilangnya sifat mekanik biomaterial. Berdasarkan hal tersebut maka penelitian ini menggunakan kombinasi 3 macam bahan yaitu kolagen hidroksiapatit kitosan, kombinasi ini diharapkan akan menghasilkan biomaterial yang kuat tetapi tidak rapuh, lentur sesuai jaringan tulang dan berpori sehingga pembentukan tulang baru dan kapiler dan restorasi jaringan tulang dapat berlangsung dengan baik.
Pada penelitian ini hidoksiapatit disintesis dengan metode pengendapan basah, metode ini mempunyai keuntungan karena produk sampingnya hanya air, yang mudah dihilangkan dengan pemanasan. Metode sintesis bone graft ada yang in situ dan ada yang ex situ. Metode in situ berpeluang menghasilkan terbentuknya senyawa lain karena penambahan polimer dilakukan pada saat pembentukan bahan utama. Oleh karena itu pada penelitian ini dipilih sintesis bone graft dengan menggunakan metode iex-situ. Beberapa peneliti telah menggunakan metode ex-situ tetapi bahan bakunya hanya 2, misalnya Xiaoling (2007) menggunakan Hidroksiapatit- kitosan; Trisnawati (2013) menggabungkan hidroksiapatit-alginat. Peneliti yang menggunakan 3 bahan baku Pallela (2011) mensintesis bone graft dari hidroksiapatit –kitosan-kolagen spons Inovasi pada penelitian ini digunakan 3 bahan baku yaitu kolagen dari tulang sapi, hidroksiapatit dari cangkang telur bebek dan kitosan dari cangkang udang. Kolagen dapat diisolasi dari berbagai
13
sumber dan setiap sumber mempunyai tipe kolagen yang berbeda, hal ini akan mempengaruhi bone graft yang dihasilkan. Komposisi CaO dan CaOH pada setiap cangkang berbeda, sehingga mempengaruhi kualitas hidroksiapatit yang dihasilkan (Suryadi, 2011). Inovasi sintesis bone graft dengan menggunakan 3 bahan baku lokal Indonesia dengan menggabungkan metode pengendapan basah dan metode ex situ diharapkan akan menghasilkan bone graft yang memiliki kualitas sesuai standar dan memberikan kontribusi pada perkembangan sintesis material maju mendukung kemandirian Indonesia dibidang biomaterial dan kesehatan.
Roadmap dari penelitian pengkajian potensi kitosan adalah sebagai berikut Adapun Roadmap (peta jalan) penelitian ini adalah :
Tahun 2001-2005 2005-2008
2009-11 2013-2015 2016-2020
Bahan
Dasar Kitosan dari limbah cangkang udang Kitosan dari limbah udang Kitosan dari limbah udang , ion logam Kitosan-alginat Kitosan – HA, kolagen alginate Proses Isolasi kitin dan deasetil asi kitin Preparasi kitosan terimpreg nasi Preparasi kitosan cair Prepara si nano beads Preparasi nano beads kitosan dg crosslink ion logam Preparasi kitosan-alginat mikrosperis Preparasi jaringan tubuh Teknologi
Batch Batch Batch encaps ulasi
encapsulasi encapsulasi Freeze dry, ex situ, pencampur an biasa Produk Kitosan serbuk Kitosan serbuk terimpreg nasi Kitosan cair Kitosan nanobe ads Matriks imobilisasi enzim Kitosan – alginat mikrosperis Jaringan organ sintesis Aplikasi/ Penerapa n Adsorb en ion logam Adsorben ion logam Aditif pada produk makanan Adsorb en Imobilisasi enzim yang digunakan pada industry pangan Penghantaran obat/ bidang farmasi Pensubstit usi jaringan tulang
Penelitian Adsorpsi ion logam pada kitosan serbuk terimpregnasi
Kitosan sebagai pengenyal tahu, bakso dan mi Adsorp si ion logam dengan kitosan nanobe ads Imobilisasi enzim pada kitosan dg crosslink ion logam Pemanfaatan kitosan- alginate pada bidang farmasi Pemanfaat an kitosan pada berbagai bidang kedokteran
BAB II TINJAUAN PUSTAKA 1. Cangkang telur bebek
14
Cangkang telur merupakan lapisan terluar dari telur yang berfungsi melindungi bagian dalam telur dari kerusakan. Bebek dengan nama latin Anas plathyrnchos menghasilkan telur dengan cangkang berwarna hijau kebiruan pucat hingga agak putih. Ukuran cangkang telur bebek lebih besar dan tebal dari pada cangkang telur ayam ras, cangkang telur ayam kampung, dan telur puyuh. Tebal bagian kulit luar telur 0,55 mm dan bagian kulit dalam 0,015 mm (Mutiara, 2008). Cangkang telur memiliki massa 11% dari kandungan total berat telur. Kandungan cangkang adalah kalsium karbonat (94%), komponen organik (4%), kalsium fosfat (1%), dan magnesium karbonat (1%) (Fazel, 2011).
Gambar 2.1. Cangkang Telur (Hincke et al., 2012).
Cangkang telur bebek memiliki kadar kalsium sebesar 75,12% (Sari, 2013). Gambar penampang cangkang telur disajikan pada gambar 2.1. Menurut Jasinda (2013), cangkang telur terdiri dari empat lapisan berbeda (dari dalam ke luar), yaitu lapisan membran, lapisan mamilary, lapisan busa (palisade), dan lapisan kutikula.
Selama ini pemanfaatan cangkang telur digunakan untuk mengadsorbsi logam berat Fe (III) dan Cd2+ (Iriany et al., 2013), meningkatkan kandungan mineral dari kompos, meningkatkan kekuatan semen, dan karya seni (Glatz and Miao, 2009). Sebagian besar yang lain dibuang sebagai limbah (Winger, 2012) dari peternakan, rumah, dan industri makanan. Cangkang telur bebek yang akan dijadikan prekursor kalsium perlu dicuci untuk menghilangkan kotoran, bau, dan lendirnya. Membran cangkang telur bebek yang mengandung senyawa organik juga harus dihilangkan agar tidak mengganggu proses sintesis hidroksiapatit.
2. Kalsinasi cangkang telur
Kalsinasi adalah pemanasan zat padat untuk menghilangkan karbon dioksida atau gas lain dan mengeliminasi senyawa organik yang terbakar pada suhu tinggi. Panas dari tanur membuat ikatan kimia material menjadi renggang. Pada suhu tertentu atom-atom yang berikatan akan bergerak sangat bebas sehingga
kutikula pori
palisade
membran sel eksternal membran sel internal
kerucut mammilary
15
menyebabkan terputusnya ikatan kimia (Suzuki et al., 2006 dan Rachmania, 2012). Proses kalsinasi cangkang telur bertujuan untuk mengubah kalsium karbonat menjadi kalsium oksida (persamaan 2.1).
Reaksi kalsinasi:
CaCO3(s) CaO(s) + CO2(g) ... (2.1)
MgCO3(s) MgO(s) + CO2(g) ... (2.2)
Cangkang telur juga perlu dihaluskan hingga ukurannya 100 mesh karena proses kalsinasi berlangsung lebih efektif apabila material berbentuk serbuk. Semua cangkang telur mengandung komponen mineral kalsium karbonat (CaCO3) yang
stabil pada suhu kamar. Menurut Gergely et al (2010), cangkang telur yang dikalsinasi memiliki 2 tahap. Pada Tahap pertama (30 menit pertama) sebagian besar bahan organik terbakar. Pada tahap ke 2 (pada suhu 900 oC dengan waktu penahanan 3 jam) terbentuk kalsium oksida.
Suhu kalsinasi yang semakin tinggi menyebabkan susunan atom pada sampel semakin teratur sehingga semakin banyak kristal yang terbentuk (Amrina, 2008). Pada proses kalsinasi, kalsium karbonat diubah menjadi kalsium oksida dengan melepaskan karbon dioksida (persamaan 2.1). Pada proses kalsinasi terjadi pengurangan massa antara serbuk cangkang telur sebelum kalsinasi dan setelah kalsinasi, hal ini disebabkan pada proses kalsinasi terjadi pelepasan senyawa organik dan gas karbon dioksida.
Kandungan kimia MgCO3 pada cangkang telur akan menjadi MgO pada proses
kalsinasi (persamaan 2.2). Kehadiran magnesium akan menimbulkan adanya pengotor pada sintesis hidroksiapatit. Adanya senyawa MgO pada proses sintesis memungkinan ion Mg untuk masuk ke kisi hidroksiapatit. Pada bidang medis keberadaan ion Mg tidak berbahaya karena pada tulang selain terdapat kandungan Ca dan P, terdapat kandungan Mg dan Na yang merupakan substitusi alami tulang. Masuknya magnesium pada kisi kristal (crystal lattice) akan meningkatkan kristalinitas (Batra et al., 2013; Bose et al., 2013). Pada pembahasan in vivo mengindikasikan Mg-hidroksiapatit memiliki sifat osteokonduktif yang baik (Shepherd et al., 2012).
16
Tulang adalah jaringan yang kompleks yang terus-menerus dihancurkan dan diganti dengan sel yang baru. Pada skala nanometer, jaringan tulang terdiri dari fasa anorganik, organik, dan air. Komposisi penyusun tulang dalam % berat, terdiri 69% fasa anorganik, 9% air, dan 22% senyawa organik. Senyawa organik terdiri dari kolagen (90-96%) (Fazel, 2011).
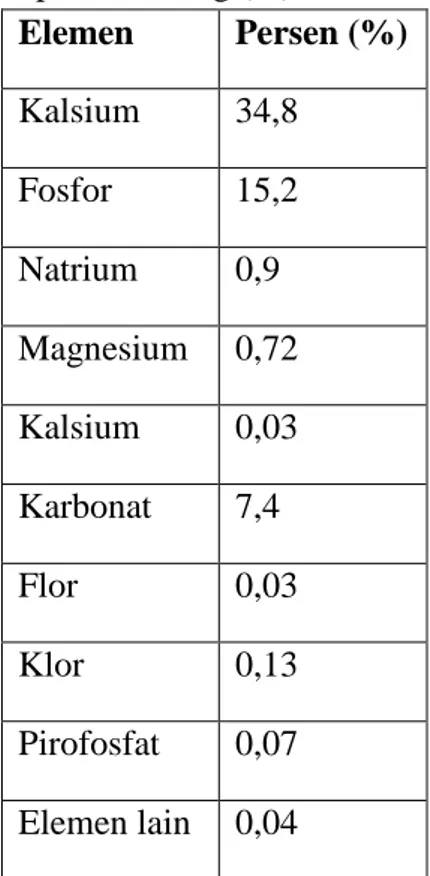
Tabel 2.1. Komposisi Tulang (%)
Elemen Persen (%) Kalsium 34,8 Fosfor 15,2 Natrium 0,9 Magnesium 0,72 Kalsium 0,03 Karbonat 7,4 Flor 0,03 Klor 0,13 Pirofosfat 0,07 Elemen lain 0,04 Sumber: Orlovskii et al., 2002.
Komponen anorganik utama tulang terdiri dari hidroksiapatit. Fase mineral yang lain terdiri dari dikalsium fosfat (Ca2P2O7), dibasic calcium phosphate (DCP,
CaHPO4), trikalsium fosfat (TCP, Ca3(PO4)2), dan beberapa fase amorf dari kalsium
fosfat. Pada tulang juga terdapat ion lain seperti sitrat (C6H5O74-), karbonat (CO32-),
flor (F-) dan hidroksil (OH-) (Neuman dalam Fazel, 2011). Pada gambar 2.2 menunjukkan tulang tersusun dari osteon, serat kolagen, serabut kolagen, dan kristal tulang berupa hidroksiapatit.
Gambar 2.2. Komposisi Dasar Tulang (Rho et al., 1998).
kristal tulang
1nm molekul kolagen
17
Unsur utama tulang adalah Ca (34,8%), P (15,2%), dan Na (0,9%). Unsur minor tulang terdiri dari Mg (0,72%), K (0,03%), CO32- (7,4%), F (0,03%), Cl (0,13%),
pirofosfat (0,07%), dan elemen lain (0,04%) (Orlovskii et al., 2002). Ion magnesium, natrium, dan kalium, ditemukan di antara garam tulang yang ditunjukkan pada Tabel 2.1. Kombinasi tersebut memberikan fungsi mekanik yang dibutuhkan oleh tulang untuk penyangga tubuh dan pendukung gerakan, karena hidroksiapatit berada di dekat setiap serat kolagen yang terikat kuat (Wati, 2014).
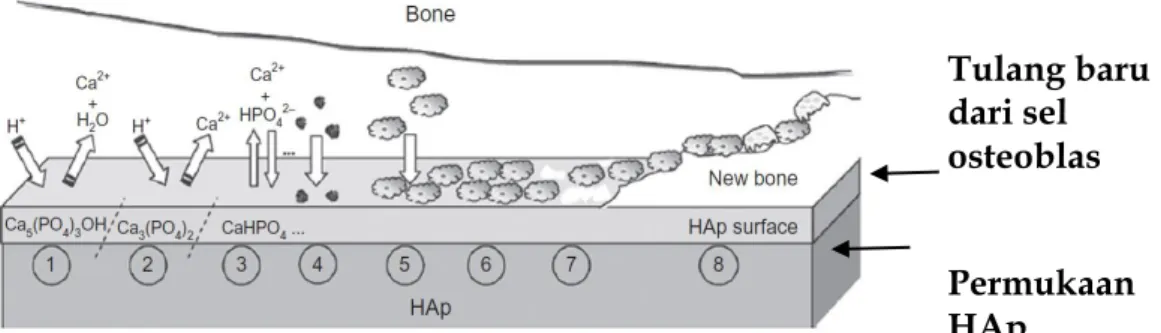
Pada gambar 2.3 menunjukkan proses penyembuhan tulang yang patah. Proses penyembuhan menggunakan implan dari material yang non-degradabel (seperti pada paduan Ti dan stainless steel) menimbulkan beberapa permasalahan. Ketika tulang telah tersambung dan sembuh, perlu operasi kembali untuk mengangkat implan karena pada kurun waktu tertentu implan bersifat toksik dan berbahaya bagi tubuh. Operasi pengangkatan implan ini memerlukan tambahan dana dan potensi terjadinya pendarahan. Selain itu, operasi pengangkatan implan juga berpotensi membuat tulang yang telah sembuh akan kembali patah. Hal ini disebabkan, logam yang diangkat dari tulang akan meninggalkan lubang. Apabila proses penyembuhan menggunakan implan dengan material biodegradabel (seperti pada HAp), tulang akan sembuh tanpa perlu operasi pengangkatan implan dan tidak menyisakan lubang (Mucalo, 2015).
Gambar 2.3. Proses Penyembuhan Patah Tulang (Mucalo, 2015).
4. Hidroksiapatit
a. Pengertian Hidroksiapatit
Hidroksiapatit adalah suatu senyawa kalsium fosfat yang mengandung hidroksida. Hidroksiapatit merupakan anggota dari mineral apatit dan mempunyai rumus kimia Ca10(PO4)6(OH)2. Kalsium fosfat telah banyak digunakan pada
Patah tulang
Implan
Implan diambil setelah penyembuhan tulang
Penyembuhan tulang selesai Implan non-degradibel
18
bidang medis dalam bentuk serbuk, padat, blok berpori, dan berbagai komposit (Ferraz et al., 2004). Hidroksiapatit memiliki rasio Ca/P yaitu 1,67 (Fazel, 2011).
Gambar 2.4. Rumus Kimia Hidroksiapatit (Ylinen, 2006). b. Struktur Hidroksiapatit
Hidroksiapatit merupakan komponen utama tulang yang terdiri dari ion Ca2+ yang dikelilingi oleh PO43- dan ion OH- (Hanson, 2007). Terdapat dua struktur
kristal berbeda yang dijumpai pada hidroksiapatit yaitu monoklinik dan heksagonal. Pada umumnya, hidroksiapatit yang disintesis memiliki struktur kristal heksagonal. Struktur Hidroksiapatit yang heksagonal memiliki space group
symmetry P63/m dengan parameter kisi a=b= 9.432 Å, c=6.881 Å, dan γ=120°.
Gambar 2.5. Struktur Hidroksiapatit (Hanson, 2007).
Hidroksiapatit dengan struktur monoklinik memiliki space group symmetry P21/b dan parameter kisi a= 9.421 Å, b= 2a, c=6.881 Å, dan γ =120° (Suryadi,
2011). Pada gambar 2.5 menunjukkan struktur hidroksiapatit. Atom kalsium berada pada 2 posisi yaitu 6 atom setiap unit sel (posisi Ca2) dan 4 atom (Ca1)
(Sadeghian, 2005). c. Sifat Hidroksiapatit
Hidroksiapatit memiliki sifat fisik, mekanik, kimia, dan biologi. Secara fisik, hidroksiapatit merupakan biokeramik bioaktif. Menurut Pane (2004), biokeramik ialah keramik yang secara inovatif yang dipergunakan untuk memperbaiki dan merekonstruksi bagian tubuh yang terkena penyakit atau cacat. Secara fisik, permukaan hidroksiapatit bersifat bioaktif sehingga dapat melekat pada jaringan dan mampu menahan beban di atasnya.
Secara kimiawi, hidroksiapatit larut dalam pelarut asam tetapi tidak larut dalam pelarut basa dan sedikit terlarut dalam air destilasi. Kelarutan hidroksiapatit dalam air meningkat dengan adanya penambahan elektrolit dan akan mengalami
Kalsium Fosfat Oksigen Atom Ca posisi 2 Atom Ca Posisi 1 Keterangan:
19
perubahan dengan adanya asam amino, protein, dan enzim (Mulyaningsih, 2007). Hidroksiapatit stabil pada pH di atas 4,2 (Pane, 2004).
Secara biologis, hidroksiapatit memiliki sifat biokompatibel dan bioaktif. Sifat ini memungkinkan jaringan sekitar untuk tumbuh ke sekitar implan sehingga ikatan dengan jaringan lebih baik. Keuntungan hidroksiapatit yang lain adalah konduktifitas listrik dan termal rendah. Hidroksiapatit bersifat osteokonduktif artinya bahan ini dapat merangsang pembentukan tulang bila diletakan didekat jaringan yang mengandung tulang (Purwasasmita dkk., 2008). Hidroksiapatit memiliki kemampuan bertahan terhadap korosi dan kemampuan bertahan terhadap perubahan dilingkungan tubuh (Pane, 2004).
d. Metode Sintesis Hidroksiapatit
Sintesis menggunakan metode yang berbeda akan menghasilkan ukuran partikel, homogenitas ukuran partikel, dan bentuk partikel yang berbeda. Ukuran partikel hidroksiapatit yang semakin kecil akan memperluas bidang kontak antara implan dengan jaringan, sehingga ikatan yang diperoleh dapat lebih baik (Purwasasmita dkk., 2008). Metode pembuatan hidroksiapatit antara lain (Suryadi, 2011; Nayak, 2010):
1. Metode Pengendapan Basah
Metode paling paling populer untuk sintesis hidroksiapatit adalah pengendapan. Teknik ini juga disebut sebagai pengendapan basah (wet
precipitation) atau pengendapan kimia (chemical precipitation) atau
pengendapan berair (aqueous precipitation). Teknik ini banyak dipilih untuk mensintesis hidroksiapatit dibandingkan teknik lain. Hal ini disebabkan jumlah hidroksiapatit yang dapat diproduksi relatif besar dan tidak memerlukan pelarut organik (Suryadi, 2011). Sintesis hidroksiapatit dengan metode basah yaitu dengan menggunakan larutan menghasilkan padatan.
Proses sintesis hidroksiapatit dengan metode basah ada dua macam yaitu
a) Proses yang melibatkan reaksi antara garam kalsium (Ca(NO3)2 dan garam
fosfat (Suryadi, 2011).
(NH4)2HPO4.10Ca(NO3)2(aq) + 6 (NH4)2HPO4(aq) + 2 H2O(l)
Ca10(PO4)6(OH)2(s) + 12 NH4NO3(aq) + 8HNO3(aq) (2.3)
b) Proses yang melibatkan reaksi antara asam (H3PO4) dan basa (Ca(OH)2).
20
Keuntungan utama sintesis dengan metode basah karena hasil samping sintesisnya adalah air, sehingga kemungkinan kontaminasi selama pengolahan sangat rendah dan biaya pengolahan rendah. Reaksi ini sederhana, murah, cocok untuk produksi industri skala besar, dan limbahnya tidak menimbulkan polusi terhadap lingkungan. Sintesis dengan metode basah menghasilkan hidroksiapatit dengan tingkat kemurnian tinggi (Muntamah dalam Wati, 2014).
2. Metode kering
Metode kering merupakan metode dengan mereaksi padatan dan padatan menjadi padatan hidroksiapatit dengan butir halus dan derajat kristalinitasnya tinggi. Pada proses ini biasanya terbentuk serbuk yang teraglomerasi. Sintesis hidroksiapatit dengan metode kering dilakukan pada suhu tinggi sehingga terbentuk fasa yang stabil (Fazel, 2011).
3. Metode hidrotermal
Metode hidrotermal merupakan metode dengan mereaksikan antara larutan dan larutan menjadi padatan hidroksiapatit pada tekanan dan suhu yang tinggi. Metode hidrotermal memiliki kristal yang baik. Namun memerlukan suhu dan tekanan yang tinggi (T>100 ºC, P>1 atm) (Yoshimura dalam Fazel, 2011).
4. Metode sol gel
Metode mereaksikan larutan dan larutan membentuk padatan hidroksiapatit menggunakan pelarut organik. Pada metode ini, serbuk hidroksiapatit yang dihasilkan memiliki ukuran butir yang relatif homogen dan derajat kristalinitas tinggi. Sintesis menggunakan metode sol gel dilakukan pada pH dan suhu yang mendekati kondisi fisiologis yaitu ada pH 7 dan suhu sekitar 37 oC. Kelemahan dari metode ini adalah perlu banyak pelarut organik untuk proses sintesis (Fazel, 2011).
5. Pengendapan Basah
Metode pengendapan basah merupakan metode yang umum digunakan karena sederhana. Hidroksiapatit yang dihasilkan menggunakan metode ini memiliki kristalinitas yang rendah. Bahan awal reaksi ini adalah kalsium hidroksida [Ca(OH)2] dan asam
ortofosfat [H3PO4] dengan produk samping adalah air (Suryadi, 2011).
Ukuran, bentuk dan permukaan morfologi hidroksiapatit yang diperoleh reaksi ini sangat sensitif terhadap laju penambahan asam ortofosfat dan suhu. Tingkat penambahan asam fosfat sangat terkait dengan pH yang diperoleh pada akhir sintesis dan stabilisasi suspensi. Suhu reaksi menentukan sintetis kristal hidroksiapatit yang monokristalin atau
21
polikristalin. Partikel hidroksiapatit yang disintesis pada suhu rendah (<60 °C) adalah monokristalin (Suryadi, 2011).
Sintesis hidroksiapatit menggunakan metode pengendapan basah dengan teknik
dropwise merupakan teknik untuk mereaksikan setetes demi setetes asam (asam fosfat)
kepada basa (Ca(OH)2). Asam fosfat yang ditambahkan setetes demi setetes lebih baik
daripada secara langsung karena tidak menyebabkan pH turun secara drastis. Laju penambahan asam fosfat sangat terkait dengan pH yang diperoleh pada akhir sintesis dan stabilisasi suspensi. Penurunan pH di bawah 7 akan menyebabkan asam fosfat terdisosiasi tidak sempurna sehingga menghasilkan β–Ca3(PO4)2 dan CaO (Angelescu et al., 2011).
Penambahan asam fosfat secara langsung pada larutan kalsium akan berpengaruh pada kehomogenan pada produk akhir. Di sisi lain, larutan yang ditambahkan secara perlahan akan meningkatkan homogenitas larutan (Agrawal et al., 2011).
Suhu sintesis hidroksiapatit pada suhu 60 oC berfungsi untuk memaksimalkan kristal yang terbentuk dan menghindari terbentuknya monokristalin yang disintesis pada suhu di bawah 60 oC. Penambahan asam fosfat pada saat sintesis akan membuat campuran bersifat asam sehingga perlu penambahan basa agar pH menjadi 10 menggunakan larutan NaOH. Konsentrasi 1 M pada NaOH bertujuan agar hidroksiapatit yang dihasilkan tidak memiliki sifat toksik dan tidak terjadi kenaikan pH secara drastis (Suryadi, 2011).
6. Kristal
Kristal adalah suatu padatan yang atom, molekul, atau ion penyusunnya terkemas secara teratur dan polanya berulang secara tiga dimensi. Zat cair membentuk kristal ketika mengalami proses pemadatan. Struktur kristal yang terbentuk dari suatu cairan tergantung pada bahan kimia dan kondisi ketika terjadi pemadatan (Setyopratomo dkk, 2003).
Hidroksiapatit diharapkan memiliki kristal densitas tinggi dan stabil sehingga perlu dilakukan sintering sampai suhu tertentu. Suhu saat sintering merupakan faktor yang dapat memengaruhi dekomposisi karena secara aktif permukaan hidroksiapatit dapat berinteraksi dengan lingkungan di sekitarnya pada suhu tertentu. Menurut penelitian Suryadi (2011), proses sintering pada suhu 900 oC merupakan suhu optimum terbentuknya hidroksiapatit. Selama proses sintering terjadi pengurangan ukuran pori-pori disertai penumbuhan butir, sehingga terjadi ikatan yang kuat antara masing-masing butir. Sintering dilakukan di bawah titik leleh hidroksiapatit sehingga hanya terbentuk padatan hidroksiapatit.
22
Sintesis hidroksiapatit dari larutan yang mengandung kalsium fosfat melalui proses kristalisasi. Proses kristalisasi dari fasa larutan berlangsung dalam larutan supersaturasi yang kemurniannya dapat dikontrol oleh kemurnian larutan. Kristalisasi merupakan proses pembentukan zat padat dari pengendapan larutan. Endapan adalah zat yang memisahkan diri sebagai suatu fasa padat dari larutannya sehingga membentuk kristal (Basset et al., 1978).
Ukuran kristal yang terbentuk selama pengendapan tergantung laju pembentukan inti dan laju pertumbuhan kristal. Laju pembentukan inti dinyatakan sebagai jumlah inti yang terbentuk dalam satuan waktu. Jika laju pembentukan inti tinggi, banyak sekali kristal yang terbentuk, tetapi dengan ukuran yang kecil (Basset et al., 1978).
Proses kristalisasi dari fasa larutan berlangsung mengikuti rule of stages by ostwald melalui tiga tahap yaitu nukleasi, agregasi, dan pertumbuhan kristal (gambar 2.6). Pada tahap nukleasi, ion dan/atau kumpulan ion bertumbukan sehingga membentuk inti kritis. Inti kritis merupakan kombinasi ion terkecil dengan struktur kristal yang tidak larut dalam medium. Tahap kedua adalah selanjutnya yaitu proses pertumbuhan kristal. Pada tahap ini terjadi penambahan ion dan/atau kumpulan ion pada inti kritis sehingga ukuran kristal bertambah besar (Indrani, 2012).
Gambar 2.6. Proses Kristalisasi dari Fase Larutan Mengikuti Rule of Stages
by Ostwald (Sanosh et al dalam Indrani., 2012).
Proses nukleasi dan pertumbuhan kristal bergantung pada kondisi kadar supersaturasi larutan. Pengadukan dapat menambah gerak ion sehingga mempercepat laju proses nukleasi maupun pertumbuhan kristal. Pada kondisi tertentu terjadi pertambahan ukuran kristal yang berlangsung setelah tahap pertumbuhan kristal selesai. Oleh karena ion mineral dalam larutan telah dipakai dalam proses nukleasi dan pertumbuhan kristal, maka pertambahan ukuran kristal berlangsung melalui proses konsolidasi yang bersamaan dengan menurunnya jumlah kristal. Kristal berukuran kecil larut menjadi ion bebas dan membentuk kristal yang lebih besar. Proses ini berlangsung terus sampai semua material
Difusi Reaksi Nukleasi Agregasi Pertumbuhan kristal
23
mengalami konsolidasi dan membentuk kristal hidroksiapatit, dan akhirnya membentuk partikel hidroksiapatit (Indrani, 2012).
Proses pembentukan hidroksiapatit secara kimiawi diinisiasi oleh pembentukan fasa kalsium fosfat intermediat yang amorf. Kemampuan kalsium fosfat amorf untuk mengabsorbsi ion-ion Ca2+ dan HPO42- mengarah ke pembentukan apatit. Perubahan
berlanjut terus dengan bertambahnya kandungan ion OH- sehingga terbentuk fasa intermediat dikalsium fosfat anhidrat dengan Ca/P 1,00. Perubahan meningkat sampai terbentuk hidroksiapatit dengan Ca/P 1,67 (Blumenthal dalam Indrani, 2012). Berdasarkan komposisi dan struktur hidroksiapatit bersifat paling stabil.
Tujuan dari proses kristalisasi adalah menghasilkan produk kristal dengan kualitas yang diharapkan. Kualitas kristal yang dihasilkan dapat ditentukan dari distribusi ukuran kristal, kemurnian kristal, dan bentuk kristal. Proses kristalisasi dapat ditingkatkan dengan meningkatkan laju pengadukan, menaikkan pH, menaikkan suhu, atau menghilangkan penghambat (Setyopratomo dkk, 2003). Pada sintesis hidroksiapatit, suspensi diaging (didiamkan) pada suhu kamar untuk memaksimalkan proses kristalisasi. Kristalinitas pada proses aging masih rendah, sehingga perlu dilakukan sintering pada suhu tinggi untuk meningkatkan kristalinitas. Hidroksiapatit sebagai implan diberi perlakuan panas untuk memperoleh kekuatan mekanik tinggi. Suhu sintering yang dilakukan pada akhir proses sintetisnya memberikan peningkatan kekuatan dari hidroksiapatit sebanyak 3-4 kali (Indrani, 2012).
8. Pengotor pada Kristal
Pengotor yang ada pada kristal terdiri dari dua katagori yaitu pengotor yang ada pada permukaan kristal dan pengotor yang ada di dalam kristal. Pengotor yang ada pada permukaan kristal berasal dari larutan induk yang terbawa pada permukaan kristal pada saat proses pemisahan padatan dari larutan induknya (retention liquid) (Setyopratomo dkk, 2003).
Pengotor pada permukaan kristal ini dapat dipisahkan hanya dengan pencucian. Cairan yang digunakan untuk mencuci harus mempunyai sifat dapat melarutkan pengotor tetapi tidak melarutkan padatan kristal. Salah satu cairan yang memenuhi sifat di atas adalah larutan jenuh dari bahan kristal yang akan dicuci, namun dapat juga dipakai pelarut pada umumnya yang memenuhi kriteria tersebut (Setyopratomo dkk, 2003).
Pada sintesis hidroksiapatit, H2O digunakan sebagai cairan pencuci untuk
24
sintesis, sehingga perlu adanya proses pencucian diakhir proses sintesis agar tidak ada pengotor NaOH. Pelarut air akan melarutkan NaOH namun tidak melarutkan hidroksiapatit, karena hidroksiapatit merupakan senyawa yang sulit larut dalam air.
Adapun pengotor yang berada di dalam kristal tidak dapat dihilangkan dengan cara pencucian. Salah satu cara untuk menghilangkan pengotor yang ada di dalam kristal adalah dengan jalan rekristalisasi, yaitu dengan melarutkan kristal tersebut kemudian mengkristalkannya kembali. Pada sintesis hidroksiapatit, pengotor kemungkinan dapat masuk ke dalam ksi hidroksiapatit adalah karbonat (CO32-) (Suryadi, 2011). Adanya unsur
lain pada prekursor sintesis hidroksiapatit juga akan memungkinkan adanya pengotor. 9. Sintering
Proses sintering pada padatan terbagi menjadi 3 tahapan yaitu tahap awal, intermediet, dan akhir (Naik, 2014):
a. Tahap 1 (Tahap awal)
Pada tahap awal terjadi pembentukan leher (neck) pada partikel secara cepat
(rapid interparticle neck growth) dan terjadi peningkatan densitas 0,65 %. Material mengalami pergerakan untuk meningkatkan jumlah titik kontak dan pada akhirnya membentuk ikatan pada titik kontak tersebut (German, 1994).
b. Tahap 2 (Tahap intermediet)
Pada tahap intermediet, leher terhubung (interconnected channels) antara butir (grain edges) sehingga terbentuk pori. Pertumbuhan leher terus berlanjut, yang diikuti dengan pertumbuhan butir dan pertumbuhan pori. Batas butir mulai meningkat sehingga butir mulai tumbuh (grow), terbentuknya saluran yang saling berhubungan (continuous channel) dan berakhir ketika pori terisolasi (German, 1994).
c. Tahap 3 (Tahap Akhir)
Pemadatan membuat pori terisolasi dan menyusut secara terus menerus. Pada proses sintering, pori akan terisolasi karena permukaan dan tegangan antar muka. Penggabungan antar butir terus terjadi hingga membentuk saluran rongga kontinyu, densitas meningkat dari 65% ke 90%, Pada kondisi tertentu pori menghilang (German, 1994).
A. Kitosan
Kitosan merupakan hasil deasetilasi dari kitin. Kitosan sebagai polimer yang tersusun dari 2-amino-2-deoksi-β-D-glukosa dapat diperoleh dengan cara merubah
25
gugus asetamida (-NHCOCH3) pada kitin menjadi gugus amina (-NH2). Dengan
demikian pelepasan gugus asetil pada asetamida kitin menghasilkan gugus amina terdeasetilasi (Ihsani, 2014).Kitosan sebagai polimer alami memiliki sifat biologi yaitu biokompatibel, biodegradabel, aman dan tidak toksik dan sifat kimia berupa poliamina linear, gugus amino reaktif, serta gugus hidroksil reaktif (Duttaet al., 2004).Kitosan merupakan material biomedis karena bersifat biodegradabel, tidak beracun, anti bakteri, dan biokompatibel, kitosan mampu menyerap banyak substrat tergantung pada jumlah gugus amino terprotonasi dalam rantai polimer yang berpengaruh pada proporsi asetilasi dan non asetilasi unit D-glukosamin (Kim et al., 2007; Santiago, 2011).
Gambar 2.3. Struktur kitin dan kitosan. (a) struktur kimia poli kitin (N-acetil- -D-glukosamin) dan (b) kitosan (poli(D--D-glukosamin) unit. (c) struktur kitosan terasetilasi sebagian (Rinaudo, 2006).
Sifat mekanik komposit kitosan/hidroksiapatit memainkan peranan penting dalam teknik jaringan tulang. Ikatan hidrogen intramolekuler daninteraksi khelat antara kitosan dan hidroksiapatit berkontribusi pada sifat mekaniknya. Interaksi yang mungkin antara gugus NH2 dan gugus OH primer dan sekunder dari kitosan dengan
Ca2+ dari Hap (ikatan koordinasi logam). Interaksi ini yang mungkin bertanggung jawab pada kekuatan mekanik yang lebih tinggi dari komposit dibandingkan dengan kitosan dan hidroksiapatit sendiri. Kuat tekan telah menjadi parameter yang digunakan secara luas untuk kekuatan mekanik dari scaffold berpori (Venkatesan, 2010).
26
Gambar2.4.Interaksi kimia antara kitosan-hidroksiapatit (Cheng et al., 2009) B. Kolagen
Kolagen menyusun hampir sepertiga total massa protein pada vertebrata dan merupakan protein yang paling berlimpah di dalam tubuh. Jaringan pengikat berkolagen terdiri dari serat, struktur ini selanjutnya tersusun atas fibril kolagen.Hampir sepertiga protein dalam tubuh vertebrata berada sebagai kolagen. Kolagen juga merupakan komponen serat utama dalam tulang. Gigi, tulang rawan, lapisan kulit dalam (dermis), dan tendon (urat daging).Kolagen ada dalam semua organ yang menampilkan kekuatan dan kekakuan.
Gambar 2.5. Struktur asam amino penyusun kolagen (Stryer, 2000)
Kolagen mengandung kira-kira 35% glisin dan kira-kira 11% alanin, kandungan prolin dan 4-hidroksiprolin yang tinggi yaitu asam amino yang jarang ditemukan pada protein selain pada kolagen dan elastin. Bersama-sama prolin dan hidroksiaprolin mencapai kira-kira 21% dari residu asam amino pada kolagen (Lehninger, 1982). Gambar 2.5 menunjukkan urutan asam amino sebagai rantai kolagen. Dalam satu penggal dengan lebih dari seribu residu, tiap residu ketiga adalah glisisn. Kandungan residu prolin dan hiroksiprolin juga tinggi.
Struktur Kolagen tersusun atas tiga tingkat yakni:
a. Kerangka kovalen terdiri dari rantai-rantai protein individual dengan bobot molekuler sebesar kira-kira 100.000 masing-masing.
b. Tiga rantai bergabung untuk membentuk tripel heliks dalam struktur sekunder. Triple heliks ini meruakan satuan struktural dasar dari kolagen dan disebut
27
tropoolagen. Tropokolagen merupakan batang berdiameter 15 dan panjang 3000 . Dalam heliks tropokolagen ketiga benang terikat hidrogen satu dengan yang lain dengan perantaraan gugus peptida –NH dari residu glisin dan gugus eptida –C=O paa rantai lain. Ini merupakan struktur heliks yang berbeda nyata dari -heliks. c. Satuan tropokolagen yang terangkaikan secara kovalen, yang kemudian membentuk
suatu ikatan atau berkas yang disebut mikrofibril. Kolagen fibril dapat terbentuk dalam ikatan paralel, dalam hal pembentukan urat, atau dalam lembaran-lembaran seperti ikatan pembntukan kertas dan dalam hal pembentukan kulit (Page dalam Katili, 2009).
Kolagen dapat diekstraksi dari ikan pari dan tuna (Kasim, 2013), kulit ikan nila hitam (Putra, dkk., 2013), cakar ayam (Prayitno, 2007) dan tulang sapi.Kolagen dapat diperoleh melalui ekstraksi bahan-bahan sumber kolagen dengan menggunakan asam-asam organik ataupun asam-asam-asam-asam anorganik (Kasim, 2013).Berdasarkan hasil penelitian Baliant dan Bowes dalam Prayitno (2007), bahwa cakar ayam mengandung protein 17,4%, kolagen berkisar 9,07%, air 60,05%, abu 5,98% dan lemak 12%. Kolagen yang paling umum adalah kolagen tipe 1 yang terdiri dari tiga rantai polipeptida. Dua rantai polipetida disebut tipe dan rantai polipeptida yang ketiga adalah tipe . Kolagen tipe 1 adalah paling banyak terdapat pada bagian tubuh yang keras seperti tulang dan gigi serta jaringan penghubung (Liu et al., 2001). Menurut hasil Penelitian Prayitno (2007) dan Chia-Wi Lin,et al. (2013), dan Hasim (2014)berdasarkan analisis elektroforegram menunukkan kolagen tipe 1 menjadi komponen kolagen terbesar dalam cakar ayam.
C. Komposit Hidroksiapatit-Kolagen-Kitosan
Komposit adalah suatu jenis bahan baru hasil rekayasa yang terdiri dari dua atau lebih bahan dimana sifat masing-masing bahan berbeda satu sama lainnya baik itu sifat kimia maupun fisikanya dan tetap terpisah dalam hasil akhir bahan tersebut (bahan komposit) (Nayiroh, 2003). Penggunaan campuran beberapa material polimer dapat mendukung sebagai komponen scaffold untuk teknik jaringan tulang. Ikatan antar muka antara fase organik dan anorganik memainkan peran penting dalam menentukan sifat mekanik utama dari komposit. Sebuah ikatan antar muka yang kuat antara dua fase biasanya diperlukan untuk komposit untuk mencapai sifat mekanik yang lebih baik (Qing, 1997).
28 D. Metode sintesis
Dalam mensintesis komposit hidroksiapatit kolagen kitosan dapat dilakukan dengan metode in-situ dan ex-situ.Metode in-situ merupakan metode sintesis yang dilakukan bersamaan dalam pembentukan sampel utama (Trisnawati, dkk., 2014). Metode ex-situ merupakan metode pencampuran yang dilakukan setelah sampel utama terbentuk, pada penelitian ini adalah suspensi hidroksiapatit dan kolagen kitosan adalah polimer yang ditambahkan. Metode ex-situ akan memiliki persen kemurnian yang lebih tinggi karena sampel telah terbentuk sempurna. Thandalam et al. (2015) dan Guo et al. (2014) menyebutkan bahwa metode ex-situ memiliki kelebihan fabrikasi komposit yang mudah.
29
BAB III TUJUAN DAN MANFAAT Tujuan khusus penelitian ini adalah:
1. Memperoleh data tentang berbagai aspek yang berkaitan dengan cara sintesis kolagen dari tulang sapi
2. Memperoleh data tentang berbagai aspek yang berkaitan dengan cara sintesis Hidroksiapatit dari cangkang telur bebek
3. Mendapatkan data kondisi optimum sintesis bone graft dari kolagen hidroksiapatit kitosan termasuk
4. Memperoleh data karakteristik kimia dan fisika kolagen, hidroksiapatit dan bone graft hasil sintesis
5. Memperoleh data hasil uji in vitro, laju degradasi, laju korosi dan uji sitotoksisitas bone graft yang disintesis dari kolagen hidroksiapatit dan kitosan Manfaat penelitian :
Manfaat kegiatan penelitian ini adalah :
1. Mampu meningkatkan potensi bahan lokal Indonesia dalam hal ini limbah cangkang telur, kitosan dan kolagen menjadi bone graft yang bernilai ekonomis tinggi
2. Mendukung ketersediaan bone graft untuk memenuhi kebutuhan bahan untuk menangani kasus fraktur tulang sehingga mandukung Inonesia mandiri di bidang medis
30
BAB IV METODE PENELITIAN
Sasaran Penelitian adalah bone graft yang dihasilkan dari bahan dasar kolegen HA kitosan. Lokasi Penelitian
Kegiatan penelitian ini dilakukan di laboratorium kimia Jurusan Kimia FMIPA UNESA. Beberapa analisa dilakukan di Laboratorium MIPA Terpadu dan di farmasi Unair.
Waktu penelitian
Penelitian ini direncanakan selama 2 tahun (2017-2018), pada tahun pertama penelitian berlangsung direncanakan selama 8 bulan dimulai bulan Mei 2017 sampai Nopember 2017.
Metodologi Penelitian Pada Tahun I Alat dan Bahan
Kitosan diisolasi dari cangkang udang windu dengan metode Hong(1989). Bahan-bahan kimia yang digunakan dalam penelitian ini cangkang udang windu, HCl, buffer pH 2-7, NaOH, akuades bebas mineral, Na2HPO4, CH3COOH, NH4OH, H3PO4, kitosan
standar, kolagen standar, Hidroksiapatit standar, buffer 7-8, cangkang bebek/itik, tulang sapi, air deminaral, etanol
Peralatan
Peralatan yang digunakan dalam penelitian ini meliputi: (1) peralatan gelas seperti labu takar, tabung reaksi, gelas pengaduk, pipet volume, corong gelas. (2) peralatan analisis seperti Spektrofotometer UV-vis Lamda bio 20, SEM, BET, XRD, PSA, UTM,. (3) peralatan penunjang seperti: shaker berpenangas, tabung sentrifus, sentrifus merk Fischer scientific dengan kecepatan maksimum 3500 RPM, botol film, pH-meter merk Orion model 710A, kertas saring Whatman 42, neraca analitik Mettler, furnace, kurs porselin. Prosedur penelitian
Sintesis kitosan dari cangkang udang windu
Sintesis kitosan dari cangkang udang windu dilakukan menggunakan metode Hong (1990) dengan 3 tahap yaitu deproteinasi dengan menggunakan NaOH 3,5%, demineralisasi menggunakan HCl 1% dan deasetilasi menggunakan NaOH 50%. Kitosan yang dihasilkan dianalisis dengan FTIR, XRD, BET, dan ditentukan rendemennya.
31
Cangkang telur bebek dibersihkan di air yang mengalir dan bagian membrannya dipisahkan. Setelah itu, cangkang telur dikeringkan pada temperatur ruangan. Selanjutnya kalsinasi dilakukan pada temperatur 1000oC selama 5 jam untuk menghilangkan komponen organik dan mengubah kalsium karbonat (CaCO3) menjadi kalsium oksida (CaO). Cangkang telur hasil kalsinasi dikarakterisasi dengan XRD untuk memastikan bahwa CaCO3 pada cangkang telur bebek telah berubah menjadi CaO. Dihitung rendemen CaO.
Sintesis Hidroksi Apatit
Hidroksi Apatit disintesis dengan metode presipitasi secara in situ, dengan meneteskan larutan KH2PO4 (0,5 M) ke dalam larutan CaO (0,3 M) dan diaduk dengan magnetic stirrer. Suhu selama presipitasi dan pengadukan dijaga konstan pada temperatur 37oC. Setelah presipitasi, proses pengadukan dilanjutkan selama 30 menit. Selanjutnya, larutan hasil presipitasi diaging (disimpan) selama 12 jam. Larutan hasil aging kemudian disaring dengan menggunakan kertas saring untuk mendapatkan endapan yang berwarna putih. Setelah itu, endapan hasil penyaringan dipanaskan dalam furnace pada temperatur 110 oC selama 3 jam, sehingga diperoleh serbuk berwarna putih. Serbuk putih tersebut selanjutnya dikarakterisasi dengan XRD dan FT-IR , BET, AFM, SEM dibandingkan dengan HA standar juga ditentukan rendemen HAnya.
Sintesis Kolagen dari tulang tulang sapi
Sintesis kolagen dari tulang sapi dilakukan dengan cara merendam 70 gram tulang dalam 5% HCl selama 24 jam pada suhu 4ºC. Perendaman dilakukan dengan perbandingan b:v 1:20. Setel ah masa perendaman, filtrat hasil perendaman ditambahkan 1N NaOH sampai pH netral. Filtrat didiamkan sampai terbentuk gumpalan putih. Gumpalan yang terbentuk dipisahkan dengan cara disaring menggunaka kertas saring. Kolagen basah yang terbentuk dikeringkan dengan metode freeze drying. Kolagen yang terbentuk dikarakterisasi dengan FTIR, XRD dan BET dibandingkan dengan kolagen standar dan juga ditentukan rendemennya..
Sintesis bone graft dari kolagen hidroksiapatit kitosan
Larutan kolagen dibuat dengan cara melarutkan kolagen dengan asam asetat 1%. Larutan kitosan dibuat dengan cara melarutkan kitosan dalam asam asetat 1%. Latutan hidroksiapatit dibuat dengan cara melarutkan hidroksiapatit dengan asam fosfat. Larutan kitosan dicampur dengan larutan kolagen dan larutan hidroksiapatit dengan perbandingan
32
kitosan : Hidroksiapatit: kolagen yang divariasi 10:50: 40; 20:50:30; 25:50:25 ; 30:50:20; 40:50:10. Larutan yang dihasilkan dinetralkan dengan NH4OH , setelah netral diaduk
perlahan-lahan. Kemudian dimasukkan dalam beker glass, dibekuakan pada suhu -10, - 40 dan -80 selama waktu yang bervariasi 2, 4, 6 dan 8 jam. Bone graft yang dihasilkan selanjutnya dikarakterisasi sifat fisika dan kimianya.
Karakterisasi Bone gratt
Material yang dihasilkan selanjutnya dikarakterisasi yaitu : gugus fungsional ; ukuran pori, distribusi pori, surface area; kristalinitas; analisis morfologi permukaan, penampang lintang.
Metodologi penelitian tahun kedua:
Bone graft yang dihasilkan pada tahun pertama dikarakterisasi fisika maupun kimia yaitu a. Analisis morfologi
b. Uji tarik mulur/ sifat mekanik c. Uji kuat tekan
d. Uji degradasi e. Uji laju korosi f. Uji in vitro g. Uji sitotoksisitas
33 Bagan Alir penelitian selama 2 tahun :
Bagan Alir penelitian Keterangan :
Sudah dilakukan Akan dilakukan Tahun pertama -karakterisasi: FTIR, SEM, XRD, rendemen Variabel:Komposisi, pH, suhu pembekuan, waktu pembekuan
-Isolasi hidroksiapatit dari cangkang telur bebek - Isolasi kolagen dari tulang sapi
-
Tahun kedua
Bone graft hasil tahun pertama
Sintesis bone graft: hidroksiapatit kolagen kitosan
-Analisis morfologi - Uji tarik mulur - Uji kuat tekan - Uji degradasi - Uji laju korosi - Uji in vitro - Uji sitotoksisitas. -
1.data kondisi optimum isolasi: a. Hidroksiapatit
b.kolagen
c sintesis bone graft dari kolagen kitosan dan hidroksiapatit
2.hasil analisis FTIR, XRD,BET, rendemen dari:
a. Hidroksiapatit b. Kolagen c. Bone graft
Luaran tahun pertama: a.Produk bone graft
b. hasil kharakteristik bone graft. c.Publikasi pada jurnal nasional bereputasi/ internasional
c. Draft Paten dan buku ajar
bone graf yang sudah terakterisasi dan memenuhi standar
Luaran tahun kedua: a. bone graft yang sudah terkarakterisasi lengkap. b.Publikasi pada jurnal internasional
c.HKI/ paten
d. Inovasi penerapan Ipteks bidang material medis. e. buku ajar
Karakterisasi FTIR, XRD, BET
Isolasi kitosan dari cangkang udang
-karakterisasi: FTIR, SEM, XRD, PSA rendemen
34 Teknik Analisis Data
Data yang diperoleh dari penelitian dianalisis secara deskriptif kuantitatif. Data hasil sintesis kitosan, kolagen, hidroksiapatit dianalisis rendemennya. Spektra IR yang dihasilkan dianalisis gugus fungsionalnya untuk menggambarkan gugus fungsional yang berperan dalam pembentukan bone graft, data defraktogram dianalisis sifat kristalinitas dan kemurnian dari hasil sintesis, data BET dianalisis ukuran pori, distribusi pori dan surface area, data SEM dianalisis untuk menggambarkan morfologi permukaan dan penamapang lintang dari material, data uji mekanik dianalisis untuk menggambarkan tarik mulur dan modulus young yang menjadi indicator kelenturan suatu material, data kuat tekan menggambarkan kemampuan material nmenahan beban, data uji degradasi dianalisis untuk menggambarkan ketahanan terhadap kerusakan, data biokompatibel, ketoksikan diperoleh dari data uji in vitro dan uji toksisistas.
35
BAB V HASIL DAN LUARANAN YANG TELAH DICAPAI
Pada bagian ini akan diuraikan capaian luaran penelitian yang telah dihasilkan sampai dengan saat ini.
A. Preparasi dan Kalsinasi Cangkang Telur Bebek
Sampel cangkang telur dicuci untuk menghilangkan kotoran, bau, lendir, dan membrannya. Membran Cangkang telur bebek mengandung senyawa organik sehingga harus diminimalkan agar tidak mengganggu proses sintesis HAp. Cangkang telur bebek yang telah bersih, dikeringkan untuk mengurangi kandungan air. Setelah kering, Cangkang telur bebek dihaluskan hingga berbentuk serbuk agar proses pemanasan berlangsung efektif. Energi panas dari tanur mengalir secara konduksi ke seluruh permukaan butir sehingga distribusi panas merata dan kalsinasi dapat maksimal (Rachmania, 2012).
Reaksi kalsinasi cangkang telur bebek: CaCO3(s) CaO(s) + CO2(g) (5.1)
Proses kalsinasi Cangkang telur bebek pada suhu 1000 oC berfungsi untuk menguraikan CaCO3 menjadi CaO dan gas CO2 (persamaan 4.1). Panas dari tanur
membuat ikatan kimia menjadi renggang dan atom yang berikatan bergerak bebas. Pada suhu 850 sampai 1000 oC ikatan kimia pada CaCO3 terputus membentuk CaO (Sari, 2013).
Setelah proses kalsinasi, dilakukan proses pendinginan cangkang telur bebek secara perlahan di dalam tanur hingga sampel mencapai suhu ruang. Apabila sampel CaO diambil secara langsung pada suhu 1000 oC, maka CaO akan mengalami kejutan termal (thermal
shock) yaitu perubahan suhu secara mendadak yang membuat morfologi permukaannya
mengalami perubahan (Oxtoby et al., 2003). Perubahan morfologi, membuat CaO membentuk gumpalan (cluster) yang retak dan terpecah (Sofyan, 2012). Setelah kalsinasi, terjadi perubahan warna Cangkang telur bebek dari hijau menjadi putih (Gambar 4.1). Menurut Rachmania (2012), perubahan warna terjadi karena perubahan komposisi unsur pada CB sebelum kalsinasi dan setelah kalsinasi. Komponen awal pada Cangkang telur bebek yaitu CaCO3, Ca(PO)4, MgCO3, MgPO4 dan senyawa organik yang memiliki warna
hijau. Pada proses kalsinasi, terjadi perubahan komposisi menjadi pada CaCO3 menjadi
CaO serta MgCO3 menjadi MgO. Perubahan komposisi disertai terbakarnya senyawa
organik pada sampel CB-K membuat sampel menjadi berwarna putih.
36
Gambar 4.1. CB Sebelum Kalsinasi (A) dan Setelah Kalsinasi (B).
Pada proses kalsinasi terjadi penurunan massa antara serbuk cangkang telur bebek sebelum kalsinasi yaitu dari 5 gram menjadi 4,180 gram, sehingga didapatkan rendemen 83,660%. Putri (2012) telah melakukan kalsinasi Cangkang telur bebek pada suhu 1000 oC dengan rendemen 55,030%. Perbedaan rendemen penelitian ini dengan penelitian Putri (2012) dapat terjadi karena berbedanya komposisi kandungan organik pada cangkang telur bebek yang belum dikalsinasi antara cangkang telur bebek pada penelitian ini dengan cangkang telur bebek pada penelitian Putri (2012). Besarnya kadar zat organik pada cangkang telur bebek yang belum dikalsinasi membuat rendemen cangkang telur bebek yang sudah dikalsinasi semakin kecil karena zat organik akan terbakar pada suhu kalsinasi yang tinggi.
Penurunan massa cangkang telur bebek selama kalsinasi disebabkan pelepasan gas CO2 dan penguraian senyawa organik. Komponen organik dari cangkang telur bebek yang
hilang selama proses kalsinasi dapat berasal dari protein (Mine, 2008). Protein pada cangkang telur adalah mukopolisakarida yang terdiri dari kondrotin sulfat A dan B, glukosamin, galaktosamin, galaktosa, manosa, dan asam sialat (Rivera et al., 1999). Komponen lain pada cangkang telur bebek adalah MgCO3 sebesar 1% (Fazel, 2011).
Menurut Oxtoby et al (2003), MgCO3 yang dikalsinasi pada suhu 800 sampai 900 oC akan
membentuk MgO disertai pelepasan CO2. Setelah suhu MgO turun, MgO dapat bereaksi
dengan air di udara membentuk Mg(OH)2 (persamaan 5.2 dan persamaan 5.3).
Reaksi kalsinasi magnesium karbonat:
MgCO3(s) MgO(s) + CO2(g) ... (5.2)
MgO(s) + H2O(l) Mg(OH)2(aq) ... (5.3)
Pada bidang medis, keberadaan ion Mg tidak berbahaya karena pada tulang juga mengandung Mg sebesar 0,72% (Orlovskii et al., 2002 and Stipniece et al., 2013). Pada penelitian Stipniece et al (2013), campuran Ca(OH)2/Mg(OH)2 direaksikan dengan H3PO4
sehingga membentuk (Mg-HAp) dengan rumus kimia Ca10-xMgx(PO4)6(OH)2. Seperti pada
HAp, Mg-HAp memiliki sifat osteokonduktif yang baik (Shepherd et al., 2012). Pada penelitian Cai et al (2009), kehadiran Mg pada HAp dapat meningkatkan sifat bioaktif pada pembentukan tulang dan meningkatkan kelarutan HAp (Batra et al., 2013; Bose et al., 2013). Pada penelitian ini, produk akhir sintesis memungkinkan masih terdapat Mg karena prekursor kalsium mengandung sebagian kecil Mg. Adanya Mg pada prekursor tidak membahayakan namun bermanfaat untuk tulang.
37
Pada penelitian ini, tidak ada komposisi Mg pada sampel yang ditunjukkan pada difraktogram Cangkang telur bebek hasil kalsinasi (Gambar 5.3). Berdasarkan literatur, terdapat Mg sebelum dan sesudah Cangkang telur bebek dikalsinasi. Fadeev et al (2003) telah membuat HAp disertai Mg menggunakan metode pengendapan basah. Kadar maksimal ion Mg2+ yaitu 10% b/b. Kadar Magnesium pada cangkang telur hanya 1% (Fazel, 2011), sehingga mengindikasikan kadar Mg pada sampel HAp tidak membahayakan bagi tubuh.
B. Sintesis HAp
Serbuk CaO dari hasil kalsinasi cangkang telur bebek direaksikan dengan air untuk membentuk larutan Ca(OH)2 (persamaan 5.4). Larutan Ca(OH)2 ditambah H3PO4 setetes
demi setetes agar pH tidak turun secara drastis. Laju penambahan asam fosfat sangat terkait dengan pH yang diperoleh pada akhir sintesis. Penurunan pH dibawah 7 menyebabkan H3PO4 terdisosiasi tidak sempurna sehingga menghasilkan β–Ca3(PO4)2 dan
CaO (Angelescu et al., 2011). Larutan H3PO4 yang ditambahkan secara perlahan juga
berfungsi meningkatkan homogenitas larutan (Agrawal et al., 2011). Reaksi kalsium oksida dengan akuademin:
CaO(s) + H2O(l) Ca(OH)2(aq) ... (5.4)
Pada penelitian ini, sintesis HAp dipilih pada suhu 60 oC untuk memaksimalkan kristal yang terbentuk dan menghindari terbentuknya struktur monoklinik yang disintesis pada suhu dibawah 60 oC (Suryadi, 2011). HAp yang disintesis, diharapkan memiliki struktur yang sama dengan tulang yaitu heksagonal (Spiers, 1968). Ketika H3PO4 ditambahkan
pada Ca(OH)2 maka secara perlahan larutan menjadi bersifat asam, sedangkan proses
kristalisasi berlangsung efektif pada suasana basa (Malina et al, 2013). Larutan selanjutnya ditambahkan NaOH agar proses kristalisasi dapat maksimal. Penambahan basa hingga pH 10 karena larutan HAp stabil pada pH tersebut (Dorozhkin, 2010).
Penambahan NaOH pada konsentrasi kecil membuat pH mengalami kenaikan secara perlahan hingga mencapai pH 10. Kenaikan pH secara drastis membuat kristal terbentuk tidak maksimal, akibatnya tidak terbentuk senyawa apatit melainkan β–Ca3(PO4)2
(Angelescu et al., 2011). Setelah pH mencapai pH 10, larutan didiamkan (aging) pada suhu kamar untuk memaksimalkan pertumbuhan kristal (kristalisasi) HAp (Byrappa and Ohachi, 2003). Laju kristalisasi ini dapat dipercepat dengan mengantisipasi masuknya penghambat (Setyopratomo dkk, 2003) yaitu karbonat. Pembentukan karbonat dapat terjadi karena