BAB 2
TINJAUAN PUSTAKA
2.1. Tumbuhan Baru Cina (Artemisia vulgaris L.)
Tumbuhan Baru Cina (Artemisia vulgaris L.) merupakan tumbuhan liar yang tumbuh di lapangan terbuka. Tanaman ini tersebar luas di seluruh dunia yang terdiri dari lebih 800 spesies, dengan ketinggian 50-150 cm, berwarna hijau dan berbunga. Daun tumbuhan Baru Cina (Artemisia vulgaris L.) berdasarkan laporan penelitian sebelumnya mengandung senyawa saponin, flavonoida, polifenol (Judzentiene dan Buzelyte, 2006). Di pulau Sumatera tumbuhan ini disebut tumbuhan Baru Cina, di Pulau Jawa disebut Suket Gajahan, di Maluku disebut Kolo. Tumbuhan ini dikenal tidak hanya sebagai tanaman yang bias dimakan, kebanyakan sebagai bumbu dan sebagai sumber obat-obatan tradisional (Judzentiene,A dan Buzelyte,J,2006) spesies tumbuhan ini diladang, pinggir jalan dan lokasi pembuangan sampah yang tumbuh subur dan menyebar.
Tumbuhan Baru Cina (Artemisia vulgaris L ) di masyarakat karo dikenal dengan tumbuhan Binara merupakan tanaman liar yang dianggap sebagai tanaman gulma yang tumbuh subur dapat menghambat pertumbuhan dari tanaman penghasil pada ladang–ladang pertanian. Tumbuhan ini adalah tumbuhan berwarna daun hijau dengan ketinggian berukuran 50-150 cm, berbunga dan tumbuh subur dilapangan terbuka (Gambar 2.1). Menurut masyarakat Karo, tumbuhan tersebut bermanfaat untuk mengobati nyeri haid, obat kuat, obat batuk, obat kejang, obat mulas, dan menambah nafsu makan (Anonim, 2012)
Gambar 2.1 Tumbuhan Baru Cina
Daun tumbuhan Binara (Artemisia vulgaris L) telah diteliti dimana diperoleh melalui hidrodestilasi dan dianalisis secara GC-MS ternyata dijumpai berbagai jenis komponen senyawa kimia yang terdiri dari monoterpen teroksigenasi, sesquiterpen dan senyawa sesquiterpen teroksigenasi (Bunrathep, dkk, 2005). Delapan puluh satu komponen diidentifikasi terbentuk sampai 81,9% - 96,8% dari total kandungan minyak. Senyawa monoterpen teroksigenasi sebanyak 17,1% dari hasil total kandungan minyak. Senyawa monoterpen teroksigenasi sebanyak 17,1% -48,7% sedangkan seskuiterpen 17,1% - 44,1% dari total kandungan minyak (Judzentiene dan Buzelyte, 2006).
Kandungan senyawa daun Artemisia vulgaris vul. Indica dari hasil destilasi bersama air adalah : monoterpen : 2,99%, monoterpen teroksigenasi : 10,46%, sesquiterpen : 6,70%, sesquiterpen teroksigenasi : 74,26%, dan yang lainnya 5,42% (Bunrathep, dkk, 2005).
2.2. Minyak Atsiri
Minyak atsiri yang dikenal dengan nama minyak terbang (volatile oil) atau minyak eteris (essensial oil) adalah minyak yang dihasilkan dari tanaman dan mempunyai sifat mudah menguap pada suhu kamar tanpa mengalami dekomposisi. Minyak atsiri merupakan salah satu hasil proses metabolisme dalam tanaman, yang terbentuk karena reaksi berbagai senyawa kimia dan air. Sifat dari minyak atsiri yang lain adalah mempunyai rasa getir (pungent taste), berbau wangi sesuai dengan bau tanaman penghasilnya, yang diambil dari bagian-bagian tanaman seperti daun, buah akar, biji, bunga, akar, rimpang, kulit kayu, bahkan seluruh bagian tanaman.
Minyak atsiri umumnya larut dalam pelarut organik seperti alkohol, petroleum, benzen, dan tidak larut dalam air (Ketaren, 1985). Kabanyakan minyak atsiri terbentuk bebas atau sebagai glukosa, karena adanya air dan enzim-enzim sehingga mengalami penguraian menjadi minyak atsiri.
Minyak atsiri bersifat mudah menguap karena titik uapnya rendah. Selain itu, susunan senyawa komponennya kuat mempengaruhi saraf manusia (terutama hidung) sehingga seringkali memberikan efek psikologis tertentu (baunya kuat). Setiap senyawa penyusun memiliki efek tersendiri, dan campurannya dapat menghasilkan rasa yang berbeda.
Secara kimiawi, minyak atsiri tersusun dari campuran yang rumit berbagai senyawa, namun suatu senyawa tertentu biasanya bergantung jawab atas suatu aroma tertentu. Sebagian besar minyak atsiri termasuk dalam golongan senyawa organik terpena dan terpenoid yang bersifat larut dalam minyak/ lipofil.
2.2.1. Penyulingan Minyak Atsiri
Minyak atsiri, minyak mudah menguap, atau minyak terbang merupakan campuran dari senyawa yang berwujud cairan atau padatan yang memiliki komposisi maupun titik didih yang beragam. Besarnya kandungan minyak atsiri pada setiap bagian tanaman berbeda-beda. Bila jumlah kelenjar minyak pada tanaman tersebut sedikit, minyak atsiri yang dihasilkannya juga sedikit. Penyulingan adalah proses pemisahan antara komponen cair atau padat dari dua macam campuran/ lebih berdasarkan perbedaan titik uapnya dan dilakukan untuk minyak atsiri yang tidak larut dalam air. Dalam industri minyak atsiri dikenal tiga metode penyulingan, yaitu:
a. Penyulingan dengan air (hydrodistillation)
Bila cara ini digunakan maka bahan yang akan disuling berhubungan langsung dengan air yang mendidih. Bahan yang akan disuling kemungkinan mengambang/ mengapung di atas air atau terendam seluruhnya. Air dapat dididihkan dengan api secara langsung. Sejumlah bahan tanaman adakalanya harus diproses dengan
penyulingan air (contoh bunga mawar, bunga-bunga jeruk) sewaktu terendam dan bergerak bebas dalam air mendidih.
b. Penyulingan dengan uap dan air (hydro and steam distillation)
Bahan tanaman yang akan diproses secara penyulingan uap dan air ditempatkan dalam suatu tempat yang bagian bawah dan tengah berlobang-lobang yang ditopang di atas dasar alat penyulingan. Bagian bawah alat penyulingan diisi air sedikit di bawah dimana bahan ditempatkan. Air dipanaskan dengan api seperti pada penyulingan air di atas.
c. Penyuliangan dengan uap (steam distillation)
Penyulingan uap disebut juga penyulingan tak langsung. Didalam proses penyulingan dengan uap ini, uap dialirkan melalui pipa uap berlingkar yang berpori dan berada si bawah bahan tanaman yang akan disuling. Kemudian uap akan bergerak menuju ke bagian atas melalui bahan yang disimpan di ats saringan (Lutony, 1994). Sistem penyulingan ini baik untuk mengekstraksi minyak dari biji-bijian, akar dan kayu-kayuan yang umumnya mengandung komponen minyak yang bertitik didih tinggi dan tidak baik dilakukan terhadap bahan yang mengandung minyak atsiri yang mudah rusak oleh pemanas dan air (Ketaren, 1985).
2.2.2. Komposisi Kimia Minyak Atsiri
Minyak atsiri umumnya terdiri dari campuran berbagai persenyawaan kimia yang terbentuk dari unsur-unsur kimia seperti karbon (C), hidrogen (H), oksigen (O), dan beberapa persenyawaan kimia yang mengandung unsur nitrogen (N), serta belerang (S). Guenther (1987) mengatakan bahwa minyak atsiri terutama terdiri dari persenyawaan kimia mudah menguap, termasuk golongan hidrokarbon asiklik dan hidrokarbon isosiklik serta turunan hidrokarbon yang telah mengikat oksigen.
Menurut Ketaren (1985) umumnya komponen kimia minyak atsiri dibagi menjadi 2 golongan yaitu hidrokarbon dan hidrokarbon beroksigen. Jenis hidrokarbon yang terdapat dalam minyak atsiri sebagian besar terdiri dari monoterpen,
sesquiterpen, diterpen, dan politerpen, serta parafin, olein dan hidrokarbon aromatik. Disamping itu minyak atsiri mengandung resin dan lilin dalam jumlah kecil. Resin dan lilin merupakan komponen yang tidak mudah menguap. Minyak atsiri memiliki struktur molekul yang kompleks yang terdiri dari semua jenis atom, termasuk hidrogen, oksigen, dan karbon serta nitrogen bahkan belerang.
2.2.3. Kegunaan Minyak Atsiri
Penggunaan minyak atsiri pada makanan sebagai penambah aroma dan penambah rasa. Dalam pembuatan makanan olahan, tidak jarang bahan yang digunakan hanya sedikit menggunakan bahan utama. Oleh karena itu, kehadiran minyak atsiri dapat memperkuat aroma dan rasa sehingga produk makanan serasa memiliki citarasa yang tidak kalah dengan produk asilnya. Minyak atsiri merupakan sumber dari aroma kimia alami yang dapat digunakan sebagai komponen flavor dan fragrance alami dan sebagai sumber yang penting dari struktur stereospesifik enansiomer murni yang biosintesisnya lebih mudah dibandingkan dengan proses sintesis.
Minyak atsiri digunakan sebagai bahan baku dalam berbagai industri, misalnya industri parfum, kosmetik, dan industri farmasi. Dalam pembuatan parfum dan wangi-wangian, minyak atsiri tersebut berfungsi sebagai zat pengikat bau (fixative) dalam parfum, misalnya minyak nilam, minyak akar wangi dan minyak lada, minyak kayu manis, minyak jahe, minyak cengkeh, minyak ketumbar, umumnya digunakan sebagai bahan penyedap (flavouring agent) dalam bahan pangan dan minuman (Ketaren, 1985).
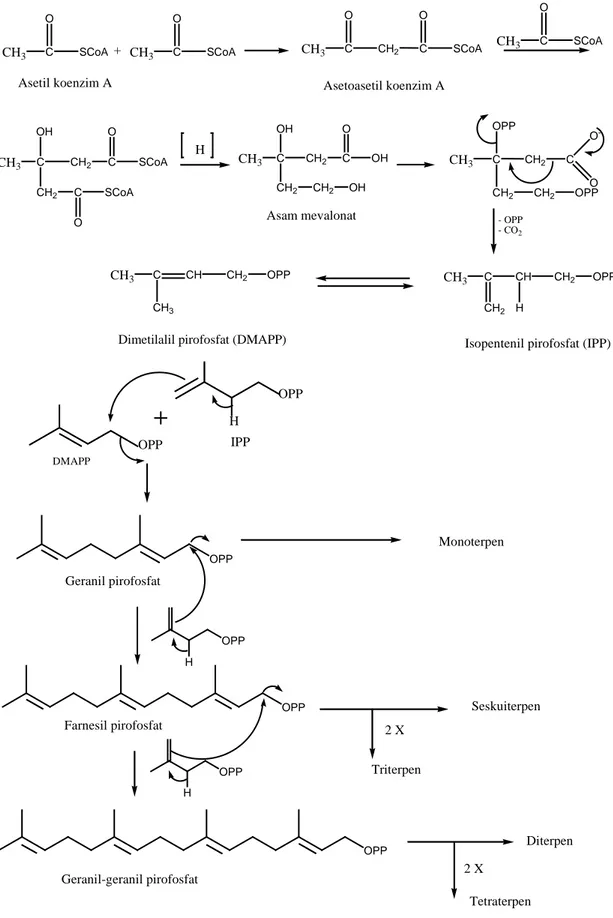
2.2.4. Biosintesa Pembentukan Minyak Atsiri
Berdasarkan proses biosintesisnya atau pembentukan komponen minyak atsiri di dalam tumbuhan, minyak atsiri dapat dibedakan menjadi dua golongan. Golongan pertama adalah turunan terpena yang terbentuk dari asam asetat melalui jalur biosintesis asam mevalonat. Golongan kedua adalah senyawa aromatik yang terbentuk
dari biosintesis asam sikimat melalui jalur fenil propanoid (Agusta, 2000). Mekanisme dari tahap-tahap reaksi biosintesis terpenoid yaitu asam asetat yang telah diaktifkan oleh koenzim A melakukan kondensasi jenis Claisen menghasilkan asam asetoasetat. Senyawa yang dihasilkan ini dengan asetil koenzim A melakukan kondensasi jenis aldol menghasilkan rantai karbon bercabang sebagaimana ditemukan pada asam mevalonat. Reaksi-reaksi berikutnya ialah fosforilasi, eliminasi asam fosfat dan dekarboksilasi menghasilkan IPP yang selanjutnya berisomerisasi menjadi DMAPP oleh enzim isomerase. IPP sebagai unit isopren aktif bergabung secara kepala ke ekor dengan DMAPP dan penggabungan ini merupakan langkah pertama dari polimerisasi isopren untuk menghasilkan terpenoid. Penggabungan ini terjadi karena serangan elektron dari ikatan rangkap IPP terhadap atom karbon dari DMAPP yang kekurangan elektron diikuti oleh penyingkiran ion pirofosfat. Serangan ini menghasilkan geranil pirofosfat (GPP) yakni senyawa antara bagi semua senyawa monoterpen.
Sintesa terpenoid sangat sederhana sifatnya. Ditinjau dari segi teori reaksi organik sintesa ini hanya menggunakan beberapa jenis reaksi dasar. Reaksi-reaksi selanjutnya dari senyawa antara GPP, FPP, dan GGPP untuk menghasilkan senyawa-senyawa terpenoid satu per satu hanya melibatkan beberapa jenis reaksi sekunder pula. Reaksi-reaksi sekunder ini lazimnya adalah hidrolisa, siklisasi, oksidasi, reduksi, dan reaksi-reaksi spontan yang dapat berlangsung dengan mudah dalam suasana netral dan pada suhu kamar, seperti isomerisasi, dehidrasi, dekarbosilasi, dan sebagainya
CH3 C SCoA O CH3 C SCoA O + CH3 C O CH2 C O SCoA CH3 C SCoA O
Asetil koenzim A Asetoasetil koenzim A
CH3 C OH CH2 C O SCoA CH2 C SCoA O H CH3 C OH CH2 CH2 OH CH2 C O OH CH3 C OPP CH2 C O O -Asam mevalonat CH2 CH2 OPP - OPP - CO2 CH3 C CH CH2 H CH2 OPP
Isopentenil pirofosfat (IPP)
CH3 C
CH3
CH CH2 OPP
Dimetilalil pirofosfat (DMAPP)
OPP OPP H IPP DMAPP OPP Monoterpen Geranil pirofosfat OPP H OPP Farnesil pirofosfat Seskuiterpen 2 X Triterpen OPP H OPP Diterpen 2 X Tetraterpen Geranil-geranil pirofosfat
2.3. Analisa Komponen Minyak Atsiri
Analisis terhadap minyak atsiri menggunakan GC-MS, dimana GC-MS merupakan metode pemisahan senyawa organik yang menggunakan dua metode analisis yaitu kromatografi gas (GC) untuk menganalisis jumlah senyawa secara kuantitatif dan spektrometri massa (MS) untuk menganalisis struktur molekul senyawa analit.
Peningkatan penggunaan GC-MS banyak digunakan yang dihubungkan dengan komputer dimana dapat merekam dan menyimpan data dari sebuah analisis akan berkembang pada pemisah yang lebih efesien. Karena komputer dapat diprogram untuk mencari spektra library yang langka, membuat indentifikasi dan menunjukkan analisis dari campuran gas tersebut.
2.3.1. Kromatografi Gas
Kromatografi adalah metode fisika untuk pemisahan, dalam mana komponen-komponen yang akan dipisahkan didistribusikan antara dua fase, salah satunya merupakan lapisan stasioner dengan permukaan yang luas, dan fase yang lain berupa zat alir (fluid) yang mengalir lambat (perkolasi) menembus atau sepanjang lapisan stasioner itu. Fase stasioner dapat berupa zat padat atau cairan, dan fase geraknya dapat berupa cairan atau gas (Underwood, 1989).
Dalam kromatografi gas, fase bergeraknya adalah gas dan zat terlarut terpisah sebagai uap. Pemisahan tercapai dengan partisi sampel antara fase gas bergerak dan fase diam berupa cairan dengan titik didih tinggi (tidak mudah menguap) yang terikat pada zat padat penunjangnya (Khopkar, 2003).
2.3.1.1. Cara Kerja Kromatografi Gas
Sampel diinjeksikan melalui suatu sampel injection port yang temperaturnya dapat diatur, senyawa-senyawa dalam sampel akan menguap dan akan dibawa oleh gas pengemban menuju kolom. Zat terlarut akan teradsorpsi pada bagian atas kolom oleh
fase diam, kenudian akan merambat dengan laju rambatan masing-masing komponen yang sesuai dengan nilai koefisien partisi masing-masing komponen tersebut. Komponen-komponen tersebut terelusi sesuai dengan urut-urutan makin membesarnya nilai koefisisen partisi menuju ke detektor. Detektor mencatat seluruh sederetan sinyal yang timbul akibat perubahan konsentrasi dan perbedaan laju elusi. Pada alat pencatat sinyal ini akan tampak sebagai kurva antara waktu terhadap komposisi aliran gas pembawa.
Ada beberapa kelebihan kromatografi gas, diantaranya kita dapat menggunakan kolom lebih panjang untuk menghasilkan efisiensi pemisahan yang tinggi. Gas dan uap mempunyai viskositas yang rendah, demikian juga kesetimbangan partisi antara gas dan cairan berlangsung cepat, sehingga analisis relatif cepat dan sensitivitasnya tinggi. Fase gas dibandingkan fase cair tidak bersifat reaktif terhadap fase diam dan zat-zat terlarut. Kelemahannya adalah teknik ini terbatas untuk zat yang mudah menguap (Khopkar, 2003).
2.3.1.2. Instrumentasi Kromatografi Gas
Kromatografi terdiri dari komponen-komponen penting, yaitu:
1. Regulator tekanan : tekanan diatur pada 4 atmosfer, sedangkan aliran diatur 1-1000 liter gas per menit. Katup pengatur aliran diatur oleh pengatup berbentuk jarum terletak pada bagian bawah penunjuk aliran. Sebelum kolm, gas pengemban dialirkan dulu pada suatu silinder berisi molekular sieve untuk menyaring adanya kontaminasi pengotor. Gas pembawa He, N2, Ar, umumnya digunakan, tetapi untuk
detektor konduktivitas termal, He lebih disukai karena konduktivitas termalnya yang tinggi.
2. Sistem injeksi sampel : sampel diinjeksikan dengan suatu macro syringe melalui suatu septum karte silicon ke dalam kotak logam yang panas. Kotak logam tersebut dipanaskan dengan pemanas listrik. Banyaknya sampel berkisar antara 0,5-10 µl. 3. Kolom kromatografi : terbuat dari tabung yang dibuat berbentuk spiral terbuka.
Baja tahan karat digunakan untuk tabung kolom kromatografi bila bekerja pada temperatur tinggi. Diameter kolom bervariasi dari 1/16 sampai 3/16. Panjang umumnya adalah 2 meter.
4. Penunjang stasioner : struktur dan sifat permukaan memegang peranan penting. Struktur berperan pada efisiensi kolom, sedangkan sifat permukaan menentukan tingkat pemisahan. Permukaan penunjang akan terselimuti oleh fase cair stasioner berupa lapisan film tipis. Penunjang yang sering digunakan adalah tanah diatomaeus.
5. Fase stasioner : salah satu keunggulan kromatografi gas cair terletak pada variasi fase cair untuk partisi yang dapat tersedia dalam jumlah tidak terbatas. Temperatur maksimum yang dapat diperlakukan terhadap suatu kolom ditentukan oleh penguapan fase stasioner. Banyaknya fase stansioner suatu kolom dinyatakan dengan persen berat.
6. Detektor : peka terhadap komponen-komponen yang terpisahkan di dalam kolom serta mengubah kepekaannya menjadi sinyal listrik. Kuat lemahnya sinyal bergantung pada laju aliran massa sampel dan bukan pada konsentrasi sampel gas penunjang.
7. Pencatat sinyal : akurasi suatu kromatogram pada suatu daerah pembacaan ditentukan oleh pemilihan pencatat sinyalnya (Khopkar, 2003).
2.3.2. Spektrometri Massa
Penggunaan spektrometri massa luas dalam kimia organik sejak 1960. Ada dua alasan utama penggunaan spektrometri massa, pertama telah ditemukan alat yang dapat mengguapkan hampir semua senyawa organik dan mengionkan uap; kedua, fragmen bermuatan yang dihasilkan dari ion molekul dapat dihubungkan dengan struktur molekulnya (Sudjadi, 1983).
Spekrometer massa menembaki bahan yang sedang diteliti dengan berkas elektron dan serta kuantitatif mencatat hasilnya sebagai suatu spektrum fragmen ion positif. Terpisahnya fragmen ion positif didasarkan pada massanya. Spektrometer massa biasa diambil pada energi berkas elektron sebesar 70 elektron volt. Kejadian tersederhana adalah tercampaknya satu elektron dari molekul dalam fasa gas oleh sebuah elektron dalam berkas elektron dam membentuk suatu kation radikal (M )
Satu proses yang disebabkan oleh tabrakan elektron pada kamar pengion spektrometer massa adalah ionisasi dari molekul yang berupa uap dengan kehilangan satu elektron dan terbentuk ion molekul bermuatan positif, karena molekul senyawa organik mempunyai elektron berjumlah genap maka proses pelepasan satu elektron menghasilkan ion radikal yang mengandung satu elektron tidak berpasangan.
M M
Proses lain, molekul yang berupa uap tersebut menangkap sebuah elektron membentuk ion radikal bermuatan negatif dengan kemudian terjadi jauh lebih kecil (10-2) dari pada ion radikal bermuatan positif (Sudjadi, 1983).
Dalam spektrometer massa, reaksi pertama suatu molekul adalah ionisasi awal-abstraksi (pengambilan) sebuah elektron. Hilangnya sebuah elektron menghasilkan ion molekul. Dari peak untuk radikal ion ini, yang biasanya adalah peak yang paling kanan dalam spektrum, bobot molekul senyawa itu dapat ditentukan (Fessenden, 1986)
Suatu spektrum massa menyatakan massa-massa sibir-sibir bermuatan positif terhadap kepekaan (konsentrasi) nisbinya. Puncak palingkuat (tertinggi) pada spektrum disebut puncak dasar (base peak), dinyatakan dengan nilai 100% dan molekulnya, dinyatakan sebagai presentase puncak dasar tersebut. Puncak ion molekul biasanya merupakan puncak-puncak dengan bilangan massa tertinggi, kecuali jika terdapat puncak-puncak isotop. Puncak-puncak isotop ada karena sejumlah molekul tertentu mengandung isotop lebih berat dari pada isotopnya yang biasa (Silverstein, 1981).
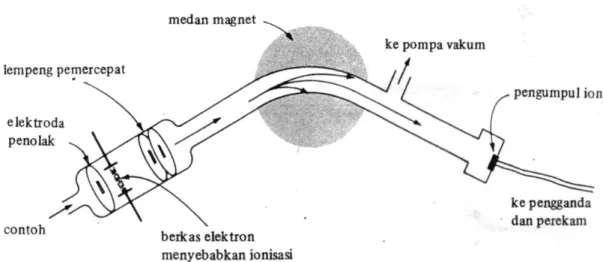
2.3.2.1. Instrumentasi Spektrometer Massa
Bagian-bagian utama suatu spektrometer massa terdiri dari tempat menginjeksikan sampel, ruangan pengion, pengumpul ion, penguat sinyal dan pencatat. Sampel diuapkan dan didorong ke dalam ruang pengion. Fungsi dari penganalisis massa adalah menguraian partikel-partikel. Kemudian molekul-molekul sampel terionisasi baik secara langsung ataupun tidak langsung oleh arus elektron sehingga menghasilkan ion positif, dan molekul-molekul dipisahkan dalam bentuk
ion-ionnya. Ion-ion positif masuk kedalam daerah penganalisis massa. Kemudian partikel yang bergerak cepat diberi medan magnit yang kuat, sehingga lintasannya menjadi lengkung. Jari-jari lengkung lintasan tergantung dari kecepatan dan kekuatan medan magnit. Partikel-partikel dengan massa yang berbeda difokuskan ke suatu celah ke luar dengan cara memvariasikan potensial akselerasi atau kekuatan medan magnit. Ion-ion yang melewati celah akan diterima oleh elektroda pengumpul. Arus ion yang dihasilkan diperkuat dan dicatat sebagai fungsi kuat medan atau potensial akselerasi (Khopkar, 2003).
1. Sistem penanganan sampel
Bagian ini berfungsi mengubah sampel agar mempunyai bentuk gas pada tekanan rendah dan reprodusibel. Untuk sampel yang tidak mudah menguap, diperlukan pemanas asalkan senyawa tersebut stabil secara termal. Senyawa-senyawa tidak mudah menguap dan tidak stabil secara termal dimasukkan ke dalam kamar pengion dengan bantuan probe sampel yang dilengkapi pemanas yang dapat menguapkan sampel tekanan rendah.
2. Sumber ion
Di sini molekul-molekul diubah menjadi ion dalam bentuk gas. Cara yang umum untuk menghasilkan ion-ion meliputi penembakan sampel dengan berkas elektron berenergi tinggi yang berasal dari suatu ion gun. Pada cara elektron impact, tumbukan dengan electron menyebabkan fragmentasi molekul-molekul yang membentuk sejumlah ion-ion positif dari berbagai massa. Pada cara chemical ionization memberikan fragmentasi lebih sederhana. Pada cara nyala, pembentukan ion dari sampel anorganik yang tidak mudah menguap dilakukan dengan cara nyala. Pada cara ionisasi medan dipakai anoda dan katoda untuk mendapat fragmentasinya.
3. Penganalisis massa
Ini adalah susunan alat-alat yang berguna untuk memisahkan ion-ion dengan perbandingan massa terhadap muatan yang berbeda-beda. Penganalisis massa harus dapat membedakan selisih massa yang kecil serta dapat menghasilkan arus ion yang tinggi (Khopkar, 2003).
4. Pengumpul ion
Terdiri dari satu celah atau lebih dan silinder Faraday. Berkas ion membentuk tegak lurus pada plat pengumpul dan isyarat yang timbul diperkuat dengan pelipat ganda elektron (Sudjadi, 1983).
5. Pencatat
Spektrum massa biasanya dibuat dari massa rendah ke massa tinggi. Pencatat yang banyak digunakan mempunyai 3-6 galvanometer yang mencatat secara bersama-sama pada kertas fotografi. Galvanometer menyimpang jika ada ion menabrak lempeng pengumpul, berkas sinar ultraviolet dapat menimbulkan berbagai puncak pada kertas pencatat yang peka terhadap sinar ultraviolet (Sudjadi, 1983).
Gambar 2.3 Diagram Spektrometer massa
2.4. Bakteri
Bakteri merupakan penghasil bermacam-macam zat organik dan obat-obatan antibiotik. Mikroorganisme memang peranan penting dalam menganalisis sistem enzim dan dalam mengalisis komposisi suatu makanan. Bakteri merupakan organisme yang sangat kecil (berukuran mikroskopis). Bakteri rata-rata berukuran lebar 0,5 – 1 mikron dan panjang hingga 10 mikron (1 mikron - 103 mm). Untuk melihat bakteri dengan jelas, tubuhnya perlu diisi dengan zat warna, pewarna ini disebut pengecatan bakteri (K. Irianto, 2006)
Ada kalanya suatu bakteri perlu diwarnai dua kali. Setelah zat warna yang pertama (ungu) terserap, maka bakteri dicuci dengan alkohol, kemudian ditumpangi dengan zat warna berlainan, yaitu dengan zat warna merah. Zat warna tambahan terhapus, sehingga yang nampak adalah zat asli (ungu). Dalam hal ini bakteri disebut
Gram Positif. Jika zat warna tambahan merah yang bertahan sehingga zat warna asli tidak tampak, dalam hal ini bakteri disebut Gram Negatif.
2.4.1. Bakteri Gram Positif
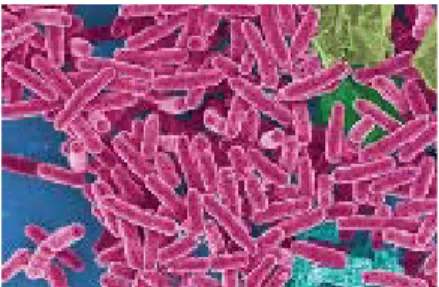
2.4.1.1. Basillus subtilis
Berbentuk batang dan membentuk spora. Sering menimbulkan permasalahan pada industri pengalengan karena sporanya sangat tahan terhadap panas. Basillus antracis menyebabkan penyakit anthrax pada manusia dan hewan, B.subtilis (B.mesentericus) menyebabkan suatu tipe kerusakan yang disebut dengan ropiness pada roti, dan B.cereus dapat menyebabkan keracunan pangan (Gaman, 1992).
Gambar 2.4. Basillus subtilis 2.4.1.2. Pseudomonas aeruginosa
Pseudomonas merupakan salah satu jenis dalam kelompok ini yang sering menimbulkan kebusukan makanan. Pertumbuhan pada kondisi aerobik berjalan cepat, dan biasanya membentuk lendir. Kebanyakan Pseudomonas, kecuali P. Syringe, bersifat oksidase positif, dan akan membentuk warna biru jika ditambah senyawa dimetil-p-fenilenediamin dihidroklorida. Tidak tahan terhadap panas dan keadaan kering. Oleh karena itu, mudah dibunuh dengan proses pemanasan dan pengeringan (Fardiaz, 1992).
2.4.2. Bakteri Gram Negatif
2.4.2.1. Escherichia coli
Escherichia berbatang pendek. Habitat utamanya adalah usus manusia dan hewan. Escherichia coli dipakai sebagai organisme indikator, karena jika terdapat dalam jumlah yang banyak menunjukkan bahwa pangan atau air telah mengalami pencemaran (Gaman, 1992).
Gambar 2.6. Escherichia coli
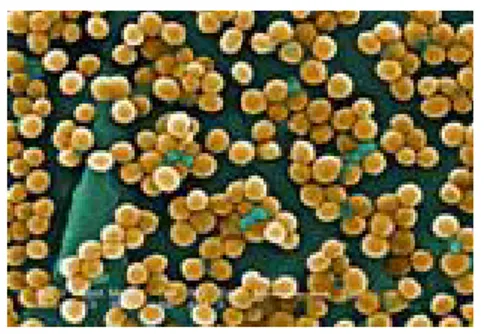
2.4.2.2. Staphylococcus aureus
Staphylococcus merupakan bakteri berbentuk bulat yang terdapat dalam bentuk tunggal, berpasangan, tetrad, atau berkelompok seperti anggur. Beberapa spesies memproduksi pigmen berwarna kuning sampai oranye, misalnya S. Aureus. Bakteri ini menbutuhkan nitrogen organik (asam amino) untuk pertumbuhannya, dan bersifat anaerobik fakultatif.
2.5. Antioksidan
2.5.1. Pengertian Antioksidan
Antioksidan merupakan senyawa pemberi elektron (electron donor) atau reduktan. Senyawa ini memiliki berat molekul kecil, tetapi mampu mengaktivasi berkembangnya reaksi oksidasi, dengan cara mencegah terbentuknya radikal. Antioksidan dapat diperoleh,
1. Dari luar tubuh (eksogen) dengan cara melalui makanan dan minuman yang mengandung vitamin C, E, atau betakaroten.
2. Dari dalam tubuh (endogen), yakni dengan enzim superoksida dismutase (SOD), gluthatione, perxidasi, dan katalase yang diproduksi oleh tubuh sebagai antioksidan.
2.5.2. Penggolongan Antioksidan
Antioksidan dapat digolongkan berdasarkan fungsinya, yaitu: 1. Primary Antioxidants (Antioksidan Utama / Antioksidan Primer)
Termasuk di sini:
- SOD (Superoxide Dismutase) - GPx (Glutathion Peroxidase)
- Metalbinding protein seperti Ferritin atau Ceruloplasmin.
Antioksidan primer ini bekerja untuk mencegah terbentuknya senyawa radikal bebas baru. Ia mengubah radikal bebas yang ada menjadi molekul yang berkurang dampak negatifnya, sebelum radikal bebas ini sempat bereaksi. Contoh Antioksidan ini adalah enzim SOD yang berfungsi sebagai pelindung hancurnya sel-sel dalam tubuh serta mencegah proses peradangan karena radikal bebas. 2. Secondary Antioxidants (Antioksidan Kedua/ Antioksidan Sekunder)
Antioksidan ini berfungsi menangkap senyawa serta mencegah terjadinya reaksi berantai. Contoh: antioksidan sekunder : vitamin E, vitamin C, betakaroten, asam urat, bilirubin dan albumin.
3. Tertiary antioxidants (Antioksidan Ketiga / Antioksidan Tersier)
Antioksidan jenis ini memperbaiki kerusakan sel-sel dan jaringan yang disebabkan radikal bebas. Contoh enzim yang memperbaiki DNA pada inti sel adalah metionin sulfoksidan reduktase. Adanya enzim-enzim perbaikan DNA ini berguna untuk mencegah penyakit misalnya kanker (Kosasih, 2004)
Senyawa antioksidan berperan penting dalam pertahanan tubuh terhadap pengaruh buruk yang disebabkan radikal bebas. Radikal bebas diketahui dapat menginduksi penyakit kanker, arteriosklerosis dan penuan, disebabkan oleh kerusakan jaringan karena oksidasi.
Radikal bebas adalah merupakan atom atau gugus atom apa saja yang memiliki satu atau lebih elektron tak berpasangan. Karena jumlah elektron ganjil, maka tidak semua elektron dapat berpasangan sehingga bersifat sangat reaktif . Jika jumlahnya sedikit, radikal bebas dapat dinetralkan oleh sistem enzimatik tubuh, namun jika berlebih akan memicu efek patologis Radikal bebas merupakan merupakan agen pengoksidasi kuat yang dapat merusak sistem pertahanan tubuh dengan akibat kerusakan sel dan penuaan dini karena elektron yang tidak berpasangan selalu mencari pasangan elektron dalam makromolekul biologi, Protein lipida dan DNA dari sel manusia yang sehat lah merupakan sumber pasangan elektron yang baik.