Informasi Dokumen
- Penulis:
- Abdurrouf
- Pengajar:
- Triyuni Kurniawati, S.Ag., M.Pd.
- Sekolah: Universitas Brawijaya
- Mata Pelajaran: Fisika
- Topik: Buku Ajar Fisika Inti MAP4217: Fisika Inti: Teori dan Penerapannya
- Tipe: buku ajar
- Tahun: 2015
- Kota: Malang
Ringkasan Dokumen
I. Mengenal Inti
Bagian ini memberikan pengantar tentang inti atom, termasuk sejarah penemuan inti dan partikel penyusunnya. Ditekankan bahwa inti terdiri dari proton dan neutron, serta pentingnya memahami struktur dan sifat inti dalam konteks fisika modern. Penjelasan mengenai eksperimen Geiger-Marsden yang menunjukkan keberadaan inti atom menjadi fondasi dari teori inti saat ini. Sejarah ini penting untuk memberikan konteks kepada mahasiswa tentang bagaimana pengetahuan fisika inti berkembang.
1.1 Sejarah Penemuan Inti
Sejarah penemuan inti dimulai dengan model atom Rutherford yang menyatakan bahwa sebagian besar massa atom terkonsentrasi di pusatnya, yang disebut inti. Eksperimen Geiger dan Marsden menunjukkan bahwa partikel alfa dapat dipantulkan, yang mengarah pada pemahaman bahwa atom memiliki struktur yang lebih kompleks dari yang diperkirakan sebelumnya. Ini menjadi dasar bagi pengembangan lebih lanjut dalam fisika inti.
1.2 Partikel Penyusun Inti
Inti terdiri dari proton dan neutron, dengan proton memiliki muatan positif dan neutron tidak bermuatan. Model proton-elektron yang awalnya diajukan mengalami banyak tantangan, seperti ketidakcocokan dengan data eksperimen mengenai spin dan momen magnetik. Ini mengarah pada pengembangan model proton-neutron yang lebih akurat dalam menjelaskan struktur inti.
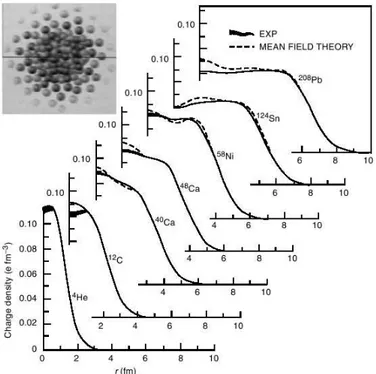
1.3 Dimensi, Massa, dan Energi Inti
Pembahasan mengenai dimensi inti menunjukkan bahwa jari-jari inti berbanding lurus dengan A^(1/3). Massa inti yang lebih kecil dari jumlah massa penyusun menunjukkan adanya energi ikat, yang merupakan energi yang diperlukan untuk memisahkan inti. Energi ini penting untuk memahami stabilitas inti dan reaksi nuklir.
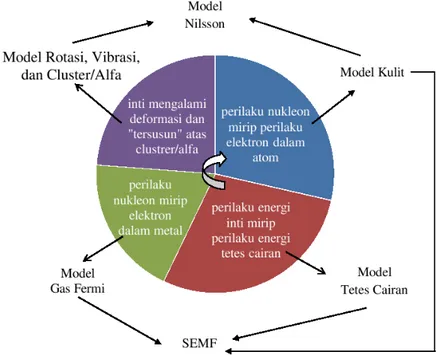
II. Model Inti Klasik
Bagian ini membahas berbagai model inti klasik, termasuk model tetes cairan yang menganggap inti sebagai tetes cairan dengan sifat-sifat tertentu. Model ini membantu menjelaskan beberapa fenomena inti, meskipun tidak dapat menjelaskan semuanya. Penjelasan tentang model ini penting untuk memahami bagaimana fisikawan mencoba menggambarkan perilaku inti dan interaksi antar nukleon.
2.1 Perlunya Model Inti
Model inti diperlukan untuk menjelaskan fenomena yang diamati dalam eksperimen, seperti energi ikat dan kestabilan inti. Dua pendekatan utama dalam pemodelan ini adalah pendekatan kolektif dan independen, yang masing-masing memiliki kelebihan dan kekurangan dalam menjelaskan perilaku inti.
2.2 Model Tetes Cairan
Model tetes cairan diusulkan untuk menggambarkan inti sebagai tetes cairan homogen yang terdiri dari nukleon. Model ini berhasil menjelaskan beberapa sifat inti, seperti energi ikat per nukleon yang relatif konstan pada rentang massa tertentu. Namun, model ini juga memerlukan koreksi untuk faktor-faktor lain seperti efek permukaan dan gaya Coulomb.
III. Model Inti Kuantum
Bagian ini membahas perkembangan model inti kuantum yang lebih kompleks. Model ini menjelaskan perilaku inti dengan mempertimbangkan aspek kuantum dan interaksi antar nukleon. Pemahaman tentang model ini sangat penting bagi mahasiswa untuk memahami fisika inti secara mendalam.
3.1 Model Kulit
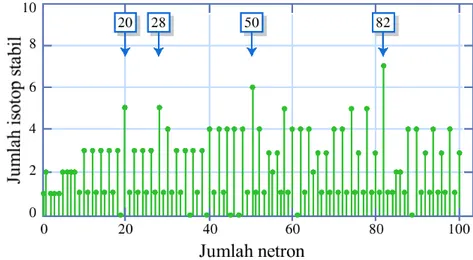
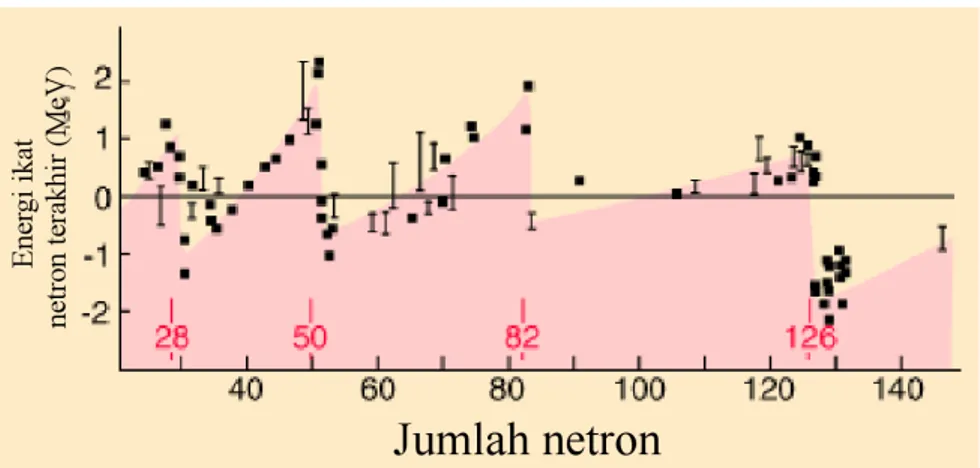
Model kulit menggambarkan distribusi energi dalam inti dan menjelaskan bagaimana nukleon terdistribusi dalam tingkat energi. Model ini membantu menjelaskan fenomena seperti kestabilan inti berdasarkan bilangan ajaib dan konfigurasi nukleon.
IV. Gaya Antar Nukleon
Bagian ini menjelaskan berbagai gaya yang beroperasi antar nukleon, termasuk gaya nuklir kuat dan gaya elektrostatik. Pemahaman tentang gaya-gaya ini penting untuk memahami interaksi dalam inti dan stabilitasnya.
4.1 Deuteron
Deuteron sebagai contoh inti sederhana menunjukkan bagaimana gaya antar nukleon berperan dalam stabilitas inti. Analisis energi ikat dan interaksi antar nukleon memberikan wawasan tentang bagaimana inti terbentuk dan bertahan.
V. Peluruhan Radioaktif
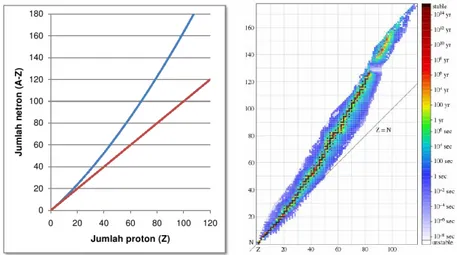
Peluruhan radioaktif adalah proses di mana inti yang tidak stabil kehilangan energi dengan memancarkan radiasi. Bagian ini membahas berbagai jenis peluruhan, mekanisme yang mendasarinya, dan bagaimana proses ini dapat diprediksi secara matematis.
5.1 Jenis Peluruhan dan Penyebabnya
Ada beberapa jenis peluruhan, termasuk peluruhan alfa, beta, dan gamma. Setiap jenis peluruhan memiliki karakteristik unik dan dipengaruhi oleh struktur inti serta gaya antar nukleon.
VI. Reaksi Inti
Bagian ini membahas reaksi inti, termasuk fisi dan fusi, serta energi yang terlibat dalam proses tersebut. Memahami reaksi inti penting untuk aplikasi dalam fisika nuklir dan teknologi energi.
6.1 Mengenal Reaksi Inti
Reaksi inti melibatkan perubahan dalam struktur inti, yang dapat menghasilkan energi dalam jumlah besar. Penjelasan tentang klasifikasi reaksi inti dan energetika memberikan konteks penting bagi mahasiswa.
Referensi Dokumen
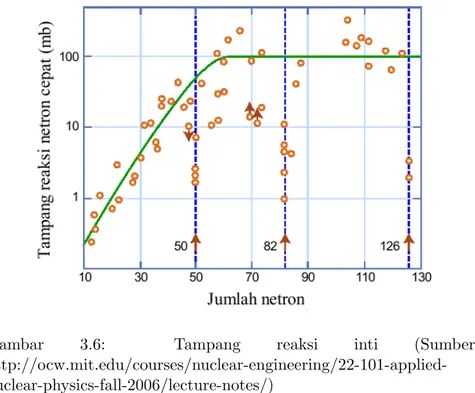
- Pengukuran tampang reaksi neutron cepat pada bahan struktur Mg, Si, V, Fe, Cu, dan Zr ( Abdurrouf )
- The Principles of Nuclear Magnetism ( Abragam, A )
- Gamma Radiation ( Adrovic, Feriz (ed.) )
- Advanced Course in Modern Nuclear Physics ( Arias, J. and M. Lozano )
- Fundamentals in Nuclear Physics: From Nuclear Structure to Cosmology ( Basdevant, J.L., J. Rich, and M. Spiro )
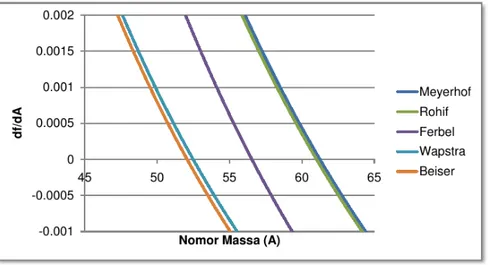
![Gambar 2.10: Plot energi sebagai fungsi Z, untuk A = 135. Ku- Ku-rva hampiran didapatkan dengan menggunakan Persamaan (2.8), se-dang nilai eksperimen didapatkan dengan menggunakan persamaan E (A, Z) = [M (A, Z) − Zm e ] c 2 , di mana M (A, Z) adalah berat](https://thumb-ap.123doks.com/thumbv2/123dok/2694805.2259981/60.659.73.564.70.413/hampiran-didapatkan-menggunakan-persamaan-eksperimen-didapatkan-menggunakan-persamaan.webp)