SCI
Rekayasa Genetika pada Zebrafish (
Denio rerio)
Sebagai Bio Indikator
dan Bio Medis
Rina Noviana 1ax
Jurusan Tadris IPA Biologi, IAIN Syekh Nurjati Cirebon, Jawa Barat, 45132, Indonesia
xCorresponding author: Jalan Perjuangan By pass, Sunyarangi, Kesambi, Kota Cirebon, Jawa Barat ,45132,
Indonesia. E-mail addresses: [email protected]
This study aims to determine This research is useful to know Genetic Engineering in Zebrafish (Denio rerio) as Bio Indicator and Bio Medical. Genetic engineering techniques continue to experience the development and refinement of methods before methods. Techniques carried out in this engineering by injecting the gene color of the
jellyfish to produce zebra fish that fluoresce as expected. Zebra fish (Danio rerio) is a
monophyletic species in Indonesia Cyprinidae family, zebra fish can be used as an indicator for natural pollutants and can be used as biomedical of certain diseases. .
Penelitian ini bertujuan untuk mengetahui Rekayasa Genetika pada Zebrafish (Denio
rerio) Sebagai Bio Indikator dan Bio Medis. Teknik rekayasa genetika terus-menerus mengalami perkembangan dan penyempurnaan dari metode-metode sebelumnya. Teknik yang dilakukan dalam rekayasa ini dengan menyuntikan gen warna ubur-bur sehingga
menghasilkan ikan zebra yang berpendar sesuai yang diharapkan. Ikan zebra (Danio
rerio) adalah spesies monofiletik di Indonesia keluarga Cyprinidae, ikan zebra ini dapat dijadikan sebagai indikator untuk polutan alam dan dapat dijadikan biomedis penyakit tertentu.
2017 Scientiae Educatia: Jurnal Pendidikan Sains. All rights reserved
1. Pendahuluan/Introduction
Bioteknologi didefinisikan sebagai organisme biologi molekuler, yang digunakan di industri produksi. Istilah ini mencakup proses yang digunakan selama berabad-abad, seperti produksi alkohol, dan juga penemuan di tahun-tahun terakhir rekayasa genetika [30, 40, 46] (Stryjewska, 2013). Teknik rekayasa genetika terus-menerus mengalami perkembangan dan penyempurnaan dari metode sebelumnya. Adapun metode-metode yang telah berhasil diterapkan dalam teknologi transfer gen antara lain adalah mikroinjeksi, elektroporasi, dan transfeksi. Keberhasilan transfer gen menggunakan
Scientiae Educatia: Jurnal Pendidikan Sains (2017) DOI:
keberhasilan tinggi, dan tidak bersifat toksik terhadap embrio. Namun demikian, umur embrio yang digunakan sama dengan metode transfer gen lainnya. Produksi hewan hasil rekayasa genetika (GM) adalah teknik yang berpotensi berdampak pada industri peternakan dan farmasi (Mora, C. et al, 2012).
Seperti keberhasilan menghasilkan ikan hias transgenik melalui biologi molekuler dengan karakter keunggulan tertentu memberikan harapan baru dalam budidaya ikan khususnya dalam menunjang peningkatan kualitas warna dan bentuk. Meskipun rekayasa genetika bukan segala-galanya, karena adanya keterbatasan dalam menghasilkan ikan transgenik seperti badan yang bengkok, kepala bercabang, dan lain-lain (Kusrini, 2012).
Danio rerio (awalnya Brachydanio rerio) ikan zebra atau zebrafish dijelaskan dalam
buku mengenai ikan di Sungai Gangga oleh seorang Dokter dari Inggris Sir Francis Hamilton (Hamilton 1822). Hamilton mengidentifikasi 10 spesies; Sekarang jumlahnya
ada 45 spesies yang diketahui dalam genus Danio. D. rerio adalah spesies monofiletik di
Indonesia keluarga Cyprinidae, yang ditandai dengan sirip ekor bilobate, dan merupakan anggota ikan bersirip sinar di infraclass Teleosti, yang mencakup lebih dari 26.000 spesies
yang masih ada (Fang et al. 2009). D. rerio merupakan ikan air tawar tropis yang tinggal di
Indonesia seperti di sungai kecil, sungai besar, sawah, dan saluran di Asia Selatan, termasuk India, Myanmar, Bangladesh, dan Nepal (Engeszer et al. 2007). Ikan ini bisa bertahan selama rentang 3-5 tahun (Spence et al., 2008). Ikan zebra adalah omnivora ikan ini biasa memakan zooplankton, serangga, larva serangga, dan fitoplankton. Cacing dan
beberapa krustasea kecil termasuk kedalam makanan favoritnya (Spence et al., 2008). Ikan
zebra mampu menghasilkan rata-rata 100-150 butir telur yang dijaga dengan ketat
dan dirawat oleh ikan jantan dan betina(Rahman, A. et al, 2012).
Zebrafish dapat meregenerasi sirip, jantung (Wade, 2010) dan kulit termasuk otak dan
mereka memiliki sel punca pada tahap larva. Yayasan Jantung Inggris di Tahun 2011 menyelidiki melalui penelitian tentang bagaimana fitur khusus ikan ini dapat dimanfaatkan mengurangi berbagai penyakit jantung manusia (Ganguly et al., 2012). Sementara sistem saraf mereka lebih sederhana dari pada mamalia, ikan zebra masih melakukan perilaku kompleks yang juga dimodulasi oleh sistem neurotransmiter pusat (Suckerman et al,. 2010).
(Green fluoroscent protein), YFP (Yellow fluoroscent protein), dan RFP (Red fluoroscent
protein) yang dapat terlihat pada kondisi cahaya biasa.
Glofish adalah zebrafish yang dimodifikasi secara genetik, atau Danio rerio yang
dimodifikasi secara genetik, yang telah diberi protein neon untuk diberikan kepada mereka penampilan yang bersinar dan penuh warna. Glofish ini awalnya dibuat untuk menguji air racun, dan mereka diprediksi akan bersinar saat menemukan adanya toksin. Glofish menjadi hewan peliharaan hasil modifikasi genetik pertama yang dijual ke masyarakat umum pada tahun 2003 (Barlow, H. K, 2012).
Selain dijadikan sebagai bio indikator lebih dari 30 tahun yang lalu, ikan air tawar kecil
Danio rerio menarik perhatian ilmuwan yang mencari hewan vertebrata yang mudah
ditangani namun kompleks untuk menganalisis fungsi gen yang dilestarikan. D. rerio lebih
dikenal dengan nama "zebrafish" untuk penampilan bergaris-garis, dan ini adalah model mapan untuk menantang isu-isu di berbagai bidang penelitian relevansi biomedis seperti penyakit kardiovaskular atau neurodegeneratif (Sasen, A. W & Koster, W. R, 2015).
2. Hasil dan Pembahasan
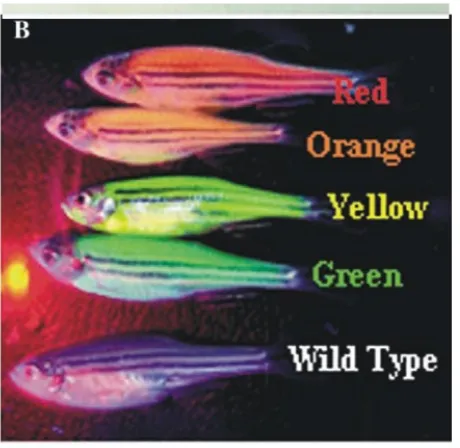
Ikan zebra (Danio rerio) biasanya berwarna perak dengan garis-garis hitam keunguan, dengan teknologi transgenik dapat memendarkan warna hijau atau merah pada tubuhnya (Gambar1). Warna tersebut diambil dari warna ubur-ubur yang disuntikan ke telur ikan zebra. Hasil rekayasa berwarna hijau karena gen warna yang disuntikan adalah GFP
(Green fluoroscentprotein) sehingga menghasilkan warna hijau yang berpendar pada ikan
zebra. Pola ekspresi GFP di ikan pukat zebrafish pasca-injeksi ke embrio selama 24 jam secara tidak merata dan di berbagai daerah embrio. Di bawah kondisi pengamatan ekspresi GFP akan menjadi sebuah indikator transformasi embrio yang baik ialah 67% (50-100%) embrio fluoresen menghasilkan ikan yang positif urutan transgen setelah analisis PCR. sesuai dengan fragmen yang disuntikkan (Gambar ). Ikan betina digunakan sebagai awal dari P1 untuk mendapatkan keturunan F1 di kawinkan ke laki-laki non transgenik. Transgen itu ditransmisikan ke 46% ikan F1 (Moraless, M. et al, 2001).
Gambar 2. Fragmen DNA (transgen) diinjeksikan ke dalam embrio zebrafish. Struktur cβ transgen p-chrtiGH
Gambar 3 struktur morfologi ikan zebra (Wixon, 2000)
Gambar 4 struktur anatomi ikan zebra (Yuniarto. dkk, 2017).
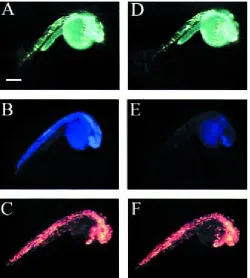
Gambar 5. GFP dan DsRed dapat direproduksi, sedangkan BFP bersifat fotolitik. Embrio 24-hpf itu diterangi selama 15 menit dengan cahaya dari yang sesuai filter eksitasi waktu dimulai (0 min) untuk GFP, BFP, dan DsRed ditampilkan di panel A, B, dan C, masing-masing. Titik waktu 15 menit ditunjukkan pada panel D, E, dan F untuk GFP, BFP, dan DsRed. Hilangnya sinyal hanya terdeteksi untuk BFP (bandingkan panel B dan E). Bilah skala = 250 μm.
mengenai ikan zebra, penyakit dan patologi (Spitsbergen, J. M & Kent, M. L., 2003). Ikan bercahaya ini merupakan alternatif untuk uji coba obat baru, ikan ini dapat dijadikan percobaan untuk mendeteksi tumor kanker karena ikan zebra ini memiliki kemiripan secara fisiologi dengan manusia dan memiliki reaksi yang sama dengan saat terindikasi kanker, ikan zebra bercahaya dapat dijadikan sebagai uji coba obat kanker dengan penggunaan biaya yang rendah, untuk menanam kanker hati pada zebra hanya dibutuhkan 6 minggu sedangkan pada percobaan tikus memrlukan waktu selama 68 minggu hal ini menunjukan percobaan pada ikan zebra lebih efisien. Yang membuat gen ikan bercahaya didapatkan dari gen ubur-ubur yang ditransplantasikan kedalam hati ikan zebra kemudian kemudian ditanamkan sel kanker untuk pengujian, hal ini akan meungkinkan ilmuan memantau perkembangan sel kanker di dalam hati ikan melalui mikroskop dan memungkinkan ilmuan untuk mengevaluasi dan cara memberikan obat (Nagare, 2009).
Selain kanker Zebrafish juga sangat sesuai pada aplikasi model gangguan ginjal yang meliputi penyakit ginjal polisistik, model gagal ginjal akut, model nefrolitiasis, dan beberapa model lainnya Govind, P. et al. (2012). Pada model penyakit ginjal polisistik, beberapa studi menjelaskan bahwa bagian yang disebut sebagai silia memiliki peranan penting terhadap terjadinya penyakit ini. Beberapa model yang dapat diterapkan pada zebrafish yang erat kaitannya dengan kerusakan pada silia antara lain Bardet Biedl Syndrome, Nephronophthisis, Oro-Facial-Digital, dan Sindroma Meckels.
Gambar 7 ikan zebra transgenik pada 385 sinar ultraviolet
Menurut penelitian yang dilakukan oleh Zhiyuan Gong dari National University of
Singapure, sejauh ini ikan-ikan zebra atau yang lebih populer disebut goldfish hasil
rekayasa tersebut tidak menimbulkan ancaman terhadap lingkungan. Ikan-ikan ini hanya memancarkan warna terang di bawah segala macam sinar, namun tidak akan mencemari lingkungan. Meskipun sebenarnya ikan ini hanya mempunyai dua macam warna tambahan, namun dapat dikembangkan menjadi lima warna yang berbeda, di mana masing-masing warna tersebut akan bersinar sesuai dengan jenis polutan yang dijumpai ikan (Kusrini, 2012).
3. Simpulan/Conclusion
Berdasarkan hasil penelitian ini maka dapat disimpulkan bahwa rekayasa genetika pada ikan zebra dengan menggunakan gen warna dari ubur-ubur dapat bermanfaat sebagai indikator pencemaran alam, karena ikan hasil rekayasa genetika ini akan memendarkan warna sesuai dengan gen yang disuntikanya jika tempat yang ia tinggali mengandung polutan atau sudah tercemar polusi, selain sebagai indikator pencemaran lingkungan ikan zebra juga dapat dijadikan sebagai biomedis yang dapat dijadikan percobaan penelitian mendeteksi suatu penyakit.
Daftar Pustaka/References
Aji, P. L. (2012). Transgenic In Aquaqulture. Volume 15 No 3D: Jurnal Penelitian Sains (118-121).
Alimudin, et al. (2003). Aplikasi Transfer Gen dalam Aquakultur. Volume 2: Jurnal Aquakultur Indonesia (41-50).
Alimuddin. at al (2007). Efektivitas Promoter Hcmv, Mef1 Dan Mact Dalam Mengatur
Ekspresi Gen Asing Pada Transgenik Ikan Zebra. Volume 6: Jurnal Aquakultur Indonesia (65-77).
Amanuma, K. et al. (2008). Genetically Modifi ed, Red Fluorescent Zebrafi sh: Detection, Crossing, Inheritance of Red Fluorescence, and Tolerance to Low Temperatures. Volume 2 : Journal Environmental Biotecnology (105-110).
Barlow, K. H. (2012). Shoaling Differences In Zebrafish, Danio Rerio, And Yellow
Glofish, Genetically Altered Danio Rerio. Biology (1-40).
Braun, M.H. et al. (2009). The responses of zebrafish (Danio rerio) to high external ammonia and urea transporter inhibition: nitrogen excretion and expression of rhesus glycoproteins and urea transporter proteins. Volume 212: The Journal of Experimental Biology (3846-3856).
Bratspies, R. M . (2006). Glowing in the Dark: How America’s First Transgenic Animal Escaped Regulation.
Eenennaam, A. V. (2008). Geneticaly Engineered Animals : On Overview. Departement Of Animals Science: California.
Ganguly, S. et al. (2012). Zebra Fish- General Biology And A Biomedical Research Tool. Volume 1 No 3 : International Of Science Environment Of Technology (193-196). Govind, P. et al. (2012). Zebra Fish- General Biology And A Biomedical Research Tool.
Internatinal Research Journal Of Parmacy (120-123).
Holtzman, G. N. et al. (2016).Learning to Fish with Genetics: A Primer on the Vertebrate
Model Danio rerio. Volume 203: Genetics Society Of America (1069-1089).
Kusrini, E. (2012). Perkembangan Rekayasa Genetika Pada Ikan Hias Di Indonesia. Volume 7 : Media Aquakultur (59-64).
Kusrini, E. (2015). Transfeksi Merupakan Metode Teknologi Transgenik Penyisipan
Green Flourescent Protein Terhadap Ikan Wild Betta. Volume 10 : Media Aquakultur (7-11).
Mora, C. et al. (2012). Factors Affecting the Adoption of Genetically Modified Animals in the Food and Pharmaceutical Chains. Volume 1: Bio- Based and Aplied Economics (313-329).
Moraless, M. et al. (2001). Tilapia chromosomal growth hormone gene expression
accelerates growth in transgenic zebrafish (Danio rerio. Volume 2: EJB Electronic
Journal of Biotechnology (0717-3458).
Mueller, M. et al. (2012).The Future of Citizen Science. Volume 2: Democracy Education (1-12).
Rahman, A. et al. (2012). SebaraN Ukuran dan Kondisi Ikan Zebra Amatitlania
nigrofasciata (Gunther, 1867) da Danau Beratan Bali. Volume 2 : Jurnal Aktiologi
Indonesia (135-145).
Rehbein, H & Bogerd, J. (2007). Identification of Genetically Modified Zebrafish (Danio
rerio) by Protein- and DNA-Analysis. Volume 2: Journal für Verbraucherschutz und
Lebensmittelsicherheit (122-125).
Sackerman, J. et al. (2010). Zebrafish Behavior in Novel Environments: Effects of Acute
Exposure to Anxiolytic Compounds and Choice of Danio rerio Line. International
Journal of Comparative Psychology (43-61).
Sassen, W.A & Koster, R.W. (2015). A Molecular Toolbox For Genetic Manipulation Of Zebrafish. Volume 5 : Advances In Genomics and Genetics (151-163).
Subyakto, S. et al. (2010). Penggunaan Metode Mikroinjeksi Dan Elektroporasi Dalam
Transfer Gen Hormon Pertumbuhan (GH) Pada Ikan Kerapu Tikus (Cromileptes
Altivelis). Volume 9: Omni Aquatika (1-8).
Snow, A. A. et al. (2005). Genetically Engineered Organisms And The Environment: Current Status And Recommendation. Volume 15 : Ecological Aplicatios (377-404). Spitsbergen, J. M & Kent, M. L. (2013). The State of the Art of the Zebrafish Model for Toxicology and Toxicologic Pathology Research—Advantages and Current Limitations. Volume 31: Toxicology Phatology (62-87).
Spence, R. (2006). The distribution and habitat preferences of the zebrafish in Bangladesh. Volume 09: Journal Fish Of Biology (1435-1448).
Stryjewska, A. et al. (2013). Biotechnology and genetic engineering in the new drug development. Part I. DNA technology and recombinant proteins. Volume 65 : Pharmacologycal Reports (1065-1075).
Wixon, J. (2000). Danio rerio The zebrafish. Volume: 12 Featured Organism (225-231).
Xu, Y. et al. (1999). Fast Skeletal Muscle-Specific Expression of a Zebrafish Myosin Light Chain 2 Gene and Characterization of Its Promoter by Direct Injection into Skeletal Muscle. Volume 18 : DNA and Cell Biology (85-95).
Yuniarto, A. et al. (2017). Aplikasi Zebrafish (Danio rerio) pada Beberapa Model Penyakit