BAB 2
TINJAUAN PUSTAKA
2.1 FISIOLOGI NYERI
Definisi nyeri berdasarkan International Association for the Study of Pain (IASP, 1979) adalah pengalaman sensori dan emosi yang tidak menyenangkan dimana berhubungan dengan kerusakan jaringan atau potensial terjadi kerusakan jaringan1,2. Sebagai mana diketahui bahwa nyeri tidaklah selalu berhubungan dengan derajat kerusakan jaringan yang dijumpai. Namun nyeri bersifat individual yang dipengaruhi oleh genetik, latar belakang kultural, umur dan jenis kelamin. Kegagalan dalam menilai faktor kompleks nyeri dan hanya bergantung pada pemeriksaan fisik sepenuhnya serta tes laboratorium mengarahkan kita pada kesalahpahaman dan terapi yang tidak adekuat terhadap nyeri, terutama pada pasien-pasien dengan resiko tinggi seperti orang tua, anak-anak dan pasien dengan gangguan komunikasi2,3,26,27,28.
Setiap pasien yang mengalami trauma berat (tekanan, suhu, kimia) atau paska pembedahan harus dilakukan penanganan nyeri yang sempurna, karena dampak dari nyeri itu sendiri akan menimbulkan respon stres metabolik (MSR) yang akan mempengaruhi semua sistem tubuh dan memperberat kondisi
pasiennya. Hal ini akan merugikan pasien akibat timbulnya perubahan fisiologi dan psikologi pasien itu sendiri, seperti1,2,3,29,30 :
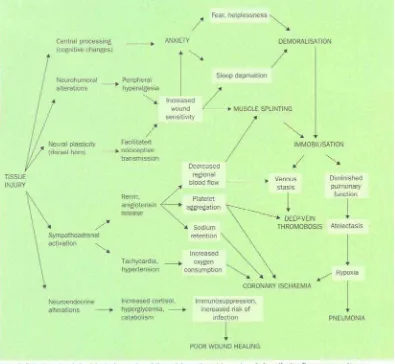
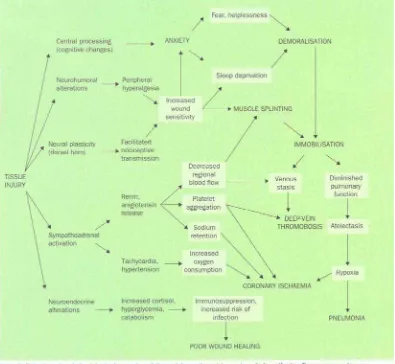
• Perubahan kognitif (sentral) : kecemasan, ketakutan, gangguan tidur dan putus asa
• Perubahan neurohumoral : hiperalgesia perifer, peningkatan kepekaan luka • Plastisitas neural (kornudorsalis), transmisi nosiseptif yang difasilitasi
sehingga meningkatkan kepekaan nyeri
Gambar 2.1-1. Efek fisiologis dan psikologis yang berhubungan dengan nyeri akut akibat kerusakan jaringan yang disebabkan oleh proses pembedahan atau trauma31.
BAB 2
TINJAUAN PUSTAKA
2.1 FISIOLOGI NYERI
Definisi nyeri berdasarkan International Association for the Study of Pain (IASP, 1979) adalah pengalaman sensori dan emosi yang tidak menyenangkan dimana berhubungan dengan kerusakan jaringan atau potensial terjadi kerusakan jaringan1,2. Sebagai mana diketahui bahwa nyeri tidaklah selalu berhubungan dengan derajat kerusakan jaringan yang dijumpai. Namun nyeri bersifat individual yang dipengaruhi oleh genetik, latar belakang kultural, umur dan jenis kelamin. Kegagalan dalam menilai faktor kompleks nyeri dan hanya bergantung pada pemeriksaan fisik sepenuhnya serta tes laboratorium mengarahkan kita pada kesalahpahaman dan terapi yang tidak adekuat terhadap nyeri, terutama pada pasien-pasien dengan resiko tinggi seperti orang tua, anak-anak dan pasien dengan gangguan komunikasi2,3,26,27,28.
Setiap pasien yang mengalami trauma berat (tekanan, suhu, kimia) atau paska pembedahan harus dilakukan penanganan nyeri yang sempurna, karena dampak dari nyeri itu sendiri akan menimbulkan respon stres metabolik (MSR) yang akan mempengaruhi semua sistem tubuh dan memperberat kondisi
pasiennya. Hal ini akan merugikan pasien akibat timbulnya perubahan fisiologi dan psikologi pasien itu sendiri, seperti1,2,3,29,30 :
• Perubahan kognitif (sentral) : kecemasan, ketakutan, gangguan tidur dan putus asa
• Perubahan neurohumoral : hiperalgesia perifer, peningkatan kepekaan luka • Plastisitas neural (kornudorsalis), transmisi nosiseptif yang difasilitasi
sehingga meningkatkan kepekaan nyeri
Gambar 2.1-1. Efek fisiologis dan psikologis yang berhubungan dengan nyeri akut akibat kerusakan jaringan yang disebabkan oleh proses pembedahan atau trauma31.
2.2 MEKANISME NYERI
Nyeri merupakan suatu bentuk peringatan akan adanya bahaya kerusakan jaringan. Pengalaman sensoris pada nyeri akut disebabkan oleh stimulus noksius yang diperantarai oleh sistem sensorik nosiseptif. Sistem ini berjalan mulai dari perifer melalui medulla spinalis, batang otak, thalamus dan korteks serebri. Apabila telah terjadi kerusakan jaringan, maka sistem nosiseptif akan bergeser fungsinya dari fungsi protektif menjadi fungsi yang membantu perbaikan jaringan yang rusak28,33.
Nyeri inflamasi merupakan salah satu bentuk untuk mempercepat perbaikan kerusakan jaringan. Sensitifitas akan meningkat, sehingga stimulus non noksius atau noksius ringan yang mengenai bagian yang meradang akan menyebabkan nyeri. Nyeri inflamasi akan menurunkan derajat kerusakan dan menghilangkan respon inflamasi28,33.
2.2.1 Sensitisasi Perifer
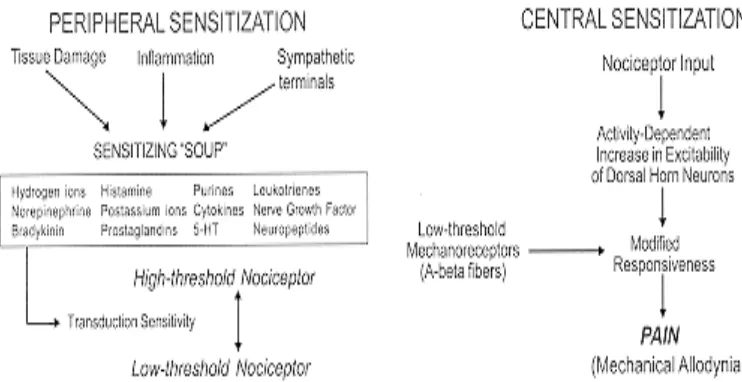
Cidera atau inflamasi jaringan akan menyebabkan munculnya perubahan lingkungan kimiawi pada akhir nosiseptor. Sel yang rusak akan melepaskan komponen intraselulernya seperti adenosine trifosfat, ion K+, pH menurun, sel inflamasi akan menghasilkan sitokin, chemokine dan growth factor. Beberapa komponen diatas akan langsung merangsang nosiseptor (nociceptor activators)
dan komponen lainnya akan menyebabkan nosiseptor menjadi lebih hipersensitif terhadap rangsangan berikutnya (nociceptor sensitizers)33,34.
Komponen sensitisasi, misalnya prostaglandin E2 akan mereduksi ambang
Gambar 2.2-1. Mekanisme sensitisasi perifer dan sensitisasi sentral34.
2.2.2 Sensitisasi Sentral
Sama halnya dengan sistem nosiseptor perifer, maka transmisi nosiseptor
di sentral juga dapat mengalami sensitisasi. Sensitisasi sentral dan perifer bertanggung jawab terhadap munculnya hipersensitivitas nyeri setelah cidera. Sensitisasi sentral memfasilitasi dan memperkuat transfer sipnatik dari nosiseptor ke neuron kornu dorsalis. Pada awalnya proses ini dipacu oleh input nosiseptor ke medulla spinalis (activity dependent), kemudian terjadi perubahan molekuler neuron (transcription dependent) 33.
2.3 NOSISEPTOR (RESEPTOR NYERI)
Nosiseptor adalah reseptor ujung saraf bebas yang ada di kulit, otot, persendian, viseral dan vaskular. Nosiseptor-nosiseptor ini bertanggung jawab terhadap kehadiran stimulus noksius yang berasal dari kimia, suhu (panas, dingin), atau perubahan mekanikal. Pada jaringan normal, nosiseptor tidak aktif sampai adanya stimulus yang memiliki energi yang cukup untuk melampaui ambang batas stimulus (resting). Nosiseptor mencegah perambatan sinyal acak (skrining fungsi) ke SSP untuk interpretasi nyeri3,28,35,36.
Saraf nosiseptor bersinap di dorsal horn dari spinal cord dengan lokal interneuron dan saraf projeksi yang membawa informasi nosiseptif ke pusat yang lebih tinggi pada batang otak dan thalamus. Berbeda dengan reseptor sensorik lainnya, reseptor nyeri tidak bisa beradaptasi. Kegagalan reseptor nyeri beradaptasi adalah untuk proteksi karena hal tersebut bisa menyebabkan individu untuk tetap awas pada kerusakan jaringan yang berkelanjutan. Setelah kerusakan terjadi, nyeri biasanya minimal. Mula datang nyeri pada jaringan karena iskemi akut berhubungan dengan kecepatan metabolisme. Sebagai contoh, nyeri terjadi pada saat beraktifitas kerena iskemia otot skeletal pada 15 sampai 20 detik tapi pada iskemia kulit bisa terjadai pada 20 sampai 30 menit3,28,36.
Tipe nosiseptor spesifik bereaksi pada tipe stimulus yang berbeda. Nosiseptor C tertentu dan nosiseptor A-delta bereaksi hanya pada stimulus panas
atau dingin, dimana yang lainnya bereaksi pada stimulus yang banyak (kimia, panas, dingin). Beberapa reseptor A-beta mempunyai aktivitas nociceptor-like. Serat –serat sensorik mekanoreseptor bisa diikutkan untuk transmisi sinyal yang akan menginterpretasi nyeri ketika daerah sekitar terjadi inflamasi dan produk-produknya. Allodynia mekanikal (nyeri atau sensasi terbakar karena sentuhan ringan) dihasilkan mekanoreseptor A-beta3,28,36.
dengan proses patologis, dan nyeri yang dicetuskan untuk mempertahankan fungsi3,28,36.
2.4 PERJALANAN NYERI (NOCICEPTIVE PATHWAY)
Perjalanan nyeri termasuk suatu rangkaian proses neurofisiologis kompleks yang disebut sebagai nosiseptif (nociception) yang merefleksikan empat proses komponen yang nyata yaitu transduksi, transmisi, modulasi dan persepsi, dimana terjadinya stimuli yang kuat diperifer sampai dirasakannya nyeri di susunan saraf pusat (cortex cerebri)1,3,30,37.
2.4.1 Proses Transduksi
Proses dimana stimulus noksius diubah ke impuls elektrikal pada ujung saraf. Suatu stimuli kuat (noxion stimuli) seperti tekanan fisik kimia, suhu dirubah menjadi suatu aktifitas listrik yang akan diterima ujung-ujung saraf perifer (nerve ending) atau organ-organ tubuh (reseptor meisneri, merkel, corpusculum paccini, golgi mazoni). Kerusakan jaringan karena trauma baik trauma pembedahan atau trauma lainnya menyebabkan sintesa prostaglandin, dimana prostaglandin inilah yang akan menyebabkan sensitisasi dari reseptor-reseptor nosiseptif dan dikeluarkannya zat-zat mediator nyeri seperti histamin, serotonin yang akan menimbulkan sensasi nyeri. Keadaan ini dikenal sebagai sensitisasi
perifer1,3,30,35,37.
2.4.2 Proses Transmisi
impuls disalurkan ke thalamus dan somatosensoris di cortex cerebri dan dirasakan sebagai persepsi nyeri1,3,30,35,37.
2.4.3 Proses Modulasi
Proses perubahan transmisi nyeri yang terjadi disusunan saraf pusat (medulla spinalis dan otak). Proses terjadinya interaksi antara sistem analgesik endogen yang dihasilkan oleh tubuh kita dengan input nyeri yang masuk ke kornu posterior medulla spinalis merupakan proses ascenden yang dikontrol oleh otak. Analgesik endogen (enkefalin, endorphin, serotonin, noradrenalin) dapat menekan impuls nyeri pada kornu posterior medulla spinalis. Dimana kornu posterior sebagai pintu dapat terbuka dan tertutup untuk menyalurkan impuls nyeri untuk analgesik endogen tersebut. Inilah yang menyebabkan persepsi nyeri sangat subjektif pada setiap orang1,3,30,35,37.
2.4.4 Persepsi
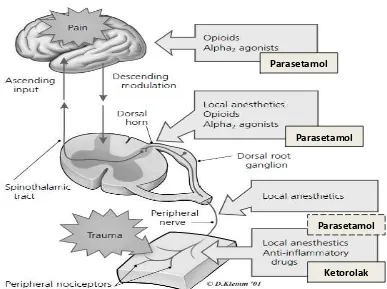
Gambar 2.4-1. Pain Pathway36.
2.5 MEKANISME KERJA OBAT ANALGETIK
Obat analgetik bekerja di dua tempat utama, yaitu di perifer dan sentral. Golongan obat AINS bekerja diperifer dengan cara menghambat pelepasan mediator sehingga aktifitas enzim siklooksigenase terhambat dan sintesa
prostaglandin tidak terjadi. Sedangkan analgetik opioid bekerja di sentral dengan cara menempati reseptor di kornu dorsalis medulla spinalis sehingga terjadi penghambatan pelepasan transmitter dan perangsangan ke saraf spinal tidak terjadi1,3.
Prostaglandin merupakan hasil bentukan dari asam arakhidonat yang mengalami metabolisme melalui siklooksigenase. Prostaglandin yang lepas ini akan menimbulkan gangguan dan berperan dalam proses inflamasi, edema, rasa nyeri lokal dan kemerahan (eritema lokal). Selain itu juga prostaglandin
Parasetamol
meningkatkan kepekaan ujung-ujung saraf terhadap suatu rangsangan nyeri (nosiseptif) 1,3.
Enzim siklooksigenase (COX) adalah suatu enzim yang mengkatalisis sintesis prostaglandin dari asam arakhidonat. Obat AINS memblok aksi dari enzim COX yang menurunkan produksi mediator prostaglandin, dimana hal ini menghasilkan kedua efek yakni baik yang positif (analgesia, antiinflamasi) maupun yang negatif (ulkus lambung, penurunan perfusi renal dan perdarahan). Aktifitas COX dihubungkan dengan dua isoenzim, yaitu ubiquitously dan
constitutive yang diekspresikan sebagai COX-1 dan yang diinduksikan inflamasi COX-2. COX-1 terutama terdapat pada mukosa lambung, parenkim ginjal dan platelet. Enzim ini penting dalam proses homeostatik seperti agregasi platelet, keutuhan mukosa gastrointestinal dan fungsi ginjal. Sebaliknya, COX-2 bersifat
inducible dan diekspresikan terutama pada tempat trauma (otak dan ginjal) dan menimbulkan inflamasi, demam, nyeri dan kardiogenesis. Regulasi COX-2 yang transien di medulla spinalis dalam merespon inflamasi pembedahan mungkin penting dalam sensitisasi sentral1,3,27.
2.6 KLASIFIKASI NYERI
Kejadian nyeri memiliki sifat yang unik pada setiap individual bahkan jika cedera fisik tersebut identik pada individual lainnya. Adanya takut, marah,
kecemasan, depresi dan kelelahan akan mempengaruhi bagaimana nyeri itu dirasakan. Subjektifitas nyeri membuat sulitnya mengkategorikan nyeri dan mengerti mekanisme nyeri itu sendiri. Salah satu pendekatan yang dapat dilakukan untuk mengklasifikasi nyeri adalah berdasarkan durasi (akut, kronik), patofisiologi (nosiseptif, nyeri neuropatik) dan etiologi (paska pembedahan, kanker)1,3.
2.6.1 Nyeri Akut dan Kronik
pasien paling tidak 1 – 6 bulan. Nyeri kronik malignan biasanya disertai kelainan patologis dan indikasi sebagai penyakit yang life-limiting disease seperti kanker,
end-stage organ dysfunction, atau infeksi HIV. Nyeri kronik kemungkinan
mempunyai baik elemen nosiseptif dan neuropatik. Nyeri kronik nonmalignan (nyeri punggung, migrain, artritis, diabetik neuropati) sering tidak disertai kelainan patologis yang terdeteksi dan perubahan neuroplastik yang terjadi pada lokasi sekitar (dorsal horn pada spinal cord) akan membuat pengobatan menjadi lebih sulit2,3,26,27.
Pasien dengan nyeri akut atau kronis bisa memperlihatkan tanda dan gejala sistem saraf otonom (takikardi, tekanan darah yang meningkat, diaforesis, nafas cepat) pada saat nyeri muncul. Guarding biasa dijumpai pada nyeri kronis yang menunjukkan allodinia. Meskipun begitu, muncul ataupun hilangnya tanda dan gejala otonom tidak menunjukkan ada atau tidaknya nyeri3,26,27.
2.6.2 Nosiseptif dan Nyeri Neuropatik
Nyeri organik bisa dibagi menjadi nosiseptif dan nyeri neuropatik. Nyeri nosiseptif adalah nyeri inflamasi yang dihasilkan oleh rangsangan kimia, mekanik dan suhu yang menyebabkan aktifasi maupun sensitisasi pada nosiseptor perifer (saraf yang bertanggung jawab terhadap rangsang nyeri). Nyeri nosiseptif biasanya memberikan respon terhadap analgesik opioid atau non opioid1,2,3,26,27.
Nyeri neuropatik merupakan nyeri yang ditimbulkan akibat kerusakan neural pada saraf perifer maupun pada sistem saraf pusat yang meliputi jalur saraf aferen sentral dan perifer, biasanya digambarkan dengan rasa terbakar dan menusuk. Pasien yang mengalami nyeri neuropatik sering memberi respon yang kurang baik terhadap analgesik opioid1,2,3,26,27.
2.6.3 Nyeri Viseral
Nyeri viseral, seperti nyeri somatik dalam, mencetuskan refleks kontraksi otot-otot lurik sekitar, yang membuat dinding perut tegang ketika proses inflamasi terjadi pada peritoneum. Nyeri viseral karena invasi malignan dari organ lunak dan keras sering digambarkan dengan nyeri difus, menggrogoti, atau keram jika organ lunak terkena dan nyeri tajam bila organ padat terkena 3,26,27.
Penyebab nyeri viseral termasuk iskemia, peregangan ligamen, spasme otot polos, distensi struktur lunak seperti kantung empedu, saluran empedu, atau ureter. Distensi pada organ lunak terjadi nyeri karena peregangan jaringan dan mungkin iskemia karena kompresi pembuluh darah sehingga menyebabkan distensi berlebih dari jaringan3,26,27.
Rangsang nyeri yang berasal dari sebagian besar abdomen dan toraks menjalar melalui serat aferen yang berjalan bersamaan dengan sistem saraf simpatis, dimana rangsang dari esofagus, trakea dan faring melalui aferen vagus dan glossopharyngeal, impuls dari struktur yang lebih dalam pada pelvis dihantar melalui nervus parasimpatis di sakral. Impuls nyeri dari jantung menjalar dari sistem saraf simpatis ke bagian tengah ganglia cervical, ganglion stellate, dan bagian pertama dari empat dan lima ganglion thorasik dari sistem simpatis. Impuls ini masuk ke spinal cord melalui nervus torak ke 2, 3, 4 dan 5. Penyebab impuls nyeri yang berasal dari jantung hampir semua berasal dari iskemia miokard. Parenkim otak, hati, dan alveoli paru adalah tanpa reseptor. Adapun, bronkus dan
pleura parietal sangat sensitif pada nyeri3,26,27.
2.6.4 Nyeri Somatik
viseralis tidak nyeri sama sekali. Berbeda dengan nyeri viseral, nyeri parietal biasanya terlokalisasi langsung pada daerah yang rusak1,3,26,27.
Munculnya jalur nyeri viseral dan parietal menghasilkan lokalisasi dari nyeri dari viseral pada daerah permukaan tubuh pada waktu yang sama. Sebagai contoh, rangsang nyeri berasal dari apendiks yang inflamasi melalui serat – serat nyeri pada sistem saraf simpatis ke rantai simpatis lalu ke spinal cord pada T10 ke T11. Nyeri ini menjalar ke daerah umbilikus dan nyeri menusuk dan kram sebagai karakternya. Sebagai tambahan, rangsangan nyeri berasal dari peritoneum parietal dimana inflamasi apendiks menyentuh dinding abdomen, rangsangan ini melewati nervus spinalis masuk ke spinal cord pada L1 sampai L2. Nyeri menusuk berlokasi langsung pada permukaan peritoneal yang teriritasi di kuadran kanan bawah3,26,27.
2.7 PENILAIAN NYERI
Ada beberapa skala penilaian nyeri pada pasien sekarang ini1,2,38,39,40,41,42:
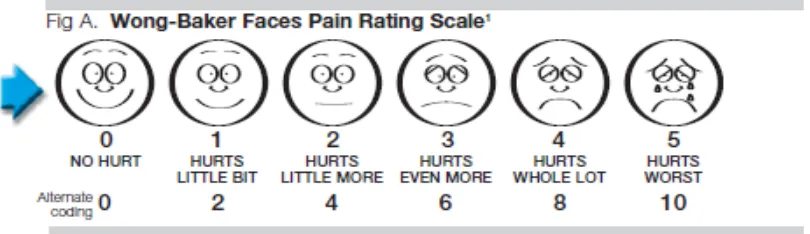
1. Wong-Baker Faces Pain Rating Scale
Skala dengan enam gambar wajah dengan ekspresi yang berbeda, dimulai dari senyuman sampai menangis karena kesakitan. Skala ini berguna pada pasien dengan gangguan komunikasi, seperti anak-anak, orang tua, pasien yang kebingungan atau pada pasien yang tidak mengerti dengan bahasa lokal setempat.
Gambar 2.7-1. Wong Baker Faces Pain Rating Scale
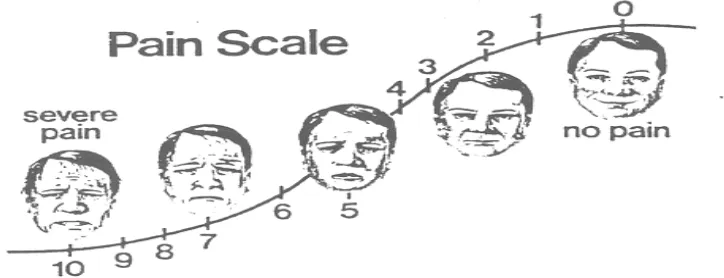
2. Verbal Rating Scale (VRS)
Pasien ditanyakan tentang derajat nyeri yang dirasakan berdasarkan skala lima poin ; tidak nyeri, ringan, sedang, berat dan sangat berat.
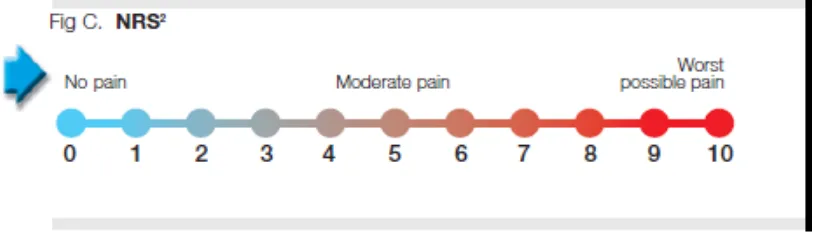
3. Numerical Rating Scale (NRS)
Pertama sekali dikemukakan oleh Downie dkk pada tahun 1978, dimana pasien ditanyakan tentang derajat nyeri yang dirasakan dengan menunjukkan angka 0 – 5 atau 0 – 10, dimana angka 0 menunjukkan tidak ada nyeri dan angka 5 atau 10 menunjukkan nyeri yang hebat.
Gambar 2.7-3. Numerical Rating Scale
4. Visual Analogue Scale (VAS)
Skala yang pertama sekali dikemukakan oleh Keele pada tahun 1948 yang merupakan skala dengan garis lurus 10 cm, dimana awal garis (0) penanda tidak ada nyeri dan akhir garis (10) menandakan nyeri hebat. Pasien diminta untuk membuat tanda digaris tersebut untuk mengekspresikan nyeri yang dirasakan. Penggunaan skala VAS lebih gampang, efisien dan lebih mudah dipahami oleh penderita dibandingkan dengan skala lainnya. Penggunaan VAS telah direkomendasikan oleh Coll dkk karena selain telah digunakan secara luas, VAS juga secara metodologis kualitasnya lebih baik, dimana juga penggunaannya realtif mudah, hanya dengan menggunakan beberapa kata sehingga kosa kata tidak menjadi permasalahan. Willianson dkk juga
melakukan kajian pustaka atas tiga skala ukur nyeri dan menarik kesimpulan bahwa VAS secara statistik paling kuat rasionya karena dapat menyajikan data dalam bentuk rasio. Nilai VAS antara 0 – 4 cm dianggap sebagai tingkat nyeri yang rendah dan digunakan sebagai target untuk tatalaksana analgesia. Nilai
nyaman sehingga perlu diberikan obat analgesic penyelamat (rescue analgetic).
Gambar 2.7-4. Visual Analogue Scale
2.8 PENANGANAN NYERI
Penanganan nyeri paska pembedahan yang efektif harus mengetahui patofisiologi dan pain pathway sehingga penanganan nyeri dapat dilakukan dengan cara farmakoterapi (multimodal analgesia), pembedahan, serta juga terlibat didalamnya perawatan yang baik dan teknik non-farmakologi (fisioterapi, psikoterapi)2,29.
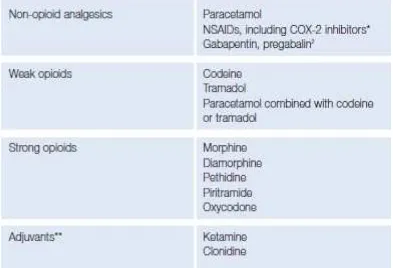
2.8.1 Farmakologis
Modalitas analgetik paska pembedahan termasuk didalamnya analgesik oral parenteral, blok saraf perifer, blok neuroaksial dengan anestesi lokal dan opioid intraspinal1.
Tabel 2.8-2. Pilihan terapi untuk penanganan nyeri berdasarkan jenis operasi2.
Pedoman terapi pemberian analgesia untuk penanganan nyeri paska pembedahan berdasarkan intensitas nyeri yang dirasakan penderita yang direkomendasikan oleh WHO dan WFSA. Dimana terapi
2.8.1.1 Analgesia Multimodal
Analgesia multimodal menggunakan dua atau lebih obat analgetik yang memiliki mekanisme kerja yang berbeda untuk mencapai efek analgetik yang maksimal tanpa dijumpainya peningkatan efek samping dibandingkan dengan peningkatan dosis pada satu obat saja. Dimana analgesi multimodal melakukan intervensi nyeri secara berkelanjutan pada ketiga proses perjalanan nyeri, yakni1,2,29,30,43:
• Penekanan pada proses tranduksi dengan menggunakan AINS
• Penekanan pada proses transmisi dengan anestetik lokal (regional) • Peningkatan proses modulasi dengan opioid
Analgesia multimodal merupakan suatu pilihan yang dimungkinkan dengan penggunaan parasetamol dan AINS sebagai kombinasi dengan opioid atau anestesi lokal untuk menurunkan tingkat intensitas nyeri pada pasien-pasien yang mengalami nyeri paska pembedahan ditingkat sedang sampai berat2. Analgesia multimodal selain harus diberikan secepatnya (early analgesia), juga harus disertai dengan inforced mobilization (early ambulation) disertai dengan pemberian nutrisi nutrisi oral secepatnya (early alimentation)43.
2.8.1.2 Analgesia Preemptif
Analgesia preemptif artinya mengobati nyeri sebelum terjadi, terutama ditujukan pada pasien sebelum dilakukan tindakan operasi (pre-operasi).
Pemberian analgesia sebelum onset dari rangsangan melukai untuk mencegah sensistisasi sentral dan membatasi pengalaman nyeri selanjutnya. Analgesia preemptif mencegah kaskade neural awal yang dapat membawa keuntungan jangka panjang dengan menghilangkan hipersensitifitas yang ditimbulkan oleh
2.8.1.3 PCA (Patient Control Analgesia)
Pasien dikontrol nyerinya dengan memberikan obat analgesik itu sendiri dengan memakai alat (pump), dosis diberikan sesuai dengan tingkatan nyeri yang dirasakan. PCA bisa diberikan dengan cara Intravenous Patient Control Analgesia
(IVPCA) atau Patient Control Epidural Analgesia (PCEA), namun dengan cara ini memerlukan biaya yang mahal baik peralatan maupun tindakannya1,30,44.
2.8.1.4 Parasetamol
Parasetamol banyak digunakan sebagai obat analgetik dan antipiretik, dimana kombinasi parasetamol dengan opioid dapat digunakan untuk penanganan nyeri berat paska pembedahan dan terapi paliatif pada pasien-pasien penderita kanker. Onset analgesia dari parasetamol 8 menit setelah pemberian intravena, efek puncak tercapai dalam 30 – 45 menit dan durasi analgesia 4 – 6 jam serta waktu pemberian intravena 2 – 15 menit. Parasetamol termasuk dalam kelas “aniline analgesics” dan termasuk dalam golongan obat antiinflamasi non steroid (masih ada perbedaan pendapat). Parasetamol memiliki efek anti inflamasi yang sedikit dibandingkan dengan obat AINS lainnya. Akan tetapi parasetamol bekerja dengan mekanisme yang sama dengan obat AINS lainnya (menghambat sintesa prostaglandin). Parasetamol juga lebih baik ditoleransi dibandingkan aspirin dan obat AINS lainnya pada pasien-pasien dengan sekresi asam lambung yang
berlebihan atau pasien dengan masa perdarahan yang memanjang48,49,50,51,52.
Gambar 2.8-1. Rumus Bangun Parasetamol53.
Dosis pada orang dewasa sebesar 500 – 1000 mg, dengan dosis maksimum direkomendasi 4000 mg perhari. Pada dosis ini parasetamol aman digunakan untuk anak-anak dan orang dewasa54,55.
Mekanisme kerja utama dari parasetamol adalah menghambat
siklooksigenase (COX) dan selektif terhadap COX-2. Analgetik dan antipiretik dari parasetamol sebanding dengan aspirin dan obat AINS lainnya, akan tetapi aktifitas anti inflamasi perifernya dibatasi oleh beberapa faktor, dimana diantaranya terdapat kadar peroksida yang tinggi di lesi inflamasi. Oleh karena itu selektifitas akan COX-2 tidak secara signifikan menghambat produksi pro-clotting tromboxane. Parasetamol menurunkan bentuk oksidasi dari enzim COX, yang melindungi dari pembentukan kimiawi bentuk pro-inflammatory. Ini juga akan menurunkan jumlah dari prostaglandin E2 di SSP, akibatnya menurunkan batas
ambang hipotalamus di pusat termoregulasi56,57,58.
Parasetamol menghambat kerja COX dengan dua jalur, yang pertama bekerja dengan cara menghambat COX-3 (variant dari COX-1). Enzim COX-3 ini hampir sama dengan enzim COX lainnya dengan menghasilkan kimiawi pro-inflammatory dan penghambat selektif oleh parasetamol. Jalur kedua bekerja seperti aspirin dengan memblok siklooksigenase, dimana didalam lingkungan inflamasi dengan konsentrasi peroksida yang tinggi dan melindungi aksi kerja parasetamol dalam keadaan oksidasi tinggi. Ini berarti bahwa parasetamol tidak
memiliki efek langsung pada tempat inflamasi, akan tetapi bereaksi di SSP dimana keadaan lingkungan tidak teroksidasi. Namun mekanisme kerja pasti dari parasetamol di COX-3 masih diperdebatkan59,60.
Bioavailibilitas dari parasetamol adalah 100%. Parasetamol dimetabolisme di hati dengan tiga jalur metabolik, yakni glucuronidation 40%, sulfation 20-40% dan N-hydroxylation serta GSH konjugasi 15%, dengan obat dan metabolitnya diekskresikan melalui ginjal61,62.
penyebab sindroma Reye pada anak-anak dengan penyakit virus63,64,65. Satu-satunya efek samping dari penggunaan parasetamol adalah resiko terjadi hepatotoksik dan gangguan gastrointestinal pada penggunaan dosis tinggi, yaitu diatas 20.000 mg perhari63.
2.8.1.5 Ketorolak
Ketorolak atau ketorolak trometamin merupakan obat golongan anti inflamasi non steroid, yang masuk kedalam golongan derivate heterocyclic acetic acid dimana secara struktur kimia berhubungan dengan indometasin. Ketorolak menunjukkan efek analgesia yang poten tetapi hanya memiliki aktifitas anti inflamasi yang sedang bila diberikan secara intramuskular atau intravena. Ketorolak dapat dipakai sebagai analgesia paska pembedahan sebagai obat tunggal maupun kombinasi dengan opioid, dimana ketorolak mempotensiasi aksi nosiseptif dari opioid3,6,11,66,67.
Gambar 2.8-2. Rumus Bangun Ketorolak66.
(±) – 5 – benzoyl - 2,3 – dihydro - 1H – pyrrolizine – 1 – carboxylic acid, 2 - amino – 2 (hydroxymethyl) - 1,3 – propanediol
Mekanisme kerja utama dari ketorolak adalah menghambat sistesa prostaglandin dengan berperan sebagai penghambat kompetitif dari enzim siklooksigenase (COX) dan menghasilkan efek analgesia. Seperti AINS pada umumnya, ketorolak merupakan penghambat COX non selektif. Efek analgesianya 200 – 800 kali lebih poten dibandingkan dengan pemberian aspirin,
Sedangkan efek anti inflamasinya kurang dibandingkan efek analgesianya, dimana efek anti inflamasinya hampir sama dengan indometasin11,66.
Setelah injeksi intramuskular dan intravena, onset analgesia tercapai dalam waktu 10 menit dengan efek puncak 30 – 60 menit dan durasi analgesia 6 – 8 jam dengan waktu pemberian intravena > 15 detik. Bioavailibilitas dari ketorolak 100% dengan semua jalur pemberian baik intravena maupun intramuskular. Metabolisme berkonjugasi dengan asam glukoronik dan para hidroksilasi di hati. Obat dan hasil metabolitnya akan diekskresikan melalui ginjal 90% dan bilier sekitar 10%66,68.
Efek samping dari ketorolak bisa bermacam-macam, yaitu3,11,66,67:
1. Secara umum
Bronkospasme yang mengancam jiwa pada pasien dengan penyakit nasal poliposis, asma dan sensitif terhadap aspirin. Dapat juga terjadi edema laring, anafilaksis, edema lidah, demam dan flushing.
2. Fungsi platelet dan hemostatik
Ketorolak menghambat asam arakhidonat dan kolagen sehingga mencetuskan agregasi platelet sehingga waktu perdarahan dapat meningkat pada pasien yang mendapatkan anestesi spinal, akan tetapi tidak pada pasien yang mendapat anestesi umum. Perbedaan ini dimungkinkan karena reflek status hiperkoagulasi yang dihasilkan respon neuroendokrin karena stress
pembedahan berbeda pada anestesi umum dan anestesi spinal. Dapat juga terjadi purpura, trombositopeni, epistaksis, anemia dan leukopeni.
3. Gastrointestinal
Dapat menimbulkan erosi mukosa gastrointestinal, perforasi, mual, muntah, dispepsia, konstipasi, diare, melena, anoreksia dan pankreatitis.
4. Kardiovaskuler
Hipertensi, palpitasi, pallor dan syncope 5. Dermatologi
6. Neurologi
Nyeri kepala, pusing, somnolen, berkeringat, kejang, vertigo, tremor, halusinasi, euforia, insomnia dan gelisah.
7. Pernafasan
Dispnu, asma, edema paru, rhinitis dan batuk 8. Urogenital
Gagal ginjal akut dan poliuri.
2.8.2 Non-Farmakologis
Ada beberapa metode metode non-farmakologi yang digunakan untuk membantu penanganan nyeri paska pembedahan, seperti menggunakan terapi fisik (dingin, panas) yang dapat mengurangi spasme otot, akupunktur untuk nyeri kronik (gangguan muskuloskletal, nyeri kepala), terapi psikologis (musik, hipnosis, terapi kognitif, terapi tingkah laku) dan rangsangan elektrik pada sistem saraf (TENS, Spinal Cord Stimulation, Intracerebral Stimulation)1,2.
2.9
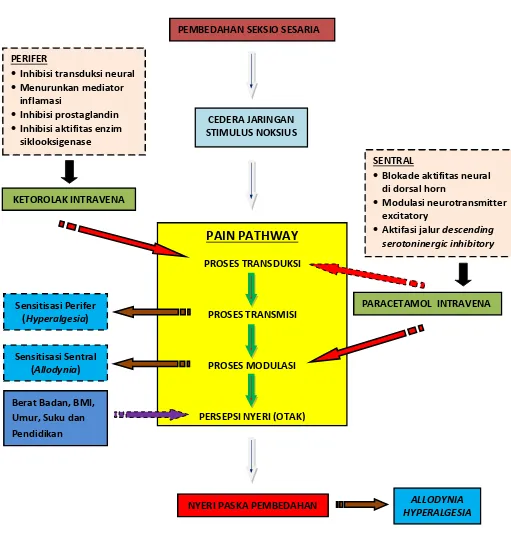
KERANGKA TEORI
Gambar 2.9-1. Skema Kerangka Teori
PEMBEDAHAN SEKSIO SESARIA
NYERI PASKA PEMBEDAHAN Sensitisasi Sentral
• Inhibisi transduksi neural
• Menurunkan mediator inflamasi
• Inhibisi prostaglandin
• Inhibisi aktifitas enzim siklooksigenase
SENTRAL
• Blokade aktifitas neural di dorsal horn
• Modulasi neurotransmitter excitatory
2.10 KERANGKA KONSEP
Gambar 2.10-1. Skema Kerangka Konsep
PEMBEDAHAN
STIMULUS NOKSIUS
ANALGESIA
VAS
NYERI PASKA BEDAH