FORMULASI TABLET EKSTRAK AKAR MANIS (Glycyrrhiza glabra Linn.) DENGAN VARIASI KOMPOSISI BAHAN
PENGISI AVICEL
®PH 101 DAN BAHAN PENGHANCUR EXPLOTAB
SKRIPSI
OLEH:
ANGGRAINY EKA PUTRI NIM 171501114
PROGRAM STUDI SARJANA FARMASI FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA MEDAN
2021
FORMULASI TABLET EKSTRAK AKAR MANIS (Glycyrrhiza glabra Linn.) DENGAN VARIASI KOMPOSISI BAHAN
PENGISI AVICEL
®PH 101 DAN BAHAN PENGHANCUR EXPLOTAB
SKRIPSI
Diajukan sebagai salah satu syarat untuk memperoleh gelar Sarjana Farmasi pada Fakultas Farmasi Universitas Sumatera Utara
OLEH:
ANGGRAINY EKA PUTRI NIM 171501114
PROGRAM STUDI SARJANA FARMASI FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA MEDAN
2021
iii
PENGESAHAN SKRIPSI
FORMULASI TABLET EKSTRAK AKAR MANIS (Glycyrrhiza glabra Linn.) DENGAN VARIASI KOMPOSISI BAHAN PENGISI AVICEL®
PH 101 DAN BAHAN PENGHANCUR EXPLOTAB
OLEH:
ANGGRAINY EKA PUTRI NIM 171501114
Dipertahankan di Hadapan Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara pada Tanggal: 27 Juli 2021
Disetujui oleh: Panitia Penguji:
Pembimbing,
T.Ismanelly Hanum, S.Si., M.Si., Apt. Prof. Dr. Hakim Bangun, Apt.
NIP 197512082009122002 NIP 195201171980031002
T.Ismanelly Hanum, S.Si., M.Si., Apt.
Ketua Program Studi Sarjana Farmasi, NIP 197512082009122002
Dr. Sumaiyah, M.Si., Apt. Mariadi, S.Farm., M.Si., Apt.
NIP 197712262008122002 NIP 198403052017041001
Medan, Juli 2021 Disahkan oleh:
Dekan,
Khairunnisa, S.Si., M.Pharm., Ph.D, Apt.
NIP 197802152008122001
iv
KATA PENGANTAR
Puji dan syukur kehadirat Tuhan Yang Maha Esa karena kasih dan anugerah-Nya yang melimpah sehingga penulis dapat menyelesaikan penulisan skripsi yang berjudul “Formulasi Tablet Ekstrak Akar Manis (Glycyrrhiza glabra Linn.) dengan Variasi Komposisi Bahan Pengisi Avicel® PH 101 dan Bahan Penghancur Explotab”. Skripsi ini diajukan sebagai salah satu syarat untuk memperoleh gelar Sarjana Farmasi pada Fakultas Farmasi Universitas Sumatera Utara.
Akar manis telah digunakan sebagai ekspektoran dan karminatif oleh orang Mesir, Cina, Yunani, India dan peradaban Romawi, juga digunakan sebagai oftalmia, anti-sifilis dan antidisentri, gangguan pencernaan, tenggorokan kering, abses, bengkak dan bertindak sebagai diuretik. Penelitian ini bertujuan untuk memformulasikan sediaan tablet menggunakan ekstrak akar manis (Glycyrrhiza glabra Linn.) dengan metode cetak langsung. Penelitian dilakukan dengan memvariasikan bahan pengisi dan bahan penghancur, yaitu F.I (35% avicel® PH 101 – 2% explotab), F.II (34,25% avicel® PH 101 – 2,75% explotab), F.III (33,5%
avicel® PH 101 – 3,5% explotab), F.IV (33% avicel® PH 101 – 4% explotab), dan F.V (32% avicel® PH 101 – 5% explotab). Dapat disimpulkan bahwa seluruh formula dapat dicetak menjadi tablet dengan F.V (32% avicel® PH 101 – 5%
explotab) memberikan hasil uji preformulasi dan uji evaluasi yang terbaik.
Harapan penulis semoga penelitian ini dapat bermanfaat bagi masyarakat dan menambah ilmu pengetahuan tentang kegunaan akar manis.
Pada kesempatan ini, penulis menyampaikan terima kasih yang sebesar- besarnya kepada Ibu T.Ismanelly Hanum, S.Si., M.Si., Apt., selaku dosen pembimbing juga sebagai dosen penasihat akademik yang telah memberikan
v
nasehat, bimbingan dan motivasi dengan penuh kesabaran, tulus dan ikhlas.
Bapak Prof. Dr. Hakim Bangun, Apt. dan Bapak Mariadi, S.Farm., M.Si., Apt., selaku penguji yang telah memberikan kritik, saran serta arahan kepada penulis dalam menyelesaikan skripsi ini. Penulis juga menyampaikan rasa hormat dan terima kasih kepada Ibu Khairunnisa S.Si., M.PHarm., PH.D, Apt., selaku Dekan Fakultas Farmasi Universitas Sumatera Utara.
Penulis juga mengucapkan terima kasih dan penghargaan yang tulus kepada kedua orangtua, Ayah Augustinus dan Ibu Lilysuriati, Adik Alexandra Dwi Putri, dan Adik Andrew Julius Triputra, yang telah memberikan cinta dan kasih sayang, doa, semangat, dorongan dan pengorbanan baik moril maupun materil kepada penulis selama ini.
Pada kesempatan ini, penulis juga menyampaikan rasa terima kasih kepada Wilson, Louis, Chelsea, Vellinda, Vivienne atas kebersamaan, dorongan, semangat dan dukungan selama ini, juga kepada ASTAB ’17 yang telah bekerja keras dan saling mendukung sampai titik ini, serta penulis ingin berterima kasih kepada diri sendiri yang telah bertahan dan berjuang hingga akhirnya dapat menyelesaikan skripsi ini.
Medan, 27 Juli 2021 Penulis,
Anggrainy Eka Putri NIM 171501114
vi
SURAT PERNYATAAN ORISINALITAS
Saya yang bertanda tangan di bawah ini:
Nama : Anggrainy Eka Putri
Nomor Induk Mahasiswa : 171501114 Program Studi : Sarjana Farmasi
Judul Skripsi : Formulasi Tablet Ekstrak Akar Manis (Glycyrrhiza glabra Linn.) dengan Variasi Komposisi Bahan Pengisi Avicel® PH 101 dan Bahan Penghancur Explotab
Dengan ini menyatakan bahwa skripsi yang saya buat adalah asli karya saya sendiri dan bukan plagiat. Apabila di kemudian hari diketahui skripsi saya tersebut terbukti plagiat karena kesalahan sendiri, maka saya bersedia diberi sanksi apapun oleh Program Studi Sarjana Farmasi Fakultas Farmasi Universitas Sumatera Utara. Saya tidak akan menuntut pihak manapun atas perbuatan saya tersebut. Demikian surat pernyataan ini saya perbuat dengan sebenarnya dan dalam keadaan sehat.
Medan, 22 Juli 2021
Anggrainy Eka Putri NIM 171501114
vii
FORMULASI TABLET EKSTRAK AKAR MANIS (Glycyrrhiza glabra Linn.) DENGAN VARIASI KOMPOSISI BAHAN PENGISI AVICEL®
PH 101 DAN BAHAN PENGHANCUR EXPLOTAB
ABSTRAK
Latar Belakang: Akar manis digunakan sebagai obat tradisional terutama untuk pengobatan tukak lambung, hepatitis C dan penyakit paru-paru dan kulit. Seiring dengan kemajuan ilmu pengetahuan dan teknologi, pemanfaatan tanaman akar manis berkembang sebagai bahan baku industri farmasi. Kelemahan utama mengkonsumsi akar manis dengan cara tradisional yaitu dikonsumsi sebagai obat secara langsung atau di dekoktasi sehingga tidak praktis dalam penggunaannya, maka dari itu dilakukan penelitian ini untuk memodifikasi sediaan dalam bentuk tablet.
Tujuan: Untuk mengetahui apakah ekstrak akar manis (Glycyrrhiza glabra Linn.) dengan variasi bahan pengisi dan bahan penghancur dapat dicetak menjadi tablet dengan metode cetak langsung, serta untuk mengetahui pengaruh variasi bahan pengisi dan bahan penghancur terhadap hasil evaluasi sifat fisik sediaan tablet.
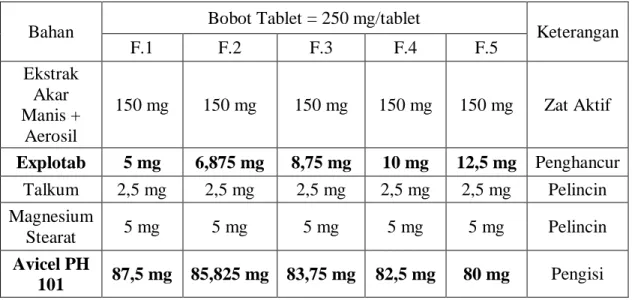
Metode: Serbuk simplisia akar manis diberi perlakuan skrining fitokimia dan karakterisasi simplisia, kemudian dibuat menjadi ekstrak kental menggunakan pelarut etanol 96% dengan cara maserasi selanjutnya ekstrak dikeringkan dengan aerosil (2:1). Tablet dibuat dengan metode cetak langsung dalam lima formula dengan variasi bahan pengisi avicel PH 101 dan bahan penghancur eksplotab yaitu formula I (35%-2%), formula II (34,25%-2,75%), formula III (33,5%-3,5%), formula IV (33%-4%), dan formula V (32%-5%). Granul yang diperoleh diuji preformulasi, kemudian granul dicetak menjadi tablet dan dilakukan uji evaluasi sediaan fisik meliputi uji keseragaman bobot, kekerasan, waktu hancur, dan friabilitas. Data kemudian dianalisis dengan metode ANOVA dan One Sample T- test.
Hasil: Hasil penelitian menunjukkan bahwa kelima formula dapat dicetak menjadi tablet dengan rata-rata hasil uji keseragaman bobot yaitu 279 mg, 265 mg, 285.5 mg, 274.5 mg, dan 262.5 mg; uji waktu hancur yaitu 14 menit, 10 menit 10 detik, 7 menit 9 detik, 5 menit 35 detik, dan 4 menit 8 detik; uji friabilitas yaitu 0.716%, 0.566%, 0.525%, 0.182%, dan 0.19%; uji kekerasan tablet yaitu 5.1 kg, 4 kg, 4.3 kg, 4.05 kg, dan 4.15 kg. Hasil dari kelima formula tersebut memenuhi persyaratan menurut Farmakope Indonesia edisi IV. Dari hasil analisis diketahui bahwa kelima formula tablet ekstrak akar manis menunjukkan perbedaan yang signifikan (p<0,05) pada keseragaman bobot, waktu hancur, dan friabilitas.
Kesimpulan: Seluruh formula dapat dicetak menjadi tablet dengan metode cetak langsung dan formula tablet dengan variasi bahan pengisi dan bahan penghancur pada formula V memberikan hasil uji preformulasi dan uji evaluasi yang paling optimal. Data statistik menunjukkan bahwa terdapat perbedaan pada rata-rata hasil pengujian keseragaman bobot, waktu hancur, dan friabilitas tetapi tidak menunjukkan perbedaan yang signifikan pada kekerasan tablet.
Kata Kunci: akar manis, avicel PH 101, eksplotab, cetak langsung
viii
TABLET FORMULATION OF LICORICE ROOT EXTRACT (Glycyrrhiza glabra Linn.) WITH VARIATION OF AVICEL® PH 101 AS FILLER-
BINDER AGENT AND EXPLOTAB AS DISINTEGRANT AGENT
ABSTRACT
Background: Licorice root has been used in traditional medicine especially for the treatment of stomach ulcers, hepatitis C and lungs and skin diseases. Along with advances in science and technology, the use of licorice root has developed as a raw material for the pharmaceutical industry. The main drawback of consuming licorice root with traditional way used as a medicine directly for consumption or in decoction is about the impracticality of its use. Therefore, the purpose of this study is to modify the dosage in tablet form.
Objective: To find out whether licorice root extract (Glycyrrhiza glabra Linn.) with a variety of filler-binder agent and disintegrant agent could be compressed into tablets using the direct compression method, as well as to find out the effect of variations of filler-binder agent and disintegrant agent on the evaluation results of the physical properties of the formulated tablets meet requirements of quality.
Method: The simplicia powder of licorice root was carried out by phytochemical screening and simplicia characterization. After that, it was made into a thick extract using 96% ethanol solvent by maceration. Then, the extract was dried with aerosil (2:1). Tablets were made by the direct compression method in five formulas with variations in the avicel PH 101 as filler-binder and the explotab as disintegrant agent, namely formula I (35%-2%), formula II (34.25%-2.75%), formula III (33,5%-3.5%), formula IV (33%-4%), and formula V (32%-5%). The obtained granules were subjected to a preformulation test. Next, the granules were compressed into tablets and finally an evaluation of the physical properties included tests of weight similarity, hardness, disintegration time, and friability was conducted. The data were than analyzed using ANOVA and One Sample T- test method.
Results: The results showed that all formulas could be compressed into tablets with the average of weight similarity results were 279 mg, 265 mg, 285.5 mg, 274.5 mg, and 262.5 mg; disintegration time tests were 14 minutes, 10 minutes 10 seconds, 7 minutes 9 seconds, 5 minutes 35 seconds, and 4 minutes 8 seconds;
friability tests were 0.716%, 0.566%, 0.525%, 0.182%, and 0.19%; tablet hardness tests were 5.1 kg, 4 kg, 4.3 kg, 4.05 kg, and 4.15 kg. These results met the requirements according to the 4th edition of Indonesian pharmacopoeia. The statistical analysis showed that there were significant differences (p<0.05) in weight similarity, disintegration time, and friability.
Conclusion: All formulas can be compressed into tablets with direct compression method and tablet formulas with variations of filler-binder and disintegrant agent in formula V provides the most optimal preformulation and evaluation test results.
Statistical data showed that there were differences in the average test results of weight similarity, disintegration time, and friability but did not show a significant difference in tablet hardness.
Keywords: licorice root, avicel PH 101, explotab, direct compression
ix DAFTAR ISI
HALAMAN SAMPUL ... i
HALAMAN JUDUL ... ii
HALAMAN PENGESAHAN ... iii
KATA PENGANTAR ... iv
HALAMAN PERNYATAAN ORISINALITAS ... vi
ABSTRAK ... vii
ABSTRACT ... viii
DAFTAR ISI ... ix
DAFTAR TABEL ... xii
DAFTAR GAMBAR ... xiii
DAFTAR LAMPIRAN ... xiv
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 6
1.3 Hipotesis ... 6
1.4 Tujuan Penelitian ... 7
1.5 Manfaat Penelitian ... 7
1.6 Kerangka Penelitian ... 8
BAB II TINJAUAN PUSTAKA ... 9
2.1 Uraian Tumbuhan ... 9
2.1.1 Sistematika Tumbuhan ... 9
2.1.2Sinonim Tumbuhan ... 9
2.1.3Nama Asing Tumbuhan ... 9
2.1.4 Morfologi Tumbuhan ... 9
2.1.5 Kandungan Kimia ... 10
2.1.6Khasiat Tumbuhan ... 10
2.2Ekstrak dan Metode Ekstraksi ... 12
2.2.1 Ekstrak ... 12
2.2.2 Metode Ekstraksi... 13
2.3Uraian Tablet ... 14
2.3.1 Metode Pembuatan Tablet ... 15
2.3.2 Bahan Tambahan dalam Sediaan Tablet ... 18
2.3.3 Komposisi Tablet ... 20
2.4Uraian Granul dan Uji Preformulasi ... 22
2.4.1 Granul ... 22
2.4.2 Uji Preformulasi ... 22
2.5Evaluasi Tablet ... 23
BAB III METODE PENELITIAN ... 25
3.1Tempat Pelaksanaan Penelitian... 25
3.2 Metode Penelitian ... 25
3.3 Alat dan Bahan... 25
3.3.1Alat ... 25
3.3.2Bahan ... 26
3.4 Penyiapan Sampel ... 26
3.4.1Pengambilan Sampel ... 26
3.4.2Identifikasi Sampel... 26
3.5 Karakterisasi Simplisia ... 27
x
3.5.1Pemeriksaan Makroskopik ... 27
3.5.2Pemeriksaan Mikroskopik ... 27
3.5.3Penetapan Kadar Air ... 27
3.5.4Penetapan Kadar Sari Larut Air ... 28
3.5.5Penetapan Kadar Sari Larut Etanol ... 28
3.5.6Penetapan Kadar Abu Total ... 28
3.5.7Penetapan Kadar Abu Tidak Larut Asam ... 29
3.6 Skrining Fitokimia Simplisia Akar Manis ... 29
3.6.1Pemeriksaan Alkaloid ... 29
3.6.2Pemeriksaan Flavonoida ... 30
3.6.3Pemeriksaan Glikosida ... 30
3.6.4Pemeriksaan Saponin ... 30
3.6.5Pemeriksaan Tanin ... 31
3.6.6Pemeriksaan Steroida/Triterpenoida ... 31
3.7 Pembuatan Ekstrak Etanol Akar Manis ... 31
3.8 Karakterisasi Ekstrak ... 32
3.9 Pembuatan Ekstrak Kering Akar Manis ... 32
3.10Penetapan Dosis dan Formula Pembuatan Tablet ... 32
3.11 Prosedur Pembuatan Tablet Ekstrak Akar Manis ... 34
3.11.1 Pembuatan Granul ... 34
3.11.2 Pencampuran Bahan ... 34
3.12Uji Preformulasi Granul ... 35
3.12.1 Indeks Tap ... 35
3.12.2 Waktu Alir ... 35
3.12.3 Sudut Diam ... 36
3.12.4 Kelembaban Granul ... 36
3.13 Uji Evaluasi Sifat Fisik Tablet ... 36
3.13.1 Uji Keseragaman Bobot ... 36
3.13.2 Uji Friabilitas ... 37
3.13.3 Uji Kekerasan ... 38
3.13.4 Uji Waktu Hancur ... 38
3.14 Analisis Data ... 38
BAB IV HASIL DAN PEMBAHASAN... 40
4.1Hasil Identifikasi Tumbuhan ... 40
4.2 Hasil Karakterisasi Simplisia ... 40
4.2.1Pemeriksaan Makroskopik ... 40
4.2.2Pemeriksaan Mikroskopik ... 40
4.2.3Hasil Uji Karakterisasi Simplisia ... 40
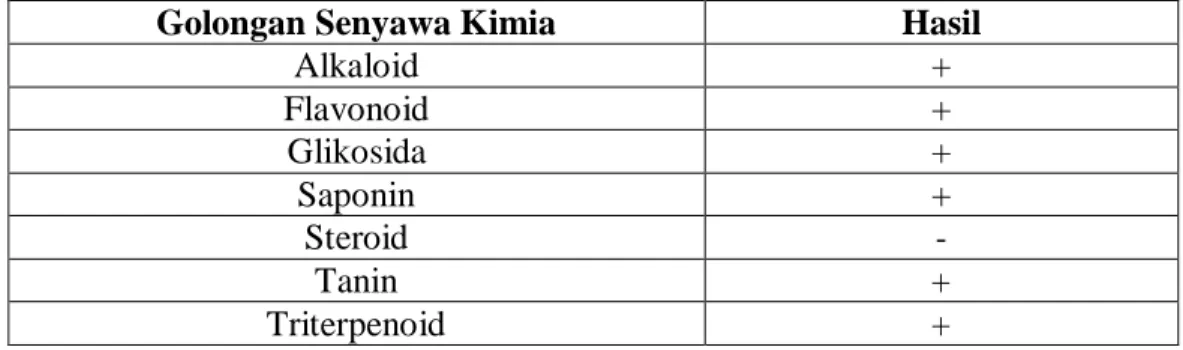
4.3Hasil Skrining Fitokimia Simplisia Akar Manis ... 42
4.4 Hasil Ekstraksi Akar Manis ... 42
4.5 Hasil Karakterisasi Ekstrak ... 43
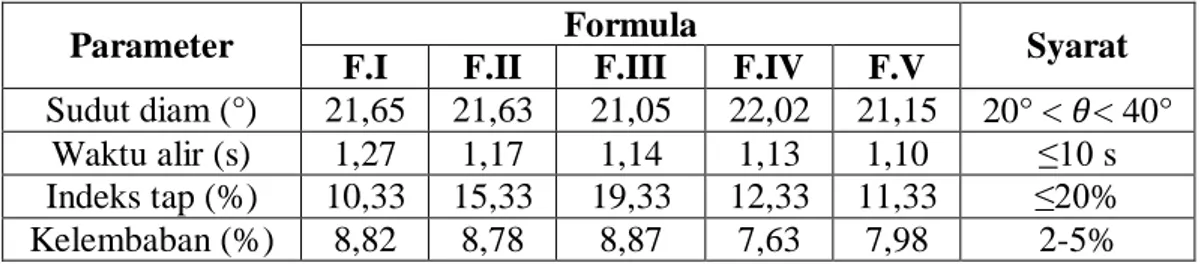
4.6 Hasil Uji Preformulasi Granul ... 43
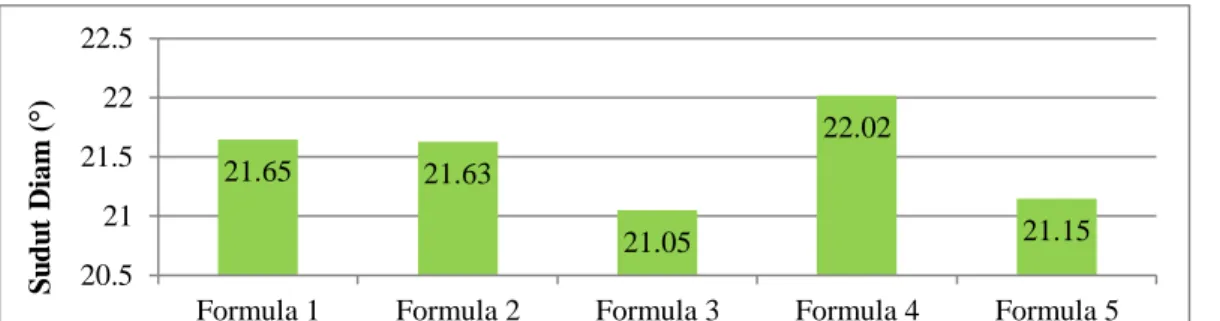
4.6.1Sudut Diam ... 44
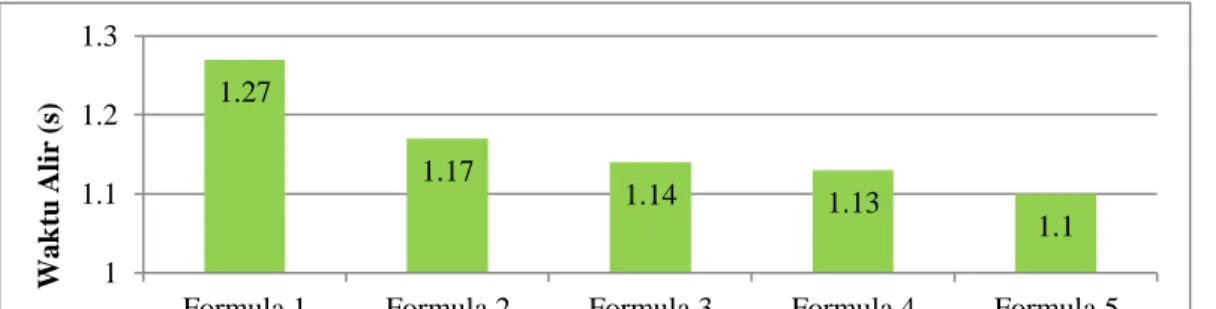
4.6.2Waktu Alir ... 45
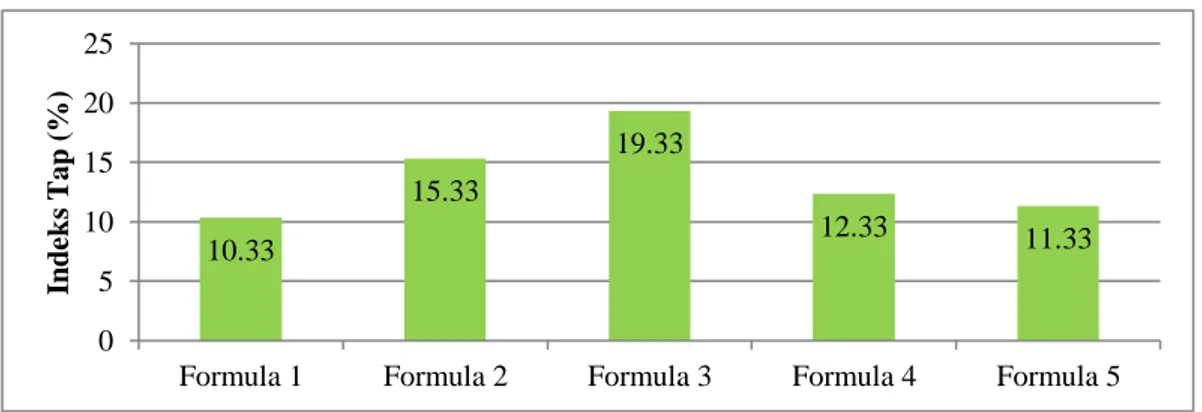
4.6.3Indeks Tap ... 46
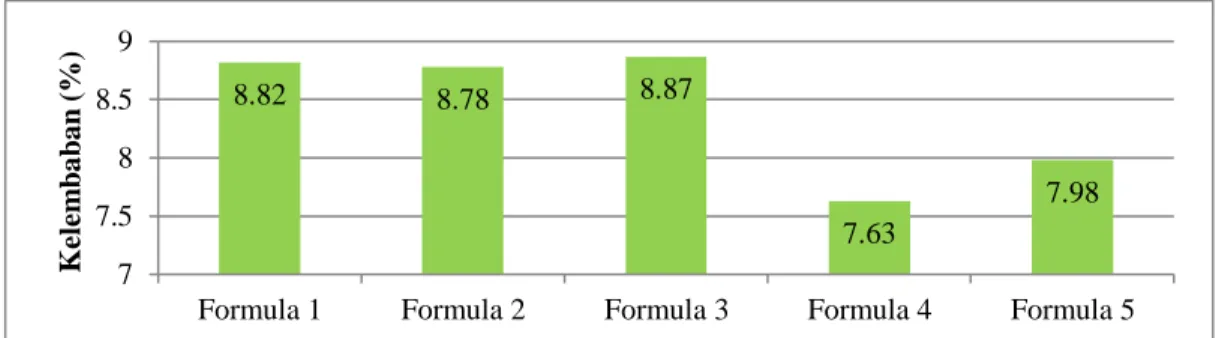
4.6.4 Kelembaban Granul... 48
4.7Hasil Uji Evaluasi Tablet ... 49
4.7.1Keseragaman Bobot ... 50
4.7.2Waktu Hancur ... 52
xi
4.7.3Kekerasan ... 53
4.7.4Uji Friabilitas ... 54
BAB V KESIMPULAN DAN SARAN ... 58
5.1 Kesimpulan ... 58
5.2 Saran ... 58
DAFTAR PUSTAKA ... 59
LAMPIRAN 63
xii
DAFTAR TABEL
Tabel 3.1 Formula Tablet Ekstrak Akar Manis ... 34
Tabel 3.2 Syarat Penyimpangan Bobot ... 37
Tabel 4.1 Hasil Karakterisasi Simplisia Akar Manis ... 40
Tabel 4.2 Hasil Skrining Fitokimia Simplisia Akar Manis ... 42
Tabel 4.3 Hasil Karakterisasi Ekstrak Akar Manis ... 43
Tabel 4.4 Hasil Pengujian Preformulasi Granul ... 43
Tabel 4.5 Hasil Pengujian Evaluasi Tablet ... 50
Tabel 4.6 Hasil Uji Keseragaman Bobot Tablet ... 50
xiii
DAFTAR GAMBAR
Gambar 1.1 Diagram Kerangka Pikir Penelitian ... 8
Gambar 4.1 Histogram Hasil Uji Sudut Diam Granul ... 44
Gambar 4.2 Histogram Hasil Uji Waktu Alir Granul ... 45
Gambar 4.3 Histogram Hasil Uji Indeks Tap Granul ... 46
Gambar 4.4 Histogram Hasil Uji Kelembaban Granul ... 48
Gambar 4.5 Histogram Hasil Uji Waktu Hancur Tablet ... 52
Gambar 4.6 Histogram Hasil Uji Kekerasan Tablet ... 53
Gambar 4.7 Histogram Hasil Uji Friabilitas Tablet ... 55
xiv
DAFTAR LAMPIRAN
1. Hasil Identifikasi Akar Manis 63
2. Gambar Simplisia Akar Manis, Serbuk Akar Manis, dan Ekstrak Kental Akar Manis 64
3. Hasil Mikroskopik Serbuk Akar Manis 65
4. Gambar Alat-alat yang digunakan 66
5. Gambar Granul Kering Ekstrak Akar Manis, Granul Eksipien, Granul Formula I, II, III, IV, dan V 68
6. Gambar Sediaan Tablet Ekstrak Akar Manis 70
7. Bagan Alir Pengujian Simplisia Akar Manis 71
8. Bagan Alir Pembuatan Ekstrak Etanol Akar Manis 72
9. Bagan Alir Pembuatan Tablet Ekstrak Akar Manis 73
10. Bagan Alir Uji Preformulasi Granul 74
11. Bagan Alir Pencetakan Tablet 76
12. Bagan Alir Uji Evaluasi Tablet 77
13. Perhitungan Hasil Karakterisasi Simplisia Akar Manis 79
14. Perhitungan Persen (%) Rendemen Ekstrak 82
15. Perhitungan Hasil Karakterisasi Ekstrak Akar Manis 83
16. Perhitungan Bahan Formula Tablet 85
17. Perhitungan Hasil Uji Preformulasi Granul 88
18. Perhitungan Hasil Uji Evaluasi Tablet 90
19. Perhitungan Dosis Ekstrak Akar Manis 95
20. Hasil Pengujian Statistika Data Evaluasi Tablet 96
1 BAB I PENDAHULUAN
1.1 Latar Belakang
Penggunaan obat tradisional secara umum dinilai lebih aman dibandingkan penggunaan obat modern. Hal ini disebabkan karena obat tradisional memiliki efek samping yang relatif lebih sedikit daripada obat modern. Akan tetapi diperlukan penggunaan secara tepat untuk meminimalisir efek sampingnya, yang meliputi kebenaran obat, ketepatan dosis, ketepatan waktu penggunaan, ketepatan cara penggunaan, ketepatan telaah informasi, dan tanpa penyalahgunaan obat tradisional itu sendiri (Sumayyah dan Salsabila, 2017).
Obat-obat kimia seperti ranitidin, famotidin, dan simetidin memiliki indikasi pengobatan tukak lambung. Akan tetapi, obat-obat kimia tersebut memiliki efek samping seperti sakit kepala, diare, demam, dan lain-lain (ISO, 2017). Menurut WHO (1998), negara-negara di Afrika, Asia dan Amerika Latin menggunakan obat herbal sebagai pelengkap pengobatan primer yang mereka terima. Penggunaan obat tradisional cukup gencar dilakukan karena lebih mudah dijangkau masyarakat Indonesia, baik harga maupun ketersediaannya. Obat tradisional pada saat ini banyak digunakan karena menurut beberapa penelitian tidak terlalu menyebabkan efek samping (Parwata, 2016). Oleh karena itu, peneliti memformulasikan ekstrak akar manis yang diketahui memiliki banyak khasiat dalam bentuk sediaan tablet.
Akar manis memiliki sifat farmakologis yang bermanfaat seperti anti- inflamasi, antivirus, antimikroba, antioksidan, antikanker dan imunomodulator.
Akar manis yang dikenal sebagai kayu legi juga digunakan sebagai obat
2
tradisional terutama untuk pengobatan tukak lambung, hepatitis C dan penyakit paru-paru dan kulit. Akar kering akar manis telah digunakan sebagai ekspektoran dan karminatif oleh orang Mesir, Cina, Yunani, India dan peradaban Romawi, juga digunakan sebagai oftalmia, anti-sifilis dan antidisentri, gangguan pencernaan, tenggorokan kering, abses bengkak dan bertindak sebagai diuretik (Dastagir dan Rizvi, 2016).
Akar manis dinyatakan memiliki khasiat sebagai ekspektoran, penawar racun, antispasmodik, anti-inflamasi dan pencahar. Secara tradisional, akar manis juga dilaporkan mempengaruhi kelenjar adrenal. Akar manis telah digunakan untuk mengobati penyakit selesema bronkial, bronkitis, gastritis kronis, tukak lambung, kolik dan insufisiensi adrenokortikal primer (Barnes et al., 2007).
Pada penelitian Rivai, dkk., (2020) tentang analisis fitokimia ramuan herbal tradisional untuk batuk dari akar manis (Glycyrrhiza glabra Linn.) dan penelitian Ringoringo dan Choiriyah (2018) tentang formulasi tablet kunyah ekstrak akar manis (Succus liquiritae) dengan kombinasi bahan pengisi sorbitol-laktosa terhadap pengaruh sifat fisik tablet kunyah menggunakan metode kempa langsung memiliki khasiat sebagai antitusif. Kandungan aktif dari akar manis yaitu 18 β- glycyrrhetinic acid yang menunjukkan efek antitusif yang bekerja untuk menekan reaksi batuk. Dari penelitian-penelitian sebelumnya, akar manis banyak digunakan oleh masyarakat dan industri farmasi sebagai obat batuk dalam bentuk ramuan dan tablet hisap, maka pada penelitian ini dilakukan modifikasi yaitu pembuatan formulasi tablet ekstrak akar manis yang penggunaannya digunakan secara oral.
Dosis untuk pemberian oral (dewasa) dengan penggunaan secara tradisional direkomendasikan dalam standar herbal yang lebih tua dan
3
kontemporer dan /atau teks referensi farmasi. Serbuk akar manis sebanyak 1 – 4 gram sebagai rebusan tiga kali sehari. Dalam bentuk ekstrak (BPC, 1973) 0,6 – 2,0 gram (Barnes et al., 2007). Menurut Farmakope Indonesia edisi V (2009), kadar glisirizin pada ekstrak akar manis (Glycyrrhizae Succus) tidak kurang dari 10% dihitung terhadap zat yang telah dikeringkan.
Menurut penelitian Santoso (2017) tentang efektivitas infusa akar manis sebagai anti tukak lambung tikus yang diinduksi asetosal, hasil yang paling optimal terlihat pada dosis 15 mg/200 g BB tikus yang setara dengan 595.236 mg/
50 kg BB manusia. Akar manis mempunyai kandungan saponin dikenal dengan glisirisin yang menghasilkan aktivitas anti ulkus dengan cara menginhibisi 15- hidroksi prostaglandin dehidrogenase dan prostaglandin reduktase. Menurut penelitian. Amin, dkk., (2015) tentang sifat antiulcer ekstrak Glycyrrhiza Glabra L. pada model eksperimen ulkus lambung mencit menunjukkan bahwa akar manis (50-150 mg/kg) menunjukkan aktivitas antiulcer terhadap lesi lambung yang diinduksi indometasin.
Dalam penelitian ini, digunakan metode kombinasi dimana sediaan tablet akan diformulasikan dengan cara menggranulasi eksipien (explotab internal dan avicel® PH 101) dengan metode granulasi basah, kemudian granul kering eksipien dan ekstrak kering akar manis dicampurkan dan dicetak menjadi tablet menggunakan metode cetak langsung dengan berat 250 mg per tablet. Menurut penelitian Krahenbuhl, dkk. (1994), diketahui waktu paruh dengan dosis 500 mg adalah kurang dari 10 jam, maka tablet ekstrak akar manis dapat dikonsumsi satu sampai dua tablet sesuai dengan kebutuhan, dimana akar manis tidak hanya berkhasiat sebagai anti ulkus tetapi juga berkhasiat sebagai ekspektoran pada dosis 50 mg/kg dan sebagai antitusif pada dosis 200 mg/kg (Kuang, dkk., 2017).
4
Pemilihan sediaan dalam bentuk tablet adalah karena penggunaannya yang sangat luas sebagai sediaan obat, tablet terbukti menunjukkan suatu bentuk yang efisien, sangat praktis, dan ideal untuk pemberian zat aktif secara oral (Murtini dan Elisa, 2018). Beberapa keuntungan sediaan tablet antara lain volumenya yang kecil tetapi dapat mengandung zat aktif dalam jumlah yang besar, merupakan bentuk sediaan oral yang paling ringan dan kompak sehingga memudahkan dalam pengemasan dan penyimpanannya, mengandung dosis zat aktif yang tepat, merupakan sediaan kering sehingga zat aktif lebih stabil baik secara kimiawi maupun fisiologik, bentuk sediaan yang sesuai untuk zat aktif yang sukar larut dalam air, rasa dan bau yang tidak enak dari zat aktif akan berkurang dalam sediaan tablet, karena ketika ditelan, tidak berkontak lama dengan selaput lendir, pelepasan zat aktif dari suatu tablet dapat diatur untuk tujuan tertentu (Lachman, et al., 1986).
Tablet adalah sediaan padat kompak, dibuat secara kempa cetak, dalam bentuk tabung pipih atau sirkuler, kedua permukaannya rata atau cembung, mengandung satu jenis obat atau lebih, dengan atau tanpa bahan tambahan. Bahan tambahan yang dapat berfungsi sebagai bahan pengisi, pengembang, pengikat, pembasah atau bahan lain yang cocok (Depkes RI, 1979).
Istilah kempa langsung telah lama digunakan untuk memperkenalkan pengempaan senyawa kristalin tunggal menjadi suatu padatan tanpa penambahan zat-zat lain. Hanya sedikit bahan kimia yang mempunyai sifat alir, kohesi, dan lubrikasi di bawah tekanan untuk membuat padatan. Sekarang istilah kempa langsung digunakan untuk menyatakan proses ketika tablet dikempa langsung dari campuran serbuk zat aktif dan eksipien yang sesuai (termasuk pengisi, disintegran, dan lubrikan), yang akan mengalir dengan seragam ke dalam lubang
5
kempa dan membentuk suatu padatan yang kokoh (Siregar dan Wikarsa, 2010).
Pada metode cetak langsung syarat suatu bahan tambahan yang digunakan adalah memiliki sifat alir dan kompresibilitas yang baik. Salah satu bahan tambahan yang digunakan adalah bahan pengisi. Avicel PH 101 merupakan serbuk yang digunakan secara luas dalam pembuatan tablet kempa langsung dan menunjukan kekerasan dan friabilitas yang baik. Avicel memiliki fungsi kemampuan yang baik sebagai pengikat maupun disintegran dalam beberapa formula tablet (Sa’adah, dkk., 2016). Bahan pengisi lainnya yang umum digunakan dalam pembuatan tablet dengan metode cetak langsung antara lain Avicel PH 102 atau Microcrystalline Cellulose, Spray Dried Lactose (SDL), Starch 1500, dan encompress (Hadisoewignyo, dkk., 2011).
Penggunaan bahan penghancur bertujuan untuk memecah bentuk sediaan menjadi partikel kecil sehingga zat aktif obat dapat terlepas dari bentuk sediaannya. Eksplotab merupakan bahan penghancur yang paling baik dan sangat populer yang dikenal dengan nama superdisintegrant. Eksplotab adalah modifikasi dari kanji, digunakan dalam konsentrasi rendah (1–8%) (Banker dan Anderson, 1986).
Pada penelitian ini, dilakukan formulasi tablet ekstrak akar manis (Glycyrrhiza glabra Linn.) dengan metode cetak langsung menggunakan avicel® PH 101 sebagai bahan pengisi dan eksplotab sebagai bahan penghancur yang kemudian dilakukan uji evaluasi sifat fisik tablet untuk mengetahui kualitas tablet yang tercetak.
6 1.2 Perumusan Masalah
Berdasarkan latar belakang di atas, maka perumusan masalah dalam penelitian ini adalah:
1. Apakah ekstrak akar manis (Glycyrrhiza glabra Linn.) dengan variasi komposisi bahan pengisi avicel® PH 101 dan bahan penghancur eksplotab dapat dicetak menjadi tablet dengan metode cetak langsung?
2. Bagaimana pengaruh variasi jumlah bahan pengisi dan bahan penghancur yang digunakan terhadap evaluasi sifat fisik sediaan tablet ekstrak akar manis (Glycyrrhiza glabra Linn.)?
1.3 Hipotesis
Berdasarkan perumusan masalah di atas, maka hipotesis dalam penelitian ini diduga:
1. Ekstrak akar manis (Glycyrrhiza glabra Linn.) dengan variasi komposisi bahan pengisi avicel® PH 101 dan bahan penghancur eksplotab dapat dicetak menjadi tablet dengan metode cetak langsung.
2. Variasi bahan pengisi dan bahan penghancur memberikan pengaruh terhadap hasil evaluasi sifat fisik sediaan tablet ekstrak akar manis (Glycyrrhiza glabra Linn.).
7 1.4 Tujuan Penelitian
Berdasarkan hipotesis di atas, maka tujuan penelitian ini adalah:
1. Untuk mengetahui apakah ekstrak akar manis (Glycyrrhiza glabra Linn.) dengan variasi komposisi bahan pengisi avicel® PH 101 dan bahan penghancur eksplotab dapat dicetak menjadi tablet dengan metode cetak langsung.
2. Untuk mengetahui pengaruh variasi bahan pengisi dan bahan penghancur terhadap hasil evaluasi sifat fisik sediaan tablet ekstrak akar manis (Glycyrrhiza glabra Linn.).
1.5 Manfaat Penelitian
Memberikan informasi kepada masyarakat mengenai pemanfaatan akar manis (Glycyrrhiza glabra Linn.) yang dapat diformulasikan menjadi sediaan tablet.
8 1.6 Kerangka Penelitian
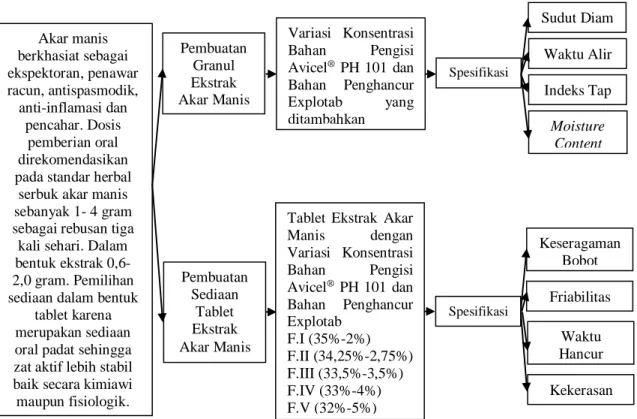
Gambar 1.1 Diagram Kerangka Pikir Penelitian
Akar manis berkhasiat sebagai ekspektoran, penawar racun, antispasmodik, anti-inflamasi dan
pencahar. Dosis pemberian oral direkomendasikan pada standar herbal
serbuk akar manis sebanyak 1- 4 gram sebagai rebusan tiga kali sehari. Dalam bentuk ekstrak 0,6- 2,0 gram. Pemilihan sediaan dalam bentuk
tablet karena merupakan sediaan oral padat sehingga zat aktif lebih stabil baik secara kimiawi maupun fisiologik.
Pembuatan Granul Ekstrak Akar Manis
Pembuatan Sediaan
Tablet Ekstrak Akar Manis
Tablet Ekstrak Akar Manis dengan Variasi Konsentrasi Bahan Pengisi Avicel® PH 101 dan Bahan Penghancur Explotab
F.I (35%-2%) F.II (34,25%-2,75%) F.III (33,5%-3,5%) F.IV (33%-4%) F.V (32%-5%)
Spesifikasi Variasi Konsentrasi
Bahan Pengisi Avicel® PH 101 dan Bahan Penghancur Explotab yang ditambahkan
Sudut Diam Waktu Alir Indeks Tap Moisture
Content
Keseragaman Bobot Friabilitas
Kekerasan Waktu Hancur Spesifikasi
Variabel Bebas
Variabel Terikat
Parameter
9 BAB II
TINJAUAN PUSTAKA
2.1 Uraian Tumbuhan 2.1.1 Sistematika Tumbuhan
Secara lengkap sistematika akar manis (Glycyrrhiza glabra L.) hasil identifikasi sampel dari Herbarium Medanense (2020) sebagai berikut:
Kingdom : Plantae
Divisi : Spermatophyta Kelas : Dicotyledoneae Ordo : Fabales
Famili : Papilionaceae Genus : Glycyrrhiza
Spesies : Glycyrrhiza glabra L.
Nama lokal : Akar manis 2.1.2 Sinonim Tumbuhan
Akar manis (Indonesia), Licoric (Amerika), Liquorice (Inggris), Gan Cao (Cina) (Wahyuno, dkk., 2020).
2.1.3 Nama Asing Tumbuhan
Jashtimadhu (Bangla); Muleti (Punjabi); Mithi Kathi (Sindhi); KhoshaWalgi (Pushto); Rub-us-soos (Arab); Bikhemahaka (Persia); Moyo (Chitrali); Boisdoux (Prancis), Regalizia (Spanyol) (Dastagir dan Rizvi, 2016).
2.1.4 Morfologi Tumbuhan
Akar manis (G. glabra) termasuk famili Papilionaceae, berupa tanaman tahunan berbentuk terna dan dapat tumbuh tinggi sampai satu meter dengan daun
10
yang tumbuh seperti sayap (pinnate) yang panjangnya 7 sampai 15 cm, dengan jumlah daun 9-17 helai dalam satu cabang. Bunga akar manis tersusun secara inflorescens (berkelompok dalam satu cabang), warnanya berkisar dari keunguan sampai putih kebiru-biruan serta berukuran panjang 0,8–1,2 cm. Buah akar manis berpolong dan berbentuk panjang 2–3cm, dan mengandung biji. Akar manis tumbuh dengan baik di tanah yang dalam, subur, cukup air dan dalam iklim yang penuh cahaya matahari. Biasanya dipanen pada musim gugur 2 atau 3 tahun setelah penanaman. Zat yang terkandung di dalamnya adalah glycyrrhizin (Wahyuno, dkk., 2020).
2.1.5 Kandungan Kimia
Akar manis mengandung berbagai komponen kimia yaitu gula, flavonoid, sterol, asam amino, resin, pati, minyak atsiri dan saponin. Saponin utama mengandung asam glisirizat atau glycyrrhizin (C42H62O16), terbanyak terdapat pada akar mencapai 6% - 20% berat kering. Asam amino yang terdapat pada akar manis adalah asam-2-betaglisirizat, asam glukuronat, asam glisiretinat (enoxolone), asam tanat, asparagin, resin, minyak atsiri. Flavonoid seperti liquiritigenin, liquiritin, isoliquiritigenin, isoliquiritin dan senyawa kumarin, seperti herniarin dan umbeliferon. Flavonoid paling terkenal yang ditemukan oleh Organisasi Standardisasi Internasional pada akar manis adalah senyawa glabridin, gliserin flavon, glabren, glabril, formononetin, isoliquiritigenin (Wahyuno, dkk.., 2020).
2.1.6 Khasiat Tumbuhan
Akar manis memiliki sifat farmakologis yang bermanfaat seperti anti- inflamasi, antivirus, antimikroba, antioksidan, antikanker dan imunomodulator.
Akar manis yang dikenal sebagai kayu legi juga digunakan sebagai obat
11
tradisional terutama untuk pengobatan tukak lambung, hepatitis C dan penyakit paru-paru dan kulit. Akar kering akar manis telah digunakan sebagai ekspektoran dan karminatif oleh orang Mesir, Cina, Yunani, India dan peradaban Romawi, juga digunakan sebagai oftalmia, anti-sifilis dan antidisentri, gangguan pencernaan, tenggorokan kering, abses bengkak dan bertindak sebagai diuretik (Dastagir dan Rizvi, 2016).
Akar manis dinyatakan memiliki khasiat sebagai ekspektoran, penawar racun (demolient), antispasmodik, anti-inflamasi dan pencahar. Secara tradisional, akar manis juga dilaporkan mempengaruhi kelenjar adrenal. Akar manis telah digunakan untuk mengobati penyakit selesema bronkial, bronkitis, gastritis kronis, tukak lambung, kolik dan insufisiensi adrenokortikal primer (Barnes et al., 2007).
Glycyrrhizin merupakan zat aktif yang terdapat dalam akar manis secara spesifik mengurangi penurunan prostlaglandin E (PGE). Kadar PGE yang rendah berhubungan dengan keadaan perut seperti kolik, inflamasi perut, dan ulkus.
Dengan mengurangi penurunan prostlagandin E tubuh maka glisirizin menyediakan lebih banyak PGE yang bersirkulasi pada darah. Dari peningkatan kadar PGE maka akan meningkatkan produksi mukus dan mengurangi produksi asam lambung. Efek tersebut membantu melindungi jaringan lambung, sehingga nyata bahwa akar manis dapat digunakan untuk perawatan ulkus (Tanaka et al., 2001).
Glycyrrhiza glabra menunjukkan efek gastroprotektif potensial dalam studi praklinis dan klinis. Mekanisme yang berhubungan dengan efek antiulserogeniknya adalah peningkatan sekresi musin, peningkatan pelepasan prostaglandin E2, dan penurunan leukotrien. Efek gastroprotektifnya terkait erat dengan aktivitas antioksidan dan antiinflamasinya (Nugroho, dkk., 2016).
12
Mekanisme tersebut mirip dengan mekanisme analog prostaglandin, dimana analog prostaglandin memiliki mekanisme kerja mengurangi sekresi asam lambung, menambah sekresi mukus, sekresi bikarbonat dan meningkatkan aliran darah mukosa.
Dosis untuk pemberian oral (dewasa) dengan penggunaan secara tradisional direkomendasikan dalam standar herbal yang lebih tua dan kontemporer dan / atau teks referensi farmasi. Serbuk akar manis sebanyak 1 – 4 gram sebagai rebusan tiga kali sehari. Dalam bentuk ekstrak (BPC, 1973) 0,6 – 2,0 gram (Barnes et al., 2007). Menurut Farmakope Indonesia edisi V (2009), kadar glisirizin pada ekstrak akar manis (Glycyrrhizae Succus) tidak kurang dari 10%
dihitung terhadap zat yang telah dikeringkan.
Ikhtisar Efek Sistemik: Paparan kronis sedang atau akut terhadap asam glisirizin, amonium glisirizat, dan metabolitnya telah terbukti menyebabkan beberapa perubahan sistemik sementara, termasuk peningkatan ekskresi kalium, retensi natrium dan air, penambahan berat badan, alkalosis, penekanan renin- sistem angiotensis-aldosteron, hipertensi, dan kelumpuhan otot. Sebagian besar efek ini adalah konsekuensi dari penghambatan asam glisirizin dari enzim 11β- hydroxysteroid dehydrogenase-2 (11β-OHSD2) di ginjal (Andersen, 2007). Dari paparan tersebut dapat diketahui bahwa glisirizin dapat diabsorpsi secara sistemik.
2.2 Ekstrak dan Metode Ekstraksi 2.2.1 Ekstrak
Ekstrak adalah sediaan kering, kental atau cair dibuat dengan menyari simplisia nabati atau hewani menurut cara yang cocok di luar pengaruh cahaya matahari langsung (Depkes RI, 1979).
13
Ekstraksi adalah kegiatan penarikan kandungan kimia yang dapat larut sehingga terpisah dari bahan yang tidak dapat larut dengan menggunakan suatu pelarut cair. Dengan diketahuinya senyawa aktif yang dikandung simplisia akan mempermudah pemilihan pelarut dengan cara ekstraksi yang tepat (Depkes RI, 2000).
2.2.2 Metode Ekstraksi
Menurut Depkes RI (2000), beberapa metode ekstraksi yang sering digunakan dalam berbagai penelitian antara lain, yaitu:
1. Cara Dingin
a. Maserasi, adalah proses pengekstraksi simplisia dengan menggunakan pelarut dengan beberapa kali pengocokan atau pengadukan pada temperatur ruangan (kamar). Secara teknologi termasuk ekstraksi dengan prinsip metode pencapaian konsentrasi pada keseimbangan. Maserasi kinetik berarti dilakukan pengadukan yang kontinu (terus-menerus). Remaserasi berarti dilakukan pengulangan penambahan pelarut setelah dilakukan penyaringan maserat pertama dan seterusnya.
b. Perkolasi, adalah ekstraksi dengan pelarut yang selalu baru sampai sempurna (exhaustive extraction) yang umumnya dilakukan pada temperatur ruangan.
Proses terdiri dari tahapan pengembangan bahan, tahap maserasi antara, tahap perkolasi sebenarnya (penetesan/penampungan ekstrak) terus-menerus sampai diperoleh ekstrak (perkolat) yang jumlahnya 1-5 kali.
2. Cara Panas
a. Refluks, adalah proses penyarian simplisia dengan menggunakan alat pada temperatur titik didihnya, selama waktu tertentu dan jumlah pelarut terbatas yang relatif konstan dengan adanya pendingin balik.
14
b. Digesti, adalah proses penyarian dengan pengadukan kontinu pada temperatur yang lebih tinggi dari pada temperatur ruangan, yaitu secara umum dilakukan pada temperatur 40o-50oC.
c. Sokletasi, adalah proses penyarian dengan menggunakan pelarut yang selalu baru, dilakukan dengan menggunakan alat soklet sehingga menjadi ekstraksi kontinu dengan pelarut relatif konstan dengan adanya pendingin balik.
d. Infundasi, adalah proses penyarian dengan menggunakan pelarut air pada temperatur 90oC selama 15 menit.
e. Dekoktasi, adalah proses penyarian dengan menggunakan pelarut air pada temperatur 90oC selama 30 menit.
2.3 Uraian Tablet
Tablet adalah sediaan padat kompak, dibuat secara kempa cetak, dalam bentuk tabung pipih atau sirkuler, kedua permukaannya rata atau cembung, mengandung satu jenis obat atau lebih, dengan atau tanpa bahan tambahan. Bahan tambahan yang dapat berfungsi sebagai bahan pengisi, pengembang, pengikat, pembasah atau bahan lain yang cocok (Depkes RI, 1979).
Sebagian besar tablet dibuat dengan cara pengempaan dan merupakan bentuk sediaan yang paling banyak digunakan. Tablet kempa dibuat dengan memberikan tekanan tinggi pada serbuk atau granul menggunakan cetakan baja.
Tablet dapat dibuat dalam berbagai ukuran, bentuk dan penandaan permukaan tergantung pada desain cetakan (Depkes RI, 1995).
Tablet dicetak dari serbuk kering, kristal atau granulat, umumnya dengan penambahan bahan pembantu, pada mesin yang sesuai, dengan menggunakan tekanan tinggi. Tablet dapat memiliki bentuk silinder, kubus, batang atau cakram,
15
serta bentuk seperti telur atau peluru. Garis tengah tablet pada umumnya 5-17 mm, sedangkan bobot tablet 0,1-1 g (Voight, 1995).
Obat-obat diberikan secara oral dalam bentuk sediaan farmasi yang beragam, masing-masing dengan keuntungan terapeutik yang mengakibatkan penggunaannya yang selektif oleh dokter. Perbedaan ukuran dan warna dari tablet dalam perdagangan, serta sering menggunakan monogram dari symbol perusahaan nomor kode, memudahkan pengenalannya oleh orang-orang yang dilatih menggunakannya dan bermanfaat sebagai tambahan perlindungan bagi kesehatan masyarakat (Ansel, 2008).
Menurut Banker dan Anderson (1994), tablet dinyatakan baik harus memenuhi kriteria sebagai berikut:
a. Memiliki kemampuan atau daya tahan terhadap pengaruh mekanis selama proses produksi, pengemasan dandistribusi;
b. Bebas dari kerusakan seperti pecah pada permukaan dari sisi-sisitablet;
c. Dapat menjamin kestabilan fisik maupun kimia dari zat berkhasiat yang terkandung didalamnya;
d. Dapat membebaskan zat berkhasiat dengan baik sehingga memberikan efek pengobatan seperti yang dikehendaki.
2.3.1 Metode Pembuatan Tablet
Tablet dibuat dengan 3 cara umum, yaitu granulasi basah, granulasi kering dan kempa langsung (Depkes RI, 1995).
Metode pembuatan tablet didasarkan pada sifat fisika kimia dari bahan obat, seperti stabilitas dari bahan aktif dalam panas atau terhadap air, bentuk partikel bahan aktif dan sebagainya. Metode pembuatan sediaan tablet yaitu:
a. Cetak langsung
16
Cetak langsung adalah pencetakan bahan obat atau campuran bahan obat dan bahan pembantu tanpa proses pengolahan awal. Cara ini hanya dilakukan untuk bahan-bahan tertentu saja yang berbentuk butir-butir granul yang mempunyai sifat-sifat yang diperlukan untuk membuat tablet yang baik.
Istilah kempa langsung telah lama digunakan untuk memperkenalkan pengempaan senyawa kristalin tunggal (biasanya garam anorganik dengan struktur kristal kubik seperti natrium klorida, natrium bromida, atau kalium bromida) menjadi suatu padatan tanpa penambahan zat-zat lain. Hanya sedikit bahan kimia yang mempunyai sifat alir, kohesi, dan lubrikasi di bawah tekanan untuk membuat padatan seperti ini (Siregar dan Wikarsa, 2010).
Sekarang istilah kempa langsung digunakan untuk menyatakan proses ketika tablet dikempa langsung dari campuran serbuk zat aktif dan eksipien yang sesuai (termasuk pengisi, disintegran, dan lubrikan), yang akan mengalir dengan seragam ke dalam lubang kempa dan membentuk suatu padatan yang kokoh. Tidak ada prosedur praperlakuan granulasi basah atau kering yang diperlukan pada campuran serbuk (Siregar dan Wikarsa, 2010).
Keuntungan metode kempa langsung yaitu: 1. Lebih ekonomis karena validasi proses lebih sedikit; 2. Lebih singkat prosesnya. Karena proses yang dilakukan lebih sedikit, maka waktu yang diperlukan untuk menggunakan metode ini lebih singkat, tenaga dan mesin yang dipergunakan juga lebih sedikit; 3. Dapat digunakan untuk zat aktif yang tidak tahan panas dan tidak tahan lembab (Siregar dan Wikarsa, 2010).
Pada penelitian Ringoringo dan Choiriyah (2018) tentang formulasi tablet kunyah ekstrak akar manis (Succus liquiritae) dengan kombinasi bahan pengisi sorbitol-laktosa terhadap pengaruh sifat fisik tablet kunyah menggunakan metode
17
kempa langsung menghasilkan sifat fisik tablet yang berbeda-beda tetapi tidak menunjukkan perbedaan yang signifikan dan memenuhi syarat pada Farmakope Indonesia. Pada penelitian Sa’adah et al., (2016) tentang formulasi granul ekstrak daun kersen (Muntingia calabura L.) menggunakan aerosil dan avicel PH 101 dengan metode granulasi basah dimana aerosil dan avicel PH 101 digunakan sebagai eksipien. Aerosil dengan konsentrasi 0-20% berfungsi sebagai adsorbent dan avicel berupa uap silika submikroskopik, ringan, dan tidak berasa. Avicel PH 101 dengan konsentrasi 20-90% berfungsi sebagai binder/diluent.
b. Granulasi kering
Granulasi kering disebut juga slugging atau prekompresi. Cara ini sangat tepat untuk tabletasi zat-zat yang peka suhu atau bahan obat yang tidak stabil dengan adanya air. Metode pembuatan tablet dengan cara mengempa campuran bahan kering menjadi massa padat.
Obat dan bahan pembantu pada mulanya dicetak dulu, artinya mula-mula dibuat tablet yang cukup besar, yang massanya tidak tertentu, selanjutnya terjadi penghancuran tablet yang dilakukan dalam mesin penggranul kering, atau dalam hal yang sederhana dilakukan di atas sebuah ayakan. Granulat yang dihasilkan kemudian dicetak dengan takaran yang dikehendaki (Voight, 1995).
Metode ini digunakan pada keadaan dosis efektif yang terlalu tinggi untuk pencetakan yang langsung, dimana bahan aktif obatnya peka terhadap pemanasan atau tidak tahan terhadap pemanasan, kelembaban atau keduanya (Lachman et al., 1994). Setelah penimbangan dan pencampuran bahan, serbuk di slug atau dikompresi menjadi tablet yang besar dan datar dengan garis tengah sekitar 1 inci.
Kempaan harus cukup keras agar ketika dipecahkan tidak menimbulkan serbuk yang berceceran. Tablet kempaan ini dipecahkan dengan tangan atau alat dan
18
diayak dengan lubang yang diinginkan, pelicin ditambahkan dan tablet dikempa (Ansel, 2008).
c. Granulasi basah
Pada teknik ini juga memerlukan langkah-langkah pengayakan, penyampuran dan pengeringan. Pada granulasi basah, granul dibentuk dengan suatu bahan pengikat. Teknik ini membutuhkan larutan, suspensi atau bubur yang mengandung pengikat yang biasanya ditambahkan ke campuran serbuk.
Cara penambahan bahan pengikat tergantung pada kelarutannya dan tergantung pada komponen campuran. Karena massa hanya sampai konsistensi lembab bukan basah seperti pasta, maka bahan pengikat yang ditambahkan tidak boleh berlebihan (Banker dan Anderson, 1994).
Proses pengeringan diperlukan oleh seluruh cara granulasi basah untuk menghilangkan pelarut yang dipakai pada pembentukan gumpalan-gumpalan granul dan untuk mengurangi kelembaban sampai pada tingkat yang optimum (Banker dan Anderson, 1994).
2.3.2 Bahan Tambahan dalam Sediaan Tablet
Pada umumnya tablet kempa mengandung zat aktif dan bahan pengisi, bahan pengikat, disintegran dan lubrikan, dapat juga mengandung bahan warna dan lak (bahan warna yang diadsorpsikan pada alumunium hidroksida yang tidak larut) yang diizinkan, bahan pengaroma dan bahan pemanis. Bahan pengisi ditambahkan jika jumlah zat aktif sedikit atau sulit dikempa. Bahan pengisi tablet yang umum adalah laktosa, pati, kalsium fosfat dibasa dan selulosa mikrokristal.
Jika kandungan zat aktif kecil, sifat tablet secara keseluruhan ditentukan oleh bahan pengisi yang besar jumlahnya. Karena masalah ketersediaan hayati obat
19
hidrofobik yang kelarutannya dalam air kecil, maka digunakan bahan pengisi yang larut dalam air (Ditjen POM, 1995).
a. Bahan pengikat memberikan daya adhesi pada massa serbuk sewaktu granulasi dan pada tablet kempa serta menambah daya kohesi yang telah ada pada bahan pengisi. Zat pengikat dapat ditambahkan dalam bentuk kering, tetapi lebih efektif jika ditambahkan dalam larutan (Ditjen POM, 1995). Menurut Kusumo dan Mita (2017), bahan pengikat memiliki peran sebagai pengikat zat aktif dengan bahan tambahan sehingga didapatkan granul yang baik, dengan didapatkannya granul yang baik akan meningkatkan kekompakan tablet.
Pengikat dapat memperbaiki kerapuhan serta kekuatan granul dan tablet, sehingga dapat meningkatkan kualitas tablet yang dihasilkan. Bahan pengikat yang berasal dari polimer sintetik adalah gelatin, selulosa, dan mikrostatin.
b. Disintegran membantu hancurnya tablet setelah ditelan. Disintegran tablet yang paling banyak digunakan adalah pati. Pati dan selulosa yang termodifikasi secara kimia, asam alginat, mikrokristal selulosa dan crosspovidone juga dapat digunakan. Campuran efervesen digunakan sebagai disintegran dalam sistem tablet larut. Kandungan disintegran, cara penambahan dan derajat kepadatan berperan dalam efektivitas daya hancur tablet (Ditjen POM, 1995).
c. Lubrikan berfungsi untuk mengurangi gesekan selama proses pengempaan tablet dan juga berguna untuk mencegah massa tablet melekat pada cetakan.
Senyawa asam stearat dengan logam, asam stearat, minyak nabati terhidrogenasi dan talkum digunakan sebagai lubrikan (Ditjen POM, 1995).
d. Glidan adalah bahan yang dapat meningkatkan kemampuan mengalir serbuk, umumnya digunakan dalam kempa langsung tanpa proses granulasi (Ditjen POM, 1995).
20
e. Bahan pewarna dan lak yang diizinkan sering ditambahkan pada formulasi tablet untuk menambah nilai estetik atau untuk identitas produk. Kebanyakan bahan pewarna peka terhadap cahaya dan warnanya akan memudar jika terpapar cahaya (Ditjen POM, 1995).
2.3.3 Komposisi Tablet
Pada umumnya bahan baku tablet terdiri dari zat aktif dan bahan tambahan.
Adapun bahan tambahan yang digunakan dalam penelitian ini, yaitu:
1. Aerosil (Colloidal Silicon Dioxide)
Aerosil adalah silika submikroskopik dengan ukuran partikel sekitar 15 nm.
Serbuk aerosil terasa ringan, berwarna putih kebiruan, tidak berbau, tidak berasa, bubuk amorf. Penggunaan aerosil sebagai bahan untuk memperbaiki aliran yaitu 0,1-1%. Praktis tidak larut dalam pelarut organik, air dan asam, kecuali asam hidroflorida. Tetapi larut dalam cairan panas hidroksi alkali. Partikelnya yang berukuran kecil dan luas permukaan yang besar terbukti sangat baik digunakan untuk memperbaiki aliran. Dalam proses pembuatan tablet juga dapat digunakan sebagai penghancur dan adsorben (Rowe et al., 2009). Aerosil mampu mengikat lembab melalui gugus sinalolnya (menyerap 40% dari massanya) tanpa menghilangkan sifat alirnya yang baik (Voight, 1994).
2. Avicel® PH 101 (Microcrystalline Cellulose)
Avicel® PH 101 merupakan nama dagang dari selulosa mikrokristal. Avicel dibuat dari hidrolisis terkontrol α-selulosa dengan larutan asam mineral encer.
Sebagai bahan farmasi, avicel® PH 101 digunakan sebagai bahan pengisi tablet yang dibuat secara granulasi basah maupun cetak langsung, bahan penghancur tablet, adsorben dan bahan anti lekat. Avicel®PH 101 diketahui mempunyai sifat alir dan kompresibilitas yang sangat baik. Konsentrasi yang digunakan sebagai
21 pengisi (diluents) 20-90% (Rowe et al., 2009).
Bahan pengisi berfungsi untuk memperbesar volume massa agar mudah dicetak karena zat aktifnya sedikit atau sulit dikempa. Untuk obat hidrofobik yang kelarutannya dalam air kecil, maka digunakan bahan pengisi yang larut dalam air.
Bahan pengisi tablet yang umum adalah laktosa, pati, kalsium fosfat, dan selulosa mikrokristal (Depkes RI, 1995).
3. Eksplotab (Sodium Starch Glycolate)
Eksplotab adalah pati yang dimodifikasi dengan sifat disintegran yang diamati.
Dalam tablet eksplotab berfungsi sebagai penghancur yang biasa digunakan dalam metode kempa langsung dan granulasi basah. Inkompatibilitas dengan asam askorbat. Konsentrasi eksplotab sebagai penghancur dalam formulasi tablet adalah 2-8% dengan konsentrasi optimum sekitar 4% (Rowe et al., 2009).
Sodium starch glycolate merupakan garam natrium dari eter karboksil metil amilum. Penambahan gugus karboksil metil pada amilum membuat butir amilum bersifat lebih hidrofilik, akan tetapi tidak larut sempurna dalam air. Dalam pembuatan tablet harus digunakan amilum sekering mungkin, agar dapat berfungsi sebagai bahan penghancur agar pengikatan air oleh gugus hidroksida pada amilum dapat menyebabkan gerak aksi yang mengakibatkan hancurnya tablet (Lachman et al., 1986).
4. Magnesium stearat
Magnesium stearat digunakan sebagai glidan dan anti-adheren untuk mengurangi gesekan antar partikulat sehingga dapat mengalir dari lubang corong yang lebih besar ke lubang yang lebih kecil dan akhirnya ke dalam lubang kempa mesin tablet (Siregar dan Wikarsa, 2010).
5. Talkum
22
Talkum berfungsi sebagai lubrikan dan glidan.Talkum juga digunakan secara luas dan mempunyai sifat menguntungkan, yaitu meminimalkan setiap kecenderungan zat yang melekat pada permukaan lubang pencetak (Banker dan Anderson, 1994).
2.4 Uraian Granul dan Uji Preformulasi 2.4.1 Granul
Granul adalah kumpulan partikel partikel serbuk yang diubah menjadi sebuah butiran. Granul yang mengandung suatu daya lekat dimaksudkan agar campuran sebuk dapat mengalir kedalam cetakan tablet secara tepat dan merata sehingga menyebabkan adanya keseragaman bentuk pada tablet. Pembuatan granul melalui tahapan pelembaban serbuk yang telah digiling kemudian adonan yang sudah lembab dilewatkan melalui celah ayakan sesuai granul yang diinginkan. Granul yang baik memiliki bentuk dan warna yang homogen, sedapat mungkin memiliki distribusi yang sempit dan komponen serbuk tidak lebih dari 10%, memiliki daya alir yang baik, menunjukan kekompakan mekanisme yang memuaskan, tidak terlampau kering (sisa lembab 3-5%), serta hancur didalam air (Voight, 1994).
2.4.2 Uji Preformulasi
Sebelum dicetak menjadi tablet, dilakukan pengujian terhadap massa granul untuk mengetahui apakah granul memenuhi syarat untuk dapat dicetak. Uji preformulasi granul meliputi:
a. Waktu alir
Waktu alir merupakan waktu yang diperlukan untuk mengalirkan sejumlah granul pada alat yang dipakai. Apabila granul mempunyai sifat alir yang baik
23
maka pengisian pada ruang kempa menjadi konstan sehingga dihasilkan tablet yang mempunyai bobot seragam (Parrot, 1971).
b. Sudut diam
Sudut diam adalah sudut yang terbentuk antara permukaan tumpukan granul dengan bidang horizontal. Corong berada pada suatu ketinggian yang dikehendaki di atas bidang horizontal. Bubuk atau granul dituang perlahan-lahan sampai di dapat tumpukan bubuk yang berbentuk kerucut. Bila sudut diam <30° biasanya menunjukkan bahwa granul dapat mengalir bebas, dan bila sudutnya >40°
biasanya sifat alirnya kurang baik (Banker dan Anderson, 1994).
c. Indeks tap
Indeks tap didefinisikan sebagai penurunan volume sejumlah granul yang disebabkan oleh kemampuannya mengisi ruang antara granul dan memampat secara lebih rapat. Alat yang digunakan volumeter, dimana terdiri dari gelas ukur yang diletakkan pada suatu alat yang dapat bergerak naik turun secara mekanik dengan bantuan alatpenggerak (Banker dan Anderson, 1994).
d. Kadar air granul
Pengujian kadar air granul dilakukan untuk mengetahui kadar air di dalam butiran granul karena air dapat mempengaruhi panjang masa penyimpanan granul.
Semakin tinggi kadar air granul, maka akan semakin mudah bagi mikroba untuk berkembang pada granul selama masa penyimpanan (Aminingsih, dkk., 2018).
2.5 Evaluasi Tablet
Parameter yang dilakukan untuk pemeriksaan kualitas sediaan tablet,yaitu:
a. Keseragaman bobot
Variasi bobot tablet dipengaruhi oleh ukuran dan distribusi granul yang
24
berbeda, sifat alir granul yang tidak baik akan menyebabkan jumlah serbuk yang masuk dalam ruang kompresi tidak seragam, sehingga menghasilkan bobot tablet yang berbeda (Lieberman et al., 1989).
Keseragaman bobot tablet ditentukan berdasarkan banyaknya penyimpangan bobot pada tiap tablet terhadap bobot rata-rata dari semua tablet sesuai syarat yang ditentukan Farmakope Indonesia.
b. Kekerasan
Dinyatakan sebagai daya tahan terhadap tekanan, tegangan, patahan, guliran, gosokan dan jatuhan (Voight, 1995). Kekerasan tablet umumnya 4-8 kg (Parrot, 1971).
c. Waktu hancur
Didefinisikan sebagai waktu yang diperlukan untuk hancurnya tablet dalam medium yang sesuai, kecuali dinyatakan lain untuk tablet tidak bersalut tidak lebih dari 15 menit (Parrot, 1971).
d. Kerapuhan
Dinyatakan sebagai ketahanan suatu tablet terhadap goncangan selama proses pengangkutan dan penyimpanan. Tablet yang mudah rapuh dan pecah akan kehilangan keindahan dalam penampilannya serta menimbulkan variasi pada bobot tablet dan keseragaman dosis obat. Nilai kerapuhan yang dapat diterima sebagai batas tertinggi adalah 0,8% (Banker dan Anderson, 1994).
25 BAB III
METODE PENELITIAN
3.1 Tempat Pelaksanaan Penelitian
Penelitian ini dilaksanakan di Laboratorium Fitokimia dan Laboratorium Teknologi Sediaan Farmasi Non Steril II Fakultas Farmasi Universitas Sumatera Utara pada bulan Januari sampai Maret 2021.
3.2 Metode Penelitian
Penelitian ini dilakukan dengan menggunakan metode eksperimental yang meliputi tahapan penyiapan sampel, pembuatan simplisia, pemeriksaan karakteristik simplisia dan ekstrak, skrining kandungan senyawa kimia simplisia, pembuatan ekstrak akar manis, pembuatan ekstrak kering akar manis, pembuatan granul eksipien dengan metode granulasi basah, pencampuran dan pencetakan ekstrak kering akar manis dan granul eksipien menjadi sediaan tablet dengan metode cetak langsung, uji preformulasi granul (indeks tap, sudut diam, waktu alir, dan kelembaban granul), uji evaluasi sifat fisik sediaan tablet (keseragaman bobot, waktu hancur, kekerasan, dan kerapuhan) dan analisis data.
3.3 Alat dan Bahan 3.3.1 Alat
Alat-alat yang digunakan dalam penelitian ini adalah alat-alat gelas, alu, aluminium foil, ayakan mesh 16 dan 20, batang pengaduk, beaker glass (Pyrex Iwaki), cawan datar, cawan penguap, corong, disintegration tester, erlenmeyer (Pyrex Iwaki), gelas ukur (Pyrex), gunting, hardness tester (Strong-Cobb), kertas
26
perkamen, kertas saring, krus porselen, lemari pengering, lumpang, mesin cetak tablet single punch (Erweka), mikroskop, neraca analitik (Boeco), neraca kasar, oven (Memmert), penjepit tabung, pipet tetes, Roche friabilator (Erweka), rotary evaporator (IKA), spatel, spatula, stopwatch, sudip dan waterbath.
3.3.2 Bahan
Bahan-bahan yang digunakan dalam penelitian ini adalah akar manis (Glycyrrhiza glabra Linn.), aerosil (Merck), akuades (Merck), asam klorida pekat (Petrokimia), asam sulfat pekat (Petrokimia), avicel PH 101 (Asahi Kasei Chemicals Corporation), etanol 96% (Bratachem), eksplotab (Yung Zip Chemical Ind. Co. Ltd.), isopropanol (Samiraschem), kloroform (Merck), metanol (Merck), magnesium stearat (Bratachem), pereaksi besi (III) klorida (Merck), pereaksi Bouchardat (ROFA), pereaksi Dragendorf (ROFA), pereaksi Liebermann- Burchard (ROFA), pereaksi Mayer (ROFA), pereaksi Molisch (ROFA), serbuk Mg (Merck), serbuk Zn (Merck), talkum (Bratachem), dan toluen (PT Trans Pacific Petrochemical).
3.4 Penyiapan Sampel 3.4.1 Pengambilan Sampel
Sampel yang digunakan pada penelitian ini adalah simplisia akar manis (Glycyrrhiza glabra Linn.) sebanyak 1 kg yang dibeli di toko obat tradisional Medan Petisah.
3.4.2 Identifikasi Sampel
Identifikasi sampel dilakukan di Laboratorium Herbarium Medanense (MEDA) Universitas Sumatera Utara, Medan.
27 3.5 Karakterisasi Simplisia
Karakterisasi simplisia meliputi pemeriksaan makroskopik dan mikroskopik, penetapan kadar air, penetapan kadar sari larut air, penetapan kadar sari larut etanol, penetapan kadar abu total, dan penetapan kadar abu tidak larut asam (Depkes RI, 1995).
3.5.1 Pemeriksaan Makroskopik
Pemeriksaan makroskopik dilakukan dengan mengamati bentuk, warna, bau, dan rasa dari serbuk simplisia akar manis.
3.5.2 Pemeriksaan Mikroskopik
Pemeriksaan mikroskopik dilakukan terhadap serbuk simplisia akar manis.
Serbuk simplisia ditaburkan di atas gelas objek kemudian ditetesi dengan kloralhidrat dan ditutup dengan kaca penutup, kemudian diamati di bawah mikroskop.
3.5.3 Penetapan Kadar Air
Penetapan kadar air dilakukan dengan metode Azeotropi (destilasi toluena).
Cara penetapan:
1. Penjenuhan toluen
Sebanyak 200 ml toluen dan 2 ml air suling dimasukkan ke dalam labu alas bulat, didestilasi selama 2 jam kemudian toluen didinginkan selama 30 menit dan volume air pada tabung penerima dibaca dengan ketelitian 0,05 ml (Depkes RI,1995).
2. Penetapan kadar air serbuk simplisia
Sebanyak 5 g serbuk simplisia yang telah ditimbang seksama dimasukkan ke dalam labu alas bulat berisi toluen tersebut, lalu dipanaskan hati-hati selama 15 menit, setelah toluen mendidih kecepatan tetesan diatur lebih kurang 2 tetes per
28
detik sampai bagian air terdestilasi. Bagian dalam pendingin dibilas dengan toluen. Destilasi dilanjutkan selama 5 menit kemudian tabung penerima dibiarkan dingin sampai suhu kamar. Setelah air dan toluen memisah sempurna, volume air dibaca sesuai dengan kandungan air yang terdapat dalam bahan yang diperiksa.
Kadar air dihitung dalam persen (Depkes RI, 1995).
3.5.4 Penetapan Kadar Sari Larut Air
Sebanyak 5 gram serbuk simplisia dikeringkan dimaserasi selama 24 jam dalam 100 ml campuran air dan kloroform (2,5 kloroform dalam air sampai 1000 ml) dalam labu bersumbat sambil sesekali dikocok selama 6 jam pertama, kemudian dibiarkan selama 18 jam. Disaring, sejumlah 20 ml filtrat diuapkan sampai kering dalam cawan dangkal berdasar rata dan telah ditara, sisanya dipanaskan pada suhu 105oC sampai bobot tetap. Kadar sari larut dalam air dihitung terhadap bahan yang telah dikeringkan di udara (Ditjen POM, 1995).
3.5.5 Penetapan Kadar Sari Larut Etanol
Sebanyak 5 gram serbuk simplisia yang telah dikeringkan dimaserasi selama 24 jam dalam 100 ml etanol 96% dalam labu bersumbat sambil dikocok sesekali selama 6 jam pertama, kemudian dibiarkan selama 18 jam. Kemudian disaring, 20 ml filtrat diuapkan sampai kering dalam cawan berdasar rata yang telah ditara dan sisanya dipanaskan pada suhu 105oC sampai bobot tetap. Kadar sari larut etanol dihitung terhadap bahan yang telah dikeringkan (Ditjen POM, 1995).
3.5.6 Penetapan Kadar Abu Total
Sebanyak 2 gram serbuk simplisia yang telah digerus dan ditimbang seksama dimasukkan dalam kurs porselen yang telah dipijar dan ditara, kemudian diratakan. Kurs dipijar perlahan-lahan, kemudian naikkan suhu secara bertahap hingga 600oC sampai arang habis, jika arang masih tidak dapat dihilangkan,
29
ditambahkan air panas, saring melalui kertas saring bebas abu. Pijarkan sisa dan kertas saring dalam kurs yang sama. Masukkan filtrat ke dalam kurs, uapkan, pijarkan hingga bobot tetap, timbang. Kadar abu dihitung terhadap bahan yang telah dikeringkan (Ditjen POM, 1995).
3.5.7 Penetapan Kadar Abu Tidak Larut Asam
Abu yang diperoleh dalam penetapan kadar abu total dididihkan dalam 25 mL asam klorida 3N selama 5 menit. Bagian yang tidak larut dalam asam dikumpulkan, disaring melalui kertas saring bebas abu, lalu dicuci dengan air panas, dipijarkan, kemudian didinginkan dan ditimbang sampai bobot tetap.
Kadar abu yang tidak larut dalam asam dihitung terhadap bahan yang telah dikeringkan (Depkes RI, 1995).
3.6 Skrining Fitokimia Simplisia Akar Manis
Menurut Depkes RI (1995), skrining fitokimia dilakukan untuk mengetahui golongan senyawa alkaloid, flavonoid, glikosida, saponin, tanin dan steroid/triterpenoid.
3.6.1 Pemeriksaan Alkaloid
Simplisia ditimbang sebanyak 0,5 g kemudian ditambahkan 1 ml asam klorida 2N dan 9 ml air suling, dipanaskan di atas penangas air selama 2 menit, didinginkan dan disaring. Filtrat yang diperoleh dipakai untuk uji alkaloid dengan cara berikut: diambil 3 tabung reaksi, lalu ke dalamnya ditambahkan 0,5 ml filtrat.
Pada masing-masing tabung reaksi ditambahkan 2 tetes pereaksi Mayer, 2 tetes pereaksi Bouchardat dan 2 tetes pereaksi Dragendorf. Alkaloid positif jika terjadi endapan atau kekeruhan paling sedikit dua dari tiga percobaan di atas (Depkes RI, 1995).
30 3.6.2 Pemeriksaan Flavonoida
Sebanyak 0,5 g simplisia ditambahkan 20 ml air panas, dididihkan selama 10 menit dan disaring dalam keadaan panas, ke dalam 5 ml filtrat ditambahkan 0,1 g serbuk magnesium dan 1 ml asam klorida pekat dan 2 ml amil alkohol, dikocok dan dibiarkan memisah. Flavonoida positif jika terjadi warna merah, kuning, jingga pada lapisan amil alkohol (Farnsworth, 1966).
3.6.3 Pemeriksaan Glikosida
Simplisia ditimbang sebanyak 3 g lalu disari dengan 30 ml campuran etanol 96% dengan air (7:3) dan 10 ml asam klorida 2N, direfluks selama 2 jam, didinginkan dan disaring. Diambil 20 ml filtrat, ditambahkan 25 ml air suling dan 25 ml timbal (II) asetat 0,4 M, dikocok, didiamkan selama 5 menit lalu disaring.
Filtrat disari dengan 20 ml campuran kloroform dan isopropanol (3:2), dilakukan berulang sebanyak 3 kali. Sari air dikumpulkan dan diuapkan pada temperatur tidak lebih dari 500C. Sisanya dilarutkan dalam 2 ml metanol. Larutan sisa digunakan untuk percobaan berikut: 0,1 ml larutan percobaan dimasukkan dalam tabung reaksi dan diuapkan di atas penangas air. Pada sisa ditambahkan 2 ml air dan 5 tetes pereaksi Molisch. Kemudian secara perlahan-lahan ditambahkan 2 ml asam sulfat pekat melalui dinding tabung, terbentuk cincin warna ungu pada batas kedua cairan, menunjukkan adanya ikatan gula (Depkes RI, 1995).
3.6.4 Pemeriksaan Saponin
Simplisia ditimbang sebanyak 0,5 g dan dimasukkan kedalam tabung reaksi, lalu ditambahkan 10 ml air panas, didinginkan, kemudian dikocok kuat-kuat selama 10 detik. Jika terbentuk busa setinggi 1-10 cm yang stabil tidak kurang dari 10 menit dan buih tidak hilang dengan penambahan 1 tetes asam klorida 2N menunjukkan adanya saponin (Depkes RI,1995).