i
ANALISIS KUALITATIF METHAMFETAMINE DALAM
TABLET DAN URINE DI BADAN NARKOTIKA NASIONAL,
JAKARTA
LAPORAN PRAKTIK KERJA LAPANGAN
Diajukan untuk memenuhi salah satu syarat Praktek Kerja Lapangan (PKL) pada Program Studi Ilmu Kimia Fakultas Matematika dan Pengetahuan Alam
Universitas Islam Indonesia
Disusun oleh: DIAN NOVITA SARI
No. Mhs: 11 612 050
PROGRAM STUDI ILMU KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS ISLAM INDONESIA
ii
ANALISIS KUALITATIF METHAMFETAMINE
DALAMTABLET DAN URINE DI BADAN NARKOTIKA
NASIONAL, JAKARTA
Disusun oleh: DIAN NOVITA SARI No. Mahasiswa: 11 612 050
Telah dipertahankan dihadapan Panitia Penguji Praktik Kerja Lapangan (PKL) Prodi Ilmu Kimia Fakultas Matematika dan Ilmu Pengetahuan Alam
iii
KATA PENGANTAR
Assalamu’alaikum Wr. Wb.
Alhamdulillah, puji syukur kami panjatkan kehadirat Allah SWT, yang telah memberikan rahmat dan hidayah-Nya sehingga Praktik Kerja Lapangan (PKL) dapat berjalan lancar dan kami dapat menyelesaikan laporan PKL ini tepat waktu. Shalawat dan salam semoga selalu tercurah limpahkan kepada Rasulullah Muhammad SAW yang senantiasa menunjukkan ummatnya pada jalan yang benar.
Laporan ini disusun sebagai pertanggungjawaban dari pelaksanaan Praktik Kerja Lapangan (PKL) yang berlangsung selama 4 minggu, yakni terhitung sejak tanggal 3 Februari sampai 28 Februari 2014 di Badan Narkotika Nasional (BNN) Jakarta. Selama pelaksanaan PKL dan penyusunan laporan ini penulis banyak memperoleh bantuan dari berbagai pihak. Oleh karena itu, dengan segala kerendahan hati, penulis haturkan terima kasih kepada :
1. Orang tua tersayang di pulau sebrang yang senantiasa tak pernah lelah untuk memberi semangat baik moril maupun materil.
2. Bapak Yandi Syukri M.Si,. Apt,. selaku Dekan Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Islam Indonesia.
3. Bapak Riyanto M.Si, Ph.D selaku Ketua Prodi Ilmu Kimia Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Islam Indonesia. 4. Bapak Kuswardani, S.SI, M.Farm, Apt selaku ketua UPT Laboratorium
iv
5. Bapak Dwiarso Rubiyanto, M.Si, selaku dosen pembimbing PKL yang telah memberikan bimbingan dan semangat hingga terselesaikannya laporan ini.
6. Ibu Rieska Dwi Widayanto, S.Si., M.Si selaku dosen pembimbing instansi. 7. Mbak tanti, mbak cici, mbak sri, mbak flo, mas andre, mbak nur, dan para
laboran UPT BNN lainnya yang telah bersabar membagi ilmunya.
8. Keluarga pak Mul yang telah memberikan tumpangan hidup selama penulis di Jakarta.
9. Avie Dianputra, terimakasih telah menjadi pendengar dan penasehat yang ulung
10.Mbak nop, Marko, Adis dan Thivoo untuk segala kegilaan yang terjadi di gubuk kita.
11.Erika Dian Puspita dan Sigit Boediarjo, teman seperjuangan saat penulis berada di Jakarta.
12.Teman-teman seperjuangan, keluarga besar kimia 2011, tetap semangat hingga nanti kita keluar dan mendapat gelar S.si
Penulis menyadari bahwa selama pelaksanaan praktik kerja lapangan (PKL) dan penyusunan laporan PKL ini masih banyak kekurangan. Oleh karena itu, kritik dan saran yang membangun dari semua pihak sangatlah diharapkan.
Yogyakarta, 23 April 2014 Penulis
v
ANALISIS KUALITATIF
METHAMFETAMINE
DALAM
TABLET DAN URINE DI BADAN NARKOTIKA NASIONAL,
JAKARTA
Dian Novita Sari NIM : 11612050
INTISARI
Narkoba adalah singkatan dari narkotika, psikotropika dan bahan adiktif lainnya. Narkoba adalah obat, bahan, atau zat dan bukan tergolong makanan jika diminum, diisap, dihirup, ditelan, atau disuntikkan, berpengaruh terutama pada kerja otak (susunan saraf pusat), dan sering menyebabkan ketergantungan. Akibatnya, kerja otak berubah demikian pula fungsi vital organ tubuh lain.
Methamfhetamine merupakan stimulan yang diproduksi secara sintesis dan termasuk salah satu jenis narkotika yang sering disalahgunakan serta diedarkan secara ilegal di Indonesia. Penelitian dilakukan pada tablet dan urine yang mengandung methamfhetamine diidentifikasi menggunakan Kromatografi Lapis Tispis (KLT) dan Kromatografi Gas-Spektrofotometri Massa (KG-SM). Hasil identifikasi mendapatkan bahwa terdapat senyawa aktif lain yang terdapat dalam methamfhetamine baik dalam bentuk tablet maupun urine. Senyawa aktif lain ini dapat mengakibatkan efek farmakologi sinergik dan non sinergik. Efek farmakologi sinergik dapat mengakibatkan kematian bagi penggunanya.
ABSTRACT
Drugs are the abbreviation of narcotics , psychotropic and other addictive substances . Drugs are drugs , materials , or substances not classified as food and if taken , smoked , inhaled , swallowed , or injected , influential especially in the brain ( central nervous system ) , and often leads to dependency . As a result , changing brain function as well as other vital organs .
Methamphetamine is a stimulant that is produced synthetically and is one type of drug that is often abused and illegally circulated in Indonesia . The study was conducted on tablets and urine containing methamphetamine were identified using Tispis Layer Chromatography ( TLC ) and gas chromatography - mass spectrophotometry ( GC-MS ) . The results of identification to get that there are other active compounds contained in the methamphetamine in the form of tablets or urine . Other active compounds may result in synergistic pharmacological effects and non- synergistic . Synergistic pharmacological effects can lead to its
death .
vi DAFTAR ISI
ANALISIS KUALITATIF METHAMFETAMINE DALAMTABLET DAN
URINE DI BADAN NARKOTIKA NASIONAL, JAKARTA ... i
ANALISIS KUALITATIF METHAMFETAMINE DALAMTABLET DAN URINE DI BADAN NARKOTIKA NASIONAL, JAKARTA ... ii
KATA PENGANTAR ... iii
2.1. Sejarah Badan Narkotika Nasional ... 5
2.2.1. Visi Bada Narkotika Nasional ... 6
2.2.2. Misi Badan Narkotika Nasional ... 6
2.4. Perkembangan Unit Pelaksana Teknis Laboratorium Badan Narkotika Nasional . 8 2.4.1. Visi UPT.Laboratorium Uji Narkoba BNN ... 10
2.4.2. Misi UPT.Laboratorium Uji Narkoba BNN ... 11
2.4.3. Struktur Organisasi UPT Lab BNN ... 12
2.4.4. Saran dan Kegiatan UPT Lab BNN ... 12
2.10. Senyawa aktif lain ... 17
vii
2.10.2. Dekstrometorfan ... 18
2.10.3. Ketamin ... 19
2.10.4. Methylone ... 20
2.11. Kromatografi Lapis Tipis ... 21
2.12.1. Parameter Penting dalam Kromatografi Gas ... 25
2.13. Spektrofotometer massa ... 30
2.13.1. Instrumen dari spektroskopi massa sebagai berikut: ... 31
2.13.2. Parameter Penting dalam Spektrofotometer Massa ... 32
2.14. Kromatografi Gas – Spektrofotometer Massa ... 34
2.14.1. Prinsip Kerja ... 35
BAB III METODE PENELITIAN... 37
3.1. Alat ... 37
3.2. Bahan ... 38
3.3. Cara Kerja ... 39
3.3.1. Kromatografi Lapis Tipis... 39
3.3.2. Kromatografi Gas-Spektrofotometer Massa ... 44
BAB IV HASIL DAN PEMBAHASAN ... 47
4.1. Hasil dan Pembahasan... 47
BAB V KESIMPULAN DAN SARAN ... 68
5.1. Kesimpulan ... 68
5.2. Saran... 68
DAFTAR PUSTAKA ... 69
Lampiran 1.Gambar alat ... 71
viii
DAFTAR TABEL
ix
DAFTAR GAMBAR
Gambar 1. Struktur Organisasi UPT Lab Uji Narkoba BNN ... 12
Gambar 4. struktur molekul ketamin ... 20
Gambar 5. Struktur senyawa Methylone ... 21
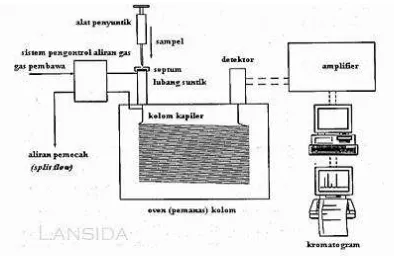
Gambar 6. Instrumentasi KG-MS ... 36
Gambar 7. Sampel tablet methamphetamine ... 48
Gambar 8. Hasil Kromatografi gas tablet 248LbI ... 54
Gambar 9. Hasil Kromatografi gas tablet 104He ... 55
Gambar 10. Hasil Kromatografi gas tablet 249Lb ... 56
Gambar 11. Hasil Kromatografi gas tablet 104Hd ... 57
Gambar 12. Hasil Kromatografi gas ss21I ... 58
Gambar 13. Sampel urine methamphetamine... 59
Gambar 14. Hasil Kromatografi gas urine 373A ... 64
Gambar 15. Hasil Kromatografi gas urine 374A ... 64
Gambar 16. Hasil Kromatografi gas urine 375A ... 65
Gambar 17. Hasil Kromatografi gas urine ss75A ... 66
1
Dewasa ini permasalahan obat terlarang (narkoba) di Indonesia sudah menjadi masalah yang serius. Hal ini dibuktikan dengan sejumlah kasus narkoba yang meningkat disetiap tahunnya. Jumlah kasus penyalahgunaan narkoba di Indonesia dari tahun 2001 sampai 2005 meningkat sebanyak 51,3% per tahun (Dit.IV/Narkoba BNN,2005).
Narkotika atau sering diistilahkan sebagai drug adalah sejenis zat. Zat narkotik ini merupakan zat yang mimiliki ciri-ciri tertentu. Narkotik adalah zat yang bisa menumbulkan pengaruh-pengaruh tertentu bagi mereka yang mbggunakan dengan memasukkannya kedalam tubuh. Pengaruh tersebut berupa pembiusan, hilangnyarasa sakit, reangsangan semangat dan halusinasi atau timbulnya khayalan-khayalan (Dirdjosisworo, 1987).
Deteksi dari senyawaan narkotika, psikotropika, dan bahan adiktif (Narkoba) menggunakan sampel hasil metabolit sekunder manusia (urine, darah, rambut, dan kuku) memiliki peranan yang sangat penting dalam bidang toksikologi forensik terutama dalam hal memberikan informasi riwayat penyalahgunakan narkotika. Obat-obatan tersebut dapat terdeteksi beberapa jam setelah konsumsi terakhir (Abdi, 2004)
mengubah pikiran, perasaan dan juga perilaku seseorang dan lebih jauh lagi narkoba akan dapat menimbulkan ketergantungan fisik dan psikologis. Penyalahgunaan Narkotika merupakan salah satu masalah pemerintah yang perlu mendapatkan perhatian serius dari semua pihak. Hal ini dibuktikan dengan semakin meningkatkan kasus narkotika yang dilaporkan oleh berbagai media. Dalam hal pemeriksaan jenis narkotika ini maka perlu dicari metode – metode yang cukup teruji yang dapat menganalisa Narkotika tersebut dengan hasil yang optimal (Baumgartner, 1979).
Pada percobaan ini narkoba yang diidentifikasi berupa identifikasi methamfetamine pada tablet dan urine. Methamfetamine atau lebih dikenal dengan shabu-shabu. Obat ini dapat ditemukan dalam bentuk kristal, tidak mempunyai warna maupun bau. Shabu-shabu dikenal juga dengan istilah Ice yang memiliki pengaruh terhadap saraf. Pengguna shabu-shabu akan memiliki ketergantungan yang sangat tinggi pada obat ini dan akan berlangsung lama, bahkan bisa mengalami sakit jantung atau kematian. Istilah lain yang sering digunakan untuk menyebut shabu-shabu ini, antara lain adalah ice, kristal, ibas, SS, mecin , glass, quartz, dan hirropon.
Belakangan ini penyalahgunaan shabu telah meningkat secara drastis salah satu contohnya banyak pemakai cocaine yang beralih ke shabu karena harganya yang lebih murah. Shabu merupakan narkotika yang mudah dibuat oleh sekalipun orang awam. Hal ini mengakibatkankan maraknya pemakai shabu-shabu di Indonesia. Shabu-shabu juga memiliki efek on lebih lama sekitar 9-15 jam dibanding cocaine yang hanya sekitar 15-20 menit. Shabu-shabu juga lebih mudah didapatkan di pasar gelap Indonesia.
1.2.Rumusan Masalah
Berdasarkan latar belakang masalah, maka dapat dirumuskan masalah sebagai berikut:
1. Apaka benar sampel urine dan tablet yang digunakan positif mengandung methamfetamine.
2. Bahan kimia apa saja yang terdapat pada sampel urine dan tablet yang digunakan.
1.3.Tujuan Penelitian
Berdasarkan rumusan masalah, maka tujuan penelitian ini adalah sebagai berikut:
1. Untuk memastikan sampel urine dan tablet yang digunakan positif methamfetamine.
1.4.Manfaat
Manfaat yang diharapkan dari penulisan ini sebagai berikut:
1. Dapat mengetahui cara analisis kualitatif sampel urine dan tablet yang mengandung methamfetamine dengan menggunakan metode Kromatografi Lapis Tipis dan Kromatografi Gas-Spektroskopi Massa. 2. Memberikan informasi mengenai kandungan methamfetamine pada urine
5
2.1.Sejarah Badan Narkotika Nasional
Penyalahgunaan dan peredaran gelap Narkoba sejak zaman dahulu merupakan masalah yang sulit untuk diatasi, oleh karena itu organisasi ASEAN merumuskan dan membuat kesepakatan dalam mempercepat pemberantasan penyalahgunaan dan peredaran gelap Narkoba untuk menjadikan negara ASEAN bebas Narkoba. Pada era kolonial pemerintahan belanda mulai diusahakan undang-undang narkotika yang dikenal dengan VERDONVENDE Middelen Ordonnatie pada tahun 1927 yang mengatur pemakaian opiat, namun jenis pemakaiannya hanya dibatasi bukan dilarang karena penyalahgunaan Narkoba dan peredaran gelap narkotika pada saat itu belum menjadi sorotan utama karena masih bisa diatasi, hal ini berlangsung sampai pada proklamasi kemerdekaan Republik Indonesia (194501960-an). Selanjutnya pada tahun 1970-an mulai muncul masalah penyalahgunaan narkotika yang dianggap sangat mengganggu keamanan dan ketertiban umum. Selanjutnya untuk mengatasi masalah penyalahgunaan dan peredaran gelap narkotika dikeluarkan Instruksi Presiden No. 6 tahun 1971 kepa Ketua Badan Koordinasi Intelijen Negara untuk menanggulangi masalah gangguan keamanan umum, termasuk uang palsu dan penyalahgunaaan narkotika. Berdasarkan intruksi presiden dibentuk Badan Koordinasi Pelaksanaan Instruksi Presiden No. 6 tahun 1971.
pemberantasan penyalahgunaan dan peredaran gelap narkotika dan prekusor narkotika dikeluarkan keputusan Presiden No. 116 tahun 1999 tentang pembentukan Badan Koordinasi Narkotika Nasional (BKKN) dan karena dipandang kurang efisien dalam menangani masalah narkotika maka diatur kembali mengenai penguatan kelembagaan yang suda ada yaitu diganti dengan Badan Narkotika Nasional (BNN). BNN melalui Keputusan Presiden No. 17 tahun 2002 (yang kemudian diganti dengan Peraturan Presiden Nomor 83 TAHUN 2007). BNN adalah sebuah lembaha nonstruktural Indonesia yang bertanggung jawab langsung kepada Presiden Republik Indonesia.
2.2.Visi dan Misi Badan Narkotika Nasional
2.2.1. Visi Bada Narkotika Nasional
Badan Narkotika Nasional (BNN) sebuah organisasi dalam penanganan masalah Narkoba memiliki visi terwujudnya masyarakat Indonesia bebas penyalahgunaan dan peredaran gelap narkotika, psikotropika, dan bahan adiktif lainnya tahun 2015.
2.2.2. Misi Badan Narkotika Nasional
Misi BNN dalam mewujudkan visinya antara lain sebagai berikut: 1. Menentukan kebijakan dalam membangun komitmen bersama
memerangi penyalahgunaan dan peredaran gelap Narkoba.
2. Melakukan upaya-upaya pencegahan yang lebih efektif dan efisien.
4. Meningkatkan metode terapi dan rehabilitasi dalam merehabilitasi penyalahgunaan narkoba.
5. Melakukan penelitian dan pengembangan dalam penyusunan database yang akurat.
6. Membangun sistem informatika sesuai perkembangan teknologi. 7. Meningkatkan peran dan fungsi Satuan Tugas Operasional.
8. Meningkatkan peran dan fungsi Badan Narkotika Porpinsi/Kabupaten/Kota.
9. Meningkatkan peran serta BNN dalam pergaulan global melalui kerjasama Internasional yang efektif dalam pemeberantasan peredaran gelap Narkoba.
2.3.Tugas Badan Narkotika Nasional
Badan Narkotika Nasional merupakan lembaga Non struktural yang bertanggung jawab langsung kepada presiden. Hal ini mengakibatkan BNN memiliki tugas membantu presiden. Berdasarkan UU No.35 tahun 2009 tentang narkotika BNN mempunyai tugas:
1. Mengkoordinasi instansi pemerintah terkait dalam penyusunan kebijakan dan pelaksanaannya dibidang ketersediaan, pencegahan, pemberantas, penyalahgunaan, dan peredaran gelap narkotika, psikotropika, perkusor, dan bahan adiktif lainnya.
instansi pemerintah terkait sesuai dengan tugas, fungsi, dan kewenangannya masing-masing.
3. Meningkatkan kemampuan lembaga rehabilitasi medis dan rehabilitasi sosial pencandu narkotika, baik yang diselenggarakan oleh pemerintah maupun masyarakat.
4. Memantau, mengarahkan, dan meningkatkan kegiatan masyarakat dalam pencegahan penyalahgunaan dan peredaran gelap narkotika dan prekusor narkotika.
5. Melakukan kerja sama bilaterak dan multirateral, baik regional maupun internasional guna mencegah dan memberantas peredaran gelap narkotika dan prekusor narkotika.
6. Mengembangkan laboratoriumnarkotika dan prekusor narkotika. 7. Melaksanakan administrasi penyelidikan dan penyidikan terhadap
perkara penyalahgunaan dan peredaran gelap narkotika dan prekusor narkotika.
8. Membuat laporan tahunan mengenai pelaksanaan tugas dan wewenang.
2.4.Perkembangan Unit Pelaksana Teknis Laboratorium Badan Narkotika
Nasional
psikotropoka, prekusor, dan bahan adiktif lainnya. Laboratorium Uji Narkoba BNN telah mendapat ijin berdasarkan pemenkes Nomor 135/MENKES/SK/XII/2004 untuk melakukan pengujian dan laboratorium rujukan dalam melakukan pemeriksaan narkotika dan psikotropik. Laboratorium ini mulai melakukan pemeriksaan Narkoba untuk projusticia mulai bulan Desember 2004. Struktur organisasi laboratorium ini pada awal pembentukannya dibawah Pusat Laboratorium Terapi dan Rehabilitasi (Pus Lab T&R) yaitu salah satu bagian yang ada di BNN, namun sejak 1 April tahun 2008 menjadi unit tersendiri yaitu UPT yang bertanggungjawab langsung kepada Kepala BNN dengan Kepala UPT adalah setingkat jabatan struktural eselon III.a.
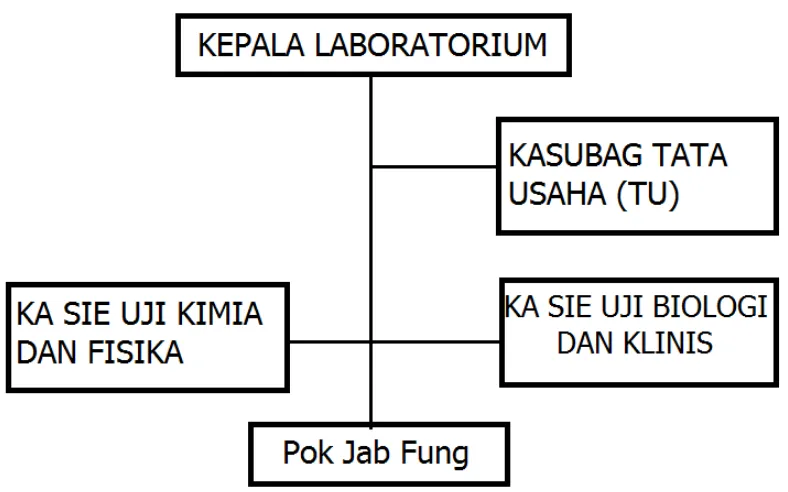
Kepala UPT laboratorium membawahi empat bagian yaitu subbagian tata usaha, seksi pengujian kimia dan fisika, seksi pengujian biologi dan klinis dan kelompok jabatan fungsional. Dalam melaksanakan tugas dan fungsi pimpinan satuan organisasi dilingkungan UPT Laboratorium Uji Narkoba BNN wajib menerapkan prinsip koordinasi, integrasi, dan sinkronisasi dilingkungan masing-masing maupun antar satuan organisasi dilingkungan BNN dengan instansi lain yang terkait sesuai dengan tugas masing-masing.
penyelidikan dan penyidikan kasus penyalahgunaan Narkoba. Dalam melaksakan tugasnya Laboratorium Uji Narkoba berdasarkan Peraturan Ketua BNN
Nomor:Per/01/IV/2008/BNN menyelenggarakan fungsi:
1. Pelayanan uji Narkoba melalui proses laboratorium dalam upaya pembuktian sampel narkotika, psikotropika, zat adiktif, prekusor, bahan berbahaya lainnya dan derivatnya untuk mendukung penyelidikan dan penyidikan kasus penyalahgunaan Narkoba. 2. Penetapan jenis narkotika, psikotropika, zat adiktif, prekusor,
bahan berbahaya lainnya dan derivatnya sesuai hasil pengujian laboratorium yang dilakukan.
3. Penelitian dan pengembangan uji narkotika, psikotropika, zat adiktif, prekusor, bahan berbahaya lainnya dan derivatnya melalui proses laboratorium.
4. Pelaksanaan urusan perencanaan, keuangan, kepegawaian, perlengkapan, rumah tangga, pelaporan, dan surat-menyurat.
2.4.1. Visi UPT.Laboratorium Uji Narkoba BNN
2.4.2. Misi UPT.Laboratorium Uji Narkoba BNN
Dalam mewujudkan visinya Laboratorium Uji Narkoba BNN memiliki misi sebagai berikut:
1. Meningkatkan pola pelayanan dalam rangka pencapaian pelayanan prima.
2. Melakukan pengembangan kemampuan personalia laboratorium. 3. Melakukan pengembagan peralatab laboratorium yang ada. 4. Melakukan penelitian dalam rangka pengembangan metode
analisa uji Narkoba.
5. Meningkatkan jejaring dan kerjasama antar laboratorium pengujian yang komprehensif.
2.4.3. Struktur Organisasi UPT Lab BNN
Gambar 1.Struktur Organisasi UPT Lab Uji Narkoba BNN
2.4.4. Saran dan Kegiatan UPT Lab BNN
2.5.Narkotika
Narkoba adalah singkatan dari narkotika, psikotropika dan bahan adiktif lainnya. Narkoba adalah obat, bahan, atau zat dan bukan tergolong makanan jika diminum, diisap, dihirup, ditelan, atau disuntikkan, berpengaruh terutama pada kerja otak (susunan saraf pusat), dan sering menyebabkan ketergantungan. Akibatnya, kerja otak berubah demikian pula fungsi vital organ tubuh lain (jantung, peredaran darah, pernapasan, dan lain-lain) (BNN, 2007).
Secara etimologis narkoba atau narkotika berasal dari bahasa Inggris narcose atau narcosis yang berarti menidurkan dan pembiusan. Narkotika berasal dari bahasa Yunani yaitu narke atau narkam yang berarti terbius sehingga tidak merasakan apa-apa. Narkotika berasal dari perkataam narcotic yang artinya sesuatu yang dapat menghilangkan rasa nyeri dan dapat menimbulkan efek stupor (bengong), bahan-bahan pembius dan obat bius (Mardani,2008).
Secara Terminologi, dalam Kamus Besar Bahasa Indonesia narkoba atau narkotika adalah obat yang dapat menenangkan syaraf, menghilangkan rasa sakit, menimnbulkan rasa mengantuk atau merangsang (Mardani, 2008).
Narkotika adalah zat atau obat yang berasal dari tanaman atau bukan tanaman baik sintesis maupun semisintesis yang dapat menyebabkan penurunan atau perubahan kesadaran, hilangnya rasa, mengurangi sampai menghilangkan rasa nyeri dan dapat menimbulkan ketergantungan (Pasal 1 angka 1 UU 22./Th.1997).
menyebabkan penurunan atau perubahan kesadaran, mengurangi sampai menghilangkan rasa nyeri dan dapat menimbulkan ketergantungan.
Zat narkotik ini ditemukan manusia yang penggunaannya ditujukan untuk kepentingan umat manusia, khusus nya dibidang pengobatan, oleh karenanya dalam ketentuan perundang-undangan mengenai narkotika penggunaannya diatur legal dibawah pengawasan dan tanggungjawab dokter dan apoteker. Penggunaan narkotika dengan dosis yang diatur oleh seorang dokter untuk kepentingan pengobatan tidak membawa akibat sampingan yang membahayakan bagi tubuh orang yang bersangkutan.
2.6.Morfin
Perkataan “morphin” berasal dari bahasa Yunani “morpheus” yang artinya
dewa mimpi yang dipuja-puja. Nama ini cocok dengan pecandu morfin, karena merasa play di awang-awang. Morfin adalah jenis narkotika yang bahan bakunya berasal dari candu atau opium. Sekitar 4-21% morfin dapat dihasilkan dari opium. Morfin adalah prototipe analgetik yang kuat, tidak berbau, rasanya pahit, berbentuk kristal putih, dan warnanya makin lama berubah menjadi kecokelatan. Morfin adalah alkaloid utama dari opium dengan rumus kimia c17H19NO3 (Mardani, 2008).
Meskipun morfin hanya merupakan salah satu dari berbagai macam narkotika, tapi para pecandu narkotika kadang disebut sebagai morfinis. Ini menunjukkan betapa populernya morfin di kalangan masyarakat. Para morfinis seringkali mendapat stigma negatif dari masyarakat, dijauhi, dan dikucilkan ( Hakim, 2004).
2.7.Heroine
Heroine berbentuk seperti bubuk atau puyer. Bentuk heroine seperti ini sering diberi nama PT, pete, etep, putih, atau bedak. Bubuk ini tampak agak kotor seperti tepung terigu. Isinya adalah heroin. Ada beberapa tingkat kualitas putaw tergantung cara pengolahannya (Partodiharjo, 2008).
Secara sembunyi-sembunyi, dalam realitas, heroin terus diproduksi di laboratorium gelap. Heroin dihasilkan dari bahan baku morfin, asam cuka anhidrid, dan asetil klorid, dengan peralatan dan temapat sederhana. Serbuk heroin (putaw) dihasilkan dari getah bunga tanaman candu melalui proses ekstraksi. Serbuk heroin kadang berwarna putih, kadang kecoklatan (brown sugar). Proses pembuatan heroin merupakan aktifitas yang sangat penting dalam belantara sindikat narkoba, terutama dalam meningkatkan nilai harga gelap di pasaran bebas (Hakim, 2004).
bereaksi atau malah sakaw. Karena dosis yang terpaksa semakin tinggi, banyak pemakai putaw yang meninggal karena overdosis (Partodiharjo, 2008).
Heroin murni adalah bubuk putih dengan rasa yang pahit dan sedikit berbau. Ada juga heroine jalanan yaitu heroin yang dikemas dalam berbagai bentuk, tergantung pada bagaimana cara pembuatannya dan bahan apa yang ditambahkan. Heroin dapat berbau seperti cuka, vitamin atau obat. Heroin merupakan narkotik yang sangat keras dengan zat adiktif yang sangat tinggi. Heroin menjerumuskan pemakainnya dengan sangat cepat sehingga usaha untuk mengurangi pemakainnya akan merasa sangat sakit dan sering kejang-kejang bila dihentikan konsumsinya (Media, 2006).
2.8.Ganja
Ganja (Cannabis sp) memiliki kandungan cannabinoid yang utama yaitu cannabinol (CBN), cannabidiol (CBD), dan Δ9-Tetrahidrocanabinol (THC), dimana Δ9-Tetrahidrocannabinol dapat membuat pemakainya mengalami euphoria. Komposisi kandungan senyawa cannabinoid ditentukan oleh tempat tumbuh dari tanaman tersebut seperti tanah, iklim dan sifat-sifat genetik, yang dapat mempengaruhi biosintesa metabolit sekunder dari Cannabis sp. Komposisi metabolit sekunder dalam Cannabis dapat menggambarkan tempat tumbuh cannabis itu sendiri.
terdapat di Indonesia karena benda resin dan bubuknya sukar didapat ( Maroef, 1976).
2.9.Kokain
Kokain merupakan alkaloid yang didapatkan dari tanaman belukar, yang berasal dari Amerika Selatan, dimana daun dari tanaman belukar ini biasanya dikunyah-kunya oleh penduduk setempat untuk mendapatkan efek stimulan. Saat ini kokain masuh digunakan sebagai anestetik lokal, khususnya untuk pembedahan mata, hidung, dan tenggorokan karena efek varokonstriksifnya juga membantu. Kokain diklasifikasikan sebaga suatu narkotik bersama dengan morfin dan heroin karena efek adiktif dan efek merugikannya telah dikenali (Budiyanto, 1997).
Efek negatif yang ditimbulkan dari penyalahgunaan kokain ini, antara lain adalah denyut jantung cepat, euforia, kejang, pupil melebar, tekanan data meningkat, berkeringat, muntah, mudah berkelahi, pendarahan otak, dan penyumbatan pembuluh darah (Rozak, 2006)
2.10. Senyawa aktif lain
2.10.1.Kafein
jantung, serta memberikan efek samping berupa gelisah (neuroses), tidak dapat tidur (insomnia), dan denyut jantung tidak beraturan (tachycardia) (Winarno 1991).
Gambar 2. Struktur molekul kafein
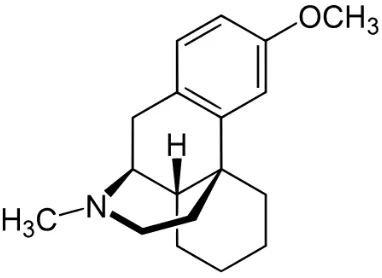
2.10.2.Dekstrometorfan
putih sampai sedikit kekuningan, tidak berbau, larut dalam air maupun etanol, dan tidak larut dalam eter. Efek samping penggunaan Dekstrometorfan antara lain euphoria, disorientasi paranoid, dan halusinasi. Selain efek diatas, dapat pula menyebabkan depresi napas dengan menghambat mekanisme pernapasan batang otak.
Gambar 3. Struktur dekstrometorfan
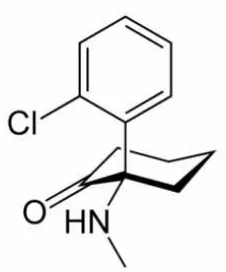
2.10.3.Ketamin
Gambar 4. struktur molekul ketamin
Rumus bangun Ketamin (Ketala, Vetalar, Ketanest [2-2- chlorphenyl)-2-(methylamino)-cyclohexanone]. Ketamin dapat diberikan secara oral, intramuskular, rectal, masal dan epidural. Ketamin memiliki biovaibilitas pada oral sebesar 20&, intramuskular 90%, rectal sebesar 25%, epidural 77% dan nasal sebesar 50%. Suatu dosus intravena 2mg/kgBB biasanya menghasilkan anastesi bedah dalam waktu 30 detik dengan efek anestesi biasanya antara5-10 detik (Wirjoatmodjo,2000).
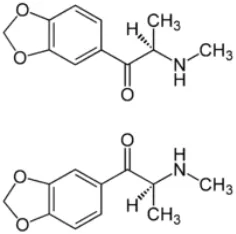
2.10.4.Methylone
Cathinone, S(-)-alpha-aminopropiophenone, merupakan zat yang konfigurasi kimia dan efeknya mirip dengan amfetamine. Obat ini terlihat seperti garam, produk yang dijual dama bentuk bubuk dalam plastik kecil atau paket foil daro 200 dan 500mg dengan nama berbagai merek.
penggina dapat mengalami halusinasi akibat peningkatan kadar serotonin. Akibat buruk lain adalah dehidrasi, kerusakan jaringan otot dan gagal ginjal yang berujung pada kematian.
Gambar 5. Struktur senyawa Methylone
2.11. Kromatografi Lapis Tipis
Kromatografi merupakan suatu metode analisis yang didasarkan pada interaksi suatu komponen zat, antara fase diam atau fase strasioner dengan fase gerak atau fase mobil. Fase gerak adalah fase yang membawa sample, sedangkan fase diam adalah fase yang menahan sampel. Fase gerak akan merambat sepanjang fase diam dan terbentuklah kromatogram. Fase gerak dapat berupa cairan atau gas, sedangkan fase diam dapat berupa padatan atau cairan. Jika pemisahan terutama meliputi suatu partisi sederhana antara fase diam diam cair dan fase gerak cair juga maka fase ini dikenal sebagai kromatografi partisi. Jika gaya fisika ke permukaan terutama meliputi kemampuan retensi dari fase diamnya maka proses ini disebut kromatografi adsorpsi (Khopkar 2008).
didasarkan pada bentuk fase diamnya yaitu: kromatografi kolom jika fase diamnya dikemas dalam suatu kolom, kromatografi kertas jika fase diamnya berupa lembaran kertas dan kromatografi lapis tipis jika fase diamnya berupa lapis tipis. Prinsip dari kromatografi lapis tipis adalah cuplikan atau contoh diteteskan pada lapisan tipis lalu dimasukkan kedalam wadah berisi eluen atau pelarut, sehingga contoh terpisah menjadi komponen-komponennya. Setiap komponen akan terpisah dan bergerak dengan laju tertentu yang dinyatakan dengan faktor retensi atau retention factor (RF), yaitu perbandingan antara jarak yang ditempuh komponen sampel dan jarak yang ditempuh pelarut.
Nilai Rf dapat dihitung menggunakan rumus
Rf= jarak komponen sampel dihitung dari tempat penetesan atau penotolan Jarak batas pelarut dihitung dari tempat penetesan atau penotolan
memiliki RF hampir nol. Nilai RF bersifat karakteristik dari spesi-spesi khusus dalam pemisahan apapu yang tak diketahui. Dalam kromatografi selulosa yang sederhana mekanisme itu umumnya bertipe partisi; proses-proses adsorpsi hanya kecil saja peranannya, tetapi biasanya efek tersebut tidak nampak bila digunakan pelarut asam kuat (Vogel, 1994).
Fase diam pada kromatografi lapis tipis biasanya silika gel, alumina, kieslguhr, magnesium silikat, dan selulosa. Lapis tipis dari fase diam terikat pada plat yang cocok terbuat dari gelas, alumunium foil, atau plastik. Pemilihan pelarut atau fase gerak tergantung pada campuran yang akan dipisahkan dan fase diam yang akan digunakan. Fase gerak yang digunakan adalah pelarut organik atau campuran pelarut organik . campuran ini bertujuan untuk mengoptimalkan kepolaran dari sampel yang dianalisis. Komponen dalam campuran akan bergerak, hal tersebut disebabkan oleh adanya salah satu fase yang bergerak. Komponen yang memiliki afinitas lebih besar terhadap fase gerak atau afinitas lebih kecil terhadap fase diam akan bergerak lebih cepat daripada komponen yang memiliki sifat sebaliknya (Sastromidjojo 2002).
2.12. Kromatografi Gas
Kromatografi Gas (KG) merupakan suatu teknik analisis uang menggunakan gas sebagai fase penggerak. Zat yang dipisahkan dilewatkan dalam kolom yang diisi dengan fase idak bergerak. Gas pembawa mengalir melalui kolom dengan kecepatan tetap, memisahkan zat dalam gas atau cairan. Teknik ini dapat digunakan untuk identifikasi (kualitatif) ataupun untuk penentuan kadar (kuantutatif). Analisis secara kualitatif dengan membandingkan waktu retensi dari standar sampel. Kromatogram merupakan grafik berupa kerucut-kerucut atau dalam istilah modern disebut “peak”, hasil rekaman yang menggambarkan urutan
keluarnya komponen campuran dari kolom (Hendayana 2006).
Kromatografi adalah pemisahan campuran komponen-komponen didasarkan pada perbedaan tingkat interaksi terhadap dua fasa material pemisah. Campuran yang akan dipisahkan dibawa fasa gerak, yang kemudian dipaksa bergerak atau disaring melalui fasa diam karena pengaruh gaya berat atau gaya-gaya yang lain. Komponen-komponen dari campuran ditarik dan diperlambar oleh fasa diam pada tingkat yang berbeda-beda sehingga mereka bergerak bersama-sama dengan fasa gerak dalam waktu retensi yang berbeda-beda dan dengan demikian mereka terpisah (Widodo, 2000)
besar sehingga senyawa akan bergerak perlahan melalui kolom, sedangkan bila Kd kecil maka senyawa akan bergerak leboh cepat (Pecsok, 1976).
Kromatografi gas merupakan salah satu teknik pemisahan yang sering digunakan pada analisis kimia. Proses pemisahan komponen-komponen sampel pada kromatografi gas berlangsung didalam kolom didasarkan pada interaksi komponen sampel pada fase diam. Komponen-komponen yang akan dipisahkan didistribusikan di antara dua fasa yaitu fasa diam dan fasa gerak. Fasa gerak berfungsi membawa sampel sedangkan fasa diam berfungsi untuk mengadsorpsi/partisi komponen. Interaksi tersebut dapat berupa adsorbsi atau partisi. Jika fasa diamnya berupa padatan berpori maka peristiwanya berupa absorpdi sedangkan bila fasa diamnya berupa cairan maka peristiwanya adalah partisi gas-cair. Prinsip dasar dari kromatografi gas yaitu pemisahan komponen-komponen dari campuran berdasarkan perbedaan laju antara fasa gas yang bergerak melalui suatu lapisan serapan (fasa diam) yang stasioner (Barry, dkk., 2011)
2.12.1. Parameter Penting dalam Kromatografi Gas
Gas Pembawa Helium
yang khas (waktu tambat). Karena laju aliran tetap, komponen mempunyai volume gas pembawa yang khas (volum tambat). Gas pembawa haruslah lembam untuk mencegah antaraksi dengan cuplikan atau pelarut (fasa diam), dapat meminimumkan difusi gas, mudah didapat, murni, dan cocok untuk detektor yang digunakan (Mc Nair, 1988).
Gas yang dapat digunakan sebagai fase gerak dalam kromatografi gas harus bersifat inert (tidak bereaksi) dengan cuplikan maupun fase diam. Gas-gas yang biasa digunakan adalah Helium (He), Argon (Ar), Nitrogen (N), dan Hidrogen (H). Karena gas disimpan dalam silinder baja bertekanan tinggi maka gas tersebut akan mengalir dengan sendirinya secara cepat sambil membawa komponen-komponen campuran yang akan atau sudah terpisah. Dengan demikian gas tersebut disebut juga gas pembawa (carrier gas). Gas He memiliki efisiensi yang naik sebagai gas pembawa. Keuntungan gas He adalah apabila percobaan dilakukan pada tekanan yang tetap, kecepatan alir akan berkurang ketika suhu naik. Keuntungan lain gas pembawa He memberikan efisiensi relatif stabil dengan perubahan kecepatan alir (Hendayana 2006).
kotoran dalam gas pembawa, biasanya gas dialirkan melalui saringan yang disebut molecular seive untuk menghilangkan air dan hidrokarbon (Hendayana, 2006)
Kolom terbuka (open Tubular Column)
Pipa kolom dapat dibuat dari tembaga, baja nirkarat, alumunium, dan kaca yang berbentuk lurus, lengkung, atau melingka. Tembaga kurang cocok karena dapat menyerap atau bereaksi dengan komponen cuplikan tertentu (amina, asetilena, terpena, dan steroid). Pada umumnya digunakan kolom baja nirkarat, dikemas kerika masih berbentuk lurus supaya kemasan seraga,, kemudian dilingkarkan agar dapat dipasang dalam ruang kolom yang terbatas. Kolom lurus lebih efisien, tetapi dapat menjadi tidak praktis, terutama bila radas bekerja pada suhu tinggi. Jika kolom dilingkarkan, garis tengah lingkaran paling sedikit harus sepuluh kali garis tengah kolom, yaitu untuk meminimumkan difusi dan pengaruh jalur balap (Mc Nair, 1988).
namun dengan semakin panjangnya kolom diharapkan kolom akan lebih efisien dan perbedaan waktu retensi senyawa satu terhadap senyawa lainnya akan bertambah yang akan memberikan dampak pada peningkatan selektivitas (Hendayana 2006).
Secara umum terdapat 2 jenis kolom, yaitu :
- Packed column, kolom pak terbuat dari stainless steel atau gelas dengan garis tengah 3-6 mm dan panjang 1-5 m. Kolom diisi dengan serbuk zat padat halus atau zat padat sebagau zat pendukung yangbdilapisi zat cair kental yang sukar menguap sebagai fasa diam. Jenis kolom pak ini lebih disukai untuk tujuan preparatif karena dapat menampung jumlah cuplikan yang banyak.
- Open tubular column, kolom terbuka lebih kecil dan lebih panjang daripada kolom pak. Diameter kolom terbuka berkisar antara 0,1-0,7 mm dan panjangnya berkisar antara 15-100 m. Jenis kolom ini disebut juga kolom kapiler. (Vogel, 1994)
Detektor
detector), detektor fotometri nyala (flame photometric detector), dan detektor nyala alkali (alkali flame detector) (Hendayana, 2006)
Komponen-komponen yang dipisahkan di dalam kolom kemudian diubah menjadi sinyal-sinyal listrik. Kuat lemahnya sinyal tergantung pada laju alir massa sampel dan bukan pada konsentrasi sampel gas penunjang. Detektor harus terletak dekat kolom baik untuk mengindarkan kondensasi cairan maupun dekomposisi sampel sebelum mencapai detektor.
Ciri-ciri detektor yang ideal dalam kromatografi gas:
1)Sensitif, sekalipun konsentrasi kecil-kecil tetapi dapat dideteksi. 2)Stabil, sekalipun dalam keadaan suhu tinggi, dapat dikatakan
detektor harus mempunyai sifat reproduksibillity yang baik. 3)Respon harus linear dengan kepekatan.
4)Mudah digunakan tidak rumit dalam pemakaian (Sastrohamidjojo, 1985)
terdeteksi berdasarkan massanya yang digambarkan sebagai spektra massa (Hendayana 2006).
Tempat injeksi
Tempat injeksi merupakan tempat penyuntikan sampel baik sampel cair atau gas dengan syarat sampel tersebut mudah menguap dan stabil. Pada bagian ini biasanya ditambahkan alat pyrolizer yaitu alat yang dapat mempirolisis bagian padat menjadi gas. Di dalam tempat injeksi sampel terdapat pemanas yang suhunya dapat diatur untuk menguapkan sampel. Suhu tempat penyuntikan sampel biasanya berkisar 500C diatas titik didih cuplikan.
Contoh cair dimasukkan dengan menggunakan spuit mikro dengan jarum hipodermik. Jarum ini ditusukkan pada sekat karet silikon yang mengendap sendiri dan contohnya diinjeksikan sengan merata ke dalam blok logam yang dipanasi pada ujung kolom. Manipulasi split dapat dianggap sebagai suatu seni yang dikembangkan dengan latihan dan sasarannya haruslah bagaimana memasukkan dengan cara yang dapat direproduksi. Untuk efisiensi terbesar, hendaknya digunakan ukuran contohnya yang sekecil mungkin (1 sampai 10 µl) yang konsisten dengan kepekaan detektor (Vogel 1994).
2.13. Spektrofotometer massa
cuplikan berdifusi kedalam sistem spektrometer massa yang bertekanan rendah, lalu diionkan dengan energi yang cukup untuk memutus ikatan kimia. Ion bermuatan positif yang terbentuk dipercepat dalam medan magnet yang menyebarkan ion tersebut dan memungkinkan pengukuran kelimpahan nisbi ion yang mempunya nisbah massa terhadap muatan tertentu. Rekaman kelimpahan ion terhadap massa merupakan grafik spektrum massa yang terdiri atas sederetan garis yang intensitasnya berbeda-beda pada satuan massa yang berlainan. Pada mayoritas senyawa, sebagian kecil dari senyawa induk tahan terhadap proses penguapan dan akan direkam sebagai puncak ion molekul atau ion induk. Massa ion induk dan ion lainnya dapat diukur dengan sangat tepat (sampai 0,00001 satuan massa). Ketetapannya sedemikian rupa sehingga dapat menunjukkan rumus molekl senyawa secara tepat dan dengan demikian analisis unsur yang lazim (yang biasanya memerlukan beberapa mg senyawa) tidak diperlukan lagi (Harborne 1987).
2.13.1. Instrumen dari spektroskopi massa sebagai berikut:
Sumber ion
elektron dan molekul, tapi karena interaksi medan elektron dan molekul, ketika berdekatan. Hal tersebut menyebabkan satu elektron dan molekul ketika berdekatan. Hal terdebut menyebabkan satu elektron lepas, sehingga terbentuk ion molekular M+, yang memiliki massa sama dengan molekul netral, tetapi bermuatan positif. Adapun perbandingan massa fragmen tersebut dengan muatannya disebut mass to charge ratio yang disimbolkan m/z. Ion yang terbentuk akan didorong ke quadrupoles atau mass filter, Quadrupoles berupa empat elektromagnet.
Filter
Pada quadrupoles, ion-ion dikelompokkan menurut m/z dengan kombinasi frekuensi radio yang bergantian dengan tegangan DC. Hanya ion dengan M/Z tertentu yang dilewatkan olehquadrupoles menuju ke detektor.
Detektor
Detektor pada spektroskopi masaa menghasilkan urutan puncak-puncak, dimana setiap puncak mewakili satu senyawa dalam campuran yang melaluinya (Roy,dkk., 1991)
2.13.2. Parameter Penting dalam Spektrofotometer Massa
1) Analisa Massa Ion dengan Ionisasi Elektron dan
Cuplikan yang diubah menjadi molekul asal dan ditunjukkan dengan spektra massa dihasilkan dari sumber ion dalam SM. Sumber ion yang digunakan adalah ionisasi Elektron (EI). Pada metode ini “pereaksi” yang menghasilkan ion adalah berupa berkas elektron dengan energi sebesar 70eV. Berkas elektron tersebut “menduduh”
filamen yang memijar dan bergerak melalui kamar pengion menuju anoda yang terletak bersebrangan. Aliran molekul cuplikan yang teruapkan (pada tekanan sekitar 10-2) masuk dalam sumber berintegrasi dengan berkas elektron membentuk berbagai hasil meliputi ion-ion positif. Ion-ion tersebut didorong keluar dari ruang ionisasi oleh potensial “penolak” yang relatif kecil, dan kemudian
dipercepat masuk kedalam perangkat analisis massa (saringan kuadrupol). Sebagian molekul cuplikan berikut hasil belahannya dikeluarkan secara kontinu menggunakan pompa vakum yang terdapat pada ruangan sumber ion. Ion-ion positif yang masuk ke dalam saringan kuadrupol kemudian akan dipisahkan lebih lanjut (multiple ion monitoring) (Mv Nair dan Bonelli 1988).
2) Mekanisme Dasar Fragmentasi Ion
mengenal molekul-molekul yang lebih kompleks dan kemungkinan-kemungkinan struktur alternatif lain yang dapat mengungkapkan spektra massa yang teramati, maka harus mempelajari spektra molekul-molekul yang mendekati (strukturnya mirip) (McNair dan bonelli 1988).
2.14. Kromatografi Gas – Spektrofotometer Massa
Kromatografi Gas-Spektrofotometer Massa (KG-SM) adalah sebuah teknik instumental yang terdiri dari Kromatografi Gas (KG) digabungkan dengan Spektrofotometer Massa (SM), dimana campuran kompleks suatu bahan kimia dapat dipisahkan dan diidentifikasi. Teknik ini dapat digunakan untuk menganalisis berbagai senyawa dengan berbagai macam berat molekul yang banyak ditemukan di alam. Kromatografi Gas - Spektrofotometri Massa merupakan alat yang dapat digunakan untuk menganalisis berbagai senyawa yang mudah menguap maupun yang tidak mudah menguap. Kromatografi gas berfungsi sebagai alat pemisah berbagai komponen campuran dalam sampel, sedangkan spektrofotometer massa berfungsi untuk mendeteksi masing-masing komponen yang telah terpisah pada sistem kromatografi gas. Kromatografi gas -spektrofotometri massa memiliki tingkat selektifitas dan sensitivitas tinggi yang ditunjukkan dengan adanya tampilan yang optimal dengan ukuran sampel nanogram (McLafferty 1980).
dan spektrometri massa memiliki keunikan masing-masing dimana keduanya memiliki kelebihan dan kekurangan. Dengan menggabungkan kedua teknik tersebut diharapkan mampu meningkatkan kemampuan dalam menganalisis sampel dengan mengambil kelebihan masing-masing teknik dan meminimalisir kekurangannya (Hites, 1985).
Kromatografi gas dan spektrometri massa dalam banyak hal memiliki banya kesamaan dalam tekniknya. Untuk kedua teknik tersebut sampel yang dibutuhkan dalam bentuk fase uap dan keduanya juga sama-sama membutuhkan jumlah sampel yang sedikit. Disisi lain, kedua teknik tersebut memiliki perbedaan yang cukup besar yakni pada kondisi operasinya. Senyawa yang terdapat pada kromatografi gas adalah senyawa yang digunakan untuk sebagai gas pembawa dalam alat GC dengan tekanan kurang lebih 760 torr, sedangkan spektrofotometer massa beroperasi pada kondisi vakum dengan kondisi tekanan 10-6-10-5torr (Hites,1985).
2.14.1. Prinsip Kerja
kromatografi gas dan memungkinkan spektrofotometer massa untuk menangkap, ionisasi, mempercepat, membelokkan dan mendeteksi molekul terionisasi secara terpisah. Spektrofotometer massa melakukan hal ini dengan memecahkan masing-masing molekul menjadi terionisasi mendeteksi fragmen menggunakan massa untuk mengisi rasio (Hites, 1985). Instrumen Kromatografi Gas-Spektrofotometer Massa sebagai berikut :
37
Alat yang digunakan dalam percobaan ini adalah: 1. Pipet tetes
16. Kromatografi Gas-Spektrofotometer Massa tipe Clarus 500 17. Lampu UV
18. Kromatogram jar
21. Omega-12ectraction solvent concentric 22. Mortar
23. pH meter 3.2.Bahan
Bahan yang digunakan dalam percobaan ini adalah: 1. 5 jenis tablet mengandung meth 2. 5 jenis urine mengandung meth 3. Aquades
4. DCM : DCE : Heptane (1:1:1) 5. NaOH 0,1N
6. Toxi-Disc Blank A 7. Toxi-Disc SA
8. Developing HAaa 25 9. Amoniak
3.3.Cara Kerja
3.3.1. Kromatografi Lapis Tipis
A. Tablet methamphetamine
a) Langkah Awal
Pertama electric warmer dinyalakan. Dipersiapkan solvent concentric dengan tutup dan 5 buah disposable concentic cups untuk tablet meth. Kemudian diberi label sesuai kode tablet meth. Sampel tablet meth yang sebelumnya sudah ditimbang sebanya 25 mg menggunakan timbangan microbalance dimasukkan kedalam toxi tub. Masing-masing toxi tub berisi sampel ditambahkan aquades sebanyak 5 mL. Setelah itu larutan dibasakan menggunakan NaOH 0,1 N hingga mencapai pH = 10.
b) Ekstraksi
Sampel yang akan dianalisis kemudian ditambahkan 1,5 ml DCM:DCE:Heptane (1:1:1). Sample kemudian dihomogenkan dengan dilakukan ekstraksi 5 menit dan divortex hingga larut sempurna. Larutan di centrifuge selama 5 menit dengan 3,000 RPM. Lalu larutan organik yang terletak dipermukaan bawah diambil sebanyak 400 µl perlahan dan diletakkan kedalam disposable concentric cups.
c) Pemekatan Sampel
concentric yang terdapat Toxic-Lab Disc Blank A. Kemudian dipanaskan dalam Omega-12extraction solvent concentric dalam kondisi tertutup menggunakan electric warmer sampai kering. Ekstrak sampel diuapkan dengan udara hangat dari heat gun yang diarahkan melewati bagian atas cups untuk mempercepat proses penguapan.
d) Inokulasi
Toxi-Grams Blank A diletakkan di atas selembar kertas HVS bersih dan kering. Sebelumnya Toxi-Gram Blank A dipanaskan terlebih dahulu menggunakan electric warmer + /- 10 detik. Lalu Toxi-Lab Disc Blank A diletakkan kedalam lubang yang sudah tersedia pada kromatogram. Pada lubang pertama diisi Toxi-Lab Disc Blank A kemudian pada lubang ketiga sampai kelima diisi oleh sampel dan lubang keenam diisi oleh standar Toxi-Disc SA. Pada saat meletakkan Disc menggunakan jarum perlahan dan ditahan menggunakan kertas parafilm. Jangan sampai merusak kromatogram. Setelah Disc sudah melekat sempurna Kromatogram ditempatkan pada kromatogram yang telah berisi cakuadesan.
e) Elusi
diambil dan dimasuukan kedalam kromatogram jar . Dilakukan elusi kromatogram dengan larutan eluen hingga mencapai titik 9,5 cm. Kemudian diangkat dan dikeringkan di atas electric warmer menghadap kebawah selama +/- 30 detik untuk menguapkan residu.
f) Identifikasi
B. Urine Methamphetamine
a) Langkah Awal
Pertama dinyalakan electric warmer. Dipersiapkan solvent concentric dengan tutup dan 5 buah disposable concentic cups untuk urine meth. Kemudian diberi label sesuai kode urine meth. Sample urine meth diambil sebanyak 5mil kemudian dimasukkan kedalam Toxi tub. Masing-masing Toxi tub berisi sampel dicek pH awal terlebih dahulu. Setelah itu larutan dibasakan menggunakan NaOh 0,1 N hingga mencapai pH = 10.
b) Ekstraksi
Sampel yang akan dianalisis kemudian ditambahkan 1,5 ml DCM:DCE:Heptane (1:1:1). Sample kemudian dihomogenkan dengan dilakukan ekstraksi 5 menit hingga larut sempurna. Larutan di centrifuge selama 5 menit dengan 3,000 rpm. Lalu larutan organik yang terletak dipermukaan bawah di ambil sebanyak 400 µl perlahan dan diletakkan kedalam disposable concentric cups.
c) Pemekatan Sampel
Ekstrak sampel diuapkan dengan udara hangat dari heat gun yang diarahkan melewati bagian atas cups untuk mempercepat proses penguapan.
d) Inokulasi
Toxi-Grams Blank A diletakkan diatas selembar kertas HVS bersih dan kering. Sebelumnya Toxi-Gram Blank A dipanaskan terlebih dahulu menggunakan electric warmer + /- 10 detik. Lalu Toxi-Lab Disc Blank A diletakkan kedalam lubang yang sudah tersedia pada kromatogram. Pada lubang pertama di isi Toxi-Lab Disc Blank A kemudian pada lubang ketiga sampai kelima diisi oleh sampel dan lubang keenam diisi oleh standar Toxi-Disc SA. Pada saat meletakkan Disc menggunakan jarum perlahan dan ditahan menggunakan kertas parafilm. Jangan sampai merusak kromatogram. Setelah Disc sudah melekat sempurna Kromatogram ditempatkan pada kromatogram yang telah berisi cakuadesan.
e) Elusi
menghadap kebawah selama +/- 30 detik untuk menguapkan residu.
f) Identifikasi
Toxi-Grams Blank A dianalisis kedalam 3 wadah yang berbeda isinya. Pada setiap tingkat dibandingkan hasil yang didapat dengan standar. Langkah awal kromatogram dimasukkan kedalam TOXI-DIP A-1 jar selama 15 menit. Selanjutnya diangkat toxi-Gram dan dipanaskan dengan electric warmer + /- 10 detik. Lalu dideteksi dimasukkan kedalam TOXI-DIP A-2 ditahan selama +/- 10 detik dan diangkat. Dibandingkan hasil spot yang didapat dengan spot standar obat. Kemudian kromatogram dimasukkan kedalam TOXI-DIP H2O untuk dilakukan pencucian. Beberapa obat akan hilang atau memudar ketika dilakukan pencucian. Kemudian diletakkan pada lampu UV. Lalu dibandingkan spot yang didapat dengan spot standar obat. Setelah itu yang ketiga dimasukkan kedalam TOXI-DIP A-3 maka akan
menggunakan Kromatografi Gas-Spektrofotometer Massa. Sampel tablet masing-masing digerus menggunakan mortar dan ditimbang sebanyak 25mg menggunakan timbangan microbalance. Kemudian dimasukkan kedalam toxi tub dan ditambahkan aquades sebanyak 5mL. Kemudian ditambahkan NaOH 0,1N hingga pH 10. Selanjutnya ditambahkan pelarut DCM:DCE:Heptane dengan perbandingan 1:1:1 sebanyak 1,5 mL. Setelah itu dilakukan ekstraksi selama 5 menit dengan kecepatan 3.000 rpm dan kemudian dimasukkan ke dalam centrifuge selama 5 menit untuk mendapatkan larutan organik. Larutan organik yang berada pada bagian bawah toxi tub diambil dan dimasuukan ke dalam glass insert. Setelah itu sampel siap dianalisis menggunakan KG-SM, sampel diambil sebanyak 0,5µL menggunakan syringe.
B. Urine methamphetamine
47
Kegiatan PKL yang dilakukan di Badan Narkotika Nasional, Jakarta ini meliputi hasil kualitatif dari tablet dan urine dari para pemakai maupun pengedar narkotika yang telah dijaring oleh Polisi. Sampel tablet dan urine yang mengandung Methamfetamine didapat dari hasil jaringan polisi dari pemakai maupun pengedar narkotika di Indonesia. Sampel yang dianalisis meliputi tablet dan urine yang mengandung Methamfetamine senyawa aktif dengan beberapa langkah pengujian.
A. Tablet Methamfetamine
a) Penampakan fisik
Tablet Methamfethamine berasal dari penangkapan polisi di daerah seluruh Indonesia. Umumnya Methamfetamine memiliki berbagai bentuk seperti kristal putih, serbuk, dan tablet. Jumlah sampel yang dianalisis sebanyak lima buah dengan penampakan yang berbeda-beda.
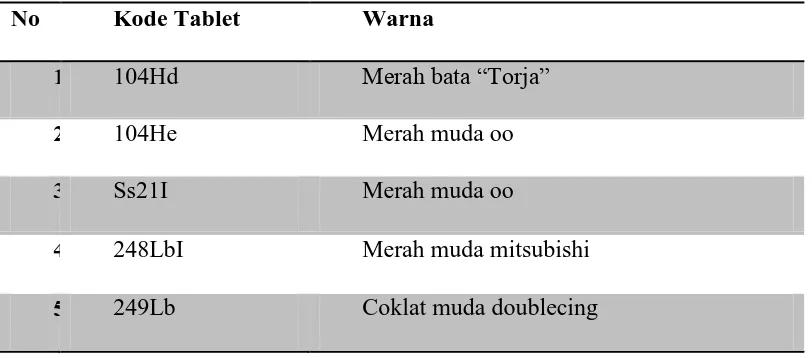
Tabel 1. Kondisi fisik tablet methamfetamine
No Kode Tablet Warna
1 104Hd Merah bata “Torja”
2 104He Merah muda oo
3 Ss21I Merah muda oo
4 248LbI Merah muda mitsubishi
Gambar 7. Sampel tablet methamfetamine
Tablet Methamfetamine yang beredar di pasar gelap memiliki penampakan yang berbeda-beda. Warna tablet yang berbeda ini dikarenakan pembuatannya berbeda-beda. Methamfetamine memiliki pengaruh yang kuat terhadap syaraf. Pemakai shabu-shabu akan selalu bergantung pada obat bius tersebut dan akan berlangsung lama.
b) Kromatografi Lapis Tipis
Metode yang digunakan pertama kali ialah Kromatografi Lapis Tipis (KLT) menggunakan Toxi Lab A Drug Detection System. Toxi-gram A adalah kertas glass fiber digunakan sebagai penunjang fasa diam yang mengandung asam silikat dan garam vanadium. Asam silikat berperan sebagai fasa diam dan garam vanadium sebagai pembentuk senyawa kompleks yang berwarna.
Eluen ini dibuat dari beberapa campuran pelarut, karena jika hanya menggunakan pelarut tunggal spot senyawa dapat bergerak terlalu jauh, bahkan tidak dapat terlihat. Sebelumnya eluen dijenuhkan terlebih dahulu agar isi chamber terisi penuh dengan uap eluen dan sehingga pada saat memasukkan plat maka aliran eluen akan rata dan cepat, sehingga diperoleh hasil yang baik. Penggunaan eluen hanya satu kali pakai karena eluen yang digunakan dimungkinkan telah terkontaminasi oleh toxi-gram sebelumnya, sehingga dapat mengganggu pemisahan. Chamber yang digunakan juga harus bersih dari air maupun pengotor. Pada tahap elusi chamber harus dalam posisi tetap, tidak boleh berpindah-pindah, sehingga elusi berjalan dengan sempurna.
Berdasarkan data analisis yang diperoleh sampel tablet yang di ekstraksi menggunakan campuran pelarut DCM:DCE:Heptane positif Methamfetamine. Pada toxi-gram pertam berisi tablet meth kode 248LbI, 249Lb, dan 104He dan toxi-gram kedua berisi 104Hd dan ss21I.
ss21I menghasilkan spot yaitu methamfetamine, methylon dan dekstrometorfan.
Kemudian toxi-gram dimasukkan kedalam Toxi-Dip H20, toxi-gram dicelupkan hingga spot yang muncul pada Toxi-Dip A2 hilang. Kemudian dimasukkan kedalam lampu UV. Pada tahap UV spot dekstrometorfan mengalami fluorosensi. Senyawa methamphetamine menyerap sinar UV karna senyawa tersebut memiliki ikatan rangkap terkonjugasi maka sinar UV dilewatkan pada fasa diam akan mengenai senyawa tersebut namun tidak mengenai indikator fluorosensi karena terhalang oleh senyawa tersebut. Hasilnya berupa spot gelap. Walaupun dektrometorfan juga memiliki cincin aromatik namun mengandung gugu –N(CH3)2 yang dapat meningkatkan fluorosensi sehingga senyawa ini spotnya berfluorosensi.
Kemudian toxi-gram dimasukkan kedalam Toxi-Dip A3 yang mengandung asam asetat ditambah iodine. Pada tahap ini spot yang akan muncul adalah spot kafein dan ketamine.
c) Kromatografi Gas-Spektrofotometer Massa
Sampel tablet methamfetamine setelah dilakukan analisis KLT untuk lebih memastikan keakuratan hasil dilakukan analisis menggunkan Kromatografi Gas-Spektrofotometer Massa (KG-SM).
ditambahkan campuran pelarut yaitu DCM:DCE:Heptane dengan perbandingan 1:1:1 sebanya 1,5mL . Setelah itu diekstraksi selama 5menit agar larutan menjadi homogen. Perlakuan selanjutnya adalah memisahkan antara cairan dan endapan berdasarkan bobot senyawa tersebut dan untuk memisahkan antara larutan organik dan larutan anorganik menggunakan centrifuge. Sampel yang telah diekstrak kemudian diambil larutan organik yang berada pada bagian bawah dan dimasukkan kedalam glass insert kemudian diinjeksikan kedalam KG-SM untuk mengetahui senyawa-senyawa lain yang terdapat dalam sampel tablet.
Volume yang diinjeksikan sebanyak 0,5µL setiap sampelnya. Waktu yang digunakan untuk identifikasi sebanyak 24 menit. Panjangnya waktu injeksi bertujuan untuk dapat mengidentifikasi senyawa aktif lain yang memilik waktu retensi (tR) yang cukup panjang. Sampel yang dianalisis dengan KG-SM akan melewati rangkaian dari KG dan saat pemisahan dengan KG berdasarkan titik didih masing-masing senyawa yang terdapat dalam sampel.
gunakan adalah HP-5ms Ultra Inert. Kolom HP-5ms UI adalah kolom non polar leburan silika yang secara khusus dirancang untuk spektrofotometer massa. Kolom HP-5ms UI bersifat non polar sehingga senyawa dalam sampel yang memiliki tingkat kepolaran tinggi akan terpisah lebih dahulu kemudian hasil pemisahan akan masuk kedalam detektor spektrofotometer masa untuk selanjutnya difragmentasi dalam bentuk pecahan massa dan akan menghasilkan spektra massa berdasarkan kelimpahan massanya dan kemudian dari spektra tersebut dapat diidentifikasi bentuk molekulnya dan yang memiliki tingkat kepolaran terendah akan terpisah terakhir.
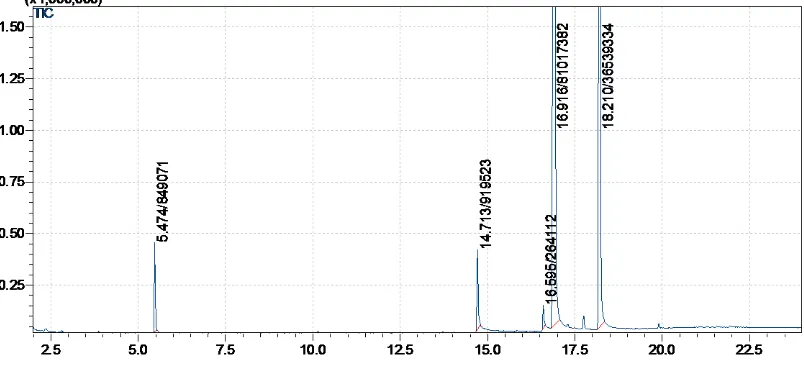
Senyawa aktif lain pada sampel tablet 248LbI hasil identifikasi menggunakan KG-SM pada gambar dibawah ini dan kemudian gambar tersebut diidentifikasi lebih lanjut dengan SM dangan hasil berupa spektra yang dapat dilihat pada lampiran
Gambar 8. Hasil Kromatografi gas tablet 248LbI
Methamfetamine memiliki tR sebesar 5.474, dekstrometorfan memiliki tR sebesar 16.916, dan promethazine memiliki rentang waktu 18.210.
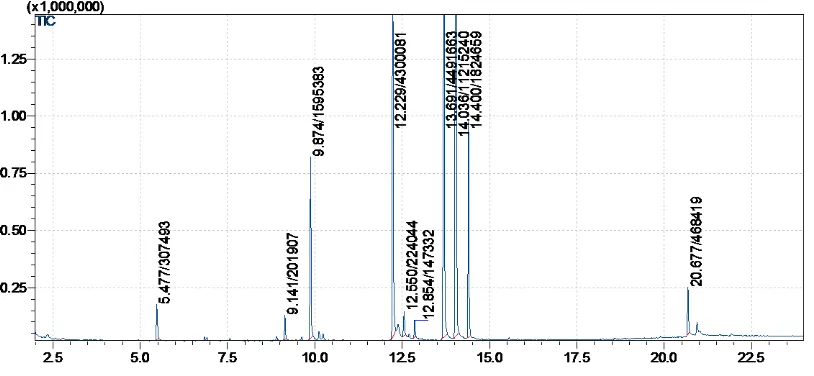
Senyawa aktif lain pada sampel tablet 104He hasil identifikasi menggunakan KG-SM pada gambar dibawah ini dan kemudian gambar tersebut diidentifikasi lebih lanjut dengan SM dangan hasil berupa spektra yang dapat dilihat pada lampiran.
Gambar 9. Hasil Kromatografi gas tablet 104He
Berdasarkan hasil identifikasi tersebut dapat dilihat bahwa terdapat senyawa lain selain methamfetamine pada sampel tablet 104He. Methamfetamine memiliki tR sebesar 5.477, caffein memiliki tR sebesar 13.691, ketamin memiliki tR sebesar 14.0367, dan methoxetamine memiliki tR sebesar 14.400.
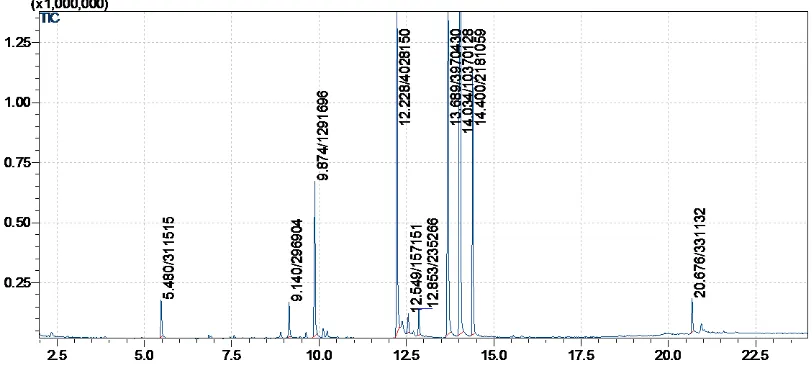
Gambar 10. Hasil Kromatografi gas tablet 249Lb
Berdasarkan hasil identifikasi tersebut dapat dilihat bahwa terdapat senyawa lain selain methamfetamine pada sampel tablet 249Lb. Methamfetamine memiliki tR sebesar 5.480, caffein memiliki tR sebesar 13.689, ketamine memiliki tR sebesar 14.034, dan methoxetamine memiliki tR sebesar 14.400.
Gambar 11. Hasil Kromatografi gas tablet 104Hd
Berdasarkan hasil identifikasi tersebut dapat dilihat bahwa terdapat senyawa lain selain methamphetamine pada sampel tablet 104Hd. Methamfetamine memiliki tR sebesar 5.480, caffein memiliki tR sebesar 13.686, dan ketamine memiliki tR sebesar 14.036.
Gambar 12. Hasil Kromatografi gas ss21I
Berdasarkan hasil identifikasi tersebut dapat dilihat bahwa terdapat senyawa lain selain methamphetamine pada sampel tablet ss21I. Methamfetamine memiliki tR sebesar 5.479, caffein memiliki tR sebesar 13.696, dan ketamine memiliki tR sebesar 14.040.
B. Urine
a) Penampakan fisik
Gambar 13. Sampel urine methamphetamine
b) Kromatografi Lapis Tipis
Metode yang digunakan pertama kali ialah Kromatografi Lapis Tipis (KLT) menggunakan Toxi Lab A Drug Detection System. Toxi-gram A adalah kertas glass fiber digunakan sebagai penunjang fasa diam yang mengandung asam silikat dan garam vanadium. Asam silikat berperan sebagai fasa diam dan garam vanadium sebagai pembentuk senyawa kompleks yang berwarna.
Toxi-Lab Disc Blank A kemudian pada lubang ketiga sampai kelima diisi oleh sampel dan lubang keenam diisi oleh standar Toxi-Disc SA. Toxi-Disc maupun toxi-gram tidak boleh terkontaminasi sehingga harus ditempatkan didaerah yang bersih dan memegannya harus menggunakan jarum dan pinset. Lalu dilekatkan Toxi-Lab Disc Blank A menggunakan kertas parafilm. Kertas parafilm yang digunakan juga harus diganti-ganti agar Toxi-gram tidak terkontaminasi oleh sampel lain. Penggesekan harus dilakukan dengan hati-hati gar tidak merusak toxi-gram. Setelah itu dilakukan elusi toxi-gram BlankA yang sudah siap diinokulasi dimasukkan kedalam kromatogram jar atau chamber yang berisi 3 mL developing HAaa25 dan 25µl amoniak. Developing HAaa 25 terbuat dari n-heksan 60 mL, aseton 40mL, dan asetaldehid 0,1 mL . Eluen ini dibuat dari beberapa campuran pelarut, karena jika hanya menggunakan pelarut tunggal spot senyawa dapat bergerak terlalu jauh, bahkan tidak dapat terlihat. Sebelumnya eluen dijenuhkan terlebih dahulu agar isi chamber terisi penuh dengan uap eluen dan sehingga pada saat memasukkan plat maka aliran eluen akan rata dan cepat, sehingga diperoleh hasil yang baik. Penggunaan eluen hanya satu kali pakai karena eluen yang digunakan dimungkinkan telah terkontaminasi oleh toxi-gram sebelumnya, sehingga dapat mengganggu pemisahan. Chamber yang digunakan juga harus bersih dari air maupun pengotor. Pada tahap elusi chamber harus dalam posisi tetap, tidak boleh berpindah-pindah, sehingga elusi berjalan dengan sempurna.
Sample urine dengan nomor kode 373A, 374A, 375A, ss75A, dan 181Bb positif mengandung methamfetamine.
Toxi-gram mula-mula dimasukkan kedalam Toxi-Dip A1 selam 15 menit. Toxi-Dip A1 berisi formaldehid. Setalah itu toxi-gram dipanaskan +/-10 detik diatas electric warmer . Kemudian toxi-gram dimasukkan kedalam Toxi-Dip A2 yang berisi asam sulfat. Sampel dengan nomor kode 373A, 374A, 375A, ss75A, dan 181Bb menghasilkan spot methamfetamine.
Kemudian toxi-gram dimasukkan kedalam Toxi-Dip H20, toxi-gram dicelupkan hingga spot yang muncul pada Toxi-Dip A2 hilang. Kemudian dimasukkan kedalam lampu fluoro. Pada tahap UV spot dekstrometorfan mengalami fluorosensi. Senyawa methamfetamine menyerap sinar UV karna senyawa tersebut memiliki ikatan rangkap terkonjugasi maka sinar UV dilewatkan pada fasa diam akan mengenai senyawa tersebut namun tidak mengenai indikator fluorosensi karena terhalang oleh senyawa tersebut. Hasilnya berupa spot gelap. Walaupun dektrometorfan juga memiliki cincin aromatik namun mengandung gugu –N(CH3)2 yang dapat meningkatkan fluorosensi sehingga senyawa ini spotnya berfluorosensi.
c) Kromatografi Gas-Spektrofotometer Massa
Sampel urine yang terlah dianalaisis menggunakan KLT kemudian dilakukan identifikasi kemabali menggunakan KG-SM untuk mengetahui senyawa lain yang terdapat dalam sampel urine yang akan dianalisis. Mula-mula sampel urine diambil masing-masing sebanyak 5 mL kemudian dimasukkan kedalam Toxi Tub, setelah itu dibasakan menggunakan NaOH 0,1N hingga pH 10. Setelah itu ditambahkan campuran pelarut yaitu DCM:DCE:Heptane dengan perbandingan 1:1:1 sebanya 1,5 mL . Setelah itu diekstraksi selama 5 menit agar larutan menjadi homogen. Perlakuan selanjutnya adalah memisahkan antara cairan dan endapan berdasarkan bobot senyawa tersebut dan untuk memisahkan antara larutan organik dan larutan anorganik menggunakan centrifuge. Sampel yang telah diektrak kemudian diambil larutan organik yang berada pada bagian bawah dan dimasukkan kedalam glass insert kemudian diinjeksikan kedalam KG-MS untuk mengetahui senyawa-senyawa lain yang terdapat dalam sampel urine.
Gambar 14. Hasil Kromatografi gas urine 373A
Berdasarkan hasil identifikasi tersebut dapat dilihat bahwa terdapat senyawa lain selain methamfetamine pada sampel urine 373A. Methamfetamine memiliki tR sebesar 5.474. Ini menunjukkan bahwa sampel urin 373A positif methamfetamine.
Hasil analisis sampel urin 374A menggunakan KG-MS dapat dilihat pada hasil gambar berikut.
Berdasarkan hasil identifikasi tersebut dapat dilihat bahwa terdapat senyawa lain selain methamfetamine pada sampel urine 374A. Methamfetamine memiliki tR sebesar 5.482. Ini menunjukkan bahwa sampel urin 374A positif methamfetamine.
Hasil analisis sampel urin 375A menggunakan KG-MS dapat dilihat pada hasil gambar berikut.
Gambar 16. Hasil Kromatografi gas urine 375A
Berdasarkan hasil identifikasi tersebut dapat dilihat bahwa terdapat senyawa lain selain methamfetamine pada sampel urine 375A. Methamfetamine memiliki tR sebesar 5.502. Ini menunjukkan bahwa sampel urin 375A positif methamfetamine.
Gambar 17. Hasil Kromatografi gas urine ss75A
Berdasarkan hasil identifikasi tersebut dapat dilihat bahwa terdapat senyawa lain selain methamfetamine pada sampel urine ss75A. Methamfetamine memiliki tR sebesar 5.492. Ini menunjukkan bahwa sampel urin ss75A positif methamfetamine.
Gambar 18. Hasil Kromatografi gas urine 181Bb
BAB V
KESIMPULAN DAN SARAN
5.1.Kesimpulan
Berdasarkan percobaan yang telah dilakukan mengenai analisis kualitatif tablet dan urine mengandung methamfetamine, dapat disimpulkan bahwa adalah:
1. Senyawa lain yang terdapat pada tablet methamfetamine adalah dekstrometorfan, promatezine, ketamine, kafein, dan methoxetamine. 2. Senyawa aktif lain yang terdapat pada urine methamfetamine adalah
dekstrometorfan.
3. Methamfetamine dalam tablet dan urine pada KG-SM muncul pada menit ke 5,5.
5.2.Saran
DAFTAR PUSTAKA
Abdi, dkk., 2004, Detection of Morphine in Opioid Abusers Hair by GC/MS, DARU Journal, Volume 12 No. 2 Hal. 71 – 75.
Baumgartner, A, dkk. , 1979, Radioimmunoassay of Hair for Determining Opiate
– Abuse Histories, The Journal of Nuclear Medicine, Hal. 748 – 752
BNN., 2007, Pencegahan Penyalahgunaan Narkoba Sejak Usia Dini, Jakarta. Dirdjosisworo, Soedjon., 1987, Hukum Narkotika Indonesia, Alumni, Bandung. Gritter., 1991, Pengantar Kromatografi, ITB, Bandung.
Hakim, M. Arief., 2004, Bahaya Narkoba-Alkohol: Cara Islam Mengatasi, Mencegah dan Melawan, Komplek Cijambe Indah, Bandung.
Hendayana, Sumar., 2006, Metode Kromatografi dan Elektroforesis Modern, PT Remaja Rosdakarya, Bandung.
Ketamine, 2009, dissociative-anaesthetic. Disitasi dari: http://www.ketamine.com/dissociative-anaesthetic. (28 september2009). Makarao, Moh Taufik., 2005, Tindak Pidana Narkotika, Ghalia, Indonesia
Mardani.,2008, Penyalahgunaan Narkoba dalam Prespektif Hukum Islam dan Hukum pidana Nasional, PT Raja Grafindo Persada, Jakarta.
Ma’roef, M. Ridha., 1976, Narkotika Masalah dan Bahayanya, CV Marga djaja,
Jakarta.
Nair, MC, dan Harlod M.,1988, Dasar Kromatografi Gas, ITB, Bandung
Partodiharjo, Subagyo., 2008, Kenali Narkoba dan Musuhi Penyalahgunaannya, Erlangga, Jakarta.
Tim Visimedia., 2006, Mengenal Jenis dan Efek Buruk Narkoba, Visimedia. Wirjoatmodjo K. 2000. Anestesiologi dan Reanimasi Modul Dasar Untuk
Lampiran 1.Gambar alat
Kromatografi Gas-Spektrofotometer Massa
Omega-12extraction solvent concentric dan electric warmer
Lampiran 2. Gambar hasil uji KLT
Hasil uji KLT tablet methamfetamine 248LbI, 249Lb, dan 104He
Hasil uji KLT urine methamfetamine 373A, 374A, dan 375A.