10
TINJAUAN PUSTAKA
Temu mangga(Curcuma mangga)
Saat ini banyak dikembangkan produk obat herbal, yang secara alami banyak tumbuh di Indonesia. Indonesia kaya akan keanekaragaman hayati yang penting untuk digali. Kunyit /kurkuma merupakan kerabat kunyit yang sudah sejak dulu ditanam sebagai bahan ramuan obat tradisional. Kunyit merupakan jenis tanaman yang dikenal sebagai temu-temuan dan semakin memasyarakat sebagai obat tradisional.
Ada banyak jenis Curcuma sp. yang dijumpai di alam (de Padue et al. 1999), seperti temu ireng (Curcuma aerogenosa Roxb), temu purot (Curcuma aurantica v.Zijp), kunir kebo (Curcuma eurochroma Valeton), temu giring (Curcuma heyneana Valeton & v. Zijp), kunyit (Curcuma longa L), temu mangga (Curcuma mangga Valeton & v. Zijp), temu badur (Curcuma petiolata Roxb), koneng pinggang (Curcuma purpurascens Blume), temu lawak (Curcuma xanthorrhiza Roxb.) dan temu putih (Curcuma zedoaria).
Temu mangga (Curcuma mangga) merupakan salah satu dari sekian jenis kunir atau temu-temuan yang dapat dimanfaatkan sebagai bahan baku obat-obatan. Temu mangga sudah banyak dibudidayakan oleh masyarakat jawa, Malaya dan Madagaskar, penyebarannya mencapai wilayah Asia tengah, Cina, Taiwan. Menurut de Padue et al. 1999, taksonomi Curcuma mangga dapat diklasifikasikan sebagai berikut: Divis Spermatophyta, sub divisi angiospermae, kelas monokotiledon, bangsa zingiberales, suku zingiberaceae, marga curcuma dan spesies curcuma sp. (Gambar 2).
11 Temu mangga dapat tumbuh mencapai 110 cm. Rimpang induk bulat telur, permukaan luar bewarna kuning pucat dan bagian dalam kuning pucat atau kuning belerang, berbau seperti wortel, rasanya seperti mangga, tunas muda berwarna putih, rimpangnya bercabang ke segala arah. Daun terdiri atas 5-7 helai berpelepah bewarna keunguan, helai daun berwarna hijau bagian ujung berekor hingga 2,5 cm. Bunga terpisah dari batang yang berdaun, tangkai bunga berukuran 15 cm. Bunga bewarna putih separuh cuping bibir berwarna kuning.
Di Indonesia, kunyit/kurkuma termasuk dalam temu mangga. Ada 10 jenis kunyit yang banyak dipakai sebagai obat tradisional. Potensi sebagai obat dimungkinkan karena kunyit terbukti mempunyai daya antiradang, antikuman (Tonnesen et al. 1987), antirematik (Deodhar et al. 1980) serta antihepatoksik (Kiso et al. 1983), bahkan diduga mempunyai potensi antitumor serta antioksidan. Disamping itu kunyit/kurkuma banyak dipakai sebagai bumbu masak, menambah rasa, dan pewarna yang menarik pada berbagai bahan makanan. Ada 3 spesies kurkuma yang mengandung kurkumin yang telah diteliti dari 9 spesies kurkuma. Ketiga spesies tersebut adalah temu giring, temu lawak, dan kunir (Prana 1995), sedangkan 6 kurkuma lainnya relatif sedikit mengandung kurkumin, tidak berwarna tetapi mengandung flavonoid yang belum diidentifikasi lebih lanjut.
Kurkumin
Kurkumin adalah zat aktif yang terkandung di dalam tanaman jenis temu-temuan. Secara kimia, kurkuminoid merupakan turunan diferoloilmetana terdiri atas dimetoksi diferuloil-metan (kurkumin) dan monodesmetoksi diferuloil-metan (desmetosi-kurkumin). Kurkumin mempunyai rumus molekul C21H20O6 dengan
bobot molekul 368, berwarna kuning dan mudah berubah menjadi kecoklatan karena sinar matahari (Quiles et al. 2002; Sreejayan et al. 1997). Kurkumin stabil pada pH di bawah 6,5 dan akan berubah strukturnya bila diatas pH 6,5. Jenis lain kurkumin adalah bisdemetoksi-kurkumin dan desmetosi-kurkumin (Gambar 3).
Bila di lihat dari struktur kurkuminoid, gugus metoksi yang terdapat pada bis-desmetoksi-kurkumin digantikan dengan atom hidrogen. Gugus fenolik diduga berfungsi sebagai antibakterial, dan gugus fenolik tersebut menjadi dasar bahwa kurkumin juga mempunyai kemampuan dalam mengeliminasi turunan radikal
12 oksigen yang terdapat pada medium dan bertanggung jawab terhadap peroksidasi lipid di dalam sel. Gugus fenolik ini adalah esensial untuk scavenger superoksid dan keberadaan gugus orto metoksi pada molekul fenolik akan meningkatkan aktivitas kurkumin (Rao 1995;Sreejayan et al. 1997).
Keterangan:
R1 R2
Kurkumin -OCH3 -OCH3
Demetoksi-kurkumin -OCH3 H
Bis-demetoksi-kurkumin H H
Gambar 3 Struktur kurkuminoid (Cikrikci et al. 2008).
Kurkumin merupakan skavenger kuat terhadap beberapa spesies oksigen reaktif dan mempunyai kemampuan untuk melindungi lipid, hemoglobin dan mencegah degradasi oksidatif DNA. Kurkumin dikenal sebagai agen antiradang dan antikarsinogenik, menghambat phorbol 12-myriatate13-acetate (PMA), Lipopolysaccharide (LPS), tumor necrosis factor- (TNF- ) dan mentraskripsi gen tissue factor (TF) pada sel endotel manusia serta dapat berfungsi sebagai antioksidan (Pendurthi et al. 1997; Rao 1995).
Kurkumin diketahui mempunyai kemampuan untuk mencegah terjadinya peroksidasi lipid, kondisi ini merupakan awal kemajuan dari beberapa penyakit. Dari hasil penelitian secara in vitro, kurkumin 2,4-9,6 umol/l dapat menghambat oksidasi LDL manusia, menghambat peroksidasi lipid pada hemogenat hati dan otak tikus yang mengalami udema, mencegah peroksidasi lipid plasmatik, lipid plasmatik berperan penting dalam patogenesis penyakit (Quiles et al. 2002). Kurkumin juga mempunyai kemampuan dalam mencegah perluasan penyakit, seperti menurunkan kerentanan LDL terhadap oksidasi, mencegah proliferasi sel-sel otot polos pembuluh darah, mempunyai efek antitrombotik, efek hipotensif sementara dan mencegah agregasi platelet in vivo- ex vivo. Penggunaan 500 mg kurkumin pada manusia yang diberikan selama 7 hari, dapat menurunkan
H R1 HO OH R2 O O 2’ 3 3’ 4’ 5’ 4 5 6’ 6 7’ 8’ 9’ 10’ 7 8 9 10 1 2
13 peroksidasi lipid darah 35% (Sreejayan et al.1997). Kurkumin dapat mengeliminasi radikal hidroksi, radikal superoksida, nitrogen dioksid, dan nitrogen monooksida, serta mencegah turunan dari radikal superoksid (Rao 1995; Ruby & Lokesh 1995; Sreejayan et al. 1997). Hasil penelitian yang dilakukan Soesanto et al. (1992) bahwa Curcuma domestica val yang dicampur dalam ransum makanan yang diberikan pada tikus, dapat menurunkan kadar kolesterol dalam serum darah tikus dan mencegah timbulnya aterosklerosis.
Metabolisme Kurkumin
Biosintesis. Berdasarkan hasil penelitian yang telah dilakukan, mengindikasikan ada dua kemungkinan jalur untuk pembentukan formasi molekul kurkumin. Dari hasil penelitian tersebut, biosintesis kurkumin melibatkan dua unit asam sinamat yang berpasangan dengan pusat atom karbon asam mevalonat, yang dimulai dengan terbentunknya fenilalanin-sinamat. Hasil penelitian lainnya berjalan secara asimetris yang diawali dengan dua bagian molekul C9 yang
berbeda, dalam hal ini melibatkan sinamat sebagai pemula yang menghasilkan lima unit asam asetat (malonat). Siklasi terjadi pada pembentukan rantai kedua cincin aromatik kemudian berlanjut dengan proses hidroksilasi (Tonnesen 1986). Katabolisme. Katabolisme dan ekskresi kurkumin telah diteliti pada tikus. Kurkumin yang diberikan secara oral, sebagian besar diekskresikan melalui tinja sebagian lainnya melalui empedu dan dapat dimetabolisme secara cepat. Kurkumin radioaktif dengan dosis 80 mg, 99% akan diekskresikan bersama tinja yang terdiri dari 34% berupa kurkumin yang tidak berubah dan 65% berupa metabolit kurkumin. Hal ini menandakan sebagian besar kurkumin diabsorpsi oleh saluran pencernaan. Data tersebut membuktikan bahwa kurkumin yang diberikan secara oral pada tikus akan diabsorbsi dan dimetabolisasi, dengan jalur eliminasi utamanya melalui empedu. Metabolit utamanya adalah glukoronida tetrahidro-kurkumin (THC), heksahidro-tetrahidro-kurkumin, dan sebagian kecil berupa asam dihidroferulat (Pan et al. 2000; Rao et al. 1995).
14
Metabolisme Lipoprotein
Lipoprotein utama yang berpotensi menyebabkan aterosklerosis adalah Low Density lipoprotein (LDL). Senyawa LDL adalah kompleks makromolekul yang intinya mengandung lipid non polar terutama ester kolesterol, lapisan permukaan LDL terdiri atas kolesterol yang tidak teresterifikasikan, fosfolipid dan apo B-100. Asam lemak yang terikat pada ester kolesterol sebagian merupakan asam lemak tak jenuh berantai bamyak polyunsurated fat acid (PUFA). Asam lemak inilah yang sangat peka terhadap oksidasi karena ikatan rangkapnya.
Kolesterol (C27H45OH) adalah lipid yang dapat dibedakan dari trigliserida
atau fosfolipidnya karena tidak mengandung gliserol, hanya terdiri atas inti steroid yang mengandung gugus hidroksil. Sebagai komponen membran plasma, kolesterol berperan penting dalam kehidupan sel (Brown & Goldstein, 1985). Struktur kolesterol seperti Gambar 4. Kolesterol yang kadarnya berlebihan di dalam tubuh dapat menyebabkan penyakit aterosklerosis.
Gambar 4 Struktur kolesterol.
Pada manusia sekitar 90%, sintesis kolesterol berlangsung di dalam hati, sedangkan sebagian kecil disintesis di usus. Hampir 75% kolesterol yang terbentuk di dalam hati digunakan untuk membentuk empedu. Kecepatan sintesis kolesterol oleh tubuh sendiri (hati dan usus) sangat dipengaruhi oleh banyaknya kolesterol yang diabsorbsi dari makanan. Kolesterol yang disintesis oleh hati dan usus dan akan distribusi ke seluruh sel yang diangkut oleh lipoprotein.
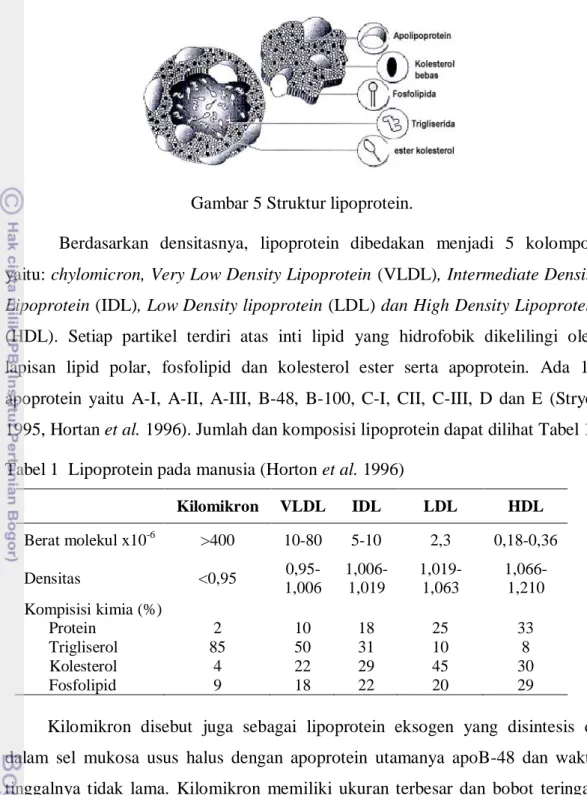
Inti lipoprotein terdiri atas lipid-lipid netral, termasuk triasilgliserol dan ester kolesterol, yang dibungkus oleh fosfolipid dan apolipoprotein maupun kolesterol yang tertanam. Struktur lipoprotein disajikan pada Gambar 5.
OH CH3 H3C CH3 CH3 H3C
15 Gambar 5 Struktur lipoprotein.
Berdasarkan densitasnya, lipoprotein dibedakan menjadi 5 kolompok yaitu: chylomicron, Very Low Density Lipoprotein (VLDL), Intermediate Density Lipoprotein (IDL), Low Density lipoprotein (LDL) dan High Density Lipoprotein (HDL). Setiap partikel terdiri atas inti lipid yang hidrofobik dikelilingi oleh lapisan lipid polar, fosfolipid dan kolesterol ester serta apoprotein. Ada 10 apoprotein yaitu A-I, A-II, A-III, B-48, B-100, C-I, CII, C-III, D dan E (Stryer 1995, Hortan et al. 1996). Jumlah dan komposisi lipoprotein dapat dilihat Tabel 1. Tabel 1 Lipoprotein pada manusia (Horton et al. 1996)
Kilomikron VLDL IDL LDL HDL Berat molekul x10-6 >400 10-80 5-10 2,3 0,18-0,36 Densitas <0,95 0,95-1,006 1,006-1,019 1,019-1,063 1,066- 1,210 Kompisisi kimia (%) Protein 2 10 18 25 33 Trigliserol 85 50 31 10 8 Kolesterol 4 22 29 45 30 Fosfolipid 9 18 22 20 29
Kilomikron disebut juga sebagai lipoprotein eksogen yang disintesis di dalam sel mukosa usus halus dengan apoprotein utamanya apoB-48 dan waktu tinggalnya tidak lama. Kilomikron memiliki ukuran terbesar dan bobot teringan diantara lipoprotein. Molekul VLDL dikenal sebagai lipoprotein endogen disintesis oleh hati dan usus, apoprotein utamanya apoB-100 dan ApoE. Kilomikron dan VLDL konsentrasinya lebih tinggi di dalam lipid, tetapi rendah untuk protein. Molekul IDL merupakan hasil katabolisme dari VLDL dengan bantuan enzim lipoprotein lipase. Hasil katabolisme selanjutnya adalah LDL, lipoprotein ini tidak mempunyai apoE-100 dan sering disebut sebagai kolesterol yang jahat yang dapat menyebabkan kejadian penyakit aterosklerosis dan penyakit
16 jantung koroner. Molekul HDL adalah lipoprotein yang bertugas mengembalikan kolesterol ke hati, dan dikenal sebagai kolesterol baik karena membantu mencegah terjadinya aterosklerosis dan penyakit jantung koroner (Strayer 1995).
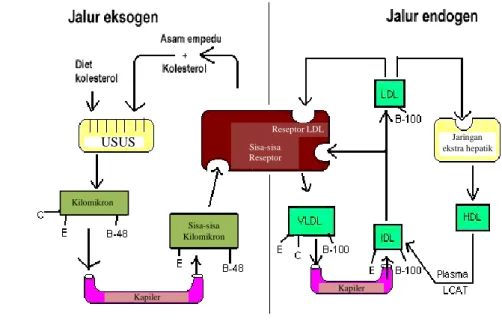
Sistem transport lipoprotein di dalam tubuh dibagi atas 2, yaitu jalur eksogen dan jalur endogen (Gambar 6). Jalur eksogen mengatur pengangkutan lipid yang berasal dari makanan. Jalur endogen mengatur transportasi kolesterol yang disintesis di hati.
Gambar 6 Metabolisme lipoprotein.
Jalur eksogen diawali dengan sekresi kilomikron yang banyak mengandung trigliserida ke pembuluh getah bening dan aliran darah. Dalam perjalanannya kilomikron akan menyusut karena trigliserida yang terdapat pada kilomikron mengalami hidrolisis oleh enzim lipoprotein lipase menjadi asam lemak bebas. Asam lemak bebas dan monogliserida pada kilomikron akan disimpan di dalam jaringan adiposa. Kilomikron yang menyusut dikenal sebagai chylomicron remnants (sisa-sisa kilomikron).
Jalur endogen diawali dengan sekresi partikel VLDL oleh hati ke sirkulasi darah. Partikel VLDL akan berinteraksi dengan lipoprotein lipase pada pembuluh kapiler. Trigliserida pada VLDL mengalami hidrolisis lipoprotein lipase, sehingga membentuk partikel IDL. Kelebihan fosfolipid dan kolesterol pada IDL akan ditranfer ke HDL. Partikel HDL akan berinteraksi dengan enzim lesitin kolesterol asiltransferase (LCAT) yang akan mengesterifikasi kelebihan kolesterol pada
USUS Kilomikron Sisa-sisa Kilomikron Sisa-sisa Reseptor Reseptor LDL Jaringan ekstra hepatik Kapiler Kapiler
17 HDL selanjutnya dipindahkan kembali oleh enzim lipoprotein lipase membentuk LDL. Dalam degradasi ini hampir semua trigliserida dibebaskan dan yang tertinggal pada LDL adalah ester kolesterol dan apoB-100 pada permukaan.
Partikel LDL mengantarkan kolesterol ke sel-sel enterohepatik dan hati. Partikel LDL berikatan dengan reseptor LDL pada membran plasma, kemudian masuk ke lisosom dan dilisosom apo-B didegradasi menjadi asam amino. Sedangkan ester kolesterol dihidrolisis oleh enzim lipase menjadi kolesterol bebas yang digunakan untuk kepentingan sel. Kelebihan kolesterol di dalam sel akan disekresikan kembali ke plasma dan diserap oleh HDL, dengan bantuan enzim LCAT kolesterol ester dipindahkan kembali ke LDL dan seterusnya. Kolesterol yang diserap oleh hati akan dibawa ke empedu dan dimetabolisme oleh asam empedu. Asam empedu dan sebagian kolesterol ini disekresikan oleh hati dan diabsorpsi kembali oleh usus lalu diangkut kembali ke hati dan seterusnya membentuk sirkulasi enterohepatik. Sebagian kecil kolestrol dibuang melalui tinja (Horton et al. 1996).
Penyerapan sisa-sisa kilomikron oleh hati dilakukan secara endositosis menggunakan reseptor khusus (receptor-mediated endocytosis). Partikel LDL akan berikatan secara spesifik dengan reseptor yang ada di daerah membran plasma yang disebut coated pits (lekuk bermantel) dan disini LDL akan mengalami internalisasi membentuk coated vesicle. Pada pH 7,0, mantel terlepas kemudian vesikel berdifusi dengan vesikel endosom (pH 5). Partikel LDL terpisah dari reseptor dan bergabung dengan lisosom di sel hati menghasilkan lisosom kedua. Sedangkan reseptor yang terpisah akan mengalami siklus ulang yang selanjutnya menangkap LDL kembali (Cotran et al. 1989; Hortan et al. 1996; Voet & Voet 1995). Setelah terjadi absorpsi, VLDL yang dihasilkan hati dari asam lemak bebas, merupakan sumber utama trigliserida plasma. Molekul VLDL masuk ke dalam sirkulasi darah lalu mengangkut kolesterol dan trigliserida ke jaringan adiposa dan otot. Dalam sirkulasi, VLDL akan mengalami hidrolis menjadi IDL dan LDL Kira-kira 50 % IDL akan ditangkap oleh hati, sisa IDL kemudian diubah menjadi LDL oleh sel di dalam tubuh dan hepatosit seperti sel adrenal, fibroblas, sel otot polos, sel limfoid, dan sel endotel melalui reseptor secara endoditosis. Jadi LDL berfungsi mengangkut kolesterol endogen dan
18 eksogen ke jaringan, sedangkan HDL berfungsi mengangkut kolesterol dari jaringan perifer ke hati. Di dalam hati kolesterol dapat diubah menjadi asam empedu kemudian disekresikan ke dalam kantung empedu menuju usus halus dan bekerja sebagai pengemulsi lemak serta vitamin larut lemak. Di dalam ilium, selanjutnya kira-kira 2 % dari asam empedu yang dieksresikan dalam usus akan dikeluarkan bersama-sama tinja dan sisanya direabsorpsi kembali melalui sirkulasi enterohepatik (Hortan et al. 1996; Mayes 1984).
Lesi awal aterosklerosis pada pembuluh darah terjadi akibat infiltrasi senyawa lemak pada sirkulasi darah. Dalam perjalanannya menembus dinding pembuluh darah, kemudian berinfiltrasi yang menyebabkan peradangan dan terjadi proliferasi serabut-serabut otot polos dinding pembuluh darah. Kondisi ini juga didukung oleh adanya faktor pertumbuhan dan sel-sel busa. Sel otot polos sendiri berperan penting dalam mensintesis matrik protein dan proteoglikan. Teori ini didasarkan pada kenyataan adanya peningkatan kejadian penyakit pembuluh darah pada individu yang memiliki kadar lemak dan kolesterol darah yang tinggi, jika dibandingkan dengan yang normal (Getz 2005; Ross 1991).
Pada Macaca fascicularis, yang diberi pakan diet kolesterol tinggi, akan terjadi hiperkolesterolemia moderat dengan gejala yang timbul sama seperti yang terjadi pada hamster dan manusia, akan tetapi sangat berbeda dengan tikus. Adanya diet kolesterol dan total kolesterol ester yang ada di hati, akan menyebabkan meningkatnya tekanan terhadap sintesis sterol hepatik, penurunan aktivitas reseptor hepar dan meningkatnya produksi LDL. Tidak hanya terjadi peningkatan konsentrasi LDL, tetapi ukuran partikel LDL juga meningkat yang disebabkan oleh akumulasi molekul oleat kolesterol di dalam partikel inti akibat kerja enzim hepatik acyl-coenzyme A Cholestrrol Acyltransferase (ACAT). Enzim ini merespon esterifikasi kolesterol sebagai oleat Ko-A. Oleat kolesteril hepatik juga berkorelasi dengan kolesterol oleat-LDL plasma, hal ini berhubungan erat dengan kejadian aterosklerosis arteria koronaria. Partikel LDL yang kaya dengan apoE bersifat aterogenik dan mungkin berkorelasi terhadap peningkatan kemampuan partikel tersebut mengikat proteoglikan (PG) yang terdapat pada dinding arteri, yang pada akhirnya akan dimetabolisme oleh makrofag (Sreejayan & Rao. 1997).
19
Aterosklerosis
Istilah aterosklerosis digunakan untuk lesi aterosklerotik yang disertai oleh perubahan degenerasi lemak. Arti kata aterosklerosis adalah pengerasan dinding arteri sebagai akibat perubahan kronis yang terjadi pada arteri. Perubahan kronis arteri disebabkan oleh hilangnya elastisitas arteri, menyempitnya lumen karena perubahan proliferatif dan degeneratif pada tunika intima dan media, dan proses radang.
Aterosklerosis merupakan kelainan degeneratif pada pembuluh darah besar dan sedang yang dicirikan oleh penebalan pembuluh darah (Munro & Cotrans 1988). Penebalan pembuluh darah karena adanya akumulasi lipid dan elemen-elemen fibrosa pada bagian ateri media maupun besar, sehingga pada akhirnya dapat terjadi obstruksi pada lumen arteri. Aterosklerosis, pada umumnya dapat menyerang arteri koronaria, aorta, iliaka, femoral dan arteri serebralis (Ross & Glomset 1973). Penebalan pembuluh darah ini ditandai dengan adanya sel busa, yaitu sel makrofag yang berisi kolesterol dan kolesterol ester. Adapun penyebab terbentuknya sel busa antara lain disebabkan oleh makrofag yang secara berlebihan mengambil LDL yang teroksidasi. Selain kolesterol atau kolesterol ester, pada lesi aterosklerosis terdapat juga protein, karbohidrat, dan komponen seluler termasuk sel otot polos, makrofag, dan limfosit (Kaplan & Aviram, 2001). Menurut Hansson (2009), aterosklerosis merupakan penyakit inflamasi, dan proses aterosklerosis dimulai saat LDL terakumulasi di intima sehingga mengaktifkan endotel, meningkatkan pengambilan monosit dan sel T. Monosit berdeferensiasi membentuk makrofag, mengubah lipoprotein akhirnya manjdi sel busa. Sedangkan sel T pada lesi akan mengenali antigen lokal yang berkontribusi pada pebentukan plak.
Perubahan awal terjadinya aterosklerosis melibatkan bagian dalam permbuluh darah dan kejadiannya dimulai sejak anak-anak yang ditandai dengan perkembangan garit-garit lemak pada pembuluh darah (Rackley 2006). Garit lemak bila berlanjut akan membentuk plak lemak yang dapat diperiksa secara biokimiawi dan secara mikroskopis (Small 1988; Stary 1990). Garit lemak dapat ditemukan pada pembuluh arteri manusia semenjak usia belasan tahun. Satu studi autopsi terhadap 2.876 laki-laki dan perempuan yang berumur 15–34 tahun
20 mempunyai garit lemak pada aorta (Rackley 2007). Garit lemak merupakan prekusor plak aterosklerosis tahapan lebih lanjut, dan ternyata faktor genetik merupakan faktor utama yang mempengaruhi percepatan garit lemak menjadi plak aterosklerosis (McGill 1968).
Patogenesis Aterosklerosis
Berdasarkan penelitian dan teori proses awal terjadinya aterosklerosis, terdapat beberapa hipotesis yang mendasari aterosklerosis. Beberapa hipotesis tersebut adalah hipotesis infiltrasi lipid (McGill 1968), hipotesis respon terhadap kelukaan sel endotel (Ross 1991), hipotesis gabungan antara keduanya (Steinberg 1993), dan hipotesis respon imun (Hansson, 2009).
Hipotesis Infiltrasi Lipid. Konsentrasi LDL yang tinggi dalam plasma atau hiperkolesterolemia merupakan faktor risiko penyebab terjadinya aterosklerosis. Hiperkolesterolemia kronis dapat menyebabkan lesi patologi awal yang ditandai oleh adanya kristal kolesterol yang berbentuk tipis dan tajam dalam jaringan (Fuller & Jialal 1994). Menurut teori yang dikemukakan oleh Ross (1991), lesi awal pada dinding pembuluh darah akan terjadi akibat infiltrasi senyawa lemak dari sirkulasi darah yang menembus dinding pembuluh darah. Hal akan mengiritasi dan mengakibatkan peradangan serta proliferasi serabut-serabut otot polos dinding pembuluh darah.
Kadar LDL yang tinggi memungkinkan LDL dapat menembus lumen pada dinding pembuluh darah masuk ke bagian intima. Pada bagian intima ini LDL akan mengalami oksidasi. LDL yang teroksidasi akan menyebabkan terjadinya peningkatan adhesi monosit ke endotel, yang diikuti dengan kemotaksis ke dalam jaringan subendotel (intima). Di intima, monosit akan berdeferensiasi menjadi makrofag. Perubahan monosit ini dipicu oleh LDL teroksidasi. Reseptor LDL tidak lagi dikenali oleh LDL teroksidasi tetapi akan dikenali oleh reseptor
skavenger dari makrofag yang menyebabkan terbentuknya sel-sel busa. Kondisi ini akan merangsang terekspresinya sejumlah gen sitokin dan faktor pertumbuhan yang mengakibatkan terjadinya proliferasi sel otot polos di bagian intima. Akibatnya permukaan dinding pembuluh darah dibagian lumen akan
21 menggelembung akibat terjadinya penimbunan plak pada bagian media (Linder 1985; Stocker & Keaney 2004).
Peneningkatan konsentrasi kolesterol tidak selalu mengakibatkan terjadinya aterosklerosis. Hal ini disebabkan dalam kondisi normal, 60-64% LDL didegradasi melalui umpan balik reseptor afinitas tinggi yang diatur melalui mekanisme umpan balik oleh peningkatan kolesterol. Sebanyak ± 35% sisanya LDL akan didegradasi melalui jalur reseptor alternatif spesifik, yaitu afinitas reseptor scavenger, reseptor tersebut hanya mampu mengenali LDL yang mengalami perubahan secara kimiawi (Weisgraber et al.1992; Goldstein & Brown 1992; Keys 1996).
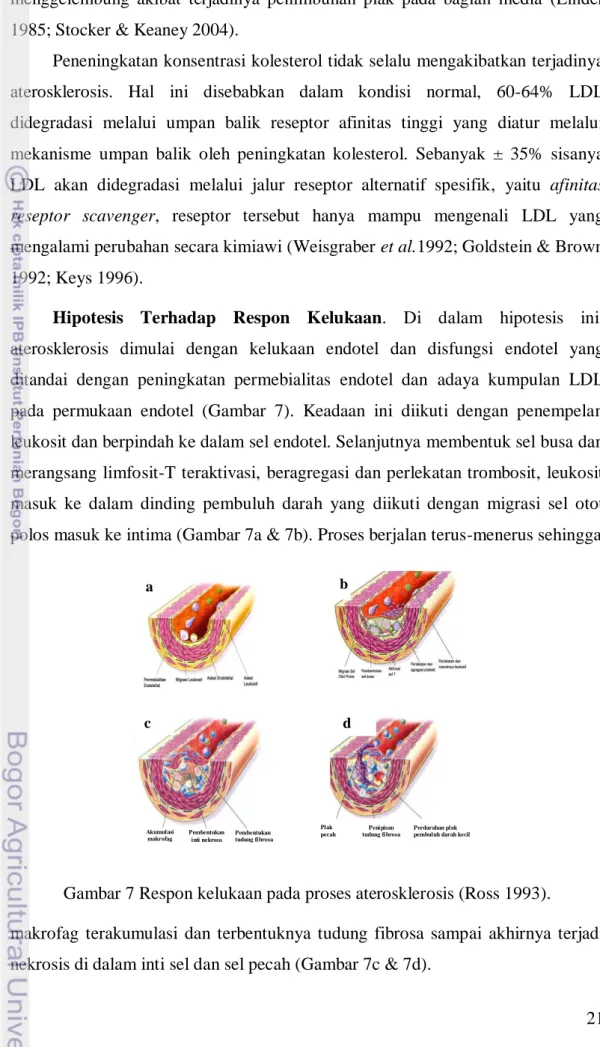
Hipotesis Terhadap Respon Kelukaan. Di dalam hipotesis ini, aterosklerosis dimulai dengan kelukaan endotel dan disfungsi endotel yang ditandai dengan peningkatan permebialitas endotel dan adaya kumpulan LDL pada permukaan endotel (Gambar 7). Keadaan ini diikuti dengan penempelan leukosit dan berpindah ke dalam sel endotel. Selanjutnya membentuk sel busa dan merangsang limfosit-T teraktivasi, beragregasi dan perlekatan trombosit, leukosit masuk ke dalam dinding pembuluh darah yang diikuti dengan migrasi sel otot polos masuk ke intima (Gambar 7a & 7b). Proses berjalan terus-menerus sehingga
Gambar 7 Respon kelukaan pada proses aterosklerosis (Ross 1993).
makrofag terakumulasi dan terbentuknya tudung fibrosa sampai akhirnya terjadi nekrosis di dalam inti sel dan sel pecah (Gambar 7c & 7d).
a b c Akumulasi makrofag Pembentukan inti nekrosa Pembentukan tudung fibrosa d Plak pecah Penipisan tudung fibrosa Perdarahan plak pembuluh darah kecil
22 Lesi yang merupakan cikal bakal pembentukan aterosklerosis diawali dengan menurunnya fungsi sel endotel (disfungsi), atau bahkan terkelupasnya sel endotel. Traub & Berk (1998) menyatakan disfungsi endotel dapat disebabkan oleh berbagai faktor, seperti kecepatan aliran darah yang bertekanan tinggi, kimiawi, imunologik maupun infeksi virus. Disfungsi endotel menyebabkan perubahan permukaan membran sehingga terjadi perlekatan trombosit pada membran. Perlekatan trombosit akan melepaskan platelet derived growth factor (PDGF), yang merangsang sel-sel otot polos untuk bermigrasi dan berproliferasi pada lapisan subendotel. Kolesterol yang teroksidasi bersifat sangat toksik bagi sel otot polos (in vitro) dan merupakan agen aterogenik (in vivo) (Stocker & Keaney 2004; Traub & Berk 1998).
Disfungsi endotel dan hilangnya sel endotel merupakan awal pembentukan plak ateroma yang ditandai oleh meningkatnya perlekatan (adhesi) monosit pada sel endotel arteri (Packard & Libby 2007). Adhesi leukosit pada sel dinding endotel merupakan mekanisme utama yang merespon pembentukan radikal bebas oksigen (ROS), yang akhirnya akan menghasilkan oksidan sitotoksik dan mediator peradangan yang mengaktifkan sistem komplemen. Oksidan yang dihasilkan akan menyebabkan kerusakan jaringan (Caterina et al. 2000; Hoorn et al. 2003; Joris et al.1983)
Hipotesis Modifikasi Oksidatif (Gabungan). Menurut teori yang dikemukan oleh Steinberg (1993), lesi aterosklerotik diawali oleh teroksidasinya LDL sehingga mengakibatkan endotel mengekspresikan perlekatan monosit dan menghasilkan monocyte chemotatic protein (MCP), macrophage colony stimulating factor (M-CSF). Induksi tersebut mengakibatkan monosit berubah menjadi makrofag dan menempel pada endotel. Selanjutnya makrofag akan memfagositose LDL teroksidasi, kemudian terakumulasi pada dinding pembuluh darah membentuk sel busa dan berakhir dengan terbentuknya lesi awal yang dikenal sebagai lempeng kolesterol.
Kerusakan lapisan endotel menyebabkan timbulnya efek sitotoksik dari lipid peroksida diakibatkan oleh reaksi oksidasi lipid, sehingga infiltrasi lipid menjadi berlebihan. Proses oksidasi diduga dimulai ketika oksigen reaktif mengambil atom hidrogen dari asam lemak tidak jenuh yang ada di dalam partikel LDL sehingga
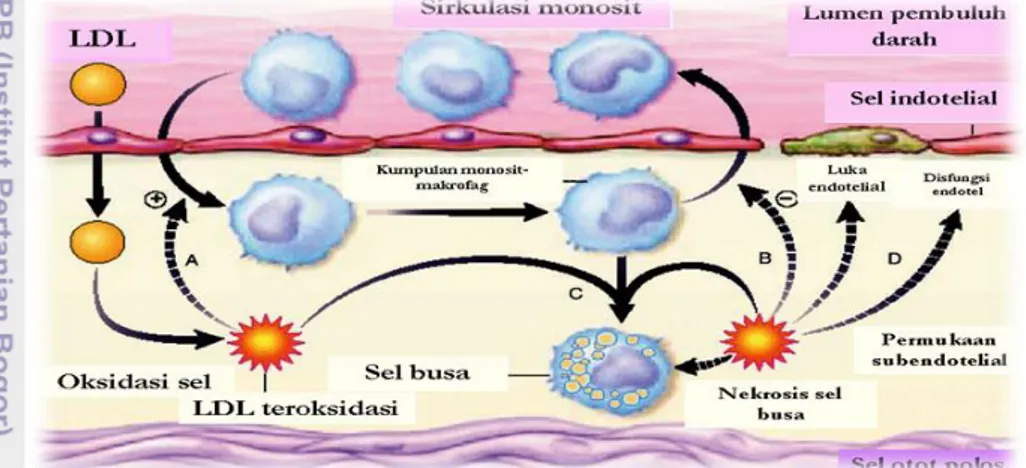
23 terbentuk lipid peroksida dan radikal alkoksi yang selanjutnya akan menginisiasi oksidasi asam lemak di sekitarnya. Dalam situasi jumlah antioksidan yang ada di dalam partikel LDL tidak cukup untuk mengeliminasi lipid peroksida yang terbentuk, maka akan terjadi propagasi lipid peroksida. Sehingga terbentuk aldehid, keton dan produk lainnya yang reaktif, serta berikatan dengan residu lisin dalam apolipoprotein B-100. Partikel LDL yang menempel pada permukaan subendotel merupakan target sasaran terjadinya modifikasi oksidatif dengan penumpukan sel otot polos, sel endotel dan makrofag pada pembuluh darah. Pada Gambar 8, terlihat jelas bagaimana LDL dapat masuk menembus dinding permukaan pembuluh darah.
Gambar 8 Patogenesis aterosklerosis (A, LDL teroksidasi menstimuli monosit; B, mencegah agresi monosit; C, pembentuk sel busa; D, oksidasi LDL menghasilkan disfungsi endotel dan perlukaan; E, sel-sel busa penyebab sel menjadi nekrosa dan terakumulasinya LDL teroksidasi) (Stocker & Keaney 2004).
Perubahan metabolit yang terbentuk akibat interaksi lipid-lisin akan mengubah muatan listrik LDL sehingga mengakibatkan terbentuknya epitop baru yang hanya dikenal oleh reseptor pemangsa (scavenger) pada makrofag. Semua reaksi di atas mendorong terjadinya perubahan struktur LDL dan pembentukan senyawa baru yang beberapa diantaranya cukup polar untuk lepas dari partikel LDL dan memiliki pengaruh biologis yang negatif, termasuk diantaranya sifat aterogenik (Steinberg 1993; Riemersma 1994; Schwenke 1998).
Hipotesis respon imun. Konsentrasi tinggi lipoprotein di dalam darah dapat meningkatkan permebialitas endotel yang akan memicu proses radang.
24 Terbentuknya radang pada pembuluh darah, menyebabkan sel mengeluarkan sitokina ke permukaan pembuluh darah sehingga menstimuli pembentukan molekul adhesi, protease maupun mediator terlarut lainya yang dapat masuk ke sirkulasi darah (Packard & Libby, 2008; Hansson 2009). Hansson (2009), menyatakan partikel LDL teroksidasi dapat merangsang sel limfosit T pada permukaan pembuluh darah. Peradangan akan mengakibatkan monosit masuk ke intima pembuluh darah yang akhirnya berubah menjadi makrofag. Pada waktu bersamaan sel limfost T masuk ke dalam pembuluh darah dan bergabung dengan makrofag
Gambar 9 Keberadaan sel antigen pada plak aterosklerosis dan sel T pada permukaan endotel menandakan dimulainya kejadian imunologik. Sitokina, khemokina, faktor pertumbuhan dan enzim hidrolitik disekresikan oleh sel sebagai respon reaksi radang. Plak akhirnya berkembang menjadi radang, ruptur atau tetap stabil sebagai plak (Robertson & Hansson, 2005).
Rangsangan awal pada pembentukan lesi aterosklerosis menyebabkan perubahan dan intergritas fungsional endotel, sehingga memudahkan lipoprotein plasma masuk ke subendotel. Hiperkolesterolemia merupakan salah satu agen penyebab teraktivasinya sel endotel pembuluh darah. Terjadinya infiltrasi dan retensi LDL di dalam intima akan menginisiasi respon radang terhadap dinding pembuluh darah. Modifikasi LDL oleh oksidasi maupun reaksi enzimatis pada intima pembuluh darah, akan melepaskan fosfolipid yang dapat mengaktifkan sel-sel endotel dalam mengekspresikan molekul adhesi (Hansson 2005; Libby 2002). Partikel LDL termodifikasi kemudian ditangkap reseptor makrofag scavenger tanpa pengaturan, dan pada akhirnya terbentuklah sel-sel busa. Keadaan ini akan
Infritasi Sel Monosit Sel-T Sel-T Sel Busa Makrofag, DC
Sel Adhesi Pengambilan LDL
Pembuluh Darah Pertumbuhan Plak peradangan dan Perlukaan atau Antigen permukaan Sel Endotel Peradangan dan reaktif imun
25 mensintesis faktor pertumbuhan dan sitokina sehingga terjadi proliferasi sel otot polos, migrasi dan kematian sel (Caterina 2000; Siekmeier 2007; Hansson 2009).
Pada awal perkembangan aterotrombosis ketika terjadi radang, molekul VCAM- 1 terekspresikan sehingga meningkatkan pengambilan monosit dan sel limfosit T ke endotel yang mengalami luka Kondisi ini menyebab leukosit melepaskan monocyte chemo-attractant protein-1(MCP-1) dan pengambilan kembali leukosit. Leukosit di dalam media pembuluh darah teraktivasi sehingga menyebabkan terjadinya proliferasi sel-sel otot polos. Respon ini memberikan tanda pada awal kejadian plak, adhesi monosit ke endotel lalu menembus lapisan bawah membran sel sebagai akibat dari aktivitas enzim. Matrix metalopoteinase (MMP) setempat pertama kali teraktivasi, lalu mendegradasi matrik jaringan konektivus. Makrofag akan melepaskan sitokina dan bermigrasi ke permukaan endotel pada bagian dalam media pembuluh darah. Proses ini selanjutnya akan meningkatkan pelepasan monocyte stimulating factor (M-CSF) setempat dan menyebabkan monosit berproliferasi (Crowther 2005). Pengaktifan monosit setempat menyebabkan sitokina merangsang perkembangan aterosklerosis dan oksidasi LDL (Hansson 2009; Libby 2002; Packard & Libby 2008).
Setiap kali terjadi inisiasi aterosklerosis, mediator-mediator radang diekpresikan oleh sel-sel otot polos ke dalam plak aterosklerosis, yang meliputi interleukin-1B (IL-B), tumor necrosis factor (TNFα-β), 6, M-CSF, MCP-1,
IL-18, dan CD-40L. Efek yang ditimbulkan oleh mediator dapat bermacam-macam, seperti mitogenesis, proliferasi matrik intraseluler, angiogenesis dan perkembangan sel busa. Molekul M-CSF merangsang reseptor scavenger pada permukaan sel makrofag, sehingga pengambilan LDL teroksidasi meningkat, yang pada akhirnya membentuk sel-sel busa busa (Crowther 2005; Linton & Fazio 2003).
Proses oksidasi lipoprotein merupakan suatu mekanisme pembentukan abnormal dalam dinding pembuluh darah (Crowther 2005). Hal ini disebabkan adanya proses oksidasi asam lemak jenuh majemuk dari lipoprotein dalam bentuk LDL dan VLDL, yang melintasi sel endotel dan terperangkap dilingkungan ekstraseluler intima. Telah diuraikan sebelumnya, bahwa partikel LDL teroksidasi merupakan salah satu penyebab terbentuknya plak ateroma. Akibat proses
26 oksidasi yang terjadi di dalam tubuh, maka radikal bebas yang ada di dalam tubuh (RO٭, ROO٭ dan OH٭) akan mengoksidasi lipid lebih lanjut menghasilkan produk oksidasi lipid seperti malonaldehid.
Molekul LDL teroksidasi dapat dikenali oleh sistem imun tubuh sebagai senyawa asing. Oleh sebab itu tubuh akan nerespon dengan cara: partikel LDL bersama sama monosit berinfiltrasi ke intima, dan menghambat pergerakan makrofag; makrofag mengambil LDL teroksidasi melalui reseptor scavenger yang akhirnya membentuk sel-sel busa; LDL teroksidasi juga merusak endotel dan meningkatkan proliferasi monosit, sel endotel dan otot polos (Steinberg et al. 1989; Steinberg et al. 1997). Respon ini makin lama makin meningkat dan semangkin menebal hingga mempersempit arteri yang pada akhirnya memperberat kondisi aterosklerosis (Stocker & Keaney 2004)
Sel imun limfosit T dapat menyesuaikan diri, berperan penting dalam pengaturan aterogenesis termasuk lesi aterosklerosis dalam merespon monokina yang diinduksi oleh interferon-γ (IFN-γ) dan IFN. Sub tipe CD4+ sel T, akan mengenali antigen yang dibawa oleh Major histocompatibility complex clas II (MHC-II) merupakan prediposisi terjadinya lesi (Packard & Libby 2008). Lesi aterosklerosis yang berisi CD4+ sel T sebagai antigen reaktif dalam mengikat LDL teroksidasi yang telah di klon dari lesi manusia. Pengaktifan CD8+ sel T pada mencit yang apoE dihilangkan, ternyata dapat menimbulkan kematian dinding arteri dan mempercepat aterosklerosis (Hansson 2009; Linton & Fazio 2003; Packard & Libby 2008) Ada dua tipe sel Th yaitu Th1 dan Th2, tipe Th1
mengaktifkan respon makrofag dan menginisiasi hipersensitivitas terhadap patogen intraseluler. Sedangkan tipe Th2 berespon pada alergi. Aterosklerosis
yang mengandung sitokin akan meningkatkan respon T helper-1 (Th1) sehingga
sel T teraktivasi untuk berdeferensiasi menjadi sel-sel Th1 efektor. Sel efektor
akan memproduksi macrophage activating colony interferon-γ. Interferon γ meningkatkan efisiensi penyajian antigen dan sintesis sitokin peradangan TNF dan IL-1 (Caterina et al, 2000; Hansson 2009; Linton & Fazio 2003; Packard & Libby 2008).
Makrofag yang berinteraksi dengan limfosit sel T dapat langsng beradaptasi (Gamabr 10), dan mensekresikan kemokin; sitokin proinflamasi (IL-1, IL-6 dan
27 TNF-α); oksigen reaktif dan spesies nitrogen: penyebab LDL teroksidasi dan kerusakan sel; ekspresi faktor jaringan (trombogenositas); menangkap LDL teroksidasi (pembentuk sel busa); dan mensekresikan protease untuk degradasi sel otot (Robetson & Hansson 2006; Hansson 2009). Aktivitas biologis dari TNF-α akan menginduksi sel-sel endotel dari gen yang mengatur berinteraksinya sel endotel dengan leukosit, seperti molekul adhesi vascular celuler adhesion molecule-1 (VCAM-1), intercellular adhesion molecule -1 (ICAM-1, P-selektin, faktor jaringan, sitokina peradangan dan kemokin (Inoue et al. 2006). Molekul intracellular adhesion molecule-1 (ICAM-1) dapat menarik netrofil dan limfosit. Sedangkan endothelium leukocyte adhesion molecule-1 (ELAM-1) meningkatkan interaksi antara monosit dan limfosit T dan vascular cell adhesion molecule-1 (VCAM-1) meningkatkan ikatan pada permukaan leukosit antara monosit dan limfosit
Gambar 10 Kaskade kejadian aterogenesis diawali oleh makrofag yang berinteraksi dengan limfosit sel T teraktivasi dan makrofag (Robertson & Hansson, 2005).
Secara in vitro, proses oksidasi LDL dapat diinisiasi melalui inkubasi dengan logam tembaga (Cu) dan atau besi (Fe) yang akan memecah lipid hidroperoksida dan menginisiasi reaksi propagasi. Umumnya LDL yang dioksidasi oleh ion logam merupakan zat kemotatik bagi monosit dan limfosit T. Sedangkan cara LDL teroksidasi dapat terjadi in vivo sampai saat ini belum diketahui secara pasti. Hal ini terjadi karena perubahan kimiawi ketika LDL mengalami oksidasi kompleks dan prosesnya sebagian besar terjadi di daerah
Pengambilan LDL terosidaksi pembentukan sel busa
Ekspresi factor jaringan Trombogenesitas
Sekresi oksigen reaktif dan spesies nitrogen : LDL teroksidasi, kerusakan sel
Sekresi properadangan Sitokina (IL-1, IL-6, TNF-(α)
Sekresi protease Degradasi ECM, pembentukan lesi dan pecahnya plak
Aktivasi Aktivasi kemokin Molekul Adhesi Protease Reseptor skavenger Sekresi kemokin migrasi sel Makrofag
28 subendotel pembuluh darah di luar sirkulasi sehingga evaluasi oksidasi LDL in vivo masih perlu diteliti secara mendalam.
Faktor-faktor yang telah dilaporkan mempunyai kemampuan mempengaruhi oksidasi LDL in vivo antara lain (1) adanya oksigen yang mendorong terbentuknya radikal bebas seperti asap rokok, tekanan darah tinggi, senyawa kimia dan obat-obat tertentu, (2) jumlah LDL yang memasuki jaringan subendotel sangat tergantung pada konsentrasi plasma LDL dan derajat kerusakan jaringan endotel, (3) faktor yang ada di dalam partikel LDL, seperti: kandungan asam lemak tidak jenuh pada partikel LDL menjadi substrat dalam proses peroksidasi lipid dan kandungan senyawa antioksidan endogen, dan (4) faktor yang ada di luar partikel LDL, seperti aktivitas berbagai pro-oksidan selular, konsentrasi senyawa pro-oksidan dan konsentrasi berbagai senyawa antioksidan di dalam plasma dan cairan ekstraselular lainnya (Wuryastuti 2000; Morrow 1995; Reaven & Witztun 1998).
Protein yang terdapat di dalam daging bila dikonsumsi dengan tidak baik dan hanya sedikit mikronutrien, dapat menimbulkan aterosklerosis karena terjadi akumulasi homosistein. Homosistein merupakan racun yang sangat kuat bagi sel otot polos dan sel endotel arteri. Homosistein adalah suatu asam amino yang mengandung gugus sulhifdril, secara in vitro mempunyai kemampuan dalam menghasilkan dan mengakumulasikan kolagen pada sel-sel otot polos pembuluh darah, tetapi prosesnya belum diketahui dengan jelas (Leaf & Weber 1989).
Homosistein merupakan senyawa antara yang terbentuk pada system metabolisme dan terdapat dalam beberapa bentuk di dalam plasma. Bebarapa hasil penelitian terhadap peningkatan homosistein dalam darah (hiperhomosisteinemia), menyatkan bahwa hiperhomosisteinemia merupakan salah satu faktor risiko independen untuk terjadinya infak miokard, stroke dan penyakit pembuluh darah perifer. Hiperhomosisteinemia moderat umumnya ditentukan oleh kadar homosistein 15-16 umol/ml dan 40-50% merupakan penderita dengan komplikasi vaskular (Verhoef et al. 2000). Kadar homosistein meningkat seiring dengan menurunnya jumlah asam folat, vitamin B12 dan B6. Vitamin ini merupakan substrat pada metabolism metionin dan homosistein.
29 Plak Ateroma
Ateroma adalah manifestasi aterosklerosis yang berarti pengerasan dinding arteri. Sklerosis berasal dari kata Yunani yang berarti keras. Perkembangan aterosklerosis diawali dengan perubahan di dalam endotel. Perubahan dimulai dengan terbentuknya plak ateroma, yang dicirikan dengan adanya penimbunan kolesterol dan asam lemak, kalsium, jaringan konektivus, sel-sel otot polos yang berproliferasi dan matrik ekstraseluler (ME). Matrik ekstraseluler pada plak ateroma tersebut berasal dari sel otot polos yang berproliferasi pada bagian intima. Sel otot polos pembuluh darah bertanggung jawab dalam mensintesis komponen matriks intraseluler termasuk proteoglikan. (Wagner 1985; Edwards dan Wagner 1988).
Kwak et al. (2001) menyatakan, bahwa ada 3 komponen utama untuk terjadinya plak aterosklerosis yaitu: (1) sel endotel, sel otot polos, makrofag, dan limfosit T, (2) matriks ekstraseluler jaringan pengikat, dan (3) akumulasi lipid intraseluler dan ekstraseluler. Ketiga komponen tersebut dapat terjadi di dalam berbagai proporsi pada plak yang berbeda dan menggambarkan peningkatan lesi. Khususnya pada permukaan serabut penyusun sel otot polos yang menebal, dan sedikit meradang.
Sel yang terlibat dalam aterosklerosis
Sel endotel merupakan lapisan pelindung utama dinding pembuluh darah terhadap segala pengaruh buruk terutama berasal dari darah. Oleh karena itu jika sel endotel mengalami kerusakan/luka, maka sel-sel otot polos dan monosit akan masuk ke dalam sel intima endotel kemudian berproliferasi dan akhirnya akan menumpuk menjadi sel busa. Akhinya terbentuklah plak pada bagian intima dinding pembuluh darah.
Sel endotel merupakan suatu struktur pembuluh darah yang sangat krusial, bukan hanya karena fungsinya, tetapi juga dapat menghasilkan mediator yang mengatur pertumbuhan vaskular, fungsi trombosit dan koagulasi darah. Endotel juga berfungsi dalam pengaturan tonus vasomotor dengan mensintesis dan metabolisme endotheliumderived hyperpolerising factor, prostacycline dan faktor penting adalah endhotelium derived relaxing factor (EDGF), yang telah
30 diidentifikasi sebagai nitrit oxide (NO) atau suatu komponen terkait. NO dibentuk dari L-arginin oleh kerja enzim NO-synthase (NOS), yang bekerja menghambat agregasi dan perlekatan trombosit, modulasi proliferasi sel otot polos, menekan pembentukan endotelin dan memodulasi perlekatan leukosit dan monosit ke endotel (Bassenge & Busse 1988; Crowther 2005; Palmer et al. 1988; Wolin 2000).
Sel endotel berfungsi sebagai vasodilator, antitrombotik dan antiinflamasi. Dalam kondisi normal, sel endotel mensintesis vasodilator yang berbeda seperti NO, prostaglandin PG12 dan endothelium derived hyperpolarizing factor (EDHF). Pada kondisi patologis, sel endotel mensintesis berbagai faktor vasokontriksi seperti endothelium derived contriction factor (EDCF) termasuk endotelin, superoksid dan prostaglandin (Shimokawa 2000). Sel endotel dan trombosit menghasilkan granula protein membran140 kD (GMP-140) yang dapat berikatan dengan netrofil dan monosit, bila sel endotel teraktivasi dengan cepat terjadi translokasi netrofil dan monosit ke dalam membran. Setelah monosit menempel pada sel endotel, selanjutnya akan bermigrasi ke lapisan intima. Migrasi ini terkait dengan kehadiran sitokina monocyte chemottractant protein-1 (MCP-1) yang dihasilkan dan disekresikan oleh sel endotel, sel otot polos dan makrofag yang banyak dijumpai pada plak ateroma manusia maupun kelinci (Carlos & Harlan 1990; Munro & Cotrans 1988; Steinberg 1993).
Peningkatan permebialitas sel endotel merupakan kelainan pertama akibat terjadi jejas arteri dan merupakan suatu respon yang tidak spesifik disebabkan oleh virus, toksin, kompleks imun, produk-produk yang dilepaskan oleh sel-sel darah putih maupun platelet-platelet yang teraktivasi, serta stres fisik yang tidak lazim (Hansson, 2009; McGill 1968). Hal ini dapat juga disebabkan adanya peningkatan konsentrasi lipoprotein dalam darah. Kerusakan endotel akan merangsang platelet-platelet terakumulasi, berdegranulasi dan menghasilkan adenosine difosfat (ADP) serta tromboksan A2. Molekul ADP dan tromboksan A2 merupakan penyebabkan penumpukan platelet. Platelet-platelet sel endotel, makrofag, dan sel T limfosit menghasilkan cytokines like stimulating factors, insulin like growth factor-1, TGF-B, interleukin-1, dan tumor necrosis factor. Semua ini menghasilkan suatu faktor yang diketahui sebagai Platelet derivate
31 growth factors (PDGF), yang menyebabkan sel-sel otot polos dapat berproliferasi masuk ke dalam intima dan mengambil lipoprotein untuk membentuk sel busa, menghasilkan elastin, kolagen kemudian membentuk plak fibrosa. plak fibrosa adalah lesi yang langsung berhubungan dengan penyakit terutama dalam kondisi perubahan degeneratif (Argman et al. 2001; Hansson, 2009; Hoffman 1996; Rackley 2006).
Sel-sel otot polos merupakan unsur paling penting dalam pembentukan ateroma. Sel-sel ini berasal dari lapisan media dan berproliferasi ke dalam intima. Sel otot polos mempunyai sifat mitogenik dan proliferatif. Sifat ini dipengaruhi oleh rangsangan dari luar melalui reseptor khusus seperti LDL, faktor pertumbuhan (PDGF), insulin (Hansson, 2005). Sel-sel otot polos pada arteri terlibat di dalam kontraktil dan pengaturan intergritas struktur pembuluh darah, serta metabolisme lipid. Sel otot polos merupakan faktor utama yang berperan dalam perkembangan lesi aterosklerosis.
Hansson (2005) menyatakan bahwa sel otot polos mempunyai sifat mitogenik dan proliferatif. Sifat ini dipengaruhi oleh adanya rangsangan dari luar melalui reseptor khusus seperti LDL, platelet derived growth factor (PDGF) dan insulin. Secara in vitro, sel otot polos yang dikultur dan diinkubasikan dengan LDL teroksidasi dapat menimbulkan gangguan terhadap integritas struktural matrik. Keadaan ini akan meningkatkan permebialitas terhadap lipoprotein plasma dan menyebabkan gangguan ketahanan jaringan terhadap daya tekan.
Dalam media dari arteri normal mamalia, hanya sel otot polos ditemukan Menurut St Clair et al. 1996, sel-sel otot polos dijumpai juga pada bagian intima normal. Sedangkan Stary et al. (1992) menyatakan bahwa hasil uji mikroskop elektron dan imunohistokimia, terdapat dua jenis selsel otot polos pada intima arteri manusia yaitu sel otot polos yang banyak mengandung miofilamen atau kontraktil dan yang banyak mengandung retikulum endoplasmik kasar (r-ER) atau sintetik.
Menurut Stary et al. (1992) dan Stary et al. (1994), pada kultur sel, sel otot polos yang banyak mengandung retikulum endoplasmik kasar dapat mensintesis komponen matrik ekstraseluler. Menurut Anitshkow, sel-sel otot polos yang terdapat pada lesi aterosklerosis mempunyai perbedaan morfologis dengan sel otot
32 polos yang terdapat pada media yaitu bersifat lebih basofilik. Hal ini disebabkan sel otot polos banyak mengandung retikulo endoplasmik kasar dan (rER-smoot muscle cells) atau sel otot polos yang termodifikasi (modified smooth muscel cells). Proliferasi sel otot polos merupakan salah satu tanda adanya gangguan pada pembuluh darah yang menyebabkan terbentuknya aterosklerosis.
Makrofag berperan penting dalam aterosklerosis dan metabolisme lipoprotein. Makrofag berasal dari monosit dan peredaran darah yang menetap di intima dan berkembang menjadi makrofag. Peran penting lainnya memediasi respon peradangan dan antigen (antigen-independent/innate). Makrofag derivat monosit adalah pemangsa dan penyaji antigen (antigen-presenting cells/APC) terhadap respon peradangan yang menghasilkan sitokina, radikal oksigen bebas, protease dan faktor komplemen. Pengambilan lipoprotein termodifikasi oleh makrofag maka akan terjadi akumulasi kolesterol ester membentuk sel busa yang dikenal sebagai garit lemak. Sel busa dapat pecah dan menghasilkan metaloproteinase (Ross, 1999; Linton & Fazio, 2003; Hansson, 2005).
Makrofag memiliki reseptor yang dapat mengikat antibodi dan senjata yang mampu mencari dan menghancurkan antigen yang khas terhadap antibodi itu. Selama terjadi proses infeksi, sel limfosit-T yang terangsang menghasilkan sejumlah limfokin yang akan menarik makrofag ke tempat yang dibutuhkannya dan terus mengaktifkannya. Makrofag dapat juga berperan sebagai sel scavenger, sel mediator sistem imun, sumber molekul kemotaksis dan sitokina (Efendi 2003; Linton & Fazio 2003; Libby 2002).
Peranan Proteoglikan dalam Aterosklerosis
Proteoglikan (PG) merupakan makromolekul matrik ekstraseluler terdiri atas protein rantai glikosaminoglikan (GAG), dihubungkan oleh oligosakarida yang tersusun atas silosa-galaktosa-galaktosa . Sebagaimana dengan glikoprotein maka PG mengandung rantai N-oligosakarida dan O-oligosakarida. Rantai oligosakarida dari PG terdiri dari unit disakarida berulang yang mengandung 1) Glukosamin atau galaktosamin, 2) Asam uronat kecuali untuk keratan sulfat, dan 3) Ikatan kovalen gugus sulfat baik sebagai ester-O atau sebagai sulfat-N, kecuali
33 untuk asam hialoronat (Poole 1986). Pada arteri normal, PG utama adalah kondroitn 4-sufat (C4S), kondroitn 6-sufat (C6S), dan dermatan sulfat (DS), sedangkan heparin sulfat (HS) dan heparin sulfat ditemukan dalam jumlah sedikit (Edwards & Wagner 1988).
Kompleks proteoglikan dengan lipoprotein (PG-lipoprotein) terjadi pada sel otot polos, hal ini merupakan bentuk terjadinya aterosklerosis. Kompleks PG-lipoprotein dapat terbentuk karena kontak langsung dengan sel otot polos yang disebabkan oleh adanya makrofag yang terstimulasi. Keadaan ini memicu terjadinya akumulasi kolesterol ester sehingga menjadi sel-sel busa.
Komposisi asam amino dan berat molekul protein inti pada DS-PG dan CS-PG aterosklerosis sama dengan normal, perbedaan ditemukan pada rantai GAG. Molekul DS-PG aterosklerosis mempunyai berat molekul GAG lebih kecil (15 kD) dari normal (18 kD), sedangkan CS-PG sebagian besar rantai GAG berukuran lebih panjang (2,0x104) dari normal (1,5x10 4) dan sebagian kecil berukuran lebih pendek (1,2 x 10 4). Pada DS-PG aterosklerosis, substitusi residu serin terhadap karbohidrat sangat tinggi (30–40%) dari normal (1-2%), monomernya berukuran lebih besar, dan memiliki afinitas yang sangat besar terhadap LDL. Rantai GAG CS-PG juga mengalami penurunan kandungan serin dan treonin yang mencapai separuh dari normalnya. Kemampuan PG ini untuk berikatan dengan asan hialoronat (HA) juga mengalami penurunan mencapai separuh PG normal. Selain itu CS-PG yang ditemukan pada aterosklerosis adalah C6S, sedangkan pada
jaringan normal adalah C4S. Perbedaan-perbedaan tersebut diatas diduga terjadi pada proses postranslasional PG dalam badan golgi (Rowe & Wagner 1985; Wagner et al. 1986).
Poole (1988) menyatakan bahwa, PG dan glikoprotein merupakan makromolekul dimana rantai oligosakarida atau polisakarida terikat secara kovalen ke kerangka polipeptida. Rantai oligosakarida dari PG terdiri atas unit-unit disakarida berulang mengandung: 1). Glukosamin atau galaktosamin, 2). Asam uronat kecuali untuk keratan sulfat, dan 3). Ikatan kovalen gugus sulfat baik sebagai ester-O atau sebagai sulfat-N, kecuali untuk asam hialoronat.
Proteoglikan merupakan matriks ekstraseluler pada permukaan sel yang mengandung polisakarida linear dengan gugus sulfat, glikosaminoglikan (GAG)
34 berikatan kovalen ke protein inti. Makromolekul karbohidrat berperan penting dalam memelihara intergritas struktural pada jaringan, karena berinteraksi dengan makromolekul jaringan penghubung seperti kolagen dan elastin, proteoglikan membentuk substansi dasar yang ada diantara sel. Proteoglikan juga memelihara struktur dan intergritas fungsional dari endotel (Key et al. 1992; Rowe & Wagner 1985).Struktur dasar PG seperti Gambar 11.
Gambar 11 Struktur dasar proteoglikan
Berdasarkan struktur dan sifat komponen penyusunnya, PG mempunyai peranan penting sebagai bagian matriks penyokong dari jaringan penghubung yang terlibat langsung dalam interaksi antar sel-sel maupun antar sel-sel dengan matriks (sel matriks). Molekul GAG bersifat hidrofilik, yang menyebabkan PG mampu membentuk gel sehingga tahan terhadap tekanan. Cairan antar sel dalam jalinan PG memungkinkan berlangsungnya difusi zat makanan dan metabolit, atau dengan kata lain PG berperan dalam mengatur dan mengontrol distribusi garam dan air. Hal ini penting untuk memelihara sel serta serabut ikat dengan baik (Poole, 1988).
Identifikasi PG. Ioozo (1998) menyatakan bahwa berdasarkan struktur dan fungsi yang sama terhadap tingkat genomik dan tingkat protein, proteoglikan terdiri atas 4 macam gen yaitu, versican, aggregan, neurocan dan brevican. Proteoglikan yang kaya akan leusin kecil disebut small leucin-rich proteoglikan (SLRPs) berisi sedikitnya 9 produk yang dikode oleh gen terpisah dan dikelompokkan menjadi 3 klas. Klas I, terdiri atas decorin dan biglycan; klas II,
35 terdiri atas fibromodulin, lumican, keratocan, PRELP, osteodorin; klas III, terdiri atas epiphycan dan osteoglycan.
Kaplan & Aviram (2000) menyatakan bahwa heparan sufat (HS) dan GAG berperan mengatur proses selular, termasuk mengatur berinteraksinya faktor transkripsi (TF) di dalam inti. Hal ini dikarenakan HS dan GAG kaya akan leusin seperti dekorin dan biglikan. Leusin dan biglikan terdapat pada jaringan arteri normal maupun berlesi.
Proteoglikan yang terdapat pada dinding pembuluh darah terdiri atas: perlecan, agrin dan bamacan.Perlecan mengkode gen HS-PG yang terletak pada kromosom Ip-36 pter (manusia) dan kromosom 4-distal (tikus) dengan GAG adalah heparan/ CS. Agrin mengkode gen AGRN terletak pada kromosom Ip-32 pter pada manusia dan kromosom 4-distal pada tikus dengan tipe GAG adalah HS, sedangkan CS adalah bamacam tipe dari GAG (Ioozo 1998).
Menurut Wagner (1985) dan Edwards & Wagner (1988) menyatakan nahwa proteoglikan utama pembuluh arteri normal adalah kondroitin 4 sulfat (C4S),
kondroitin 6 sulfat (C6S) dan dermatan sulfat (DS), sedangkan heparan sulfat (HS)
dan heparin dijumpai dalam jumlah sedikit.
Mekanisme Sintesis Tempat Intraseluler
Protein inti Retikulum endoplasmik Intermediet dolikol Penambahan oligosakarida
difosfat manosa tinggi–N linked Transferase glikosil glikosilasi
Transferase glikosil Penambahan rantai CS, KS,HS, &H Golgi dengan UDP-glu & dan O- linked oligosakarida
UDP-N-asetilglukosamin
3’fosfoadenosin- Sulfasi secara bersama dgn GAG lalu 5’fosfosulfat (PAPS) terjadi epimerasi dari as glukoronik
untuk iduronik pada DS, HS & H Perubahan OS manosa tinggi
ke asam sialik tipe OS
terjadi sekresi vakuola Gambar 12 Biosintesis proteoglikan (poole 1988)
36 Biointesis proteoglikan berlangsung di dalam retikulum endoplasmik dan disempurnakan di dalam golgi kemudian disekresikan melalui vakuola (Gambar 12). Pengaturan biosintesis melibatkan beberapa molekul penting seperti hidrokortison, testosteron, follicle stimulation hormone (FSH) maupun growth factor seperti PDGF, insulin-like growth factor II, pituitary-derived fibroblast growth factor. Setiap jenis dari masing-masing sel mempunyai fungsi yang berbeda (Poole 1988).
Fungsi lain PG dalam aterosklerosis adalah adanya hubungan tidak langsung DS-PG dengan HS-PG. DS-PG dan heparin dapat mempercepat penghambatan reaksi pembentukan trombin melalui stimulasi heparin cofactor II (HC-II). Trombin merupakan serin proteinase yang berperan dalam hemostasis dan trombosis melalui kemampuannya menghasilkan fibrin dan mengaktifkan platelet. Molekul HC-II distimulasi oleh DS-PG-HA, selanjutnya akan diaktifkan oleh HS-PG. Penurunan konsentrasi HS-PG pada penderita aterosklerosis menimbulkan ganggguan terhadap pengaturan trombin, sehingga aktivitas trombin menjadi berlebihan. Aktivitas trombin yang berlebihan ini selanjutnya akan menghambat aktivitas DS-PG untuk menstimulasi dan melepaskan HC II (Cadroy et al. 1993; Shirk et al. 1996).
Faktor Risiko
Faktor risiko merupakan penyebab yang dapat mendorong terbentuknya aterosklerosis dan dapat menyebabkan PJK. Salah satu cara pencegahan PJK yaitu menghindari berbagai faktor risiko. Faktor risiko tersebut antara lain: tingginya kolesterol di dalam darah (hiperkolesterolemia), hipertensi, merokok, usia, gender, estrogen, obesitas, etnis, diet, diabetes, gaya hidup, dan genetik. Saat ini dikenal faktor risiko baru PJK seperti kadar homosistein, C-reactive Protein (CRP) serta lipoprotein (a) (Libby 2000; Packard & Libby 2008).
Hiperkolesterolemia adalah kenaikan konsentrasi kolesterol dalam peredaran dan darah tidak dapat disanggah lagi sebagai penyebab utama aterosklerosis. Hal ini telah dibuktikan oleh para ahli dengan penurunan kolesterol dalam darah menurunkan juga pembentukan aterosklerosis. Kolesterol sendiri tidak dapat dipisahkan dengan lipoprotein dan lipid lainnya sebagai faktor
37 aterogenik. Kolesterol-HDL dapat memediasi hati untuk mengeluarkan kolesterol melalui rivers transpotasi keperifer. Faktor genetik diketahui berkontribusi terhadap rendahnya konsentrasi kolesterol HDL yang melibatkan perubahan terhadap: gen untuk apolipoprotein A1-C11; lipoprotein lipase; protein transfer ester kolesterol; lipase hepatik dan lesitin asiltransferase kolestrol.
Hipertensi dapat merangsang aterogenesis namun mekanisme kejadian hipertensi tidak diketahui dengan pasti. Penurunan tekanan darah secara nyata menurunkan resiko terjadinya stroke. Hipertensi diduga dapat menyebabkan disfungsi endotel dengan menurunkan kadar Nitrit Oxide (NO), sehingga vasodilatasi jadi berkurang dan resistensi pembuluh darah menjadi meningkat (Panaza et al. 1993). Kondisi ini berkaitan erat dengan adanya peningkatan Ca2+ dan penuruan NO sintetase, atau sebagai efek radikal bebas derivat oksigen yang menghambat produksi NO. Selain itu juga diduga beberapa jenis zat yang dikeluarkan oleh tubuh seperti rennin, angiotensi dan lain lain dapat menginduksi perubahan seluler yang menyebabkan aterogenesis.
Merokok, metabolit rokok adalah allylamine dengan produk akhir acreolin dan spesies oksigen reaktif. Penurunan tekanan oksidatif pada level antioksidan meneybabkan menurunnya kemampuan tehadap peroksidasi lipid, disfungsi endotel dan pembengkakan mitokondria (Zimmerman & McGeaccliie 1987). Merokok juga menyebabkan terjadi peningkatan agregasi dan fibrinogen plasma yang berkontribusi terhadap gangguan di arteri (Badimon et al. 1999).
Diabetes berhubungan dengan aterosklerosis. Diabetes berperan dalam penyakit vascular sebagai komplikasi jangka panjang seperti gangguan ginjal. Pada diabetes terdapat peningkatan LDL yang mudah mengalami glikolasi dan oksidasi, disamping itu VLDL dan HDL juga mengalami oksidasi dan glikolasi (Bierman 1992). Hiperglikemia berkontribusi terhadap fungsi endotel yang merespon produksi abnormal asetetilkolin, meningkatkan tromboksan dan prostaglandin, meningkatkan Ca2+ intraselular. Semua molekul kimia ini menyebabkan pelepasan agen vasokontriksi endotel seperti: asetilkolin1 dan endotelin1. Hiperglikemia juga beraselerasi menghasilkan radikal bebas untuk memediasi terjadinya LDL teroksidasi (Kawamura et al. 1994).
38 Fibrinogen merupakan prekursor dari fibrin dan berhubungan dengan viskositas darah, aliran dan koagulasi darah. Peningkatan agregasi platelet, fibrin dan pembentukan thrombin akan menstimuli proliferasi dan pembentukan plak. Proses juga karena tingginya level faktor VII dan aktivator plasminogen yang dapat sebagai prediksi dari aterosklerosis (Cartellaro et al. 1993).
Homosistein dilaporkan cukup signifikan sebagai faktor risiko untuk penyakit pembuluh darah aterotrombotik. Mekanisme patogenik homosistein diduga terkait dengan penyakit penyakit jantung termasuk efek dari fungsi platelet, faktor pembekuan dan endotel yang menyebabkan migrasi dan proliferasi sel (Mayer et al. 1996, Robinson, 2000). Level homosistein dapat dipengaruhi oleh vitamin B12, B6 dan suplemen asam folat dalam pengaturan metabolisme homosistein (Toole, et al. 2004).
Radikal Bebas dan Antioksidan
Dewasa ini, dunia kedokteran dan kesehatan banyak membahas tentang radikal bebas dan antioksidan. Hal ini terjadi karena sebagian besar penyakit diawali oleh adanya reaksi oksidasi yang berlebihan di dalam tubuh. Reaksi oksidasi terjadi setiap saat, ketika kita bernafas reaksi oksidasi juga terjadi. Reaksi oksidasi dapat menimbulkan radikal bebas yang sangat aktif dan dapat merusak struktur dan fungsi sel. Tetapi reaktivitas radikal bebas dapat dihambat oleh system anti oksidan yang melengkapi sistem kekebalan tubuh (Winarsih, 2007).
Dalam kehidupan aerobik, oksigen mempunyai beberapa peranan penting antara lain memproduksi energi, mensintesis berbagai senyawa esensial, menurunkan aktivitas molekul yang tidak dikehendaki dan melawan mikroorganisme yang masuk ke dalam tubuh. Pada orang dewasa, oksigen yang dikonsumsi 90-95 % akan diubah oleh proses respirasi di dalam mitokondria menjdi air (H2O). Sekitar 5-10% sisanya akan mengalami reduksi univalent atau
bivalent menghasilkan senyawa oksigen reaktif, yaitu: radikal superoksida, hydrogen peroksida dan hidroksi radikal (Estaerbauer 1993; Wuryastuti 2000).
Untuk pertahanan diri terhadap senyawa kimia yang berbahaya dan mikrobah patogen yang masuk ke dalam tubuh, terdapat suatu sistem detoksikasi
39 dan respon imunologik yang melibatkan berbagai organ tubuh. Mekanisme detoksifikasi ditunjukan untuk menanggulangi senyawa-senyawa kimia asing seperti logam berat, pestisida, insektisida dan lain-lain. Berbagai logam berat dan logam transisi telah diketahui sebagai katalis radikal bebas (Halliwel et al.1992). Mekanisme detoksifikasi dapat meliputi pembentukan senyawa radikal (elektrofil) dan radikal bebas. Reaksi ini terjadi didalam hati melalui system enzim monooksigenase sitokrom P-50 (Zakaria 1996). Jumlah P-450 dalam hati tergantung ukuran tubuh dan jangka hidup serta berbanding terbalik dengan kemampuan jaringan membentuk peroksida. Selain itu, sitokrom P-450 memproduksi sejumlah besar oksigen aktif, dan NADPH-sitokrom P-450 reduktase yang membantu dalam pembentukan oksigen radikal.
Radikal Bebas
Radikal bebas, yang sering disebut sebagai senyawa oksigen reaktif (SOR) adalah sebagai atom atau molekul yang mempunyai satu atom lebih yang tidak berpasangan pada orbital luarnya (Halliwell et al. 1992). Ada dua cara untuk terbentuknya radikal bebas yaitu: secara endogen, sebagai respon normal dari rantai biokimia di dalam tubuh, sel (intrasel) maupun ekstrasel; secara eksogen radikal bebas diperoleh dari polusi, makanan dan penyerapan kulit (Supari 1996). Radikal bebas dan senyawa reaktif yang diproduksi dalam jumlah normal sesungguhnya berperan penting dalam menjalankan fungsi biologik seperti sel darah putih menghasilkan H2O2 untuk membunuh beberapa jenis bekteri
(Wuryastuti 2000). Radikal bebas dianggap berbahaya karena menjadi sangat reaktif dalam upaya mendapat pasangan elektronnya, dan dapat membentuk radikal bebas baru dari atom atau molekul yang elektronnya terambil untuk berpasangan dengan radikal sebelumnya (Muhilal 1991).
Reaktivitas radikal bebas merupakan upaya untuk mencari pasangan elektron. Sebagai dampak kerja radikal bebas tersebut akan terbentuk radikal bebas baru yang berasal dari atom atau molekul elektronnya untuk berpasangan dengan radikal sebelumnya. Tetapi apabila dua senyawa radikal bertemu dengan elektron-elektron yang tidak berpasangan, dan kedua senyawa tersebut akan bergabung membentuk ikatan kovalen yang stabil. Sedangkan bila radikal bebas
40 bertemu dengan senyawa bukan radikal bebas akan berpasangan dengan jalan:1. Radikal bebas memberikan elektronnya yang tidak berpasangan (reduktor) yang bukan radikal: 2. Radikal bebas menerima elektron (oksidator) dari senyawa bukan radikal bebas dan 3. Radikal bebas bergabung dengan senyawa bukan radikal bebas (Winarsi 2007; Halliwell et al. 1992).
Menurut Sadikin (2001), serangan radikal bebas terhadap molekul sekelilingnya akan menyebabkan terjadinya reaksi berantai, kemudian menghasilkan senyawa radikal baru. Dampak reaktivitas senyawa radikal bebas dapat bermacam-macam dimulai dari kerusakan sel atau jaringan, penyakit autoimun, penyakit degeneratif hingga kanker. Radikal bebas dapat menyebabkan kerusakan di berbagai bagian sel, karena sangat reaktif dalam gerakan yang tidak beraturan (Halliwell et al. 1992; Muhilal 1991). Kerusakan dapat terjadi pada komponen penyusun membran sel seperti asam lemak tak jenuh yang merupakan bagian dari fosfolipid, kerusaakan lebih lanjut terjadi pada organel sel sampai pada kerusakan DNA di dalam inti (Halliwel 2005).
Pembentukan radikal bebas pada awalnya diketahui terjadi di netrofil dan makrofag yang terinfeksi mikroorganisme (Jenssen et al. 1993). Radikal anion superoksida (O2٭-) dapat dibentuk dari oksigen tereduksi menjadi air dengan
penambahan 4 elektron selama proses fosforilasi oksidatif. Radikal anion kemudian akan dubah menjadi peroksida (H2O2) oleh enzim superoksid
dismutase. Oksigen yang teraktivasi dapat terjadi dalam brbagai sel, termasuk mitokondra, glioksosom, perioksisom dan sitosol (Elastner,1991). Ion superoksida terbentuk dalam kloroplas, mitokondria dan peroksisom merupakan senyawa oksigen yang sangat reaktif (Fridovich 1986). Molekul H2O2 dapat tereduksi
membentuk radikal hidroksil (OH٭) yang sangat aktif dengan adanya ion logam melalui reaksi feton (Breen & Murphy 1995). Radikal hidroksil dapat juga terbentuk akibat reaksi non enzimatis selama pemaparan radiasi ion (Clark et al. 1987).
Peroksidasi lipid dapat mempegaruhi struktur dan fungsi membran seperti: penurunan kandungan relatif asam eikosapentaenoat (C20:5) dan asam dokosaheksaenoat (C22:6), pembentukan lipid hidroksi peroksida yang dapat merangsang atau menghambat enzim spesifik yang berhubungan dengan
41 biomembran. Selain itu terjadinya oksidasi tiol grup dapat mempengaruhi aktivitas enzim di dalam membran, konformasi protein yang berhubungan dengan lipoprotein, penurunan fluiditas lipid biomembran. Terbebasnya produk pecahan dari peroksidasi lipid akan menghasilkan efek-efek kerusakan sel (Donelly & Robinson 1990). Bahan aditif pangan seperti asam karmiat dapat membentuk radikal bebas yang berperan sebagai inisiator dalam proses peroksidasi lipid sehingga menimbulkan kerusakan jaringan (Zakaria 1996).
Penelitian terhadap radikal bebas dan antioksidan sampai saat ini cukup menarik. Telah diketahui bahwa berbagai pengaruh radikal bebas dapat menyebabkan kanker, penyakit jantung koroner, rematik, gangguan respiratorik, hepar, diabetes melitus dan proses penuaan. Akibat kerusakan sel ini dapat mengakibatkan terjadinnya berbagai penyakit degenertif. Berbagai hasil penelitian telah membuktikan bahwa reaksi senyawa elektrofil dapat diredam oleh antioksidan (Esterbeurer 1991; Thies & Siege 1989). Radikal bebas di dalam tubuh dapat dicegah pembentukannya dengan menghindari sinar matahari, langsung, asap rokok, polusi udara, serta meningkatkan asupan makanan yang kaya akan senyawa antioksidan seperti sayuran, buah-buahan , biji-bijian serta kacang-kacangan.
Antioksidan
Antioksidan adalah senyawa/ zat yang dalam konsentrasi kecil dapat mencegah reaksi oksidasi dengan mengikat radikal bebas dan molekul yang sangat reaktif. Secara biologis, antioksidan adalah senyawa yang mampu meredam dampak negatif oksidan dalam tubuh. Antioksidan bekerja dengan cara mendonorkan satu elektronnya kepada senyawa yang bersifat oksidan sehingga senyawa oksidan tersebut dapat dihambat reaksinya (Winarsi 2007). Selanjutnya dikatakan bahwa, konsumsi antioksidan dapat menurunkan kejadian penyakit degeneratif seperti: penyakit jantung koroner, kenker, aterosklerosis dan osteoporosis. Antioksidan dapat meningkatkan status imunologis dan menghambat timbulnya penyakit degeneratif akibat penuaan.
Keseimbangan oksidan dan antioksidan sangat penting karena berkaitan dengan berfungsinya sistem imunitas tubuh. Kondisi ini untuk menjaga intergrites