OF CHLOROPHORM EXTRACT OF MANGO (Mangifera indica L. Var Arumanis) SEED Oleh, Happy Albertina NIM: 652011002 TUGAS AKHIR
Diajukan kepada Program Studi Kimia, Fakultas Sains dan Matematika guna memenuhi sebagian dari persyaratan untuk mencapai gelar Sarjana Sains (Kimia)
Program Studi Kimia
Fakultas Sains dan Matematika Universitas Kristen Satya Wacana
Salatiga 2015
iii
1
OPTIMASI EKSTRAKSI MINYAK DAN AKTIVITAS ANTIBAKTERI EKSTRAK KLOROFORM BIJI MANGGA (Mangifera indica L. Var Arumanis) OPTIMIZATION OF OIL EXTRACTION AND ANTIBACTERIAL ACTIVITY
OF CHLOROPHORM EXTRACT OF MANGO (Mangifera indica L. Var Arumanis) SEED
Happy Albertina*, Hartati Soetjipto**, Silvia Andini** *Mahasiswa Program Studi Kimia Fakultas Sains dan Matematika
**Dosen Program Studi Kimia Fakultas Sains dan Matematika Universitas Kristen Satya Wacana, Salatiga
Jl. Diponegoro no 52-60 Salatiga 50711 Jawa Tengah – Indonesia
652011002@student.uksw.edu
ABSTRACT
This research has determining the optimal time of oil extract of mango seed (Mangifera indica L. var Arumanis) as a purpose by soxhlet method with n-hexane as the solvent and its effect to the result of the mango seed oil physico-chemical characteristic. Physico-chemical determination of mango seed oil is determined based on SNI 01-3555-1998. The yield data and physico-chemical characteristic of mango seed oil is analyzed by Randomized Block Design (RBD), through 6 treatments: 3; 6; 9; 12; 15; and 18 hours, and 4 repetitions, while as a group is analysis time. The research result show that the highest oil yield is produced in the 15 hours extraction: 19,31 ± 0,76%. The extraction duration gives effect on the yield, oil water amount, sour nominal, lathering nominal, peroxide nominal, hence it doesn’t influence the mango seed oil density. GCMS analysis result, the mango seed oil ingredients content of 3 chemical components, they are heksadekanoat sour 12,16%, 9-octadecanoic 59,42%, and octadecanoic sour 28,42%. The act of determining antibacterial activity toward Salmonella sp. and Bacillus subtilis mango seed chlorophorm extract using Harborne method. Antibacterial activity is analyzed by Randomized Block Design (RBD) sub sampling in 8 ways, 3 replications, and 4 sub samples. As the treatments of chlorophorm extract dosage are 0; 0,5; 1; 1,5; 2; 3; 6 mg and positive control using tetracycline. Antibacterial power in 0,5 – 1 mg dosage included in low category, 1,5 – 3 mg included in medium category, and for 6 mg dosage include in the strong category toward bacteria Bacillus subtilis. For Salmonella sp bacteria in 0,5 – 1,5 mg dosage included in the low category and in 2 – 6 mg dosage included in medium category. Keywords: antibacterial, chemical-physic characteristic, inhibition, mango seed, vegetable oil.
PENDAHULUAN
Indonesia memberikan kontribusi produksi mangga sekitar 5% dari produksi mangga dunia. Negara produsen mangga terbesar adalah India (51%). Di Asia, negara penghasil mangga yang cukup berarti selain Indonesia ialah Cina (9%), Thailand (6%), Pakistan (4%), dan Filipina (2%). Ekspor mangga Indonesia menunjukkan peningkatan dari tahun ke tahun, tetapi dibanding dengan produksinya sendiri maka ekspor tersebut relatif masih sangat rendah, yaitu 0,07% (BPS, 2007 dalam Utama dkk., 2011). Setidaknya Indonesia menghasilkan limbah biji mangga sekitar 1 juta ton setiap tahunnya dan yang bisa dimanfaatkan sekitar 200 ribu ton per tahun (Sajarwo, 2012).
Biji buah mangga memberikan kontribusi sekitar 20% sampai 60% dari berat buah, tergantung pada varietasnya (Sahu et al, 2013). Daging biji mangga bambangan (Mangifera indica) mengandung: air (41,38%), karbohidrat total (38,68%), lemak (9,85%), serat kasar (4,79%), protein (3,08%), dan abu total (2,23%) (Ali, 2010).Selain itu, biji buah mangga juga memiliki kandungan flavonoid, tanin, steroid, dan saponin yang mampu berperan sebagai antibakteri (Sahu et al., 2013).
Minyak nabati merupakan minyak yang bersumber dari tumbuh-tumbuhan ataupun tanaman yang diperoleh dari pengolahan bagian batang, daun, biji, kulit buah, maupun bunga melalui proses ekstraksi (Prapti dkk., 2011). Untuk keperluan industri, minyak nabati dapat digunakan sebagai bahan dalam pembuatan sabun dan lotion
(produk kesehatan kulit dan kosmetik), agen pengering dalam pembuatan cat, maupun bahan bakar biodiesel (Tambun, 2006 dalam Wibowo, 2013).
Akhir-akhir ini, pemanfaatan herbal mulai dikembangkan kembali sebagai upaya
back to nature. Sehingga diperlukan eksplorasi tanaman Indonesia untuk memperoleh manfaat lebih. Salah satu permasalahan yang terjadi di negara tropis yang beriklim hangat adalah bakteri yang bersifat patogen. Penyakit yang disebabkan oleh bakteri ini cukup serius karena menimbulkan berbagai gangguan, seperti infeksi kulit, infeksi usus, infeksi saluran pencernaan, dan infeksi saluran pernafasan. Sedangkan dapat kita ketahui untuk upaya penanggulangan dibutuhkan obat-obatan antibakteri yang harganya cukup tinggi (Nasiyah, 2009).
Berbagai macam cara atau metode dapat digunakan untuk memperoleh minyak nabati dari berbagai sumber. Salah satu cara dengan hasil terbaik adalah dengan menggunakan metode ekstraksi soxhlet dengan pelarut organik. Pada penelitian ini akan dilakukan optimasi ekstraksi minyak biji mangga dengan pelarut n-heksana dan diamati aktivitas antibakterinya ekstrak kloroform dari biji buah mangga jenis arumanis.
Tujuan
Adapun tujuan diadakan penelitian ini adalah:
1. Menentukan optimasi ekstraksi minyak biji mangga menggunakan pelarut n-heksana ditinjau dari lama ekstraksi.
2. Menentukan sifat fisiko-kimia minyak biji mangga yang meliputi: kadar air, rendemen, viskositas, massa jenis, bilangan asam, bilangan peroksida, dan bilangan penyabunan.
3. Mengidentifikasi komponen penyusun minyak biji mangga (Mangifera indica L.)
menggunakan Kromatografi Gas yang terhubung dengan Spektrofotometer Massa. 4. Menentukan efek antibakteri ekstrak kloroform biji mangga dengan metode cakram
kertas.
METODOLOGI Bahan dan sampel
Sampel yang digunakan berupa biji buah mangga Indonesia (Mangifera indica L.) jenis arumanis yang diperoleh dari pedagang buah-buahan di wilayah Salatiga. Bahan lain seperti n-heksana (teknis), etanol (pro analysis, Merck, Jerman), kloroform (pro analysis, Merck, Jerman), asam asetat glasial (Merck, Jerman), asam klorida (Merck, Jerman), akuades, kanji, natrium hidroksida (Merck, Jerman), kalium iodida (pra kristal, Merck, Jerman), kalium hidroksida (Merck, Jerman), metanol (teknis), Bacillus subtilis,
Salmonella sp., nutrient broth (Merck, Jerman), natrium klorida (Merck, Jerman), medium Mueller Hinton Agar (Merck, Jerman), tetrasiklin (Oxoid), dan paper disc
(Whatman, Inggris) yang diperoleh dari laboratorium kimia Universitas Kristen Satya Wacana.
Piranti
Piranti yang digunakan antara lain moisturizer balance (Ohaus TAJ602, USA),
soxhlet, penangas air, neraca analitik 4 digit (Metler H 80, USA), neraca analitik 2 digit (Ohaus TAJ602, USA), drying Cabinet, rotary evaporator (Buchi R0114, Swiss), grinder, buret, spektrofotometer UV mini (Shimadzu U-1240, Jepang), autoklaf (Tomy Seiko SS-140, Jepang), inkubator, Kromatografi Gas Spektrofotometer Massa (Shimadzu QP 2010 SE, Jepang), dan peralatan gelas.
Metode
Preparasi Serbuk Biji Mangga
Biji mangga yang telah dicuci bersih dan dibebaskan dari selaput pembungkusnya, dipotong tipis dan dikeringkan dengan oven pada suhu 50ºC selama 5 jam. Lalu dihaluskan dengan grinder dan disimpan dalam wadah yang tertutup rapat.
Ekstraksi Minyak biji mangga (Dewi, 2012 yang, dimodifikasi)
Sebanyak 100 g serbuk biji mangga di soxhlet dengan menggunakan n-heksana sebanyak 400 mL dengan variasi waktu 3; 6; 9; 12; 15; dan 18 jam pada suhu 80ºC. Hasil ekstraksi dipekatkan dengan rotary evaporator pada suhu 50-60°C. Minyak hasil ekstraksi dipindahkan ke dalam botol sampel yang telah ditimbang lalu disimpan pada suhu 20°C sampai siap untuk dianalisis lebih lanjut.
Karakterisasi Sifat Fisiko-Kimia Minyak Aroma dan Warna
Penentuan aroma dan warna ditentukan secara deskriptif. Kadar Air
Sebanyak 1 gram minyak ditimbang dan diukur kadar airnya menggunakan
moisturizer balance dengan tiga kali pengulangan. Rendemen (Sudarmadji, 1997)
Penentuan rendemen dilakukan secara gravimetri dengan menggunakan neraca 4 digit.
Massa Jenis (Sudarmadji, 1997)
Sebanyak 1 mL minyak diukur seksama dan ditimbang dengan ketelitian 0,0001 g. Massa jenis dinyatakan dalam g/mL.
Bilangan Asam (SNI 01-3555-1998)
Sebanyak 2-5 gram minyak ditambahkan dengan 50 mL etanol 95%. Ditambahkan sebanyak 3 – 5 tetes indikator fenolftalein dan dititrasi dengan NaOH 0,1 M hingga warna merah muda tetap (tidak berubah selama 15 detik).
Bilangan Peroksida (SNI 01-3555-1998)
Minyak ditambah 30 mL campuran kloroform, asam asetat glasial dan etanol 95% dengan perbandingan 11 : 4 : 5. Satu gram kristal KI ditambahkan dalam campuran tersebut. Penentuan dilakukan dengan mengukur jumlah KI yang teroksidasi melalui titrasi dengan Na2S2O3 0,02 N.
Bilangan Penyabunan (SNI 01-3555-1998)
Sebanyak 2 gram minyak ditambah dengan 25 mL KOH 0,5 M, lalu direfluks selama satu jam. Ditambahkan sebanyak 0,5 - 1 mL indikator fenolftalein. Jumlah KOH yang tidak bereaksi dititrasi dengan HCl 0,5 M.
Analisis Komposisi Kimia Minyak Biji Mangga
Analisa GC dilaksanakan di Laboratorium Terpadu, Fakultas MIPA Universitas Islam Indonesia, Sleman Yogyakarta, pada kondisi operasional:
Kolom : Egilent J&W DB-5 Panjang : 30 meter x 0,25 mm Gas Pembawa : Helium
Flowrate : 0,75 mL/min Temperatur Injektor : 200ºC
Gradien Suhu :
60ºC (selama 5 menit awal) meningkat sampai 300ºC dengan kecepatan 10ºC/min
Pengionan MS : Electron impact (EI) Elektron Multiplier Energy : 0,80 Kv
Monitoring Unit Mass (m/z) : 30,00 sampai 400,00 Temperatur Interface : 300ºC
Temperatur Sumber Pengionan : 200ºC Detektor GC : FID-TCD
Uji Aktivitas Antibakteri Ekstrak Kloroform Biji Mangga Pembuatan Ekstrak Kloroform Biji Mangga (Harborne, 1987) Fraksi heksana
Sebanyak 225,5 g serbuk biji mangga dimaserasi dengan total pelarut n-heksana 1000 mL selama 45 menit diulang sebanyak 3 kali. Ekstrak biji mangga dievaporasi pada suhu 80ºC.
Fraksi kloroform
Ampas hasil maserasi fraksi heksana ditambah dengan metanol 80% sebanyak 100 mL, kemudian dimaserasi selama 15 menit. Hasil ekstrak kemudian disaring, filtrat dimasukkan ke dalam corong pisah dan diasamkan dengan H2SO4 2 M. Ditambah pelarut kloroform 3 kali tahapan dengan total 300 mL. Lapisan kloroform dipisahkan, kemudian dievaporasi pada suhu 60ºC.
Persiapan Inokulum Bakteri
Bakteri Bacillus subtilis sebanyak satu ose diinokulasi ke dalam medium nutrient broth (NB), lalu diinkubasi selama 24 jam pada suhu 37C. Hal yang sama juga dilakukan untuk bakteri Salmonella sp.
Penentuan Aktivitas Antibakteri (Alim, 2009)
Larutan NB yang mengandung bakteri dimasukkan ke dalam larutan 25 mL natrium klorida 0,9% agar diperoleh kekeruhan suspensi bakteri yang sama dengan larutan baku Mc Farlan dengan cara diukur absorbansinya pada panjang gelombang 620 nm dengan blanko natrium klorida 0,9% (nilai absorbansi 0,08 – 0,13; suspensi bakteri 1,5 x 108 CFU/mL).
Penentuan Aktivitas Antibakteri Ekstrak Kloroform Biji Mangga (Alim, 2009, dimodifikasi)
Larutan yang telah berisi sejumlah bakteri diambil sebanyak 1 mL lalu dimasukkan kedalam cawan petri. Ditambahkan medium Mueller Hinton Agar (MHA) sebanyak 9 ml dalam keadaan suam-suam kuku dengan kisaran suhu (40-45 ºC), lalu digoyang dan didiamkan sampai medium memadat. Paperdisc yang telah ditetesi 20 µL ekstrak dengan kandungan dosis 0,5; 1; 1,5; 2; 3; dan 6 mg diletakkan di atas medium yang berisi bakteri uji. Kontrol negatif digunakan akuades, sedangkan kontrol positif digunakan tetrasiklin 30 µg. Cawan petri diinkubasi pada suhu 37 ºC selama 18-24 jam.
Daerah terang pada sekitar cakram menunjukkan adanya aktivitas antibakteri dan diukur sebagai Diameter Daerah Hambat (DDH).
Analisa Data
Data rendemen dan sifat fisiko-kimia dianalisis dengan menggunakan rancangan dasar RAK (Rancangan Acak Kelompok) dengan 6 perlakuan dan 4 ulangan. Sebagai perlakuan adalah lama waktu ekstraksi yaitu 3; 6; 9; 12; 15; dan 18 jam, sedangkan sebagai kelompok adalah waktu analisis. Aktivitas antibakteri dianalisis dengan Rancangan Acak Kelompok (RAK) sub sampling dengan 8 perlakuan, 3 ulangan, dan 4 sub sampel. Sebagai perlakuan adalah dosis ekstrak kloroform yaitu 0; 0,5; 1; 1,5; 2; 3; 6 mg dan kontrol positif. Pengujian antar rataan perlakuan dilakukan dengan menggunakan uji Beda Nyata Jujur (BNJ) dengan tingkat kebermaknaan 5% (Steel dan Torrie, 1980).
HASIL DAN PEMBAHASAN
Minyak biji mangga yang dihasilkan berwarna kuning kecoklatan dengan aroma manis buah mangga. Warna kuning kecoklatan disebabkan oleh zat warna xanthofil yang secara alamiah ikut terekstrak bersama minyak pada saat proses ekstraksi (Ketaren, 1986).
Rendemen Minyak
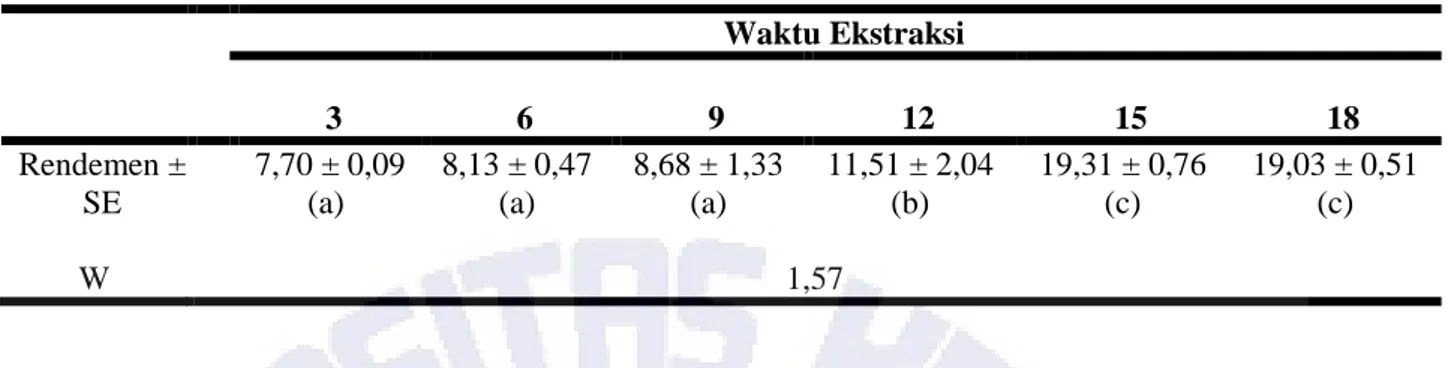
Hasil rataan rendemen minyak biji mangga (Mangifera indica L.) yang dihasilkan antar lama waktu ekstraksi disajikan pada Tabel 1.
Tabel 1. Rataan Rendemen (% ± SE) Minyak Biji Mangga antar Lama Waktu Ekstraksi
Keterangan :
*SE = Simpangan Baku Taksiran *W = BNJ 5 %
*Angka yang diikuti huruf yang tidak sama menunjukkan berbeda nyata sedangkan angka yang diikuti huruf yang sama menunjukkan antar perlakuan tidak berbeda nyata.
Rendemen (% ± SE) Waktu Ekstraksi 3 6 9 12 15 18 7,70 ± 0,09 (a) 8,13 ± 0,47 (a) 8,68 ± 1,33 (a) 11,51 ± 2,04 (b) 19,31 ± 0,76 (c) 19,03 ± 0,51 (c) W 1,57
Tabel 1 menunjukkan bahwa rendemen minyak biji mangga tidak mengalami peningkatan untuk lama ekstraksi 3 sampai 9 jam. Peningkatan rendemen terjadi ketika ekstraksi diperpanjang menjadi 12 dan 15 jam. Pada ekstraksi selama 18 jam rendemen minyak yang dihasilkan tidak mengalami peningkatan. Peningkatan rendemen ekstrak seiring dengan lama waktu sampai dengan 15 jam diduga karena pada waktu ekstraksi yang relatif singkat, masih banyak molekul minyak yang terperangkap dalam jaringan sel (Handajani dkk., 2010). Sedangkan pada lama waktu ekstraksi 15 jam semua minyak telah terekstrak, sehingga sampai lama waktu 18 jam sudah tidak ada peningkatan lagi.
Hasil pengukuran sifat fisiko-kimia minyak biji mangga antar lama waktu ekstraksi ditampilkan pada Tabel 2.
Tabel 2. Rataan Sifat Fisiko-Kimia Minyak Biji Mangga antar Lama Waktu Ekstraksi
Keterangan :
*SE = Simpangan Baku Taksiran *W = BNJ 5 %
*Angka yang diikuti huruf yang tidak sama menunjukkan berbeda nyata sedangkan angka yang diikuti huruf yang sama menunjukkan antar perlakuan tidak berbeda nyata.
Massa Jenis
Massa jenis merupakan pengukuran massa setiap satuan volume benda. Semakin besar massa jenis benda, maka semakin besar pula massa setiap volumenya. Minyak memiliki massa jenis sebesar 0,8 gram/ml (Sultan, 2013). Berdasarkan penelitian yang dilakukan, massa jenis minyak biji mangga berkisar antara antara 0,82 ± 0,04 – 0,85 ± 0,01 g/mL. Lama pemanasan tidak berpengaruh terhadap massa jenis minyak. Setiap jenis minyak mempunyai massa jenis yang khas, tergantung pada jenis asam lemak penyusun minyak tersebut (Nichols et al., 2003).
Waktu Ekstraksi (Jam) Massa Jenis Minyak (g/mL) Kadar Air Minyak (% ) Bilangan Peroksida (mgek/kg ) Bilangan Asam (mg KOH/g minyak) Bilangan Penyabunan (mg KOH/g minyak) 3 0,84± 0,01a 1,25± 0,80a 40,00 ± 4,50a 5,47 ± 0,85c 282,48 ± 4,07a 6 0,85± 0,01a 1,25± 0,80a 40,50 ± 1,59a 3,51 ± 0,45ab 287,03 ± 2,11ab 9 0,82± 0,04a 2,50± 0,92b 50,00 ± 2,60b 3,65 ± 0,51b 288,22 ± 2,24b 12 0,82± 0,04a 1,25± 0,80a 52,50 ± 1,59b 2,53 ± 0,52a 286,52 ± 4,54b 15 0,82± 0,03a 1,50± 0,92b 56,00 ± 0,00c 3,37 ± 0,73sb 287,52 ± 2,58b 18 0,82± 0,02a 1,50± 0,92b 59,00 ± 1,84c 2,95 ± 0,86ab 285,26 ± 3,86b W 0,04 1,05 5,23 1,04 4,48
Kadar Air
Tabel 2 menunjukkan bahwa kadar air minyak biji mangga yang dihasilkan bersifat fluktuatif berkisar antara 1,25 ± 0,80% - 2,50 ± 0,92%. Minyak yang baik memiliki kadar air kurang dari 0,2%, karena minyak dengan kadar air yang tinggi dapat memperpendek masa umur simpan minyak dan akan menjadi pemicu pertumbuhan mikroba (Toscano, 2007). Kadar air merupakan salah satu parameter uji penting terhadap sifat kimia minyak, karena terkait dengan reaksi hidrolisis. Reaksi tersebut dapat menyebabkan kerusakan minyak, karena adanya kandungan sejumlah air dalam minyak (Ketaren, 1986). Tingginya kadar air dalam minyak biji mangga diduga karena proses penyerapan uap air pada minyak yang dipengaruhi oleh kelembaban udara sekitarnya (Winarno dkk., 1980).
Bilangan Peroksida
Bilangan peroksida merupakan salah satu hal penting dalam menentukan derajat kerusakan pada minyak, asam lemak tidak jenuh dapat mengikat oksigen pada ikatan rangkapnya sehingga membentuk peroksida (Ketaren, 1986). Menurut Ojeh (1981) dalam Kittiphoom (2013) minyak dengan nilai bilangan peroksida yang tinggi bersifat tidak stabil dan akan mudah tengik. Minyak yang baik memiliki kadar bilangan peroksida rendah, sehingga semakin rendah bilangan peroksida semakin baik kualitas minyak (Arlene, 2010).
Tabel 2 menunjukkan bahwa bilangan peroksida antar lama waktu ekstraksi meningkat. Hal ini merupakan suatu indikasi bahwa persenyawaan peroksida bersifat tidak stabil terhadap panas (Ketaren, 1986). Nilai bilangan peroksida yang diperoleh berkisar antara 40,00 ± 4,50 – 59,00 ± 1,84 mgek/kg. Hasil ini lebih tinggi dibandingkan dengan penelitian Kittiphoom (2013) dimana nilai bilangan peroksidanya hanya 8,72 ± 3,4 mg/g minyak. Tingginya bilangan peroksida diduga karena terjadi autooksidasi pada minyak. Autooksidasi merupakan pembentukan radikal bebas pada asam lemak tidak jenuh yang disebabkan oleh faktor-faktor yang mempercepat terjadinya reaksi seperti cahaya dan panas (Winarno, 2004). Dalam penelitian ini, ekstraksi minyak biji mangga dilakukan dengan metoda soxhlet yang menggunakan panas untuk waktu yang relatif panjang yaitu sampai dengan 18 jam, sehingga peluang terjadinya proses autooksidasi sangat besar. Minyak mengalami proses autooksidasi menjadi senyawa peroksida dan
hidroperoksida, namun proses tersebut akan menurun dengan terbentuknya aldehid dan keton pada senyawa tersebut (Ketaren, 1986).
Bilangan Asam
Bilangan asam merupakan ukuran dari jumlah asam lemak bebas dari satu gram minyak atau lemak (Ketaren, 1986). Bilangan asam yang kecil menunjukkan kandungan asam lemak bebasnya cukup kecil dan terjadi sedikit kerusakan (Handayani, 2008). Berdasarkan Tabel 2 tampak bahwa bilangan asam minyak biji mangga bersifat fluktuatif selama waktu ekstraksi.
Berdasarkan hasil penelitian, nilai bilangan asam minyak biji mangga berkisar antara 2,53 ± 0,52 – 5,47 ± 0,85 mg KOH/g minyak. Hasil ini berbeda dengan Kittiphoom (2013) yang melaporkan minyak biji mangga Thailand (Sam Roi Yot Co., ltd) memiliki bilangan asam 0,10 ± 0,012 mg KOH/g minyak. Tingginya bilangan asam diduga karena terjadi reaksi hidrolisis. Reaksi hidrolisis dapat disebabkan oleh lipase yang berasal dari mikroorganisme, serta adanya sejumlah air yang terkandung dalam minyak tersebut. Kandungan air yang tinggi akan menyebabkan minyak mudah terhidrolisis menjadi gliserol dan asam lemak bebas (Ketaren, 1986). Minyak biji mangga yang diperoleh pada penelitian ini mengandung air yang relatif tinggi sehingga peluang terjadinya reaksi hidrolisis relatif besar. Minyak dengan bilangan asam yang kecil mengindikasikan bahwa minyak tersebut memiliki kestabilan yang besar dan bersifat
non irritant bagi kulit (Kurnia, 2014). Bilangan Penyabunan
Tabel 2 menunjukkan bahwa bilangan penyabunan minyak biji mangga antar perlakuan waktu ekstraksi berbeda. Nilai bilangan penyabunan yang diperoleh berkisar antara 282,48 ± 4,07 – 288,22 ± 2,24 mg KOH/g minyak. Nilai bilangan penyabunan dalam penelitian ini relatif tidak jauh berbeda dibandingkan dengan penelitian Kitiphoom (2013) yang mempunyai bilangan penyabunan 207,5 ± 14,2 mg KOH/g minyak. Bilangan penyabunan merupakan jumlah alkali yang dibutuhkan untuk menyabunkan sejumlah sampel minyak atau lemak (Dewi, 2012). Bilangan penyabunan menunjukkan rata-rata massa molekul atau panjang rantai asam lemak bebas (Kittiphoom, 2012). Menurut Ketaren (1986) perbedaan ini dapat disebabkan karena varietas mangga yang digunakan berbeda, perbedaan iklim, serta keadaan tempat tumbuh mangga yang berbeda.
Identifikasi Senyawa Penyusun Minyak Biji Mangga (Mangifera indica L.)
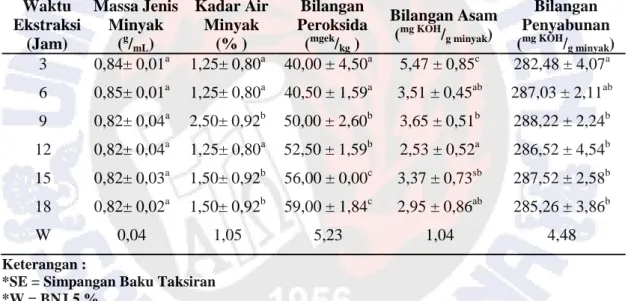
Hasil analisa GCMS ekstrak minyak biji mangga disajikan dalam Gambar 1. Analisa minyak biji mangga dengan GCMS menunjukkan adanya 3 puncak yang muncul pada kromatogram dengan kadar yang berbeda.
Gambar 1. Kromatogram GCMS Minyak Biji Mangga (Mangifera indica L.)
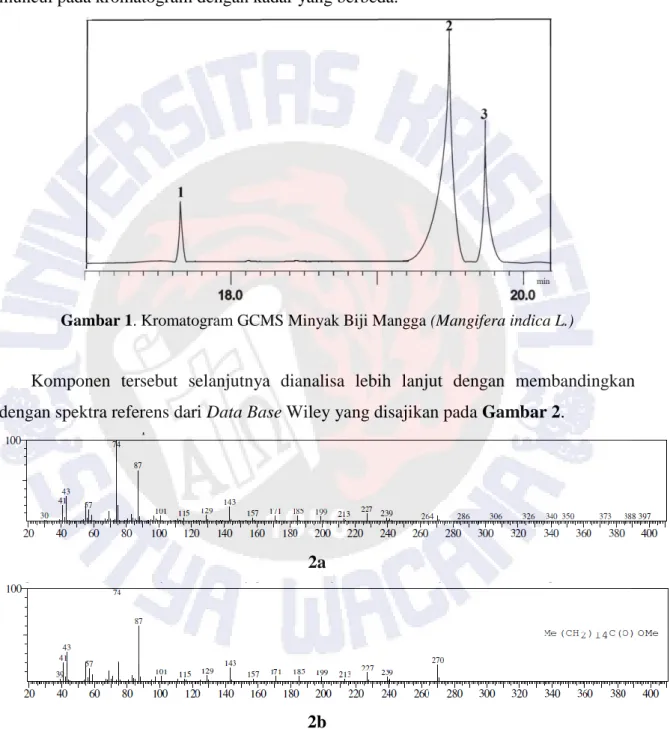
Komponen tersebut selanjutnya dianalisa lebih lanjut dengan membandingkan dengan spektra referens dari Data Base Wileyyang disajikan pada Gambar 2.
2a
2b
Gambar 2. Perbandingan Spektrum Minyak Biji Mangga dengan data base Wiley (2a) Asam Heksadekanoat Minyak Biji Mangga
Spektrum 2a (sampel) merupakan spektrum dari puncak nomor 1 (Gambar 1), dan memiliki fragmentasi yang serupa dengan spektrum 2b (Wiley), yang teridentifikasi sebagai asam heksadekanoat, sehingga dapat disimpulkan bahwa puncak nomor 1 (Gambar 1) merupakan puncak dari asam heksadekanoat.
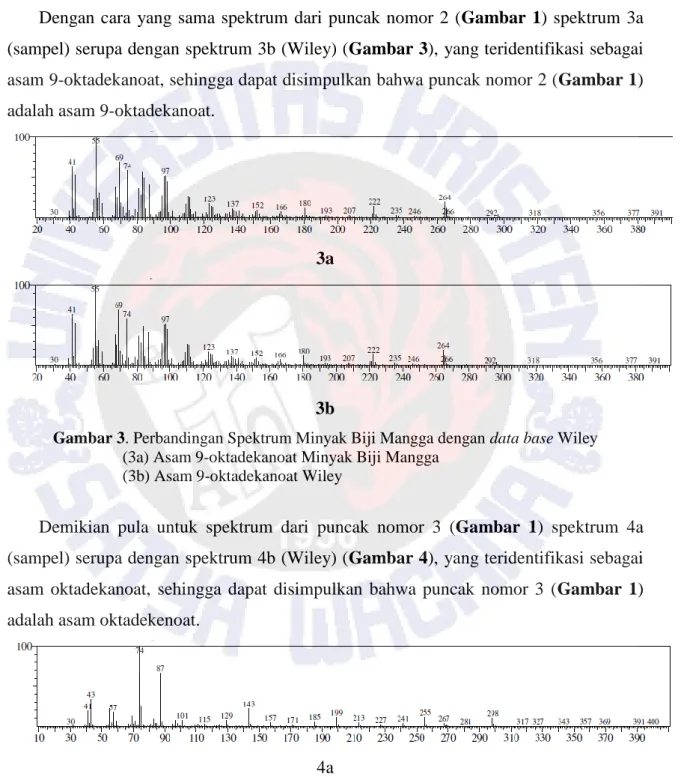
Dengan cara yang sama spektrum dari puncak nomor 2 (Gambar 1) spektrum 3a (sampel) serupa dengan spektrum 3b (Wiley) (Gambar 3), yang teridentifikasi sebagai asam 9-oktadekanoat, sehingga dapat disimpulkan bahwa puncak nomor 2 (Gambar 1) adalah asam 9-oktadekanoat.
3a
3b
Gambar 3. Perbandingan Spektrum Minyak Biji Mangga dengan data base Wiley (3a) Asam 9-oktadekanoat Minyak Biji Mangga
(3b) Asam 9-oktadekanoat Wiley
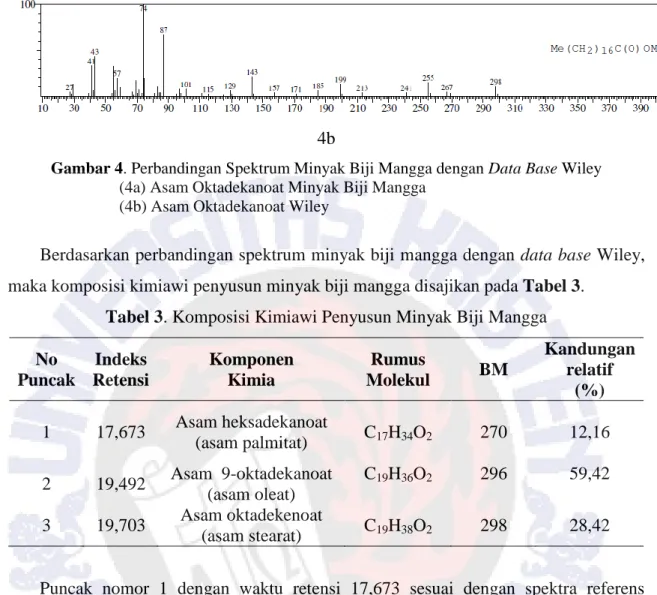
Demikian pula untuk spektrum dari puncak nomor 3 (Gambar 1) spektrum 4a (sampel) serupa dengan spektrum 4b (Wiley) (Gambar 4), yang teridentifikasi sebagai asam oktadekanoat, sehingga dapat disimpulkan bahwa puncak nomor 3 (Gambar 1) adalah asam oktadekenoat.
4b
Gambar 4. Perbandingan Spektrum Minyak Biji Mangga dengan Data Base Wiley (4a) Asam Oktadekanoat Minyak Biji Mangga
(4b) Asam Oktadekanoat Wiley
Berdasarkan perbandingan spektrum minyak biji mangga dengan data base Wiley, maka komposisi kimiawi penyusun minyak biji mangga disajikan pada Tabel 3.
Tabel 3. Komposisi Kimiawi Penyusun Minyak Biji Mangga No Puncak Indeks Retensi Komponen Kimia Rumus Molekul BM Kandungan relatif (%) 1 17,673 Asam heksadekanoat (asam palmitat) C17H34O2 270 12,16 2 19,492 Asam 9-oktadekanoat (asam oleat) C19H36O2 296 59,42 3 19,703 Asam oktadekenoat (asam stearat) C19H38O2 298 28,42
Puncak nomor 1 dengan waktu retensi 17,673 sesuai dengan spektra referens senyawa metil heksadekanoat (gambar 2) dengan kadar 12,16%. Begitupun dengan hasil analisa selanjutnya Selanjutnya puncak nomor 2 dengan waktu retensi 19,408 sesuai dengan spektra referensi senyawa asam 9-oktadekanoat dengan kadar 59,42% dan merupakan senyawa paling dominan dalam minyak biji mangga. Puncak terakhir pada waktu retensi 19,703 sesuai dengan spektra referens asam oktadekanoat dengan kadar 28,42%.
Komponen utama minyak nabati adalah senyawa trigliserida yang merupakan ester asam lemak rantai panjang (Ardiana, 2010). Asam lemak terdiri dari karbon, hidrogen, dan oksigen (Desnelli, 2009). Asam palmitat dan asam stearat merupakan asam lemak jenuh, sedangkan asam lemak oleat termasuk asam lemak tidak jenuh. Asam palmitat, stearat, dan oleat merupakan beberapa asam lemak yang penting dalam ilmu gizi (Nursanyoto, 1993 dalam Desnelli, 2009). Asam palmitat dan stearat berpotensi untuk dijadikan bahan bakar biodiesel berkualitas baik (Ardiana, 2010).
Asam stearat banyak ditemukan pada lemak atau minyak yang berasal dari biji-bijian. Sedangkan asam oleat sendiri sering dikenal dengan asam lemak esensial yang berfungsi untuk membantu proses pertumbuhan dan mampu mempertahankan kesehatan kulit terutama mencegah terjadinya peradangan kulit (Marsetyo, 1991 dalam Desnelli, 2009).
Aktivitas Antibakteri Ekstrak Kloroform Biji Mangga (Mangifera indica L.)
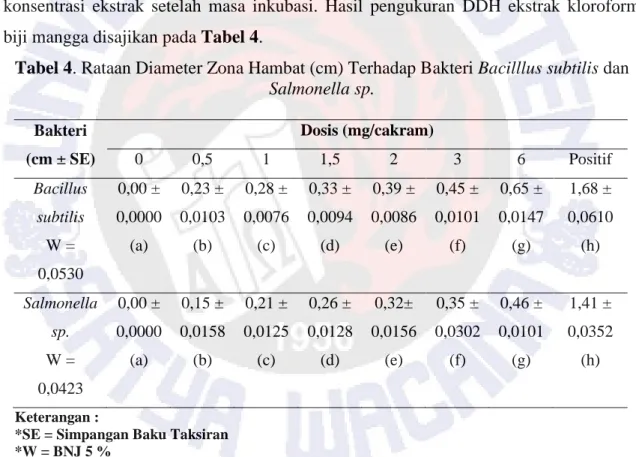
Pengujian aktivitas antibakteri ekstrak kloroform biji mangga dilakukan dengan menggunakan metode difusi agar cakram kertas. Terbentuknya zona terang menunjukkan Daerah Diameter Hambatan (DDH) pada cakram dengan berbagai konsentrasi ekstrak setelah masa inkubasi. Hasil pengukuran DDH ekstrak kloroform biji mangga disajikan pada Tabel 4.
Tabel 4. Rataan Diameter Zona Hambat (cm) Terhadap Bakteri Bacilllus subtilis dan
Salmonella sp. Bakteri (cm ± SE) Dosis (mg/cakram) 0 0,5 1 1,5 2 3 6 Positif Bacillus subtilis 0,00 ± 0,0000 0,23 ± 0,0103 0,28 ± 0,0076 0,33 ± 0,0094 0,39 ± 0,0086 0,45 ± 0,0101 0,65 ± 0,0147 1,68 ± 0,0610 W = 0,0530 (a) (b) (c) (d) (e) (f) (g) (h) Salmonella sp. 0,00 ± 0,0000 0,15 ± 0,0158 0,21 ± 0,0125 0,26 ± 0,0128 0,32± 0,0156 0,35 ± 0,0302 0,46 ± 0,0101 1,41 ± 0,0352 W = 0,0423 (a) (b) (c) (d) (e) (f) (g) (h) Keterangan :
*SE = Simpangan Baku Taksiran *W = BNJ 5 %
*Angka yang diikuti huruf yang tidak sama menunjukkan berbeda nyata sedangkan angka yang diikuti huruf yang sama menunjukkan antar perlakuan tidak berbeda nyata.
Tabel 4 menunjukkan rataan nilai ekstrak kloroform biji mangga arumanis sebagai antibakteri penghambat pertumbuhan bakteri Bacilllus subtilis dan Salmonellasp. Hasil pengukuran rataan zona hambat pada perlakuan kontrol positif menggunakan tetrasiklin memiliki diameter zona hambat sebesar 1,68 ± 0,0610 cm (Bacillus subtilis) dan 1,41 ± 0,0352 cm (Salmonella sp.). Purata penghambatan bakteri (DDH) ekstrak kasar biji mangga ekstrak kloroform dengan dosis 0 sampai 6 mg/cakram terhadap bakteri gram
positif Bacillus subtilis berkisar antara 0,00 ± 0,0000 sampai 0,65 ± 0,0147 cm, sedangkan terhadap bakteri gram negatif Salmonella sp. berkisar antara 0,00 ± 0,0000 sampai 0,46 ± 0,0101 cm.
Pada cawan yang berisi kontrol negatif bakteri tetap tumbuh dengan subur, ini berarti media yang digunakan sesuai untuk pertumbuhan bakteri uji. Sedangkan pada cakram yang berisi tetrasiklin menunjukkan adanya DDH yang cukup kuat yakni memiliki rata-rata DDH 1,68 ± 0,0610 cm terhadap Bacillus subtilis dan 1,41 ± 0,0352 cm untuk Salmonella sp.. Pemilihan tetrasiklin sebagai antibiotik pembanding karena tetrasiklin memiliki sifat antibiotik yang kuat dan spektrum luas (Pelczar dan Chan, 1988).
Tabel 4 menunjukkan bahwa semakin tinggi dosis ekstrak biji mangga, sifat antibakteri penghambat pertumbuhan bakteri Bacilllus subtilis dan Salmonella sp.
semakin besar pula. Hal ini sesuai dengan Pelzar dan Chan (1988) menyatakan semakin tinggi konsentrasi zat antibakteri maka semakin besar kemampuannya untuk mengendalikan penghambat dan membunuh mikroorganisme. Dengan meningkatnya konsentrasi ekstrak berarti semakin besar bahan aktif yang berfungsi sebagai antibakteri (Lathifah, 2008). Besarnya zona hambat dipengaruhi oleh kemampuan difusi senyawa antibakteri pada media, kemampuan difusi yang baik yaitu yang memiliki sifat yang sama dengan media yakni bersifat polar.
Untuk penentuan kategori penghambatan antibakteri dapat dibandingkan dengan Tabel 5.
Tabel 5. Kategori Penghambatan Antibakteri Berdasarkan Diameter Zona Hambat
Diameter (cm) Respon Hambatan
0-0,3 Lemah
0,3-0,6 Sedang
> 0,6 Kuat
Sumber: Pan, Chen, Wu, Tang, and Zhao (2009)
Berdasarkan Tabel 5 dapat diketahui bahwa kekuatan antibakteri ekstrak kloroform biji mangga pada dosis 0,5 – 1 mg termasuk kategori lemah, 1,5 – 3 mg masuk kedalam kategori sedang, dan untuk dosis 6 mg termasuk dalam kategori kuat terhadap bakteri
antibakteri termasuk kedalam kategori lemah dan pada dosis 2 – 6 mg tergolong kedalam kategori sedang.
Aktivitas antibakteri yang dimiliki biji mangga berasal dari unsur-unsur yang terkandung di dalam biji mangga antara lain flavonoid, tanin, steroid, dan saponin (Sahu
et al., 2013). Penghambatan ekstrak biji mangga terhadap Salmonella sp. lebih lemah dibandingkan dengan Bacillus subtilis. Perbedaan penghambatan disebabkan karena adanya perbedaan kepekaan pada struktur dinding sel antara bakteri gram positif dan bakteri gram negatif.
Bakteri gram positif memiliki komponen penyusun dinding sel yang lebih tipis dibandingkan bakteri gram negatif. Latifah (2008) melaporkan bahwa antibakteri diartikan sebagai bahan yang dapat mengganggu pertumbuhan dan metabolisme bakteri, cara kerja antibakteri antara lain dengan merusak dinding sel, merubah permeabilitas sel, menghambat kerja enzim, merubah molekul protein dan asam nukleat, serta menghambat sintesis asam nukleat dan protein. Oleh sebab itu ketahanan bakteri gram positif lebih lemah dibandingkan bakteri gram negatif.
Branen dan Davidson (1993) menyatakan bahwa bakteri gram negatif mempunyai sistem seleksi terhadap zat aktif yaitu pada lapisan lipopolisakarida. Menurut Pelczar dan Chan (1988) struktur dinding sel bakteri gram negatif lebih kompleks, lapisan luar berupa lipoprotein, lapisan tengah berupa lipopolisakarida, dan lapisan paling dalam adalah peptidoglikan. Sedangkan dinding sel pada bakteri gram positif lebih sederhana sehingga memudahkan senyawa antibakteri untuk berdifusi dan menembus membran sel.
KESIMPULAN
Berdasarkan hasil penelitian maka dapat disimpulkan bahwa:
1) Hasil minyak biji mangga (Mangifera indica L.) paling optimal sebesar 19,31 ± 0,76 % dalam waktu ekstraksi 15 jam.
2) Lama waktu ekstraksi berpengaruh terhadap rendemen, kadar air minyak (terendah pada lama waktu ekstraksi ke 3 jam sebesar 1,25± 0,80%), bilangan peroksida (terendah pada lama ekstraksi ke 3 jam sebesar 40,00 ± 4,50 mgek/kg), bilangan asam (terendah pada lama waktu ekstraksi ke 12 jam sebesar 2,53 ± 0,52 mg KOH/g minyak), dan bilangan penyabunan (tertinggi pada lama ekstraksi ke 9 sebesar 288,22 ± 2,24
mg KOH
/g minyak), sebaliknya tidak berpengaruh terhadap massa jenis minyak biji mangga.
3) Komposisi penyusun minyak biji mangga tersusun atas 3 komponen kimiawi yaitu asam 9-oktadekenoat 59,42%, asam oktadekenoat 28,42%, dan asam heksadekanoat 12,16%.
4) Aktivitas antibakteri ekstrak kloroform biji mangga memiliki purata penghambatan bakteri (DDH) dengan dosis 0 sampai 6 mg/cakram terhadap bakteri gram positif
Bacillus subtilis berkisar antara 0,00 ± 0,0000 sampai 0,65 ± 0,0147 cm, sedangkan terhadap bakteri gram negatif Salmonella sp. berkisar antara 0,00 ± 0,0000 sampai 0,46 ± 0,0101 cm.
SARAN
1. Diperlukan penelitian lebih lanjut untuk meningkatkan kualitas minyak biji mangga agar dapat diaplikasikan.
DAFTAR PUSTAKA
Ali, S. 2010. Biji Mangga Sebagai Bahan Baku Produksi Dekstrin. Jurnal Penelitian Ilmu Teknik, 10 (1), pp. 6-10.
Alim, A., 2009. Antimicrobial activity of the essential oil of Cyclotrichium niveum (Boiss.) Manden. Et Scheng. Microbiology Research, III(8), p.423.
Ardiana, D. S. dan S. Saktika, 2010. Pembuatan biodiesel dari Asam Lemak Jenuh Biji Karet. Prosiding Seminar Rekayasa Kimia dan Proses 2010 Jurusan Teknik Kimia Fakultas Teknik, Universitas Diponegoro Semarang.
Arlene, Ariestya., Steviana, K., dan Ign Suharto. (2010). Pengaruh Temperatur dan F/S terhadap Ekstraksi Minyak dari Biji Kemiri Sisa Penekanan Mekanik. Seminar Nasional Rekayasa Kimia dan Proses. Universitas Diponegoro Semarang.
Badan Standarisasi Nasional Indonesia. SNI 01-3555-1998: Cara Uji Lemak dan Minyak . Jakarta: Badan Standarisasi Nasional Indonesia.
Brannen, L. A., dan Davidson P. M., 1993. Antimicrobial in Food. Marcell Dekker, Inc., New York.
Dewi, R. K. 2012. Studi Awal Pemanfaatan Minyak Biji Mangga (Mangifera indica L. var Arumnis) Sebagai Bahan Pembuatan Lotion. Skripsi. Fakultas Sains dan Matematika, Universitas Kristen Satya Wacana, Salatiga.
Desnelli. dan Z. Fanani. 2009. Kinetika Reaksi Oksidasi Asam Miristat, Atearat, dan Oleat dalam Medium Minyak Kelapa, Minyak Kelapa Sawit, serta Tanpa Medium.
Jurnal Penelitian Sains, 12 (1), pp. 12107-1 – 12107-6.
Handajani, S., Godras & Baskara, 2010. Pengaruh Suhu Ekstraksi Terhadap Karakteristik Fisik, Kimia, dan Sensoris Minyak Wijen (Sesamum indicum L.).
Majalah Agritech, Vol. 30, No 2.
Harborne, J. B. 1987. Metode Fitokimia. ITB : Bandung.
Ketaren S. 1986. Minyak dan Lemak Pangan, Ed. 1. Jakarta: UI-Press.Prapti , C. M., Wiwik & A. Fatoni, 2011. Perbandingan Minyak Nabati Kasar Hasil Ekstraksi Buah Kepayang Segar dengan Luwek. Prosiding Seminar Nasional VoER ke-3, hal 471-481, Universitas Sriwijaya, Palembang, 26-27 Oktober 2011.
Kittiphoom, S. 2012. Utilization of Mango Seed. International Food Research Journal, 19 (4), pp. 1312-1335.
Kittiphoom, S., Sutasinee, S. 2013. Mango seed kernel oil and its physic chemical properties. International Food Research Journal, 20 (3), pp.1145-1149.
Kurnia , M. D., Hartati & A. Ign. Kristijanto, 2014. Karakterisasi dan Komposisi Kimia Minyak Biji Tumbuhan Kupu-kupu (Bauhinia purpurea L.) Bunga Merah Muda. Prosiding Seminar Nasional Sains dan Pendidikan Sains IX, hal 11-17, Universitas Kristen Satya Wacana, Salatiga, 21 Juni 2014.
Lathifah, Q. 2008. Uji Efektifitas Ekstrak Kasar Senyawa Antibakteri pada Buah Belimbing Wuluh (Averrhoa bilimbi L.) dengan Variasi Pelarut. Jurusan Kimia Fakultas Sains dan Teknologi.Universitas Islam Negeri (UIN) Malang.
Nasiyah, S. 2009. Uji Aktivitas Antibakteri dari Ekstrak n-Heksana dan Etanol Daun Sirih (Piper betle Linn.) serta identifikasi Senyawa Aktifmya. Skripsi. Fakultas Sains dan Teknologi, UIN Sunan Kalijaga, Yogyakarta.
Nichols, D.S. dan K. Sanderson, 2003. The Nomenclature, Structure, and Properties of Food Lipids. In: Sikorski, Z.E and A. Kolakowska, Ed. Chemical and Functional Properties of Food Lipids. CRC Press Washington. Pp. 29-59.
Pan, X., Chen, F., Wu, T., Tang, H., and Zhao, Z. 2009. The acid, Bile Tolerance and Antimicrobial property of Lactobacillus acidophilus NIT. J. Food Control 20 : 598-602.
Pleczar M J, dan S Chan, 1988. Dasar-dasar Mikrobiologi 2, Indonesia University Press, Jakarta.
Prapti , C. M., Wiwik & A. Fatoni, 2011. Perbandingan Minyak Nabati Kasar Hasil Ekstraksi Buah Kepayang Segar dengan Luwek. Prosiding Seminar Nasional VoER ke-3, hal 471-481, Universitas Sriwijaya, Palembang, 26-27 Oktober 2011.
Sahu, S., B. Kumar., B. Kumar, 2013. Multiple Antibacterial and Phytochemical Analysis of Mango Kernel Extracts on Aquatic and Animal Pathogens.
International Journal of Pharm and Bio Sciences, 4 (2), pp. 809-818.
Sajarwo, G., Mahasiswa UGM Ciptakan Es Biji Mangga Kaya Antioksidan. 2012, http://health.kompas.com/read/2012/05/15/14494957/Mahasiwa.UGM.Ciptakan.Es.Biji.Mangga. Kaya.Antioksidan. (11 Maret 2015).
Steel, R.G.D dan J.H. Torrie, 1989. Prinsip dan Prosedur Statistika. PT. Gramedia, Jakarta.
Sudarmadji, S., B. Haryono dan Suhandi. 1997. Prosedur untuk Analisa Bahan Makanan dan Pertanian. Yogyakarta: Penerbit Liberty.
Sultan, R., Massa jenis. 2013, http://sijagofisika.blogspot.com/2013/02/massa-jenis.html, (10 Maret 2015)
Toscano, G. And E. Maldini, “Analysis of The Physical and Chemical Characteristics of Vegetable Oils as Fuel”. J. Of Ag. Eng. Vol 3, pp. 39-47, 2007.
Utama, I. M., Y. Setiyo., I. Ayu Rina & N. S. Antara, 2011. Kajian Atmosfir Terkendali untuk Memperlambat Penurunan Mutu Buah Mangga Arumanis selama
Penyimpanan. J. Hort. Indonesia, 2 (1), pp. 27-33.
Wibowo, D. 2013. Kombinasi Metode Spektrofotometri Inframerah dan Kalibrasi Multivariat untuk Autentikasi Minyak Biji Jinten Hitam. Skripsi.Fakultas Famasi, Universitas Gajah Mada Yogyakarta.
Winarno, F. G., Srikandi Fardiaz, dan Dedi Fardiaz, 1980, Pengantar Teknologi Pangan, P.T. Gramedia, Jakarta.
LAMPIRAN
I
MAKALAH SEMINAR I
SN-KPK VII 2015
UNS, SURAKARTA
18 APRIL 2015
arum manis. Berbagai macam cara atau metode dapat digunakan untuk
memperoleh minyak nabati dari berbagai sumber. Salah satu cara dengan hasil terbaik adalah dengan menggunakan metode ekstraksi soxhlet
dengan pelarut organik. Penelitian ini bertujuan untuk:
1. Menentukan optimasi ekstraksi minyak biji mangga menggunakan metoda ekstraksi pelarut n-heksana ditinjau dari lama ekstraksi.
2. Menentukan sifat fisiko-kimiawi minyak biji mangga meliputi: warna, aroma, rendemen, massa jenis, kadar air, bilangan peroksida, bilangan asam, dan bilangan penyabunan.
METODE PENELITIAN Bahan dan alat
Biji buah mangga Indonesia (Mangifera indica L.) jenis arumanis diperoleh dari pedagang buah-buahan di wilayah Salatiga dan sekitarnya. Bahan kimiawi yang digunakan adalah n-heksana (teknis), etanol (pro analysis, Merck), kloroform (pro analysis, Merck), asam asetat glasial (Merck), asam klorida (Merck), akuades, kanji, natrium tiosulfat (Merck), indikator fenolftalein (Merck), natrium hidroksida (Merck),
digunakan yaitu jenis mangga arum manis. Berbagai macam cara atau metode dapat digunakan untuk memperoleh minyak nabati dari berbagai sumber. Salah satu cara dengan hasil terbaik adalah dengan menggunakan metode ekstraksi soxhlet dengan pelarut organik. Penelitian ini bertujuan untuk:
3. Menentukan optimasi ekstraksi minyak biji mangga menggunakan metoda ekstraksi pelarut n-heksana ditinjau dari lama ekstraksi.
4. Menentukan sifat fisiko-kimiawi minyak biji mangga meliputi: warna, aroma, rendemen, massa jenis, kadar air, bilangan peroksida, bilangan asam, dan bilangan penyabunan.
METODE PENELITIAN Bahan dan alat
Biji buah mangga Indonesia (Mangifera indica L.) jenis arumanis diperoleh dari pedagang buah-buahan di wilayah Salatiga dan sekitarnya. Bahan kimiawi yang digunakan adalah n-heksana (teknis), etanol (pro analysis, Merck), kloroform (pro analysis, Merck), asam asetat glasial (Merck), asam klorida (Merck), akuades, kanji, natrium tiosulfat (Merck), indikator fenolftalein (Merck), natrium hidroksida (Merck), kalium iodida (pra kristal, Merck), kalium hidroksida (Merck).
Piranti yang digunakan antara lain moisturizer balance (Ohaus TAJ602, Ohaus Corp, USA), soxhlet, penangas air (Memmert., Germany), neraca analitik 4 digit (Metler H 80, Mettler Instrument Corp., USA), neraca analitik 2 digit (Ohaus
TAJ602, Ohaus Corp., USA), drying
cabinet, rotary evaporator (Buchi R0114,
Swiss), grinder, buret, dan peralatan gelas.
Metode
Preparasi sampel
Biji mangga (Mangifera indica L.) yang telah dicuci bersih dan dibebaskan dari selaput pembungkusnya, dipotong tipis-tipis dan dikeringkan dengan drying cabinet dengan suhu 50ºC selama 5 jam. Kemudian biji dihaluskan dengan grinder dan disimpan dalam wadah yang tertutup rapat.
Ekstraksi minyak biji mangga ([6], dimodifikasi)
Sebanyak 100 gram serbuk biji mangga diekstraksi menggunakan soxhlet dengan pelarut n-heksana sebanyak 400 mL dengan variasi waktu 3; 6; 9; 12; 15; dan 18 jam pada suhu 80ºC. Hasil ekstraksi dipekatkan dengan rotary evaporator pada suhu 50-60°C. Minyak hasil ekstraksi dipindahkan ke dalam botol sampel yang telah ditimbang lalu disimpan pada suhu 20°C sampai siap untuk dianalisis lebih lanjut.
Penentuan Sifat Fisiko-Kimiawi Minyak Biji Mangga
Penentuan aroma dan warna ditentukan dengan pemaparan secara deskriptif, rendemen, massa jenis, penentuan kadar air, bilangan peroksida (SNI 01-3555-1998), bilangan asam (SNI 01-3555-1998), dan bilangan penyabunan (SNI 01-3555-1998).
Analisa Data
Data rendemen minyak biji mangga dianalisis dengan rancangan dasar Rancangan Acak Kelompok (RAK) 6
perlakuan dan 4 kali ulangan. Sebagai perlakuan adalah lama waktu ekstraksi yaitu 3; 6; 9; 12; 15; dan 18 jam, sedangkan sebagai kelompok adalah waktu analisis. Pengujian antar rataan perlakuan dilakukan dengan uji Beda Nyata Jujur (BNJ) dengan tingkat kebermaknaan 5% [7].
HASIL DAN PEMBAHASAN
Minyak biji mangga yang dihasilkan berwarna kuning kecoklatan dengan aroma manis buah mangga. Warna kuning kecoklatan disebabkan oleh zat warna xanthofil yang secara alamiah ikut terekstrak bersama minyak pada saat proses ekstraksi [8].
Rendemen
Hasil rataan rendemen dan sifat fisiko kimia minyak biji mangga (Mangifera indica L.) yang dihasilkan antar lama waktu ekstraksi disajikan pada Tabel 1. Pada Tabel 1 tampak rendemen minyak biji mangga tidak mengalami peningkatan untuk lama ekstraksi 3 sampai 9 jam. Peningkatan rendemen terjadi ketika ekstraksi diperpanjang menjadi 12 dan 15 jam. Pada ekstraksi selama 18 jam tidak meningkat lagi rendemen minyak yang dihasilkan. Peningkatan rendemen ekstrak seiring dengan lama waktu sampai dengan 15 jam diduga karena pada waktu ekstraksi yang relatif singkat, masih banyak molekul minyak yang terperangkap dalam jaringan sel [9]. Sedangkan pada lama waktu ekstraksi 15 jam semua minyak telah terekstrak, sehingga sampai lama waktu 18 jam sudah tidak ada peningkatan lagi.
Massa Jenis
Massa jenis merupakan pengukuran massa setiap satuan volume benda. Semakin tinggi besarnya massa jenis benda, maka semakin besar pula massa setiap volumenya. Minyak memiliki massa jenis sebesar 0,8 g/mL [10]. Berdasarkan penelitian yang dilakukan, massa jenis minyak biji mangga berkisar antara 0,82 ± 0,04 – 0,85 ± 0,01 g/mL dan lama pemanasan tidak berpengaruh terhadap massa jenis minyak (Tabel 2). Setiap jenis minyak mempunyai massa jenis yang khas, tergantung pada jenis asam lemak penyusun minyak tersebut [11].
Kadar Air
Tabel 2. menunjukkan bahwa kadar air minyak biji mangga yang dihasilkan bersifat fluktuatif, berkisar antara 1,25 ± 0,80% - 2,50 ± 0,92% dan relatif tinggi jika dibandingkan dengan kriteria minyak yang baik, yaitu kandungan air kurang dari 0,2% [12]. Kadar air merupakan salah satu parameter uji yang penting terhadap sifat kimia minyak, karena terkait dengan reaksi hidrolisis. Reaksi tersebut dapat menyebabkan kerusakan minyak, karena adanya kandungan sejumlah air dalam minyak [8]. Minyak dengan kadar air yang tinggi dapat memperpendek masa umur simpan minyak dan akan memicu pertumbuhan mikroba [12].
Bilangan Peroksida
Bilangan peroksida juga merupakan salah satu hal penting dalam menentukan derajat kerusakan pada minyak. Asam lemak tidak jenuh dapat mengikat oksigen pada ikatan rangkapnya sehingga
membentuk peroksida [8]. Menurut Ojeh (1981) dalam [13] minyak dengan nilai bilangan peroksida yang tinggi bersifat tidak stabil dan akan mudah tengik. Minyak yang baik memiliki kadar bilangan peroksida rendah, sehingga semakin rendah bilangan peroksida semakin baik kualitas minyak [14].
Tabel 2. menunjukkan bahwa bilangan peroksida antar lama waktu ekstraksi meningkat. Hal ini merupakan suatu indikasi bahwa persenyawaan peroksida bersifat tidak stabil terhadap panas [8]. Nilai bilangan peroksida yang diperoleh berkisar antara 40,00 ± 4,50 – 59,00 ± 1,84 mgek/kg. Hasil ini lebih tinggi dibandingkan dengan penelitian Kittiphoom (2013), dimana nilai bilangan peroksida minyak biji mangga Thailand (Sam Roi Yot Co., ltd) hanya 8,72 ± 3,4 mg/g minyak. Tingginya bilangan peroksida diduga karena terjadinya autooksidasi pada minyak. Autooksidasi merupakan pembentukan radikal bebas pada asam lemak tidak jenuh yang disebabkan oleh faktor-faktor yang mempercepat reaksi seperti cahaya dan panas [15]. Dalam penelitian ini, ekstraksi minyak biji mangga dilakukan dengan metoda soxhlet yang menggunakan panas untuk waktu yang relatif panjang yaitu sampai dengan 18 jam, sehingga peluang terjadinya proses autooksidasi sangat besar. Minyak mengalami proses autooksidasi menjadi senyawa peroksida dan hiperperoksida, namun proses tersebut akan menurun dengan terbentuknya aldehid dan keton pada senyawa tersebut [8].
Bilangan Asam
Tabel 2. menunjukkan bahwa bilangan asam minyak biji mangga berfluktuasi selama ekstraksi. Nilai bilangan asam minyak biji mangga berkisar antara 2,53 ± 0,52 – 5,47 ± 0,85 mg KOH
/g minyak. Hasil ini berbeda dengan Kittiphoom (2013) yang melaporkan minyak biji mangga Thailand (Sam Roi Yot Co., ltd) memiliki bilangan asam 0,10 ± 0,012 mg KOH/g minyak. Bilangan asam merupakan ukuran dari jumlah asam lemak bebas dari satu gram minyak atau lemak [8]. Bilangan asam yang kecil menunjukkan kandungan asam lemak bebasnya cukup kecil dan terjadi sedikit kerusakan [16]. Tingginya bilangan asam diduga karena terjadi reaksi hidrolisis. Reaksi hidrolisis dapat disebabkan oleh lipase yang berasal dari mikroorganisme, serta adanya sejumlah air yang terkandung dalam minyak tersebut. Kandungan air yang tinggi akan menyebabkan minyak mudah terhidrolisis menjadi gliserol dan asam lemak bebas [8]. Minyak biji mangga yang diperoleh pada penelitian ini mengandung air yang relatif tinggi sehingga peluang terjadinya reaksi hidrolisis relatif besar. Minyak dengan bilangan asam yang kecil mengindikasikan bahwa minyak tersebut memiliki kestabilan yang besar dan bersifat non irritant bagi kulit [17].
Bilangan Penyabunan
Tabel 2. menunjukkan bahwa bilangan penyabunan minyak biji mangga antar perlakuan waktu ekstraksi berbeda. Nilai bilangan penyabunan yang diperoleh berkisar antara 282,48 ± 4,07 – 288,22 ± 2,24 mg KOH/g minyak. Nilai bilangan penyabunan dalam penelitian ini relatif
berbeda dibandingkan dengan penelitian Kitiphoom (2013) yang mempunyai bilangan penyabunan 207,5 ± 14,2 mg KOH/g
minyak. Bilangan penyabunan merupakan
jumlah alkali yang dibutuhkan untuk menyabunkan sejumlah sampel minyak atau lemak [6]. Bilangan penyabunan menunjukkan rata-rata massa molekul atau panjang rantai asam lemak bebas [18]. Menurut Ketaren (1986) perbedaan ini disebabkan karena varietas yang digunakan berbeda, perbedaan iklim, serta keadaan tempat tumbuh [8].
KESIMPULAN
Berdasarkan penelitian yang telah dilakukan maka dapat disimpulkan bahwa: 1. Hasil penelitian menunjukkan rendemen
minyak tertinggi dihasilkan pada soxhletasi selama 15 jam yaitu 19,31 ± 0,42%.
2. Lama waktu ekstraksi berpengaruh terhadap rendemen, kadar air minyak, bilangan peroksida, bilangan asam, dan bilangan penyabunan. Namun, tidak berpengaruh terhadap massa jenis minyak biji mangga.
3. Massa jenis tertinggi terdapat pada lama waktu ekstraksi ke 6 jam sebesar 0,85± 0,01 g/mL, kadar air terendah pada lama waktu ekstraksi ke 3; 6; dan 12 jam yaitu sebesar 1,25± 0,80%, bilangan peroksida terendah pada lama ekstraksi ke 3 jam sebesar 40,00 ± 4,50 mgek/kg, bilangan asam terendah pada lama waktu ekstraksi ke 12 jam sebesar 2,53 ± 0,52 mg KOH/g minyak, dan bilangan penyabunan tertinggi pada lama
ekstraksi ke 9 sebesar 288,22 ± 2,24 mg KOH
/g minyak.
DAFTAR RUJUKAN
[1] Prapti , C. M., Wiwik & A. Fatoni, 2011.
Perbandingan Minyak Nabati Kasar
Hasil Ekstraksi Buah Kepayang Segar dengan Luwek. Prosiding Seminar Nasional VoER ke-3, hal 471-481, Universitas Sriwijaya, Palembang, 26-27 Oktober 2011.
[2] Wibowo, D. 2013. Kombinasi Metode
Spektrofotometri Inframerah dan
Kalibrasi Multivariat untuk Autentikasi
Minyak Biji Jinten Hitam.
Skripsi.Fakultas Famasi, Universitas Gajah Mada Yogyakarta.
[3] Utama, I. M., Y. Setiyo., I. Ayu Rina & N. S. Antara, 2011. Kajian Atmosfir Terkendali untuk Memperlambat Penurunan Mutu Buah Mangga Arumanis selama Penyimpanan. J. Hort. Indonesia, 2 (1), pp. 27-33.
[4] Sajarwo, G., Mahasiswa UGM Ciptakan Es Biji Mangga Kaya Antioksidan. 2012,
http://health.kompas.com/read/2012/05/15/1 4494957/Mahasiwa.UGM.Ciptakan.Es.Biji. Mangga.Kaya.Antioksidan. (11 Maret 2015).
[5] Ali, S. 2010. Biji Mangga Sebagai Bahan Baku Produksi Dekstrin. Jurnal Penelitian Ilmu Teknik , 10 (1), pp. 6-10.
[6] Dewi, R. K. 2012. Studi Awal Pemanfaatan Minyak Biji Mangga (Mangifera indica L. var Arumnis) Sebagai Bahan Pembuatan Lotion.
Skripsi. Fakultas Sains dan Matematika, Universitas Kristen Satya Wacana, Salatiga.
[7] Steel, R.G.D dan J.H. Torrie, 1989. Prinsip dan Prosedur Statistika. PT. Gramedia, Jakarta.
[8] Ketaren S. 1986. Minyak dan Lemak Pangan, Ed. 1. Jakarta: UI-Press.
[9] Handajani, S., Godras & Baskara, 2010. Pengaruh Suhu Ekstraksi Terhadap Karakteristik Fisik, Kimia,
dan Sensoris Minyak Wijen
(Sesamum indicum L.). Majalah
Agritech, Vol. 30, No 2.
[10] Sultan, R., Massa jenis. 2013,
diunduh dari
http://sijagofisika.blogspot.com/2013/ 02/massa-jenis.html, (10 Maret 2015)
[11] Nichols, D.S. dan K. Sanderson, 2003. The Nomenclature, Structure, and Properties of Food Lipids. In: Sikorski, Z.E and A. Kolakowska, Ed. Chemical and Functional Properties of Food Lipids. CRC Press Washington. Pp. 29-59
[12] Toscano, G. And E. Maldini, “Analysis
of The Physical and Chemical Characteristics of Vegetable Oils as Fuel”. J. Of Ag. Eng. Vol 3, pp. 39-47, 2007.
[13] Kittiphoom, S., Sutasinee, S. 2013. Mango seed kernel oil and its physic chemical properties. International Food Research Journal, 20 (3), pp.1145-1149.
[14] Arlene, Ariestya., Steviana, K., dan Ign Suharto. (2010). Pengaruh
Temperatur dan F/S terhadap
Ekstraksi Minyak dari Biji Kemiri Sisa
Penekanan Mekanik. Seminar
Nasional Rekayasa Kimia dan Proses. Universitas Diponegoro Semarang
[15] Winarno F.G. 2004. Kimia Pangan dan Gizi. PT Gramedia Pustaka Utama.Jakarta
[16] Handayani, M, Putri., dan Subagus, W. 2008. Analisis Biji Ketapang (Terminalia catappa L.) sebagai suatu Alternatif Sumber Minyak Nabati. Majalah Obat Tradisional, Vol. 13, No. 45.
[17] Kurnia , M. D., Hartati & A. Ign. Kristijanto, 2014. Karakterisasi dan Komposisi Kimia Minyak Biji Tumbuhan Kupu-kupu (Bauhinia purpurea L.) Bunga Merah Muda. Prosiding Seminar Nasional Sains dan Pendidikan Sains IX, hal 11-17, Universitas Kristen Satya Wacana, Salatiga, 21 Juni 2014.
[18] Kittiphoom, S. 2012. Utilization of Mango Seed. International Food Research Journal, 19 (4), pp. 1312-1335.
Lampiran 1
Tabel 1. Rataan Rendemen (% ± SE)Minyak Biji Mangga antar Lama Waktu Ekstraksi
Tabel 2. Rataan Sifat Fisiko-Kimia Minyak Biji Mangga antar Lama Waktu Ekstraksi
Keterangan : *SE = Simpangan Baku Taksiran *W = BNJ 5 %
*Angka yang diikuti huruf yang tidak sama menunjukkan berbeda nyata sedangkan angka yang diikuti huruf yang sama menunjukkan antar perlakuan tidak berbeda nyata.
Waktu Ekstraksi 3 6 9 12 15 18 Rendemen ± SE 7,70 ± 0,09 (a) 8,13 ± 0,47 (a) 8,68 ± 1,33 (a) 11,51 ± 2,04 (b) 19,31 ± 0,76 (c) 19,03 ± 0,51 (c) W 1,57 Waktu Ekstraksi (Jam) Massa Jenis Minyak (g/mL ± SE) Kadar Air Minyak (% ± SE) Bilangan Peroksida (mgek/kg ± SE) Bilangan Asam (mg KOH/g minyak ± SE) Bilangan Penyabunan (mg KOH/g minyak ± SE) 3 0,84± 0,01a 1,25± 0,80a 40,00 ± 4,50a 5,47 ± 0,85c 282,48 ± 4,07a 6 0,85± 0,01 a 1,25± 0,80a 40,50 ± 1,59a 3,51 ± 0,45ab 287,03 ± 2,11ab 9 0,82± 0,04 a 2,50± 0,92b 50,00 ± 2,60b 3,65 ± 0,51b 288,22 ± 2,24b 12 0,82± 0,04 a 1,25± 0,80a 52,50 ± 1,59b 2,53 ± 0,52a 286,52 ± 4,54b 15 0,82± 0,03 a 1,50± 0,92b 56,00 ± 0,00c 3,37 ± 0,73sb 287,52 ± 2,58b 18 0,82± 0,02 a 1,50± 0,92b 59,00 ± 1,84c 2,95 ± 0,86ab 285,26 ± 3,86b W 0,04 1,05 5,23 1,04 4,48