i SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm)
Program Studi Ilmu Farmasi
Diajukkan oleh : Lina NIM : 058114081
FAKULTAS FARMASI UNIVERSITAS SANATA DHARMA
ii
PERSETUJUAN PEMBIMBING
STANDARISASI EKSTRAK RIMPANG KUNYIT
(
Curcuma domestica
Val.)
Yang diajukan oleh : Lina
NIM : 058114081
iii
Oleh :
Lina NIM : 058114081
Dipertahankan di hadapan Panitia Penguji Skripsi Fakultas Farmasi
Universitas Sanata Dharma pada tanggal : 10 Januari 2009
Panitia Penguji :
1. Yohanes Dwiatmaka, M.Si. 2. Erna Tri Wulandari, M.Si., Apt. 3. Yustina Sri Hartini, M. Si, Apt.
iv
HALAMAN PERSEMBAHAN
“
Berbahagialah orang yang mendapat hikmat, orang yang memperoleh
kepandaian karena keuntungannya melebihi keuntungan perak dan
hasilnya melebihi emas”
(Amsal 3 : 13 – 14)Kupersembahkan untuk :
Mama dan papaku tercinta yang telah mendukungku
Andreas R. Tan Wijaya dan Theresa Oktavia, adik-adikku tersayang
vi PRAKATA
Puji dan syukur kepada Allah Yang Maha Pengasih atas berkat dan kasih-Nya sehingga penulis dapat menyelesaikan skripsi yang berjudul “ Standarisasi Ekstrak Rimpang Kunyit (Curcuma domesticaVal.) “.
Skripsi ini disusun sebagai salah satu syarat untuk mencapai gelar sarjana farmasi pada Fakultas Farmasi Universitas Sanata Dharma.
Penulisan skripsi ini terwujud berkat bimbingan dan pengarahan serta bantuan dari banyak pihak, maka pada kesempatan ini penulis menyampaikan banyak terima kasih kepada :
1. Ibu Rita Suhadi, M.Si., Apt. selaku Fakultas Farmasi Universitas Sanata Dharma, Yogyakarta.
2. Bapak Yohanes Dwiatmaka, M.Si. selaku dosen pembimbing yang telah memberikan bimbingan dan pengarahan baik selama penelitian maupun penyusunan skripsi.
3. Ibu Erna Tri Wulandari, M. Si, Apt selaku dosen penguji yang telah memberikan saran dan perhatian baik selama pengujian dan perbaikan skripsi.
vii
6.
Orang-orang terdekat yaitu keluarga terutama orang tua yang telah memberikan dukungan moril dan materil yang sangat berarti bagi penulis.7.
Sahabatku yaitu Sekar, Anna, Tami, Nolen, dan Mba Iponk yang telahmemberi dukungan kepada penulis selama perkuliahan dan penyelesaian skripsi ini.
8.
Teman-temanku yaitu Bustan, Yesi, Ika, Siska, Dewi, dan Wisely yang telah membantu dan bekerja sama dalam penelitian dan penyelesaian skripsi ini.9.
Teman-teman kelas A FKK 2005 khususnya kelompok B dan semua pihak yang telah membantu dalam penyusunan skripsi ini.Penulis menyadari bahawa masih banyak kekurangan dalam penelitian dan penyusunan skripsi ini, oleh karena itu penulis sangat mengharapkan kritik dan saran dari berbagai pihak. Akhirnya penulis berharap semoga skripsi ini dapat bermanfaat bagi perkembangan ilmu pengetahuan khususnya bidang farmasi dan bagi masyarakat.
viii
PERNYATAAN KEASLIAN KARYA
Saya menyatakan bahwa sesungguhnya skripsi yang saya tulis ini tidak memuat karya atau bagian orang lain, kecuali yang telah disebutkan dalam kutipan dan daftar pustaka, sebagaimana layaknya karya ilmiah.
ix
salah satu bahan penyusun “Jamu Kunyit Asam” sehingga perlu dilakukan suatu standarisasi ekstrak rimpang kunyit untuk memenuhi persyaratan sebagai produk kefarmasian yaitu aman, mutu, dan manfaat.
Tujuan penelitian ini adalah untuk mengetahui hasil identifikasi dan pengukuran beberapa parameter standar ekstrak rimpang kunyit yang diteliti dan untuk mengetahui kesesuaian hasil identifikasi dan pengukuran beberapa parameter standar ekstrak rimpang kunyit yang diteliti dengan persyaratan yang tercantum dalam Monografi Ekstrak Tumbuhan Obat Indonesia.
x ABSTRACT
Turmeric rhizome (Curcuma domestica Val.) has been used by people as traditional medicine for generations. One of the active substances in turmeric rhizome is curcuminoid. Turmeric rhizome is one of the materials in making “Sour Turmeric Tonic”, so the standardization of the turmeric rhizome extract is necessary to fulfill the requirement as the product of pharmacy that is save, qualify and useful.
This research aims to find out the results of the identification and measuring several standard parameter of turmeric rhizome extract and to find out the compatibility between the results from the identification and measuring of several standard parameter of turmeric rhizome extract with the requirement of the extract on the Indonesian Herbs Medicine Extract Monographic.
This was a non experimental research. The material analyzed was the extract of turmeric rhizome. The research step included the identification (the assessment and the check of curcuminoid identity compound by Thin Layer Chromatography), the purity test (the determination of total ashes degree and acid dissoluble ashes degree), the determination of curcuminoid degree, volatile oil degree and water degree from the turmeric rhizome extract.
The result of turmeric rhizome extract organoleptic assessment was compatible with the Indonesian Herbs Medicine Extract Monographic. The identification of chemical content showed that turmeric rhizome extract contained curcuminoid. The purity test showed that the ashes degree was 0.32% and the acid dissoluble ashes degree was 0.058%. Turmeric rhizome extract had volatile oil degree (0,10 0,0058) %, water degree (26,35 1,4357) % and curcuminoid degree (10,72 0,2207) %. The result of organoleptic and purity test had fulfilled the requirement but astiri oil degree, water degree, and curcuminoid degree had not fulfilled the requirement stamped on the Indonesian Herbs Medicine Extract Monographic yet.
xi
HALAMAN PERSETUJUAN PEMBIMBING ... ii
HALAMAN PENGESAHAN... iii
HALAMAN PERSEMBAHAN ... iv
LEMBAR PERNYATAAN PERSETUJUAN PUBLIKASI KARYA ILMIAH UNTUK KEPENTINGAN AKADEMIS ... v
PRAKATA... vi
PERNYATAAN KEASLIAN KARYA ... viii
INTISARI... ix
ABSTRACT... x
DAFTAR ISI... xi
DAFTAR TABEL... xiv
DAFTAR GAMBAR ... xvi
DAFTAR LAMPIRAN... xviii
BAB I. PENDAHULUAN ... 1
A. Latar Belakang ... 1
1. Rumusan masalah... 2
2. Keaslian Penelitian ... 3
3. Manfaat Penelitian ... 3
B. Tujuan Penelitian ... 3
BAB II. TINJAUAN PUSTAKA ... 4
A. Tanaman Kunyit ... 4
1. Keterangan Botani ... 4
2. Pemerian tanaman ... 4
3. Ekologi dan penyebaran ... 5
4. Persyaratan tumbuh... 5
5. Panen dan pasca panen... 5
6. Kandungan kimia ... 8
xii
B. Kurkuminoid ... 9
C. Persyaratan Ekstrak Kental Rimpang Kunyit ... 11
D. Ekstraksi ... 12
E. Ekstrak... 13
1. Ekstrak encer... 13
2. Ekstrak kental (extractum spissum) ... 13
3. Ekstrak kering (extactum siccum)... 13
4. Ekstrak cair (extractum fluidum) ... 14
F. Identifikasi Kandungan Kimia ... 14
1. Uji tabung ... 14
2. Kromatografi lapis tipis ... 14
G. Spektrofotometri ... 16
H. Keterangan Empiris ... 19
BAB III. METODE PENELITIAN ... 20
A. Jenis dan Rancangan Penelitian ... 20
B. Definisi Operasional ... 20
C. Bahan dan Alat Penelitian ... 22
1. Bahan Penelitian ... 22
2. Alat penelitian ... 23
D. Tatacara Penelitian ... 23
1. Pengentalan ekstrak rimpang kunyit ... 23
2. Identifikasi ekstrak rimpang kunyit ... 23
3. Uji kemurnian ekstrak rimpang kunyit ... 24
4. Penetapan kadar minyak atsiri ... 24
5. Penetapan kadar air ... 25
6. Penetapan kadar kurkuminoid ... 25
E. Tatacara Analisis Hasil ... 28
BAB IV. HASIL DAN PEMBAHASAN ... 29
A. Pengentalan Ekstrak Rimpang Kunyit ... 29
B. Identifikasi Ekstrak Rimpang Kunyit ... 30
xiii
F. Penetapan Kadar Kurkuminoid ... 40
1. Penetapan Operating Time(OT)... 40
2. Penetapan panjang gelombang maksimum (λmax)... 41
3. Pembuatan kurva baku ... 43
4. Validasi metode... 44
5. Penetapan kadar kurkuminoid dalam sampel... 46
BAB V. KESIMPULAN DAN SARAN... 49
A. Kesimpulan ... 49
B. Saran ... 49
DAFTAR PUSTAKA ... 50
LAMPIRAN... 53
xiv
DAFTAR TABEL
Halaman Tabel I. Perbandingan organoleptis ekstrak kental
rimpang kunyit dengan Monografi Ekstrak
Tumbuhan Obat Indonesia... 30
Tabel II. Data penetapan kadar abu... . 36
Tabel III. Data penetapan kadar abu tidak larut asam... . 37
Tabel IV. Data penetapan kadar minyak atsiri... 38
Tabel V. Data penetapan kadar air... . 40
Tabel VI. Data pengukuran absorbansi kurva baku... . 43
Tabel VII. Data perhitungan recovery... 44
Tabel VIII. Data perhitungan kesalahan sistemik ……….... 45
Tabel IX. Data perhitungan kesalahan acak (cv) ………. . 46
Tabel X. Data penetapan kadar kurkuminoid... . 48
Tabel XI. Penimbangan berat abu ... 53
Tabel XII. Penimbangan berat abu tidak larut asam ... 54
Tabel XIII. Penimbangan bobot ekstrak dan volume minyak atsiri 55 Tabel XIV. Penimbangan bobot konstan ekstrak setelah dikeringkan……… 56
Tabel XV. Pengukuran Operating Time ... 57
Tabel XVI. Penentuan panjang gelombang maksimum ... 57
xv
yang diamati secara visible, UV 254, UV 365, dan
disemprot pereaksi asam borat-metanol ……… 63 Tabel XIX. Data uji KLT kurkuminoid ekstrak kental rimpang
kunyit dengan fase diam silika gel GF 254 dan fase gerak kloroform : etanol : asam asetat (95:4:1) yang diamati secara visible, UV 254, UV 365, dan
xvi
DAFTAR GAMBAR
Gambar Halaman
Gambar 1. Struktur kimia kurkumin, desmetoksikurkumin,
bisdesmetoksikurkumin ... 9 Gambar 2. Degradasi kurkumin pada pH netral atau basa... 11 Gambar 3. Foto kromatogram KLT kurkuminoid ekstrak kental
rimpang kunyit dengan fase diam silika gel GF 254 dan fase gerak kloroform : etanol : asam asetat
(80:19,5:0,5)... 32 Gambar 4. Foto kromatogram KLT kurkuminoid ekstrak kental
rimpang kunyit dengan fase diam silika gel GF 254 dan fase gerak kloroform : etanol : asam asetat
(95 : 4 : 1)... 33 Gambar 5. Grafik penetapan operating time kurkuminoid ... 40 Gambar 6. Grafik penetapan panjang gelombang maksimum
kurkuminoid ... 42 Gambar 7. Kurva baku kurkuminoid ... 43 Gambar 8. Reaksi antara kurkumin, asam borat, dan asam oksalat
membentuk senyawa Rubrocurcumin... 47 Gambar 9. Foto ekstrak kental rimpang kunyit ... 68 Gambar 10. Foto abu ekstrak kental rimpang kunyit... 68 Gambar 11. Foto abu tidak larut asam ekstrak kental
xviii
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Data Pengentalan Ekstrak Rimpang Kunyit ... 53
Lampiran 2. Data Penimbangan dan Perhitungan Kadar Abu ... 53
Lampiran 3. Data Penimbangan dan Perhitungan Kadar Abu Tidak Larut Asam ... 54
Lampiran 4. Data Kadar Minyak Atsiri ... 55
Lampiran 5. Data Perhitungan Kadar Air secara Gravimetri... 56
Lampiran 6. Penentuan Operating Time (OT) ... 57
Lampiran 7. Penentuan Panjang Gelombang Maksimum pada Konsentrasi 0,032; 0,128; 0,512 mg % b/v ... 57
Lampiran 8. Data Validasi Metode dan Perhitungan Recovery, Kesalahan acak, dan Kesalahan Sistemik ... 58
Lampiran 9. Perhitungan Orientasi Penimbangan Sampel ... 61
Lampiran 10. Perhitungan Kadar Kurkuminoid dalam Sampel ... 61
Lampiran 11. Data pemeriksaan kandungan kimia kurkuminoid secara KLT ... 63
1
Obat tradisional banyak digunakan di masyarakat secara turun-temurun sehingga diyakini khasiat dan keamanannya. Salah satu tanaman yang dapat digunakan sebagai obat tradisional adalah kunyit. Pada umumnya bagian tanaman kunyit yang digunakan adalah bagian rimpang. Rimpang kunyit berkhasiat untuk obat sakit perut, memperbaiki pencernaan dan merangsang gerakan usus serta menyembuhkan perut kembung (karminativa), anti diare, obat peluruh empedu (kolagoga), dan penenang (sedativa) (Rukmana, 1999).
Kandungan kimia yang terdapat dalam rimpang kunyit meliputi minyak atsiri; kurkuminoid yang terdiri dari kurkumin, desmetoksikurkumin, dan bidesmetoksikurkumin; zingiberen (Duke, 2008). Kurkuminoid sebagai salah satu zat aktif dalam ekstrak rimpang kunyit yang bertanggung jawab atas timbulnya respon biologi sehingga keberadaan dan kandungannya mempengaruhi tingkat mutu dan khasiat ekstrak rimpang kunyit.
2
Obat tradisional yang digunakan dalam upaya pelayanan kesehatan harus memenuhi persyaratan yaitu bermutu, aman, dan bermanfaat. Oleh karena itu untuk memenuhi ketiga persyaratan tersebut maka diperlukan suatu standarisasi ekstrak rimpang kunyit sebagai salah satu bahan penyusun “Jamu Kunyit Asam”, dimana dilakukan identifikasi dan pengukuran beberapa parameter standar ekstrak rimpang kunyit dan membandingkan hasil idenifikasi dan pengukuran tersebut dengan persyaratan yang tercantum dalam Monografi Ekstrak Tumbuhan Obat Indonesia. Standarisasi ekstrak rimpang kunyit perlu dilakukan untuk setiap produksi ekstrak karena kualitas dan kuantitas kandungan kimia ekstrak rimpang kunyit dipengaruhi oleh lingkungan tempat tumbuh, umur, cara panen dan pasca panen, serta cara ekstraksi rimpang kunyit.
Beberapa parameter standar ekstrak yang diukur antara lain identifikasi ekstrak rimpang kunyit yang meliputi pemerian dan pemeriksaan kandungan kurkuminoid secara KLT, uji kemurnian yang terdiri dari penetapan kadar abu dan kadar abu tidak larut asam, penetapan kadar minyak atsiri dimana minyak atsiri juga merupakan zat yang memberikan respon biologi selain kurkuminoid, penetapan kadar air dimana air dapat menyebabkan ketidakstabilan ekstrak rimpang kunyit selama penyimpanan, dan penetapan kadar kurkuminoid.
1. Rumusan Masalah
b. Bagaimana kesesuaian hasil identifikasi dan pengukuran beberapa parameter standar ekstrak rimpang kunyit yang diteliti dengan persyaratan yang tercantum dalam Monografi Ekstrak Tumbuhan Obat Indonesia ? 2. Keaslian Penelitian
Sejauh yang diketahui penulis, penelitian mengenai Standarisasi Ekstrak Rimpang Kunyit penyusun “Jamu Kunyit Asam” belum pernah dilakukan.
3. Manfaat Penelitian
Manfaat yang diharapkan dari penelitian ini adalah : a. Manfaat teoritis
Memberikan sumbangan ilmiah dan menambah khasanah ilmu pengetahuan di bidang kesehatan khususnya pemanfaatan ekstrak rimpang kunyit sebagai obat tradisional.
b. Manfaat praktis
Memberikan pengetahuan mengenai identifikasi dan pengukuran beberapa parameter standar ekstrak rimpang kunyit yang diperoleh dari PT SM.
B. TUJUAN
Tujuan penelitian ini adalah :
1. Untuk mengetahui hasil identifikasi dan pengukuran beberapa parameter standar ekstrak rimpang kunyit yang diteliti.
4 BAB II
TINJAUAN PUSTAKA A. Tanaman Kunyit 1. Keterangan botani
Tanaman kunyit (Curcuma domestica Val.) merupakan herba yang
termasuk dalam familia Zingiberaceae. Kunyit dikenal dengan beberapa nama :
a. Nama Indonesia : kunyit (Rukmana, 1994).
b. Nama Inggris : turmeric(Duke, 2008)
c. Nama daerah
1) Sumatera : kakunye, kunye, kinung, odil, ondil
2) Jawa Tengah : kunyit, konye, kunir, temukuning
3) Kalimantan : jange henda, cahang, dio, kalesiau
4) Nusa Tenggara : kunyit, wingoro, kawunyi, kuneh, gumi, kunir
5) Sulawesi : uinida, alawaha, pagidon, uni, kunyi
6) Maluku : kurlai, lulu malai, ulin, tum, kunine, gogohiki
7) Irian : rame, kankeiyo, nikwai, mingguwai, yaw
8) Sunda : koneng, temukoneng (Anonim, 1985).
2. Pemerian tanaman
Tanaman kunyit berupa herba yang tingginya dapat mencapai 1 meter.
Tanaman ini tidak mempunyai bulu, tetapi mempunyai warna hijau. Bunganya
pucat dan pada pangkalnya berwarna kuning. Daun pelindungnya berwarna putih,
sedangkan daging rimpangnya berwarna kuning tua. Banyak tumbuh di kebun
3. Ekologi dan penyebaran
Kunyit tumbuh dan ditanam di Asia selatan, Cina selatan, Taiwan, Indonesia, dan Filipina. Tumbuh dengan baik di tanah yang baik tata pengairannya, curah hujan yang cukup banyak 2.000 mm sampai 4.000 mm tiap tahun dan di tempat yang sedikit kenaungan, tetapi untuk menghasilkan rimpang yang baik dan besar menghendaki tempat yang terbuka. Tanah yang ringan seperti tanah yang lempung berpasir, baik untuk pertumbuhan rimpang (Anonim, 1977). 4. Persyaratan tumbuh
Penanaman tanaman kunyit di dataran rendah dan tempat terbuka akan mendapatkan produksi rimpang kunyit yang tinggi. Sedangkan di dataran tinggi, produksi rimpang sedikit berkurang dan pertumbuhan tanaman lambat, tetapi kadar pati dan minyak atsirinya tinggi (Rukmana, 1994).
Jenis tanah yang paling baik untuk pertumbuhan tanaman kunyit adalah pada tanah liat berpasir (lempung berpasir) yang gembur, subur, dan berpengairan baik dan ditambahkan pupuk organik (Rukmana, 1994).
5. Panen dan pasca panen
6
Proses pemanenan, pasca panen, dan preparasi simplisia dan ekstrak merupakan proses yang dapat menentukan mutu simplisia dalam berbagai artian, yaitu komposisi zat kandungan, kontaminasi, dan stabilitas bahan (Komarawinata, 2008).
Pasca panen merupakan kelanjutan dari proses panen terhadap tanaman budidaya atau hasil dari penambangan alam yang fungsinya antara lain untuk membuat bahan hasil panen tidak mudah rusak dan memiliki kualitas yang baik serta mudah disimpan untuk diproses selanjutnya. Selama proses pasca panen sangat penting diperhatikan kebersihan alat dan bahan yang digunakan dan juga bagi pelaksananya perlu memperhatikan perlengkapan seperti masker dan sarung tangan. Tujuan dari pasca panen ini untuk menghasilkan simplisia tanaman obat yang bermutu, efek terapinya tinggi sehingga memiliki nilai jual yang tinggi. Secara umum faktor-faktor dalam penanganan pasca panen yang perlu diperhatikan adalah sebagai berikut :
a. Penyortiran
Penyortiran segar dilakukan setelah selesai panen dengan tujuan untuk memisahkan kotoran-kotoran atau bahan-bahan asing, bahan yang tua dengan yang muda atau bahan yang ukurannya lebih besar atau lebih kecil (Anonim, 2008).
b. Pencucian
pencucian harus dilakukan dalam waktu yang sesingkat mungkin untuk menghindari larut dan terbuangnya zat yang terkandung dalam bahan (Anonim, 2008). Pencucian rimpang kunyit dengan air yang mengandung kapur dapat menyebabkan perubahan pH yang berakibat mengaktifkan enzim tertentu dan merubah zat kurkumin yang ada menjadi asam ferulat (Komarawinata, 2008). c. Perajangan
Perajangan pada bahan dilakukan untuk mempermudah proses selanjutnya seperti pengeringan, pengemasan, penyulingan minyak atsiri dan penyimpanan. Perajangan terlalu tipis dapat mengurangi zat aktif yang terkandung dalam bahan. Sedangkan jika terlalu tebal, maka pengurangan kadar air dalam bahan agak sulit dan memerlukan waktu yang lama dalam penjemuran dan kemungkinan besar bahan mudah ditumbuhi oleh jamur (Anonim, 2008). d. Pengeringan
8
e. Pengemasan
Persyaratan jenis kemasan yaitu dapat menjamin mutu produk yang dikemas, mudah dipakai, tidak mempersulit penanganan, dapat melindungi isi pada waktu pengangkutan, tidak beracun dan tidak bereaksi dengan isi dan kalau boleh mempunyai bentuk dan rupa yang menarik (Anonim, 2008).
f. Penyimpanan
Ruang tempat penyimpanan harus bersih, udaranya cukup kering dan berventilasi. Ventilasi harus cukup baik karena hama menyukai udara yang lembab dan panas. Gudang harus terpisah dari tempat penyimpanan bahan lainnya ataupun penyimpanan alat dan dipelihara dengan baik. Suhu gudang tidak melebihi 30 0C. Kelembaban udara sebaiknya diusahakan serendah mungkin (650 C) untuk mencegah terjadinya penyerapan air. Kelembaban udara yang tinggi dapat memacu pertumbuhan mikroorganisme. Masuknya sinar matahari langsung menyinari simplisia harus dicegah. Mencegah masuknya hewan, baik serangga maupun tikus (Anonim, 2008).
6. Kandungan kimia
Rimpang kunyit mengandung zat warna curcuminoid suatu senyawa diarylheptanoide 3–4 % terdiri dari curcumin, dihydrocurcumin desmethoxycurcumin, dan bidesmethoxy-curcumin. Minyak atsiri 2 – 5 % terdiri dari seskuiterpen dan turunan phenylpropane yang meliputi turmeron, ar-turmeron, á- dan â-turmeron, curlon, curcumol, atlanton, turmerol, â-bisabolen, â-sesquiterphellandren, zingiberen, ar-curcumene, humulen. Selain itu rimpang
mineral, yaitu Mg, Mn, Fe, Cu, Ca, Na, K, Pb, Za, Co, Al, dan Bi (Sudarsono, 1996).
7. Khasiat dan kegunaan
Minyak atsiri dari rimpang kunyit berkhasiat untuk mencegah keluarnya asam lambung yang berlebihan dan mengurangi peristaltik usus yang terlalu kuat (Tampubolon, 1981). Rimpang kunyit juga berkhasiat untuk mengobati sakit perut, diare, asma, sakit kepala, sakit keputihan, haid tidak lancar, dan sebagai ekspektoran (Duke, 2008).
B. Kurkuminoid
Kunyit memiliki senyawa yang berkhasiat obat yang disebut kurkuminoid. Kurkuminoid terdiri atas kurkumin sebanyak 50 – 60 %, desmetoksikurkumin, dan bidesmetoksikurkumin (Stancovic, 2004). Kurkumin merupakan komponen terbesar dari kurkuminoid sehingga sering kadar total kurkuminoid dihitung sebagai % kurkumin. Karena alasan tersebut beberapa penelitian baik fitokimia maupun farmakologi lebih ditekankan pada kurkumin (Sumiati, 2006).
10
Kurkumin merupakan senyawa kandungan utama tanaman kunyit yang banyak tumbuh di Indonesia dan digunakan sebagai kosmetika, pewarna makanan, bumbu, dan pengobatan tradisional (Oetari, 1995). Kurkumin terdapat juga dalam tanaman temulawak (C. xanthorrhiza Roxb.) dan pada tanaman temugiring (C. heyneana Val.). Kurkumin murni sangat sulit diperoleh langsung dari rimpang kunyit karena seringkali tercampur dengan dua turunannya yaitu desmetoksikurkumin dan bidesmetoksikurkumin (Donatus, 1994).
Gambar 2. Degradasi kurkumin pada pH netral atau basa (Stancovic, 2004). C. Persyaratan Ekstrak Kental Rimpang Kunyit
Berdasarkan Monografi Ekstrak Tumbuhan Obat Indonesia (Anonim, 2004), ekstrak kental rimpang kunyit adalah ekstrak yang dibuat dari rimpang tumbuhan Curcuma domestica Val., suku Zingeberaceae, mengandung minyak atsiri tidak kurang dari 3,2 % dan kurkuminoid tidak kurang dari 33,9 %.
a. Pemerian
1. Bentuk : kental 2. Warna : kuning 3. Bau : khas 4. Rasa : agak pahit b. Identitas
12
Senyawa identitas dari rimpang kunyit adalah kurkumin, desmetoksikurkumin, dan bidesmetoksikurkumin
c. Kadar air : tidak lebih dari 4 %
d. Kadar abu total : tidak lebih dari 0,4 %
e. Kadar abu tidak larut asam : tidak lebih dari 0,08 % (Anonim, 2004). D. Ekstraksi
Ekstraksi adalah kegiatan penarikan kandungan kimia yang terlarut supaya terpisah dari bahan yang tidak dapat larut dengan pelarut cair. Simplisia yang diekstrak mengandung senyawa aktif yang dapat larut dan senyawa yang tidak dapat larut dalam cairan penyari. Ekstrak adalah sediaan kental yang diperoleh dengan mengekstraksi senyawa aktif dari simplisia nabati atau simplisia hewani menggunakan pelarut yang sesuai, kemudian semua atau hampir semua pelarut diuapkan dan massa yang tersisa diperlakukan sedemikian hingga memenuhi baku yang telah ditetapkan (Anonim,2000).
Cairan penyari dalam proses pembuatan ekstrak adalah pelarut yang optimal untuk senyawa kandungan yang berkhasiat atau aktif, dengan demikian senyawa tersebut dapat terpisahkan dari bahan dan dari senyawa kandungan lainnya. Ekstrak yang diperoleh hanya mengandung sebagian besar senyawa yang diinginkan. Dalam hal ekstrak total, maka cairan pelarut dipilih yang melarutkan hampir semua metabolit sekunder yang terkandung (Anonim,2000).
adalah air dan alkohol (etanol) serta campurannya. Jenis pelarut lain seperti metanol, heksana, toluen, kloroform, aseton, umumnya digunakan sebagai pelarut untuk tahap pemurnian (Anonim,2000).
E. Ekstrak
Ekstrak merupakan sediaan sari pekat tumbuh-tumbuhan atau hewan yang diperoleh dengan cara melepaskan zat aktif dari masing-masing bahan obat, menggunakan pelarut yang cocok, kemudian pelarut diuapkan sebagian atau semua, dan sisa endapan atau serbuk diatur untuk ditetapkan standarnya (Ansel, 1985).
Pada ekstrak tumbuhan jika bahan pengekstraksinya sebagian atau
saluruhnya diuapkan, maka diperoleh ekstrak yang dikelompokkan menurut sifat-sifatnya menjadi :
1. Ekstrak encer
Sediaan ini memiliki konsistensi seperti madu dan dapat dituang. 2. Ekstrak kental (extractum spissum)
Sediaan ini liat dalam keadaan dingin dan tidak dapat dituang. Ekstrak kental mengandung air tidak lebih dari 30%.
3. Ekstrak kering (extactum siccum)
14
4. Ekstrak cair (extractum fluidum)
Diartikan sebagai suatu ekstrak cair yang dibuat sedemikian sehingga satu bagian jamu sesuai dengan satu bagian atau dua bagian ekstrak cair (Voigt, 1994).
F. Identifikasi Kandungan Kimia
Identifikasi kandungan kimia merupakan suatu bentuk pengujian terhadap simplisia yang bersifat uji secara kualitatif dengan tujuan untuk mengetahui kandungan kimia dari suatu simplisia yang diperiksa. Metode yang dapat dilakukan untuk mengidentifikasi kandungan kimia adalah sebagai berikut :
1. Uji tabung
Uji tabung adalah uji yang dilakukan untuk mengetahui kandungan kimia suatu tanaman melalui pengamatan warna yang terbentuk oleh karena adanya reaksi antara zat aktif yang ada dengan pereaksi yang digunakan.
2. Kromatografi lapis tipis
(Stahl, 1985). Untuk mengelusi fraksi yang bersifat non polar, fase diam yang digunakan dapat berupa silika gel G atau silika GF 254, fase geraknya adalah campuran pelarut yang bersifat non polar. Untuk mengelusi fraksi yang bersifat polar, fase diamnya dapat menggunakan selulosa dan sebagai fase geraknya dapat digunakan campuran pelarut yang bersifat polar (Stahl, 1985).
Kromatografi lapis tipis merupakan metode analisis yang sensitif, cepat, sederhana, dan tidak mahal (Gritter, 1991). Di samping itu pemakaian pelarut dan cuplikan hanya sedikit. KLT dapat digunakan untuk analisis kualitatif, kuantitatif, dan preparatif, dapat juga digunakan untuk mencari pelarut yang digunakan pada kromatografi kolom, mengetahui arah reaksi, mengidentifikasi, dan mengisolasi senyawa murni berskala kecil (Gritter, 1991).
Prinsip kerja KLT berupa lapisan yang memisah, yang terdiri atas bahan berbutir-butir atau fase diam ditempatkan pada penyangga berupa pelat gelas, logam, atau lapisan yang cocok. Campuran yang akan dipisah berupa larutan yang ditotolkan berupa bercak atau pita, setelah pelat ditaruh di dalam bejana tertutup rapat yang berisi larutan pengembang atau fase gerak yang cocok, pemisahan terjadi selama perambatan kapiler atau pengembangan, selanjutnya senyawa yang tidak berwarna harus ditampakkan atau dideteksi dengan lampu UV atau dengan pereaksi semprot (Stahl, 1985).
16
Jarak pengembangan senyawa pada kromatogram biasanya dinyatakan dengan angka Rf atau hRf. Harga Rf didefinisikan sebagai perbandingan antara jarak senyawa dari titik awal dan jarak tepi muka pelarut dari awal.
Rf = Jarak titik pusat bercak dari titik awal Jarak garis depan dari titik awal
Angka Rf berkisar antara 0,01 – 1,00 dan hanya dapat ditentukan dengan dua desimal. hRf adalah angka Rf dikalikan faktor 100 (h), menghasilkan nilai berkisar antara 0 – 100 (Harborne, 1984 ; Stahl, 1985).
Faktor-faktor yang mempengaruhi gerakan bercak dan harga Rf dalam KLT antara lain adalah :
1. Struktur dan sifat kimia dari senyawa yang dipisahkan. 2. Sifat dari bahan penyerap dan derajat aktivitasnya. 3. Tebal dan kerapatan dari lapisan penyerap.
4. Derajat kemurnian fase gerak.
5. Derajat kejenuhan uap dalam bejana pengembangan. 6. Jumlah cuplikan yang dianalisis.
7. Suhu.
8. Kesetimbangan (Stahl, 1985).
G. Spektrofotometri
yang mempunyai gugus kromofor dan radiasi elektromagnetik pada daerah ultraviolet (200-400 nm) dan sinar tampak (400-800 nm) akan menghasilkan spektra serapan elektronik. Spektra serapan ini dapat digunakan untuk analisis kuantitatif karena jumlah radiasi elektromagnetik yang diserap ada hubungannya dengan jumlah molekul penyerap (Skoog, 1985).
Secara kuantitatif pengukuran absorbsi spektra dapat dihitung dengan menggunakan hukum Beer – Lambert. Pada analisis kuantitatif dengan spektrofotometer, maka sebagai dasar digunakan hubungan antara jumlah cahaya yang diabsorbsi dan jumlah zat yang mengabsorbsi. Hubungan ini dinyatakan sebagai berikut :
A= k.c.b ... (1) A : absorban (serapan)
k : suatu tetapan khas dari bahan larutan c. : konsentrasi dari larutan
b : panjang jalur
Bila c dinyatakan dalam mol per liter, dan panjang jalur (b) dinyatakan dalam sentimeter, persamaan menjadi :
A= å.c.b ... (2)
Istilah å diketahui sebagai absortifitas molar. Di dalam konsentrasi (c) dari larutan yang didefinisikan sebagai gram/liter, persamaan menjadi :
A= a.b.c ... (3)
18
a. Radiasi yang melewati adalah monokromatik
b. Pada proses absorbsi, zat pengabsorbsi tidak bereaksi dengan zat-zat lain dalam larutan tersebut
c. Degradasi energi berjalan cepat (tak terjadi fluoresensi) d. Absorbsi tidak merata di semua bagian yang dilewati radiasi e. Tak terjadi pembiasan pada konsentrasi tersebut (Fatah, 1989).
Pada analisis kuantitatif, pengukuran serapan dilakukan pada panjang gelombang maksimum, disebabkan dua alasan :
1. Sensitivitas maksimum diperoleh dengan mengerjakan pada pita maksimum karena pada konsentrasi yang diberikan, maka pada panjang gelombang tersebut memberi respon yang kuat.
2. Pada pita maksimum itu perubahan yang kecil pada panjang gelombang memberikan perubahan absorban yang minimal, dengan demikian kesalahan kecil dalam meletakkan tanda pemilih panjang gelombang pada instrumen tidak akan mengakibatkan kesalahan besar dalam pengukuran absorban (Fatah, 1989).
H. Keterangan Empiris
20
BAB III
METODE PENELITIAN A. Jenis dan Rancangan Penelitian 1. Jenis penelitian
Jenis penelitian ini termasuk penelitian non eksperimental, karena tidak ada manipulasi terhadap subyek uji. Penelitian ini dilakukan di laboratorium Farmakognosi Fitokimia Fakultas Farmasi Universitas Sanata Dharma Yogyakarta.
2. Rancangan Penelitian
Langkah-langkah penelitian : a. Pengentalan ekstrak rimpang kunyit b. Identifikasi ekstrak rimpang kunyit
1) Pemeriksaan pemerian
2) Pemeriksaan senyawa identitas kurkuminoid secara KLT c. Uji kemurnian ekstrak rimpang kunyit
1) Penetapan kadar abu
2) Penetapan kadar abu tidak larut asam d. Penetapan kadar minyak atsiri
e. Penetapan kadar air dalam ekstrak rimpang kunyit
f. Penetapan kadar kurkuminoid dalam ekstrak rimpang kunyit
B. Definisi Operasional
50 0C dan tekanan 72 mbar selama 1 jam 15 menit dan oven pada suhu 40 0C selama 19 jam 25 menit
b. Standarisasi ekstrak adalah serangkaian identifikasi dan pengukuran parameter standar ekstrak rimpang kunyit dan membandingkan hasil pengukuran tersebut dengan persyaratan yang tercantum dalam Monografi Ekstrak Tumbuhan Obat Indonesia.
c. Identifikasi dan pengukuran parameter standar ekstrak pada penelitian ini adalah pemerian, pemeriksaan senyawa identitas kurkuminoid secara KLT, pengukuran kadar abu total, kadar abu tidak larut asam, kadar minyak atsiri, kadar air, dan kadar kurkuminoid.
d. Pemerian meliputi pengamatan bentuk, warna, bau, dan rasa ekstrak rimpang kunyit yang diteliti.
e. Identifikasi konstituen aktif kurkuminoid merupakan pengamatan kandungan kurkuminoid dalam ekstrak rimpang kunyit secara KLT dengan fase diam silika gel GF 254 dan fase gerak kloroform : etanol : asam asetat glasial (80:19,5:0,5).
f. Pemeriksaan kemurnian ekstrak meliputi penetapan kadar abu dan penetapan kadar abu tidak larut asam.
22
h. Penetapan kadar abu tidak larut asam adalah penetapan tingkat pengotoran oleh senyawa-senyawa anorganik non logam dan silikat yang tidak larut dalam HCl P, dimana bahan yang tidak larut asam tersebut dipanaskan pada temperatur 350 – 5000C.
i. Penetapan kadar air adalah pengukuran kandungan air yang terdapat di dalam ekstrak secara gravimetri.
j. Kadar minyak atsiri adalah volume minyak atsiri yang dihasilkan dari setiap bobot penimbangan ekstrak dengan menggunakan destilasi Stahl.
k. Penetapan kadar kurkuminoid adalah penetapan kadar kurkuminoid total sebagai kompleks kurkumin-asam borat dengan adanya asam oksalat yang terukur oleh spektrofotometer visibel pada operating time selama 30 menit dan panjang gelombang maksimum 428 nm.
C. Bahan dan Alat Penelitian 1. Bahan Penelitian
Bahan-bahan yang digunakan dalam penelitian ini adalah :
a. Bahan utama yang digunakan adalah ekstrak cair rimpang kunyit yang diperoleh dari PT Sido Muncul
2. Alat Penelitian
Alat-alat yang digunakan dalam penelitian ini adalah Vacuum Rotary Evaporator, spektrofotometer OPTIMA SP-300, destilasi Stahl, penangas air, alat
vakum, timbangan, alat-alat gelas, labu alas bulat 500 ml, penyemprot reagen, lempeng kromatografi lapis tipis (KLT).
D. Tatacara Penelitian 1. Pengentalan ekstrak rimpang kunyit
Ekstrak cair yang diperoleh dari PT Sido Muncul dikentalkan dengan menggunakan Vacuum Rotary Evaporator pada suhu 50 0C dan tekanan 72 mbar dan menggunakan oven pada suhu 40 0C.
2. Identifikasi ekstrak rimpang kunyit
Identifikasi ini dilakukan untuk memastikan bahwa ekstrak yang diteliti benar-benar ekstrak rimpang kunyit dengan membandingkan hasilnya dengan Monografi Ekstrak Tumbuhan Obat Indonesia.
Identitas ekstrak rimpang kunyit diamati melalui : a. Pemerian yang meliputi bentuk, warna, bau , dan rasa. b. Pemeriksaan kandungan kurkuminoid secara KLT
24
3. Uji kemurnian ekstrak rimpang kunyit a. Penetapan kadar abu
Kurang lebih 2-3 g ekstrak yang telah ditimbang seksama dimasukkan dalam krus platina/silikat yang telah dipijarkan dan ditara, kemudian ratakan. Pijarkan perlahan hingga arang habis, didinginkan dan ditimbang hingga bobot tetap. Jika dengan cara ini arang tidak dapat dihilangkan maka ditambah dengan air panas, kemudian disaring dengan kertas saring bebas abu. Kertas saring beserta sisa penyaringan dipijarkan dalam krus yang sama hingga bobot tetap. Kadar abu total dihitung terhadap berat ekstrak, dinyatakan dalam % b/b (Anonim, 2004). b. Penetapan kadar abu tidak larut asam
Abu yang diperoleh pada penetapan kadar abu, dididihkan dengan 25 ml HCl P selama 5 menit. Bagian yang tidak larut dalam asam dikumpulkan dan disaring dengan krus kaca masir atau kertas saring bebas abu kemudian dicuci dengan air panas, dipijarkan hingga bobot tetap. Kadar abu yang tidak larut dalam asam terhadap berat ekstrak, dinyatakan dalam % b/b (Anonim, 2004).
4. Penetapan kadar minyak atsiri
5. Penetapan kadar air
Lebih kurang 10 gram ekstrak dimasukkan dan timbang saksama dalam wadah yang telah ditara. Kemudian dikeringkan pada suhu 105 0C selama 5 jam dan ditimbang. Lanjutkan pengeringan dan ditimbang pada jarak 1 jam sampai perbedaan antara 2 penimbangan berturut-turut tidak lebih dari 0,25 %. Bobot yang hilang setelah pengeringan dikurangi dengan bobot minyak atsiri yang terkandung dalam lebih kurang 10 gram ekstrak. Kadar air dihitung dalam % b/b (Anonim, 1977).
6. Penetapan kadar kurkuminoid a. Pembuatan larutan stok
Kurang lebih 10,0 mg kurkuminoid baku yang ditimbang seksama dilarutkan dalam aseton sampai 50 ml.
b. Pembuatan larutan intermediet
Larutan baku dengan kadar 20 mg % diambil sebanyak 5 ml dan dimasukkan ke dalam labu ukur 25 ml, kemudian diencerkan dengan aseton sampai tanda sehingga diperoleh larutan intermediet kurkuminoid dengan kadar 4 mg %.
c. Penetapan operating time (OT)
26
d. Penetapan panjang gelombang maksimum
Larutan intermediet dengan kadar 4 mg % diambil 0,2 ml; 0,8 ml; dan 3,2 ml dan dimasukkan ke dalam labu ukur 25 ml, kemudian diencerkan dengan aseton sampai tanda dan ditambahkan dengan 50 mg asam borat dan 50 mg asam oksalat. Ketiga larutan kurkuminoid dengan konsentrasi 0,032 mg %; 0,128 mg %; 0,512 mg % ini kemudian dibaca serapannya pada operating time dan pada panjang gelombang 400 nm sampai 450 nm.
e. Pembuatan kurva baku
Larutan intermediet dengan kadar 4 mg % diambil 0,2 ml; 0,4 ml; 0,8 ml; 1,6 ml; dan 3,2 ml dan dimasukkan ke dalam labu ukur 25 ml, kemudian diencerkan dengan aseton sampai tanda sehingga diperoleh konsentrasi seri larutan kurva baku sebesar 0,032 mg %; 0,064 mg %; 0,128 mg %; 0,256 mg %; 0,512 mg %. Lalu ditambahkan dengan 50 mg asam borat dan 50 mg asam oksalat. Seri kadar larutan ini kemudian dibaca serapannya pada operating time dan pada panjang gelombang maksimum. Kemudian digambar kurva hubungan antara konsentrasi larutan dengan serapan.
f. Penetapan recovery, kesalahan sistemik dan kesalahan acak
1) Penentuan recovery (perolehan kembali). Recovery dihitung dari kadar yang terukur pada kurva baku dibandingkan dengan kadar yang diketahui dikalikan 100 %.
2) Penghitungan kesalahan sistemik. Rumus kesalahan sistemik = 100 – P%
3) Penghitungan kesalahan acak. Kesalahan acak diukur dengan cv (coeficient variancy)
g. Penetapan kadar kurkuminoid dalam sampel
28
E. Tatacara Analisis Hasil
29
Pengentalan ekstrak cair rimpang kunyit sebanyak 700 ml dilakukan
dengan menggunakan Vacuum Rotary Evaporator pada suhu 50 0C dan pada
tekanan 72 mbar. Prinsip Vacuum Rotary Evaporator adalah memindahkan
pelarut dari sampel dengan menggunakan sistem evaporasi. Penggunaan Vacuum
Rotary Evaporator bertujuan untuk mempercepat proses pengentalan dan
mencegah banyaknya minyak atsiri yang menguap. Vakum evaporator bekerja
dengan menurunkan tekanan dalam bulk cairan dan menurunkan titik didih
komponen cairan yang akan dipindahkan sehingga proses pemindahan komponen
cairan dapat terjadi tanpa pemanasan yang berlebih.
Pada penelitian ini, pelarut yang akan dipindahkan adalah air yang
mempunyai titik didih 100 0C pada tekanan 1 atm atau 1013,25 mbar dan dengan
adanya vakum evaporator diharapkan air dapat dipindahkan pada suhu 50 0C dan
tekanan 72 mbar sehingga tidak perlu menggunakan pemanasan berlebih yang
dapat menyebabkan banyak minyak atsiri yang ikut menguap. Pengentalan ekstrak
dilakukan dengan menggunakan Vacuum Rotary Evaporator selama 1 jam 15
menit. Hal ini disebabkan karena jika proses pengentalan ekstrak dengan
menggunakan Vacuum Rotary Evaporator terlalu lama maka akan dihasilkan
ekstrak kental yang sulit dikeluarkan dari labu alas bulat pada Vacuum Rotary
Evaporator sehingga proses pengentalan dilanjutkan dengan menggunakan oven
30
300 ml. Ekstrak kental inilah yang akan digunakan untuk identifikasi dan
pengukuran beberapa parameter ekstrak rimpang kunyit selanjutnya.
B. Identifikasi Ekstrak Rimpang Kunyit
Identifikasi ekstrak rimpang kunyit dilakukan dengan pemeriksaan
organoleptis dan pemeriksaan senyawa identitas kurkuminoid secara KLT.
Pemeriksaan organoleptis ekstrak rimpang kunyit bertujuan untuk mengetahui
adanya kekhususan bau, rasa, bentuk, dan warna ekstrak yang diuji dan
dibandingkan dengan ciri-ciri organoleptis ekstrak kental rimpang kunyit yang
tercantum dalam Monografi Ekstrak Tumbuhan Obat Indonesia.
Tabel I. Perbandingan organoleptis ekstrak kental rimpang kunyit dengan Monografi Ekstrak Tumbuhan Obat Indonesia.
Jenis Pemeriksaan
Ciri-ciri Organoleptis
Ekstrak kental rimpang kunyit
Ekstrak kental rimpang kunyit berdasarkan Monografi Ekstrak
Tumbuhan Obat Indonesia
Bau Khas kunyit Khas
Rasa Pahit Agak pahit
Bentuk Kental Kental
Warna Coklat kekuningan Kuning
Tabel I menunjukkan adanya kemiripan ciri-ciri organoleptis antara
ekstrak kental rimpang kunyit dengan persyaratan yang tercantum dalam
Monografi Ekstrak Tumbuhan Obat Indonesia (Anonim, 2004).
Pemeriksaan kandungan kimia secara kromatografi lapis tipis (KLT)
dilakukan untuk memperoleh gambaran mengenai kandungan senyawa kimia
yang terdapat dalam ekstrak rimpang kunyit. Pemeriksaan senyawa identitas
kurkuminoid secara KLT bertujuan untuk mengetahui apakah ekstrak rimpang
bercak ekstrak tersebut dengan standar kurkuminoid. Pada pemeriksaan
kandungan kurkuminoid secara KLT digunakan fase diam berupa silika gel GF
254 dan fase gerak berupa kloroform : etanol : asam asetat dengan dua macam
perbandingan komposisis yaitu 80 : 19,5 : 0,5 dan 95 : 4 : 1 v/v. Hal ini bertujuan
untuk mengetahui fase gerak mana yang dapat memisahkan kandungan dalam
ekstrak rimpang kunyit dengan baik. Jarak pengembangannya sejauh 10 cm.
Kandungan kurkuminoid yang akan diidentifikasi bersifat non polar sehingga fase
diam yang digunakan bersifat lebih polar dibandingkan dengan fase geraknya.
32
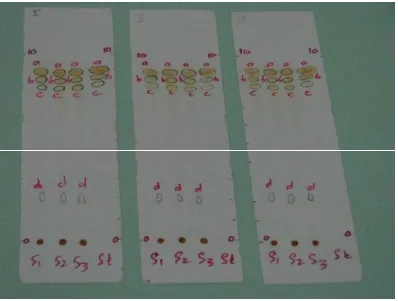
Gambar 3. Foto kromatogram KLT kurkuminoid ekstrak rimpang kunyit fase diam silika gel GF 254 dan fase gerak kloroform : etanol : asam asetat (80:19,5:0,5)
Keterangan gambar :
Jarak pengembangan : 10 cm
Deteksi : secara visibel, sinar UV 254, sinar UV 365, dan pereaksi semprot asam borat – metanol
Bercak a : bidesmetoksikurkumin Bercak b : desmetoksikurkumin
Bercak c : kurkumin
Bercak d : kandungan kimia lain selain kurkuminoid S1 : sampel ekstrak rimpang kunyit 1
S2 : sampel ekstrak rimpang kunyit 2
S3 : sampel ekstrak rimpang kunyit 3
Gambar 4. Foto kromatogram KLT kurkuminoid ekstrak rimpang kunyit fase diam silika gel GF 254 dan fase gerak kloroform : etanol : asam asetat (95:4:1)
Keterangan gambar :
Jarak pengembangan : 10 cm
Deteksi : secara visibel, sinar UV 254, sinar UV 365, dan pereaksi semprot asam borat – metanol
Bercak a : bidesmetoksikurkumin Bercak b : desmetoksikurkumin
Bercak c : kurkumin
Bercak d : kandungan kimia lain selain kurkuminoid S1 : sampel ekstrak rimpang kunyit 1
S2 : sampel ekstrak rimpang kunyit 2
S3 : sampel ekstrak rimpang kunyit 3
34
Hasil pemeriksaan kurkuminoid pada sampel dan standar dengan KLT
yang dielusi dengan kedua macam fase gerak tersebut menunjukkan pemisahan
yang baik. Walaupun pada penggunaan fase gerak kloroform : etanol : asam asetat
(95:4:1) menunjukkan pemisahan yang lebih baik hal ini dilihat dari jarak antara
bercak a, b, c, dan d pada sampel dan standar cukup jauh (gambar 4). Tetapi pada
pemeriksaan kurkuminoid secara KLT dengan fase gerak kloroform : etanol :
asam asetat dengan perbandingan 80 : 19,5 : 0,5 menunjukkan kedekatan nilai Rf
bercak kurkuminoid dalam sampel dengan bercak kurkuminoid standar (gambar
3). Oleh karena itu fase gerak yang dipakai pada pemeriksaan kurkuminoid secara
KLT menggunakan fase gerak kloroform : etanol : asam asetat dengan
perbandingan 80 : 19,5 : 0,5.
Bercak diamati secara visible, ketiga sampel dan standar kurkuminoid
pada ketiga replikasi tampak adanya bercak berwarna kuning. Tetapi bercak
kurkumin pada standar kurkuminoid tidak tampak pada pengamatan secara
visibel. Pada pengamatan dibawah sinar UV 254 dan UV 365, ketiga bercak pada
ketiga sampel dan standar kurkuminoid tampak berpendar kuning dimana ketiga
bercak tersebut diperkirakan sebagai bercak bidesmetoksikurkumin (bercak a),
desmetoksikurkumin (bercak b), dan kurkumin (bercak c). Kurkumin mempunyai
nilai log P sebesar 2,56, nilai log P desmetoksikurkumin sebesar 2,69, dan nilai
log P bidesmetoksikurkumin sebesar 2,81. Semakin besar nilai log P maka
senyawa tersebut semakin bersifat non polar. Berdasarkan nilai log P tersebut
maka urutan kepolaran senyawa-senyawa dalam kurkuminoid dari yang paling
desmetoksikurkumin, dan kurkumin. Pada penelitian ini digunakan fase diam
yang bersifat polar dan fase gerak yang bersifat non polar. Senyawa yang bersifat
lebih polar memiliki afinitas yang lebih besar terhadap fase diam sehingga
senyawa tersebut diperkirakan memiliki nilai Rf yang lebih kecil. Sebaliknya
senyawa yang bersifat lebih non polar memiliki afinitas yang lebih besar terhadap
fase gerak sehingga senyawa tersebut diperkirakan memiliki nilai Rf yang lebih
besar. Berdasarkan afinitas terhadap fase gerak dan fase diam maka dapat
diperkirakan urutan nilai Rf dari senyawa-senyawa dalam kurkuminoid dari yang
paling besar adalah bidesmetoksikurkumin, desmetoksikurkumin dan yang paling
kecil adalah kurkumin. Pada ketiga sampel terdapat bercak keempat (bercak d)
berwarna coklat yang merupakan kandungan kimia lain di dalam ekstrak kental
rimpang kunyit selain kurkuminoid. Setelah disemprot dengan pereaksi asam
borat-metanol, bercak a pada ketiga sampel dan standar kurkuminoid berwarna
jingga tua, bercak b berwarna jingga, bercak c berwarna kuning, dan bercak d
berwarna coklat muda. Bercak a, b, dan c pada ketiga sampel pada ketiga replikasi
mempunyai warna yang sama dan nilai Rf yang mirip dengan bercak a, b, dan c
pada standar kurkuminoid. Hal ini menunjukkan bahwa pada ketiga sampel
ekstrak kental rimpang kunyit mengandung kurkuminoid.
C. Uji Kemurnian Ekstrak Rimpang Kunyit 1. Penetapan Kadar Abu
Penetapan kadar abu merupakan salah satu pemeriksaan mutu ekstrak
rimpang kunyit. Pemeriksaan ini bertujuan untuk mengetahui pencemaran bahan
36
gravimetri. Metode gravimetri yaitu bahan diabukan pada suhu tinggi yaitu sekitar
350 – 500 0C dan kemudian ditimbang hingga bobot konstan. Pada suhu tersebut
bahan-bahan organik yang terkandung dalam ekstrak rimpang kunyit akan
terdestruksi sehingga yang tertinggal hanya bahan-bahan anorganik dan mineral.
Semakin sedikit kadar abu menandakan bahwa pencemaran bahan anorganik dan
mineral semakin sedikit.
Tabel II. Data penetapan kadar abu
Replikasi I Replikasi II Replikasi III
Berat ekstrak awal 3,0005 g 3,0004 g 3,0005 g
Berat abu konstan 0,0098 g 0,0096 g 0,0095 g
Kadar abu 0,33 % 0,32 % 0,32 %
Rata-rata kadar abu 0,32 %
SD 0,0058
cv 1,81 %
Tabel II menunjukkan hasil penetapan kadar abu rata-rata ekstrak
rimpang kunyit sebesar 0,32 %. Kadar abu ekstrak rimpang kunyit telah sesuai
dengan persyaratan yang tercantum dalam Monografi Ekstrak Tumbuhan Obat
Indonesia yaitu kurang dari 0,4 % (Anonim, 2004).
2. Penetapan Kadar Abu Tidak Larut Asam
Penetapan kadar abu tidak larut asam dilakukan untuk mengetahui
Tabel III. Data penetapan kadar abu tidak larut asam
Replikasi I Replikasi II Replikasi III
Berat ekstrak awal 3,0005 g 3,0004 g 3,0005 g
Berat abu tidak
larut asam 0,0017 g 0,0017 g 0,0018 g
Kadar abu tidak
larut asam 0,057 % 0,057 % 0,060 %
Rata-rata kadar abu
tidak larut asam 0,058 %
SD 0,0017
cv 2,93 %
Tabel III menunjukkan ekstrak rimpang kunyit memiliki kadar abu tidak
larut asam rata-rata sebesar 0,058 %. Hasil ini menunjukkan bahwa ekstrak
rimpang kunyit yang diteliti telah sesuai dengan persyaratan dalam Monografi
Ekstrak Tumbuhan Obat Indonesia yaitu kurang dari 0,08 % (Anonim, 2004).
D. Penetapan Kadar Minyak Atsiri
Kadar minyak atsiri dilakukan untuk mengetahui jumlah kandungan
minyak atsiri yang terkandung dalam ekstrak rimpang kunyit. Minyak atsiri juga
merupakan salah satu komponen dari ekstrak rimpang kunyit yang mempunyai
efek farmakologi sehingga kadar minyak atsiri dalam ekstrak rimpang kunyit
mempengaruhi mutu dan khasiat obat tradisional yang mengandung ekstrak
rimpang kunyit. Kadar minyak atsiri dihitung dalam persen v/b. Kadar minyak
38
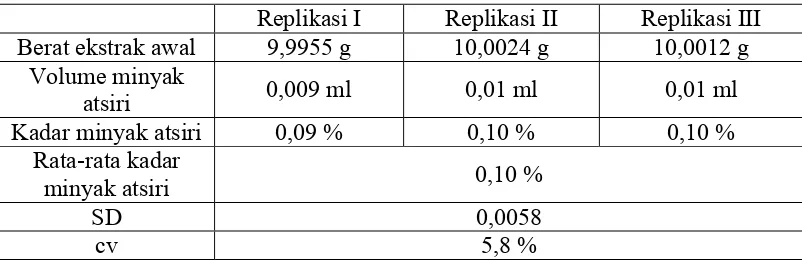
Tabel IV. Data penetapan kadar minyak atsiri
Replikasi I Replikasi II Replikasi III
Berat ekstrak awal 9,9955 g 10,0024 g 10,0012 g
Volume minyak
atsiri 0,009 ml 0,01 ml 0,01 ml
Kadar minyak atsiri 0,09 % 0,10 % 0,10 %
Rata-rata kadar
minyak atsiri 0,10 %
SD 0,0058
cv 5,8 %
Tabel IV menunjukkan hasil rata-rata kadar minyak atsiri yang
terkandung dalam ekstrak rimpang kunyit adalah sebesar 0,10 %. Hasil kadar
minyak atsiri dari ekstrak rimpang kunyit yang diteliti tidak sesuai atau tidak
memenuhi persyaratan dalam Monografi Ekstrak Tumbuhan Obat Indonesia yaitu
tidak kurang dari 3,2 % (Anonim, 2004). Hal ini dapat disebabkan karena minyak
atsiri larut dalam pelarut lipofil tetapi ekstrak rimpang kunyit yang diteliti
diperoleh dari hasil pengepresan rimpang kunyit segar sehingga hanya sedikit
minyak atsiri yang terekstraksi ke dalam ekstrak rimpang kunyit. Pada saat
pengentalan ekstrak, walaupun suhu yang digunakan relatif rendah yaitu 40-50 0C
tetapi tidak dapat dipastikan adanya kandungan minyak atsiri yang menguap.
E. Penetapan Kadar Air
Penetapan kadar air bertujuan untuk mengetahui jumlah kandungan air
dalam ekstrak rimpang kunyit. Kadar air ekstrak yang tinggi dapat menyebabkan
ketidakstabilan ekstrak rimpang kunyit selama penyimpanan akibat pertumbuhan
mikroorganisme. Air merupakan media pertumbuhan yang baik untuk
mikroorganisme karena air merupakan komponen terbesar dari sel sehingga
Pada penelitian ini, kadar air ekstrak rimpang kunyit ditetapkan dengan
metode gravimetri dimana ekstrak dipanaskan pada suhu 105 0C hingga bobot
konstan. Ekstrak rimpang kunyit memiliki kandungan minyak atsiri yang cukup
tinggi yaitu sekitar 2–5 % sehingga metode gravimetri ini kurang cocok
digunakan untuk penetapan kadar air ekstrak rimpang kunyit karena selama
pemanasan tidak hanya air yang hilang tetapi juga minyak atsiri karena sifatnya
yang mudah menguap sehingga bobot yang hilang selama pemanasan tidak
menggambarkan bobot air yang terkandung dalam ekstrak. Metode penetapan
kadar air ekstrak rimpang kunyit yang lebih baik adalah destilasi dengan toluen.
Pendekatan metode penetapan kadar air dengan metode gravimetri digunakan
pada penelitian ini karena ketiadaan alat destilasi air. Pada penelitian ini juga
dilakukan penetapan bobot dan kadar minyak atsiri yang terkandung dalam
ekstrak rimpang kunyit sehingga bobot air yang terkandung dalam ekstrak
rimpang kunyit dapat dihitung dari bobot yang hilang selama pemanasan
dikurangi dengan bobot minyak atsiri. Jika bobot air telah diketahui maka kadar
air ekstrak rimpang kunyit dapat ditetapkan. Kelemahan pendekatan metode
penetapan kadar air dengan metode gravimetri ini adalah tidak dapat mengetahui
bobot oleoresin yang hilang selama pemanasan. Oleoresin merupakan campuran
dari 45 % kurkuminoid, 25 % minyak atsiri, dan resin sehingga oleoresin juga
menguap selama pemanasan karena mengandung minyak atsiri dan ketika
penetapan bobot minyak atsiri menggunakan destilasi Stahl tidak dapat menjamin
40
Tabel V. Data penetapan kadar air
Replikasi I Replikasi II Replikasi III
Berat ekstrak awal 10,0019 g 10,0049 g 10,0022 g
Bobot yang hilang setelah pemanasan
2,8086 g 2,5422 g 2,5836 g
Bobot minyak atsiri 0,0091 g 0,0095 g 0,0094 g
Bobot air (bobot yang hilang – bobot minyak atsiri)
2,7995 g 2,5327 g 2,5742 g
Kadar air 27,99 % 25,32 % 25,74 %
Rata-rata kadar air 26,35 %
SD 1,4357
cv 5,45 %
Tabel V menunjukkan rata-rata kadar air dari ekstrak rimpang kunyit
yang diteliti adalah sebesar 26,35 %. Kadar air yang terkandung dalam ekstrak
kental rimpang kunyit yang diteliti tidak sesuai atau tidak memenuhi persyaratan
yang tercantum pada Monografi Ekstrak Tumbuhan Obat Indonesia yaitu tidak
lebih dari 4 % (Anonim, 2004). Hal ini terjadi karena dapat disebabkan oleh
waktu pengentalan ekstrak yang kurang lama.
F. Penetapan Kadar Kurkuminoid 1. Penetapan Operating Time(OT)
Pada penelitian ini, kadar kurkuminoid ditetapkan sebagai kompleks
kurkumin-asam borat dengan adanya asam oksalat sehingga dibutuhkan waktu
untuk pembentukan kompleks tersebut secara maksimal agar menghasilkan
serapan yang stabil. Oleh karena itu diperlukan penetapan operating time untuk
mengetahui waktu pengukuran dimana pada rentang waktu tersebut senyawa
memberikan serapan yang stabil. Pada rentang waktu tersebut, larutan kurva baku
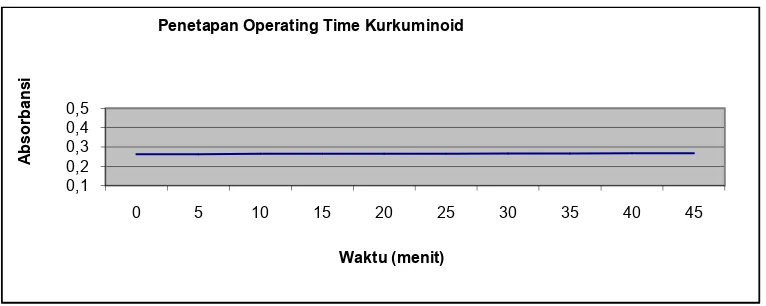
Gambar 5. Grafik penetapan operating time kurkuminoid
Gambar 5 menunjukkan bahwa sejak menit ke-0 sampai 45, kompleks
kurkumin-asam borat mempunyai absorbansi yang stabil. Berdasarkan Monografi
Ekstrak Tumbuhan Indonesia, setelah penambahan asam borat dan asam oksalat,
larutan dibiarkan selama 30 menit. Jadi OT yang digunakan pada penetapan kadar
kurkuminoid ini adalah 30 menit.
2. Penetapan panjang gelombang maksimum (λmax)
Penetapan panjang gelombang maksimum bertujuan untuk mengetahui
panjang gelombang dari suatu larutan yang mempunyai absorban (serapan)
maksimum. Pengukuran serapan pada panjang gelombang maksimum dapat
memberikan sensitivitas maksimum dan perubahan yang kecil pada panjang
gelombang memberikan perubahan absorban yang minimal. Dalam penelitian ini
pengukuran panjang gelombang maksimum dimulai dari panjang gelombang 400
nm – 500 nm.
0,1 0,2 0,3 0,4 0,5
0 5 10 15 20 25 30 35 40 45
A
b
s
o
rb
a
n
s
i
42
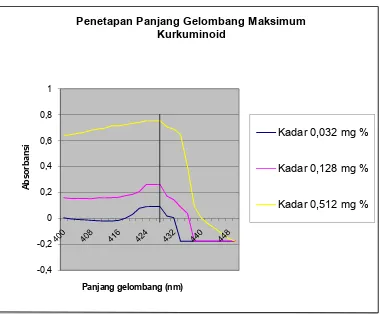
Gambar 6. Grafik penetapan panjang gelombang maksimum kurkuminoid
Dari grafik panjang gelombang yang diukur pada tiga konsentrasi (0,032
mg%; 0,128 mg%; 0,512 mg%) terlihat bahwa panjang gelombang maksimum
kurkuminoid adalah 428 nm. Hasil pengukuran panjang gelombang maksimum
hanya berbeda 2 nm dari panjang gelombang maksimum kurkuminoid yang
tercantum pada Monografi Ekstrak Tumbuhan Indonesia yaitu sebesar 430 nm
sehingga hasil pengukuran panjang gelombang maksimum (428 nm) ini dapat
digunakan untuk pengukuran absorban (serapan) larutan baku dan sampel yang
akan dianalisis.
3. Pembuatan kurva baku
Dalam pembuatan kurva baku diperlukan satu seri larutan kurkuminoid
murni dengan kadar yang berbeda. Seri larutan kurkuminoid ini selanjutnya
-0,4 -0,2 0 0,2 0,4 0,6 0,8 1
A
b
s
o
rb
a
n
s
i
Panjang gelombang (nm)
Penetapan Panjang Gelombang Maksimum Kurkuminoid
Kadar 0,032 mg %
Kadar 0,128 mg %
diukur absorbannya pada panjang gelombang maksimum yaitu sebesar 428 nm,
kemudian dibuat kurva hubungan antara konsentrasi dengan absorban.
Tabel VI. Data pengukuran absorbansi kurva baku
Kadar (% mg v/b)
Absorbansi
Replikasi I Replikasi II Replikasi III 0,032
Dari ketiga replikasi kurva baku kurkuminoid diatas memiliki nilai
koefisien korelasi (r) yang lebih besar dari nilai r tabel dengan taraf kepercayaan
99 % (0,959 dengan df 3) sehingga untuk persamaan kurva baku dipilih r yang
paling mendekati 1 yaitu persamaan kurva baku replikasi I yaitu Y = 1,359669 x +
0,069042 ; r = 0,998413.
Gambar 7. Kurva baku kurkuminoid
44
4. Validasi metode
Metode penetapan kadar yang baik harus memenuhi berbagai kriteria
yaitu nilai perolehan kembali (recovery), kesalahan sistemik, dan kesalahan acak.
Ketiga hal tersebut merupakan parameter validitas metode untuk menunjukkan
apakah suatu metode sudah optimal untuk digunakan dalam menetapkan kadar
suatu zat dalam sampel.
Recovery menggambarkan tingkat akurasi suatu metode analisis yang
menunjukkan seberapa dekat hasil analisis yang diperoleh dengan hasil
sebenarnya. Menurut Harmita (2004), suatu metode yang digunakan untuk
mengukur sampel dengan kadar analit lebih besar dari 10 % maka metode tersebut
dapat dikatakan memiliki akurasi yang baik jika recovery yang diperoleh masih
dalam rentang 98 – 102 %. Tabel VII menunjukkan pengukuran dengan tiga kali
replikasi didapatkan nilai rata-rata nilai untuk recovery 99,32%. Jadi metode yang
digunakan pada penelitian ini dapat dikatakan memiliki akurasi yang baik.
Tabel VII. Data perhitungan recovery
Kadar teoritis
Kesalahan sistemik merupakan tolok ukur inakurasi penetapan kadar.
Kesalahan sistemik merupakan parameter lain untuk akurasi selain recovery. Nilai
nilai kesalahan sistemik rata-rata yang diperoleh dari hasil pengukuran tiga kali
replikasi adalah sebesar 2,34 %. Walaupun nilai kesalahan sistemik pada metode
ini lebih besar dari 2 %, tetapi nilai recovery masih memenuhi rentang yang
diijinkan sehingga metode ini dapat digunakan untuk menetapkan kadar
kurkuminoid dalam ekstrak rimpang kunyit.
Tabel VIII. Data Perhitungan Kesalahan Sistemik
Recovery (%)
Kesalahan sistemik (%)
Rata-rata kesalahan sistemik 103,13
96,88 101,04
98,96 96,61
3,13 3,12 1,04 1,04 3,39
0,34 %
Kesalahan acak yang diukur dengan cv (coefficient variancy) merupakan
tolok ukur inpresisi suatu analisis yang berarti dalam suatu seri pengukuran atau
penetapan kadar dapat diperoleh hasil yang hampir sama satu sama lain. Dengan
kata lain harga cv menunjukkan keterulangan hasil yang diperoleh. Semakin besar
cv, maka semakin kecil pula keterulangan hasil yang diperoleh, begitu juga
sebaliknya. Menurut Harmita (2004), nilai kesalahan acak yang baik adalah 2 %
atau kurang. Akan tetapi kriteria ini sangat fleksibel tergantung pada konsentrasi
analit yang diperiksa, jumlah sampel, dan kondisi laboratorium. Koefisien variansi
meningkat dengan menurunnya kadar. Pada kadar 1 % atau lebih, koefisien
variansi adalah sekitar 2,5 %. Tabel IX menunjukkan nilai cv yang diperoleh dari
46
Tabel IX. Data Perhitungan Kesalahan Acak (cv)
Simpangan baku
5. Penetapan kadar kurkuminoid dalam sampel
Kadar kurkuminoid total dalam sampel ekstrak kental rimpang kunyit
ditetapkan sebagai kompleks kurkumin - asam borat yang diukur dengan
menggunakan spektrofotometer visibel setelah operating time selama 30 menit
dan pada panjang gelombang 428 nm. Pelarut yang digunakan adalah pelarut yang
dapat melarutkan kurkuminoid dan memiliki panjang gelombang di luar panjang
gelombang maksimum kurkuminoid agar pelarut yang digunakan tidak
mengganggu pengukuran absorbansi kurkuminoid sehingga pelarut yang
digunakan adalah aseton yang memiliki absorbansi maksimum pada panjang
gelombang 330 nm (Willard, 1988).
Gambar 8 menunjukkan reaksi antara kurkumin dan asam borat dengan
adanya asam oksalat yang akan membentuk senyawa Rubrocurcumin dimana
+ +
Curcumin Asam borat Asam oksalat
Rubrocurcumin
Gambar 8. Reaksi antara kurkumin, asam borat, dan asam oksalat membentuk
48
Tabel X. Data penetapan kadar kurkuminoid
Replikasi I Replikasi II Replikasi III
Berat ekstrak awal 191,8 mg 191,5 mg 191,5 mg
Bobot kurkuminoid
dalam eksrak 21 mg 20,5 mg 20,13 mg
Kadar kurkuminoid 10,95 % 10,70 % 10,51 %
Rata-rata kadar
kurkuminoid 10,72 %
SD 0,2207
cv 2,06 %
Tabel X menunjukkan kadar kurkuminoid dalam ekstrak kental rimpang kunyit
dengan tiga kali replikasi diperoleh kadar rata-rata kurkuminoid sebesar 10,72 %.
Hasil yang diperoleh tidak sesuai atau tidak memenuhi persyaratan kadar
kurkuminoid yang tercantum dalam Monografi Ekstrak Tumbuhan Indonesia
yaitu sebesar 33,9 % (Anonim, 2004). Hal ini dapat disebabkan karena ekstrak
rimpang kunyit diperoleh dari hasil pengepresan rimpang kunyit segar, padahal
menurut Stancovic (2004), kurkumin lebih larut dalam larutan yang bersifat lipofil
seperti etanol, metanol, dan aseton. Selain itu kadar kurkuminoid dalam rimpang
kunyit dapat juga dipengaruhi oleh kondisi lingkungan tempat tumbuh tanaman
kunyit dan umur tanaman saat panen. Ketidakstabilan kurkuminoid dalam ekstrak
rimpang kunyit selama penyimpanan juga dapat mempengaruhi kadar
kurkuminoid. Ketidakstabilan ini dapat disebabkan karena kurkuminoid dapat
terdegradasi oleh cahaya dan dalam suasana pH netral atau basa. Oleh karena itu
bahan penyusun ”Jamu Kunyit Asam” tidak hanya ekstrak rimpang kunyit saja
tetapi juga ekstrak buah asam sebagai penstabil kurkuminoid dalam ekstrak
49
Dari hasil penelitian yang dilakukan dapat disimpulkan bahwa :
1. Hasil identifikasi dan pengukuran beberapa parameter standar ekstrak rimpang
kunyit yang diteliti yaitu ekstrak rimpang kunyit memiliki bau khas, rasa
pahit, bentuk kental, dan warna coklat kekuningan, secara KLT menunjukkan
ekstrak rimpang kunyit mengandung kurkuminoid, ekstrak rimpang kunyit
memiliki kadar abu 0,32 %; kadar abu tidak larut asam 0,058 %; kadar minyak
atsiri 0,10 %; kadar air 26,35 %; kadar kurkuminoid 10,72 %
2. Hasil identifikasi dan pengukuran beberapa parameter standar ekstrak rimpang
kunyit yang diteliti belum sepenuhnya sesuai dengan persyaratan yang
tercantum pada Monografi Ekstrak Tumbuhan Obat Indonesia karena kadar
minyak atsiri, kadar air, dan kadar kurkuminoid belum memenuhi persyaratan.
B. Saran
Dari hasil penelitian dapat disarankan :
1. Perlu dilakukan standarisasi ekstrak rimpang kunyit mengenai cemaran
mikroba, aflatoksin, logam berat, dan angka kapang khamir.
2. Perlu dilakukan ekstraksi dengan menggunakan pelarut yang bersifat semi
polar atau non polar seperti etanol atau aseton agar kurkuminoid dan minyak
atsiri yang terekstraksi lebih banyak.
3. Perlu dilakukan penambahan waktu pengentalan ekstrak agar diperoleh kadar
50
DAFTAR PUSTAKA
Anief, Moh., 1999, Ilmu Meracik Obat, Cetakan Kelima, 168, UGM Press, Yoyakarta.
Anonim, 1974, Extra Farmakope Indonesia, 1092 – 1093, Departemen Kesehatan Republik Indonesia, Jakarta.
Anonim, 1977, Materia Medika Indonesia I, 130 Departemen Kesehatan Republik Indonesia, Jakarta.
Anonim, 2000, Parameter Standar Umum Ekstrak Tumbuhan Obat, cetakan pertama, 16, Departemen Kesehatan RI, Jakarta.
Anonim, 2004, Monografi Ekstrak Tumbuhan Obat Indonesia, Volume 1, 51-54,122-123, Badan Pengawas Obat dan Makanan Republik Indonesia, Jakarta.
Anonim, 2008, Teknologi Penyiapan Simplisia Terstandar Tanaman Obat, Balai Penelitian Tanaman Obat dan Aromatik, file:///H:/KUNYIT/cara%20 panen% 20yang%20baik.htm, diakses pada tanggal 3 Desember 2008.
Ansel, 1985, Pengantar Bentuk Sediaan Farmasi, Edisi Keempat, diterjemahkan oleh Farida Ibrahim, 244-271, 608-617, UI Press, Jakarta.
Duke, 2008, Phytochemical and Ethnobotanical Databases http://www.ars- grin.gov/cgi-bin/duke/farmacy2.plhttp://www.ars-grin.gov/cgi-bin/duke/farmacy2.pl, diakses pada 7 April 2008.
Fardiaz, 1992, Mikrobiologi Pangan 1, 105, 195, PT Gramedia Pustaka Utma, Jakarta.
Fatah, A. M., 1989, Spektofotometri UV-Vis, 1-3; 7-8, Fakultas Farmasi Universitas Gadjah Mada, Yogyakarta.
Gritter, R.J., Bobit, J.M. dan Schwarting, A.E., 1991, Pengantar Kromatografi, diterjemahkan oleh Kosasih Padmawinata, Edisi II, 107-1555, Penerbit Insitut Teknologi Bandung, Bandung.
Harmita, 2004, Petunjuk Pelaksanaan Validasi Metode dan Cara Perhitungannya, Majalah Ilimu Kefarmasian, Vol. I, No. 3, 117 – 135,
http://jurnal.farmasi.ui.ac.id/pdf/2004/v01n03/Harmita010301.pdf, diakses pada tanggal 30 Oktober 2008.
Komarawinata, 2008, Budidaya dan Pasca Panen Tanaman Obat Untuk Meningkatkan Kadar Bahan Aktif, Unit Riset dan Pengembangan PT. Kimia Farma (Persero) Tbk., http://balittro.litbang.deptan.go.id/pdf/ edisikhusus/2006_02/edisi_khusus_2006_02_05.pdf, diakses pada tanggal 3 Desember 2008.
Rukmana, R., 1994, Kunyit, 13, 17-18, 25-27, Kanisius, Yogyakarta.
Skoog, D. A., 1985, Principles of Instrumental Analysis, Third edition, 183, Saunders College Publishing, New York.
Soedibjo, 1998, Alam Sumber Kesehatan Manfaat dan Kegunaan, 264-265, Balai Pustaka, Jakarta.
Stahl, E., 1985, Analisis Obat Secara Kromatografi dan Manajemen Agribisnis, P. T. Kepurun Pawana Indonesia, Universitas gajah Mada, Yogyakarta.
Stancovic, 2004, Chemical and Technical Assesment of Curcumin, 61stJECFA, 1(8) – 5(8) ftp://ftp.fao.org/es/esn/jecfa/cta/CTA_61_Curcumin.pdf, diakses pada tanggal 18 September 2008
Sudarsono, 1996, Tumbuhan Obat, 56, PPOT, UGM, Yogyakarta.
Sumiati, Triyani, S.Si., 2006, Kunyit, Si Kuning yang Kaya Manfaat,
http://www.pikiran-rakyat.com/cetak/ 0704/22/cakrawala/lainnya02. htm, diakses pada tanggal 12 Desember 2008.
Tampubolon, T., 1981, Tumbuhan Obat, 27-28, Bhatara Karya Aksara, Jakarta.
Voigt, 1971, Buku Pelajaran Teknologi Farmasi, Edisi Kelima, diterjemahkan oleh Soendani Noerono, 141-142, 159, 163-164, 172-178, 571, 586, Gadjah Mada University Press, Yogyakarta.
Wang YJ, Pan MH, Chong AL, Lim LI, HO YS, Hsieh CY, dan Lin JK, 1997, Stability of curcumin in buffer solution and characterization of its degradation products. J Pharm Biomed Anal15 : 1867 – 1876.
52