PREPARASI LIGAN ANILINDITIOKARBAMAT SEBAGAI
PENGOMPLEKS LOGAM TRANSISI MELALUI EKSTRAKSI CAIR-CAIR
SKRIPSI
Diajukan untuk Memenuhi Sebagian dari Syarat Memperoleh Gelar Sarjana Sains
Program Studi Kimia
Oleh
Vera Musfiroh
0807642
JURUSAN PENDIDIKAN KIMIA
FAKULTAS PENDIDIKAN MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS PENDIDIKAN INDONESIA
Preparasi Ligan Anilinditiokarbamat Sebagai Pengompleks Logam
Transisi Melalui Ekstraksi Cair-Cair
Oleh Vera Musfiroh
Sebuah skripsi yang diajukan untuk memenuhi salah satu syarat memperoleh gelar Sarjana Science pada Fakultas Pendidikan Matematika dan Ilmu Pengetahuan Alam
© Vera Musfiroh di 2013 Universitas Pendidikan Indonesia
April 2013
Hak Cipta dilindungi undang-undang.
LEMBAR PENGESAHAN
VERA MUSFIROH
PREPARASI LIGAN ANILINDITIOKARBAMAT SEBAGAI
PENGOMPLEKS LOGAM TRANSISI MELALUI EKSTRAKSI CAIR-CAIR
DISETUJUI DAN DISAHKAN OLEH :
Pembimbing I
Dra. Soja Siti Fatimah, M. Si.
NIP. 19680216199402001
Pembimbing II
Dra. Zackiyah, M. Si
NIP.1959122919912001
Mengetahui,
Ketua Jurusan Pendidikan Kimia FPMIPA UPI
Dr. rer. nat. Ahmad Mudzakir, M. Si
Abstrak
Senyawa ditiokarbamat merupakan senyawa organosulfur mengandung dua atom donor belerang yang bersifat nukleofil. Dalam bentuk terkoordinasi dengan logam, senyawa ditiokarbamat memiliki aplikasi yang luas. Reaksi antara anilin dan karbon disulfida pada suasana basa akan menghasilkan ligan anilinditiokarbamat. Ligan anilinditiokarbamat memiliki satu donor elektron yang digunakan untuk berikatan dengan logam. Karakterisasi dilakukan dengan menggunakan spektroskopi UV-VIS, FTIR, HPLC, dan XRD. Hasil analisis ligan pada spektra UV-VIS menunjukkan adanya pergeseran pita serapan yang signifikan terjadi pada ikatan NCS2 yang disebabkan oleh transisi elektron n-π*
pada 273 nm dan π – π* pada 204,0 nm. Sedangkan pada spektra FTIR menunjukkan adanya ikatan (C=N) pada bilangan gelombang 1450,4 cm-1 dan ikatan (C=S) pada bilangan gelombang 1002,9 cm-1 dan 1070, 4 cm-1. Pada HPLC, puncak kromatogram yang paling baik pada fasa gerak metanol : asetonitril dengan perbandingan 40:60. Berdasarkan data XRD ligan anilinditiokarbamat bersifat kristalit. Sedangkan hasil ekstraksi ligan anilinditiokarbamat dengan larutan logam Cu(II), Co(II), Cr(III) dan Ni(II) pada pH antara 4-9 menunjukan persen ekstraksi berkisar 90,45% - 99,99%.
Kata kunci : Senyawa organosulfur, Anilin, Anilinditiokarbamat.
Abstract
Dithiocarbamate compound is an organosulfur compound containing two atoms of sulfur donor nucleophiles that are easy to react with metals such as copper, iron, cobalt, and nickel. In the form of coordinated metal dithiocarbamate derivative compounds have large application. A mixture of aniline and carbon disulfide ligand would produce anilindithiocarbamate. Characterization is done by using VIS spectroscopy, FTIR, HPLC, and XRD. Analysis results ligands on UV-VIS spectra showed a significant shift in absorption bands occur in the bond
NCS2 caused by electron transitions π - π * at 273 nm and n-π * at 204.0 nm. While the FTIR spectra indicate the presence of a bond (C = N) in the wave number 1450.4 cm-1 and the bond (C = S) at wave number 1002.9 cm-1 and 1070, 4 cm-1. On HPLC, peak of chromatogram of the best the mobile phase of methanol: acetonitrile in the ratio 40:60. Based on the XRD difractogram of anilindithiocarbamate ligands are crystallites. While the results of solvent extraction of Cu (II), Co (II), Cr (III) and Ni (II) at pH between 4-9 shows the extraction percent ranged from 90.45% - 99.99%.
KATA PENGANTAR
Alhamdulillah, puji syukur kehadirat Allah SWT yang telah memberikan hidayah dan kekuatan-Nya sehingga penulis dapat menyelesaikan skripsi yang
berjudul “Preparasi Ligan Anilinditiokarbamat sebagai Pengompleks Logam Transisi melalui Ekstraksi Cair-cair” ini. Shalawat serta salam semoga selalu tercurah kepada junjungan kita, Nabi Muhammad SAW beserta para keluarga, sahabat dan orang-orang yang berjuang di jalan Allah SWT hingga akhir zaman. Skripsi ini disusun sebagai syarat memperoleh gelar sarjana sains kimia, Program Studi Kimia, Jurusan Pendidikan Kimia, Fakultas Pendidikan Matematika dan Ilmu Pengetahuan Alam, Universitas Pendidikan Indonesia.
Dalam menyusun skripsi ini tidak terlepas dari doa, dukungan, dan bantuan dari berbagai pihak. Dengan demikian, penulis mengucapkan terima kasih kepada :
1. Kedua Orang tua dan keluarga tercinta yang telah memberikan dukungan moriil, materil, dan doa.
2. Ketua Jurusan Pendidikan Kimia FPMIPA UPI, Dr. Ahmad Mudzakir, M.Si 3. Ketua Prodi Kimia FPMIPA UPI, Dr.Ratnaningsih Eko, M.Si.
4. Drs. Soja Siti Fatimah, M.Si selaku pembimbing I yang telah memberikan pengarahan dan bimbingan ketika praktek di laboratorium dan dalam penyusunan skripsi ini.
5. Drs. Zackiyah, M.Si selaku pembimbing II yang telah memberikan pengarahan dalam penyusunan skripsi ini.
6. Seluruh dosen Kimia UPI atas ilmu dan masukannya.
7. Seluruh staf dan laboran Jurusan Pendidikan Kimia yang telah memberikan bantuan dan kemudahan kepada penulis dalam pelaksaan praktikum maupun penelitian.
9. Julia, Mariya, Siti Robiah, Iis, Kamilah, Attin, Aprilia, Franscisca, Imas, Sefti, Ayu, Djati, Fatia, Rima, Pingky, dan teman-teman lainnya yang telah memberikan semangat dan motivasi.
10. Kepada semua pihak yang telah membantu penyelesaian skripsi yang tidak dapat penulis sebutkan satu per satu.
Penulis menyadari bahwa tulisan ini masih memiliki kekurangan, oleh karena itu kritik dan saran yang bersifat membangun demi perbaikan sangat penulis harapkan. Semoga skripsi ini dapat memberikan manfaat dan sumbangan ilmiah yang sebesar-besarnya bagi penulis maupun pembaca.
Bandung, April 2013
DAFTAR ISI
Halaman
ABSTRAK ... i
KATA PENGANTAR ... ii
DAFTAR ISI ... iv
DAFTAR TABEL ... vii
DAFTAR GAMBAR ... viii
DAFTAR LAMPIRAN ... ix
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Rumusan Masalah ... 3
1.3 Batasan Masalah ... 3
1.4 Tujuan Penelitian ... 3
1.5 Manfaat Penelitian ... 3
BAB II TINJAUAN PUSTAKA ... 4
2.1 Metode Pemisahan dalam Analisis Kimia ... 4
2.2 Jenis- jenis Ligan ... 5
2.2.1 Ligan Monodentat ... 6
2.2.2 Ligan Bidentat ... 6
2.2.4 Senyawa dan Kompleks Ditiokarbamat ... 7
2.3 Ekstraksi Pelarut atau Ekstraksi Cair-cair ... 10
2.3.1 Prinsip Dasar dari Ekstraksi Pelarut ... 12
2.4 Ekstraksi dengan Menggunakan Ligan Pengkhelat ... 14
BAB III METODE PENELITIAN ... 17
3.1 Waktu dan Lokasi Penelitian ... 17
3.2 Desain Penelitian ... 17
3.3 Alat dan Bahan ... 19
3.3.1 Alat ... 19
3.3.2 Bahan ... 20
3.4 Preparasi ... 20
3.4.1 Sintesis Ligan Anilinditiokarbamat ... 20
3.4.2 Pembuatan Larutan Logam Krom, Tembaga, Kobalt, dan Nikel 20 3.4.2.1 Pembuatan Larutan Logam Standar Kromium, Tembaga, Kobal, dan Nikel 1M ... 20
3.4.3 Pembuatan Larutan Buffer ... 21
3.5 Karakterisasi Ligan Anilinditiokarbamat ... 21
3.5.1 Uji Kelarutan ... 21
3.5.2 Uji Titik Leleh ... 21
3.5.3 Uji Nyala Unsur Kalium pada Ligan Anilinditiokarbamat ... 21
3.5.4 Karakterisasi Ligan dengan UV-VIS, HPLC, FTIR, dan XRD . 21 3.6 Aplikasi Ekstraksi Kompleks Logam Anilinditiokarbamat untuk Variabel pH ... 22
BAB IV HASIL DAN PEMBAHASAN ... 23
4.1 Sintesis Ligan Anilin Ditiokarbamat ... 23
4.2 Karakterisasi Ligan Anilinditiokarbamat ... 24
4.2.1 Uji Kelarutan Ligan Anilinditiokarbamat ... 24
4.2.3 Uji Nyala Ligan Anilinditiokarbamat ... 26
4.2.4 Spektroskopi UV-VIS Ligan Anilinditiokarbamat ... 26
4.2.5 Spektra FTIR Ligan Anilinditiokarbamat ... 28
4.2.6 Analisis Ligan Anilinditiokarbamat dengan Kromatografi Cair-cair (HPLC). ... 30
4.2.7 Difraktogram ligan Anilinditiokarbamat... 32
4.3 Aplikasi Ekstraksi Anilinditiokarbamat untuk Variabel pH ... 33
BAB V KESIMPULAN DAN REKOMENDASI ... 37
5.1 Kesimpulan ... 37
5.2 Rekomendasi... 37
DAFTAR PUSTAKA ... 38
DAFTAR TABEL
Halaman
DAFTAR GAMBAR
Halaman
Gambar 2.1 Ligan Bidentat... 6
Gambar 2.2 Ligan Polidentat ... 7
Gambar 2.3 Kerangka Ditiokarbamat ... 7
Gambar 2.4 Mekanisme Pembentukan Ligan Anilinditiokarbamat ... 8
Gambar 2.5 Struktur Senyawa Kompleks dari Logam dengan Bilangan Oksidasi 2 ... 10
Gambar 2.6 Struktur Senyawa Kompleks dari Logam dengan Bilangan Oksidasi 3 ... 10
Gambar 2.7. Hasil Plot Efisiensi Beberapa Logam menggunakan Dithizone dalam CCl4. Ion-ion logamnya adalah: (a) Cu2+; (b) Co2+; (c) Ni2+; (d)Sn2+; (e) Pb2+; dan (f) Cd2+. ... 15
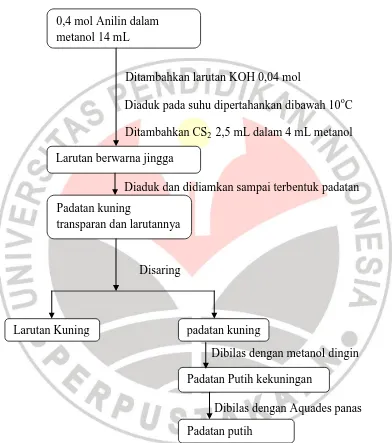
Gambar 3.1 Diagram Alir Sintesis Anilinditiokarbamat ... 18
Gambar 3.2 Diagram Alir Ekstraksi dengan Ligan Anilinditiokarbamat .... 19
Gambar 4.1 Data UV-VIS Anilin dalam Metanol ... 27
Gambar 4.3 Spektra FTIR Anilin ... 29 Gambar 4.4 Spektra FTIR Anilinditiokarbamat ... 29 Gambar 4.5 Ikatan Monodentat dan Bidentat. ... 30 Gambar 4.6 Kromatogram HPLCAnilin ditiokarbamat dengan perbandingan fasa gerak 40:60 ... 31 Gambar 4.7 Difraktogram XRD untuk Ligan Anilinditiokarbamat ... 33
DAFTAR LAMPIRAN
Halaman
BAB I
PENDAHULUAN
1.1 Latar Belakang
Ligan ditiokarbamat adalah ligan serbaguna yang mampu membentuk kompleks dan mampu menstabilkan logam transisi dalam berbagai bilangan oksidasi. Dalam bentuk terkoordinasi dengan logam, ligan ditiokarbamat memiliki aplikasi yang sangat beragam. (Khotib, 2010). Beberapa aplikasi dalam bidang kimia seperti kimia supramolekul. Sifat optik dan elektrokimia dari kompleks ditiokarbamat dapat digunakan untuk menghasilkan sensor untuk mendeteksi suatu molekul. Kompleks logam ditiokarbamat telah digunakan juga untuk nanopartikel dan kawat nano dari berbagai bahan semikonduktor. Selain itu, karena sifatnya sebagai agen pengkhelat, ligan ditiokarbamat dapat juga digunakan dalam treatment pengolahan air limbah. (Katari, 2012). Sedangkan dalam pembentukan senyawa kompleks, ligan ditiokarbamat dapat digunakan untuk memisahkan logam dari senyawa kompleksnya melalui ekstraksi.
Ekstraksi adalah proses pemisahan satu atau lebih komponen dari suatu campuran homogen menggunakan pelarut cair (solven) sebagai agen pemisah. Ekstraksi pelarut merupakan proses pemisahan suatu komponen dari suatu campuran berdasarkan proses distribusi terhadap dua macam pelarut yang tidak saling bercampur. Ekstraksi pelarut umumnya digunakan untuk memisahkan sejumlah gugus yang diinginkan dan mungkin merupakan gugus pengganggu dalam analisis secara keseluruhan. (Soebagio, dkk. 2003)
2
pemisahan selanjutnya. Ekstraksi perlu dilakukan sebagai upaya pemisahan dari ion logam lainnya yang dapat mengganggu dalam penetapan kadar suatu sampel. Agar ion logam tersebut dapat diekstraksi ke dalam fasa organik, maka ion-ion tersebut harus diubah menjadi bentuk molekul yang tidak bermuatan sehingga sifatnya sesuai dengan sifat pelarut organik yang nonpolar. Molekul yang tidak bermuatan itu berupa senyawa kompleks yaitu kompleks kelat (sepit) atau kompleks asosiasi ion. (Hamzah, 2008)
Perkembangan terakhir metode pemisahan secara ekstraksi cenderung ke arah peningkatan selektivitas terhadap logam tertentu dengan cara pencarian ligan-ligan baru melalui sintesis senyawa berbobot molekul besar atau polimer. Ligan merupakan komponen penting dalam proses pemisahan yang efisien dalam ekstraksi pelarut. Dengan demikian sangatlah penting dikembangkan ligan untuk ion-ion logam yang menjadi target dalam proses pemisahan, karena pemilihan pengompleks sangat menentukan keberhasilan proses pemisahan. Ligan yang baik adalah yang selektif, mudah dan sederhana pembuatannya, persen ekstraksinya tinggi, serta bersifat aman terhadap lingkungan.
Mayoritas dari senyawa ditiokarbamat disintesis dengan logam transisi. Logam-logam transisi merupakan asam yang baik dalam pembentukan senyawa kompleks dengan ligan basa anilinditiokarbamat. Prinsip yang digunakan adalah prinsip reaksi kondensasi dimana dua atau lebih molekul bergabung menjadi satu molekul yang lebih besar, dengan atau tanpa hilangnya suatu molekul. (Sembiring, 2008).
Sintesis ligan terjadi melalui reaksi kondensasi pada Anilin dan CS2
3
ion logam pusatnya, geometri senyawa kompleks logam ditiokarbamat dapat berbentuk tetrahedral, heksagonal, atau oktahedral. (Kaludjerovicet, et al., 2002).
Senyawa kompleks terbentuk akibat terjadinya kovalen koordinasi antara suatu atom atau ion logam dengan suatu ligan (ion logam atau molekul netral). Studi pembentukan kompleks menjadi hal yang menarik untuk dikembangkan karena kompleks yang terbentuk memberikan banyak manfaat dalam berbagai bidang seperti bidang kesehatan, farmasi, pertanian, industri dan lingkungan.
2.1 Rumusan Masalah
1. Bagaimana karakteristik anilinditiokarbamat hasil preparasi?
2. Bagaimana aplikasi ligan anilinditiokarbamat pada ekstraksi logam transisi?
3.1 Batasan Masalah
Adapun batasan masalahnya sebagai berikut:
1. Logam yang dijadikan sampel dalam penelitian ini adalah logam Cu, Cr, Ni, dan Co.
2. Variabel uji yang digunakan pada proses ekstraksi yaitu pH.
4.1 Tujuan Penelitian
Penelitian ini bertujuan untuk :
1. Mengetahui karakteristik ligan anilinditiokarbamat hasil preparasi.
2. Mengetahui aplikasi ligan anilinditiokarbamat pada ekstraksi logam transisi.
5.1 Manfaat Penelitian
Ada beberapa luaran yang diharapakn dari hasil penelitian ini, yaitu :
1. Memberikan informasi ilmiah mengenai pembentukan senyawa kompleks yang dapat digunakan untuk berbagai keperluan diantaranya pemurnian logam, ekstraksi pada pengolahan logam dan berbagai kebutuhan lainnya. 2. Menghasilkan artikel ilmiah yang dapat menjelaskan mekanisme dan
BAB III
METODE PENELITIAN
3.1 Waktu dan Lokasi Penelitian
Penelitian dilaksanakan dari bulan Juni tahun 2012 – Januari 2013 di Laboratorium Riset Kimia dan Laboratorium Kimia Analitik Instrumen Jurusan Pendidikan Kimia Fakultas Pendidikan Matematika dan Pengetahuan Alam Universitas Pendidikan Indonesia. Beberapa analisis hasil penelitian dilakukan di Laboratorium ITB dan UNPAD.
3.2 Desain Penelitian
18
Ditambahkan larutan KOH 0,04 mol
Diaduk pada suhu dipertahankan dibawah 10oC Ditambahkan CS2 2,5 mL dalam 4 mL metanol
Diaduk dan didiamkan sampai terbentuk padatan
Disaring
Dibilas dengan metanol dingin
Dibilas dengan Aquades panas
Gambar 3.1 Diagram alir preparasi Anilinditiokarbamat 0,4 mol Anilin dalam
metanol 14 mL
Larutan berwarna jingga
Padatan kuning
transparan dan larutannya
Padatan Putih kekuningan
19
Ditambahkan larutan ligan anilinditiokarbamat 1% dan larutan buffer antara pH 4-9 sebanyak 4 mL
Dikocok dan diekstraks dengan kloroform 7,5 mL selama 10 menit
Didiamkan Dipisahkan
Lakukan ekstraksi yang kedua kali
dengan kloroform 7,5 mL
Gambar 3.2 Diagram alir Ekstraksi dengan ligan Anilinditiokarbamat
3.3 Alat dan Bahan
3.3.1 Alat
Peralatan yang digunakan untuk sintesis ligan dan karakterisasi adalah gelas kimia, tabung vial, gelas ukur, spatula, batang pengaduk, tabung reaksi, pipet, pipet volumetri, ball pipet, magnetik stirer, vibrator ultrasonik, termometer, corong Pisah, plastik wrap, labu ukur, plat tetes, botol coklat, pengocok, aluminium foil, kertas saring, statif dan klep.
Larutan logam 100 ppm 10 mL
Campuran jernih dua fasa
Fasa Organik I Fasa air
20
Peralatan yang digunakan untuk karakterisasi ligan adalah set alat spektroskopi FTIR (SHIMADZU, FTIR-8400), XRD, HPLC dan UV-VIS. Adapun untuk mengukur kadar logam hasil ekstraksi adalah set alat AAS.
3.3.2 Bahan
Bahan-bahan yang digunakan pada penelitian ini adalah Karbon disulfida, Anilin, Aquades, Aseton, kalium hidroksida, Natrium asetat, larutan logam krom dari logam kromium (III) klorida, larutan logam tembaga dari logam tembaga (II) nitrat, larutan logam kobal dari logam kobal (II) klorida dan larutan logam nikel dari logam nikel (II) klorida, Asam asetat, Metanol, Klorofrom, Petroleum eter, Heksana, dan Etil asetat.
3.4 Preparasi
3.4.1 Preparasi Ligan Anilinditiokarbamat
Sebanyak 0,4 mol anilin dilarutkan kedalam 14 mL metanol, kemudian ditambahkan kalium hidroksida 0,04 mol dalam metanol kemudian diaduk secara konstan. Reaksi dipertahankan dibawah 10oC. Kemudian tambahkan karbon disulfida 0,04 mol sebanyak 2,5 mL dalam metanol, diaduk dan didiamkan dalam suhu ruangan sampai campuran tersebut terbentuk padatan, jika terbentuk padatan bilas dengan metanol kemudian rekristalisasi dengan aquades panas.
3.4.2 Pembuatan Larutan Logam Krom,Tembaga, Kobalt, dan Nikel
3.4.2.1Pembuatan Larutan Logam Standar Kromium, Tembaga, Kobal, dan Nikel 1M
21
3.4.3 Pembuatan Larutan Buffer
Sebanyak 4, 0824 gram serbuk natrium asetat ditimbang untuk membuat buffer dengan pH 4, setelah itu larutkan kedalam aquades sebanyak 100 mL, aduk sampai semua natrium asetat larut, kemudian buffer diukur pH nya dengan pHmeter sampai pH nya 4. Lakukan hal yang sama untuk membuat larutan buffer 5,6, 7, 8 dan 9.
3.5 Karakterisasi Ligan Anilinditiokarbamat
3.5.1 Uji Kelarutan
Masing-masing tabung reaksi diberi ligan dalam bentuk padatan, kemudian ditambahkan masing-masing sebanyak 10 mL pelarut. Pelarut yang dipakai yaitu etil asetat, metanol, kloroform, petroleum eter, heksana, aseton. Kemudian diaduk menggunakan ultrasonik vibrator selama 5 menit.
3.5.2 Uji Titik Leleh
Uji titik leleh dilakukan dengan cara memasukkan ligan anilin ditiokarbamat ke dalam pipa kapiler yang diletakkan dalam alat melting point, kemudian diamati saat ligan meleleh pertama kali dan ketika ligan meleleh seluruhnya.
3.5.3 Uji Nyala Unsur Kalium pada Ligan Anilinditiokarbamat
Kalium adalah logam putih perak yang lunak. Logam ini melebur pada 63,5°C, cepat teroksidasi dalam udara lembab. Logam itu menguraikan air dengan dahsyat, sambil melepaskan hidrogen dan terbakar dengan nyala lembayung.
Uji titik nyala dilakukan dengan cara memasukan ligan kedalam kawat krom yang sudah dibilas dengan HCl, kemudian dibakar dengan bunsen, nyala api dari ligan anilin ditiokarbamat dilihat dengan menggunakan kaca kobalt.
3.5.4 Karakterisasi Ligan dengan UV-VIS, HPLC, FTIR, dan XRD
22
1. Karakterisasi spektroskopi dengan menggunakan UV-VIS, FTIR, dan XRD.
2. Karakterisasi kromatografi dengan menggunakan HPLC.
3.6 Aplikasi Ekstraksi Anilinditiokarbamat untuk Variabel pH
BAB V
KESIMPULAN DAN REKOMENDASI
5.1 Kesimpulan
Berdasarkan hasil penelitian yang telah dilakukan, maka kesimpulan yang dapat diambil yaitu:
1. Ligan anilinditiokarbamat yang dihasilkan sebanyak 3,16 gram yang memiliki titik leleh berkisar 148-152oC. Pada spektrum UV-VIS memiliki absorbansi maksimum pada 273 nm dan 204,0 nm. Sedangkan pada spektra FTIR menunjukkan adanya ikatan (C=N) pada bilangan gelombang 1450,4 dan ikatan (C=S) pada bilangan gelombang 1002,9 dan 1070, 4. Pada kromatogram HPLC, menggunakan fasa gerak metanol : asetonitril dengan perbandingan 40:60. Berdasarkan data XRD ligan anilinditiokarbamat bersifat kristalit.
2. Berdasarkan hasil ekstraksi, pH memiliki peranan yang sangat baik dalam pemisahan sehingga persen ekstraksi untuk setiap logam berkisar antara 90,73 - 99,99%.
5.2Rekomendasi
Dari penelitian yang telah dilakukan, rekomendasi yang dapat diberikan untuk penelitian berikutnya:
1. Lakukan ekstraksi dengan menggunakan logam lain untuk membandingkan persen ekstraksi.
2. Selain rekristalisasi, lakukan analisis kuantitatif seperti NMR untuk mengetahui kemurnian ligan.
38
DAFTAR PUSTAKA
Arsyad, M. N. (1997). Kamus Kimia Arti dan Penjelasan Istilah. Jakarta: Gramedia.
Cotton, Albert dan Wilkinson, Geoffrey. (1989). Kimia Anorganik Dasar. Jakarta: Universitas Indonesia (UI-Press). 628-630.
Effendy. (2007). Kimia Koordinasi Jilid I. Malang:Jurusan Kimia Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas Negeri Malang(UNM).
Griffo & Keshavan. (2007). High Performance Rock Bit Grease.
Hamzah, Baharuddin. (2008). Sintesis Ligan Kelat
4-Benzoil-1-Fenil-3-Metil-2-Pirazolin-5-On Dan Aplikasinya Pada Ekstra Ksi Ion Nikel Dalam Larutan.
J. Sains & Teknologi. Palu: Jurusan Pendidikan Kimia, Universitas Tadulako.
Kaludjerovic, et al,. 2002. Synthesis and characterization of
tris-butyl-(1-methyl-3-phenyl-propyl)-dithiocarbamato]-cobalt(III) seskvitoluene.
J.Serb.Chem.Soc. 67, (2), 123–126.
Khopkar, S. M. (1990). Konsep Dasar Kimia Analitik. Jakarta: Universitas Indonesia Press.
Khotib, Mohammad. (2010). Density Funtional Theory Dalam Sintesis,
Karakterisasi, Dan Prediksi Aplikasi Senyawa Zn-Dialkylditiokarbamat
Rantai Panjang. Bogor : Insitut pertanian Bogor(IPB).
Laddha, G.S. and Degalesan, T.E. (1976). Transport Phenomena in Liquid
Extraction. New Delhi: Tata Mc Graw-Hill Publishing Co, ltd.
Manav, N, et al.,( 2006). In vitro antitumour and antibacterial studies of some
39
Katari, Naresh Kumar. 2012. Studies directed towards the synthesis of
dithiocarbamates and its application in organic synthesis. India: Jawaharlal
Nehru Technological University.
Permanasari, Ana, dkk. (2007). Kimia Analitik 2. Jakarta: Universitas Terbuka. R. A. Day dan A.L. Underwood. (2002). Analisis kimia kuantitatif. Edisi ke-6.
Jakarta: Erlangga.
Sembiring, Zipora. (2008). Sintesis Senyawa Kompleks Cu(II) dan Mn(II) dengan
Derivat Ligan Basa Schiff 1,5 Dimethylcarbazone dan Anilina. Lampung:
Seminar Hasil Penelitian & Pengabdian kepada Masyarakat Unila.
Siddiqi, et al., (2006). Template synthesis of symmetrical transition metal
dithiocarbamates. Brazil: J. Braz.Chem. Soc. 17, (1), 107-112.
Skoog, Douglas, A. (2004). Fundamentals of Analitical Chemistry Eight Edition. Kanada: Brooks/Cole.
Soebagio, dkk. (2003). Kimia Analitik II. Malang: Jurusan Pendidikan Kimia FPMIPA, Universitas Negeri Malang.
Thoifahmuthohharoh. (2003). Senyawa Kompleks. [Online]. Tersedia: thoifahmut.wordpress.com/2011/04/30/senyawa-kompleks/. [30 januari 2012].
Vasiliev, A.N. & Polackov, A.D. (2000). Synthesis of Potassium
(1,1-Dioxothiolan-3-yl)-dithiocarbamate. Molecules. 5, (10), 14-101.