i
UJI AKTIVITAS ANTIBAKTERI EKSTRAK ETANOL DAUN JERUK BALI (Citrus maximaMerr.) TERHADAP
PERTUMBUHAN BAKTERI PADA JERAWAT
TUGAS AKHIR
Diajukan untuk memenuhi salah satu persyaratan memperoleh gelar Ahli Madya D3 Farmasi
Oleh :
KHARISMA QONITAH
NIM. M3509037
DIPLOMA 3 FARMASI
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SEBELAS MARET
perpustakaan.uns.ac.id digilib.uns.ac.id
iii
PERNYATAAN
Antibakteri Ekstrak Etanol Daun Jeruk Bali (Citrus maxima Merr.) terhadap Pertumbuhan Bakteri pada Jerawat adalah penelitian saya sendiri dan tidak terdapat karya yang pernah diajukan untuk memperoleh gelar apapun disuatu perguruan tinggi, serta tidak terdapat karya atau pendapat yang pernah ditulis atau diterbitkan oleh orang lain, kecuali secara tertulis diacu dalam naskah ini dan disebutkan dalam daftar pustaka.
Apabila di kemudian hari dapat ditemukan adanya unsur penjiplakan maka gelar yang telah diperoleh dapat ditinjau dan/atau dicabut.
Surakarta, Desember 2012
perpustakaan.uns.ac.id digilib.uns.ac.id
iv
UJI AKTIVITAS ANTIBAKTERI EKSTRAK ETANOL DAUN JERUK BALI (Citrus maximaMerr.) TERHADAP
PERTUMBUHAN BAKTERI PADA JERAWAT
KHARISMA QONITAH
Jurusan D3 Farmasi, Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Sebelas Maret Surakarta
INTISARI
Jerawat merupakan salah satu penyakit yang disebabkan oleh bakteri dan umumnya ditemukan pada usia remaja. Walaupun telah banyak antibiotik ditemukan, kenyataan menunjukkan bahwa masalah penyakit terus berkelanjutan, sehingga diperlukan senyawa antibakteri baru yang dapat mengatasi jerawat. Flavonoid merupakan salah satu kandungan daun jeruk bali (Citrus maxima
Merr.) yang dikenal memiliki potensi sebagai agen antibakteri. Tujuan dari penelitian ini untuk mengetahui : a. bentuk dan susunan sel serta sifat Gram bakteri pada jerawat yang diisolasi dari apusan darah jerawat, b. potensi aktivitas antibakteri dari ekstrak etanol daun jeruk bali terhadap pertumbuhan bakteri pada jerawat, c. konsentrasi optimum ekstrak etanol daun jeruk bali yang mampu menghambat pertumbuhan bakteri pada jerawat.
Senyawa aktif yang terkandung dalam daun jeruk bali diekstraksi menggunakan metode maserasi dengan pelarut etanol 75%. Uji aktivitas antibakteri ekstrak etanol daun jeruk bali dilakukan dengan metode difusi agar dengan seri konsentrasi 10-100%. Sebagai kontrol digunakan CMC-Na 0,1%, etanol 75% dan klindamisin 0,025%.
Hasil isolasi dari apusan darah jerawat didapatkan bakteri bentuk kokus Gram positif, bentuk basil Gram positif dan bentuk basil Gram negatif. Hasil uji aktivitas antibakteri menunjukan bahwa aktivitas penghambatan optimum terjadi pada konsentrasi 80% dengan DDH sebesar 5,29 mm terhadap bakteri bentuk kokus Gram positif, pada konsentrasi 90% dengan DDH sebesar 4,39 mm terhadap bakteri bentuk basil Gram positif dan pada konsentrasi 90% dengan DDH sebesar 4,34 mm terhadap bakteri bentuk basil Gram negatif. Dari hasil penelitian ini ekstrak etanol daun jeruk bali memiliki daya hambat yang bersifat lemah namun memiliki spektrum kerja antibakteri luas yaitu mampu menghambat bakteri Gram positif dan Gram negatif.
v
THE ANTIBACTERIAL ACTIVITY OF ETHANOL EXTRACT OF POMELO (Citrus maximaMerr.) LEAF
ON THE GROWTH OF BACTERIA IN ACNE
KHARISMA QONITAH
Departement of Pharmacy, Faculty of Mathematics and Natural Sciences Sebelas Maret University, Surakarta
ABSTRACT
Acne is disease caused by bacteria and is commonly found in adolescence. Although many antibiotics have been discovered, the reality shows that still ongoing disease problems, so needed new antibacterial compounds that can treat acne. Flavonoids are a compound of pomelo (Citrus maxima Merr.) leaf are known to have potential as an antibacterial agent. The purpose of this study to determine : a. shape and arrangement of cells and the Gram of bacteria in acne that isolated from blood smears acne, b. potential antibacterial activity of ethanol extract of pomelo leaf on the growth of bacteria in acne, c. the optimum concentration of ethanol extract of pomelo leaf were able to inhibit the growth of bacteria in acne.
The active compound contained in pomelo leaf extracted using maceration with ethanol 75%. The antibacterial activity of ethanol extract of pomelo leaf conducted by agar diffusion method with a series of concentration of 10-100%. As a control used CMC-Na 0.1%, ethanol 75% and Clindamycin 0.025%.
The result of isolation from blood smears acne obtained Gram-positive cocci bacteria form, Gram-positive bacilli bacteria form and Gram-negative bacilli bacteria form. The result of the antibacterial activity showed that the optimum inhibitory activity occurred at concentrations of 80% with DDH at 5.29 mm against Gram-positive cocci bacteria form, at concentration of 90% with DDH at 4.39 mm against Gram-positive bacteria bacilli form and at concentration of 90% with DDH at 4.34 mm against Gram-negative bacteria bacilli form. From the results of this study ethanol extract of pomelo leaf has weak potency to inhibit bacteria but has broad spectrum to the test bacteria.
perpustakaan.uns.ac.id digilib.uns.ac.id
vi MOTTO
orang yang berhenti belajar akan menjadi pemilik masa lalu. Orang-orang yang masih terus belajar, akan menjadi pemilik masa depan
--Mario
Teguh--Tugas kita bukanlah untuk berhasil. Teguh--Tugas kita adalah untuk mencoba, karena didalam mencoba itulah kita menemukan dan belajar membangun kesempatan
untuk berhasil
--Mario
Teguh--Verily, along with every hardship is relief So
And to your Lord (Alone) turn (all your) intentions and hopes
vii
perpustakaan.uns.ac.id digilib.uns.ac.id
viii
KATA PENGANTAR
Puji syukur penulis panjatkan ke hadirat Tuhan Yang Maha Esa yang telah melimpahkan rahmat dan karunia-Nya sehingga penulis dapat menyelesaikan Uji Aktivitas Antibakteri Ekstrak Etanol Daun Jeruk
Bali (Citrus maxima Merr.) terhadap Pertumbuhan Bakteri pada Jerawat
dengan baik dan lancar. Penyusunan laporan tugas akhir merupakan salah satu syarat untuk dapat memperoleh gelar Ahli Madya Farmasi di Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Sebelas Maret Surakarta.
Dalam penulisan laporan Tugas Akhir ini penulis telah berusaha semaksimal mungkin untuk memberikan hasil yang terbaik. Dan tak mungkin terwujud tanpa adanya dorongan, bimbingan, semangat, motivasi serta bantuan baik mori
kesempatan ini mengucapkan terima kasih dan penghargaan serta penghormatan setinggi-tingginya kepada:
1. Prof. Ir. Ari Handono Ramelan, M.Sc.(Hons), Ph.D., selaku Dekan Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Sebelas Maret Surakarta. 2. Bapak Ahmad Ainurofiq, M.Si., Apt., selaku Ketua Program Studi D3
Farmasi Universitas Sebelas Maret Surakarta.
3. Ibu Estu Retnaningtyas N., S.TP., M.Si., selaku pembimbing Tugas Akhir atas segala ketulusan, kesabaran dan keikhlasannya dalam memberikan arahan pengertian, saran, dan ilmunya yang tiada tara nilainya.
ix
5. Seluruh staf pengajar dan karyawan Program Studi D3 Farmasi, Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Sebelas Maret Surakarta. 6. Ayah, Ibu dan adik-adikku tersayang yang telah memberikan dukungan dan
semangat.
7. Sahabat-sahabatku yang selalu ada disehat dan sakitku, disuka dan dukaku, disantai dan sibukku.
8. Teman-teman seperjuangan khususnya teman-teman angkatan 2009 yang telah berbagi suka dan duka serta pengalaman selama masa-masa kuliah.
9. Semua pihak yang tidak dapat disebutkan satu persatu, yang telah membantu pelaksanaan Tugas Akhir dan penyusunan laporan ini. Penulis hanya dapat
membalas dengan yang terbaik.
Penulis menyadari masih banyak kekurangan dalam penulisan laporan Tugas Akhir ini. Untuk itu penulis mengharapkan adanya kritik dan saran yang membangun dari semua pihak untuk perbaikan sehingga akan menjadi bahan pertimbangan dan masukan untuk penyusunan tugas-tugas selanjutnya. Penulis berharap semoga laporan Tugas Akhir ini dapat bermanfaat bagi pembaca pada umumnya dan dapat menjadi bekal bagi penulis dalam pengabdian Ahli Madya Farmasi di masyarakat pada khususnya.
Surakarta, Desember 2012
perpustakaan.uns.ac.id digilib.uns.ac.id
x DAFTAR ISI
Halaman
HALAMAN JUDUL ... i
HALAMAN PENGESAHAN ... ii
HALAMAN PERNYATAAN ... iii
INTISARI ... iv
ABSTRACT ... v
MOTTO ... vi
PERSEMBAHAN ... vii
KATA PENGANTAR ... viii
DAFTAR ISI ... x
DAFTAR TABEL... xiii
DAFTAR GAMBAR ... . xiv
DAFTAR LAMPIRAN ... xvi
DAFTAR SINGKATAN ... xvii
BAB I. PENDAHULUAN 1 A. Latar Belakang Masalah... 1
B. Perumusan Masalah ... 3
C. Tujuan Penelitian... 4
D. Manfaat Penelitian... 4
BAB II. TINJAUAN PUSTAKA 5 A. Jeruk Bali (Citrus maximaMerr.) ... 5
A.1. Klasifikasi Tumbuhan ... 5
A.2. Nama Lokal dan Sinonim ... 5
A.3. Morfologi Tumbuhan... 6
A.4. Kandungan Kimia dan Manfaat... 6
A.5. Flavonoid... 7
B. Metode Penyarian... 9
B.1. Ekstraksi... 9
xi
C. Jerawat... 10
C.1. ... 10
C.2. ... 11
D. ... 12
E. Pewarnaan Gram Bakteri 13 15 G. Antibakteri... 16
H. Uji Aktivitas Antibakteri... 18
18 I. Kerangka Pemikiran... 19
J. Keterangan Empiris... 21
BAB III. METODE PENELITIAN 23 A. Desain Penelitian... 23
B. Waktu dan Tempat Penelitian... 23
C. Alat dan Bahan... 23
C.1 Alat yang digunakan ... 23
C.2 Bahan yang digunakan... 24
D. Cara Kerja... 25
D.1. Penyiapan Alat... 26
D.2. Determinasi dan Preparasi Sampel... 26
D.3. Ekstraksi ... 27
D.4. Pengambilan Apusan, Isolasi dan Identifikasi Bakteri Uji 28 31 D.6. Uji Aktivitas Antibakteri... 34
E. Analisis Hasil ... 42
BAB IV. HASIL DAN PEMBAHASAN ... 43
A. Determinasi dan Pengumpulan Sampel ... 43
B. Penyiapan Bahan ... 43
C. 44 D. Pengambilan Apusan Darah Jerawat ... 46
perpustakaan.uns.ac.id digilib.uns.ac.id
xii
F. Pembuatan S 54
G. Uji Aktivitas Antibakteri Ekstrak Etanol Daun Citrus maxima... 55
BAB V. PENUTUP... 63
A. Kesimpulan ... 63
B. Saran ... 63
DAFTAR PUSTAKA ... 64
xiii
DAFTAR TABEL
Halaman Tabel I. Kategori daya hambat bakteri ... 19 Tabel II. Komposisi Bahan dalam Pembuatan Seri Konsentrasi Ekstrak
Etanol Daun Jeruk Bali (Citrus maxima Merr.) ... 37 Tabel III. Hasil Pengecatan Gram Koloni Bakteri yang Tumbuh dari
Apusan Darah Jerawat ... 49 Tabel IV. Hasil uji aktivitas antibakteri ekstrak etanol daun Citrus maxima
perpustakaan.uns.ac.id digilib.uns.ac.id
xiv
DAFTAR GAMBAR
Halaman
Gambar 1. Jeruk bali (Citrus maximaMerr.) ... 5
Gambar 2. Stuktur Kimia Senyawa Flavonoid ... 8
Gambar 3. Struktur Kimia Senyawa Naringin ... 9
Gambar 4. Alur Kerangka Pemikiran ... 21
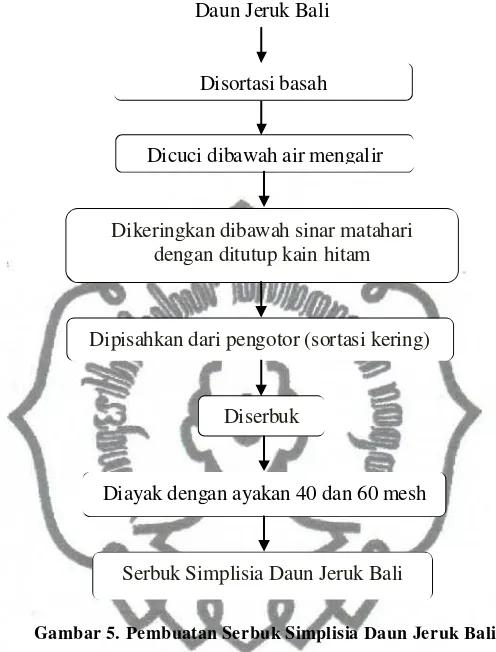
Gambar 5. Pembuatan Serbuk Simplisia Daun Jeruk Bali ... 27
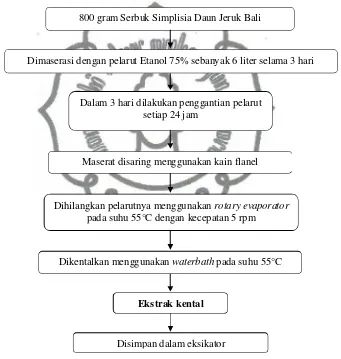
Gambar 6. Pembuatan Ekstrak Etanol Daun Jeruk Bali ... 28
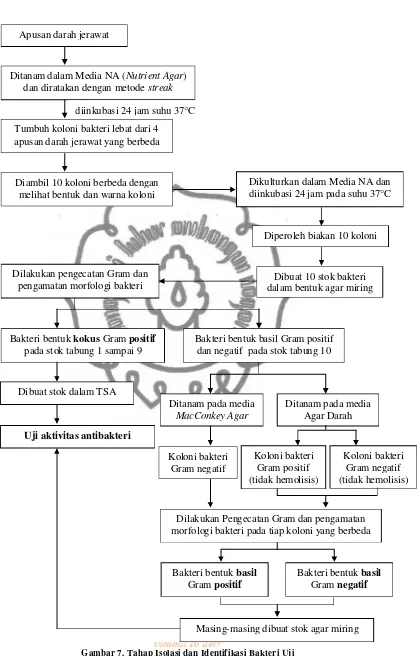
Gambar 7. Tahap Isolasi dan Identifikasi Bakteri Uji ... 30
Gambar 8. Pengecatan Gram Bakteri Uji ... 33
Gambar 9. Pembuatan Stok Bakteri Uji ... 36
Gambar 10. Pembuatan Seri Konsentrasi Ekstrak Etanol Daun Jeruk Bali .. 38
Gambar 11. Pengujian Aktivitas Antibakteri Metode Difusi Padat ... 41
Gambar 12. Koloni bakteri yang tumbuh dari apusan darah jerawat ... 47
Gambar 13. Sepuluh stok bakteri hasil isolasi tahap I ... 48
Gambar 14. (A) Pertumbuhan koloni bakteri nomor 1-9 (B) Hasil pengecatan stok bakteri tabung 1-9 (C) Pertumbuhan koloni bakteri nomor 10 (D) Hasil pengecatan stok bakteri tabung 10 ... 50
Gambar 15. Pertumbuhan koloni bakteri tabung 10 pada (A) media MacConkey Agar(B) media Agar Darah ... 51 Gambar 16. (A) Hasil pengecatan bakteri bentuk kokus Gram positif.
(B) Pertumbuhan koloni bakteri bentuk kokus Gram positif. (C) Stok bakteri bentuk kokus Gram positif. 52 Gambar 17. (A) Hasil pengecatan bakteri bentuk basil Gram positif.
(B) Pertumbuhan koloni bakteri bentuk basil Gram positif.
(C) Stok bakteri bentuk . 53
xv
Gambar 19. Hasil uji aktivitas antibakteri ekstrak etanol daun Citrus maxima
perpustakaan.uns.ac.id digilib.uns.ac.id
xvi
DAFTAR LAMPIRAN
Halaman Lampiran 1. Determinasi Tanaman Jeruk Bali (Citrus maximaMerr.) 69
Lampiran 2. Perhitungan Rendemen 70
Lampiran 3. Hasil Pemindahan 10 Koloni Bakteri dari Apusan Darah
Jerawat 71
Lampiran 4. Ekstrak Etanol Daun Citrus maximadan Seri Konsentrasi
Ekstrak Etanol Daun Citrus maxima 72
Lampiran 5. Hasil Uji Aktivitas Antibakteri Ekstrak Etanol Daun Jeruk Bali (Citrus maximaMerr.) terhadap Bakteri Bentuk Kokus
Gram Positif 73
Lampiran 6. Hasil Uji Aktivitas Antibakteri Ekstrak Etanol Daun Jeruk Bali (Citrus maximaMerr.) terhadap Bakteri Bentuk Basil
Gram Positif 74
Lampiran 7. Hasil Uji Aktivitas Antibakteri Ekstrak Etanol Daun Jeruk Bali (Citrus maximaMerr.) terhadap Bakteri Bentuk Basil
xvii
DAFTAR SINGKATAN
µ L : mikroliter
cm :centimeter
CMC-Na : Natrium Carboxymetilcellulose DDH : Diameter Daya Hambat
LAF :Laminar Air Flow
MHA :Mueller Hinton Agar
mm : milimeter
ml : mililiter
NA :Nutrient Agar
NB :Nutrient Broth
TSA :Tryptone Soya Agar
perpustakaan.uns.ac.id digilib.uns.ac.id
1 BAB I
PENDAHULUAN
A. Latar Belakang Masalah
Penyakit infeksi merupakan salah satu jenis penyakit yang banyak diderita masyarakat luas. Infeksi dapat ditularkan dari satu orang ke orang lain atau dari hewan ke manusia. Infeksi dapat disebabkan oleh berbagai mikroorganisme seperti bakteri, virus, riketsia, jamur, dan protozoa (Gibson, 1996).
Jerawat merupakan salah satu penyakit yang disebabkan oleh bakteri dan umumnya ditemukan pada usia remaja. Penyakit ini dijumpai pada hampir semua (90%) periode akil baliq yang menginjak masa pubertas pada usia 15-19 tahun, orang dewasa dan dapat juga pada usia lanjut. Jerawat adalah peradangan kronik folikel pilosebaseus dengan gambaran klinis berupa komedo, papul, pustul, nodus dan kista yang terutama didapatkan di daerah kulit yang kaya akan kelenjar sebasea seperti muka, leher, dada dan punggung (Djuanda dkk., 2007). Menurut Athikomkulchai, et al. (2008) faktor utama yang terlibat dalam pembentukan jerawat adalah peningkatan produksi sebum, peluruhan keratinosit, pertumbuhan bakteri dan inflamasi. Bakteri yang sering berperan pada pertumbuhan jerawat yaitu Propionibacterium acne dan Staphylococcus epidermidis (Djuanda dkk., 2007).
2
Propionibacterium acne dapat diturunkan dengan memberikan suatu zat antibakteri seperti eritromisin, klindamisin dan benzoil peroksida.
Sampai saat ini belum ada cara penyembuhan yang tuntas terhadap jerawat, meskipun ada beberapa cara yang sangat menolong. Salah satunya penggunaan antibiotik sebagai solusi untuk jerawat yang beberapa dekade ini masih banyak diresepkan (Yang, et al., 2009). Walaupun telah banyak antibiotik ditemukan, kenyataan menunjukkan bahwa masalah penyakit terus berkelanjutan. Hal tersebut terjadi akibat pergeseran pada bakteri penyebab penyakit dan perkembangan resistensi bakteri terhadap antibiotik. Karena berkembangnya populasi bakteri yang resisten, maka antibiotik yang pernah efektif untuk mengobati penyakit-penyakit tertentu kehilangan nilai kemoterapeutiknya (Pelczar dan Chan, 1988).
Pemanfaatan bahan alam sebagai obat tradisional di Indonesia akhir-akhir ini meningkat, bahkan beberapa bahan alam telah diproduksi secara fabrikasi dalam skala besar. Penggunaan obat tradisional dinilai memiliki efek samping yang lebih kecil dibandingkan dengan obat yang berasal dari bahan kimia, di samping itu harganya lebih terjangkau (Tampubolon, 1981).
perpustakaan.uns.ac.id digilib.uns.ac.id3
aeruginosa, Klebsiella pneumonia dan Staphylococcus aureus. Penelitian yang dilakukan oleh Pinkee Pandey, et al. (2010) menyatakan bahwa ekstrak etanol daun jeruk lemon (Citrus limon) yang mengandung flavonoid, tanin, alkaloid, steroid dan glikosida juga memiliki aktivitas antibakteri terhadap Escherichia coli,
Pseudomonas aeruginosa,Klebsiella pneumonia, Staphylococcus aureus, Bacillus subtilis danSalmonella typhimurium.
Pada penelitian Thavanapong (2006) kandungan dalam daun jeruk bali diantaranya adalah: asam amino, n-methylanthranilate, karbohidrat, flavonoid, monoterpen, sesquiterpen, triterpen, asam fumarat, asam malonat, asam oksalat, asam suksinat, asam tartrat.
Berdasarkan penelitian yang telah dilakukan oleh Thavanapong (2006), Ekwenye dan Edeha (2010) dan Pinkee Pandey, et al. (2010), penelitian ini dimaksudkan untuk menguji aktivitas antibakteri ekstrak etanol daun jeruk bali (Citrus maxima Merr.) terhadap pertumbuhan bakteri pada jerawat karena di dalam daun jeruk bali (Citrus maxima Merr.) terdapat kandungan senyawa metabolit yang hampir sama dengan yang terkandung dalam daun jeruk manis (Citrus sinesis) dan daun jeruk lemon (Citrus limon)diantaranya adalah flavonoid yang memiliki potensi sebagai agen antibakteri.
B. Perumusan Masalah
Berdasarkan latar belakang masalah di atas maka dirumuskan beberapa permasalahan sebagai berikut:
2. Apakah ekstrak etanol daun jeruk bali (Citrus maxima Merr.) memiliki aktivitas antibakteri terhadap pertumbuhan bakteri pada jerawat ?
3. Berapakah konsentrasi optimum ekstrak etanol daun jeruk bali (Citrus maxima Merr.) yang mampu menghambat pertumbuhan bakteri pada jerawat ?
C. Tujuan Penelitian
1. Mengetahui bentuk dan susunan sel serta sifat Gram bakteri pada jerawat yang diisolasi dari apusan darah jerawat.
2. Mengetahui potensi aktivitas antibakteri dari ekstrak etanol daun jeruk bali (Citrus maximaMerr.) terhadap pertumbuhan bakteri pada jerawat.
3. Mengetahui konsentrasi optimum ekstrak etanol daun jeruk bali (Citrus maxima Merr.) yang mampu menghambat pertumbuhan bakteri pada jerawat.
D. Manfaat Penelitian
1. Melalui penelitian ini diharapkan ekstrak etanol daun jeruk bali (Citrus maxima Merr.) dapat digunakan sebagai agen antibakteri terhadap pertumbuhan bakteri pada jerawat.
perpustakaan.uns.ac.id digilib.uns.ac.id
5 BAB II
TINJAUAN PUSTAKA
A. Jeruk Bali (Citrus maximaMerr.)
1. Klasifikasi Tumbuhan
Divisi : Spermatophyta (berbiji)
Sub Divisi : Angiospermae (berbiji tertutup) Kelas : Dicotylendonae (berkeping dua) Sub kelas : Choripetalae
Bangsa : Geraniales
Suku : Rutaceae
Marga :Citrus maxima
Jenis :Citrus maxima(Burm. Fz) Merr (Van Steenis, 1978).
Gambar 1. Daun Jeruk Bali (Citrus maximaMerr.)(Anonim, 2012)
2. Nama Lokal dan Sinonim
Sinonim: Citrus Celebia, koord, Sin; Citrus decumanus L, Sin; Citrus grandisL, Osbeck (Nuraini, 2011).
3. Morfologi Tumbuhan
Jeruk bali (Citrus maxima Merr.) merupakan tumbuhan menahun (perennial) dengan karakteristik tinggi pohon 5-15 meter. Batang tanaman agak kuat, garis tengah 10-30 cm, berkulit agak tebal, dimana kulit bagian luarnya berwarna coklat kekuningan dan bagian dalamnya berwarna kuning. Pohon jeruk mempunyai banyak cabang yang terletak saling berjauhan dan merunduk pada bagian ujungnya. Cabang yang masih muda bersudut dan berwarna hijau, tetapi lama-lama menjadi berbentuk bulat dan berwarna hijau tua (Nuraini, 2011).
Daun tanaman berbentuk bulat telur dan berukuran besar dengan bagian puncak atau ujung tumpul dan bagian tepi hampir rata, serta bagian dekat ujung agak berombak. Lerak daun terpencar dengan tangkai daun bersayap lebar, warna kekuningan, dan berbulu agak suram. Buah berbentuk bulat atau bola yang tampak tertekan dan berkulit agak tebal, berisi 11-16 segmen. Warna daging buah merah muda atau merah jambu dengan tekstur keras sampai lunak, rasa manis sampai sedikit asam, dan berbiji sedikit (Nuraini, 2011).
4. Kandungan Kimia dan Manfaat
perpustakaan.uns.ac.id digilib.uns.ac.id7
dan fosfor 27 mg. Kandungan lain seperti flavonoid, pektin dan lycopene
(Sekar, T. R., 2011).
Kandungan senyawa kimia dalam daun jeruk bali (Citrus maxima Merr.) diantaranya adalah: asam amino (alanine, asparagine, asam aspartat, coline, asam glutamat, glycine, proline), n-methylanthranilate, karbohidrat (phytol,
fructose, glucose), flavonoid (acacetin, cosmosiin, luteolin, naringenin,
naringin, narirutin, neoriocitrin, neohesperidin, poncirin, rhoifolin, rutin), monoterpen ( -pinene, -pinene,citral,citronellal,geraniol acetate, limonene,
linalool, linalyl acetate, myrcene, neral), sesquiterpen ( -caryophyllene), triterpen (limonin, nomilin, obacunone), asam fumarat, asam malonat, asam oksalat, asam suksinat, asam tartrat (Thavanapong, 2006).
Senyawa yang terkandung di dalam jeruk bali mampu mencegah kanker, menurunkan resiko penyakit jantung, melancarkan saluran pencernaan, menjaga kesehatan kulit, mencegah konstipasi, menurunkan kolesterol dan mencegah anemia (Sekar, T. R., 2011). Manfaat lain jeruk bali, yakni membersihkan sel darah merah yang telah tua didalam tubuh dan menormalkan hematokrit (persentase sel darah per volume darah) (Yanuarta, I. M., 2007). Kandungan kalium dari jeruk bali dapat menyehatkan prostat dan kandungan bioflavonoidnya dapat menghentikan penyebaran sel-sel kanker payudara (Anonim, 2009).
5. Flavonoid
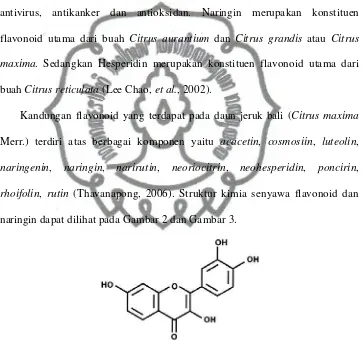
(misalnya bawang merah, kale, brokoli, paprika hijau, bayam), kedelai dan rempah-rempah. Flavonoid terdapat di sebagian besar tanaman dengan konsentrasi tinggi ditemukan pada kulit buah, daun dan bunga. Dalam beberapa tahun terakhir, flavonoid telah menarik perhatian karena flavonoid memiliki berbagai keuntungan efek farmakologi termasuk antiinflamasi, anti-alergi, antivirus, antikanker dan antioksidan. Naringin merupakan konstituen flavonoid utama dari buah Citrus aurantium dan Citrus grandis atau Citrus maxima. Sedangkan Hesperidin merupakan konstituen flavonoid utama dari buahCitrus reticulata(Lee Chao, et al., 2002).
Kandungan flavonoid yang terdapat pada daun jeruk bali (Citrus maxima
Merr.) terdiri atas berbagai komponen yaitu acacetin, cosmosiin, luteolin,
naringenin, naringin, narirutin, neoriocitrin, neohesperidin, poncirin,
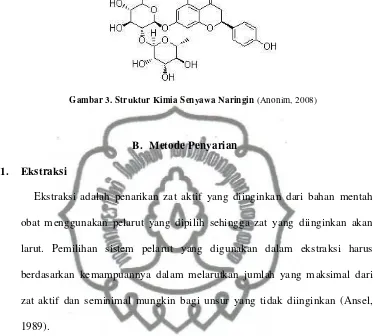
rhoifolin, rutin (Thavanapong, 2006). Struktur kimia senyawa flavonoid dan naringin dapat dilihat pada Gambar 2 dan Gambar 3.
perpustakaan.uns.ac.id digilib.uns.ac.id9
Gambar 3. Struktur Kimia Senyawa Naringin(Anonim, 2008)
B. Metode Penyarian
1. Ekstraksi
Ekstraksi adalah penarikan zat aktif yang diinginkan dari bahan mentah obat menggunakan pelarut yang dipilih sehingga zat yang diinginkan akan larut. Pemilihan sistem pelarut yang digunakan dalam ekstraksi harus berdasarkan kemampuannya dalam melarutkan jumlah yang maksimal dari zat aktif dan seminimal mungkin bagi unsur yang tidak diinginkan (Ansel, 1989).
2. Maserasi
Maserasi merupakan metode ekstraksi yang sederhana. Maserasi merupakan proses merendam bahan simplisia yang telah dihaluskan dalam pelarut sampai meresap dan melunakkan susunan sel, sehingga zat-zat yang mudah larut akan terlarut. Proses ini dilakukan dalam bejana bermulut lebar, serbuk ditempatkan lalu ditambah pelarut dan ditutup rapat, isinya diaduk berulang-ulang kemudian disaring. Proses ini dilakukan pada temperatur kamar selama tiga hari (Ansel, 1989).
Pada umumnya maserasi dilakukan dengan mencampur 10 bagian simplisia dengan 75 bagian pelarut/cairan penyari. Metode ini memiliki keuntungan yaitu cara pengerjaannya mudah, alat yang digunakan sederhana dan cocok untuk bahan yang tidak tahan panas (Anonim, 1986).
C. Jerawat
1. Definisi Jerawat
perpustakaan.uns.ac.id digilib.uns.ac.id11
Jerawat terbatas pada folikel pilosebacea kepala dan badan bagian atas karena kelenjar sebacea di wilayah ini sangat aktif (Webster, 2002). Apabila folikel pilosebaceatersumbat, maka sebum tidak dapat keluar dan terkumpul di dalam folikel sehingga folikel membengkak, dan terjadilah komedo yang merupakan bentuk permulaan dari jerawat (Tranggono, 1996). Komedo adalah gejala bagi jerawat berupa papul miliar yang di tengahnya merupakan sumbatan sebum, bila berwarna hitam akibat mengandung unsur melanin disebut komedo hitam atau komedo terbuka. Bila berwarna putih karena letaknya lebih dalam sehingga tidak mengandung unsur melanin disebut sebagai komedo putih atau komedo tertutup (Djuanda dkk., 2007).
2. Patogenesis
Faktor-faktor yang mempengaruhi terjadinya penyakit jerawat (acne vulgaris) adalah penyumbatan ductus pilosebaseus, meningkatnya produksi sebum, perubahan biokimia susunan lemak-lemak permukaan kulit dan kolonisasi kuman di dalam folikel sebaseus (Halim dan Sambijono, 1986).
Mikroorganisme yang sering berperan adalah Propionibacterium acne, Staphylococcus epidermidis atau Pitysrosporum ovale dan P. orbiculare. Kadang-kadang jerawat menyebabkan rasa gatal yang mengganggu atau rasa sakit kecuali bila terjadi pustul atau nodus yang besar (Djuanda dkk., 2007).
Mekanisme terjadinya jerawat adalah bakteri Propionibacterium acne
mengeras. Jika jerawat disentuh maka inflamasi akan meluas sehingga padatan asam lemak dan minyak kulit yang mengeras akan membesar (Anonim, 2007).
D. Bakteri
Bakteri adalah organisme uniseluler yang berkembang biak dengan cara pembelahan diri dan dapat dilihat dengan menggunakan mikroskop (Dwijoseputro, 1994). Bentuk dan ukuran bakteri bervariasi, ukuran berkisar 0,4-2 µ m (Pelczar dan Chan , 1988). Bakteri dapat diklasifikasikan berdasarkan morfologi, biokimia dan perwarnaan (bakteri Gram positif dan bakteri Gram negatif) (Jawetz et al., 2005).
Bakteri dapat didefinisikan secara morfologi yaitu dengan mempelajari bentuk, ukuran dan susunan sel. Perubahan lingkungan mungkin dapat sedikit mempengaruhi bentuk dan ukuran sel, misalnya bakteri berbentuk batang dapat menjadi lebih panjang atau lebih pendek. Bentuk dasar bakteri, yaitu bulat (tunggal: coccus, jamak: cocci), batang atau silinder (tunggal: bacillus, jamak:
bacilli), dan spiral yaitu berbentuk melingkar-lingkar atau batang melengkung (Pratiwi , 2008).
Berdasarkan pewarnaan Gram, bakteri dibedakan menjadi bakteri Gram positif dan Gram negatif.
1. Bakteri Gram Negatif
perpustakaan.uns.ac.id digilib.uns.ac.id13
mana membran plasmanya diselimuti oleh membran luar permeable. Bakteri ini mempunyai dinding sel tebal berupa peptidoglikan, yang terletak di antara membran dalam dan membran luarnya. Sel bakteri Gram negatif mungkin berbentuk bulat, lonjong, batang lurus atau lengkung, helix, dan filamen (seperti tali) (Jawetz et al., 2005).
2. Bakteri Gram Positif
Bakteri Gram positif terdiri dinding sel yang mengandung banyak lapisan peptidoglikan dengan membentuk struktur tebal dan kaku, membran dalam, membran sitoplasma. Bakteri Gram positif hanya mempunyai membran plasma tunggal yang dikelilingi dinding sel tebal berupa peptidoglikan. Sekitar 90 persen dari dinding sel tersebut tersusun atas peptidoglikan sedangkan sisanya berupa molekul lain bernama asam teikhoat (Pratiwi, 2008).
E. Pewarnaan Gram Bakteri
pada mikroorganisasi yang dilanjutkan dengan prosedur pencucian zat warna dengan air mengalir dapat menyebabkan mikroorganisme ikut tercuci.
Ada tiga macam prosedur pewarnaan: 1. Pewarnaan Sederhana
Pada pewarnaan sederhana hanya digunakan satu macam pewarna dan bertujuan mewarnai seluruh sel mikroorganisme sehingga bentuk seluler dan struktur dasarnya dapat terlihat. Contoh pewarna sederhana adalah carbol fuchsindan safranin.
2. Pewarnaan Diferensial
Pewarnaan diferensial menggunakan lebih dari satu pewarna dan memiliki reaksi berbeda untuk setiap bakteri, sehingga digunakan untuk membedakan bakteri. Pewarnaan diferensial yang sering digunakan adalah pewarnaan Gram. Pewarnaan Gram ini mampu membedakan dua kelompok besar bakteri yaitu bakteri Gram positif dan bakteri Gram negatif.
3. Pewarnaan Primer
perpustakaan.uns.ac.id digilib.uns.ac.id15
merah. Bakteri yang tetap berwarna ungu digolongkan ke dalam Gram positif, sedangkan bakteri yang berwarna merah digolongkan ke dalam Gram negatif.
Perbedaan warna antara bakteri Gram positif dan bakteri Gram negatif disebabkan oleh adanya perbedaan struktur pada dinding selnya. Dinding bakteri Gram positif banyak mengandung peptidoglikan, sedangkan dinding bakteri Gram negatif banyak mengandung lipopolisakarida.
Kompleks kristal violet-iodin yang masuk ke dalam sel bakteri Gram positif tidak dapat tercuci oleh alkohol karena adanya lapisan peptidoglikan yang kokoh pada dinding sel, sedangkan pada bakteri Gram negatif, alkohol akan merusak lapisan lipopolisakarida. Kompleks kristal violet-iodin pada bakteri Gram negatif dapat tercuci dan menyebabkan sel bakteri tampak transparan yang akan berwarna merah setelah diberi safranin (Pratiwi, 2008).
F. Media
Supaya mikroba dapat tumbuh dengan baik dalam suatu media, perlu dipenuhi syarat-syarat sebagai berikut:
1. Media harus mengandung semua nutrien yang mudah digunakan oleh mikroba.
2. Media harus mempunyai tekanan osmose, tegangan permukaan dan pH yang sesuai.
3. Media tidak mengandung zat-zat penghambat. Media harus steril (Anonim, 1989).
G. Antibakteri
perpustakaan.uns.ac.id digilib.uns.ac.id17
Target mekanisme antibakteri adalah sebagai berikut: 1. Kerusakan pada dinding sel
Struktur dinding sel dapat rusak dengan cara menghambat pembentukannya atau setelah selesai terbentuk. Antibiotik yang bekerja dengan mekanisme ini diantaranya adalah penisilin (Pelczar dan Chan, 1988).
2. Perubahan permeabilitas sel
Membran sitoplasma mempertahankan bagian-bagian tertentu dalam sel serta mengatur aliran keluar masuknya bahan-bahan lain, kemudian memelihara integritas komponen komponen seluler. Kerusakan pada membran ini akan mengakibatkan terhambatnya pertumbuhan sel (Jawetz et al., 2005).
3. Perubahan molekul protein dan asam nukleat
Hidup suatu sel tergantung pada terpeliharanya molekul-molekul protein dan asam nukleat dalam keadaan alamiahnya. Suatu antibakteri dapat mengubah keadaan ini dengan mendenaturasikan protein dan asam-asam nukleat sehingga merusak sel tanpa dapat diperbaiki lagi (Pelczar dan Chan, 1988).
4. Penghambatan sintesis asam nukleat dan protein
5. Penghambatan kerja enzim
Sulfonamid merupakan zat kemoterapi sintesis yang bekerja dengan cara bersaing dengan PABA, sehingga dapat menghalangi sintesis asam folat yang merupakan asam esensial yang berfungsi dalam sintesis purin dan pirimidin. Dengan demikian karena tidak adanya enzim, maka aktivitas seluler yang normal akan terganggu (Jawetz et al., 2005).
H. Uji Aktivitas Antibakteri
Potensi antibakteri dari suatu zat dapat diketahui melalui uji aktivitas antibakteri yang dilakukan dengan metode difusi agar. Prinsip metode difusi agar yaitu uji potensi yang berdasarkan pengamatan luas daerah hambatan pertumbuhan bakteri karena berdifusinya antibakteri dari titik awal pemberian ke daerah difusi. Media yang dipakai adalah agar Mueller Hinton. Pada metode difusi ini ada beberapa cara, yaitu:
a. Cara Kirby Bauer
b. Cara Sumuran
c. Cara Pour Plate(Anonim, 1993). Difusi Agar dengan Cara Sumuran
perpustakaan.uns.ac.id digilib.uns.ac.id19
Hasil inkubasi dibaca sebagai berikut :
a. Zona radikal yaitu suatu daerah di sekitar disk di mana sama sekali tidak ditemukan adanya pertumbuhan bakteri. Potensi antibakteri diukur dengan mengukur diameter dari zona radikal.
[image:36.595.154.500.256.495.2]b. Zona irradikal yaitu suatu daerah di sekitar disk dimana pertumbuhan bakteri dihambat oleh antibakteri, tetapi tidak dimatikan (Anonim, 1993). Berikut ini adalah kategori daya hambat bakteri menurut Davis dan Stout (1971).
Tabel I. Kategori daya hambat bakteri (Davis dan Stout, 1971) Daya hambat bakteri Kategori
Sangat kuat 10-20 mm Kuat
5-10 mm Sedang
Lemah
I. Kerangka Pemikiran
Daun jeruk bali (Citrus maxima Merr.) merupakan salah satu bagian dari tanaman yang memiliki khasiat antibakteri. Salah satu senyawa aktif pada daun jeruk bali yang memiliki aktivitas antibakteri adalah flavonoid. Diketahui dari penelitian sebelumnya, ekstrak etanol 75% daun jeruk lemon (Citrus limon)
yang mengandung flavonoid, tanin, alkaloid, steroid dan glikosida memiliki aktivitas antibakteri terhadap Escherichia coli, Pseudomonas aeruginosa,
typhimurium. Ekstrak etanol daun jeruk bali (Citrus maximaMerr.) didapatkan dengan cara maserasi menggunakan etanol 75%.
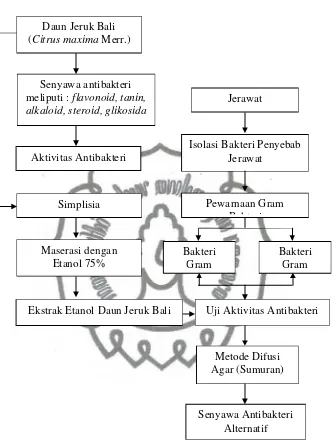
Jerawat merupakan salah satu penyakit yang disebabkan oleh bakteri, sehingga salah satu pengobatan jerawat dapat dilakukan dengan cara menurunkan jumlah koloni bakteri dan menurunkan inflamasi pada kulit. Pada penelitian ini dilakukan uji aktivitas antibakteri ekstrak etanol daun jeruk bali (Citrus maxima Merr.) terhadap bakteri uji yang diambil dan diisolasi dari apusan darah jerawat. Pada bakteri uji tersebut dilakukan pewarnaan Gram bakteri untuk mengetahui bentuk, susunan sel dan sifat Gram-nya. Uji aktivitas antibakteri ekstrak etanol daun jeruk bali (Citrus maxima Merr.) dilakukan dengan metode difusi agar (sumuran).
perpustakaan.uns.ac.id digilib.uns.ac.id21
Gambar 4. Alur Kerangka Pemikiran J. Keterangan Empiris
Daun jeruk bali (Citrus maxima Merr.) merupakan bagian dari salah satu tanaman obat tradisional Indonesia yang dipercaya mampu mencegah kanker, menurunkan resiko penyakit jantung, melancarkan saluran pencernaan, menjaga kesehatan kulit, mencegah konstipasi, menurunkan kolesterol dan
Uji Aktivitas Antibakteri Pewarnaan Gram
Bakteri
Bakteri Gram
Bakteri Gram Isolasi Bakteri Penyebab
Jerawat Jerawat
Senyawa Antibakteri Alternatif Metode Difusi Agar (Sumuran) Aktivitas Antibakteri
Daun Jeruk Bali (Citrus maxima Merr.)
Senyawa antibakteri meliputi : flavonoid, tanin, alkaloid, steroid, glikosida
Simplisia
Ekstrak Etanol Daun Jeruk Bali Maserasi dengan
mencegah anemia. Flavonoid merupakan salah satu kandungan daun jeruk bali (Citrus maximaMerr.) yang dikenal memiliki potensi sebagai agen antibakteri.
Berdasarkan penelitian sebelumnya daun jeruk lemon (Citrus limon) mengandung flavonoid, tanin, alkaloid, steroid dan glikosida yang merupakan senyawa antibakteri, hal ini terbukti dengan penelitian Pinkee Pandey, et al.
(2010) terhadap ekstrak etanol daun jeruk lemon (Citrus limon) yang dapat menghambat pertumbuhan bakteri Escherichia coli, Pseudomonas aeruginosa,
perpustakaan.uns.ac.id digilib.uns.ac.id
23 BAB III
METODE PENELITIAN
A. Desain Penelitian
Penelitian ini merupakan penelitian eksploratif laboratorium yaitu dengan melakukan isolasi bakteri pada apusan darah jerawat, mengamati sifat morfologinya dan menguji aktivitas antibakteri ekstrak etanol daun jeruk bali (Citrus maximaMerr.) terhadap bakteri uji.
B. Waktu dan Tempat Penelitian
Penelitian ini dilakukan selama 5 bulan di Laboratorium Biologi Pusat Sub Lab Mikrobiologi UNS dan Laboratorium Teknologi Farmasi FMIPA UNS.
C. Alat dan Bahan
1. Alat yang digunakan
a. Penyarian (Ekstraksi)
Seperangkat alat maserasi, timbangan analit (Mettler Toledo®),
grinder, ayakan nomor 40 dan 60, kain flanel, corong kaca, rotary evaporator(Bibby RE 200®), beaker glass (Pyrex®), gelas ukur (Pyrex®), labu ukur (Pyrex®), batang pengaduk, cawan porselen, eksikator.
b. Preparasi Alat dan Pembuatan Media Bakteri
Erlenmeyer (Pyrex®), gelas ukur (Pyrex®)), batang pengaduk, timbangan analit (Mettler Toledo®), autoclave (Sturdy®), LAF cabinet
c. Pengambilan Apusan dan Isolasi Bakteri Uji
Cotton buddsteril, cawan petri , bunsen burner, jarum ose, inkubator suhu 37°C (J.P. Selecta Hotcold M®), masker, , handscoon, LAF cabinet
(Labconco®) .
d. Pengecatan Gram Bakteri
Kertas label, handscoon, masker, jarum ose, object glass, degglass,
tabung reaksi (Pyrex®), pipet tetes, bunsen burner, mikroskop (Olympus CX-21®), spidol.
e. Pembuatan Suspensi Bakteri Uji
Erlenmeyer (Pyrex®), jarum ose, LAF cabinet (Labconco®), shaker
(IKA Labortechnik®), tabung reaksi (Pyrex®), gelas ukur (Pyrex®). f. Uji Aktivitas Antibakteri
Tabung reaksi (Pyrex®), rak tabung reaksi, flakon, handscoon, masker, cawan petri, jarum ose, mikropipet 10-100 µL (Master ptt®), yellow tips, bunsen burner, hot-plate, timbangan analit (Mettler Toledo®), gelas ukur (Pyrex®), pipet tetes, pelubang gabus, autoclave (Sturdy®),
Laminar Air Flow (LAF) cabinet (Labconco®), inkubator suhu 4°C (J.P. Selecta Hotcold M®), inkubator (P-Selecta®), jangka sorong digital (Bdq®). 2. Bahan yang digunakan
a. Bahan Utama
perpustakaan.uns.ac.id digilib.uns.ac.id25
b. Bahan Penyari
Bahan penyari yang digunakan adalah Etanol 75% (Pinkee Pandey, et al., 2010).
c. Bakteri Uji
Bakteri yang diambil dari apusan darah jerawat. d. Pengambilan Apusan dan Isolasi Bakteri Uji
Alkohol 70%, aquadest steril, media NA (Nutrient Agar) (Merck®), Media TSB (Tryptone Soya Broth) (Merck®), Media MC ( MacConkey) (Merck®), Media Agar Darah.
e. Pengecatan Gram Bakteri
Bakteri yang telah diisolasi dari apusan darah jerawat, cat Gram A (Kristal violet), cat Gram B (Lugol/Iodine), cat Gram C (Alkohol 96% dan Aceton), cat Gram D (Safranin), tissue, kapas.
f. Pembuatan Stok Bakteri
Media NA (Nutrient Agar) (Merck®),aquadest. g. Pembuatan Suspensi Bakteri Uji
Media NB (Nutrient Broth) (Merck®),aquadest. h. Uji Aktivitas Antibakteri
Media MHA (Muller Hinton Agar) (Merck®), aquadest steril, etanol 75%, suspensi CMC-Na 0,1% b/v, antibiotik Klindamisin 0,025%, kapas.
D. Cara Kerja
bakteri uji, pengecatan Gram bakteri dan uji aktivitas antibakteri secara in vitro
dengan metode difusi agar. 1. Penyiapan Alat
Alat yang digunakan untuk penelitian ini adalah alat yang dipinjam dari Laboratorium Biologi Pusat Sub Lab Mikrobiolgi UNS dan Laboratorium Teknologi Farmasi FMIPA UNS. Alat yang digunakan untuk uji aktivitas antibakteri disterilkan menggunakan autoklaf pada suhu 121oC, tekanan 1 atm selama 15 menit.
2. Determinasi dan Preparasi Sampel
Langkah ini bertujuan untuk memastikan kebenaran sampel daun jeruk bali (Citrus maxima Merr.), dengan mencocokkan ciri-ciri morfologis yang ada pada tanaman jeruk bali (Citrus maxima Merr.) terhadap kepustakaan yang dibuktikan oleh Lembaga Penelitian dan Pengabdian pada Masyarakat (LPPM)
Universitas Setia Bu Flora
perpustakaan.uns.ac.id digilib.uns.ac.id27
Gambar 5. Pembuatan Serbuk Simplisia Daun Jeruk Bali 3. Ekstraksi
Pembuatan ekstrak etanol daun jeruk bali (Citrus maximaMerr.) dilakukan dengan metode maserasi yakni serbuk simplisia daun jeruk bali (Citrus maxima
Merr.) sebanyak 800 gram dimasukkan ke dalam bejana dan direndam dalam pelarut (Etanol 75%) sebanyak 6 liter selama 3 hari sambil diaduk. Dalam 3 hari tersebut dilakukan penggantian pelarut setiap 24 jam supaya penyarian berlangsung lebih optimal dan senyawa bioaktif dapat terlarut sempurna. Hasil maserasi (maserat) disaring menggunakan kain flanel kemudian maserat yang didapat dihilangkan pelarutnya menggunakan rotary evaporator pada suhu
Daun Jeruk Bali
Dikeringkan dibawah sinar matahari dengan ditutup kain hitam Dicuci dibawah air mengalir
Diserbuk
Diayak dengan ayakan 40 dan 60 mesh
Serbuk Simplisia Daun Jeruk Bali Dipisahkan dari pengotor (sortasi kering)
55°C dengan kecepatan 5 rpm. Hasil ekstrak yang didapat kemudian dikentalkan menggunakan waterbathpada suhu 55°C hingga diperoleh ekstrak kental. Ekstrak etanol daun jeruk bali (Citrus maxima Merr.) kemudian ditimbang dan disimpan di dalam eksikator. Diagram alir pembuatan ekstrak etanol daun jeruk bali (Citrus maximaMerr.) dapat dilihat pada Gambar 6.
Gambar 6. Pembuatan Ekstrak Etanol Daun Jeruk Bali
4. Pengambilan Apusan, Isolasi dan Identifikasi Bakteri Uji
Pengambilan apusan dilakukan dengan cara mengusap darah pada jerawat probandus menggunakan cotton budd steril yang sebelumnya telah dicelupkan
Dalam 3 hari dilakukan penggantian pelarut setiap 24 jam
Ekstrak kental
Disimpan dalam eksikator
800 gram Serbuk Simplisia Daun Jeruk Bali
Dimaserasi dengan pelarut Etanol 75% sebanyak 6 liter selama 3 hari
Maserat disaring menggunakan kain flanel
Dihilangkan pelarutnya menggunakan rotary evaporator pada suhu 55°C dengan kecepatan 5 rpm
perpustakaan.uns.ac.id digilib.uns.ac.id29
Gambar 7. Tahap Isolasi dan Identifikasi Bakteri Uji
Dikulturkan dalam Media NA dan diinkubasi 24 jam pada suhu 37°C
Diperoleh biakan 10 koloni
Dibuat 10 stok bakteri dalam bentuk agar miring Dilakukan pengecatan Gram dan
pengamatan morfologi bakteri
Bakteri bentuk kokusGram positif
pada stok tabung 1 sampai 9
Dibuat stok dalam TSA
Ditanam dalam Media NA (Nutrient Agar) dan diratakan dengan metode streak
Tumbuh koloni bakteri lebat dari 4 apusan darah jerawat yang berbeda
Diambil 10 koloni berbeda dengan melihat bentuk dan warna koloni
diinkubasi 24 jam suhu 37°C
Bakteri bentuk basil Gram positif dan negatif pada stok tabung 10
Ditanam pada media Agar Darah Ditanam pada media
MacConkey Agar Koloni bakteri Gram negatif Koloni bakteri Gram positif (tidak hemolisis) Koloni bakteri Gram negatif (tidak hemolisis)
Uji aktivitas antibakteri
Dilakukan Pengecatan Gram dan pengamatan morfologi bakteri pada tiap koloni yang berbeda
Bakteri bentuk basil
Gram positif
Bakteri bentuk basil
Gram negatif
perpustakaan.uns.ac.id digilib.uns.ac.id31
5. Pengecatan Gram Bakteri Uji
Langkah pengecatan Gram bakteri uji dimulai dengan membersihkan
object glass dan degglass dengan alkohol kemudian masing-masing ujung
object glass diberi label untuk membedakan bakteri yang akan dicat. Pada bagian bawah object glass digambar bulatan berdiameter 1 cm dengan spidol (daerah ini digunakan untuk pengecatan bakteri). Pada sisi sebaliknya diteteskan 1 tetes aquadest dalam daerah bulatan, kemudian diambil sedikit biakan bakteri dengan jarum ose secara aseptis dan digoreskan pada daerah bulatan lalu diratakan pada seluruh area bulatan kemudian dikering anginkan hingga membentuk noda.
Permukaan object glass ditutup dengan deglass dan diamati dibawah mikroskop dengan perbesaran kuat dengan minyak imersi. Sel bakteri diamati bentuk dan warnanya. Sel berwarna merah muda merupakan Gram negatif dan sel berwarna biru-ungu merupakan Gram positif.
perpustakaan.uns.ac.id digilib.uns.ac.id33
Gambar 8. Pengecatan Gram Bakteri Uji
DiperolehMorfologi bakteri, Gram negatif (merah muda), Gram positif (biru-ungu) Ditambahakan dan disuspensikan 1 ose
biakan bakteri Ditetesi 1 tetes
akuades
Preparat kering
Digenangi Cat Gram A selama 1-3 menit Diratakan sebesar area bulatan
Difiksasi di atas nyala api Object Glassdibalik
Object Glass Ditempeli label
Digambar bulatan diameter ±1cm
Daerah pengecatan mikroba Dibersihkan
dengan alkohol
Ditetesi cat Gram C selama 30 detik hingga warna hilang Cat Gram A buang tanpa dicuci air kemudian
digenangi cat Gram B selama 1 menit
Ditetesi cat Gram D selama 2 menit
Ditutup denganDegglass
Diamati dengan mikroskop perbesaran 1000x minyak imersi
Dicuci air kemudian dikering-anginkan,
Dikering-anginkan
Dicuci cepat dengan air
6. Uji Aktivitas Antibakteri
Langkah-langkah pengujian aktivitas antibakteri ekstrak etanol daun jeruk bali (Citrus maximaMerr.) adalah sebagai berikut :
a. Penyiapan Alat
Alat uji yang digunakan untuk uji aktivitas antibakteri disterilisasi dengan autoklaf pada suhu 121ºC, tekanan 1 atm selama 15 menit.
b. Pembuatan Media
1) Media NA (Nutrient Agar)
Media NA dibuat dengan cara mensuspensikan 20 gram NA dalam
aquadestsampai volume 1 liter. Larutan media dipanaskan hingga larut, dan dimasukkan dalam erlenmeyer, kemudian dilakukan sterilisasi menggunakan autoklaf dengan suhu 121oC selama 15 menit.
2) Media NA (Nutrient Agar)dalam bentuk agar miring
Media NA dibuat dengan cara mensuspensikan 20 gram NA dalam
aquadest sampai volume 1 liter, kemudian dipanaskan hingga larut dan dimasukkan dalam tabung reaksi masing-masing sebanyak 5 ml. Selanjutnya media tersebut disterilkan terlebih dahulu sebelum digunakan. Media disterilisasi menggunakan autoklaf selama 15 menit pada suhu 121°C. Tabung reaksi selanjutnya dimiringkan agar media NA didalamnya membeku berbentuk miring.
3) Media TSA (Tryptone Soya Agar)
perpustakaan.uns.ac.id digilib.uns.ac.id35
larut. Untuk membuat media agar miring yang akan digunakan untuk stok bakteri, media TSA yang telah larut dimasukan kedalam tabung reaksi steril sebanyak 5 ml kemudian disterilisasi menggunakan autoklaf selama 15 menit pada suhu 121oC. Tabung reaksi selanjutnya dimiringkan agar media TSA didalamnya membeku berbentuk miring. 4) Media NB (Nutrient Broth)
Media NB dibuat dengan cara mensuspensikan 8 gram bubuk media NB dalam aquadest, sampai volume 1 liter. Larutan media dipanaskan hingga larut, dan dimasukkan dalam erlenmeyer, kemudian dilakukan sterilisasi menggunakan autoklaf dengan suhu 121oC selama 15 menit, jika diperlukan dapat dibagi terlebih dahulu kedalam wadah yang lebih kecil sebelum disterilkan kemudian disimpan pada suhu 25oC dengan pH penyimpanan 7±0,2.
5) Media MHA (Muller Hinton Agar)
c. Pembuatan Stok Bakteri Uji
[image:53.595.137.499.257.496.2]Memindahkan dan membiakan koloni bakteri yang berasal dari hasil pemisahan bakteri apusan darah jerawat dengan cara digoreskan 1-2 mata ose pada media agar miring yaitu media agar miring NA dan TSA dalam tabung reaksi yang kemudian diinkubasi pada suhu 37oC selama 24 jam. Diagram alir pembuatan stok bakteri uji dapat dilihat pada Gambar 9.
Gambar 9. Pembuatan Stok Bakteri Uji d. Pembuatan Suspensi Bakteri
Bakteri uji diambil 1-2 mata ose dari stok bakteri, dicampurkan dalam 25 ml media NB (Nutrient Broth) steril. Dihomogenkan dan diinkubasi pada suhu kamar dengan cara digoyang-goyang menggunakan
shakerdengan kecepatan 200 rpm selama 18-24 jam. e. Pembuatan Suspensi CMC-Na 0,1% b/v
Suspensi CMC-Na 0,1% b/v dibuat dengan cara melarutkan 0,05 gram serbuk CMC-Na dilarutkan dalam 50 mlaquadest.
Kultur bakteri bentuk
kokusGram positif
Diinkubasi pada suhu 37°C selama 24 jam
Digunakan sebagai stok Kultur bakteri bentuk
basilGram positif
Kultur bakteri bentuk
basilGram negatif
distreak pada Media Agar miring TSA
perpustakaan.uns.ac.id digilib.uns.ac.id37
f. Pembuatan Seri Konsentrasi Ekstrak Etanol Daun Jeruk Bali (Citrus maximaMerr.)
[image:54.595.157.488.267.588.2]Ekstrak etanol daun jeruk bali (Citrus maximaMerr.) dibuat 11 seri konsentarsi (0%-100%) dengan menggunakan suspensi CMC-Na 0,1% b/v. Setiap seri konsentrasi dibuat dengan menambahkan suspensi CMC-Na 0,1% b/v kedalam beberapa gram ekstrak etanol daun jeruk bali (Citrus maxima Merr.), sampai volumenya 5 ml. Komposisi bahan yang digunakan dalam pembuatan seri konsentrasi ekstrak etanol daun jeruk bali (Citrus maximaMerr.) dapat dilihat dalam Tabel II.
Tabel II. Komposisi Bahan dalam Pembuatan Seri Konsentrasi Ekstrak Etanol Daun Jeruk Bali (Citrus maximaMerr.)
Konsentrasi akhir ekstrak
(%)
Berat ekstrak etanol daun jeruk
bali (gram)
Suspensi CMC-Na 0,1% b/v (ml)
0 0,0 ad 5
10 0,5 ad 5
20 1,0 ad 5
30 1,5 ad 5
40 2,0 ad 5
50 2,5 ad 5
60 3,0 ad 5
70 3,5 ad 5
80 4,0 ad 5
90 4,5 ad 5
100 5,0 ad 5
(A)
(B) Diambil Ekstrak Etanol Daun Jeruk Bali
2,5 gram
Ditambah
Suspensi CMC-Na sampai 5 ml
Didapat
Konsentrasi Ekstrak 50% b/v
Konsentrasi Ekstrak 70% b/v
3,5 gram gram
Ditambah
Suspensi CMC-Na sampai 5 ml
Didapat
Konsentrasi Ekstrak 40% b/v
2 gram gram
Ditambah
Suspensi CMC-Na sampai 5 ml
Didapat
Konsentrasi Ekstrak 60% b/v
3 gram gram
Ditambah
Suspensi CMC-Na sampai 5 ml
Didapat Diambil
Ekstrak Etanol Daun Jeruk Bali
0,5 gram
Ditambah
Suspensi CMC-Na sampai 5 ml
Didapat
Konsentrasi Ekstrak10% b/v
Konsentrasi Ekstrak 20% b/v
1 gram gram
Ditambah
Suspensi CMC-Na sampai 5 ml
Didapat
Konsentrasi Ekstrak 0% b/v
0 gram gram
Ditambah
Suspensi CMC-Na sampai 5 ml
Didapat
Konsentrasi Ekstrak 30% b/v
1,5 gram gram
Ditambah
Suspensi CMC-Na sampai 5 ml
perpustakaan.uns.ac.id digilib.uns.ac.id39
[image:56.595.170.488.137.405.2](C)
Gambar 10. Pembuatan Seri Konsentrasi Ekstrak Etanol Daun Jeruk Bali. (A) Pembuatan Konsentrasi Ekstrak 0-30% b/v. (B) Pembuatan Konsentrasi Ekstrak
40-70% b/v. (C) Pembuatan Konsentrasi Ekstrak 80-100% b/v g. Larutan Kontrol
Kontrol yang digunakan pada uji aktivitas antibakteri ini terdiri dari :
1) Kontrol suspensi CMC-Na 0,1% b/v 2) Kontrol etanol 75%
3) Kontrol antibiotik Klindamisin 0,025% h. Pengujian Aktivitas Antibakteri Metode Difusi Padat
Pengujian aktivitas antibakteri dilakukan menggunakan metode difusi padat dengan langkah kerja sebagai berikut :
1) Menyiapkan media uji MHA disterilisasi pada suhu 121°C selama 15 menit kemudian didinginkan hingga 40-50°C
Diambil
4,5 gram
Ditambah
Suspensi CMC-Na sampai 5 ml
Didapat
Konsentrasi Ekstrak 90% b/v Konsentrasi
Ekstrak 80% b/v 4 gram gram
Ditambah
Suspensi CMC-Na sampai 5 ml
Didapat
Konsentrasi Ekstrak 100% b/v
5 gram gram
Ditambah
Suspensi CMC-Na sampai 5 ml
2) Suspensi bakteri uji yang berusia 24 jam dipindahkan ke dalam MHA yang bersuhu 40-50°C sebanyak 1% dari volume total MHA, kemudian dihomogenkan.
3) Menuang media MHA ke dalam cawan petri sebanyak 15 ml dan dibiarkan memadat.
4) Membuat lubang sumuran dengan menggunakan pelubang gabus dengan diameter lubang sebesar 6 mm pada media MHA padat.
5) Memasukkan 20µ L seri konsentrasi ekstrak etanol daun jeruk bali, kontrol pelarut ekstrak (CMC-Na 0,1% b/v), etanol 75% dan antibiotik Klindamisin 0,025% ke dalam masing-masing lubang, kemudian diberi label dan diinkubasi pada suhu 37°C selama 24 jam.
6) Mengukur diameter zona hambat pada masing-masing sumuran menggunakan jangka sorong dengan pengukuran sebanyak 3 kali untuk tiap lubang.
7) Replikasi dilakukan sebanyak 2 kali pada tiap pengujian. Nilai diameter zona hambat dari kedua replikasi tersebut dirata-rata.
8) Membandingkan nilai diameter zona hambat antar bakteri uji.
perpustakaan.uns.ac.id digilib.uns.ac.id41
Gambar 11. Pengujian Aktivitas Antibakteri Metode Difusi Padat Replikasi 2 kali
Diukur diameter zona hambat Diinkubasi pada suhu 37oC selama 24 jam
Perhitungan 3 kali masing-masing lubang Dituang sebanyak 15 ml ke cawan petri
Dibiarkan hingga media memadat
Dibuat lubang pada media
Dimasukkan 20µL larutan seri konsentrasi ekstrak dan larutan kontrol CMC-Na, kontrol etanol dan kontrol antibiotik ke dalam lubang
Bakteri dan media dihomogen Suspensi
bakteri uji
Media uji MHA disterilisasi
Media MHA yang bersuhu 40-50ºC
Dibandingkan hasil pada sampel uji dengan kontrol suspensi CMC-Na 0,1% , kontrol etanol 75 % dan kontrol antibiotik Klindamisin 0,025%
E. Analisis Hasil
Analisis data dilakukan secara eksploratif melalui pengamatan morfologi koloni (bentuk dan warna), sifat Gram bakteri pada jerawat dan diameter daya hambat ekstrak terhadap pertumbuhan bakteri uji.
perpustakaan.uns.ac.id digilib.uns.ac.id
43 BAB IV
HASIL DAN PEMBAHASAN
A. Pengumpulan dan Determinasi Tanaman
Tanaman yang digunakan untuk penelitian diambil dari kawasan perkebunan jeruk bali di Tamanan, Sukomoro, Magetan, Jawa Timur. Sampel yang akan digunakan dikumpulkan dari tempat dan waktu tertentu untuk menghindari adanya variasi kandungan kimia tumbuhan yang terlalu besar karena perbedaan kondisi tempat tumbuh. Sampel tanaman Citrus maxima dideterminasi untuk mengetahui kebenaran bahan dan menghindari adanya kesalahan dalam pengambilan sampel. Determinasi tanaman dilakukan oleh Lembaga Penelitian dan Pengabdian pada Masyarakat (LPPM) Universitas Setia Budi, Surakarta dengan mencocokkan ciri-ciri morfologis yang ada pada tanaman Jeruk Bali
(Citrus maximaMerr.) dengan Flora .
B. Penyiapan Bahan
Bahan utama penelitian ini diperoleh dalam bentuk segar. Daun Citrus maximayang digunakan dipilih yang tidak terlalu muda dan tidak terlalu tua yaitu dipilih daun pada urutan ke 3, 4, 5 dan 6 dari ujung tangkai pohon dengan tujuan mendapatkan kandungan kimia daun yang optimal. Daun Citrus maxima
kemudian disortir dan dibersihkan dengan cara dicuci di bawah air mengalir yang bersih. Pengeringan daun dilakukan dengan cara menjemur daun Citrus maxima
sampel tidak rusak oleh sinar ultraviolet (UV) dari sinar matahari, selain itu kain hitam dapat menyerap panas secara optimal.
Daun Citrus maxima yang telah kering dipisahkan dari pengotor kemudian diserbuk dan diayak. Pembuatan serbuk simplisia daun Citrus maxima bertujuan untuk memperluas permukaan partikel yang berinteraksi dengan pelarut sehingga penetrasi pelarut ke dalam jaringan tanaman berlangsung efektif, hal ini mempermudah melarutkan metabolit sekunder (Cannell, 1998), serta senyawa metabolit sekunder dapat terekstrak dengan sempurna. Serbuk tidak boleh terlalu halus karena akan mempersulit penyarian, butir-butir yang terlalu halus akan membentuk suspensi yang sulit dipisahkan dengan hasil penyarian. Dengan demikian hasil penyarian tidak murni lagi tetapi bercampur dengan partikel-partikel yang terlalu halus tadi. Setelah diserbuk dan diayak dengan ayakan nomor 40 dan 60 diperoleh serbuk simplisia daun Citrus maximasebanyak 800 gram.
C. Tahap Ekstraksi
Metode ekstraksi yang digunakan adalah metode maserasi. Metode ini merupakan metode perendaman sampel dengan pelarut yang sesuai pada temperatur ruang. Maserasi dipilih karena metode ini dapat menghasilkan ekstrak dalam jumlah banyak, serta terhindar dari perubahan kimia senyawa-senyawa tertentu karena pemanasan (Pratiwi, 2009).
perpustakaan.uns.ac.id digilib.uns.ac.id45
Pinkee Pandey, et al. (2010) digunakan etanol 75% untuk mengekstraksi daun jeruk lemon (Citrus limon) yang mengandung flavonoid, tanin, alkaloid, steroid dan glikosida, dan terbukti bahwa ekstrak etanol daun jeruk lemon (Citrus limon) dapat menghambat pertumbuhan bakteri Escherichia coli, Pseudomonas aeruginosa, Klebsiella pneumonia, Staphylococcus aureus, Bacillus subtilis dan
Salmonella typhimuriumdengan konsentrasi ekstrak 20% b/v.
Maserasi dengan etanol 75% dilakukan selama 24 jam dan diulang sebanyak tiga kali. Tujuan dari pengulangan maserasi supaya penyarian berlangsung lebih optimal dan senyawa bioaktif dapat terlarut sempurna. Proses maserasi disertai dengan pengadukan untuk mempermudah kontak pelarut pada rongga sel tumbuhan, sehingga senyawa-senyawa yang terkandung di dalamnya dapat ditarik keluar oleh pelarut. Pengadukan dapat menimbulkan sirkulasi pelarut sehingga ekstraksi dapat berlangsung optimal. Adanya perbedaan konsentrasi antara cairan di dalam sel dan cairan di luar sel akan menyebabkan senyawa aktif terdesak ke luar sel yang memiliki konsentrasi yang lebih rendah. Proses ekstraksi akan terus berlanjut hingga terjadi keseimbangan konsentrasi antara cairan di dalam dan di luar sel sehingga cairan menjadi jenuh dan proses ekstraksi terhenti (Ristiningsih, 2009).
Hasil ekstrak yang didapat kemudian dikentalkan menggunakan waterbath pada suhu 55°C hingga diperoleh ekstrak etanol daun Citrus maxima yang kental. Ekstrak etanol daun Citrus maxima yang diperoleh adalah 86,64 gram dengan rendemen 10,83%.
D. Pengambilan Apusan Darah Jerawat
Pengambilan apusan darah jerawat dilakukan secara aseptis terhadap 4 jerawat probandus. Kulit wajah probandus harus dibersihkan terlebih dahulu, kemudian jerawat dipencet hingga keluar darah dan nanahnya, selanjutnya darah yang keluar dari jerawat probandus diusap menggunakan cotton buddsteril yang sebelumnya telah dicelupkan ke dalam aquadest steril. Penggunaan aquadest steril bertujuan untuk mensuspensikan darah agar koloni yang tumbuh pada media dapat tumbuh secara terpisah. Darah yang telah diusap dengan cotton buddsteril diapus pada media NA (Nutrient Agar) dengan metode streak. Prinsip metode
perpustakaan.uns.ac.id digilib.uns.ac.id47
Gambar 12. Koloni bakteri yang tumbuh dari apusan darah jerawat (A) Apusan darah jerawat 1. (B) Apusan darah jerawat 2. (C) Apusan darah jerawat 3. (D) Apusan darah jerawat 4.
E. Isolasi dan Identifikasi Bakteri Uji
Gambar 13. Sepuluh stok bakteri hasil isolasi tahap I
Langkah selanjutnya adalah melakukan pengecatan Gram terhadap 10 stok bakteri yang diperoleh untuk mengidentifikasi morfologi dan jenis Gram bakteri yang telah diisolasi. Proses pengecatan Gram menggunakan 4 macam cat. Cat Gram A yang terdiri dari kristal violet, alkohol dan amonium oksalat berfungsi sebagai pewarna primer. Cat Gram B yang terdiri dari iodium, kalium iodida dan akuades berfungsi sebagai penguat warna. Cat Gram C yang terdiri dari aseton dan alkohol berfungsi sebagai peluntur. Cat Gram D yang terdiri dari safranin, alkohol dan akuades berfungsi sebagai pewarna kontras atau pembeda (Pelczar & Chan,1988).
violet-perpustakaan.uns.ac.id digilib.uns.ac.id49
iodin yang masuk ke dalam sel bakteri Gram positif tidak dapat tercuci oleh alkohol karena adanya lapisan peptidoglikan yang kokoh pada dinding sel, sedangkan dinding bakteri Gram negatif banyak mengandung lipopolisakarida sehingga alkohol akan merusak lapisan lipopolisakarida. Kompleks kristal violet-iodin pada bakteri Gram negatif dapat tercuci dan menyebabkan sel bakteri tampak transparan yang akan berwarna merah setelah diberi safranin (Pratiwi, 2008).
[image:66.595.125.501.259.588.2]Hasil dari pengecatan Gram menunjukkan bahwa ditemukan bakteri bentuk kokus Gram positif pada tabung 1, 2, 3, 4, 5, 6, 7, 8, 9, dan campuran antara bakteri bentuk basil Gram positif dan bakteri bentuk basil Gram negatif pada tabung 10 seperti pada Tabel III dan Gambar 14.
Tabel III. Hasil Pengecatan Gram Koloni Bakteri yang Tumbuh dari Apusan Darah Jerawat
NO SAMPEL HASIL
1. Tabung 1 Diketemukan bakteri CoccusGram (+) 2. Tabung 2 Diketemukan bakteri CoccusGram (+) 3. Tabung 3 Diketemukan bakteri CoccusGram (+) 4. Tabung 4 Diketemukan bakteri CoccusGram (+) 5. Tabung 5 Diketemukan bakteri CoccusGram (+) 6. Tabung 6 Diketemukan bakteri CoccusGram (+) 7. Tabung 7 Diketemukan bakteri CoccusGram (+) 8. Tabung 8 Diketemukan bakteri CoccusGram (+) 9. Tabung 9 Diketemukan bakteri CoccusGram (+)
(A) (B)
(C) (D)
Gambar 14. (A) Pertumbuhan koloni bakteri nomor 1-9. (B) Hasil pengecatan stok bakteri tabung 1-9. (C) Pertumbuhan koloni bakteri nomor 10.
(D) Hasil pengecatan stok bakteri tabung 10.
[image:67.595.137.492.131.475.2]perpustakaan.uns.ac.id digilib.uns.ac.id51
Proses isolasi tahap II dilakukan terhadap stok bakteri dalam tabung 10 sehingga didapatkan koloni bakteri bentuk basil Gram positif dan bentuk basil Gram negatif yang terpisah. Proses ini diawali dengan memindahkan campuran antara bakteri bentuk basil Gram positif dan bentuk basil Gram negatif pada tabung 10 ke media selektif yaitu media MacConkey Agardan media Agar Darah. Media MacConkey Agar merupakan media selektif dan diferensial yang mempunyai keistimewaan memisahkan bakteri enterik Gram negatif dari campuran bakteri yang memfermentasikan laktosa, karena dalam MacConkey Agar ini terdapat laktosa, crystal violet dan neutral red bile salt. Bile salt yang terkandung dalam media ini digunakan sebagai penghambat tumbuhnya bakteri Gram positif sehingga koloni yang tumbuh pada media ini adalah koloni bakteri Gram negatif. Media Agar Darah adalah media diperkaya yang menyediakan nutrisi ekstra untuk pertumbuhan bakteri. Media Agar Darah termasuk dalam media differensial dimana dapat membedakan bakteri yang memiliki kemampuan untuk hemolisis dan tidak, yang ditandai oleh adanya zona (halo) disekitar koloni. Pertumbuhan koloni bakteri tabung 10 pada media MacConkey Agar dan media Agar Darah dapat dilihat pada Gambar 15.
[image:68.595.160.461.569.719.2](A) (B)
Langkah selanjutnya dilakukan penggambilan koloni yang berbeda kemudian dilakukan pengecatan Gram untuk pengamatan morfologi serta sifat Gram-nya. Hasil pengecatan yang menunjukan koloni bakteri bentuk basil Gram positif dan koloni bakteri bentuk basil Gram negatif yang sudah terpisah masing-masing dibuat stok agar miring menggunakan media NA. Bakteri bentuk basil Gram positif memiliki ciri berbentuk batang dan berwarna ungu setelah dilakukan pengecatan, sedangkan bakteri bentuk basil Gram negatif memiliki ciri berbentuk batang dan berwarna merah setelah dilakukan pengecatan.
Tahap selanjutnya adalah identifikasi bakteri uji yang dilakukan melalui pengamatan bentuk dan warna koloninya serta pengamatan morfologi bakteri yang dilakukan di bawah mikroskop. Pengamatan bentuk dan warna koloni bakteri uji dilakukan secara langsung terhadap pertumbuhan bakteri pada media agar. Sedangkan pengamatan morfologi bakteri uji dilakukan di bawah mikroskop menggunakan perbesaran 1000x dengan minyak imersi dengan cara mengamati bentuk, susunan dan sifat Gram bakteri setelah dilakukan pengecatan terhadap bakteri uji. Hasil identifikasi bakteri uji dapat dilihat pada Gambar 16, 17 dan 18.
(A) (B) (C) Gambar 16. (A) Hasil pengecatan bakteri bentuk kokus Gram positif.
[image:69.595.129.496.547.683.2]perpustakaan.uns.ac.id digilib.uns.ac.id53
Gambar 16 menunjukkan ciri-ciri bakteri hasil isolasi sebagai berikut :
Bentuk koloni : bulat
Warna koloni : krem
Susunan sel : bergerombol
Morfologi sel : bulat
Bentuk tepian : rata
Warna pengecatan Gram : ungu
Jenis Gram : positif
(A) (B) (C) Gambar 17. (A) Hasil pengecatan bakteri bentuk basil Gram positif.
(B) Pertumbuhan koloni bakteri bentuk basil Gram positif. (C) Stok bakteri bentuk basil Gram positif.
Gambar 17 menunjukkan ciri-ciri bakteri hasil isolasi sebagai berikut :
Bentuk koloni : bulat
Warna koloni : krem
Susunan sel : berderet
Morfologi sel : batang
Bentuk tepian : bergelombang Warna pengecatan Gram : ungu
[image:70.595.122.496.155.498.2](A) (B) (C) Gambar 18. (A) Hasil pengecatan bakteri bentuk basil Gram negatif.
(B) Pertumbuhan koloni bakteri bentuk basil Gram negatif. (C) Stok bakteri bentuk basil Gram negatif.
Gambar 18 menunjukkan ciri-ciri bakteri hasil isolasi sebagai berikut :
Bentuk koloni : bulat
Warna koloni : krem
Susunan sel : monobasil (sel bakteri basil tunggal)
Morfologi sel : batang
Bentuk tepian : bergelombang Warna pengecatan Gram : merah
Jenis Gram : negatif
F. Pembuatan Seri Konsentrasi Ekstrak
[image:71.595.121.490.134.515.2]perpustakaan.uns.ac.id digilib.uns.ac.id55
sukar larut dalam pelarut air, maka diperlukan suspending agent agar didapatkan suatu suspensi yang baik antara media dan ekstrak. CMC-Na dipilih sebagai suspending agent karena CMC-Na mensuspensikan dengan baik antara media dengan ekstrak etanol. Selain itu, sesuai dengan prinsip like dissolve like dimana CMC-Na bersifat polar sehingga dapat melarutkan ekstrak yang polar seperti ekstrak etanol daun Citrus maxima.
G. Uji Aktivitas Antibakteri Ekstrak Etanol Daun Citrus maxima
Bakteri uji yang digunakan dalam penelitian ini adalah bakteri bentuk kokus Gram positif, bakteri b