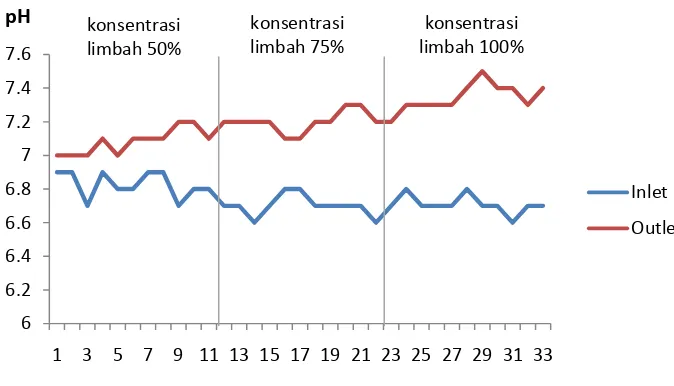
Pengolahan Limbah Cair Rumah Potong Hewan (RPH) Menggunakan Reaktor Upflow Anaerobic Sludge Blanket (UASB) Chapter III V
Teks penuh
Gambar




Dokumen terkait
Penelitian ini bertujuan untuk mengetahui perang seorang Camat dalam memimpin para pegawai di Kantor Camat Kecamatan Bongomeme, adapun metode penelitian menggunakan
Peneliti kembali ke lapangan untuk melakukan pengamatan untuk mengetahui kebenaran data yang diperoleh maupun menemukan data baru. Melakukan pengamatan secara lebih
Penelitian ini bertujuan untuk memperoleh gambaran tentang hubungan karakteristik partisipan kegiatan Keluarga Muda-Mudi dengan partisipasi dalam kegiatan Keluarga Muda- Mudi di RW
Masalah kependudukan tidak hanya persoalan kuantitasnya saja, tetapi juga kualitasnya. Kualitas sumber daya manusia Indonesia masih rendah, yang menyebabkan pula rendahnya
Adapun yang menjadi tujuan dari penelitian ini adalah : untuk mengetahui sejauh mana unsur fisik, teknik, taktik dan mental latihan pembinaan cabang olahraga bola voli
Berdasarkan uraian diatas, peneliti terdorong untuk membuat penelitian yang berjudul “Penerapan Model Problem Based Learning (PBL) dengan Pendekatan.. Adapun tujuan
Fungsi utama dari suatu Negara adalah kepala Negara, yang merupakan dengan fungsi. jantung dalam tubuh
eksperimen digunakan untuk mengetahui perbandingan peningkatan pemahaman konsep dan keterampilan proses sains siswa yang menggunakan model pembelajaran