TESIS
GLYCATED ALBUMIN
SEBAGAI PENANDA KONTROL
GLIKEMIK PADA PENDERITA DIABETES MELITUS
TIPE 2
ANSELMUS AKE
PROGRAM PASCASARJANA
UNIVERSITAS UDAYANA
1
TESIS
GLYCATED ALBUMIN
SEBAGAI PENANDA
KONTROL GLIKEMIK PADA PENDERITA DIABETES
MELITUS TIPE 2
ANSELMUS AKE NIM 1014048106
PROGRAM MAGISTER
PROGRAM STUDI ILMU BIOMEDIK
PROGRAM PASCASARJANA
UNIVERSITAS UDAYANA
DENPASAR
GLYCATED ALBUMIN
SEBAGAI PENANDA
KONTROL GLIKEMIK PADA PENDERITA DIABETES
MELITUS TIPE 2
Tesis untuk Memperoleh Gelar Magister pada Program Magister, Program Combined Degree,
Program Pascasarjana Universitas Udayana
ANSELMUS AKE NIM 1014048106
PROGRAM MAGISTER
PROGRAM STUDI ILMU BIOMEDIK
PROGRAM PASCASARJANA
UNIVERSITAS UDAYANA
DENPASAR
Lembar Pengesahan
TESIS INI TELAH DISETUJUI
TANGGAL 7 April 2016
…77
Pembimbing I,
Dr.dr. Made Ratna Saraswati, Sp.PD-KEMD, FINASIM NIP. 19700627 200312 2 001
Pembimbing II,
Prof. Dr. dr. I Gde Raka Widiana, Sp.PD-KGH NIP. 19560707 198211 1 001
Mengetahui
Ketua Program Studi Ilmu Biomedik Program Pascasarjana Universitas Udayana
Dr. dr. Gde Ngurah Indraguna Pinatih,MSc,SpGK NIP. 19580521 198503 1 002
Direktur Program Pascasarjana Universitas Udayana
Tesis Ini Telah Diuji pada
Tanggal 7 April 20167………..
Panitia Penguji Tesis Berdasarkan SK Rektor
Universitas Udayana, No : 1328/UN14.4/HK/2016,Tanggal 29 Maret 2016……
…………
Ketua : Dr. dr. Made Ratna Saraswati, Sp.PD-KEMD, FINASIM
Anggota :
1. Prof. Dr. dr. I Gde Raka Widiana, Sp.PD-KGH
2. Prof. dr. Nyoman Agus Bagiada, Sp.BIOK
3. Prof. Dr. dr. A.A Gede Budhiarta, Sp.PD-KEMD
UCAPAN TERIMA KASIH
Pertama-tama perkenankanlah penulis memanjatkan puji syukur ke hadapan
Tuhan Yang Maha Esa / Ida Sang Hyang Widhi Wasa, karena hanya atas
kurnia-Nya / asung wara nugraha-kurnia-Nya, tesis ini dapat diselesaikan.
Pada kesempatan ini perkenankanlah penulis mengucapkan terimakasih
yang sebesar- besarnya kepada Dr. dr. Made Ratna Saraswati,
SpPD-KEMD,FINASIM sebagai pembimbing I yang dengan penuh perhatian telah
memberikan dorongan, semangat, bimbingan, dan saran selama penulis mengikuti
program magister, khususnya dalam penyelesaian tesis ini. Terima kasih
sebesar-besarnya pula penulis sampaikan kepada Prof. Dr. dr. I Gde Raka Widiana,
SpPD-KGH sebagai pembimbing II yang dengan penuh perhatian dan kesabaran telah
memberikan bimbingan dan saran kepada penulis.
Ucapan yang sama juga ditujukan kepada Rektor Universitas Udayana Prof.
Dr. dr. Ketut Suastika, SpPD-KEMD, FINASIM atas kesempatan dan fasilitas yang
diberikan kepada penulis untuk mengikuti dan menyelesaikan pendidikan Program
Magister di Universitas Udayana. Ucapan terimakasih ini juga ditujukan kepada
Direktur Program Pascasarjana Universitas Udayana yang dijabat Prof. Dr. dr. A.A.
Raka Sudewi, Sp.S (K) atas kesempatan yang diberikan kepada penulis untuk
menjadi mahasiswa Program S2 pada Program Pascasarjana Universitas Udayana.
Tidak lupa penulis ucapkan terimakasih kepada Prof. Dr. dr. Putu Astawa, SpOT,
M.Kes, Dekan Fakultas Kedokteran Universitas Udayana atas ijin yang diberikan
kepada penulis untuk mengikuti pendidikan program magister. Pada kesempatan
Ilmu Penyakit Dalam, Prof. Dr. dr. IDN. Wibawa SpPD-KGEH dan Dr. dr. I Ketut
Suega SpPD-KHOM selaku Kepala Laboratorium Ilmu Penyakit Dalam RSUP
Sanglah Denpasar. Ungkapan terima kasih penulis sampaikan pula kepada para
penguji, yaitu Prof. dr. Nyoman Agus Bagiada Sp.BIOK, Prof. Dr. dr. A.A Gede
Budhiarta SpPD-KEMD dan Dr. dr. I Wayan Putu Sutirta Yasa, M.Si, yang telah
memberikan masukan, saran, sanggahan, dan koreksi sehingga tesis ini dapat
terwujud seperti ini.
Pada kesempatan ini ijinkan juga penulis mengucapkan terima kasih dan
penghormatan yang tulus kepada Prof. Dr. dr Tjok Raka Putra, SpPD-KR, sebagai
mantan Kepala Bagian /SMF Ilmu Penyakit Dalam FK Unud/ RSUP Sanglah dan
Prof. Dr. dr Ketut Suwitra, SpPD-KGH sebagai mantan Ketua Program Studi Ilmu
Penyakit Dalam FK Unud/ RSUP Sanglah yang pada masanya telah memberi
kesempatan kepada penulis untuk mengikuti pendidikan spesialisasi. Penulis juga
memberikan ucapan yang sama kepada Prof. Dr. dr. IDN Wibawa, SpPD-KGEH
sebagai pembimbing akademik penulis atas arahan dan bimbingan selama
mengikuti pendidikan spesialis Ilmu Penyakit Dalam.
Pada kesempatan ini penulis menyampaikan ucapan terima kasih yang tulus
disertai penghargaan kepada seluruh guru-guru yang telah membimbing penulis,
mulai dari sekolah dasar sampai perguruan tinggi. Juga penulis ucapkan terima
kasih kepada kedua orang tua, Bpk. Gaspar Wala dan Ny. Bernadetha Goo serta
kedua mertua penulis, Bpk. Vinsensius Ura Sima (Alm) dan Ny. Elisabeth Aphia
serta semua anggota keluarga yang telah memberikan motivasi dan nasehat kepada
Restiana Sima, serta ananda Maria Gracela Sima Wea tersayang, yang dengan
penuh pengorbanan telah sabar menunggu dan memberikan dukungan kepada
penulis untuk menyelesaikan tesis ini. Penulis juga mengucapkan terimakasih pada
rekan residen seperjuangan: angkatan Juli 2010 (dr. Adhy, dr. Baskoro, dr, Oscar,
dr. Ria, dr. Siswadi, dr. Riastana & dr. Hendrata), dr. Petrus Irianto, dr. Andi
Manaek, dr. Jarwa, dr. Sang Bagus, dr. Mayura, dr. Yohanes Satrio serta
teman-teman lainnya, terimakasih atas motivasi dan persahabatan yang kalian berikan
selama ini. Juga kepada paramedis, staf tata usaha Bagian /SMF Ilmu Penyakit
Dalam FK Unud/ RSUP Sanglah atas segala bantuan serta kerjasama yang baik
selama menjalani pendidikan spesialis Ilmu Penyakit Dalam.
Semoga Tuhan Yang Maha Esa / Ida Sang Hyang Widhi Wasa selalu
melimpahkan rahmat-Nya kepada semua pihak yang telah membantu pelaksanaan
dan penyelesaian tesis ini, serta kepada penulis sekeluarga.
Denpasar, 20 Februari 2016
ABSTRAK
GLYCATED ALBUMIN SEBAGAI PENANDA KONTROL GLIKEMIK PADA
PENDERITA DIABETES MELITUS TIPE 2
Diabetes melitus (DM) merupakan penyakit metabolik kronik yang ditandai dengan kondisi hiperglikemia. Kontrol glikemik merupakan salah satu hal penting dalam pengelolaan pasien DM yang secara skematik dapat digambarkan sebagai ‘triad glukosa’, dengan komponen Hemoglobin Adult 1C (HbA1C), kadar glukosa puasa, dan kadar glukosa 2 jam postprandial (2JPP).
Glycated albumin (GA) merupakan indeks kontrol glikemik yang relatif baru yang merupakan bentuk formasi ikatan antara molekul-molekul albumin dan glukosa melalui reaksi oksidasi non-enzimatik. GA merupakan indeks kontrol glikemik yang tidak dipengaruhi oleh gangguan metabolisme hemoglobin dan mencerminkan status glukosa darah yang lebih pendek dibandingkan HbA1C, yakni 2-4 minggu sebelumnya. Sebagai parameter yang relatif baru, GA memiliki beberapa keuntungan sehingga menjadi pemeriksaan yang menjanjikan bagi dokter maupun pasien sebagai penanda kontrol glikemik jangka menengah pada pasien diabetes melitus.
Tujuan penelitian ini untuk mengetahui apakah GA dapat digunakan sebagai penanda kontrol glikemik pada penderita DM tipe 2 (DMT2) dengan mencari sensitivitas, spesifisitas, nilai duga positif (NDP), dan nilai duga negatif (NDN) dari GA. Selain itu, pada penelitian ini akan dikaji korelasi antara GA dengan HbA1C, glukosa puasa dan glukosa 2JPP pada penderita DMT2.
Penelitian ini merupakan uji diagnostik, studi potong lintang, dilaksanakan di RSUP Sanglah dari Desember 2015 hingga Februari 2016 dengan menggunakan 59 pasien DMT2 sebagai sampel. Kontrol glikemik ditentukan dengan pemeriksaan HbA1C, glukosa puasa dan glukosa 2JPP (baku emas). Kadar HbA1C dikategorikan terkontrol bila <7%, kadar glukosa puasa dikategorikan terkontrol bila <100 mg/dL dan kadar glukosa 2JPP dikategorikan terkontrol bila <140 mg/dL. GA darah merupakan uji baru, dikategorikan terkontrol menggunakan nilai batas yang ditentukan dengan kurva Receiver Operating Characteristic (ROC).
Dari 59 subjek penelitian terdiri dari 31 orang laki-laki dan 28 orang perempuan. Hasil area under ROC curve GA adalah 0,9135 (91,35%). Dalam penelitian ini, peneliti mendapatkan 5 cut off point GA dimana 2 cut off point sebagai batas yang menunjukkan kemampuan GA dalam hal skrining yakni ≥18,7% dan ≥19%, 2 cut off point sebagai batas yang menunjukkan kemampuan GA dalam hal diagnostik yakni ≥21,4% dan 22,4%, dan 1 cut off point optimal yang menunjukkan kemampuan GA yang berimbang yakni 20,4%. Hasil uji diagnostik dengan menggunakan tabel silang 2x2 pada cut off point GA ≥18,7% didapatkan sensitivitas 94,7%, spesifisitas 76,2%, NDP 87,8% dan NDN 88,9%. Pada cut off point GA ≥19% didapatkan sensitivitas 89,5%, spesifisitas 81%, NDP 89,5% dan NDN 81%. Pada cut off point GA ≥20,4% didapatkan sensitivitas 81,6%, spesifisitas 85,7%, NDP 91,2% dan NDN 72%. Pada cut off point GA ≥21,4% didapatkan sensitivitas 76,3%, spesifisitas 90,5%, NDP 93,5% dan NDN 67,9%. Pada cut off point GA ≥22,4% didapatkan sensitivitas 63,2%, spesifisitas 95,2%, NDP 96% dan NDN 58,8%. Dengan uji korelasi Spearman, didapatkan hubungan positif kuat antara GA dengan HbA1C ( r = 0,842 dengan nilai p <0,001), GA dengan glukosa puasa ( r = 0,779 dengan nilai p <0,001) dan GA dengan glukosa 2JPP ( r = 0,714 dengan nilai p <0,001).
Pemeriksaan GA darah dapat digunakan sebagai modalitas diagnostik dalam menilai kontrol glikemik pada penderita DMT2 khususnya pada penderita dimana HbA1C, glukosa puasa, atau glukosa 2JPP sulit digunakan.
ABSTRACT
GLYCATED ALBUMIN AS A GLYCEMIC CONTROL MARKER IN TYPE 2 DIABETES MELLITUS PATIENTS
Diabetes mellitus (DM) is a chronic metabolic disorders characterized by hyperglycemia conditions. Glycemic control is one amongst the important factor in management of DM patients, which schematically, can be described as 'glucose triad', consist of Hemoglobin Adult 1C (HbA1C), fasting glucose levels, and two-hour after meal glucose levels.
Glycated albumin (GA) as a relatively new index of glycemic control, is a formed bond between molecules of albumin and glucose through non - enzymatic oxidation reactions. GA is a marker glycemic control that are not affected by metabolic disorders of hemoglobin and reflects the status of blood glucose in 2-4 weeks duration, which is shorter than HbA1C. As a relatively new parameter, GA has several advantages, placing it as a promising parameter for doctors and patients as a marker of medium-term glycemic control in patients with diabetes mellitus.
The purpose of this study is to determine whether GA can be used as a marker of glycemic control in patients with type 2 DM (DMT2) by determining the sensitivity, spesificity, Positive Predictive Value (PPV), and Negative Predictive Value (NPV) of GA. In addition, this study will assessed the correlation between GA with HbA1C, fasting glucose levels, and 2HAM glucose levels in DMT2 patients.
This study is a diagnostic, cross-sectional study, conducted in Sanglah General Hospital from December 2015 to February 2016 with 59 DMT2 patients as subjects. Glycemic control was determined with HbA1C, fasting glucose levels, and two-hour after meal glucose levels (gold standard). HbA1C levels are categorized controlled when < 7%, fasting glucose levels categorized controlled when < 100 mg/dL and two-hour after meal glucose levels were categorized controlled when < 140 mg/dL. GA blood levels, as a new test, categorized controlled using the limit values specified by the Receiver Operating Characteristic (ROC) curve.
From the 59 DMT2 subjects, consists of 31 were men and 28 were women. GA ‘area under the ROC curve’ results is 0.9135 (91.35%). This study found 5 GA’s cut off points, two of them shown GA’s ability as a screening tool, which were ≥18.7% and ≥19.2%, two cut off points that reflected GA’s ability as a diagnostic tool ≥21.4% and 22.4%, and 1 optimal cut off point that showed GA’s equity, which was 20,4%. The diagnostic test using the 2x2 cross table at cut off point of 18.7%, obtained a sensitivity of 94.7%, a specificity of 76.2%, PPV of 87.8%, and a NPV of 88.9%. At cut off point of ≥19%, obtained a sensitivity of 89.5%, a specificity of 81%, PPV of 89.5%, and a NPV of 81%. At cut off point of ≥20.4%, obtained a sensitivity of 81.6%, a specificity of 85.7%, PPV of 91.2%, and a NPV of 72%.%. At cut off point of ≥21.4%, obtained a sensitivity of 76.3%, a specificity of 90.5%, PPV of 93.5%, and a NPV of 67.9%. At cut off point of ≥22.4%, obtained a sensitivity of 63.2%, a specificity of 95.2%, PPV of 96%, and a NPV of 58.8%. Spearman correlation test found a positive and strong corellation between GA and HbA1C (r=0.842;p <0.001), GA and fasting glucose levels (r=0.779;p <0.001), and GA and two-hour after meal glucose levels (r=0.714;p <0.001).
GA blood levels can be used as a diagnostic tool in assessing glycemic control in DMT2 patients, especially in whom with HbA1C levels, fasting glucose levels, or two-hour after meal glucose levels are limited.
Keywords: DMT2, HbA1C, fasting glucose levels, 2HAM glucose levels, GA, glycemic
DAFTAR ISI
DAFTAR ARTI LAMBANG, SINGKATAN, DAN ISTILAH ... xvii
2.5Hemoglobin Terglikasi (HbA1C) ... 13
2.5.1Definisi ... 13
2.5.2HbA1C sebagai parameter kontrol DM ... 14
2.5.3Kelebihan dan kekurangan pemeriksaan HbA1C ... 16
2.6 Albumin Terglikasi / GlycatedAlbumin (GA) ... 17
2.6.1 Metabolisme Albumin ... 17
2.6.2 Proses glikasi albumin ... 18
2.6.3 Manfaat GA ... 20
2.6.3.1Pemantauan perubahan kadar glukosa darah ... 20
2.6.3.2 Pemantauan kadar glukosa darah pada pasien ... 21
2.6.3.3 Pemantauan kadar glukosa darah pada kehamilan ... 22
2.6.3.4 Pemantauan hiperglikemia postprandial ... 23
2.6.4 GA sebagai penanda kontrol glikemik pada penderita DM... ... 24
2.6.5 Kondisi yang mempengaruhi hasil GA ... 26
2.6.5.1 Sirosis hati ... 26
2.6.5.2 Gangguan metabolisme albumin. ... 26
BAB III KERANGKA BERPIKIR, KONSEP DAN HIPOTESIS.. ... 28
3.1 Kerangka Berpikir ... 28
4.5.1 Identifikasi variabel ... 33
4.5.2 Klasifikasi variabel ... 33
4.5.3 Definisi operasional variabel ... 33
4.7 Prosedur Penelitian ... 37
4.8 Analisis Data ... 38
BAB V HASIL DAN PEMBAHASAN ... .... 40
BAB VI SIMPULAN DAN SARAN ... .... 51
DAFTAR PUSTAKA ... .... 53
DAFTAR TABEL
Tabel 2.1 Kriteria Diagnosis DM ... 10
Tabel 5.1 Gambaran Karakteristik Subyek Penelitian ... 41
Tabel 5.2 Uji Diagnostik (cut off pointGA ≥17,8%) ... 43
Tabel 5.3 Uji Diagnostik (cut off pointGA ≥19%) ... 44
Tabel 5.4 Uji Diagnostik (cut off pointGA ≥20,4%) ... 45
Tabel 5.5 Uji Diagnostik (cut off pointGA ≥20,4%) ... 46
Tabel 5.6 Uji Diagnostik (cut off pointGA ≥20,4%) ... 46
DAFTAR GAMBAR
Gambar 2.1 Triad Glukosa ... 12
Gambar 2.2 Proses Glikasi Hemoglobin ... 14
Gambar 2.3 Struktur Albumin ... 18
Gambar 2.4 Proses Glikasi Albumin ... 19
Gambar 3.1 Kerangka Konsep Penelitian... 29
Gambar 4.1 Rancangan Penelitian... 30
Gambar 4.2 Alur Penelitian ... 38
Gambar 5.1 Kurva ROC Kemampuan GA ... 43
DAFTAR ARTI LAMBANG, SINGKATAN, DAN ISTILAH
ADA : American Diabetes Association
AACE : American Association College of Endocrinologists
ADVANCE : Action in Diabetes and Vascular Disease: Preterax and
Diamicron Modified Release Controlled Evaluation
ACCORD : Action to Control Cardiovascular Risk in Diabetes
AGE : Advanced Glycated End products
BCP : Bromocresolpurple
DCCT : Diabetes Control and Complication Trial
DepKes : Departemen Kesehatan
DM : Diabetes Melitus
DMT1 : Diabetes Melitus Tipe 1
DMT2 : Diabetes Melitus Tipe 2
HPLC : Ion-Exchange High-Performance Liquid Chromatography
IDF : International Diabetes Federation
IFG : Impair Fasting Glucose
IGT : Impair Glucose Tolerance
KAOD : Ketoamine Oxidase
RSUP : Rumah Sakit Umum Pusat
T3 : Triiodothyronine
T4 : Tiroxin
TSH : Thyroid Stimulating Hormone
TTGO : Tes Toleransi Glukosa Oral
UKPDS : United Kingdom Prospective Diabetes Study
WHO : World Health Organization
2JPP : 2 Jam Post Prandial
DAFTAR LAMPIRAN
Lampiran 1 : Keterangan Kelaikan Etik ... 58
Lampiran 2 : Surat Ijin Penelitian. ... 59
Lampiran 3 : Rencana dan Jadwal Penelitian ... 60
Lampiran 4 : Anggaran Penelitian.. ... 61
Lampiran 5 : Informed Consent ... 62
Lampiran 6 : Formulir Persetujuan ... 64
Lampiran 7 : Formulir Pengumpulan Data ... 65
Lampiran 8 : Prosedur Pemeriksaan GA (GA-L REAGENT) ... 68
Lampiran 9 : Prosedur Pemeriksaan HbA1C ... 70
Lampiran 10 : Hasil Penelitian ... 71
1 BAB I
PENDAHULUAN
1.1 Latar Belakang
Diabetes melitus (DM) merupakan salah satu diantara penyakit degeneratif
dan merupakan suatu penyakit metabolik kronik yang ditandai dengan kondisi
hiperglikemia (ADA, 2010). Prevalensi DM terus meningkat dari tahun ke tahun. Di
tahun 2012 diperkirakan 371 juta jiwa penduduk dunia (8,3%) menderita DM (IDF,
2012). Berdasarkan studi epidemiologi terbaru, Indonesia telah memasuki epidemi
diabetes melitus (PERKENI, 2011). World Health Organization (WHO)
memprediksi peningkatan jumlah penderita DM di Indonesia dari 8,4 juta pada
tahun 2000 menjadi sekitar 21,3 juta pada tahun 2030. Senada dengan WHO,
International Diabetes Federation (IDF) memprediksi peningkatan penderita DM
dari 7,0 juta pada tahun 2009 menjadi 12,0 juta pada tahun 2030 (IDF, 2005;
PERKENI, 2011). Di Indonesia, berdasarkan hasil riset kesehatan dasar
(RISKESDAS) oleh Departemen Kesehatan (DepKes) pada tahun 2007, prevalensi
DM mencapai 5,7% (PERKENI, 2011). Di Bali juga didapatkan prevalensi DM
yang cukup tinggi yakni mencapai 5,9% (Suastika, 2008). Hasil riset kesehatan
dasar (RISKESDAS) oleh Departemen Kesehatan (DepKes) pada tahun 2013,
prevalensi DM mencapai 6,9%.
Kontrol glikemik merupakan salah satu hal penting dalam evaluasi pasien DM
karena berhubungan dengan komplikasi mikrovaskular dan makrovaskuler akibat
DM yang akan atau telah terjadi. Buruknya kontrol glikemik pada pasien DM akan
2010). Kontrol glikemik pada pasien diabetes melitus tipe 2 (DMT2) secara
skematik dapat digambarkan sebagai ‘triad glukosa’, dengan komponen
Hemoglobin Adult 1C (HbA1C), kadar glukosa puasa, dan kadar glukosa 2 jam
postprandial (2JPP). Saat ini, meskipun masih ada perdebatan namun tampaknya
penilaian kontrol glikemik terbaik ditentukan oleh ketiga komponen tersebut
(Monnier & Colette, 2009).
HbA1C merupakan zat yang terbentuk dari reaksi kimia antara glukosa dan
hemoglobin, melalui reaksi non-enzimatik antara glukosa dengan N-terminal valine
pada rantai beta hemoglobin A (Mahajan & Mishra, 2011).HbA1C telah digunakan
secara luas sebagai indikator kontrol glikemik, karena mencerminkan konsentrasi
glukosa darah 3 bulan sebelum pemeriksaan dan tidak dipengaruhi oleh diet
sebelum pengambilan sampel darah (Schneider et al., 2003; ADA, 2012). Saat ini,
ada dua nilai HbA1C yang digunakan untuk menilai diabetes yang terkontrol yaitu
7% oleh American Diabetes Association (ADA) yang juga diadopsi oleh PERKENI
dan 6,5% oleh the American Association College of Endocrinologists (AACE) dan
IDF.
Studi yang dilakukan oleh McCance et al. tahun 1994 dalam menilai
kompilkasi mikrovaskular yakni kejadian retinopati pada pasien diabetes
mendapatkan cut off point optimum HbA1C adalah ≥7% dengan nilai sensitivitas
78% dan spesifisitas 85%. Cut off point glukosa puasa adalah ≥7,2 mmol/L (126
mg/dL) dengan nilai sensitivitas 81% dan spesifisitas 80%, sedangkan cut off point
optimum dari glukosa 2JPP adalah ≥13.0 mmol/L (234 mg/dL) dengan sensitivitas
Penelitian Action in Diabetes and Vascular Disease: Preterax and Diamicron
Modified Release Controlled Evaluation (ADVANCE) menunjukkan sedikit
keuntungan bertahap pada mikrovaskular outcome dengan HbA1C mendekati
normal; untuk pasien tanpa risiko hipoglikemi atau efek samping lain, kadar
HbA1C yang diharapkan adalah <7%. Sebaliknya penelitian Action to Control
Cardiovascular Risk in Diabetes (ACCORD) menunjukkan bahwa target HbA1C
yang tidak terlampau ketat dari <7% lebih dianjurkan pada pasien yang mendapat
terapi obat hipoglikemik seperti sulfonilurea dan/ atau insulin yang dapat
mengakibatkan hipoglikemi (Monnier & Colette, 2009).
Meskipun saat ini HbA1C secara luas telah digunakan sebagai penanda
kontrol glikemik, namun HbA1C tidak mencerminkan perubahan glikemia dalam
periode yang relatif singkat, dan akurasinya dikatakan menurun jika disertai dengan
abnormalitas metabolisme hemoglobin seperti anemia dan pada pasien penyakit
ginjal kronis (PGK) tahap akhir atau end stage ranal disease (ESRD) (Peacock et
al., 2008).
Tujuan pemeriksaan glukosa darah untuk mengetahui apakah sasaran terapi
telah tercapai dan untuk melakukan penyesuaian dosis obat, bila belum tercapai
sasaran terapi. Guna mencapai tujuan tersebut perlu dilakukan pemeriksaan kadar
glukosa darah puasa, glukosa 2JPP, atau glukosa darah pada waktu yang lain secara
berkala sesuai dengan kebutuhan (PERKENI, 2011). Meskipun demikian,
pemeriksaan kadar glukosa sangat berfluktuasi dan hasilnya dapat dipengaruhi oleh
stres, penundaan pemeriksaan serum, merokok serta aktifitas sebelum uji
Glycated albumin (GA) merupakan bentuk formasi ikatan antara
molekul-molekul albumin dan glukosa melalui reaksi oksidasi non-enzimatik. GA
merupakan indeks kontrol glikemik yang tidak dipengaruhi oleh gangguan
metabolisme hemoglobin. Selain itu, GA mencerminkan status glukosa darah yang
lebih pendek dibandingkan HbA1C, yakni 2-4 minggu sebelumnya. GA tidak
dipengaruhi oleh kadar protein serum, karena GA menghitung rasio antara kadar
albumin glikat dengan total albumin serum (Koga & Kasayama, 2010). Glukosa
berikatan kuat dengan albumin serum pada 4 situs residu lisin, dan reaksi glikasi
terjadi 10 kali lipat lebih cepat dibandingkan glikasi pada hemoglobin. Karena itu,
GA dapat lebih menangkap fluktuasi dan perubahan status glikemik lebih cepat dan
nyata dibandingkan HbA1C (Yoshiuchi et al., 2008).
Beberapa studi pernah melaporkan nilai rujukan GA antara lain oleh
Tominaga et al (1999) pada populasi orang Jepang adalah 12,3-16,9%. Penelitian
oleh Kohjuma et al (2011) mendapatkan nilai rujukan GA pada populasi Amerika
adalah 11,9-15,8%. Penelitian sebelumnya mengenai validitas GA dalam hal
memprediksi DM telah dikerjakan meskipun kemampuan GA dalam hal ini masih
dipertanyakan. Uji validasi oleh Ma et al (2010) pada populasi Cina didapatkan cut
offpoint GA adalah 17,1% dengan nilai sensitivitas 76,82% (CI: 73,64-79,79%) dan
spesifisitas 76,89% (CI: 74,42-79,23). Penelitian lain oleh Yang et al (2012)
didapatkan cut off point dari GA 15,7% dengan nilai sensitivitas 73,3% (CI:
73,64-79,79%) dan spesifisitas 80,1% (CI: 74,42-79,23). Oleh Roohk & Zaidi (2008),
target kendali glikemik yang diukur dengan parameter GA yang dianggap terkontrol
adalah <20%, dengan nilai normalnya adalah 11-16%. Studi oleh Pu et al (2007),
predective values dari GA dan HbA1C dalam menilai penyakit jantung koroner
(ROC) curve GA adalah 0,620 (62%) lebih baik dibanding HbA1C (54,3%) dengan
cut off point GA ≥19% (Pu et al, 2007). Sebagai parameter yang relatif baru, GA
memiliki beberapa keuntungan sehingga menjadi pemeriksaan yang menjanjikan
bagi dokter maupun pasien sebagai penanda kontrol glikemik pada pasien diabetes
melitus (Yoshiuchi et al., 2008).
Penelitian ini bertujuan untuk mengetahui apakah GA dapat digunakan
sebagai penanda kontrol glikemik penderita DMT2 dengan melakukan pemeriksaan
GA dibandingkan dengan pemeriksaan HbA1C, glukosa puasa dan glukosa 2JPP.
Hal ini dapat diketahui dengan mencari nilai sensitivitas, spesifisitas, nilai duga
positif (NDP) dan nilai duga negatif (NDN) dari GA sebagai penanda kontrol
glikemik pada penderita DMT2. Selain itu, pada penelitian ini akan dikaji korelasi
antara GA dengan HbA1C, glukosa puasa dan glukosa 2JPP pada penderita DMT2.
Penelitian ini diharapkan mampu menghasilkan parameter baru untuk penanda
kontrol glikemik pada penderita DMT2.
1.2 Rumusan Masalah
Berdasarkan uraian dalam latar belakang masalah tersebut diatas, dapat
disusun rumusan masalah sebagai berikut:
Apakah GA dapat digunakan sebagai penanda kontrol glikemik pada penderita
DMT2 dan apakah terdapat korelasi antara GA dengan HbA1C, glukosa puasa dan
glukosa 2JPP pada penderita DMT2 ?, dengan mengetahui :
1. Bagaimana nilai sensitivitas GA sebagai penanda kontrol glikemik penderita
DMT2 ?
2. Bagaimana nilai spesifisitas GA sebagai penanda kontrol glikemik penderita
3. Bagaimana nilai duga positif GA sebagai penanda kontrol glikemik penderita
DMT2 ?
4. Bagaimana nilai duga negatif GA sebagai penanda kontrol glikemik penderita
DMT2 ?
5. Bagaimana korelasi antara GA dengan HbA1C, GA dengan glukosa puasa dan
GA dengan glukosa 2JPP pada penderita DMT2 ?
1.3 Tujuan Penelitian
1.3.1 Tujuan umum
Untuk membuktikan bahwa GA dapat digunakan sebagai penanda kontrol
glikemik pada penderita DMT2 dan untuk mengetahui korelasi antara GA dengan
HbA1C, GA dengan glukosa puasa dan GA dengan glukosa 2JPP pada penderita
DMT2.
1.3.2 Tujuan khusus
1. Untuk mencari nilai sensitivitas GA sebagai penanda kontrol glikemik penderita
DMT2.
2. Untuk mencari nilai spesifisitas GA sebagai penanda kontrol glikemik penderita
DMT2.
3. Untuk mencari nilai duga positif GA sebagai penanda kontrol glikemik
penderita DMT2.
4. Untuk mencari nilai duga negatif GA sebagai penanda kontrol glikemik
penderita DMT2.
5. Untuk mencari korelasi antara GA dengan HbA1C, GA dengan glukosa puasa
1.4 Manfaat Penelitian
1.4.1Manfaat akademik
Hasil penelitian ini memberi informasi nilai sensitivitas, spesifisitas, NDP dan
NDN dari GA sebagai penanda kontrol glikemik pada penderita DMT2. Selain itu,
penelitian ini memberi informasi korelasi antara GA dengan HbA1C, GA dengan
glukosa puasa dan GA dengan glukosa 2JPP pada penderita DMT2. Informasi ini
dapat digunakan sebagai data dasar untuk penanda kontrol glikemik oleh para
dokter dalam penatalaksanaan DMT2.
1.4.2Manfaat praktis
1. Bila terbukti bahwa nilai sensitivitas, spesifisitas, NDP dan NDN dari GA
sebagai penanda kontrol glikemik cukup baik dibanding HbA1C, glukosa puasa
dan 2JPP maka GA bisa dipergunakan sebagai alternatif diagnostik penanda
kontrol glikemik penderita DMT2 khususnya pada penderita dimana HbA1C,
glukosa puasa, atau glukosa 2JPP sulit digunakan.
2. Bila terdapat korelasi antara GA dengan HbA1C, GA dengan glukosa puasa dan
GA dengan glukosa 2JPP pada penderita DMT2, diharapkan pemeriksaan GA
1
BAB II
KAJIAN PUSTAKA
2.1 Diabetes Melitus
2.1.1 Definisi
Diabetes melitus adalah suatu penyakit metabolik kronik yang ditandai dengan
kondisi hiperglikemia akibat gangguan sekresi insulin, aktifitas insulin atau
keduanya (ADA, 2010). Hiperglikemia kronis dihubungkan dengan kerusakan,
disfungsi dan kegagalan organ-organ tubuh khususnya mata, ginjal, saraf, jantung
dan pembuluh darah (PERKENI, 2011).
2.1.2 Epidemiologi
Prevalensi DM terus meningkat dari tahun ke tahun. Total penduduk dengan
DM di seluruh dunia diperkirakan akan bertambah dari 171 juta pada tahun 2000
menjadi 366 juta penduduk pada tahun 2030 (Wild et al., 2004). Di tahun 2012
diperkirakan 371 juta jiwa penduduk dunia (8,3%) menderita DM (IDF, 2012).
Pertumbuhan populasi penduduk, perubahan gaya hidup, penuaan dan
meningkatnya prevalensi kegemukan akan meningkatkan prevalensi DM (Wild et
al., 2004; Braunwald et al., 2005).
Berdasarkan studi epidemiologi terbaru, Indonesia telah memasuki epidemi
diabetes melitus. World Health Organization (WHO) memprediksi peningkatan
jumlah penderita DM di Indonesia dari 8,4 juta pada tahun 2000 menjadi sekitar
21,3 juta pada tahun 2030. Senada dengan WHO, International Diabetes
Federation (IDF) memprediksi peningkatan penderita DM dari 7,0 juta pada tahun
2009 menjadi 12,0 juta pada tahun 2030 (IDF, 2005; PERKENI, 2011). Di
Indonesia berdasarkan hasil RISKESDAS oleh DepKes pada tahun 2007, prevalensi
DM mencapai 5,7% (PERKENI, 2011). Di Bali juga didapatkan prevalensi DM
yang cukup tinggi yakni mencapai 5,9% (Suastika, 2008). Hasil riset kesehatan
dasar (RISKESDAS) oleh Departemen Kesehatan (DepKes) pada tahun 2013,
prevalensi DM mencapai 6,9%. Perubahan gaya hidup dan urbanisasi nampaknya
merupakan penyebab penting masalah ini, dan terus menerus meningkat pada
milenium baru ini (PERKENI, 2011).
2.1.3 Diagnosis DM
Berbagai keluhan dapat ditemukan pada penderita DM. Kecurigaan adanya
DM perlu dipikirkan apabila terdapat keluhan klasik DM seperti poliuria, polidipsia,
polifagia, dan penurunan berat badan yang tidak dapat dijelaskan sebabnya.
Keluhan lain dapat berupa: sering lelah dan lemas, kesemutan, gatal, mata kabur,
dan disfungsi ereksi pada pria, serta pruritus vulvae pada wanita (PERKENI, 2011).
Diagnosis DM dapat ditegakkan melalui tiga cara, yaitu jika keluhan klasik
ditemukan, maka pemeriksaan glukosa plasma sewaktu >200 mg/dL sudah cukup
untuk menegakkan diagnosis DM. Cara kedua yaitu pemeriksaan glukosa plasma
puasa ≥126 mg/dL dengan adanya keluhan klasik. Yang ketiga adalah dengan tes
toleransi glukosa oral (TTGO). Meskipun TTGO dengan beban 75 gram glukosa
lebih sensitif dan spesifik dibanding dengan pemeriksaan glukosa plasma puasa,
namun pemeriksaan ini memiliki keterbatasan tersendiri. TTGO sulit untuk
dilakukan berulang-ulang dan dalam praktek sangat jarang dilakukan karena
membutuhkan persiapan khusus (PERKENI, 2011). American Diabetes Association
(HbA1C) dapat mendiagnosis DM selain sebagai kontrol glikemik pasien DM. Cut
off point HbA1C dalam mendiagnosis DM berdasarkan kadar glukosa puasa 7
mmol/l atau 126 mg/dL pada populasi high risk Indigenous dimana data
dikumpulkan dari Aboriginal and Torres Strait Islander communities di Australia
dan Canadian First Nations community (n=431) adalah 7.0% dengan sensitivitas
plasma sewaktu merupakan hasil pemeriksaan sesaat pada suatu hari tanpa
memperhatikan waktu makan terakhir
ATAU
2. Gejala klasik DM + Kadar glukosa plasma puasa 126 mg/dL (7.0 mmol/L). Puasa
diartikan pasien tak mendapat kalori tambahan sedikitnya 8 jam
ATAU
3. Kadar gula plasma 2 jam pada TTGO 200 mg/dL (11,1 mmol/L) TTGO yang
dilakukan dengan standar WHO, menggunakan beban glukosa yang setara dengan 75 g
glukosa anhidrus yang dilarutkan ke dalam air.
2.2 Diabetes Melitus Tipe 2 (DMT2)
Diabetes melitus tipe 2 (DMT2) merupakan tipe DM dengan persentase
terbesar, yaitu 90-95%. Tipe ini sebelumnya juga dikenal sebagai
non-insulin-dependent diabetes (NIDDM) atau DM onset dewasa. Risiko akan meningkat
sejalan dengan umur, obesitas, dan kurangnya aktivitas fisik. Penyakit ini lebih
sering ditemukan pada wanita dengan riwayat diabetes melitus gestasional dan
DMT2 yang juga disebut diabetes melitus tidak tergantung insulin atau
NIDDM, disebabkan oleh penurunan sensitivitas jaringan target terhadap efek
metabolik insulin, penurunan sensitivitas terhadap insulin ini disebut sebagai
resistensi insulin. DMT2 dikaitkan dengan peningkatan konsentrasi insulin plasma
(hiperinsulinemia). Hal ini terjadi sebagai upaya kompensasi oleh sel beta pankreas
terhadap penurunan sensitivitas jaringan terhadap efek metabolik insulin.
Penurunan sensitivitas insulin mengganggu penggunaan dan penyimpanan
karbohidrat, yang akan meningkatkan kadar gula darah dan merangsang
peningkatan sekresi insulin sebagai upaya kompensasi (Guyton, 2008).
Gejala klasik dari DMT2 adalah terjadi peningkatan frekuensi buang air kecil
(polyuria), rasa haus (polydipsia), rasa lapar (polyphagia), penglihatan kabur, dan
lemas. Gejala tersebut merupakan manifestasi dari kondisi hiperglikemi. Akan
tetapi pasien DMT2 biasanya mengalami gejala hiperglikemi insidental dan
seringkali tidak memiliki gejala yang signifikan sebelum munculnya komplikasi
(PERKENI, 2011).
Seiring dengan peningkatan usia (umur 40 tahun), kejadian obesitas (obesitas
sentral) dan kurangnya aktivitas fisik maka risiko perkembangan diabetes juga akan
meningkat (Leahy, 2005). Faktor lain yang dapat meningkatkan kejadian DMT2
adalah faktor genetik, penyakit vaskular, dislipidemia, riwayat menderita DM
gestasional dan adanya riwayat kegagalan toleransi glukosa impair fasting glucose
(IFG) / impair glucose tolerance (IGT).
Salah satu hal penting dalam evaluasi pasien DM adalah kontrol glikemik
karena berhubungan dengan komplikasi mikrovaskular dan makrovaskuler akibat
DM yang akan atau telah terjadi (Lehman & Krumholz, 2009 ; Montori & Balsells,
2009). Studi UK Prospective Diabetes Study (UKPDS) menyatakan bahwa
komplikasi mikrovaskular dapat diturunkan dengan kontrol glikemik yang baik
dengan menggunakan obat anti diabetes. Rekomendasi lain menyatakan bahwa
terapi penurunan kadar gula darah secara baik dan tepat mendekati nilai normal
dapat menurunkan komplikasi mikrovaskular maupun makrovaskular (Skyler, 2004;
Stolar, 2010; WHO, 2011).
Pentingnya kontrol glikemik dalam managemen DM karena hal ini dapat
mengetahui efektivitas dari terapi yang telah dilakukan dan kepatuhan dalam
berobat (Skyler, 2004; Qaseem et al., 2007). Kontrol glikemik pada pasien DM
dapat memprediksi komplikasi yang telah dan akan terjadi dan memperkirakan
prognosis dari pasien DM. Selain itu juga dapat dipakai sebagai pegangan dalam
penyesuaian diet, latihan jasmani dan obat-obatan untuk mencapai kadar glukosa
senormal mungkin sehingga terhindar dari hiperglikemia maupun hipoglikemia
(PERKENI, 2011). Kontrol glikemik pada pasien DMT2 secara skematik dapat
digambarkan sebagai ‘triad glukosa’, dengan komponen HbA1C, kadar glukosa
puasa, dan kadar glukosa 2JPP (Monnier & Colette, 2009).
Gambar 2.1
Triad glukosa (Monnier & Colette, 2009)
2.4 Pemeriksaan Kadar Glukosa Darah
Glukosa darah adalah sumber utama energi untuk sel-sel tubuh. Umumnya
tingkat gula darah bertahan pada batas-batas yang sempit sepanjang hari: 4-8
mmol/l (70-150 mg/dl). Tingkat ini meningkat setelah makan dan biasanya berada
pada level terendah pada pagi hari sebelum makan. Tingkat gula darah diatur
melalui umpan balik negatif untuk mempertahankan keseimbangan di dalam tubuh.
Tujuan pemeriksaan glukosa darah untuk mengetahui apakah sasaran terapi telah
tercapai dan untuk melakukan penyesuaian dosis obat, bila belum tercapai sasaran
terapi. Guna mencapai tujuan tersebut perlu dilakukan pemeriksaan kadar glukosa
darah puasa, glukosa 2JPP, atau glukosa darah pada waktu yang lain secara berkala
sesuai dengan kebutuhan (PERKENI, 2011). Meskipun demikian, pemeriksaan
kadar glukosa sangat berfluktuasi dan hasilnya dapat dipengaruhi oleh stres,
penundaan pemeriksaan serum, merokok serta aktifitas sebelum uji laboratorium
dilakukan.
2.5 Hemoglobin Terglikasi (HbA1C)
2.5.1 Definisi
Hemoglobin terglikasi (HbA1C) merupakan zat yang terbentuk dari reaksi
kimia antara glukosa dan hemoglobin, melalui reaksi non-enzimatik antara glukosa
dengan N-terminal valine pada rantai beta hemoglobin A. Glukosa membentuk
ikatan aldimine dengan N H2- dari valine dalam rantai beta, basa Schiff yang
dihasilkan bersifat tidak stabil,kemudian melalui suatu penyusunan ulang(Amadori
& Mishra, 2011). HbA1C yang lebih dikenal dengan hemoglobin glikat adalah
salah satu fraksi hemoglobin di dalam tubuh manusia yang berikatan dengan
glukosa secara non enzimatik. HbA1C terbentuk dari protein dalam sel darah merah
atau disebut juga hemoglobin yang bereaksi dengan glukosa sehingga disebut
hemoglobin terglikasi. Ketika kadar glukosa dalam darah tinggi (hiperglikemi),
molekul-molekul glukosa dalam darah semakin banyak yang berikatan dengan
hemoglobin dan menyebabkan peningkatan dari HbA1C. Usia HbA1C mengikuti
usia dari sel darah merah yaitu 120 hari (Nathan et al., 2008).
Gambar 2.2
Proses glikasi hemoglobin (Jones, 2013)
2.5.2 HbA1C sebagai parameter kontrol DM
Hemoglobin terglikasi telah digunakan secara luas sebagai indikator kontrol
glikemik, karena mencerminkan konsentrasi glukosa darah 3 bulan sebelum
pemeriksaan dan tidak dipengaruhi oleh diet sebelum pengambilan sampel darah.
(Schneider et al., 2003; ADA, 2012). Kontrol glikemik pada pasien DMT2 secara
skematik dapat digambarkan sebagai ‘triad glukosa’, dengan komponen HbA1C,
kadar glukosa puasa, dan kadar glukosa postprandial. Saat ini, meskipun masih ada
perdebatan namun tampaknya penilaian kontrol glikemik terbaik ditentukan oleh
Pada sebuah analisis set data dari Diabetes Control and Complication Trial
(DCCT), dilaporkan hubungan lebih baik terhadap HbA1C didapatkan dari
konsentrasi glukosa setelah makan siang dan rata-rata kadar glukosa per hari
(Rohlfing et al., 2002). Studi lain lagi melaporkan apabila pasien dibagi menjadi 5
kelompok menurut kuintil HbA1C, glukosa postprandial memberikan kontribusi
terbesar (70%) pada kuintil HbA1C yang lebih rendah pada pasien dengan kontrol
diabetes baik hingga sedang. Sebaliknya, glukosa puasa tampaknya menjadi
kontributor utama kadar glukosa sepanjang hari pada pasien diabetes tidak
terkontrol (HbA1C >8,4%) (Monnier et al., 2003) Untuk pasien dengan kadar
HbA1C antara 7,3 dan 8,4%, kontribusi glukosa puasa dan postprandial adalah
sama (Rohlfing et al., 2002).
Kadar HbA1C memberikan informasi yang berguna pada kontribusi
postprandial hiperglikemi dan basal hiperglikemi pada pasien DMT2. Karena
glukosa postprandial adalah kontributor utama pada pasien dengan kadar HbA1C
6,5%-7,5%, maka logis untuk menurunkan glukosa postprandial mencapai kadar
HbA1C di bawah 6,5%. Sebaliknya, pada pasien dengan kadar HbA1C di atas
7,5%, hiperglikemi basal menjadi yang utama, sehingga terapi perbaikan kontrol
glikemik sebaiknya dimulai dengan obat yang bekerja menurunkan hiperglikemia
basal dan interprandial. Saat ini, ada dua nilai HbA1C yang digunakan untuk
menilai diabetes yang terkontrol yaitu: 7% oleh ADA dan 6,5% oleh AACE dan
IDF (Monnier & Colette, 2009).
Penelitian ADVANCE menunjukkan sedikit keuntungan bertahap pada
risiko hipoglikemi atau efek samping lain, kadar HbA1C yang diharapkan adalah
<7% (Monnier & Colette, 2009). Sebaliknya penelitian ACCORD menunjukkan
bahwa target HbA1C yang tidak terlampau ketat dari <7% lebih dianjurkan pada
pasien yang mendapat terapi obat hipoglikemik seperti sulfonilurea dan/ atau insulin
yang dapat mengakibatkan hipoglikemi. Rekomendasi lebih fleksibel sebaiknya
diaplikasikan kepada pasien dengan harapan hidup rendah atau dengan komplikasi
mikro dan makrovaskuler yang sudah lanjut (Monnier & Colette, 2009).
Studi yang dilakukan oleh McCance et al. tahun 1994 dalam menilai
kompilkasi mikrovaskular yakni kejadian retinopati pada pasien diabetes
mendapatkan cut off point optimum HbA1C adalah ≥7% dengan nilai sensitivitas
78% dan spesifisitas 85%. Cut off point glukosa puasa adalah ≥7,2 mmol/L (126
mg/dL) dengan nilai sensitivitas 81% dan spesifisitas 80%, sedangkan cut off point
optimum dari glukosa 2JPP adalah ≥13.0 mmol/L (234 mg/dL) dengan sensitivitas
88% dan spesifisitas 81% (WHO, 2011).
2.5.3Kelebihan dan kekurangan pemeriksaan HbA1C
Tidak ada tes diagnostik klinis yang sempurna. Untuk penggunaan klinis, tes
yang ideal adalah akurat, spesifik, terstandardisasi, mudah dilakukan dan tidak
mahal. Keuntungan dalam melakukan pemeriksaan HbA1C dalam mendiagosis DM
antara lain tidak diperlukan puasa sehingga nyaman untuk pasien, hasil yang stabil
untuk memantau kondisi hiperglikemik selama tiga bulan yang lalu tanpa
dipengaruhi kondisi stres dan sakit. Selain itu, HbA1C dapat digunakan sebagai tes
saring bagi seseorang dengan risiko tinggi terkena DM (Gillett, 2009; Kilpatrick et
Pada beberapa keadaan, HbA1C tidak dapat mencerminkan kontrol glukosa
darah. Hal ini penting diketahui karena dapat menyebabkan under- atau over
treatment. Meskipun saat ini HbA1C secara luas telah digunakan sebagai penanda
kontrol glikemik, namun HbA1C tidak mencerminkan perubahan glikemia dalam
periode yang relatif singkat, dan akurasinya dikatakan menurun jika disertai dengan
abnormalitas metabolisme hemoglobin seperti anemia dan pada pasien penyakit
ginjal kronis (PGK) tahap akhir atau end stage ranal disease (ESRD) (Peacock et
al., 2008; Nitin, 2010; Son et al., 2013; WHO, 2011).
2.6Albumin Terglikasi / GlycatedAlbumin (GA)
2.6.1 Metabolisme albumin
Dalam tubuh manusia dewasa albumin disintesa oleh hati sekitar 100-200
mikrogram per gram jaringan hati per hari. Albumin didistribusikan secara vaskuler
dalam plasma dan secara ekstravaskuler dalam kulit, otot, dan beberapa jaringan
lain. Sintesa albumin dalam sel hati dilakukan dalam dua tempat, pertama pada
polisom bebas dimana dibentuk albumin untuk keperluan intravaskuler. Kedua,
poliribosom yang berkaitan dengan retikulum endoplasma dimana dibentuk albumin
untuk didistribusikan ke seluruh tubuh (Kim & Lee, 2012).
Sintesa albumin dipengaruhi beberapa faktor, yaitu nutrisi terutama asam
amino, hormon dan adanya suatu penyakit. Asam amino yang dapat merangsang
terjadinya sintesa albumin adalah triptofan, arginin, ornitin, lisin, fenilalanin,
treonin dan prolin. Sedangkan hormon yang dapat merangsang sintesa albumin
adalah tiroid, hormon pertumbuhan, insulin, adrenokortikotropik, testosteron, dan
korteks adrenal. Adapun yang dapat menghambat sintesa albumin adalah alkohol
pada seseorang penderita penyakit hati kronis, ginjal, dan kekurangan gizi seperti
kwashiorkor (Kim & Lee, 2012).
2.6.2 Proses glikasi albumin
Albumin adalah salah satu protein plasma yang telah diketahui paling
lama dan merupakan komponen terbesar dari protein plasma, mewakili lebih dari
80% molekul total dan 60% konsentrasi protein plasma total (Roohk & Zaidi,
2008). Konsentrasi normal albumin adalah 35-50 g/l, yang membuatnya menjadi
protein paling banyak dalam plasma dengan berbagai fungsi fisiologis (Evans,
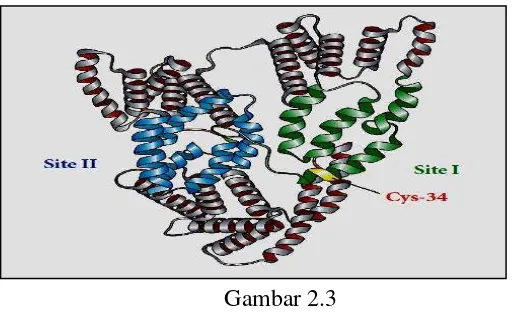
2002). Secara struktural, albumin terbuat dari 585 asam amino dan mengandung 35
residu sistein penting (kecuali Cys-34) yang membentuk jembatan disulfida yang
berkontribusi terhadap struktur protein tersier secara keseluruhan (Kim & Lee,
2012).
Gambar 2.3
Struktur albumin (Kim & Lee, 2012)
Glikasi (kadang disebut glikosilasi nonenzimatik) merupakan proses
sederhana dimana kelebihan molekul gula seperti fruktosa atau glukosa,
menempelkan dirinya sendiri dengan molekul protein atau lipid yang normal dalam
darah tanpa intervensi enzimatik (Kim & Lee, 2012). Monosakarida memiliki
memiliki sekitar 10 kali aktivitas glikasi glukosa. Kekhawatiran mengenai glikasi
pada diabetes muncul dari fakta bahwa gula tereduksi berpotensi untuk
menginduksi glikasi dan mengganggu fungsi sejumlah protein. Karena semua
protein rentan terhadap glikasi, gangguan ini dapat menimbulkan efek yang
menonjol. Produk glikasi dapat diklasifikasikan menjadi produk awal dan produk
tahap lanjut. Awalnya, basa Schiff yang reversibel dan tidak stabil dibentuk dari
ikatan glukosa atau derivatnya dengan grup albumin yang memiliki amin bebas
(glikasi reversibel, glikasi 1-2 minggu), menyebabkan pembentukan residu
fruktosamin yang stabil (ketoamin) melalui dibuangnya air. Pengaturan ulang
senyawa ini akhirnya menghasilkan senyawa amadori yang ireversibel (glikasi
ireversibel, glikasi 6-8 minggu). Ini merupakan proses glikasi awal dan juga dikenal
sebagai reaksi Maillard. Modifikasi tahap lanjut pada produk glikasi tahap awal ini
(aduksi Amadori), seperti pengaturan ulang, oksidasi, polimerisasi, dan
pembelahan, menghasilkan konjugat ireversibel yang disebut advanced glycated
end products (AGE). Produk AGE dianggap sebagai penanda berbagai penyakit
seperti arteriosklerosis, gagal ginjal, penyakit alzheimer, atau diabetes, dan juga
mengalami peningkatan selama proses penuaan (Koga & Kasayama, 2010 ;Kim &
Gambar 2.4
Proses glikasi albumin (Kim & Lee, 2012)
2.6.3Manfaat GA
2.6.3.1Pemantauan perubahan kadar glukosa darah yang lebih cepat
Masa paruh albumin serum lebih pendek dibandingkan eritrosit. Hal tersebut
menyebabkan perubahan kadar GA lebih cepat ketika terjadi perubahan status
kontrol glukosa dalam waktu yang singkat. Perubahan yang singkat biasanya terjadi
karena ada faktor terapi luar, seperti pengobatan oral maupun injeksi insulin. Di sisi
lain, kadar GA juga lebih baik dibanding HbA1C ketika status glukosa darah
memburuk (terjadi peningkatan kadar glukosa) dalam waktu yang singkat. Dalam
kasus ini, GA menangkap sinyal kenaikan kadar glukosa lebih dini dibandingkan
HbA1C. HbA1C tetap normal atau terjadi sedikit peningkatan pada diagnosis
fulminan diabetes melitus tipe 1 (DMT1) dimana sel-sel β-pankreas rusak dengan
cepat, sehingga terjadi peningkatan kadar glukosa plasma dan ketoasidosis dalam
jangka sangat pendek. Pada kasus-kasus tersebut, GA merupakan parameter yang
lebih baik dibandingkan HbA1C karena lebih cepat menggambarkan perubahan
status glukosa darah yang disebabkan oleh efek pengobatan (Koga & Kasayama,
2010).
Perubahan status glikemik pada GA yang lebih cepat dibandingkan HbA1C,
dapat membantu dokter dalam memberikan dosis yang akan diberikan kepada
pasien yang sedang dalam pengobatan. Dengan respons yang lebih cepat pada
perubahan kadar glukosa dibandingkan HbA1C, GA dapat sangat bermanfaat pada
saat penyesuaian dosis untuk pasien dalam terapi. Takahashi et al, menemukan
HbA1C dengan pemberian terapi insulin intensif, walaupun pada akhirnya
persentase penurunan HbA1C dan GA akan sama pada minggu ke-16 setelah terapi.
Rasio GA/HbA1C sangat menurun pada 8 minggu terapi, dan berangsur naik dalam
8 minggu berikutnya. Dengan demikian, GA dapat dijadikan parameter pemantauan
yang lebih sensitif untuk mendeteksi perbaikan kontrol glikemik yang lebih dini
ketika memulai atau sedang dalam proses pengobatan. Hal ini menjelaskan bahwa
GA dapat menggambarkan efek pengobatan lebih baik, sehingga dokter dapat
memberikan penyesuaian dosis obat yang diberikan kepada pasien dengan lebih
efektif (Takahashi et al., 2007 ; Koga & Kasayama, 2010).
2.6.3.2Pemantauan kadar glukosa darah pada pasien dengan dialisis dan anemia
Telah diketahui jika pada kondisi pasien yang mengalami kerusakan ginjal
tingkat akhir yang mengharuskan pasien menjalani hemodialisis, umur dari eritrosit
menjadi lebih pendek. Hal ini menyebabkan penurunan kadar HbA1C (rendah
palsu) sehingga pemeriksaan kadar glukosa darah menggunakan HbA1C tidak dapat
dipakai dengan baik. Selama hemodialisis, uremia, kehilangan darah pada saat
pengobatan, dan pengambilan darah secara frekuentif dapat berkontribusi pada
pengurangan waktu paruh sel darah merah. Umur paruh eritrosit yang memendek
dan transfusi dapat menurunkan kadar HbA1C, yang berpotensial untuk membuat
penilaian kontrol glikemik tidak dapat digunakan. Studi menyebutkan bahwa kadar
HbA1C relatif lebih rendah pada pasien diabetes melitus dengan dialisis
dibandingkan dengan GA. Pada pasien PGK tahap akhir atau ESRD, kadar rendah
HbA1C berkorelasi dengan rendahnya kadar hemoglobin dan tingginya dosis terapi
mendorong pembentukan eritrosit dan meningkatkan kelangsungan hidup eritrosit.
Namun, pasien dialisis dengan kadar hemoglobin rendah dapat mengurangi
kelangsungan hidup eritrosit dan menurunkan waktu paruh hemoglobin yang tidak
dapat diatasi dengan pemberian dosis tinggi eritropoietin. Hal tersebut menunjukkan
bahwa GA dapat menjadi parameter yang lebih baik dibandingkan HbA1C pada
pasien hemodialisis (Peacock et al., 2008).
2.6.3.3Pemantauan kadar glukosa darah pada kehamilan
Kontrol glikemik pada wanita hamil dengan DM atau diabetes gestasional
menjadi sangat penting untuk menurunkan risiko terjadinya kematian janin, dan
penyulit maternal. Studi menunjukan terjadi penurunan kadar HbA1C pada
trimester kedua, dilanjutkan peningkatan yang cukup signifikan pada trimester
ketiga kehamilan. Dari trimester kedua ke trimester ketiga kehamilan, kadar HbA1C
meningkat dan kadar transferin jenuh serta feritin menurun, sedangkan GA tidak
menunjukkan perubahan yang signifikan (Hashimoto et al., 2010 ; Danese et al.,
2015).
Perubahan kadar HbA1C selama kehamilan diduga disebabkan karena
kekurangan zat besi. Hal tersebut terjadi karena sebagian besar wanita hamil
mengalami kekurangan zat besi. Kadar transferin dan feritin ditemukan relatif lebih
rendah pada wanita hamil. Feritin merupakan protein penyimpan zat besi paling
utama dalam tubuh, sedangkan transferin adalah protein yang membawa besi dalam
dan feritin. Kenaikan HbA1C pada masa akhir kehamilan sangat dipengaruhi oleh
kekurangan zat besi (Hashimoto et al., 2010 ; Danese et al., 2015).
Korelasi terbalik antara HbA1C dan zat besi menyimpulkan bahwa kenaikan
HbA1c terjadi akibat dari kekurangan zat besi di trimester ketiga kehamilan, baik
wanita sehat maupun diabetes melitus. Hal ini menunjukkan bahwa HbA1C bukan
indeks kontrol yang baik untuk pemantauan kadar glukosa darah pada kehamilan.
Pada kasus ini, karena GA tidak terpengaruh oleh kekurangan zat besi dan dapat
merefleksikan perubahan jangka pendek rerata glukosa darah, GA dapat dijadikan
parameter yang lebih baik sebagai pemantauan kadar glukosa (Hashimoto et al.,
2010 ; Danese et al., 2015).
2.6.3.4Pemantauan hiperglikemia postprandial dan fluktuasi glukosa
Beberapa studi epidemiologi telah menunjukkan bahwa hiperglikemia
postprandial menjadi faktor risiko penyakit kardiovaskular. Studi Funugata
menunjukkan bahwa glukosa plasma postprandial dalam tes toleransi glukosa
merupakan faktor risiko yang lebih kuat untuk kejadian kardiovaskular daripada
glukosa plasma puasa. Selain itu dilaporkan bahwa pemberian α-glucosidase
inhibitor acarbose untuk pasien dengan gangguan toleransi glukosa atau diabetes
melitus dikaitkan dengan pengurangan risiko kardiovaskular (Tominaga et al.,
1999).
Lanjutnya, GA dapat menangkap perubahan pada kadar glukosa
postprandial dibandingkan glukosa darah rerata dan HbA1C. Rasio GA/HbA1C
pada pasien DMT1 yang lebih besar dibandingkan DMT2 memperlihatkan bahwa
memiliki fluktuasi glukosa yang lebih tinggi dibandingkan DMT2. Berdasarkan
fenomena tersebut, pada pasien DMT1 dan DMT2 yang tidak menunjukkan
perbedaan pada kadar HbA1C, kadar GA signifikan lebih tinggi. Hal tersebut
menunjukkan bahwa GA mungkin lebih kuat mencerminkan kadar glukosa plasma
postprandial dan berbagai fluktuasi glukosa plasma dari HbA1C (Koga &
Kasayama, 2010).
Studi DCCT menunjukkan bahwa injeksi insulin intensif dapat mengurangi
risiko retinopati dibandingkan dengan insulin konvensional pada pasien DMT1,
bahkan pada keadaan dimana tidak ada perubahan kadar HbA1C. Injeksi insulin
intensif diduga dapat menurunkan fluktuasi dan perubahan kadar glukosa darah, dan
akan dapat menurunkan risiko kejadian mikroangiopati. Kadar glukosa postprandial
ditemukan menjadi prediktor yang lebih baik untuk retinopati diabetik
dibandingkan HbA1C pada DMT2. Kenaikan fluktuasi glikemik dan/atau
perubahan glukosa postprandial telah menunjukkan adanya kenaikan risiko pada
makroangiopati diabetik. GA sebagai parameter jangka pendek-menengah dapat
menagkap perubahan/fluktuasi glukosa plasma. Yoshiuchi et al menjelaskan bahwa
rasio GA/HbA1C lebih tinggi pada pasien DMT1 dibandingkan DMT2, dimana
terjadi fluktuasi kadar glukosa darah yang cukup tinggi pada pasien DMT1 (Koga &
Kasayama, 2010 ; Yoshiuchi et al., 2008). Studi DCCT menunjukkan bahwa secara
independen, GA dan HbA1C menjadi parameter yang baik untuk risiko
mikroangiopati. Korelasi paling kuat adalah ketika kadar GA dan HbA1C digabung
sebagai parameter, sehingga saling mendukung dari potensi masing-masing
5.2GA sebagai penanda kontrol glikemik pada penderita DM
Fruktosamin, GA, dan HbA1C, merupakan glycated protein non-enzimatik
yang digunakan sebagai penanda kontrol glikemik pasien diabetes. GA merupakan
bentuk formasi ikatan antara molekul-molekul albumin dan glukosa melalui reaksi
oksidasi non-enzimatik. Serupa dengan fruktosamin, GA merupakan indeks kontrol
glikemik yang tidak dipengaruhi oleh gangguan metabolisme hemoglobin. Selain
itu, GA mencerminkan status glukosa darah yang lebih pendek dibandingkan
HbA1C, yakni 2-4 minggu sebelumnya. GA tidak dipengaruhi oleh kadar protein
serum layaknya fruktosamin, karena GA menghitung rasio antara kadar albumin
glikat dengan total albumin serum (Koga & Kasayama, 2010). Glukosa berikatan
kuat dengan albumin serum pada 4 situs residu lisin, dan reaksi glikasi terjadi 10
kali lipat lebih cepat dibandingkan glikasi pada hemoglobin. Karena itu, GA dapat
lebih menangkap fluktuasi dan perubahan status glikemik lebih cepat dan nyata
dibandingkan HbA1C (Yoshiuchi et al., 2008).
GA menggambarkan kendali glikemik dalam jangka waktu yang lebih pendek,
namun GA tidak dipengaruhi oleh kadar albumin serum karena dihitung dari rasio
albumin serum total. Beberapa studi pernah melaporkan nilai rujukan GA antara
lain oleh Tominaga et al (1999) pada populasi orang Jepang adalah 12,3-16,9%.
Penelitian oleh Kohjuma et al (2011) mendapatkan nilai rujukan GA pada populasi
Amerika adalah 11,9-15,8%. Oleh Roohk & Zaidi (2008), target kendali glikemik
yang diukur dengan parameter GA adalah <20%, dengan nilai normalnya adalah
11-16%. Studi oleh Pu et al (2007), predective values dari GA dan HbA1C dalam
Receiver Operating Characteristic(ROC) curve GA adalah 0,620 (62%) lebih baik
dibanding HbA1C (54,3%) dengan cut off pointGA ≥19%.
Dalam 15-20 tahun terakhir, selain GA, banyak publikasi laporan yang
mendeskripsikan pemeriksaan penanda protein serum yakni fruktosamin (FA)
sebagai metode untuk menilai status glikemik dalam periode intermediet (2-4
minggu). Dinamakan fruktosamin karena kesamaan struktur kimianya dengan
fruktosa yang mengacu kepada jumlah semua ikatan ketoamin yang dihasilkan dari
glikasi protein serum dalam sirkulasi. Pemeriksaan cepat untuk FA dijabarkan oleh
Food and Drug Administration (FDA) pada tahun 1997, dan dilaporkan beberapa
studi klinis dengan berbagai hasil, namun jalur komersil yang berliku untuk
pemeriksaan ini membuat penyediaannya susah, dan saat ini sudah tidak lagi
tersedia sebagai pemeriksaan komersil cepat. (Edelman et al., 2000; Roohk & Zaidi,
2008).
2.6.5 Kondisi yang mempengaruhi hasil GA
2.6.5.1Sirosis hati
Hati merupakan organ vital yang penting untuk meregulasi kadar glukosa
plasma. Gangguan metabolik glukosa muncul secara frekuentif pada pasien dengan
penyakit hati kronik, seperti hepatitis kronik dan sirosis hati. Pada pasien dengan
penyakit hati kronik, sekitar 70-90% terdiagnosa memiliki gangguan toleransi
glukosa dan 30-60% diantaranya adalah pasien DM. Sangat penting untuk tetap
dapat mengontrol kadar glukosa darah pada pasien tersebut. HbA1C memiliki
korelasi yang rendah pada pasien penyakit hati kronik, karena umur eritrosit yang
memendek. Sebaliknya nilai GA dan fruktosamin lebih tinggi pada pasien tersebut,
sintesis albumin yang menurun. Sangat sulit untuk memantau kadar glukosa darah
pada pasien dengan penyakit hati kronik karena tidak ada parameter yang bekerja
dengan baik pada kondisi tersebut (Koga & Kasayama, 2010).
2.6.5.2Gangguan metabolisme albumin
GA menunjukkan nilai yang lebih rendah pada pasien dengan sindrom
nefrotik, hipertiroid dan pada pengobatan steroid seperti glukokortikoid dimana
dapat meningkatkan metabolisme albumin. Penurunan kadar GA pada kondisi
tersebut disebabkan karena memendeknya masa paruh albumin serum karena
peningkatan metabolisme serum albumin. Sedangkan GA menunjukkan nilai yang
lebih tinggi dibandingkan kadar glukosa plasma pada pasien dengan sirosis hati dan