1. ANALISIS PESTISIDA GOLONGAN KARBAMAT PADA SAYURAN SAWI DENGAN METODE GC-MS YANG DI JUAL DI PASAR KUMBASARI DENPASAR
Sathya Indrayana, Didik Setiawan, Ida Ayu Manik Partha Sutema ... 1-5
2. ANALISIS KADAR TIMBAL DALAM DARAH PEKERJA SENI LUKIS DI DAERAH LODTUNDUH, UBUD DENGAN METODE MP-AES
Ni Putu Ayu Nopita Dewi, I Made Oka Adi Parwata, I. A. Manik Partha S ... 6-12
3. ANALISIS KADAR BESI PADA BAYAM HIJAU YANG DIANGIN-ANGINKAN DAN DIPANASKAN Ni Putu Dian Lufita Sari, Didik Setiawan, Nyoman Sudarma ... 13-17
4. ANALISIS KADAR METAMFETAMINA PADA SAMPEL DARAH DENGAN METODE GC-MS
Dunika Ayu Ni Made, I Made Oka Adi Parwata, I.A Manik Parthasutema ... 18-29
5. ANALISIS KADAR KAFEIN PADA KOPI HITAM DI LEBAH BUKIAN GIANYAR MENGGUNAKAN SPEKTROFOTOMETER UV-VIS
Ni Made Dwi Aptika, I Ketut Tunas, Ida Ayu Manik Parta Sutema ... 30-37
6. PENGARUH SUHU DAN LAMA PENYIMPANAN TERHADAP KADAR VITAMIN C PADA PAPRIKA (Capsicum annum) HIJAU
Laily Kurniawati, Ni Luh Nova Dilisca Dwi Putri, Adreng Pamungkas ... 38-45
7. ANALISIS KADAR ENZIM CHOLINESTERASE DALAM DARAH PADA PETANI PENYEMPROT SAYURAN
Ni Wayan Pariati, Ni Luh Nova Dilisca Dwi Putri, Agus Nurcolis ... 46-55
8. PERBEDAAN KADAR ZAT ORGANIK SEBAGAI KMnO4 BERDASARKAN PEMBUATAN TITRAN KMnO4 Komang Peri Sukma Rahmawan, Ketut Tunas, Nyoman Sudarma ... 56-63
9. PENENTUAN pH OPTIMUM UNTUK ANALISIS KADAR KLORIDA PADA AIR MINUM
I Made Suddharnatha, M. Fairuz Abadi, Nyoman Sudarma ... 64-70
10. IDENTIFIKASI FORMALIN PADA TAHU YANG DI JUAL DI PASAR PUJUNG GIANYAR DENGAN PEREAKSI SCHIFF
ANALISIS KADAR METAMFETAMINA PADA SAMPEL DARAH DENGAN METODE GC-MS
Metamphetamina Rate Analysis in Blood Sample with GC-MS Method
Dunika Ayu Ni Made1, I Made Oka Adi Parwata2, I.A Manik Parthasutema1 1Program Studi Analis Kesehatan STIKes Wira Medika Bali1
2Program Studi Kimia FMIPA Universitas Udayana2
ABSTRAK
Pendahuluan: Analisis zat-zat golongan narkoba penting dilakukan mengingat tingginya penyalahgunaan narkoba, terutama golongan metamfetamina (MA). Tahun 2007―2010 ditemukan 582 kasus metamfetamina atau 45% dari 1305 kasus narkotika. Penelitian ini bertujuan untuk mendeteksi kandungan MA pada sampel darah pecandu narkoba.Metode: Metode yang digunakan yaitu metode GC-MS yang tervalidasi dan memiliki nilai kepastian yang tinggi. Hasil analisis pada 3 sampel darah pengguna narkoba golongan metamfetamina terdeteksi 2 sampel yang positif. Hasil: Sampel A mengandung MA 64 ppm dan sampel B mengandung MA 28,2 ppm; pada sampel C tidak terdeteksi.Diskusi:Pembuktian hubungan linier antara konsentrasi dan luas area dapat ditentukan persamaan Regresi dan Kurva Kalibrasi. Berdasarkan data GC-MS secara kuantitatif didapatkan data senyawa standar dengan konsentrasi 25 ppm dengan luas area 31907, dan 50 ppm dengan luas area 1130990 dan 100 ppm dengan luas area 34224455 sehingga didapatkan persamaan regresi linier y=42043x-82765 dengan nilai ketepatan yang cukup tinggi.
Kata kunci:Analisis metamphetamina, Sampel darah,GC-MS.
ABSTRACT
Introduction:Analyze the unsure of drugs and it the highert effect of metamphetamina, where in 2007 until 2010 it found 582 case of metamphetamina used 45% from 1305 case of drugs using. The research for detection the metamphetamina contenct of blood sampel.Method:In this research we use Gase Cromatography that have a good validation and high accuracy.Result:The results of 3 drug users of metamphetamina in found that 2 sample have positive results, that is sample A = 64 ppm, and sample B= 28,2 ppm, but in sample C not found the metamphetamina. So, the conclusion of this research is the metamphetamina compound can be accumulate in the blood of drug users.Discussion:Proof linear relationship between the concentration and the area can be determined and the calibration curve regression equation. Based on data from quantitative GC-MS data obtained with the standard compound concentration of 25 ppm and an area of 1907, and 50 ppm with an area of 113099, and 100 ppm with an area of 34224455 to obtain the linear regression equation y = 42043x-82 765 with sufficient precision values high.
Keywards:Analysis Metamphetamina, Blood Sample, GC-MS.
Alamat Korespondensi : Jl. Raya Celuk Sukawati, Gianyar-Bali
Email : [email protected]
PENDAHULUAN
Dewasa ini penyalahgunaan Narkoba atau NAPZA (Narkotika, Psikotropika, dan Zat Aditif lainnya) semakin marak. Pengguna dari usia belasan sampai puluhan tahun, dari kelas ekonomi rendah sampai tinggi, baik laki-laki maupun perempuan. Korban penyalahgunaan narkoba di Indonesia menunjukkan prevalensi dan peningkatan yang sangat tinggi. Tahun 2007 s/d 2010 ditemukan 582 kasus metamfetamin atau 45% dari 1305 kasus narkotika. Data tersebut menunjukkan bahwa penyalahgunaan metamfetamina telah menjadi ancaman serius dan perlu dilakukan penanggulangan masalah secara simultan dan berkesinambungan oleh pemerintah dan seluruh komponen masyarakat (Putra, 2011).
Narkoba singkatan dari narkotik dan obat berbahaya atau NAPZA singkatan dari
Narkotika, Psikotropika dan Zat Adiktif lainnya. Narkoba merupakan zat atau senyawa yang berasal dari tanaman atau bukan tanaman, baik sintesis maupun semi sintetis, yang dapat menyebabkan penurunan atau perubahan kesadaran, hilangnya rasa, mengurangi sampai menghilangkan rasa nyeri dan dapat menimbulkan ketergantungan (BNN, 2004).
semangat, halusinasi atau timbulnya khayalan-khayalan yang menyebabkan efek ketergantungan bagi pemakainya.
Narkotika dibagi menjadi 3 golongan, diantaranya (Darmono, 2006): golongan I merupakan golongan narkotika yang hanya dapat digunakan untuk pengembangan ilmu pengetahuan saja (IPTEK), tidak digunakan untuk terapi, di samping itu golongan ini mempunyai potensi sangat tinggi akan
terjadinya efek
ketergantungan/adiksi/ketagihan. Golongan I, termasuk diantaranya Papaver somniferum L (opiat) serta produk yang dihasilkan; Erytroxylum coca(kokain) serta produk yang dihasilkan, dan Canabis sativa (ganja) serta produk yang dihasilkan.
Golongan II merupakan golongan yang berkhasiat untuk pengobatan, tetapi digunakan sebagai pilihan terakhir dalam pengobatan tersebut. Narkotika golongan ini juga digunakan untuk tujuan ilmu pengetahuan, tetapi juga berpotensi tinggi mengakibatkan ketergantungan. Golongan II, termasuk diantaranya morfin; petidin; metadon; opium; dihidromorfin;danekogin.
Golongan III merupakan jenis narkotika yang berkhasiat untuk pengobatan, tetapi juga untuk pengembangan ilmu pengetahuaan. Obat ini hanya berpotensi ringan untuk mengakibatkan ketergantungan. Golongan III, termasuk diantaranya Kodein; Etil-morfin; Asetil dihidrokodein; dekstropropoksifein; Dihidrokodein dan Norkodein (Darmono, 2006)
Psikotropika merupakan zat atau obat yang dapat menurunkan aktivitas otak atau merangsang susunan syaraf pusat dan menimbulkan prilaku disertai dengan timbulnya halusinasi (khayalan), ilusi, gangguan cara berfikir, perubahan alam perasaan dan dapat menyebabkan ketergantungan, serta mempunyai efek stimulasi bagi pemakainya. Psikotropika dibedakan dalam 4 golongan (UU RI No.5, 2009), antara lain: golongan I merupakan obat yang tidak atau belum mempunyai khasiat pengobatan yang jelas tetapi bila disalahgunakan, sangat merugikan perorangan atau tata kehidupan masyarakat sehingga, diperlukan pengawasan yang sangat ketat peredarannya. Golongan ini hanya digunakan untuk tujuan pengembangan ilmu pengetahuan dan tidak digunakan dalam terapi, serta mempunyai potensi amat kuat untuk mengakibatkan ketergantungan. Golongan I, diantaranya termasuk 3,4methylen dioxi methyl
amphetamine(MDMA) terkenal dengan nama ekstasi ADAM; methylen dioxi amphetamine (MDA) terkenal dengan nama ekstasi saja; methylen dioxi ethyl amphetamine (MDEA) terkenal dengan nama ekstasi EVA;meskalin; lysergic acid diethylamid(LSD); danpsilosibin.
Golongan II merupakan psikotropika yang mempunyai khasiat pengobatan yang jelas, dan apabila disalahgunakan sangat merugikan kesehatan perorangan, atau tata kehidupan masyarakat, karena itu diperlukan pengawasan ketat terhadap pengedarnya. Golongan ini selain berkhasiat pengobatan juga dapat digunakan untuk terapi dan untuk tujuan ilmu pengetahuan, serta mempunyai potensi kuat untuk menyebabkan ketergantungan. Golongan II, termasuk diantaranya: amfetamin; metamfetamin yang terkenal dengan nama shabu-shabu; deksampetamin; fenetilin; dan PCP (Pensiklidin).
Golongan III merupakan psikotropika yang mempunyai khasiat pengobatan jelas dan bila disalahgunakan merugikan kesehatan perorangan atau tatanan kehidupan bermasyarakat, sehingga masih memerlukan pengawasan peredarannya. Golongan ini dapat digunakan untuk terapi dan tujuan pengembangan ilmu pengetahuan serta berpotensi sedang untuk menimbulkan ketagihan/ ketergantungan. Termasuk golongan III, diantaranya: amobarbital; butabarbital; flunitazepam; glutemide; pentobarbital; siklobarbitaldankatina.
Golongan IV merupakan psikotropika yang mempunyai khasiat pengobatan yang jelas, dan apabila disalahgunakan dapat merugikan kesehatan pengguna dan mengganggu tata kehidupan masyarakat sekitarnya sehingga diperlukan pengawasan yang memadai. Golongan ini selain dapat digunakan dalam pengobatan, juga untuk keperluan ilmu pengetahuan, serta berpotensi ringan untuk menyebabkan ketergantungan. Termasuk golongan IV, diantaranya:alpazolam; barbital; bromazepam; diazepam; fenobarbital.
Chemistry Laboratory Juli Vol. 2 No. 1 2015
20 dalam air dan alkohol. Bahan atau zat
berbahaya ini dapat berpengaruh pada fisik dan mental seseorang apabila digunakan dengan dosis yang tidak tepat (Adi, 2009). Senyawa ini merupakan psikotropikadengan daya aktif yang kuat sehingga menyebabkan sindroma ketergantungan (Martono, 2006). Metamfetamine (MA) sering disebut d-deoxyepedhrine; desoxyephedrine; atau methylamfetamine; mempunyai rumus molekul c10h15n, dengan berat molekul 149,23 g/mol,
bentuk cairan yang tidak berwarna, jernih, tidak mudah menguap, berat jenis 0,91-0,92 g/L, titik didih 214oC dengan struktur kimia seperti
gambar 1.
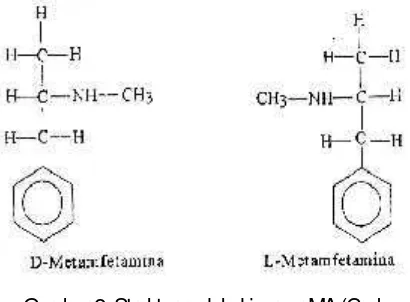
Gambar 1. Molekul MA (Moffatet al., 2004) MA termasuk salah satu dari derivate metal amphetamineyang mempunyai 2 isomer: d-metamphetamina dan l-metamphetamina dimana masing-masing memiliki perbedaan efek farmakologi. d-metamphetamina adalah stimulan karena mempunyai efek yang sangat kuat pada sistem saraf pusat, menambah tenaga sehingga disebut menimbulkan efek euphoria terhadap manusia. biasanya dikonsumsi dengan cara ditelan, dihirup, dihisap serta disuntikkan. sedangkan, l-metamphetamina bersifat decongestan dan tidak memiliki aktivitas sebagai stimulant (putra, 2011). struktur molekul isomer dari ma dapat dilihat pada gambar 2.
Gambar 2. Struktur molekul isomer MA (Cody, 2000)
MA digolongkan sebagai obat anti depresi atau stimulan yang berguna untuk mengatasi tekanan mental karena secara langsung
merangsang susunan saraf pusat (pada dosis rendah; 5 mg/hari), sedangkan pada dosis yang dinaikkan dapat meningkatkan tekanan darah, dalam peredaran gelapnya, MA seringkali ditemukan sebagai senyawa garam hidroklorida, biasanya dalam bentuk kristal yang berwarna putih, dengan titik leleh 170-175oC,
larut dalam air (1:2), larut dalam etanol (1:4), larut dalam kloroform (1:5), praktis tidak larut dalam eter (Putra, 2005). Adapun contoh kristal MA dapat dilihat pada gambar 3.
Gambar 3. Kristal MA (Putra, 2005)
Setelah dikonsumsi dalam waktu 24 jam maka sekitar 70% dosis obat akan tereliminasi melalui ginjal dan diekskresikan dalam bentuk urine. Pada kondisi normal lebih dari 43% dari dosis diekskresikan sebagai MA, 15% sebagai 4-hidroksi metamphetamina(HMA) dan sekitar 5% sebagaiamphetamine. Tingkat ekskresi dan jumlah presentase sebagai metabolit obat dalam bentuk tidak berubah tergantung pada pH urin, akan bertambah jika urin dalam keadaan asam dan akan berkurang sekitar 2% jika urine dalam keadaan basa (Nendrosuwito, 1998). Jalur metabolisme MA dapat dilihat pada gambar 4 (Putra, 2005).
Ketika mengkonsumsi metamphetamina maka obat tersebut turun melalui esophagus (kerongkongan), masuk lambung, dan menuju ke usus halus. Sejumlah kecil zat yang terkandung pada obat diserap melalui aliran darah dalam membrane mukus, dan sebagaian besar masuk ke aliran darah melalui dinding usus halus. Zat yang terkandung pada obat terlarang tersebut larut dalam air dan aliran darah dengan cepat menyalurkan keseluruh bagian tubuh dan diserap kedalam jaringan tubuh (Wirasuta, 2008)
Aktivitas metamfetamin di seluruh otak tampaknya lebih spesifik, reseptor tertentu yang merespon metamfetamin, tetapi beberapa daerah otak cenderung tidak melakukannya di wilayah lain. Sebagai contoh dopamine D2
reseptor di hippocampus, suatu daerah otak yang terkait dengan membentuk ingatan baru, tampaknya tidak terpengaruh oleh kehadiran metamfetamin. Sistem saraf utama yang dipengaruhi oleh metamfetamina sebagaian besar terlibat didalam sirkuit otak. Selain itu, neurotransmitteryang terlibat jalur berbagai hal penting di otak tampaknya menjadi target utama dari metamfetamina. Salah satu neurotransmitter adalah dopamine, sebuah pembawa pesan kimia yang sangat akktif. MA menyebabkan terjadinya pelepasan norepinefrin, dopamine, serotonin, dan neuron pra-sinaps. Menghambatre-uptakenorepinefrin dan dopamine. Menghambat sistem MAO pada neuronpra-sinaps(BNN Jakarta, 2004).
Mekanisme kerja metamfetamina antara lain: dosis kecil, semua jenis metamfetamine akan menaikkan tekanan darah, mempercepat denyut jantung, melebarkan bronkus, meningkatkan kewaspadaan, menimbulkan euphoria, menghilangkan ngantuk, mudah terpacu, menghilangkan rasa lelah dan rasa lapar, meningkatkan aktifitas motorik, banyak bicara dan merasa kuat, misalnya pada fisik atlet meningkat. Efek ini sangat bervariasi dan dapat terjadi hal-hal yang sebaliknya pada dosis berlebihan atau pengguna berulang-ulang. Pengguna lama atau dosis besar hampir selalu diikuti oleh depresi mental dan kelelahan fisik, banyak orang yang mengkonsumsi metamfetamina mengalami sakit kepala, palpitasi, rasa pusing, gangguan vasomotor, rasa khawatir, kacau, disforia, delirium atau rasa lelah (BNN Jakarta, 2004).
Dosis sedang (20-50 mg), menstimulasi pernapasan, menimbulkan tremor ringan, gelisah, meningkatkan aktivitas motorik,
insomnia, agitasi, mencegah lelah, menekan nafsu makan, menghilangkan ngantuk dan mengurangi tidur (BNN Jakarta, 2004). Dosis Tinggi (> 50 mg), metamfetamina yang masuk secara berlebihan dapat langsung mengakibatkan kematian, gejala yang ditimbulkan sebelum kematian adalah tremor berat, meningkatnya aktivitas motorik yang berlebihan, dan gangguan pernafasan yang hebat hingga nafas berhenti (BNN Jakarta, 2004).
Ketika seseorang menggunakanupperzat tersebut akan merangsang sistem saraf pusat penggunanya. Zat bekerja pada sistem neurotransmitter norepinefrin dan dopamine otak. Menggunakan metamfetamina dapat menyebabkan otak menghasilkan tingkat dopamine yang lebih tinggi. Jumlah dopamine yang berlebihan di dalam otak akan menghasilkan perasaan euphoria dan kesenangan yang biasa dikenal sebagai“high”. Seiring berjalannya waktu, orang yang menggunakan shabu akan mengembangkan toleransi terhadap zat metamphetamin yang terkandung didalam shabu. Toleransi artinya seseorang akan membutuhkan dosis yang lebih tinggi untuk mendapatkan efek yang sama. Jika sejumlah dosis yang dibutuhkan tidak terpenuhi maka pengguna zat metamfetamina akan muncul perasaanwithdrawal/cravingatau lebih dikenal dengan sakaw (Darmono, 2006).
Sensasi yang ditimbulkan membuat otak lebih jernih dan bisa berpikir lebih fokus. Otak menjadi lebih bertenaga untuk berpikir berat dan bekerja keras, namun akan muncul kondisi arogan yang tanpa sengaja muncul akibat penggunaan zat ini. Pupil akan berdilatasi (melebar). Nafsu makan akan sangat ditekan. Tekanan darah akan naik secara signifikan. Secara mental, pengguna akan mempunyai rasa percaya diri yang lebih karena, seluruh sistem saraf pusat terstimulasi maka kewaspadaan dan daya tahan tubuh juga meningkat (Harian Umum Pelita, 2013).
Chemistry Laboratory Juli Vol. 2 No. 1 2015
22 lapar menjadi sangat lapar (Agsya, 2010). Efek
metamfetamina jangka pendek, antara lain: meningkatkan suhu tubuh; kerusakan sistem kardiovaskuler; paronoia; meningkatkan denyut jantung; meningkatkan tekanan darah; menjadi hiperaktif; mengurangi rasa kantuk; menjadi hiperaktif; tremor; menurunkan nafsu makan; mulut kering; mual; sakit kepala, dan perubahan prilaku (Arief, 2005).
Efek metamfetamina jangka panjang, selama mengkonsumsi metamfetamina dalam jangka panjang, seseorang yang menggunakan metamfetamina secara teratur menemukan tanda-tanda efek samping jangka panjang yang biasanya terdiri dari: pandangan kabur; pusing; peningkatan detak jantung; sakit kepala; tekanan darah tinggi; kurang nafsu makan; nafas cepat dan gelisah (Arief, 2005)
Gejala lain yang ditimbulkan dari metamfetamina antara lain: kerusakan otak, kerusakan hati, depresi, gelisah, berkeringat dingin, berpikir lambat, serta gangguan memori karena berkurangnya serotonin dan dopamine dalam jangka lama. Depresi menyebabkan individu menyendiri, menurunnya prestasi kerja atau sekolah. Penyalahgunaan senyawa ini dapat menimbulkan efek samping yang sangat berbahaya bahkan dapat mematikan (Darmono, 2006).
Metamfetamina merangsaang faal dan fungsi otak, serta memiliki potensi perangsangan dan halusinogenik yang lebih besar (Nasution, 2001). Metamfetamina berpotensi merusak reseptor serotonin dan juga neuron serotonin dalam otak. Serotonin adalah sistem kimia saraf (neurochemical) yang mengatur emosi, perasaan, berpikir mengingat (memory)dan tidur (Darmono, 2006). Stimulan dalam metamfetamina memacu sistem saraf pusat, akibat dari kadar toksin yang dihasilkan untuk masing-masing obat tidak bisa diperkirakan, overdosis merupakan kemungkinan yang nyata (BNN Jakarta, 2004).
Penyalahgunaan metamfetamina sering kali terjadi karena kebanyakan zat dalam narkoba sebenarnya digunakan untuk pengobatan dan penelitian. Tetapi, karena berbagai alasan maka narkoba kemudian disalahgunakan. Penggunaan terus menerus dan berlanjut akan menyebabkan ketergantungan dan bisa juga disebut dengan kecanduan. Tingkat penyalahgunaan biasanya sebagai berikut: coba-coba; senang; menggunakan pada saat ataukeadaantertentu;
penyalahgunaan dan ketergantungan (BNN Jakarta, 2004).
Banyak yang masih bisa dilakukan untuk mencegah penyalahgunaan narkoba, antara lain yaitu: secara primer, sebelum penyalahgunaan terjadi, biasanya dalam bentuk pendididkan, penyebaran informasi mengenai bahaya narkoba, pendekatan melaliu keluarga, dll. Secara sekunder, pada saat pengguna sudah terjadi dan diperlukan upaya penyembuhan (treatment). Secara tersier, yaitu upaya untuk merehabilitasi mereka yang sudah memakai dan dalam proses penyembuhan (BNN Jakarta, 2004).
Maka dari itu diperlukan pemeriksaan narkoba yang digunakan untuk penanganan penyalahgunaan narkoba. Pemeriksaan narkoba dapat dilakukan dengan berbagai macam alat serta metode. Salah satunya dengan metode GC-MS. GC-MS adalah kependekan dari gas chromaography massa spektrofotometri. Instrumen alat ini merupakan gabungan dari alat GC dan MS. Sampel yang hendak diperiksa diidentifikasi dahulu dengan alat GC(gas chromatography)baru, kemudian diidentifikasi dengan alat ms (mass spectrometry). GC dan MS merupakan kombinasi yang simultan dan digunakan untuk memisahkan serta mengidentifikasi komponen-komponen campuran (Mulyono, 2011).
Kromatografi Gas-Spektroskopi Massa atau sering disebut GC-MS (gas cromatography-mass spectrometry) adalah teknik analisis yang menggabungkan 2 metode analisis yaitukromatografi gas dan spektroskopi massa. kromatografi gas adalah metode analisis, dimana sampel terpisahkan secara fisik menjadi bentuk molekul-molekul yang lebih kecil (hasil pemisahan dapat dilihat berupa kromatogram). Sedangkan spektrofotometri massa adalah metode analisis, dimana sampel yang dianalisis akan diubah menjadi ion-ion gasnya. Masa dari ion-ion tersebut dapat diukur berdasarkan hasil deteksi berupa spektrum massa. Pada GC hanya terjadi pemisahan untuk mendapatkan komponen yang diinginkan, sedangkan bila dilengkapi dengan MS (berfungsi sebagai detektor) akan dapat mengidentifikasi komponen tersebut, karena bisa membaca spektrum bobot molekul pada suatu komponen, juga terdapatreferencepada software(Hermanto, 2008).
Kromatografi gas merupakan salah satu teknik kromatografi, dimana yang bertindak sebagai fase diam dapat berupa fase padat atau fase cair dan sebagai fase gerak adalah gas. Kromatografi gas merupakan salah satu metode yang dapat dipergunakan untuk menganalisis keberadaan MA dalam sampel darah (Putra, 2011)
Kromatografi gas dan spektrometer massa dalam banyak hal memiliki banyak kesamaan dalam tekniknya, untuk kedua teknik tersebut, sampel yang dibutuhkan dalam bentuk fase uap, dan keduanya juga sama-sama membutuhkan jumlah sampel yang sedikit (umumnya kurang dari 1 mg). Di sisi lain, kedua teknik tersebut memiliki perbedaan yang cukup besar yakni pada kondisi operasinya. Senyawa yang terdapat pada kromatografi gas adalah senyawa yang digunakan untuk sebagai gas pembawa dalam alat GC dengan tekanan kurang lebih 760 torr, sedangkan spektrometer massa beroperasi pada kondisi vakum dengan kondisi tekanan 10-6sampai 10-5torr
(Hermanto, 2008).
GC-MS terdiri dari dua blok bangunan utama: kromatografi gas dan spektrometer massa. Kromatografi gas menggunakan kolom kapiler yang tergantung pada dimensi kolom itu (panjang, diameter, ketebalan film) serta sifat fase (misalnya 5% fenil polisiloksan). Perbedaan sifat kimia antara molekul-molekul yang berbeda dalam suatu campuran dipisahkan dari molekul dengan melewatkan
sampel sepanjang kolom. Molekul-molekul memerlukan jumlah waktu yang berbeda (disebut waktu retensi) untuk keluar dari kromatografi gas, dan ini memungkinkan spektrometer massa untuk menangkap, ionisasi, mempercepat, membelokkan, dan mendeteksi molekul terionisasi secara terpisah. Spektrometer Massa melakukan hal ini dengan memecah masing-masing molekul menjadi terionisasi mendeteksi fragmen menggunakan massa untuk mengisi rasio (Hermanto, 2008).
Gambar 5. GC-MS Shimadzu(Hermato,2008)
Dasar pemisahan secara kromatografi gas ialah penyebaran cuplikan pada fase diam sedangkan gas sebagai fase gerak mengelusi fase diam. Maka dari itu prinsip kerjanya sebagai berikut: suatu fase gerak berbentuk gas mengalir dibawah tekanan melewati pipa yang dipanaskan dan disalut dengan fase diam cair, atau dikemas dengan fase diam cair yang disalut pada suatu penyangga padat. Analit tersebut dimuatkan kebagian atas kolom melalui suatu portal injeksi yang dipanaskan, tempat analit menguap. Analit ini kemudian berkondensasi dibagian atas kolom tersebut, yaitu pada suhu yang lebih rendah. Suhu oven dijaga konstan atau diprogram agar meningkat secara bertahap. Ketika sudah berada dikolom, pemisahan suatu campuran yang terjadi bergantung pada waktu lamanya waktu relatif yang dibutuhkan oleh komponen-komponen didalam fase diam (Hermanto, 2008).
Chemistry Laboratory Juli Vol. 2 No. 1 2015
24 k =
Keterangan:
CS : Konsentrasi solute dalam fase diam
CM : Konsentrasi solute dalam fase gerak
(Putra, 2011).
Derajat keterpisahan/resolusi masing-masing komponen dalam campuran dengan metode analisis kromatografi dinyatakan dengan persamaan:
2(tR2– tR1)
W2+ W1
Keterangan:
tR1 : waktu retensi kromatogram 1
tR2 : waktu retensi kromatogram 2
W1 : lebar dasar puncak kromatogram1
W2 : lebar dasar puncakkromatogram2
(Putra, 2011).
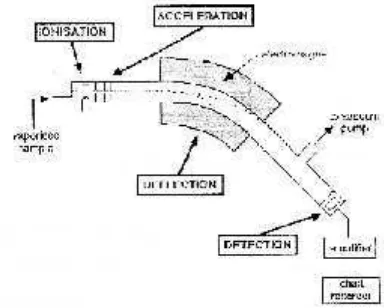
Gambar 6. Bagan instrument GC MS (Rohman, 2009)
Bentuk puncak kromatogramKromatografi Gas dapat dilihat pada gambar 7 berikut:
Gambar 7. Puncak kromatogram GC (Gritteret al., 1991).
Instrument spectrometer massa diperlukan untuk identifikasi senyawa organik yaitu penentuan bobot molekul dan penentuan rumus molekul. Prinsip dasar Spektrometri Massa adalah molekul bermuatan atau fragmen molekul dihasilkan dalam suatu ruang sangat hampa atau segera sebelum suatu sampel memasuki ruang sangat hampa, dengan menggunakan berbagai metode untuk produksi ion. Ion-ion dihasilkan dalam fase gas sehingga ion tersebut kemudian dapat dimanipulasi dengan penerapan pada medan magnet atau medan listrik agar dapat menentukan bobot molekulnya dan bobot molekul semua fragmen yang dihasilkan dari pemecahan molekul. Umumnya spektrometer massa terdiri dari lima komponen yaitu: sistem pemasukan sampel, kamar ionisasi, penganalisis massa, detektor dan rekorder (David, 2005). Contoh bagan MS dapat dilihat pada gambar 6. berikut:
Gambar 8. Bagan instrumen MS (David, 2005)
Spektrum massa biasanya digambarkan seperti grafik batang, dimana setiap puncak menyatakan suatu fragmen molekul, fragmen ditata menurut kenaikan m/z dari kiri ke kanan dengan intesitas puncak sebanding dengan kelimpahan relative fragmen, puncak tertinggi (puncak dasar) diberi nilai 100%, puncak yang lain relative terhadap puncak dasar, untuk mengetahui rumus molekul atau fragmen tertentu dapat dibantu dengan tabel Beynon (David, 2005).Mode selected ion monitoring (SIM) pada GC MS adalah mode operasi yang tidak merekam keseluruhan spectra, tetapi hanya merekam sinyal karakteristik dari ion-ion tertentu (Moffat,et al, 2004). Proses scanper ion pada mode SIM lebih banyak dibandingkan dengan modefull scan dalam waktu yang bersamaan, hal ini disebabkan pada tingkat sensitivitasnya (Putra, 2011).
Instrumen/Alat GC-MS terdiri dari: injection port, dalam pemisahan dengan GLC cuplikan harus dalam bentuk fase uap. Tetapi kebanyakan senyawa organik berbentuk cairan dan padatan, oleh karena itu, senyawa yang berbentuk cairan dan padatan pertama-tama harus diuapkan. Ini membutuhkan pemanasan sebelum masuk ke dalam kolom. Panas itu terdapat pada tempat injeksi. Namun, suhu tempat injeksi tidak boleh terlalu tinggi, sebab kemungkinan akan terjadi perubahan karena panas atau penguraian dari senyawa yang akan dianalisa. pengguna juga tidak boleh menginjeksikan cuplikan terlalu banyak, karena GC sangat sensitif. Biasanya jumlah cuplikan yang diinjeksikan pada waktu kita mengadakan analisa 0,5―50 ml gas dan 0,2―20 ml untuk cairan (Hermanto, 2008). Oven digunakan untuk memanaskan kolom pada temperature tertentu sehingga mempermudah proses pemisahan komponen sampel. Biasanya oven memiliki jangkauan suhu 30oC―320oC (Hermanto, 2008). Kolom
merupakan jantung dari kromatografi gas. Ada beberapa bentuk kolom, diantaranya lurus, bengkok, misal berbentuk V atau W, dan kumparan/spiral. Kolom selalu merupakan bentuk tabung. Berisi fasa diam, sedangkan fasa bergerak akan lewat didalamnya sambil membawa sample. Secara umum terdapat 2 jenis kolom, yaitu: packed column, umumnya terbuat dari glass atau stainless steel coil dengan panjang 1–5 m dan diameter kira-kira 5 mm. Capillary column, umumnya terbuat dari purified silicate glassdengan panjang 10―100 m dan diameter kira-kira 250 mm. Beberapa jenisstationary phaseyang sering digunakan: polysiloxanesuntuknonpolar analytes/sample;
polyethylene glycol untuk polar
analytes/sample, danInorganic atau polymer packinguntuk sampel bersifat small gaseous species(Hermanto, 2008). Massa Spektrometer (MS) yang terdiri dari beberapa komponen diantaranya: sumber ion setelah analit melalui kolom kapiler, ia akan diionisasi. Ionisasi pada spektroskopi massa yang terintegrasi dengan GC ada dua, antara lain: electron impact ionization (EI) atau chemical ionization (CI), yang lebih jauh lagi terbagi menjadi negatif (NCI) dan positif (PCI). Berikutnya akan dijelaskan ionisasi EI. Ketika analit keluar dari kolom kapiler, ia akan diionisasi oleh elektron dari filament tungsten yang diberi tegangan listrik. Ionisasi terjadi bukan karena tumbukan elektron dan molekul, tapi karena interaksi
medan elektron dan molekul, ketika berdekatan. Hal tersebut menyebabkan satu elektron lepas, sehingga terbetuk ion molekular M+, yang
memiliki massa sama dengan molekul netral, tetapi bermuatan lebih positif. Adapun perbandingan massa fragmen tersebut dengan muatannya disebutmass to charge ratioyang disimbolkan M/Z. Ion yang terbentuk akan didorong ke quadrupoles atau mass filter. Quadrupoles berupa empat elektromagnet (Hermanto, 2008). Filter, pada quadrupoles, ion-ion dikelompokkan menurut M/Z dengan kombinasi frekuensi radio yang bergantian dan tegangan DC. Hanya ion dengan M/Z tertentu yang dilewatkan olehquadrupolesmenuju ke detector (Hermanto, 2008). Detektor terdiri atas high energy dynodes (HED) dan electron multiplier(EM)detector. Ion positif menuju HED, menyebabkan elektron terlepas. Elektron kemudian menuju kutub yang lebih positif, yakni ujung tanduk EM. Ketika elektron menyinggung sisi EM, maka akan lebih banyak lagi elektron yang terlepas, menyebabkan sebuah arus/aliran. Kemudian sinyal arus dibuat oleh detektor proporsional terhadap jumlah ion yang menujudetector (Hermanto, 2008). Data dari spektrometri masa dikirim ke komputer dan diplot dalam sebuah grafik yang disebut spektrum masa. Secara umum, penggunaan metode GC-MS hanya terbatas untuk senyawa dengan tekanan uap berkisar 10-10 torr.
Kebanyakan senyawa dengan tekanan lebih rendah hanya dapat dianalisis jika senyawa tersebut merupakan senyawa turunan (contoh: trimetilsili eter). Penentuan gugus fungsional pada cincin aromatik masih sulit, untuk senyawa isomer tidak dapat dibedakan oleh Spektofotometer (contoh:naftalena vs azulena), tapi dapat dipisahkan dengan Kromatografi (Hermanto, 2008).
Chemistry Laboratory Juli Vol. 2 No. 1 2015
26 Pelarut harus bersifat volatile dan organik
(sebagai contoh heksana atau dikllorometana). Jumlah sampel bergantung pada metode ionisasi yang dilakukan, biasanya yang sering digunakan untuk analisis sensivitas adalah sebesar 1–100 pg per komponen (Hermanto, 2008).
Keunggulan metode GC-MS antara lain: efisien, resolusi tinggi sehingga dapat digunakan untuk menganalisa partikel berukuran sangat kecil seperti polutan dalam udara. Aliran fasa bergerak (gas) sangat terkontrol dan kecepatannya tetap. Pemisahan fisik terjadi didalam kolom yang jenisnya banyak sekali, panjang dan temperaturnya dapat diatur. Banyak sekali macam detektor yang dapat dipakai pada kromatografi gas (saat ini dikenal 13 macam detektor) dan respons detektor adalah proporsional dengan jumlah tiap komponen yang keluar dari kolom. Sangat mudah terjadi pencampuran uap sampel kedalam fasa bergerak. Kromatograf sangat mudah digabung dengan instrumen fisika-kimia yang lainnya, contohnya GC/FT-IR/MS. Analisis cepat, biasanya hanya dalam hitungan menit. Tidak merusak sampel. Sensitivitas tinggi sehingga dapat memisahkan berbagai senyawa yang saling bercampur dan mampu menganalisa berbagai senyawa meskipun dalam kadar/konsentrasi rendah. Seperti dalam udara, terdapat berbagai macam senyawa yang saling bercampur dan dengan ukuran partikel/molekul yang sangat kecil (Hermanto, 2008).
Selain keunggulan metode GC-MS juga memiliki kekurangan antara lain sebagai berikut: teknik Kromatografi Gas terbatas untuk zat yang mudah menguap. Kromatografi Gas tidak mudah dipakai untuk memisahkan campuran dalam jumlah besar. Pemisahan pada tingkat mg mudah dilakukan, pemisahan pada tingkat gram mungkin dilakukan, tetapi pemisahan dalam tingkat pon atau ton sukar dilakukan kecuali jika ada metode lain. Fase gas dibandingkan sebagian besar fase cair tidak bersifat reaktif terhadap fase diam dan zat terlarut (Hermanto, 2008).
Metode ini digunakan untuk menganalisis obat-obatan terlarang baik pada sampel urine, serum, maupun darah. Ketika mengkonsumsi obat-obat terlarang, obat tersebut turun melalui esophagus (kerongkongan), masuk lambung, dan menuju ke usus halus. Sejumlah kecil zat yang terkandung pada obat diserap melalui aliran darah dalam membrane mukus, dan
sebagian besar masuk ke aliran darah melalui dinding usus halus. Zat yang terkandung pada obat terlarang tersebut larut dalam air dan aliran darah dengan cepat menyalurkan ke seluruh bagian tubuh dan diserap ke dalam jaringan tubuh (Wirasuta, 2008). Berdasarkan uraian di atas maka penulis merasa perlu melakukan analisis kadar narkotika golongan metamfetamina pada sampel darah dengan metodeGC-MS.
BAHAN DANMETODE
Penelitian ini menggunakan jenis penelitian yang bersifat deskriptif, yaitu penelitian yang dilakukan dengan tujuan mengetahui gambaran atau deskripsi tentang suatu keadaan objek (Notoatmodjo, 2005). Populasi pada penelitian ini adalah seluruh pengguna narkoba yang direhabilitasi di Laboratorium Forensik Cabang Denpasar, sehingga sampel dalam penelitian ini adalah darah pengguna narkoba yang terdapat di Laboratorium Forensik Cabang Denpasar. Penelitian ini telah telah dilaksanakan pada tanggal 12-17 Mei 2014, dan dianalisis di Laboratorium Forensik Polri Cabang Denpasar. Adapun alat-alat yang digunakan dalam penelitian ini, antara lain: neracaanalitik; batang pengaduk; labu ukur 10 ml; spektofotometer infrared(ir); lemari es;cartridge spe;eksterlute (spe bond elute c-18); beaker glass 10 ml; mikropipet disposable; ph meter atau kertas ph indikator;laminar air flow; dan seperangkat alat GC-MS. Selain itu bahan yang digunakan antara lain sebagai berikut: bahan yang digunakan dalam penelitian ini, antara lain: kloroform; methanol; NaOH;aquadest; MA-HCl dan darah sampel pengguna narkoba.
standar 100 ppm, dimasukkan ke dalam labu ukur 10 mL, kemudian ditambahkan methanol sampai garis tanda. Larutan standar metamfetamina 25 ppm dibuat dengan cara memipet 5 mL larutan standar 50 ppm, dimasukkan ke dalam labu ukur 10 mL, kemudian ditambahkan methanol sampai garis tanda. Preparasi sampel darah pecandu narkoba: disiapkan alat dan bahan yang digunakan, dituangeksterlute(SPEBond Elute C-18) kedalam cartridge SPE sampai tanda batas (secukupnya), dikeluarkan sampel darah pengguna narkoba dan ditampung padabeaker glass sebanyak 5 mL, ditambahkan larutan NaOH hingga basa (pH 8), dihomogenkan dengan batang pengaduk kemudian ditambahkanaquadestsecukupnya hingga larut sempurna, setelah itu, dituang padacoloumb SPE sampai eksterlute terisi sampai merata, dielusi dengan kloroform sebanyak 10 mL, kemudian diambil ekstrak darah yang dihasilkan, dikeringkan padalaminar air flow, setelah kering dilarutkan kembali dengan larutan methanol sebanyak 5 mL, dipipet ekstrak darah yang sudah dilarutkan dengan methanol sebanyak 100 µl, dan dituang kedalam tabung eppendro, ekstak darah / sampel siap diinjeksi pada alat MS. Uji GC-MS: Sampel dari ekstraksisolid-phase, diinjek 1 µl pada GC-MS dengan kondisi: temperatur ijektor/detektor 2800C, kecepatan alir gas He
40ml/min, temperatur kolom 700C untuk 3 menit, kemudian 120C/min sampai 2100C dan tahan selama 15 menit, kolom DB-5/HP-5. berdasarkan data yang didapatkan diperoleh hasil pemeriksaan kadar metamfetamina pada sampel darah dan disajikan dalam bentuk tabel.
HASIL
Berdasarkan penelitian yang telah dilaksanakan di Laboratorium Forensik Polri Cabang Denpasar diperoleh hasil penelitian sebagai berikut:
Tabel 1. Kadar metamfetaminadari hasil analisis denganGC-MS
Sampel Darah A B C
Luas Area 459511 15452 3
Sampel darah yang digunakan pada penelitian ini diperoleh dari Laboratorium Forensik Cabang Denpasar yang diketahui sebagai barang bukti kasus pengguna narkoba. Sampel darah dipreparasi terlebih dahulu dengan cara dielusi dengan menggunakan larutan NaOH dandiukur dengan menggunakan pH meter hingga basa (pH 8), dimana larutan NaOH berfungsi untuk mengkondisikan sampel darah pada pH basa karena metamfetamina lebih mudah diekstraksi pada kondisi basa serta memiliki kelarutan yang lebih tinggi pada suasana basa, kemudian dihomogenkan dengan batang pengaduk serta ditambahkan aquadestsecukupnya hingga larut sempurna, setelah larut sempurna sampel darah dituang pada coloumb SPE sampai eksterlute terisi sampai merata, kemudian dielusi dengan menggunakan larutan kloroform sebanyak 10 ml yang digunakan untuk mengekstraksi senyawa metamfetamina dari darah, kemudian diambil ekstrak darah dan dikeringkan pada laminar air flow. Setelah kering kemudian ekstrak darah dilarutkan kembali dengan menggunakan larutan methanol sebanyak 100 µl.
Sampel darah yang dipreparasi kemudian diinjeksikan ke alat GC-MS sebanyak 1 µl, dengan menggunakan data luas area kromatogram sampel dan persamaan garis regresi senyawa standar, maka dapat ditentukan kadar metamfetamina yang terdapat pada sampel darah, untuk menentukan kadar metamfetamina pada sampel darah diperlukan standar MA, pemeriksaan standar MA meliputi pemeriksaan pemerian, kelarutan serta uji dengan menggunakan instrument Infrared spektofotometer. Standar MA yang digunakan berbentuk kristal berwarna putih dan tidak berbau, titik leleh 1720C, larut dalam air, alkohol,
dan kloroformtetapi tidak larut dalam eter. Maka kristal metamfetamina yang dipakai telah memenuhi syarat untuk dipergunakan sebagai standar MA.
Chemistry Laboratory Juli Vol. 2 No. 1 2015
28 sehingga diharapkan bisa meningkatkan
sensitivitas metode analisis. Optimasi kromatografi gas spektofotometri massa dilakukan dengan memilih sistem dan kondisi yang sesuai sehingga diperoleh pemisahan yang baik diantara senyawa-senyawa yang dipisahkan. Komponen sistemkromatografi gas terdiri dari gas pembawa, kolom, dandetector. Kondisi yang dipilih meliputi suhuinjector, suhu kolom, suhudetector, dan kecepatan aliran gas pembawa. Sistem dan kondisi kromatografi gas yang digunakan berdasarkan pada penelitian sebelumnya serta dengan memperhatikan sifat fisik komponen yang dipisahkan (Putra, 2011).
Pembuktian hubungan linier antara konsentrasi dan luas area dapat ditentukan persamaan regresi dan kurva kalibrasi. Berdasarkan data GC-MS secara kuantitatif didapatkan data senyawa standar dengan konsentrasi 25 ppm dengan luas area 319077, 50 ppm dengan luas area 1130990, dan 100 ppm dengan luas area 3424455 sehingga didapatkan persamaan regresi linier y=42043x-82765 dengan nilai regresi R2=0,993. Hal ini
menunjukkan bahwa secara analisis senyawa metamfetamina dapat terdeteksi dengan nilai ketepatan yang cukup tinggi. Sehingga, diperoleh hasil analisis pada tiga orang pengguna metamfetamina terdeteksi hanya 2 dua orang yang positif yaitu: pada sampel darah A: 64ppm, sampel darah B: 28,2 ppm dan sampel darah C: tidak terdeteksi, hal ini kemungkinan terjadi karena jeda waktu menggunakan obat tersebut (sudah lama tidak menggunakan), faktor lama penggunaan MA, pecandu kronis serta pengguna pemula, konsentrasi MA pada sampel darah C sangat kecil dibawah nilai limit deteksi atau karena telah hilang saat proses ekstraksi, faktor metabolisme dalam tubuh, faktor rute perjalanan MA setelah dikonsumsi belum sampai pada peredaran darah.
Senyawa metamfetamin (MA) dapat terdeteksi dalam darah dengan kadar yang kecil, walaupun pada urinnya sudah tidak terdeteksi. Hal ini terjadi karena dalam waktu 24 jam setelah dikonsumsi maka sekitar 70% dosis obat akan tereliminasi melalui ginjal dan disekresikan dalam bentuk urine, dalam kondisi normal lebih dari 43% dari dosis disekresikan, tingkat ekskresi dan jumlah presentase sebagai metabolit obat dalam bentuk tidak berubah tergantung pada pH urine, akan bertambah jika urine dalam keadaan asam dan akan berkurang
2% jika urine dalam keadaan basa (Putra, 2011).
SIMPULAN DAN SARAN
Simpulan
Berdasarkan penelitian yang telah dilaksanakan maka dapat disimpulkan bahwa sampel darah A, B, dan C masing-masing secara berurutan mengandung methampetamin dalam satuan ppm adalah: 64,00; 28,2 dan 0,00.
Saran
Saran yang dapat disampaikan: perlu dilakukan penelitian lebih lanjut mengenai NAPZA dengan metode yang lain, perlu dilakukan penelitian lebih lanjut mengenai NAPZA dengan mengambil sampel bagian tubuh yang lain, perlu dilakukan pengawasan lebih ketat dan berkesinambungan terhadap NAPZA.
KEPUSTAKAAN
Arief, B.N., 2005. Bunga Rampai Kebijakan Hukum Pidana. Bandung: Citra Aditya Bakti.
Asya, F., 2009. Narkotika dan Psikotropika. Jakarta: Asa Mandiri.
Badan Narkotika Nasional, 2003a. Pedoman Pencegahan Penyalahgunaan NARKOBA.Jakarta.
Badan Narkotika Nasional, 2004b. Pedoman Pencegahan Penyalahgunaan NARKOBA.Jakarta.
Cody, J. T., 2000.Amphetamines. In: Maciej J Bogusz. editors. Handbook of Analytical Separations. Vol. 2. Elsevier, 107
Darmono, 2006.Toksologi Narkoba danAlkohol (Pengaruh Neorotoksisitasnya pada Saraf Otak). UIP. Jakarta: Universitas Indonesia.
Gritter, R. J., James, M. B. and Arthur E. S., 1991. Pengantar Kromatografi. (Kosasih, Penjt). Edisi kedua. Bandung: ITB
Harian Umum Pelita. Kasus NARKOBA Banten Masih Tinggi Edisi Rabu 1 Mei 2013. (online), (http://pelita.or.id.)
Hermanto, 2008.Aplikasi Alat HPTLC dan GC-MS.Jakarta.
Kusno, A., 2009. Kebijakan Kriminal Dalam Penanggulangan Tindak Pidana Narkotika Oleh Anak. Malang: UMM Press.
Nair M.H. and Bonelli E. J., 1988. Dasar Kromatografi Gas. (Kosasih, Penjt). Bandung: ITB
Nendrosuwito, D., 1998.Petunjuk Pemeriksaan Narkotika dan Psikotropika dengan KLT dan KG.Jakarta: Depkes R.I
Notoatmojo, S., 2007.Kesehatan Masyarakat Ilmu dan Seni.Jakarta: PT. Rineka Cipta.
Padmohoedojo, P.G., 2003. Pencegahan Penyalahgunaan NARKOBA. Jakarta: Yayasan Research Consultant Indonesia.
Pastika, M.M., dkk. 2008. Pencegahan Penyalahgunaan NARKOBA Sejak Usia Dini. Jakarta.
Putra, N.W., 2011. Deteksi Senyawa Metamfetamina (MA) Pada Rambut Dengan Metode SIM GCMS. Denpasar: UNUD
Puspitasari, C.D., 2005. Narkoba Ancaman Bagi Generasi Muda. Yogyakarta.
Rohman, A., 2009.Kromatografi untuk Analisis Obat.Yogyakarta: Graha Ilmu.