VERIFIKASI METODE ANALISIS SENYAWA KONTAMINAN
3-MCPD ESTER DALAM MINYAK SAWIT DENGAN TEKNIK
GAS CHROMATOGRAPHY
-
MASS SPECTROMETRY
(GC-MS)
CONY ARISYA PUTRI
DEPARTEMEN ILMU DAN TEKNOLOGI PANGAN FAKULTAS TEKNOLOGI PERTANIAN
INSTITUT PERTANIAN BOGOR BOGOR
PERNYATAAN MENGENAI SKRIPSI DAN
SUMBER INFORMASI SERTA PELIMPAHAN HAK CIPTA*
Dengan ini saya menyatakan bahwa skripsi berjudul verifikasi metode analisis senyawa kontaminan 3-MCPD ester dalam minyak sawit dengan teknik
Gas Chromatography-Mass Spectrometry (GC-MS) adalah benar karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir skripsi ini.
Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
Bogor, September 2014
Cony Arisya Putri
ABSTRAK
CONY ARISYA PUTRI. Verifikasi Metode Analisis Senyawa Kontaminan 3-MCPD Ester dalam Minyak Sawit dengan Teknik Gas Chromatography-Mass Spectrometry (GC-MS). Dibimbing oleh HANIFAH NURYANI LIOE dan NANCY DEWI YULIANA.
Senyawa 3-mono-chloropropane-1,2-diol (3-MCPD) ester merupakan senyawa kontaminan yang banyak ditemukan pada minyak sawit yang mengalami pemurnian. Tujuan dilakukan penelitian ini yaitu untuk melakukan verifikasi metode analisis 3-MCPD ester yang telah dilakukan oleh Lanovia (2013) untuk laboratorium pemerintah Badan POM, Jakarta. Kuantifikasi kandungan 3-MCPD ester dilakukan dengan menghitung selisih antara kandungan 3-MCPD total dan 3-MCPD bebas. Analisis dilakukan menggunakan instrumen Gas Chromatography-Mass Spectrometer (GC-MS) dan standar internal 3-MCPD-D5. Senyawa analat 3-MCPD dan 3-MCPD-D5 diderivatisasi oleh phenylboronic acid (PBA) menjadi senyawa yang dapat dideteksi oleh instrumen GC-MS yang masing-masing muncul pada menit ke- 16.476 – 17.065 dan 16.402 – 16.996 dengan presisi waktu retensi kurang dari 2.0 %. Hasil unjuk kerja instrumen menunjukkan instrumen memiliki linearitas yang baik pada rentang konsentrasi 3-MCPD 0.25 – 7.50 µg/mL dengan nilai R2 0.999. Nilai limit deteksi (LOD) dan limit kuantifikasi (LOQ) instrumen diperoleh masing-masing sebesar 0.17 dan 0.59 µg/mL. Hasil verifikasi menunjukkan metode analisis memiliki spesifisitas yang baik serta linieritas metode dengan nilai R2 0.995 pada rentang konsentrasi 3-MCPD 0 – 60 µg/g sampel. Nilai limit deteksi metode yang diperoleh adalah 4.59 µg/g. Hasil uji rekoveri pada konsentrasi spike 40 µg/g sampel diperoleh rata-rata rekoveri sebesar 83.29 ± 7.12 % pada rentang 77.89 – 96.49 % dan presisi yang baik yaitu sebesar 5.38 %. Nilai intralab reprodusibilitas yang diperoleh cukup baik dengan nilai RSD 7.70 %. Berdasarkan hasil tersebut maka metode analisis 3-MCPD ester yang telah terverifikasi dinyatakan valid. Pengujian 14 sampel minyak goreng sawit komersial menunjukkan 100 % sampel positif mengandung 3-MCPD ester yang berada pada rentang konsentrasi 8.15 – 58.14 µg/g minyak.
ABSTRACT
CONY ARISYA PUTRI. Method Verification for Analysis of Food Contaminant 3-MCPD esters in Palm Oils By Gas Chromatotography-Mass Spectrometry (GC-MS). Supervised by HANIFAH NURYANI LIOE and NANCY DEWI YULIANA.
3-monochoropropane-1,2-diol (3-MCPD) esters are food contaminants that found in refined palm oils. The objective of this research was to verify the method of analysis of 3-MCPD esters that have been validated by Lanovia (2013) for Badan POM, Jakarta. Quantification of 3-MCPD esters was obtained from the concentration of 3-MCPD total minus the concentration of free 3-MCPD. The analysis carried out using Gas Chromatotography-Mass Spectrometer (GC-MS) instrument and 3-MCPD-D5 as internal standard. The compound of 3-MCPD and 3-MCPD-D5 were derivatized with phenylboronic acid (PBA) to form products detected by GC-MS at retention time of 16.476 – 17.065 and 16.402 – 16.996 min respectively (precision of retention time is less than 2.0 %). The results of instrument performance showed a good linearity in the concentration range of 3-MCPD 0.25 – 7.5 µg/mL with coefficient of determination (R2) 0.999. Limit of detection (LOD) and limit of quantification (LOQ) in instrument were determined at 0.17 and 0.59 μg/mL respectively. Verification results showed the method has a good specificity and linearity of method at a concentration range of 3-MCPD 0 – 60 µg/g sample with R2 0.995. The value of method detection limit (MDL) was 4.59 μg/g sample. Recovery test was obtained by spiking 3-MCPD at medium concentration 40 μg/g sample. The average of recovery test was determined at 83.29 ± 7.12 % with a range of 77.89 – 96.49 % and the precision was 5.38 %. Within lab reproducibility was determined at 7.70 %. Based on these results, this method was verified and can be used for routine analysis in an accredited laboratory. Testing of 14 commercial palm oil samples indicated that all of samples contained 3-MCPD esters at a range of 8.15 – 58.14 μg/g.
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Teknologi Pertanian
pada
Departemen Ilmu dan Teknologi Pangan
VERIFIKASI METODE ANALISIS SENYAWA KONTAMINAN
3-MCPD ESTER DALAM MINYAK SAWIT DENGAN TEKNIK
GAS CHROMATOGRAPHY
MASS-SPECTROMETRY
(GC-MS)
Cony Arisya Putri
DEPARTEMEN ILMU DAN TEKNOLOGI PANGAN FAKULTAS TEKNOLOGI PERTANIAN
INSTITUT PERTANIAN BOGOR BOGOR
PRAKATA
Puji dan syukur penulis panjatkan kepada Allah, karena atas segala karunia-Nya skripsi ini berhasil diselesaikan. Penelitian yang berjudul verifikasi metode analisis senyawa kontaminan 3-MCPD ester dalam minyak sawit dengan teknik
Gas Chromatography-Mass Spectrofotometry (GC-MS) ini dapat diselesaikan dengan baik berkat bantuan dan bimbingan dari berbagai pihak.
Melihat hal tersebut penulis ingin menyampaikan penghargaan dan ungkapan terima kasih yang sebesar-besarnya kepada:
1. Dr. Ir. Hanifah N. Lioe, M.Si selaku dosen pembimbing akademik pertama penulis yang telah bersedia memberikan saran, waktu, motivasi dan bimbingan serta perhatian dengan penuh kesabaran kepada penulis sejak perkuliahan hingga skripsi ini selesai.
2. Dr. Ir. Nancy Dewi Yuliana selaku dosen pembimbing akademik kedua penulis atas segala perhatian, waktu, dan bantuan yang telah diberikan.
3. Dr. Didah Nur Faridah, S.TP, M.Si selaku dosen penguji yang telah bersedia meluangkan waktu dan memberikan saran kepada penulis.
4. Segenap staff LDITP khususnya kepada mbak Yane Regiana S.TP, M.Si selaku teknisi yang membantu penggunaan instrumen GC-MS selama penelitian berlangsung sehingga penelitian dapat berjalan dengan lancar. 5. Orang tua dan keluarga yang telah mendukung, memotivasi, mendoakan dan
memberikan kasih sayang yang sangat berarti bagi penulis.
6. Teman-teman ITP 47 khususnya kepada Fitri Suryani Ginting, Mutiara Pratiwi, Ni Kadek Willy Rusiana, Fardilla Ayu, Yuwanita Ardillasari, Kartika Sari Touw, Annisa Defriana, M. Wildan Mukholad, Gina Nur Rahmasari atas segala dukungan serta kerjasamanya selama studi dan penelitian ini berlangsung.
Akhir kata, penulis mengucapkan terima kasih pula yang sebesar-besarnya pada seluruh pihak yang tidak dapat disebutkan satu persatu. Semoga karya ilmiah ini bermanfaat.
Bogor, Mei 2014
DAFTAR ISI
DAFTAR TABEL xiii
DAFTAR GAMBAR xiii
DAFTAR LAMPIRAN xiv
PENDAHULUAN 1
Latar Belakang 1
Tujuan Penelitian 2
Manfaat Penelitian 2
METODOLOGI PENELITIAN 3
Bahan dan Alat 3
Metode Penelitian 3
HASIL DAN PEMBAHASAN 10
Uji Unjuk Kerja Instrumen GC-MS untuk Analisis 3-MCPD 12
Verifikasi Metode Analisis 3-MCPD Ester 15
Penetapan 3-MCPD Ester dalam Minyak Goreng Sawit 22
SIMPULAN DAN SARAN 24
Simpulan 24
Saran 24
DAFTAR PUSTAKA 25
LAMPIRAN 27
DAFTAR TABEL
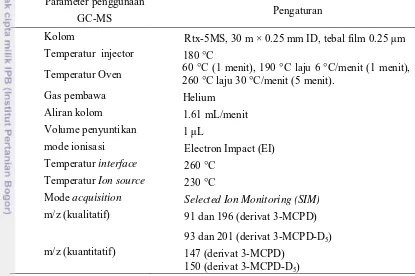
1 Karakteristik ion (m/z) electron impact (EI) mass spectra senyawa derivat 3-MCPD oleh agen penderivat phenylboronic acid (PBA)1) 4 2 Parameter kondisi Gas Chromatography-Mass Spectrometer (GC-MS)
pada analisis 3-MCPD ester yang diderivatisasi dengan PBA 9 3 Waktu retensi larutan standar derivat 3-MCPD hasil injeksi instrumen
GC-MS pada berbagai konsentrasi 3-MCPD, sedangkan konsentrasi standar internal 3-MCPD-D5 yang ditambahkan tetap 2.0 µg 14 4 Hasil analisis unjuk kerja instrumen GC-MS untuk analisis 3-MCPD
dengan penderivatisasi phenylboronic acid (PBA) 15 5 Waktu retensi analisis 3-MCPD total pada campuran standar 3-MCPD
dan 3-MCPD-D5, minyak goreng sawit unspike, dan sampel minyak goreng sawit dengan spike 3-MCPD konsentrasi 40 µg/g sampel dengan
menggunakan GC-MS 16
6 Hasil uji linearitas metode analisis 3-MCPD total pada matriks sampel minyak goreng sawit menggunakan instrumen GC-MS 18 7 Hasil analisis 3-MCPD bebas dalam minyak sawit komersial. Analisis
dilakukam dengan penderivatisasi phenylboronic acid (PBA) dan tanpa proses transesterifikasi dalam persiapan sampel 19 8 Hasil pengukuran 3-MCPD ester dalam sampel minyak goreng sawit
tanpa spiking dengan instrumen GC-MS. Pengukuran dilakukan dua
kali ulangan analisis 20
9 Nilai akurasi dan presisi dari uji rekoveri metode analisis 3-MCPD ester
dalam minyak sawit pada instrumen GC-MS 21
10 Hasil uji intralab reprodusibilitas analisis 3-MCPD ester dalam minyak sawit menggunakan instrumen GC-MS yang dilakukan pada waktu
yang berbeda* 21
11 Kadar 3-MCPD ester dalam sampel minyak goreng sawit komersial dengan metode analisis terverifikasi yang diinjeksikan pada instrumen
GC-MS 22
DAFTAR GAMBAR
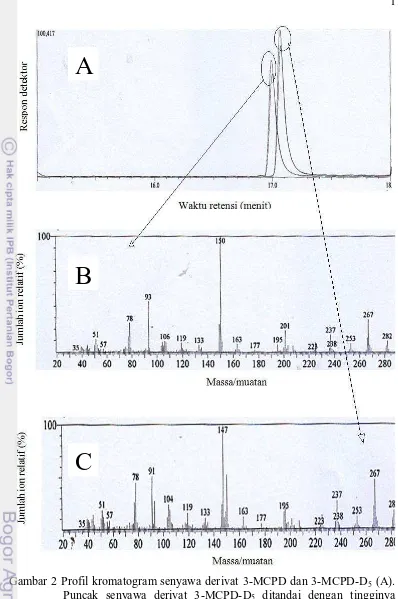
1 Reaksi 3-MCPD dengan agen penderivat phenylboronic acid (PBA) menjadi senyawa 4-chloromethyl-2-phenyl-1,3,2-dioxaborolane, yang dapat dideteksi oleh GC-MS (Hamlet dan Sadd 2009) 4 2 Profil kromatogram senyawa derivat 3-MCPD dan 3-MCPD-D5 (A).
Puncak senyawa derivat 3-MCPD-D5 ditandai dengan tingginya persen ion relatif pada ion m/z 150 (B). Senyawa derivat 3-MCPD ditandai dengan tingginya kelimpahan atau persen ion relatif pada ion m/z 147
(C) 11
3-MCPD-D5 yang ditambahkan tetap yaitu 2.0 µg. Kurva diperoleh dari dua
ulangan uji linearitas 12
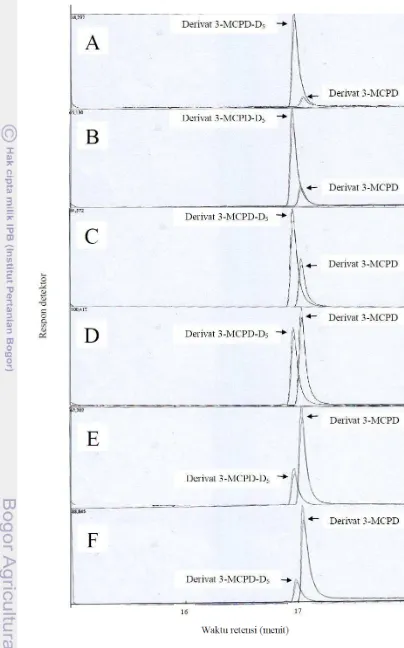
4 Kromatogram standar campuran derivat 3-MCPD dan 3-MCPD-D5 hasil injeksi GC-MS pada pengujian linieritas instrumen dengan konsentrasi 3-MCPD 0.25 μg/mL (A), 0.50 μg/mL (B), 1.00 μg/mL (C),
2.50 μg/mL (D), 5.00 μg/mL (E), dan 7.50 μg/mL (F). Konsentrasi 3 -MCPD-D5 yang ditambahkan tetap yaitu 2.0 µg 13 5 Profil kromatogram senyawa derivat 3-MCPD dan 3-MCPD-D5 dalam
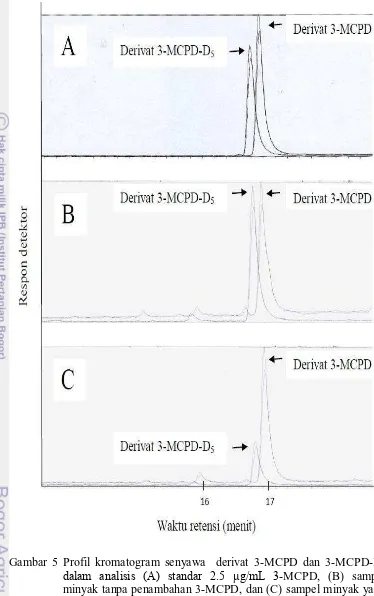
analisis (A) standar 2.5 μg/mL 3-MCPD, (B) sampel minyak tanpa penambahan MCPD, dan (C) sampel minyak yang ditambahkan MCPD 40 µg/g sampel, dengan masing masing larutan mengandung 3-MCPD-D5 2.0 µg. Analisis menggunakan instrumen GC-MS dengan mode selected ion monitoring pada ion m/z 147 dan 150 masing-masing
untuk analisis derivat 3-MCPD dan 3-MCPD-D5 17
6 Kurva linearitas metode untuk analisis 3-MCPD total pada sampel minyak goreng sawit yang ditambahkan larutan standar 3-MCPD dengan rentang 0 – 60 µg/g sampel. Kurva linieritas diperoleh melalui dua kali ulangan analisis. Analisis menggunakan instrumen GC-MS dan
standar internal 3-MCPD-D5 19
DAFTAR LAMPIRAN
1 Metode Weiβhaar untuk analisis 3-MCPD ester dalam minyak dengan GC-MS. Analisis menggunakan sodium metoksi untuk transesterifikasi, PBA sebagai agen penderivat dan 3-MCPD-D5 sebagai standar internal
(Weiβhaar et al. 2008) 27
2 Linieritas kurva yang diperoleh dari dua ulangan analisis, pada pengujian linieritas instrumen untuk analisis 3-MCPD dengan instrumen GC-MS. Analisis dilakukan menggunakan 3-MCPD-D5 sebagai standar internal dan derivatisasi oleh PBA 28 3 Linieritas kurva yang diperoleh dari dua ulangan analisis, pada
pengujian linieritas metode untuk analisis 3-MCPD total dengan instrumen GC-MS. Analisis dilakukan menggunakan 3-MCPD-D5 sebagai standar internal dan derivatisasi oleh PBA 28 4 Hasil uji intralab reprodusibilitas analisis 3-MCPD ester terhadap
sampel yang sama pada bulan yang berbeda. Analisis menggunakan standar internal 3-MCPD-D5 dan instrumen GC-MS 29 5 Hasil pengujian statistika one way ANOVA dan uji lanjut Duncan
PENDAHULUAN
Latar Belakang
Senyawa 3-MCPD ester merupakan suatu kontaminan proses pada makanan, yang artinya senyawa ini bukan berasal dari bahan baku tetapi muncul selama pengolahan. Senyawa MCPD ester ini terdiri dari MCPD monoester dan 3-MCPD diester. Kedua bentuk ester tersebut memiliki potensi terhidrolisis oleh enzim lipase dalam saluran pencernaan menjadi 3-MCPD, dimana bentuk monoester lebih mudah terhidrolisis dibandingkan bentuk diesternya (Seefelder et al. 2008). Senyawa 3-MCPD yang merupakan senyawa hasil hidrolisis 3-MCPD ester memiliki efek terhadap ginjal, sistem saraf pusat dan sistem reproduksi pada hewan percobaan (ILSI 2009). Menurut International Agency for Research on Cancer (IARC) senyawa 3-MCPD kemungkinan dapat menyebabkan kanker bagi manusia (kelompok 2B) (IARC 2012).
Senyawa 3-MCPD dalam makanan, ditemukan dalam bentuk ester maupun bebasnya. Bentuk 3-MCPD ester diketahui lebih tinggi kadarnya jika dibandingkan dalam bentuk bebasnya, yaitu bisa mencapai 5 hingga 396 kali lebih tinggi (Svejkovska et al. 2004). Kontaminan 3-MCPD ester dilaporkan ada pada berbagai produk makanan, salah satunya ditemukan pada minyak sawit yang mengalami pemurnian (Weiβhaar 2011). Kadar 3-MCPD ester dalam minyak goreng sawit yang mengalami pemurnian dapat dikatakan cukup tinggi yaitu berada pada kisaran 4.5 – 13 mg/kg (ILSI 2009).
Senyawa 3-MCPD ester dalam minyak terutama terbentuk selama proses pemurnian, khususnya pada proses deodorisasi suhu tinggi yaitu 240 – 270 oC (Crews 2012). Senyawa ini mulai terbentuk saat suhunya lebih dari 200 oC (MacMahon 2014). Terbentuknya 3-MCPD ester melibatkan pembentukan ion asiloksonium dari triasilgliserol, diasilgliserol, dan monoasilgliserol. Ion asiloksonium kemudian bereaksi dengan ion klorida membentuk 3-MCPD ester (Rahn dan Yaylayan 2011). Senyawa ion klorida sendiri dapat bersumber dari tanah, fertilizer atau dapat pula berasal dari pestisida. Ada beberapa bukti yang menyebutkan ion klorida berasal dari tanah dan atau berasal dari komponen alami organoklorin (MacMahon 2014). Selain itu, adanya proses pemucatan dengan
bleaching earths dapat berpotensi menjadi sumber ion klorin, karena pada proses tersebut seringkali diberi perlakuan asam (HCl) untuk meningkatkan efisiensi. Proses pemucatan sendiri berkontribusi terhadap pembentukan 3-CPD ester yaitu sebesar 20 – 30 % dari seluruh proses pemurnian (Hrncirik 2010).
2
Berdasarkan fakta yang telah dipaparkan tersebut, maka analisis kadar 3-MCPD ester pada minyak sangat penting dilakukan. Hal ini karena terkait dengan keamanan pangan. Telah banyak metode analisis 3-MCPD ester yang dikembangkan. Salah satunya adalah metode yang telah divalidasi oleh Lanovia (2013) untuk laboratorium pemerintahan Badan POM Jakarta. Metode tersebut menggunakan agen penderivat phenylboronic acid (PBA) dan transesterifikasi oleh sodium methoxide (NaOCH3) mengikuti metode Weiβhaar et al. (2008) yang terlampir pada Lampiran 1. Sebelum metode yang telah tervalidasi tersebut digunakan secara rutin oleh suatu laboratorium, perlu dilakukan verifikasi terlebih dahulu. Verifikasi metode analisis diperlukan untuk mengonfirmasi performa/kinerja suatu laboratorium terhadap metode standar yang telah tervalidasi. Verifikasi metode perlu dilakukan agar metode yang telah terverifikasi tersebut dapat digunakan untuk analisis rutin oleh suatu laboratorium. Selain itu, dengan dilakukan verifikasi dapat menghasilkan data analisis yang valid dan dapat dipercaya (Prichard dan Barwich 2007).
Tujuan Penelitian
Tujuan penelitian ini yaitu melakukan verifikasi metode analisis senyawa kontaminan 3-MCPD ester dalam minyak sawit dengan menggunakan instrumen GC-MS, sebelum digunakan untuk keperluan analisis rutin di laboratorium Departemen Ilmu dan Teknologi Pangan, Institut Pertanian Bogor. Tujuan lain adalah menentukan kandungan 3-MCPD ester pada beberapa sampel minyak sawit komersial di pasar kota Bogor. Sebelum dilakukan verifikasi, dilakukan uji unjuk kerja instrumen yang terdiri dari linieritas instrumen, presisi instrumen, limit deteksi atau limit of detection (LOD), dan limit kuantitasi atau limit of quantitation (LOQ). Verifikasi sendiri dilakukan dengan melakukan uji spesifisitas, linieritas metode, limit deteksi metode atau Method Detection Limit
(MDL), rekoveri, ripitabilitas, dan intralab reprodusibilitas.
Manfaat Penelitian
3
METODOLOGI PENELITIAN
Bahan dan Alat
Bahan yang digunakan dalam penelitian ini adalah sampel minyak sawit komersial yang diperoleh di pasar kota Bogor (pasar tradisional, minimarket, dan supermarket). Bahan-bahan kimia yang digunakan untuk analisis meliputi standar internal 3-MCPD-D5 dengan konsentrasi 1 mg/mL dari Cambridge Laboratories Inc. (Amerika Serikat) dan 3-MCPD dengan kemurnian > 98 % yang diperoleh dari Sigma Aldrich Chemie GmbH (Jerman), Methyl tertiary-butyl ether (MTBE) yang diperoleh dari Merck (Jerman), larutan pro analysis etil asetat, sodium metoksi (NaOCH3) dengan merek Sigma Aldrich (USA), asam asetat glasial dengan merek Merk kGaA (Jerman), phenylboronic acid (PBA) dari Sigma Aldrich (Cina), aseton, n-heksana dari Merck kGaA (Jerman), NaCl dari Merck kGaA (Jerman), dan Milli-Q akuades (air bebas ion).
Alat-alat yang digunakan untuk menganalisis meliputi tabung reaksi tutup ulir, gelas piala, labu takar, pipet volumetrik, pipet Mohr, pipet tetes, mikropipet, vortex, vial, botol waste, botol semprot, timbangan, pengaduk kaca, sudip, dan
waterbath. Instrumen analisis yang digunakan adalah Gas Chromatography-Mass Spectrometer (GC-MS) dengan model QP2010 Plus yang dilengkapi autosampler
AOC-20i (Shimadzu Corporation, Jepang) yang berada di Laboratorium Departemen Ilmu dan Teknologi Pangan Institut Pertanian Bogor, serta pengolahan data mass spectra dengan program GCMS Postrun Analysis. Sementara, windows software yang digunakan untuk mengontrol GCMS-QP2010 Plus, autosampler dan semua unit komponen yaitu program GCMS Solution.
Metode Penelitian
Penelitian yang telah dilakukan terbagi menjadi 3 (tiga) tahap, yaitu (1) tahap unjuk kerja instrumen yang terdiri dari linieritas instrumen, presisi instrumen, limit deteksi atau limit of detection (LOD), dan limit kuantitasi atau
limit of quantitation (LOQ) instrumen (2) tahap verifikasi yang meliputi uji spesifisitas, linieritas metode, limit deteksi metode atau Method Detection Limit
(MDL), uji rekoveri, ripitabilitas, dan intralab reprodusibilitas (3) tahap analisis 3-MCPD ester pada sampel minyak sawit komersial menggunakan metode yang telah terverifikasi.
4
ditambahkan diketahui jumlahnya. Selain itu, penambahan standar internal dapat mengoreksi hilangnya sampel dalam tahap persiapan seperti derivatisasi dan ekstraksi yang dapat mengakibatkan berkurangnya sampel. Standar internal 3-MCPD-D5 dipilih karena senyawa ini memiliki sifat kimia yang mirip dengan MCPD namun dapat dibedakan, sehingga dapat terpisah baik dengan senyawa 3-MCPD. Senyawa isotop 3-MCPD-D5 ini juga bersifat stabil dan tidak mempengaruhi sampel.
Tahapan transesterifikasi dilakukan oleh sodium metoksi (NaOCH3) yang merupakan transesterifikasi basa. Setelah proses transesterifikasi, dilanjutkan dengan proses netralisasi dan salting out. Senyawa 3-MCPD bebas kemudian diderivatisasi oleh larutan phenylboronic acid (PBA) menghasilkan senyawa 4-chloromethyl-2-phenyl-1,3,2-dioxaborolane yang dapat dilihat pada Gambar 1 (Hamlet dan Sadd 2009). Derivatisasi perlu dilakukan mengingat senyawa 3-MCPD memiliki tingkat volatilitas yang rendah dan kepolaran tinggi, yang artinya dapat meningkatkan resiko interaksi yang tidak diinginkan dengan komponen yang berada dalam sistem GC atau dengan komponen lainnya. Hal ini dapat menyebabkan menurunnya sensitifitas dan pemisahan puncak yang kurang baik. Bobot molekul 3-MCPD yang rendah akan berpengaruh terhadap deteksi yang dilakukan oleh detektor Mass Spectrometer (MS), sehingga derivatisasi sangat diperlukan (Baer et al. 2010).
Hasil derivatisasi kemudian diinjeksikan pada instrumen Gas Chromatography-Mass Spectrometer (GC-MS). Larutan yang diinjeksi akan mengalami proses fragmentasi, yang nantinya akan dibaca oleh detektor. Tabel 1 menunjukkan karakteristik ion (m/z) fragmentasi senyawa derivat 3-MCPD oleh PBA pada ion m/z 196, 147, dan 91, sementara derivat 3-MCPD-D5 pada ion m/z 201, 150, dan 93 (Svejkovska et al. 2006; Zelinkova et al. 2006; Weiβhaar 2008). Gambar 1 Reaksi 3-MCPD dengan agen penderivat phenylboronic acid (PBA)
menjadi senyawa 4-chloromethyl-2-phenyl-1,3,2-dioxaborolane, yang dapat dideteksi oleh GC-MS (Hamlet dan Sadd 2009)
Tabel 1 Karakteristik ion (m/z) electron impact (EI) mass spectra senyawa derivat 3-MCPD oleh agen penderivat phenylboronic acid (PBA)1)
Bobot
[M]+ [M-CH2Cl]+ [C7H7]+
molekul
Derivat 3-MCPD oleh PBA 196 196 147 91
Derivat 3-MCPD-D5 oleh PBA 201 201 150 93
1)
5 Uji Unjuk Kerja Instrumen GC-MS untuk Analisis 3-MCPD
Tahap pertama penelitian yaitu uji unjuk kerja instrumen untuk analisis 3-MCPD. Tahapan ini berfungsi untuk melihat performa/kinerja instrumen GC-MS yang digunakan. Analisis dilakukan dengan mengukur respon instrumen terhadap analat 3-MCPD dalam larutan standar yang diinjeksikan, kemudian dievaluasi linieritas instrumen, presisi instrumen, limit deteksi atau limit of detection (LOD), dan limit kuantitasi atau limit of quantitation (LOQ). Persiapan larutan sampel pada uji unjuk kerja instrumen dilakukan tanpa menggunakan matriks sampel minyak. Dalam persiapannya, larutan analat 3-MCPD diderivatisasi menggunakan
phenylboronic acid (PBA) dan hasilnya diekstrak dengan heksana, selanjutnya diinjeksikan ke GC-MS.
Persiapan larutan standar
Pembuatan larutan standar dilakukan dengan membuat larutan kerja standar internal 3-MCPD-D5 10 µg/mL dan larutan kerja 3-MCPD 10 µg/mL. Larutan kerja standar internal 3-MCPD-D5 10 µg/mL diperoleh melalui pengenceran 100 kali larutan stok 3-MCPD-D5 konsentrasi 1 mg/mL dengan etil asetat. Jumlah 3-MCPD-D5 yang ditambahkan dalam setiap analisis tetap yaitu sebesar 2 µg, sehingga pada persiapan sampel ditambahkan 200 µL larutan yang diambil dari larutan kerja 10 µg/mL 3-MCPD-D5.
Larutan kerja 3-MCPD 10 µg/mL dihasilkan melalui pengenceran larutan stok MCPD konsentrasi 1 mg/mL dengan etil asetat. Larutan stok 1 mg/mL 3-MCPD dibuat dengan mengencerkan sebanyak 77.30 μL larutan 3-MCPD kemurnian > 98 % yang diperoleh dari Sigma Aldrich Chemie GmbH (Jerman) dengan etil asetat ke dalam labu takar 100 mL. Larutan etil asetat yang digunakan memiliki kualitas pro analysis. Larutan standar 3-MCPD pada konsentrasi tertentu diperoleh dengan mengencerkan larutan kerja 10 µg/mL 3-MCPD dengan etil asetat.
Linieritas instrumen
linieritas instrumen dilakukan dengan menginjeksikan enam vial larutan standar yang berbeda konsentrasi 3-MCPD. Konsentrasi 3-MCPD yang digunakan yaitu 0.25, 0.50, 1.00, 2.50, 5.00, dan 7.50 µg/mL. Pengujian dilakukan sebanyak dua kali ulangan analisis pada masing-masing konsentrasi yaitu dengan pembuatan larutan standar yang berbeda. Pembuatan larutan standar dilakukan dengan mencampurkan larutan 3-MCPD dengan konsentrasi tertentu dan 2 µg standar internal 3-MCPD-D5 yaitu ditambahkan 200 µL larutan yang diambil dari larutan kerja 10 µg/mL 3-MCPD-D5. Campuran kemudian diderivatisasi dengan
250 μL reagen PBA. Larutan selanjutnya dimasukkan pada waterbath yang bersuhu 80 °C selama 20 menit. Setelah didinginkan dalam suhu ruang, larutan diekstrak dengan 2 x 0.5 mL heksana.
6
sumbu x). Melalui kurva yang telah dibuat dapat diketahui persamaan linier dan nilai korelasinya (R2). Nilai koefisien korelasi menggambarkan proporsionalitas respon analat terhadap konsentrasi analat yang diuji (Novelina 2009). Linieritas dianggap baik apabila memiliki R2 lebih dari 0.990 (AOAC 2002).
Presisi instrumen
Presisi instrumen dapat diketahui dengan melihat nilai relative standard deviation (RSD) dari waktu retensi analat pada berbagai konsentrasi larutan standar 3-MCPD yang berbeda. Konsentrasi 3-MCPD yang diuji yaitu berada pada rentang 0.25 – 7.5 µg/mL MCPD dengan jumlah standar internal 3-MCPD-D5 yang ditambahkan tetap yaitu 2 µg. Waktu retensi dari MCPD dan 3-MCPD-D5 yang diperoleh kemudian dirata-ratakan dan dihitung nilai RSD-nya. Keberterimaan RSD dalam uji ini ialah < 2.0 % (JECFA 2006). Nilai RSD dari waktu retensi yang memenuhi syarat menandakan bahwa instrumen mampu memberikan keterulangan deteksi analat yang baik.
Limit of detection (LOD) dan limit of quantitation (LOQ) instrumen
Uji limit deteksi instrumen atau LOD dilakukan dengan membaca rasio S/N (signal-to-noise ratio) yang diperoleh pada uji linieritas instrumen. Nilai limit deteksi atau LOD merupakan konsentrasi terkecil dari analat yang memberikan tinggi puncak 3 kali noise. Nilai limit kuantifikasi atau LOQ merupakan 10 kali
noise.
Verifikasi Metode Analisis 3-MCPD Ester
Parameter verifikasi meliputi uji spesifisitas, linieritas metode, limit deteksi metode atau Method Detection Limit (MDL), uji rekoveri, ripitabilitas, dan intralab reprodusibilitas. Verifikasi metode analisis 3-MCPD ester dilakukan dengan mengkuantifikasi 3-MCPD hasil transesterifikasi oleh sodium metoksi (NaOCH3).
Spesifisitas
Spesifisitas metode adalah kemampuan suatu metode yang dapat secara akurat dan presisi mengukur zat tertentu walaupun terdapat komponen lain yang mungkin ada dalam matriks sampel (Harmita 2004). Pengujian dilakukan dengan menginjeksikan larutan standar 3-MCPD 2.5 µg/mL, sampel minyak tanpa spiking, dan sampel minyak yang di-spike 3-MCPD dengan konsentrasi 40 µg/g sampel. Kromatogram yang diperoleh dari ketiga injeksi larutan berbeda tersebut, diamati bentuk dan waktu retensi puncak derivat 3-MCPD dan 3-MCPD-D5 dari waktu retensi puncak lainnya. Bentuk puncak derivat 3-MCPD dan 3-MCPD-D5 yang runcing, simetris, dan tidak bercabang serta waktu retensi dapat dibedakan dari waktu retensi puncak komponen lain, dalam kromatogram sampel baik yang
7 Linieritas metode dan limit deteksi metode
Linieritas metode dilakukan dengan menyuntikkan larutan sampel yang ditambahkan larutan standar dengan rentang konsentrasi 3-MCPD 0 – 60 µg/g sampel. Pengujian dilakukan sebanyak dua kali ulangan analisis pada masing-masing konsentrasi. Hasil pembacaan GC-MS selanjutnya, diplotkan pada kurva hubungan antara rasio luas area derivat 3-MCPD dengan 3-MCPD-D5 (sebagai sumbu y) dan konsentrasi larutan standar (µg/g sampel) (sebagai sumbu x). Melalui kurva yang telah dibuat dapat diketahui persamaan linier dan nilai korelasinya (R2). Linieritas metode dianggap baik apabila memiliki R2 lebih dari 0.990 (AOAC 2002). Nilai limit deteksi metode atau method detection limit
(MDL) ditentukan dengan melihat hasil detection limit yang terbaca pada alat GC-MS dalam uji linieritas metode tersebut.
Akurasi dan presisi dengan uji rekoveri
Akurasi dan presisi dapat ditentukan dengan melakukan uji rekoveri. Pengujian dilakukan dengan menggunakan sampel yang di-spike oleh analat
3-MCPD pada konsentrasi sedang (40 μg/g sampel). Prosedur pengujian dilakukan
sama dengan prosedur analisis pengujian analisis 3-MCPD ester pada sampel minyak, hanya saja sebelum ditambah larutan MTBE-etil asetat, ditambahkan analat 3-MCPD sebanyak 40 μg/g sampel. Pengujian dilakukan sebanyak tujuh kali ulangan analisis. Hasil analisis kemudian dihitung rata-rata persen rekoverinya. Persen rekoveri dihitung pada masing-masing ulangan dengan menggunakan rumus:
Rekoveri (%) =Konsentrasi sampel yang di �� � −konsentrasi sampel tanpa �� � �
Konsentrasi analat yang di �� � × 100%
Akurasi ditentukan dengan melihat persen rekoverinya. Keberterimaan persen rekoveri untuk penambahan analat sebesar 10 µg/g yaitu 80 – 110% (AOAC 2012). Persen rekoveri yang diperoleh pada masing-masing ulangan dihitung nilai RSD analisisnya. Nilai RSD yang diperoleh dari tujuh ulangan tersebut merupakan nilai ripitabilitas. Presisi ditentukan dengan membandingkan nilai RSD analisis (RSDa) dengan RSD Horwitz (RSDh). Nilai RSD Horwitz (RSDh) dapat dihitung dengan menggunakan rumus:
RSDh (%) = [2 exp(1−0.5 log C)]
Keterangan:
C = Nilai rata-rata konsentrasi analat (dalam bentuk fraksi) Intralab reprodusibilitas
8
baik memiliki nilai RSD analisis (RSDa) yang lebih kecil dibanding RSD Horwitz (RSDh).
Analisis statistika
Analisis statistik deskriptif berupa perhitungan rata-rata, standar deviasi, dan relative standard deviation (RSD) dilakukan dengan menggunakan Microsoft Excel 2011. Pengolahan data pada pengujian intralab reprodusibilitas, menggunakan analisis statistika one way ANOVA dari IBM Statistic SPSS 20. Data hasil analisis kemudian dilakukan uji lanjut Duncan pada tingkat kepercayaan 95 %, untuk mengetahui adanya perbedaan hasil analisis 3-MCPD ester yang dilakukan dalam uji intralab reprodusibilitas.
Prosedur analisis 3-MCPD ester (Weiβhaar (2008) yang dimodifikasi oleh Lanovia (2013))
Sampel minyak goreng sebanyak 100 ± 5 mg dimasukkan ke dalam tabung kaca 10 mL bertutup. Kedalam tabung tersebut kemudian ditambahkan 0.5 mL MTBE - etil asetat (8:2 v/v) dan 2 µg larutan standar 3-MCPD-D5 yaitu diambil 200 µL larutan dari larutan kerja 10 μg/mL 3-MCPD-D5 (dimodifikasi dari 5 μg menurut Lanovia (2013)). Larutan yang telah dicampurkan tersebut, dibiarkan pada suhu ruang selama 2 jam setelah divortex sebelumnya. Kedalam tabung kemudian ditambahkan 1 mL NaOCH3 (0.5 mol/L dalam metanol HPLC grade) dan didiamkan pada suhu kamar selama 10 menit. Setelah itu, larutan ditambahkan 3 mL heksana, 0.1 mL asam asetat glasial dan 3 mL NaCl (200 g/L). Setelah dilakukan homogenisasi, lapisan organik dibuang. Setelah itu, lapisan air ditambahkan 3 mL heksana dan divortex. Kemudian, lapisan organiknya dipisahkan dan dibuang.
Larutan yang diperoleh kemudian diderivatisasi dengan PBA (5 g PBA dalam 20 mL pelarut (aseton:air (19:1)) sebanyak 250 μL dan dipanaskan dalam
waterbath bersuhu 80 °C selama 20 menit. Setelah didinginkan pada suhu kamar, derivat 3-MCPD diekstraksi dengan 2 x 0.5 mL (dimodifikasi dari 1 x 3 mL menurut Lanovia (2013)) heksana. Setelah dilakukan ekstraksi, pisahkan bagian heksana. Hasil ekstraksi kemudian ditambahkan Na2SO4 anhidros. Larutan siap diinjeksikan pada instrumen GC-MS. Sebelum larutan disuntikkan dilakukan persiapan instrumen GC-MS terlebih dahulu. Pengaturan parameter instrumen GC-MS dapat dilihat pada Tabel 2.
Penentuan kadar 3-MCPD ester dalam sampel, diperoleh melalui hasil pengurangan antara kadar 3-MCPD total dengan 3-MCPD bebas pada sampel. Kadar 3-MCPD total ditentukan apabila pada persiapan sampel ditambahkan bahan sodium metoksi (NaOCH3) yang berfungsi untuk proses transesterifikasi. Kadar 3-MCPD bebas ditentukan apabila bahan sodium metoksi (NaOCH3) tidak ditambahkan dalam persiapan sampelnya, sehingga proses transesterifikasi dilewati. Berikut merupakan rumus penentuan kadar 3-MCPD total atau bebas:
�� � � �� =Konsentrasi dari kurva μg
mL
× Volume akhir larutan sampel (mL)
9 Konsentrasi 3-MCPD total atau bebas yang berasal dari kurva (μg/mL) diperoleh dengan memasukkan nilai rasio area senyawa derivat 3-MCPD/3-MCPD-D5 hasil injeksi sampel, pada kurva standar hubungan konsentrasi 3-MCPD dan rasio area (derivat 3-3-MCPD/3-3-MCPD-D5). Proses ekstraksi senyawa 3-MCPD bebas yang merupakan tahap akhir persiapan sampel, dilakukan dengan 2 x 0.5 mL heksana. Hal ini menandakan volume akhir larutan sampel yaitu sebesar 1 mL.
Analisis 3-MCPD ester dalam Minyak Sawit
Analisis 3-MCPD ester dalam sampel minyak dilakukan dengan menggunakan metode analisis yang telah terverifikasi. Nilai 3-MCPD ester pada sampel yang diperoleh, merupakan selisih nilai 3-MCPD total dan 3-MCPD bebas pada sampel. Metode terverifikasi ini merupakan metode Weiβhaar (2008) yang telah termodifikasi oleh Lanovia (2013). Analisis dilakukan sebanyak satu kali ulangan analisis pada masing-masing sampel.
Sampel minyak yang diuji merupakan minyak sawit goreng komersial yang diperoleh di pasar kota Bogor. Pengambilan sampel dilakukan pada tiga tempat yang berbeda yaitu di pasar tradisional, minimarket, dan supermarket. Jumlah sampel yang diuji sebanyak 14 sampel yaitu empat sampel yang diperoleh dari pasar tradisional, lima sampel dari minimarket, dan lima sampel dari supermarket. Hasil analisis kemudian diolah dengan statistik sederhana, berupa nilai rata-rata dan standar deviasi menggunakan Microsoft Excel 2011.
Tabel 2 Parameter kondisi Gas Chromatography-Mass Spectrometer (GC-MS) pada analisis 3-MCPD ester yang diderivatisasi dengan PBA
Parameter penggunaan 260 °C laju 30 °C/menit (5 menit).
Gas pembawa Helium
Mode acquisition Selected Ion Monitoring (SIM)
m/z (kualitatif) 91 dan 196 (derivat 3-MCPD)
93 dan 201 (derivat 3-MCPD-D5)
10
HASIL DAN PEMBAHASAN
Prinsip dasar analisis 3-MCPD ester yaitu mengkuantifikasi 3-MCPD bebas hasil transesterifikasi 3-MCPD ester oleh sodium metoksi (NaOCH3). Senyawa 3-MCPD bebas kemudian diderivatisasi menggunakan phenylboronic acid (PBA). Pemilihan senyawa PBA karena senyawa ini sangat selektif dan dapat bereaksi secara spesifik dengan senyawa diol, membentuk senyawa turunan nonpolar siklik. Hal ini menyebabkan hasil produk derivat dapat diekstrak dengan pelarut nonpolar, serta tidak perlu dilakukan proses pemurnian dengan diatomaceous earth (penggunaan reagen HFBI proses ini diperlukan) (Divinova et al. 2004).
Senyawa derivat 3-MCPD dan 3-MCPD-D5 yang diperoleh kemudian diekstrak oleh heksana. Senyawa heksana dipilih karena harganya yang ekonomis serta umum digunakan sebagai larutan pengekstraksi dalam industri minyak nabati (Lanovia 2013). Larutan hasil ekstraksi kemudian diinjeksikan dan dikuantifikasi oleh instrumen Gas Chromatography-Mass Spectrometer (GC-MS). Hasil deteksi instrumen GC-MS yaitu berupa profil kromatogram dan spektrum. Kromatogram hasil analisis kemudian diamati dan diidentifikasi komponen pada masing-masing puncaknya. Puncak yang teridentifikasi sebagai komponen derivat 3-MCPD dan 3-MCPD-D5, dihitung luas areanya. Kuantifikasi dilakukan dengan merasiokan luas area derivat 3-MCPD dengan luas area derivat standar internal 3-MCPD-D5.
Identifikasi komponen analat derivat 3-MCPD dan 3-MCPD-D5 dilakukan dengan melihat profil spektrum pada masing-masing puncak yang terbentuk pada kromatogram. Hal ini merupakan keunggulan penggunaan instrumen yang menggunakan detektor MS (Mass Spectrometer) yaitu dapat mengidentifikasi identitas komponen pada suatu puncak berdasarkan sifat spesifik spektra massa ion tertentu. Senyawa derivat 3-MCPD ditandai oleh tingginya intensitas ion m/z 147 pada puncaknya, sedangkan derivat 3-MCPD-D5 didominasi oleh besarnya intensitas ion m/z 150 yang dapat dilihat pada Gambar 2. Besarnya kelimpahan kedua ion m/z tersebut menjadikan ion m/z 147 dan 150 dijadikan sebagai ion untuk analisis kuantitatif. Ion m/z 91 dan 196 juga merupakan indikator senyawa derivat 3-MCPD, sementara ion m/z 93 dan 201 mencirikan senyawa 3-MCPD-D5 (Svejkovska et al. 2006; Zelinkova et al. 2006; Weiβhaar 2008).
11
Gambar 2 Profil kromatogram senyawa derivat 3-MCPD dan 3-MCPD-D5 (A). Puncak senyawa derivat 3-MCPD-D5 ditandai dengan tingginya persen ion relatif pada ion m/z 150 (B). Senyawa derivat 3-MCPD ditandai dengan tingginya kelimpahan atau persen ion relatif pada ion m/z 147 (C)
A
B
12
Uji Unjuk Kerja Instrumen GC-MS untuk Analisis 3-MCPD
Uji unjuk kerja instrumen GC-MS untuk analisis 3-MCPD dilakukan untuk mengukur performa/kinerja instrumen dalam mendeteksi komponen analat yang diuji. Instrumen dikatakan baik dan dapat digunakan apabila semua parameter uji unjuk kerja instrumen yang telah disebutkan sebelumnya, dapat memenuhi keberterimaan.
Linieritas instrumen
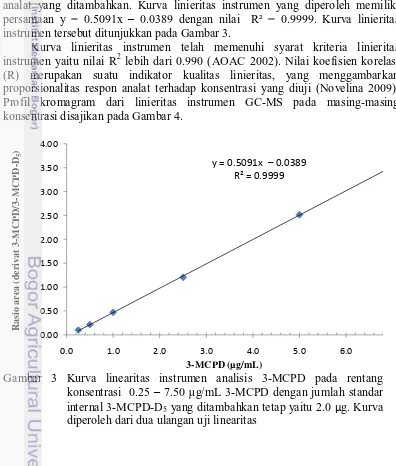
Kurva linieritas instrumen diperoleh dengan memplotkan konsentrasi larutan standar MCPD yang diuji pada sumbu x dan rasio area derivat 3-MCPD/3-MCPD-D5 pada sumbu y. Konsentrasi 3-MCPD yang diujikan yaitu 0.25, 0.50, 1.00, 2.50, 5.00, dan 7.50 µg/mL, yang pada masing-masing konsentrasi uji tersebut dilakukan dua kali pengulangan analisis. Hasil menunjukkan instrumen memberikan respon yang proporsional sesuai konsentrasi analat yang ditambahkan. Kurva linieritas instrumen yang diperoleh memiliki persamaan y = 0.5091x – 0.0389 dengan nilai R² = 0.9999. Kurva linieritas instrumen tersebut ditunjukkan pada Gambar 3.
Kurva linieritas instrumen telah memenuhi syarat kriteria linieritas instrumen yaitu nilai R2 lebih dari 0.990 (AOAC 2002). Nilai koefisien korelasi (R) merupakan suatu indikator kualitas linieritas, yang menggambarkan proporsionalitas respon analat terhadap konsentrasi yang diuji (Novelina 2009). Profil kromagram dari linieritas instrumen GC-MS pada masing-masing konsentrasi disajikan pada Gambar 4.
Gambar 3 Kurva linearitas instrumen analisis 3-MCPD pada rentang konsentrasi 0.25 – 7.50 µg/mL 3-MCPD dengan jumlah standar internal 3-MCPD-D5 yang ditambahkan tetap yaitu 2.0 µg. Kurva diperoleh dari dua ulangan uji linearitas
13
Gambar 4 Kromatogram standar campuran derivat 3-MCPD dan 3-MCPD-D5 hasil injeksi GC-MS pada pengujian linieritas instrumen dengan konsentrasi 3-MCPD 0.25 μg/mL(A), 0.50 μg/mL (B), 1.00 μg/mL
14
Presisi instrumen
Presisi instrumen diukur dengan menghitung RSD waktu retensi dari senyawa derivat 3-MCPD dan 3-MCPD-D5 yang diperoleh dari hasil injeksi larutan standar 3-MCPD pada konsentrasi yang berbeda. Waktu retensi analat dengan konsentrasi 3-MCPD pada rentang 0.25 – 7.50 µg/mL dapat dilihat pada Tabel 3. Hasil menunjukkan RSD waktu retensi senyawa derivat MCPD dan 3-MCPD-D5 yaitu 0.03 %. Persyaratan presisi yang baik yaitu bila nilai RSD hasil pengukuran analat < 2 % (JECFA 2006). Berdasarkan persyaratan tersebut RSD waktu retensi senyawa derivat 3-MCPD maupun 3-MCPD-D5 pada berbagai konsentrasi dapat diterima. Hal ini menandakan instrumen GC-MS dapat memberikan keterulangan deteksi analat yang baik.
Limit of detection (LOD) dan limit of quantitation (LOQ) instrumen
Limit deteksi instrumen atau Limit of Detection (LOD) adalah jumlah analat terkecil yang masih dapat terdeteksi akan tetapi masih memberikan respon yang berbeda dibandingkan dengan blanko. Sementara Limit kuantitasi atau Limit of Quantification (LOQ) merupakan batas terendah konsentrasi yang dapat dilaporkan, nilai di bawah konsentrasi tersebut dapat dilaporkan ‘tidak terdeteksi’ (Harmita 2004). Secara berurut nilai LOD dan LOQ instrumen yang terukur oleh alat GC-MS yaitu 0.17 μg/mL dan 0.59 µg/mL.
Sebagai perbandingan, nilai LOD instrumen yang diperoleh pada penelitian Zhou et al. (2014) untuk mengukur 3-MCPD ester dengan menggunakan instrumen HPLC dengan menggunakan Standar 1,2-dioleoyl-3-chloropropanediol
dan 1-stearoyl-3-chloropropanediol sebagai reference standard yaitu 3.45 µg/mL. Nilai LOD instrumen yang diperoleh dalam penelitian ini, dua puluh kali lebih rendah dibandingkan dengan metode analisis 3-MCPD ester yang dilakukan oleh Tabel 3 Waktu retensi larutan standar derivat 3-MCPD hasil injeksi instrumen
GC-MS pada berbagai konsentrasi 3-MCPD, sedangkan konsentrasi standar internal 3-MCPD-D5 yang ditambahkan tetap 2.0 µg
Konsentrasi 3-MCPD Waktu Retensi (menit)
(µg/mL) Derivat 3-MCPD Derivat 3-MCPD-D5
0.250 17.051 16.984
0.500 17.058 16.988
1.000 17.060 16.988
2.500 17.065 16.993
5.000 17.064 16.996
7.500 17.054 16.982
Rata-rata 17.059 16.989
SD 0.006 0.005
15 Zhou et al. (2014). Hal ini menandakan analisis yang telah dilakukan lebih sensitif dibanding dengan metode analisis yang dilakukan oleh Zhou et al. (2014). Prinsip pengukuran 3-MCPD yang dilakukann pada penelitian Zhou et al. (2014) yaitu pengukuran 3-MCPD ester secara langsung yaitu mengukur 3-MCPD ester yang terdapat dalam sampel tanpa melakukan proses transesterifikasi, dimana proses tersebut berfungsi untuk membebaskan 3-MCPD ester menjadi bentuk bebasnya.
Sementara, penelitian yang dilakukan oleh Hori et al. (2012) untuk mengukur 3-MCPD monoester dan diester dalam minyak dengan instrumen LC/TOF-MS memiliki nilai LOD secara berurut yaitu 0.86 dan 0.22 ng/mL. Prinsip pengukuran dilakukan dengan melakukan ekstraksi analat pada solid-phase extraction. Limit deteksi yang diperoleh pada penelitian Hori et al. (2012) dapat dikatakan lebih sensitif dan lebih selektif. Dikatakan lebih selektif karena metode tersebut dapat mengukur 3-MCPD dalam bentuk monoester dan diesternya, sementara metode yang terverifikasi pada penelitian ini hanya mengukur total ester yang terdapat dalam sampel. Hasil analisis unjuk kerja instrumen pada penelitian ini secara ringkas dapat dilihat pada Tabel 4.
Verifikasi Metode Analisis 3-MCPD Ester
Verifikasi metode analisis dilakukan untuk mengonfirmasi performa/kinerja suatu laboratorium terhadap metode standar yang telah tervalidasi. Metode yang telah diverifikasi merupakan hasil validasi metode Weiβhaar yang dimodifikasi untuk analisis 3-MCPD ester yang dilakukan oleh Lanovia (2013). Verifikasi metode perlu dilakukan agar metode analisis 3-MCPD ester yang telah Tabel 4 Hasil analisis unjuk kerja instrumen GC-MS untuk analisis 3-MCPD
dengan penderivatisasi phenylboronic acid (PBA)
Unjuk Kerja Instrumen GC-MS
Hasil
Ketentuan Ulangan 1 Ulangan 2
Linearitas (y = ax – b)
slope (a) 0.5306 0.4872
intercept (b) 0.0614 0.0176
coefficient of determination (R2) 0.9997 0.9999 R2>0.990* Presisi Instrumen
RSD waktu retensi derivat 3-MCPD 0.03% <2.0 %** RSD waktu retensi derivat 3-MCPD-D5 0.03%
LODinstrumen (µg/mL) 0.17
LOQinstrumen (µg/mL) 0.59
*AOAC (2002)
16
terverifikasi dapat digunakan untuk analisis rutin oleh suatu laboratorium. Selain itu, data yang dihasilkan dari metode terverifikasi dapat dikatakan valid dan dapat dipercaya (Prichard dan Barwich 2007).
Spesifisitas
Spesifisitas suatu metode adalah kemampuan metode analisis untuk dapat mengukur konsentrasi analat dengan adanya komponen-komponen lain yang mungkin ada dalam sampel. Spesifisitas metode dapat ditentukan dengan mengamati profil kromatogram pada hasil injeksi larutan standar 3-MCPD, sampel unspike, dan sampel yang telah di-spike 3-MCPD. Melalui profil kromatogram ketiganya, diamati keterpisahan analat dengan komponen pengganggu. Keterpisahan yang baik dapat dilihat dari puncak analat yang terpisah dan dapat dikuantifikasi areanya secara individu.
Kromatogram hasil injeksi larutan standar 3-MCPD dengan konsentrasi 2.5
µg/mL, sampel tanpa penambahan 3-MCPD, dan sampel yang telah ditambahkan 3-MCPD sebanyak 40 µg/g sampel dapat dilihat pada Gambar 5. Respon hasil deteksi pada sampel minyak unspike dan sampel minyak yang di-spike (Gambar 5B dan 5C) memiliki waktu retensi derivat 3-MCPD dan 3-MCPD-D5 yang sesuai dengan waktu retensi standar derivat 3-MCPD dan 3-MCPD-D5 (Gambar 5A). Hal ini menandakan bahwa peak yang diperoleh pada sampel unspike dan sampel yang di-spike tersebut dapat diidentifikasi sebagai senyawa derivat 3-MCPD dan 3-MCPD-D5. Secara umum, senyawa derivat 3-MCPD-D5 muncul terlebih dahulu dibanding senyawa derivat MCPD. Waktu retensi derivat MCPD dan 3-MCPD-D5 pada ketiga sampel uji disajikan pada Tabel 5.
Respon yang diperoleh sesuai dengan yang diharapkan, yaitu peak derivat 3-MCPD yang terbentuk pada Gambar 5C lebih tinggi sesuai dengan percobaan, yaitu terdapat penambahan standar 3-MCPD dalam sampel minyak sebanyak 40
µg/g sampel. Berbeda dengan puncak derivat 3-MCPD pada gambar 5B yang relatif lebih kecil karena tidak ada penambahan 3-MCPD pada sampel. Secara umum, ketiga kromatogram pada Gambar 5 menunjukkan bahwa senyawa derivat 3-MCPD dan 3-MCPD-D5 dapat membentuk puncak yang dapat dikuantifikasi areanya secara individu, meskipun analat dan standar internalnya memiliki waktu retensi yang berdekatan. Selain itu, bila diamati pada profil kromatogram yang diperoleh, peak analat yang dihasilkan tidak terganggu oleh peak senyawa lain yang mungkin ada dalam sampel. Puncak yang dihasikan juga membentuk peak
yang runcing, simetris, dan tidak bercabang. Hal ini menunjukkan bahwa metode analisis 3-MCPD ester yang diverifikasi memiliki spesifisitas yang baik.
Tabel 5 Waktu retensi analisis 3-MCPD total pada campuran standar 3-MCPD dan 3-MCPD-D5, minyak goreng sawit unspike, dan sampel minyak
17
Gambar 5 Profil kromatogram senyawa derivat 3-MCPD dan 3-MCPD-D5
18
Linieritas metode dan limit deteksi metode
Pengujian linieritas metode analisis 3-MCPD total dilakukan dengan menginjeksikan sampel yang di-spike dengan larutan standar 3-MCPD. Larutan standar 3-MCPD yang ditambahkan yaitu berkisar pada rentang 0 – 60 µg/g sampel. Pengujian dilakukan dengan dua kali ulangan analisis. Hasil pengujian menghasilkan kurva linieritas dengan persamaan y = 0.0475x + 1.1546 dan nilai R2 = 0.9950. Persamaan kurva tersebut diperoleh dengan memplotkan rataan rasio derivat 3-MCPD/3-MCPD-D5 dari dua kali ulangan analisis dengan konsentrasi 3-MCPD. Hasil uji linearitas metode secara rinci pada masing-masing ulangan disajikan pada Tabel 6.
Kurva linieritas metode analisis 3-MCPD total dapat dilihat pada Gambar 6. Kurva linieritas metode yang diperoleh memiliki nilai korelasi R2 yang sudah memenuhi kriteria persyaratan, yaitu nilai R2 > 0.990 (AOAC 2012). Dengan demikian, metode yang digunakan memiliki linearitas yang baik, yaitu instrumen mampu menghasilkan kurva linieritas yang proporsional, semakin tinggi konsentrasi larutan standar 3-MCPD yang ditambahkan, maka akan semakin besar rasio area derivat 3-MCPD/3-MCPD-D5 yang diperoleh.
Melalui percobaan yang telah dilakukan limit deteksi metode atau method detection limit (MDL) yang terbaca oleh GC-MS yaitu 4.59 μg/g. Nilai MDL yang diperoleh ini lebih tinggi dibandingkan dengan nilai LOQ instrumen yaitu 0.59 µg/mL. Hal ini menunjukkan metode analisis memiliki tingkat sensitifitas yang lebih rendah saat mendeteksi senyawa derivat 3-MCPD dalam matriks sampel hingga pada konsentrasi 4.59 μg/g sampel.
Tabel 6 Hasil uji linearitas metode analisis 3-MCPD total pada matriks sampel minyak goreng sawit menggunakan instrumen GC-MS
Linearitas Metode
Hasil
Persyaratan Ulangan 1 Ulangan 2
Linearitas (y=ax+b)
Rentang (µg/g) 0 – 60 0 – 60
slope (a) 0.0536 0.0416
intercept (b) 1.1314 1.1391
coefficient of determination (R2) 0.9953 0.9933 R2>0.990*
19
Akurasi dan presisi dari uji rekoveri
Akurasi menunjukkan derajat kedekatan hasil analisis dengan kadar analat sebenarnya, yang biasanya dinyatakan sebagai persen perolehan kembali atau rekoveri (Harmita 2004). Hasil rekoveri menyatakan rasio antara hasil yang diperoleh dengan hasil yang sebenarnya. Uji rekoveri dilakukan dengan menambahkan larutan 3-MCPD konsentrasi sedang (40 µg/g sampel) pada matriks sampel minyak goreng sawit. Agar diketahui besarnya 3-MCPD ester yang diperoleh kembali maka perlu dilakukan penentuan kadar 3-MCPD bebas pada matriks sampel minyak uji. Nilai 3-MCPD bebas pada sampel uji minyak sawit dapat dilihat pada Tabel 7, yaitu rata-rata memiliki kadar 0.80 µg/g minyak.
Gambar 6 Kurva linearitas metode untuk analisis 3-MCPD total pada sampel minyak goreng sawit yang ditambahkan larutan standar 3-MCPD dengan rentang 0 – 60 µg/g sampel. Kurva linieritas diperoleh melalui dua kali ulangan analisis. Analisis menggunakan instrumen GC-MS dan standar internal 3-MCPD-D5
20
Hasil pengukuran kadar 3-MCPD ester sampel unspike dapat dilihat pada Tabel 8. Melalui Tabel 8 dapat diketahui bahwa sampel minyak yang digunakan untuk pengujian rekoveri, memiliki rata-rata kadar 3-MCPD ester sebesar 19.58
μg/g. Nilai rekoveri diperoleh dengan menggunakan persamaan dari kurva linieritas instrumen yaitu dengan persamaan y = 0.5091x – 0.0389 dengan nilai R2 sebesar 0.999.
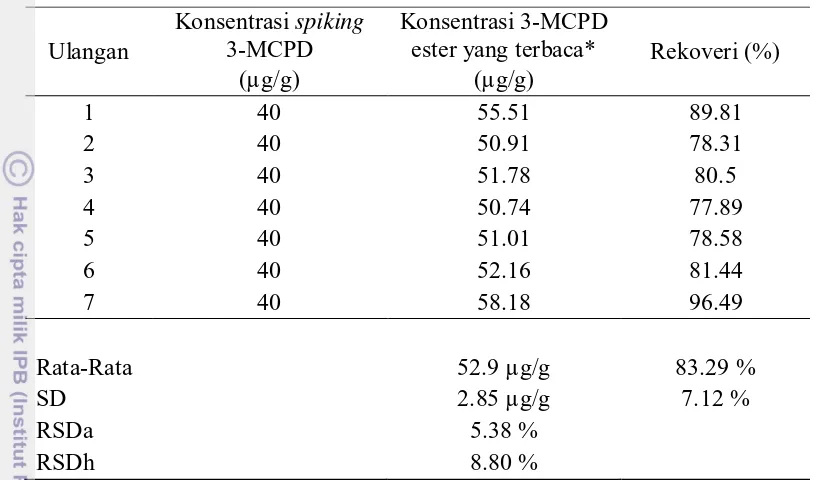
Nilai perolehan kembali (rekoveri) memiliki rata-rata sebesar 83.29 ± 7.12 % dengan rentang rekoveri 77.89 – 96.49 % yang dapat dilihat pada Tabel 9. Nilai rekoveri pada konsentrasi spiking 40 µg/g ini telah memenuhi persyaratan AOAC (2012) yaitu keberterimaan rata-rata rekoveri sebesar 80 – 115 %. Hal ini menunjukkan metode analisis yang digunakan memiliki akurasi yang baik. Persen rekoveri pada penelitian yang dilakukan Razak et al. (2012) dengan konsentrasi
spiking 6 µg/g sebanyak enam kali ulangan yaitu sebesar 107.9 ± 0.115 %. Penelitian tersebut dilakukan dengan menginjeksikan sampel yang telah di-spiking
pada instrumen Gas Chromatography-Mass Selective Detector (GC-MSD). Sementara, pada penelitian yang dilakukan oleh Lanovia (2013) diperoleh rekoveri sebesar 101.60 ± 6.26 %.
Presisi merupakan nilai yang menunjukkan derajat kedekatan di antara serangkaian pengukuran yang diperoleh dari pengujian beberapa sampel homogen dengan metode analisis yang sama. Ukuran ketelitian atau presisi dapat dilihat melalui parameter RSD hasil pengulangan analisis (Harmita 2004). Bila nilai RSD analisis (RSDa) kurang dari RSD Horwitz (RSDh) maka dapat dikatakan analisis yang dilakukan memiliki presisi yang baik atau telah memenuhi persyaratan. Presisi analisis 3-MCPD ester dalam minyak sawit dengan penderivatisasi PBA yang diinjeksikan pada instrumen GC-MS dapat dilihat pada Tabel 9. Hasil menunjukkan nilai RSD analisis (RSDa) yang diperoleh yaitu 5.38 %, dimana nilainya kurang dari RSDh (8.80 %). Hal ini menunjukkan analisis yang dilakukan memiliki presisi yang baik yaitu variabilitas pengukuran yang dilakukan masih dapat diterima. Nilai presisi yang diperoleh dalam penelitian Razak et al. (2012) dan Lanovia (2013) secara berurut yaitu 0.11 dan 6.16 %.
Tabel 8 Hasil pengukuran 3-MCPD ester dalam sampel minyak goreng sawit tanpa spiking dengan instrumen GC-MS. Pengukuran dilakukan dua kali ulangan analisis
21
Intralab reprodusibilitas
Pengujian within lab reproducibility (WLR) atau dikenal dengan intralab reprodusibilitas dilakukan dengan mengkuantifikasi standar deviasi relatif hasil analisis sampel yang sama pada tiga bulan yang berbeda. Hasil pengujian dapat dilihat pada Tabel 9. Berdasarkan tabel tersebut dapat diketahui bahwa RSD analisis (RSDa) yang dihasilkan adalah 7.70 %. Nilai tersebut telah memenuhi batas keberterimaan yaitu nilainya lebih rendah dari RSDh (10.57 %). Selain itu, pengujian menunjukkan hasil analisis 3-MCPD ester yang dilakukan pada bulan yang berbeda terhadap sampel yang sama, memiliki nilai yang tidak berbeda nyata pada taraf uji 5 % (uji Duncan). Hasil ini menunjukkan metode analisis yang diverifikasi memiliki nilai keterulangan yang baik pada jangka waktu tertentu.
Tabel 9 Nilai akurasi dan presisi dari uji rekoveri metode analisis 3-MCPD ester dalam minyak sawit pada instrumen GC-MS
Ulangan
Konsentrasi spiking
3-MCPD
Konsentrasi 3-MCPD
ester yang terbaca* Rekoveri (%)
(µg/g) (µg/g)
* Konsentrasi 3-MCPD ester diperoleh dari pengurangan hasil analisis 3-MCPD total dan 3-MCPD bebas.
Tabel 10 Hasil uji intralab reprodusibilitas analisis 3-MCPD ester dalam minyak sawit menggunakan instrumen GC-MS yang dilakukan pada waktu yang berbeda*
* Melalui uji statistika diperoleh bahwa hasil uji pada bulan yang berbeda pada sampel yang sama memiliki nilai 3-MCPD ester yang tidak berbeda nyata pada taraf uji 5% (uji lanjut Duncan)
22
Penetapan 3-MCPD Ester dalam Minyak Goreng Sawit
Senyawa 3-MCPD ester banyak ditemukan dalam berbagai pangan. Bentuk esternya ditemukan jauh lebih besar dibandingkan dalam bentuk bebasnya. Menurut CFS (2012) kadar 3-MCPD ester ditemukan dalam kadar yang tinggi pada kelompok makanan biskuit, lemak dan minyak, snack serta pastry dengan rata-rata kadarnya berturut-turut yaitu 440, 390, 270 dan 270 µg/kg. Melihat besarnya penggunaan (intake) minyak, khususnya minyak sawit dibandingkan biskuit, snack serta pastry oleh masyarakat Indonesia, maka diperlukan
monitoring jumlah paparan 3-MCPD ester ke dalam tubuh yang berasal dari minyak goreng sawit. Oleh karena itu, diperlukan adanya data kadar 3-MCPD ester dalam minyak sawit yang beredar dimasyarakat. Pengujian kadar 3-MCPD ester dilakukan dengan menggunakan metode yang telah terverifikasi agar diperoleh data yang dapat dipercaya serta valid.
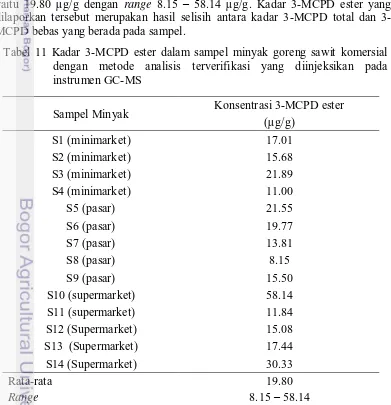
Pengujian 3-MCPD ester dilakukan terhadap 14 (empat belas) sampel minyak sawit komersial yang diperoleh dari tiga tempat yang berbeda yaitu pasar tradisional, minimarket dan supermarket yang diperoleh dari kota Bogor. Hasil penetapan kadar 3-MCPD ester hasil analisis tercantum pada Tabel 10. Hasil tersebut menandakan bahwa semua sampel yang diukur positif 100 % mengandung 3-MCPD ester. Rata-rata 3-MCPD ester pada minyak yang terukur yaitu 19.80 µg/g dengan range 8.15 – 58.14 µg/g. Kadar 3-MCPD ester yang dilaporkan tersebut merupakan hasil selisih antara kadar MCPD total dan 3-MCPD bebas yang berada pada sampel.
Tabel 11 Kadar 3-MCPD ester dalam sampel minyak goreng sawit komersial dengan metode analisis terverifikasi yang diinjeksikan pada instrumen GC-MS
23
Sebagai perbandingan, dalam penelitian Lanovia (2013) terhadap enam sampel minyak goreng sawit, diperoleh kadar 3-MCPD ester dengan rata-rata kadar 13.24 µg/g pada range 12.23 – 14.47 µg/g. Berbeda dengan hasil yang diperoleh Razak et al. (2012), kadar 3-MCPD ester dalam minyak goreng sawit di Malaysia diperoleh nilai yang lebih rendah, yaitu kadarnya memiliki rentang konsentrasi 0.25 – 5.77 µg/g. Perbedaan kadar 3-MCPD ester yang cukup jauh antara nilai yang diperoleh dalam penelitian ini dengan hasil yang diperoleh oleh Razak et al.(2012), kemungkinan disebabkan oleh beberapa hal.
Perbedaan metode analisis yang digunakan bisa saja menjadi penyebab utamanya. Penelitian ini dilakukan dengan menggunakan transesterifikasi basa dan menggunakan NaCl sebagai pereaksinya (proses salting out). Hal ini menyebabkan saat preparasi bisa saja terjadi pembentukan 3-MCPD dari glisidol dengan adanya keberadaan ion klorin dari NaCl. Hal ini menyebabkan hasil yang diperoleh bisa jadi lebih besar dari nilai yang sebenarnya (Hrncirik et al. 2011). Menurut Ermacora dan Hrncirik (2012) kadar 3-MCPD ester akan menjadi
overestimated bila dalam preparasi ditambahkan ion klorin lebih dari 1.7 mmol/kg minyak. Sementara dalam penelitian yang dilakukan dilakukan oleh Razak et al.
(2012) proses transesterifikasi dilakukan dengan menambahkan H2SO4 (transesterifikasi asam) dan proses salting out oleh (NH4)2SO4, sehingga pembentukan 3-MCPD dari glisidol dapat diminimalisir. Selain itu, bisa jadi sampel minyak yang digunakan memang memiliki kadar 3-MCPD ester yang berbeda. Perbedaan dapat disebabkan proses pengolahan yang berbeda, sumber bahan baku berasal dari daerah yang berbeda, serta lama penyimpanan. Kadar air yang tinggi dan enzim lipase yang ada dalam minyak sawit dapat membentuk asilgliserol dan diasilgliserol, yang merupakan salah satu prekursor pembentukan 3-MCPD ester (Karsulinova et al. 2007).
Kadar 3-MCPD ester minyak goreng sawit dari 14 sampel yang telah dianalisis memiliki kadar tertinggi 58.14 µg/g. Nilai tersebut dapat dianggap sebagai resiko tertinggi saat menggunakan minyak goreng sawit, maka orang dengan berat badan 50 kg hanya dapat mengkonsumsi kira-kira 6 gram minyak goreng sawit perharinya. Hal ini, dengan asumsi 3-MCPD ester yang masuk ke dalam tubuh hanya berasal dari minyak goreng sawit, yang seluruhnya dapat dihidrolisis dalam saluran pencernaan menjadi senyawa 3-MCPD, dan nilai
tolerable daily intake (TDI) maksimum untuk 3-MCPD yaitu 7 µg 3-MCPD/kg berat badan/hari. Faktanya 3-MCPD ester yang masuk ke dalam tubuh tidak hanya berasal dari minyak goreng saja, banyak produk pangan lainnya yang juga mengandung 3-MCPD ester serta tidak semua 3-MCPD ester dapat dihidrolisis sempurna menjadi 3-MCPD. Persen potensi sesungguhnya seberapa besar yang dapat dihidrolisis oleh enzim dalam pencernaan masih menjadi tanda tanya besar, sehingga perlu kajian yang lebih mendalam lagi.
Industri minyak dapat saja menurunkan senyawa 3-MCPD ester dalam produknya yaitu dengan menggunakan tandan sawit kualitas baik (rendah kadar DAG), dengan proses pengolahan dilakukan segera. Beberapa cara seperti pencucian minyak untuk menghilangkan komponen polar; penambahan senyawa kompetitor ion klorin seperti diacetin; optimasi temperatur pemanasan dan
24
SIMPULAN DAN SARAN
Simpulan
Senyawa hasil derivatisasi 3-MCPD dan 3-MCPD-D5 masing-masing muncul pada menit ke- 16.476 – 17.065 dan 16.402 – 16.996 dengan presisi yang baik, yaitu RSD waktu retensi kurang dari 2 %. Unjuk kerja instrumen menunjukkan, linieritas instrumen pada rentang konsentrasi 3-MCPD 0.25 – 7.50 µg/mL memiliki nilai koefisien korelasi R2 yang baik, yaitu sebesar 0.999. Limit deteksi dan limit kuantifikasi (LOD dan LOQ) instrumen masing-masing adalah 0.17 dan 0.59 µg/mL. Hasil verifikasi menunjukkan metode memiliki spesifisitas yang baik. Linieritas metode pada rentang konsentrasi 3-MCPD 0 – 60 µg/g memiliki nilai R2 (0.995) yang memenuhi ketentuan. Nilai limit deteksi metode yang diperoleh yaitu 4.59 µg/g. Uji rekoveri pada konsentrasi sedang (40 µg/g sampel) memiliki rata-rata rekoveri sebesar 83.29 ± 7.12 % dengan rentang 77.89
– 96.49 % dan presisi yaitu sebesar 5.38 %. Metode analisis memiliki nilai intralab reprodusibilitas yang baik yaitu sebesar 7.70 %.
Berdasarkan hasil tersebut maka metode analisis 3-MCPD ester modifikasi Weiβhaar telah terverifikasi dan dinyatakan valid. Hal ini menunjukkan metode tersebut dapat digunakan untuk analisis rutin di laboratorium Departemen Ilmu dan Teknologi Pangan, IPB. Pengujian terhadap 14 sampel minyak sawit komersial dengan metode terverifikasi menunjukkan 100 % sampel positif mengandung 3-MCPD ester yang berada pada rentang konsentrasi 8.15 – 58.14 µg/g minyak.
Saran
Penelitian lebih lanjut untuk meminimalkan pembentukan 3-MCPD ester dalam produk minyak goreng sawit. Penelitian dapat dilakukan dengan menambahkan senyawa diacetin yang merupakan kompetitor ion klorin.
Monitoring dilakukan dengan menggunakan metode yang telah terverifikasi untuk mengetahui besarnya konsentrasi diacetin yang dapat memberikan hasil optimal untuk menekan kadar 3-MCPD ester pada produk.
25
DAFTAR PUSTAKA
[AOAC] Association of Official Analytical Chemists. 2002. Peer Verified Methods Program, Manual on Policies and Procedures. Washington D.C.: The Association Analytical Chemist Inc.
[AOAC] Association of Official Analytical Chemists. 2012. AOAC Official Methods of Analysis, Appendix K: Guidelines for Single Laboratory Validation of Chemical Methods for Dietary Supplements and Botanical.
[BPOM] Badan Pengawas Obat dan Makanan. 2009. Peraturan Kepala Badan Pengawas Obat dan Makanan Republik Indonesia Nomor HK.00.06.1.52.4011 tentang Penetapan Batas Maksimum Cemaran Mikroba dan Kimia dalam Makanan. Jakarta (ID): BPOM.
[CFS] Centre for Food Safety Food and Environmental Hygiene Department The Government of the Hong Kong Special Administrative Region. Risk Assesment Studies Report No. 50 Fatty Acid Esters of 3-monochloropropane-1,2-diol (3-MCPD) in Food [internet]. [diunduh 17 juli 2014]. Tersedia pada: http://www.cfs.gov.hk/english/programme/programme_rafs/files/programme_r afs_fc_01_33_3MCPD_Report.pdf
[IARC] International Agency for Research on Cancer. 2012. Some Chemicals Present in Industrial and Consumer Products, Food and Drinking-water. Lyon, France. 349-374.
[JECFA] Joint Expert Committee on Food Additives. 2006. Combined Compendium of Food Additive Specification Volume 4. Anlaytical Methods, Test Procedures and Laboratory Solutions Used by and Referenced in the Food Additive Specifications. Rome: Food and Agriculture Organization of the United Nations.
Baer l, Calle BDL, Taylor P. 2010. Review 3-MCPD in food other than soy sauce or hydrolysed vegeTabel protein (HVP). Anal Bional Chem. 396:443-456.doi: 10.1007/s00216-009-3177-y
Crews C. 2012. Fatty acid esters of chloropropanols and glycidol in food-analysis and exposure [internet]. [diunduh 23 Agustus 2013]. Tersedia pada: http://www.foodprotection.org/downloads/meetings/program-activities/
programs/colin-crews-fatty-acid-esters-of-chloropopanols-and-glycidol-in-foods-analysis-and-exposure.pdf.
Divinova V, Svejkovska B, Dolezal M, Velisek J. 2004. Determinationof free and bound 3-chloropropane-1,2-diol by gas chromatography with mass spectrometric detection using deuterated 3-chloropropane-1,2-diol as internal standard. Czech J Food Sci. 22(5):182–189
Ermacora A, Hrncirik K. 2012. Evaluation of an improved indirect method for the analysis of 3-MCPD esters based on acid transesterification. J Am Oil Chem Soc. 89: 211–217.
Hamlet CG, Sadd PA. 2009. Chloropropanols and Chloroesters. Stadler RH dan Lineback DR, editor. John Wiley &Sons, Inc: UK.
26
Hori K, Koriyama N, Omori H, Kuriyama M, Arishima T, Tsumura K. 2012. Simultaneous determination of 3-MCPD fatty acid esters and glycidol fatty acid esters in edible oils using liquid chromatography time-of-flight mass spectrometry. Elsevier Food Science and Technology. 48: 204-208.
Hrncirik K, Zelinkova Z, Ermacora A. 2011. Critical factors of indirect determination of 3-chloropropane-1,2-diol esters. Eur J Lipid Sci Technol. 113: 361–367
Hrncirik K. 2010. 3-MCPD Esters Formation in Vegetable Oil Refining. OVID - Association of the oilseed crushing and oil refining Industry in Germany, Berlin [internet]. [diunduh 17 juli 2014]. Tersedia pada: http://www.ovid-verband.de/fileadmin/user_upload/ovidverband.de/downloads/Unilever_Hrncir ik.pdf
ILSI. 2009. Workshop 3-MCPD Esters in Food Products. 5–6 Februari, Brussels,
Belgium [internet]. [diunduh 20 juli 2013]
Lanovia T. 2013. Validasi metode Weiβhaar yang dimodifikasi untuk analisis 3 -monochloropropane-1,2-diol (3-MCPD) dan esternya pada minyak goreng Sawit [Tesis]. Bogor (ID): Institut Pertanian Bogor.
MacMahon Shaun. 2014. Book review processing contaminants in edible oils: MCPD and glycidyl Ester [internet]. [diunduh 17 Juli 2014]. Tersedia pada: www.oilfats.org.nz/wp-content/uploads/2014/06/FNZJun14OilsBook
Review.pdf.
Novelina, Yus M, Sutanto, Alia F. 2009. Validasi metode analisis penetapan kadar senyawa siklamat dalam minuman ringan. Jakarta: Prodising PPI Standardisasi 2009.
Prichard E, Barwick V. 2007. Quality Assurance in Analytical Chemistry. John Wiley - Sons: Teddington, UK.
Rahn AKK, Yaylayan VA. 2011. What do we know about the molecular mechanism of 3-MCPD ester formation?. Eur. J. Lipid Sci. Technol. 113: 323– 329.
Razak RAA, Kuntom A, Siew WL, Ibrahim NA, Ramli MR, Hussein R, Nesaretnam K. 2012. Detection and Monitoring of 3-monochloropropane-1,2-diol (3-MCPD) esters in cooking oils. Elsevier Food Control. 25: 355-360 Rietjens IMCM, Scholz G, Berg I, Schilter B, Slob W. 2012. Refined hazard
27 Svejkovska B, Novotny, O Divinova V, Reblova Z. et al. 2004. Esters of 3
chloropropane-1,2-diol in foodstuffs. Czech J. Food Sci. 22: 190–196.
Weiβhaar R. 2008. Determination of Total 3-Chloropropane-1,2-diol (3-MCPD) in Edible Oils by Cleavage of MCPD esters with Sodium Methoxide. Eur. J. Lipid Sci. Technol. 110:183-186.doi:10.1002/ejlt.200700197
Weiβhaar R. 2010. Fatty acid esters of 3-MCPD: overview of occurrence and exposure estimates. Eur. J. Lipid Sci. Technol. 113: 304–308.doi: 10.1002/ejlt.201000312
Zelinkova Z, Svejkovska B, Velisek J, Dolezal M. 2006. Fatty acid esters of 3-chloropropane-1,2-diol in edible oils. Food Addit. Contam. 23: 1290–1298. Zhou H, Jin Q, Wang X, Xu X. 2014. Direct measurement of
3-chloropropane-1,2-diol fatty acid esters in oils and fats by HPLC method. Elsevier Food Control. 36: 111-118.
LAMPIRAN
Lampiran 1 Metode Weiβhaar untuk analisis 3-MCPD ester dalam minyak dengan GC-MS. Analisis menggunakan sodium metoksi untuk transesterifikasi, PBA sebagai agen penderivat dan 3-MCPD-D5 sebagai standar internal (Weiβhaar et al. 2008)
Sejumlah 100 mg sampel, dimasukkan dalam tabung bertutup dan ditambahkan 500 µL MTBE-etil asetat (8:2 vol/vol), 250 µL larutan standar internal 3-MCPD-D5 (20 µg/mL dalam MTBE) dan 1 mL larutan NaOCH3 (0.5 mol/L dalam methanol anhidrat). Tabung ditutup rapat dan didiamkan selama 10 menit. Tambahkan 3 mL isoheksan, 100 µL asam asetat glasial, dan 3 mL larutan NaCl (200 g/L). Bagian atas dipipet dan dibuang. Bagian air diekstrak dengan 3 mL isoheksan, bagian atas kembali dibuang.
Bagian air ditambahkan 250 µL reagen penderivat (5 grm PBA dilarutkan dalam 19 mL aseton dan 1 mL air). Tabung ditutup dan dipanaskan pada suhu 80 o
C selama 20 menit. Campuran didinginkan pada suhu kamar dan diekstrak dengan 3 mL heksana. Lapisan heksana dipisahkan dan dianalisis dengan GC-MS. Berikut merupakan parameter penggunaan GC-MS :
Temperatur Oven 80 °C (1 menit), 300 °C laju 10 °C/menit (37 menit) Gas pembawa Helium
Mode acquisition Selected Ion Monitoring (SIM)
m/z (kualitatif) 147 dan 150 m/z (kuantitatif) 196 dan 201