SKRIPSI
OPTIMASI PEMEKATAN KAROTENOID PADA METIL ESTER KASAR (CRUDE METHYL ESTER) MINYAK SAWIT DENGAN MENGGUNAKAN
METODE KROMATOGRAFI KOLOM ADSORPSI
Oleh
EKO WIDAYANTO F24102049
2007
DEPARTEMEN ILMU DAN TEKNOLOGI PANGAN FAKULTAS TEKNOLOGI PERTANIAN
Eko Widayanto. F24102049. Optimasi Pemekatan Karotenoid pada Metil Ester Kasar (Crude Methyl Ester) Minyak Sawit dengan Menggunakan Metode Kromatografi Kolom Adsorpsi. Di bawah bimbingan Tien R. Muchtadi dan Nur Wulandari.
RINGKASAN
Penelitian ini bertujuan untuk mempelajari teknik pemekatan karotenoid pada metil ester kasar (crude methyl ester) minyak sawit dengan menggunakan metode kromatografi kolom adsorpsi serta mencari kondisi optimum prosesnya agar didapat pekatan karotenoid dengan tingkat pemekatan dan perolehan kembali karotenoid yang tinggi. Penelitian diharapkan dapat menghasilkan teknologi yang meningkatkan nilai ekonomi minyak sawit melalui penjumputan mikronutrien karotenoid, terutama dalam kerangka proses produksi biodiesel.
Penelitian produksi konsentrat karotenoid dari crude methyl ester (CME) terdiri dari dua tahap utama yaitu: (1) Optimasi proses produksi CME dengan kandungan karotenoid tinggi; dan (2) Optimasi pemekatan karotenoid pada CME dengan metode kromatografi kolom adsorpsi. Tahap optimasi proses produksi CME terdiri dari tahap optimasi proses dengan perlakuan kecepatan pengadukan serta optimasi proses dengan kombinasi tiga perlakuan (konsentrasi katalis, waktu reaksi dan suhu reaksi). Sedangkan tahap optimasi pemekatan karotenoid terdiri dari tahap optimasi proses dengan perlakuan nisbah adsorben abu sekam padi dan silika gel serta tahap optimasi proses dengan perlakuan jumlah sampel yang dilewatkan dalam kolom kromatografi.
Alkoholisis minyak sawit untuk menghasilkan metil ester dilakukan secara kimiawi menggunakan katalis NaOH dan pereaksi metanol. Parameter analisisnya adalah kadar ester dan kandungan karotenoid dari produk ester. Proses optimasi alkoholisis yang telah dilakukan menghasilkan kondisi optimum pada penambahan NaOH 1% dengan perbandingan molar minyak sawit:metanol = 1:10, suhu 50oC dan kecepatan pengadukan 250 rpm selama 1 jam. Rendemen metil ester yang diperoleh sebesar 80.67% dengan kadar ester 97.06% serta dapat mempertahankan karotenoid sebesar 85.74%.
OPTIMASI PEMEKATAN KAROTENOID PADA METIL ESTER KASAR (CRUDE METHYL ESTER) MINYAK SAWIT DENGAN MENGGUNAKAN
METODE KROMATOGRAFI KOLOM ADSORPSI
SKRIPSI
Sebagai salah satu syarat untuk memperoleh gelar SARJANA TEKNOLOGI PERTANIAN pada Departemen Ilmu dan Teknologi Pangan
Fakultas Teknologi Pertanian Institut Pertanian Bogor
Oleh Eko Widayanto
F24102049
2007
DEPARTEMEN ILMU DAN TEKNOLOGI PANGAN FAKULTAS TEKNOLOGI PERTANIAN
INSTITUT PERTANIAN BOGOR FAKULTAS TEKNOLOGI PERTANIAN
OPTIMASI PEMEKATAN KAROTENOID PADA METIL ESTER KASAR (CRUDE METHYL ESTER) MINYAK SAWIT DENGAN MENGGUNAKAN
METODE KROMATOGRAFI KOLOM ADSORPSI
SKRIPSI
Sebagai salah satu syarat untuk memperoleh gelar SARJANA TEKNOLOGI PERTANIAN pada Departemen Ilmu dan Teknologi Pangan
Fakultas Teknologi Pertanian Institut Pertanian Bogor
Oleh Eko Widayanto
F24102049
Dilahirkan pada tanggal 12 Oktober 1983 di Boyolali, Jawa Tengah
Tanggal lulus:
Menyetujui, Bogor, Februari 2007
Prof. Dr. Ir. Tien R. Muchtadi, MS Nur Wulandari, STP, MSi Dosen Pembimbing I Dosen Pembimbing II
Mengetahui,
Dr. Ir. Dahrul Syah, MSc Ketua Departemen ITP
RIWAYAT HIDUP
Penulis bernama lengkap Eko Widayanto yang dilahirkan di Boyolali pada tanggal 12 Oktober 1983. Penulis merupakan anak pertama dari dua bersaudara dari pasangan Bapak Sudomo dan Ibu Mursiti. Penulis lulus dari SD Negeri Bhayangkari di Bogor pada tahun 1996, lulus SLTP Negeri 2 Bogor tahun 1999 dan lulus SMU Negeri 1 Bogor tahun 2002. Setelah lulus SMU, penulis melanjutkan pendidikan di Departemen Ilmu dan Teknologi Pangan, Fakultas Teknologi Pertanian, Institut Pertanian Bogor melalui jalur Undangan Seleksi Masuk IPB (USMI).
Semasa kuliah penulis aktif dalam organisasi dan berbagai kegiatan kemahasiswaan. Tahun 2002-2003 penulis menjadi staf Pengembangan Sumberdaya Manusia Badan Eksekutif Mahasiswa Tingkat Persiapan Bersama IPB. Kepanitiaan yang pernah diikuti penulis di antaranya yaitu Pelatihan Kesehatan Mahasiswa tahun 2002 dan Seminar Nasional Pangan Halal tahun 2004. Pada tahun 2005 penulis mengikuti Kuliah Kerja Nyata (KKN) di Kecamatan Panyingkiran Kabupaten Majalengka, Jawa Barat. Penulis juga pernah menjadi Asisten Praktikum Mata Kuliah Analisis Pangan pada tahun 2006.
KATA PENGANTAR
Segala puji bagi Allah SWT yang telah memberikan karunia-Nya sehingga penulis dapat menyelesaikan kuliah dan penyusunan skripsi ini dengan baik. Skripsi ini disusun setelah penulis melakukan kegiatan penelitian di laboratorium. Isi skripsi merupakan data-data yang berasal dari penelitian, studi pustaka, serta analisis hasil penelitian.
Selama penelitian dan penyusunan skripsi, penulis mendapatkan bantuan dari berbagai pihak. Oleh karena itu, dalam kesempatan ini penulis mengucapkan terima kasih kepada:
1. Bapak dan Ibu tercinta, serta adikku Ari atas segala perhatian, pengertian, pengorbanan, dorongan dan doa yang selalu dipanjatkan selama masa studi yang cukup panjang ini. Semoga penulis dapat menjalankan amanah yang telah diberikan dengan sebaik-baiknya.
2. Ibu Prof. Dr. Ir. Tien R. Muchtadi, MS selaku dosen pembimbing akademis yang banyak memberikan arahan, bimbingan dan motivasi yang sangat berarti bagi penulis baik dalam penelitian maupun di luar penelitian.
3. Ibu Nur Wulandari, STP, MSi selaku dosen pembimbing akademis yang senantiasa memberikan arahan, bimbingan dan perhatian yang luar biasa selama penelitian.
4. Bapak Dr. Ir. Nugraha Edhi Suyatma, DEA selaku dosen penguji yang telah memberikan saran dan nasihat yang begitu berarti dalam upaya penyempurnaan skripsi ini.
5. Bapak Ade dan Teh Yuli yang banyak membantu dalam pelaksanaan penelitian, yang tidak hanya memberikan arahan tapi juga sekaligus menjadi teman terdekat.
6. Ibu Tri Haryati dan Bapak Soenar yang banyak memberikan masukan serta pengajaran di bidang minyak sawit.
7. Abah (Pak Karna), Ibu Sri, Mbak Ari, Bu Sari, Pak Taufik, dan Mas Edi sebagai laboran yang sekaligus menjadi sahabat penulis.
9. Teman-teman TPG 39, Yudhan, Yoga, Didin, Dadik, Fahrul, Irwan, Heru, Yayah, Fafa, Tina, Adjeng, Tmin, Hanif, Qyas, Samsul, Manto, Ulik, Inal, Evrin, Evie, Izal, Putra, Dora, Eva, Astri, Kiki, Molid, Tono, Reza, Iqbal, Christ, Dikres, teman-teman lain di golongan B, teman satu kelompok B4, Zae, Marlyn, Qco, dan Anita. Terima kasih atas semua bantuan, kerjasama dan kebersamaan teman-teman semua selama kuliah di IPB.
10.Teman-teman sebimbingan (Nya2, Endang, Deddy, Sendhi, Zen, Kaninta, Martin, Yoga). Terima kasih atas kebersamaan dan dukungannya selama kuliah dan penelitian.
11.Teman satu kost, Zaenal dan Daris yang juga memberikan warna di hari-hari penulis menyelesaikan penelitian.
12.Para dosen, laboran dan staf di Departemen ITP dan SEAFAST Center yang telah banyak membantu penulis dalam menyelesaikan kuliah dan penelitian. 13.Pihak-pihak yang tidak dapat disebutkan satu per satu. Terima kasih yang
sebesar-besarnya atas segala bantuan yang diberikan.
Skripsi ini tidak luput dari kekurangan dan kesalahan. Meskipun demikian penulis berharap semoga skripsi ini dapat berguna bagi semua pihak yang memerlukannya.
Bogor, Februari 2007
DAFTAR ISI
Halaman
KATA PENGANTAR ... iv
DAFTAR ISI ... vi
DAFTAR TABEL ... viii
DAFTAR GAMBAR ... ix
DAFTAR LAMPIRAN ... xi
I. PENDAHULUAN ... 1
A. LATAR BELAKANG ... 1
B. TUJUAN PENELITIAN ... 4
II. TINJAUAN PUSTAKA ... 5
A. MINYAK SAWIT ... 5
B. KAROTENOID ... 7
C. METIL ESTER ... 11
D. METODE EKSTRAKSI DAN PEMEKATAN KAROTENOID ... 16
1. Metode Penyabunan ... 16
2. Metode Ekstraksi Pelarut ... 17
3. Metode Adsorpsi ... 18
4. Metode Distilasi Molekuler ... 19
5. Metode Ekstraksi dengan Fluida Superkritik ... 20
E. KROMATOGRAFI KOLOM ADSORPI ... 21
F. ABU SEKAM PADI ... 23
III. METODOLOGI PENELITIAN ... 25
A. BAHAN DAN ALAT ... 25
B. METODE PENELITIAN ... 25
1. Persiapan dan Karakterisasi Bahan Baku ... 26
2. Optimasi Produksi Metil Ester Kasar (Crude Methyl Ester) ... 27
a. Penentuan kecepatan pengadukan optimum ... 28
b. Penentuan konsentrasi katalis, suhu dan waktu reaksi optimum . 28
3. Optimasi Pemekatan Karotenoid ... 29
b. Penentuan jumlah sampel yang dilewatkan dalam kolom
optimum ... 31
C. METODE PENGAMATAN ... 31
1. Analisis Kandungan Karotenoid ... 31
2. Penetapan Komposisi Asam Lemak ... 33
3. Kadar Air ... 34
4. Rendemen ... 35
5. Bilangan Asam ... 35
6. Bilangan Penyabunan ... 35
7. Total Gliserol ... 36
8. Kadar Ester ... 37
9. Perolehan Metil Ester ... 38
D. RANCANGAN PERCOBAAN ... 38
IV. HASIL DAN PEMBAHASAN ... 43
A. PERSIAPAN DAN KARAKTERISASI BAHAN BAKU ... 43
B. OPTIMASI PROSES PRODUKSI CME ... 44
1. Penentuan Kecepatan Pengadukan Optimum ... 46
2. Penentuan Konsentrasi Katalis, Suhu dan Waktu Reaksi Optimum ... 50
C. OPTIMASI PEMEKATAN KAROTENOID ... 67
1. Penentuan Nisbah Abu Sekam Padi/Silika Gel Optimum ... 68
2. Penentuan Jumlah CME yang Dilewatkan dalam Kolom Optimum 77
D. PRODUKSI DAN KARAKTERISASI PRODUK KONSENTRAT ... 83
V. KESIMPULAN DAN SARAN ... 87
A. KESIMPULAN ... 87
B. SARAN ... 88
DAFTAR PUSTAKA ... 89
SKRIPSI
OPTIMASI PEMEKATAN KAROTENOID PADA METIL ESTER KASAR (CRUDE METHYL ESTER) MINYAK SAWIT DENGAN MENGGUNAKAN
METODE KROMATOGRAFI KOLOM ADSORPSI
Oleh
EKO WIDAYANTO F24102049
2007
DEPARTEMEN ILMU DAN TEKNOLOGI PANGAN FAKULTAS TEKNOLOGI PERTANIAN
Eko Widayanto. F24102049. Optimasi Pemekatan Karotenoid pada Metil Ester Kasar (Crude Methyl Ester) Minyak Sawit dengan Menggunakan Metode Kromatografi Kolom Adsorpsi. Di bawah bimbingan Tien R. Muchtadi dan Nur Wulandari.
RINGKASAN
Penelitian ini bertujuan untuk mempelajari teknik pemekatan karotenoid pada metil ester kasar (crude methyl ester) minyak sawit dengan menggunakan metode kromatografi kolom adsorpsi serta mencari kondisi optimum prosesnya agar didapat pekatan karotenoid dengan tingkat pemekatan dan perolehan kembali karotenoid yang tinggi. Penelitian diharapkan dapat menghasilkan teknologi yang meningkatkan nilai ekonomi minyak sawit melalui penjumputan mikronutrien karotenoid, terutama dalam kerangka proses produksi biodiesel.
Penelitian produksi konsentrat karotenoid dari crude methyl ester (CME) terdiri dari dua tahap utama yaitu: (1) Optimasi proses produksi CME dengan kandungan karotenoid tinggi; dan (2) Optimasi pemekatan karotenoid pada CME dengan metode kromatografi kolom adsorpsi. Tahap optimasi proses produksi CME terdiri dari tahap optimasi proses dengan perlakuan kecepatan pengadukan serta optimasi proses dengan kombinasi tiga perlakuan (konsentrasi katalis, waktu reaksi dan suhu reaksi). Sedangkan tahap optimasi pemekatan karotenoid terdiri dari tahap optimasi proses dengan perlakuan nisbah adsorben abu sekam padi dan silika gel serta tahap optimasi proses dengan perlakuan jumlah sampel yang dilewatkan dalam kolom kromatografi.
Alkoholisis minyak sawit untuk menghasilkan metil ester dilakukan secara kimiawi menggunakan katalis NaOH dan pereaksi metanol. Parameter analisisnya adalah kadar ester dan kandungan karotenoid dari produk ester. Proses optimasi alkoholisis yang telah dilakukan menghasilkan kondisi optimum pada penambahan NaOH 1% dengan perbandingan molar minyak sawit:metanol = 1:10, suhu 50oC dan kecepatan pengadukan 250 rpm selama 1 jam. Rendemen metil ester yang diperoleh sebesar 80.67% dengan kadar ester 97.06% serta dapat mempertahankan karotenoid sebesar 85.74%.
OPTIMASI PEMEKATAN KAROTENOID PADA METIL ESTER KASAR (CRUDE METHYL ESTER) MINYAK SAWIT DENGAN MENGGUNAKAN
METODE KROMATOGRAFI KOLOM ADSORPSI
SKRIPSI
Sebagai salah satu syarat untuk memperoleh gelar SARJANA TEKNOLOGI PERTANIAN pada Departemen Ilmu dan Teknologi Pangan
Fakultas Teknologi Pertanian Institut Pertanian Bogor
Oleh Eko Widayanto
F24102049
2007
DEPARTEMEN ILMU DAN TEKNOLOGI PANGAN FAKULTAS TEKNOLOGI PERTANIAN
INSTITUT PERTANIAN BOGOR FAKULTAS TEKNOLOGI PERTANIAN
OPTIMASI PEMEKATAN KAROTENOID PADA METIL ESTER KASAR (CRUDE METHYL ESTER) MINYAK SAWIT DENGAN MENGGUNAKAN
METODE KROMATOGRAFI KOLOM ADSORPSI
SKRIPSI
Sebagai salah satu syarat untuk memperoleh gelar SARJANA TEKNOLOGI PERTANIAN pada Departemen Ilmu dan Teknologi Pangan
Fakultas Teknologi Pertanian Institut Pertanian Bogor
Oleh Eko Widayanto
F24102049
Dilahirkan pada tanggal 12 Oktober 1983 di Boyolali, Jawa Tengah
Tanggal lulus:
Menyetujui, Bogor, Februari 2007
Prof. Dr. Ir. Tien R. Muchtadi, MS Nur Wulandari, STP, MSi Dosen Pembimbing I Dosen Pembimbing II
Mengetahui,
Dr. Ir. Dahrul Syah, MSc Ketua Departemen ITP
RIWAYAT HIDUP
Penulis bernama lengkap Eko Widayanto yang dilahirkan di Boyolali pada tanggal 12 Oktober 1983. Penulis merupakan anak pertama dari dua bersaudara dari pasangan Bapak Sudomo dan Ibu Mursiti. Penulis lulus dari SD Negeri Bhayangkari di Bogor pada tahun 1996, lulus SLTP Negeri 2 Bogor tahun 1999 dan lulus SMU Negeri 1 Bogor tahun 2002. Setelah lulus SMU, penulis melanjutkan pendidikan di Departemen Ilmu dan Teknologi Pangan, Fakultas Teknologi Pertanian, Institut Pertanian Bogor melalui jalur Undangan Seleksi Masuk IPB (USMI).
Semasa kuliah penulis aktif dalam organisasi dan berbagai kegiatan kemahasiswaan. Tahun 2002-2003 penulis menjadi staf Pengembangan Sumberdaya Manusia Badan Eksekutif Mahasiswa Tingkat Persiapan Bersama IPB. Kepanitiaan yang pernah diikuti penulis di antaranya yaitu Pelatihan Kesehatan Mahasiswa tahun 2002 dan Seminar Nasional Pangan Halal tahun 2004. Pada tahun 2005 penulis mengikuti Kuliah Kerja Nyata (KKN) di Kecamatan Panyingkiran Kabupaten Majalengka, Jawa Barat. Penulis juga pernah menjadi Asisten Praktikum Mata Kuliah Analisis Pangan pada tahun 2006.
KATA PENGANTAR
Segala puji bagi Allah SWT yang telah memberikan karunia-Nya sehingga penulis dapat menyelesaikan kuliah dan penyusunan skripsi ini dengan baik. Skripsi ini disusun setelah penulis melakukan kegiatan penelitian di laboratorium. Isi skripsi merupakan data-data yang berasal dari penelitian, studi pustaka, serta analisis hasil penelitian.
Selama penelitian dan penyusunan skripsi, penulis mendapatkan bantuan dari berbagai pihak. Oleh karena itu, dalam kesempatan ini penulis mengucapkan terima kasih kepada:
1. Bapak dan Ibu tercinta, serta adikku Ari atas segala perhatian, pengertian, pengorbanan, dorongan dan doa yang selalu dipanjatkan selama masa studi yang cukup panjang ini. Semoga penulis dapat menjalankan amanah yang telah diberikan dengan sebaik-baiknya.
2. Ibu Prof. Dr. Ir. Tien R. Muchtadi, MS selaku dosen pembimbing akademis yang banyak memberikan arahan, bimbingan dan motivasi yang sangat berarti bagi penulis baik dalam penelitian maupun di luar penelitian.
3. Ibu Nur Wulandari, STP, MSi selaku dosen pembimbing akademis yang senantiasa memberikan arahan, bimbingan dan perhatian yang luar biasa selama penelitian.
4. Bapak Dr. Ir. Nugraha Edhi Suyatma, DEA selaku dosen penguji yang telah memberikan saran dan nasihat yang begitu berarti dalam upaya penyempurnaan skripsi ini.
5. Bapak Ade dan Teh Yuli yang banyak membantu dalam pelaksanaan penelitian, yang tidak hanya memberikan arahan tapi juga sekaligus menjadi teman terdekat.
6. Ibu Tri Haryati dan Bapak Soenar yang banyak memberikan masukan serta pengajaran di bidang minyak sawit.
7. Abah (Pak Karna), Ibu Sri, Mbak Ari, Bu Sari, Pak Taufik, dan Mas Edi sebagai laboran yang sekaligus menjadi sahabat penulis.
9. Teman-teman TPG 39, Yudhan, Yoga, Didin, Dadik, Fahrul, Irwan, Heru, Yayah, Fafa, Tina, Adjeng, Tmin, Hanif, Qyas, Samsul, Manto, Ulik, Inal, Evrin, Evie, Izal, Putra, Dora, Eva, Astri, Kiki, Molid, Tono, Reza, Iqbal, Christ, Dikres, teman-teman lain di golongan B, teman satu kelompok B4, Zae, Marlyn, Qco, dan Anita. Terima kasih atas semua bantuan, kerjasama dan kebersamaan teman-teman semua selama kuliah di IPB.
10.Teman-teman sebimbingan (Nya2, Endang, Deddy, Sendhi, Zen, Kaninta, Martin, Yoga). Terima kasih atas kebersamaan dan dukungannya selama kuliah dan penelitian.
11.Teman satu kost, Zaenal dan Daris yang juga memberikan warna di hari-hari penulis menyelesaikan penelitian.
12.Para dosen, laboran dan staf di Departemen ITP dan SEAFAST Center yang telah banyak membantu penulis dalam menyelesaikan kuliah dan penelitian. 13.Pihak-pihak yang tidak dapat disebutkan satu per satu. Terima kasih yang
sebesar-besarnya atas segala bantuan yang diberikan.
Skripsi ini tidak luput dari kekurangan dan kesalahan. Meskipun demikian penulis berharap semoga skripsi ini dapat berguna bagi semua pihak yang memerlukannya.
Bogor, Februari 2007
DAFTAR ISI
Halaman
KATA PENGANTAR ... iv
DAFTAR ISI ... vi
DAFTAR TABEL ... viii
DAFTAR GAMBAR ... ix
DAFTAR LAMPIRAN ... xi
I. PENDAHULUAN ... 1
A. LATAR BELAKANG ... 1
B. TUJUAN PENELITIAN ... 4
II. TINJAUAN PUSTAKA ... 5
A. MINYAK SAWIT ... 5
B. KAROTENOID ... 7
C. METIL ESTER ... 11
D. METODE EKSTRAKSI DAN PEMEKATAN KAROTENOID ... 16
1. Metode Penyabunan ... 16
2. Metode Ekstraksi Pelarut ... 17
3. Metode Adsorpsi ... 18
4. Metode Distilasi Molekuler ... 19
5. Metode Ekstraksi dengan Fluida Superkritik ... 20
E. KROMATOGRAFI KOLOM ADSORPI ... 21
F. ABU SEKAM PADI ... 23
III. METODOLOGI PENELITIAN ... 25
A. BAHAN DAN ALAT ... 25
B. METODE PENELITIAN ... 25
1. Persiapan dan Karakterisasi Bahan Baku ... 26
2. Optimasi Produksi Metil Ester Kasar (Crude Methyl Ester) ... 27
a. Penentuan kecepatan pengadukan optimum ... 28
b. Penentuan konsentrasi katalis, suhu dan waktu reaksi optimum . 28
3. Optimasi Pemekatan Karotenoid ... 29
b. Penentuan jumlah sampel yang dilewatkan dalam kolom
optimum ... 31
C. METODE PENGAMATAN ... 31
1. Analisis Kandungan Karotenoid ... 31
2. Penetapan Komposisi Asam Lemak ... 33
3. Kadar Air ... 34
4. Rendemen ... 35
5. Bilangan Asam ... 35
6. Bilangan Penyabunan ... 35
7. Total Gliserol ... 36
8. Kadar Ester ... 37
9. Perolehan Metil Ester ... 38
D. RANCANGAN PERCOBAAN ... 38
IV. HASIL DAN PEMBAHASAN ... 43
A. PERSIAPAN DAN KARAKTERISASI BAHAN BAKU ... 43
B. OPTIMASI PROSES PRODUKSI CME ... 44
1. Penentuan Kecepatan Pengadukan Optimum ... 46
2. Penentuan Konsentrasi Katalis, Suhu dan Waktu Reaksi Optimum ... 50
C. OPTIMASI PEMEKATAN KAROTENOID ... 67
1. Penentuan Nisbah Abu Sekam Padi/Silika Gel Optimum ... 68
2. Penentuan Jumlah CME yang Dilewatkan dalam Kolom Optimum 77
D. PRODUKSI DAN KARAKTERISASI PRODUK KONSENTRAT ... 83
V. KESIMPULAN DAN SARAN ... 87
A. KESIMPULAN ... 87
B. SARAN ... 88
DAFTAR PUSTAKA ... 89
DAFTAR TABEL
Halaman Tabel 1. Komposisi asam lemak minyak sawit kasar ... 6 Tabel 2. Jenis-jenis karotenoid yang mempunyai nilai gizi ... 10 Tabel 3. Residu pelarut organik yang diijinkan dalam makanan ... 17 Tabel 4. Penerapan perlakuan pada tahap optimasi produksi CME dengan
perlakuan kecepatan pengadukan ... 39 Tabel 5. Penerapan perlakuan pada tahap optimasi produksi konsentrat
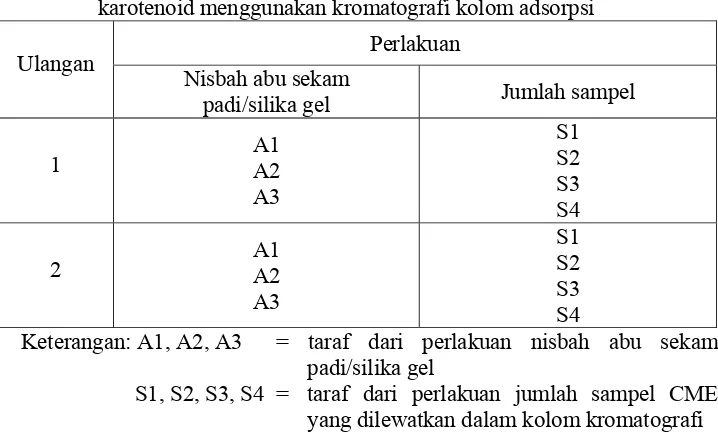
karotenoid menggunakan kromatografi kolom adsorpsi ... 39 Tabel 6. Penerapan perlakuan pada tahap optimasi produksi CME dengan
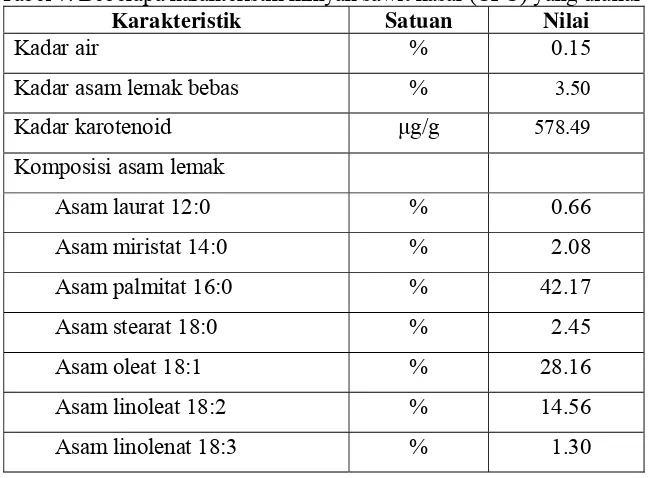
perlakuan kombinasi tiga faktor ... 40 Tabel 7. Beberapa karakteristik minyak sawit kasar (CPO) yang diukur ... 43 Tabel 8. Karakteristik abu sekam padi yang digunakan ... 44 Tabel 9. Konsentrasi karotenoid dan perolehan karotenoid CME pada
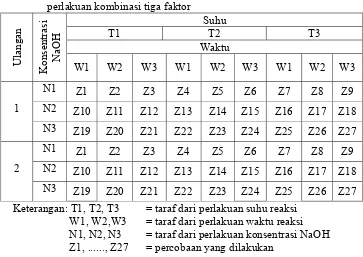
kombinasi perlakuan konsentrasi NaOH, suhu dan waktu reaksi .. 54 Tabel 10. Rendemen CME, kadar ester, dan perolehan metil ester pada
kombinasi perlakuan konsentrasi NaOH, suhu dan waktu reaksi ... 58 Tabel 11. Rekapitulasi hasil optimasi perlakuan konsentrasi NaOH, suhu dan
waktu reaksi dalam produksi CME berkarotenoid tinggi ... 66 Tabel 12. Rekapitulasi hasil optimasi perlakuan nisbah abu sekam padi/silika
gel pada produksi konsentrat karotenoid ... 77 Tabel 13. Rekapitulasi hasil optimasi perlakuan jumlah CME yang dilewatkan
dalam kolom pada produksi konsentrat karotenoid ... 83 Tabel 14. Karakteristik bahan baku CPO, produk CME dan konsentrat
DAFTAR GAMBAR
Halaman Gambar 1. Struktur molekul isoprena ... 8 Gambar 2. Struktur dasar karotenoid ... 8 Gambar 3. Struktur β-karoten dan retinol ... 10 Gambar 4. Persamaan reaksi metanolisis ... 13 Gambar 5. Diagram alir proses produksi metil ester dari minyak sawit pada
industri biodiesel ... 15 Gambar 6. Diagram alir penelitian optimasi pemekatan karotenoid dari
minyak sawit kasar skala laboratorium ... 26 Gambar 7. Diagram alir persiapan bahan abu sekam padi ... 27 Gambar 8. Proses produksi metil ester ... 27 Gambar 9. Diagram alir pemekatan karotenoid pada CME menggunakan
kolom kromatografi ... 29 Gambar 10. Skema analisis konsentrasi karotenoid ... 32 Gambar 11. Pemisahan fase ester dengan fase air menggunakan sentrifus .... 46 Gambar 12. Konsentrasi karotenoid metil ester pada berbagai kecepatan
pengadukan ... 48 Gambar 13. Perolehan karotenoid metil ester pada berbagai kecepatan
pengadukan ... 48 Gambar 14. Rendemen CME pada berbagai kecepatan pengadukan ... 49 Gambar 15. Kadar ester CME pada berbagai kecepatan pengadukan ... 50 Gambar 16. Perolehan metil ester pada berbagai kecepatan pengadukan ... 50 Gambar 17. Konsentrasi karotenoid metil ester pada kombinasi perlakuan
konsentrasi NaOH, suhu dan waktu reaks ... 53 Gambar 18. Perolehan karotenoid metil ester pada kombinasi perlakuan
konsentrasi NaOH, suhu dan waktu reaksi ... 56 Gambar 19. Rendemen CME (crude methyl ester) pada kombinasi perlakuan
konsentrasi NaOH, suhu dan waktu reaksi ... 57 Gambar 20. Sabun yang terbentuk pada penambahan katalis 2% ... 59 Gambar 21. Kadar ester CME (crude methyl ester) pada kombinasi perlakuan
konsentrasi NaOH, suhu dan waktu reaksi ... 62 Gambar 22. Perolehan metil ester pada kombinasi perlakuan konsentrasi
Gambar 24. Konsentrasi karotenoid fraksi kolom kromatografi yang ditampung pada berbagai nisbah adsorben abu sekam
padi/silika gel ... 70 Gambar 25. Konsentrasi karotenoid produk konsentrat pada berbagai nisbah
adsorben abu sekam padi/silika gel ... 72 Gambar 26. Tingkat pemekatan karotenoid produk konsentrat pada berbagai
nisbah adsorben abu sekam padi/silika gel ... 73 Gambar 27. Skema interaksi sorpsi (penempelan) molekul dalam CME pada
permukaan adsorben ... 75 Gambar 28. Interaksi pergantian molekul heksana oleh fraksi cair karotenoid
pada permukaan adsorben ... 75 Gambar 29. Perolehan karotenoid produk konsentrat pada berbagai nisbah
adsorben abu sekam padi/silika gel ... 76 Gambar 30. Konsentrasi karotenoid setiap fraksi eluat pada berbagai jumlah
CME yang dilewatkan dalam kolom ... 78 Gambar 31. Konsentrasi karotenoid produk konsentrat pada berbagai jumlah
CME yang dilewatkan ke dalam kolom ... 80 Gambar 32. Tingkat pemekatan karotenoid produk konsentrat pada berbagai
jumlah CME yang dilewatkan ke dalam kolom ... 81 Gambar 33. Perolehan karotenoid produk konsentrat pada berbagai jumlah
CME yang dilewatkan ke dalam kolom ... 82 Gambar 34. Perolehan karotenoid pada proses pemisahan karotenoid
DAFTAR LAMPIRAN
Halaman Lampiran 1. Hasil analisis komposisi asam lemak CPO ... 96 Lampiran 2. Pengaruh kecepatan pengadukan terhadap konsentrasi dan
perolehan karotenoid CME ... 99 Lampiran 3. Hasil analisis sidik ragam konsentasi karotenoid CME pada
berbagai perlakuan kecepatan pengadukan ... 100 Lampiran 4. Hasil analisis sidik ragam perolehan karotenoid CME pada
berbagai perlakuan kecepatan pengadukan ... 101 Lampiran 5. Pengaruh kecepatan pengadukan terhadap rendemen CME,
kadar ester dan perolehan CME ... 102 Lampiran 6. Hasil analisis sidik ragam rendemen CME pada berbagai
perlakuan kecepatan pengadukan ... 103 Lampiran 7. Hasil analisis sidik ragam kadar ester CME pada berbagai
perlakuan kecepatan pengadukan ... 104 Lampiran 8. Hasil analisis sidik ragam perolehan CME pada berbagai
perlakuan kecepatan pengadukan ... 105 Lampiran 9. Data pengukuran konsentrasi dan perolehan karotenoid CME
pada kombinasi perlakuan konsentrasi NaOH, suhu Lampiran 12. Rekapitulasi perhitungan kadar ester CME ... 111 Lampiran 13. Hasil analisis sidik ragam rendemen CME pada kombinasi
perlakuan konsentrasi NaOH, suhu dan waktu reaksi ... 112 Lampiran 14. Hasil analisis sidik ragam kadar ester CME pada kombinasi
perlakuan konsentrasi NaOH, suhu dan waktu reaksi ... 114 Lampiran 15. Hasil analisis sidik ragam perolehan metil ester pada
kombinasi perlakuan konsentrasi NaOH, suhu dan waktu reaksi ... 116 Lampiran 16. Konsentrasi karotenoid tiap fraksi berwarna yang ditampung
Lampiran 17. Konsentrasi karotenoid, perolehan karotenoid dan tingkat pemekatan karotenoid produk konsentrat pada berbagai
perlakuan nisbah abu sekam padi/silika gel ... 119 Lampiran 18. Hasil analisis sidik ragam konsentrasi karotenoid produk
konsentrat pada berbagai perlakuan nisbah abu sekam padi/ silika gel ... 120 Lampiran 19. Hasil analisis sidik ragam pemekatan karotenoid produk
konsentrat pada berbagai perlakuan nisbah abu sekam
padi/silika gel ... 121 Lampiran 20. Hasil analisis sidik ragam perolehan karotenoid produk
konsentrat pada berbagai perlakuan nisbah abu sekam padi/ silika gel ... 122 Lampiran 21. Konsentrasi karotenoid tiap fraksi berwarna yang ditampung
dalam kromatografi kolom pada berbagai jumlah ekstrak yang dilewatkan dalam kolom ... 123 Lampiran 22. Konsentrasi karotenoid, perolehan karotenoid dan tingkat
pemekatan karotenoid produk konsentrat pada berbagai
perlakuan jumlah CME yang dilewatkan dalam kolom ... 124 Lampiran 23. Hasil analisis sidik ragam konsentrasi karotenoid produk
konsentrat pada berbagai perlakuan jumlah CME yang
dilewatkan ke dalam kolom ... 125 Lampiran 24. Hasil analisis sidik ragam tingkat pemekatan karotenoid
produk konsentrat pada berbagai perlakuan jumlah CME yang dilewatkan ke dalam kolom ... 126 Lampiran 25. Hasil analisis sidik ragam perolehan karotenoid produk
konsentrat pada berbagai perlakuan jumlah CME yang
I. PENDAHULUAN
A. LATAR BELAKANG
Kelapa sawit merupakan komoditas unggulan yang mempunyai kontribusi penting dalam pembangunan ekonomi pada umumnya dan pembangunan agroindustri pada khususnya. Luas total area perkebunan kelapa sawit di Indonesia mencapai 5.5 juta hektar dan mampu memproduksi minyak sawit kasar (Crude Palm Oil/CPO) sebesar 13.1 juta ton sepanjang tahun 2005 (IPOC, 2005). Jumlah tersebut merupakan terbesar kedua di dunia setelah Malaysia dan diproyeksikan akan menjadi yang terbesar di dunia pada lima tahun mendatang.
Industri pengolahan kelapa sawit di Indonesia saat ini masih didominasi oleh industri kilang CPO dan industri pemurnian menjadi minyak makan. Padahal terdapat banyak produk hilir lain yang dapat dikembangkan. Produk hilir industri sawit yang telah diproduksi di Indonesia sementara ini adalah minyak goreng, margarin, shortening dan produk oleokimia berupa surfaktan, gliserin, asam lemak, dan fatty alkohol. Oleokimia merupakan produk olahan CPO kelompok non pangan.
Salah satu produk turunan oleokimia adalah ester, contohnya adalah metil ester. Asam lemak metil ester mempunyai peranan utama dalam industri oleokimia. Metil ester digunakan sebagai senyawa intermediate untuk sejumlah oleokimia seperti fatty alkohol, alkanolamida, α-sulfonat, gliserol monostearat, surfaktan, gliserin dan asam lemak lainnya. Metil ester dapat dihasilkan melalui reaksi transesterifikasi antara trigliserida (minyak sawit) dengan metanol menjadi metil ester dan gliserol dengan bantuan katalis basa. Produk samping yang dihasilkan adalah gliserin.
penggunaan metil ester sebagai biodiesel inilah yang memicu pertumbuhan industri oleokimia di Indonesia.
Salah satu peluang untuk meningkatkan daya saing metil ester berbahan baku minyak sawit adalah adanya kandungan mikronutrien karotenoid. Dengan melakukan penjumputan (recovery) terhadap karotenoid minyak sawit selama proses produksi metil ester, selain dihasilkan nilai tambah dari metil ester, juga akan diperoleh nilai tambah yang tinggi dari penjumputan karotenoid.
Minyak sawit kasar memiliki kandungan karotenoid yang cukup tinggi yaitu berkisar 400-700 µg/g dan lebih dari 80% dalam bentuk α-, β-, - karoten (Choo et al., 1989). Komponen ini memiliki banyak kegunaan bagi kesehatan manusia selain sebagai komponen vitamin, di antaranya merupakan senyawa antikanker, mencegah penuaan dini dan penyakit kardiovaskuler, serta kegunaan lainnya. Mengkonsumsi β-karoten jauh lebih aman daripada mengkonsumsi vitamin A yang dibuat secara sintetis. Sekitar 25% β-karoten yang diabsorpsi pada mukosa usus tetap dalam bentuk utuh, sedangkan 75% sisanya diubah menjadi retinol (vitamin A) (Brody, 1993).
Beberapa peneliti sebenarnya telah melakukan perhitungan kadar ester produk yang dihasilkan walaupun dengan cara yang berbeda-beda. Saat ini standar biodiesel Indonesia telah disahkan sebagai SNI dengan nomor 04-7182-2006.
Berbagai metode ekstraksi dan perolehan kembali β-karoten dari minyak sawit telah dilakukan oleh peneliti terdahulu, di antara berbagai metode yang digunakan adalah metode adsorpsi (Naibaho, 1983), alkoholisis diikuti saponifikasi (Rahayu, 1996), alkoholisis diikuti distilasi molekuler (Ooi et al., 1994), ekstraksi dengan fluida superkritik (Muchtadi, 1992), saponifikasi diikuti kromatografi kolom preparatif (Roidi, 1998), ekstraksi pelarut diikuti kromatografi kolom adsorpsi (Masni, 2004; Hasanah, 2006), dan alkoholisis diikuti membran filtrasi (Darnoko, 2005).
dibandingkan teknik lainnya. Instrumen yang digunakan tidak begitu rumit dan memiliki prinsip kerja yang sederhana. Penggunaan abu sekam padi dipandang perlu karena potensinya yang besar sebagai bahan penjerap serta merupakan upaya pemanfaatan bahan baku lokal yang mudah dibuat dengan biaya rendah.
Penjumputan karotenoid dari CME minyak sawit yang selanjutnya dapat digunakan untuk produksi biodiesel, diharapkan dapat meningkatkan nilai tambah dalam proses produksi biodiesel. Selain itu, konsentrat karotenoid yang diperoleh mempunyai nilai lebih yaitu selain mengandung komponen pro vitamin A (β-karoten), juga mengandung senyawa bermanfaat lainnya yaitu α -karoten yang dapat menjadi senyawa antikanker. Karotenoid dalam minyak sawit dapat bermanfaat untuk penanggulangan kebutaan karena xerophtalmia, mengurangi peluang terjadinya penyakit kanker, mencegah proses menua yang terlalu dini, meningkatkan imunisasi tubuh dan mengurangi terjadinya penyakit degeneratif. Penggunaan teknik kromatografi kolom adsorpsi diharapkan mampu memberikan gambaran mengenai profil pemekatan karotenoid yang berasal dari CME menggunakan adsorben abu sekam padi dan silika gel.
B. TUJUAN PENELITIAN
Tujuan dari penelitian adalah:
1. Mendapatkan proses transesterifikasi yang optimum untuk menghasilkan metil ester kasar minyak sawit dengan kandungan karotenid dan kadar ester yang tinggi.
2. Mendapatkan proses pemekatan karotenoid yang optimum pada metil ester kasar dengan menggunakan metode kromatografi kolom adsorpsi menggunakan adsorben abu sekam padi dan silika gel.
II. TINJAUAN PUSTAKA
A. MINYAK SAWIT
Indonesia dikaruniai kondisi tanah dan iklim yang sangat cocok untuk pertumbuhan pohon sawit. Pohon sawit menghasilkan minyak sawit yang sangat penting peranannya pada perekonomian nasional. Industri pengolahan kelapa sawit merupakan salah satu industri berbasis pertanian yang menempati posisi strategis di Indonesia. Indonesia mampu memproduksi minyak sawit kasar (CPO/Crude Palm Oil) sebesar 13.1 juta ton sepanjang tahun 2005 dengan luas total perkebunan kelapa sawit mencapai 5.5 juta hektar (IPOC, 2005).
Kelapa sawit mengandung kurang lebih 80% perikarp dan 20% buah yang dilapisi kulit yang tipis, kadar minyak dalam perikarp sekitar 34-40%. Dari kelapa sawit ini dapat dihasilkan dua jenis minyak yang sangat berlainan, yaitu minyak yang berasal dari sabut (mesokarp) kelapa sawit disebut minyak sawit (CPO/Crude Palm Oil) dan minyak yang berasal dari inti kelapa sawit yang dinamakan minyak inti sawit (PKO/Palm Kernel Oil) (Ketaren, 1986).
Perbedaan antara minyak sawit dengan minyak inti sawit adalah adanya pigmen karotenoid pada minyak sawit sehingga berwarna kuning merah. Komposisi karotenoid yang terdeteksi pada minyak sawit terdiri dari α-, β-, - karoten dan xantofil sedangkan pada PKO tidak terdeteksi adanya karoten. Perbedaan lain pada kandungan asam lemaknya. Pada minyak inti sawit terdeteksi adanya asam lemak kaproat dan asam lemak kaprilat, sedangkan kedua asam lemak ini tidak terdeteksi pada minyak sawit (Muchtadi, 1992).
rantai C18 dan memiliki satu ikatan rangkap. Titik cair asam oleat lebih rendah dibanding asam palmitat yaitu 14oC (Ketaren, 1986).
Timms (1985) menyatakan bahwa minyak sawit dapat dibedakan dari minyak lainnya berdasarkan kandungan gliseridanya yang spesifik dan terdapat dalam jumlah yang seimbang. Minyak sawit memiliki sifat yang unik karena kandungan asam lemak jenuhnya yang tinggi pada molekul gliseridanya, 10-16% pada posisi kedua, sehingga minyak sawit terdiri dari 3 jenis trigliserida, yaitu: (1) Ketiganya berikatan jenuh, umumnya PPP (tripalmitin); (2) Dua yang berikatan jenuh, umumnya POP (palmitat, oleat, palmitat); (3) Hanya satu yang berikatan jenuh, dan pada umumnya POO (palmitat, oleat, oleat). Komposisi minyak sawit di Indonesia rata-rata mengandung PPP: 10.5%, PPO: 8.6%, POP: 40%, POO: 34.0% dan OOO: 6.6% (Hamilton, 1980). Komposisi asam lemak minyak sawit kasar disajikan pada Tabel 1.
Tabel 1. Komposisi asam lemak minyak sawit kasara Asam Lemak Kadar (%) Laurat (C 12:0)
Miristat (C 14:0) Palmitat (C 16:0) Stearat (C 18:0) Oleat (C 18:1) Linoleat (C 18:2) Linolenat (C 18:3)
0-1
Ketaren (1986) menggambarkan pengolahan minyak sawit secara umum dengan beberapa tahap, yaitu ekstraksi, pemurnian, dan winterisasi (fraksinasi). Ekstraksi adalah suatu cara untuk mendapatkan minyak atau lemak dari bahan yang diduga mengandung minyak atau lemak. Adapun cara ekstraksi yaitu rendering, mechanical expresion, dan solvent extraction.
dalam industri. Pada umumnya minyak untuk tujuan bahan pangan dimurnikan melalui tahap proses sebagai berikut: (1) pemisahan bahan berupa suspensi dan dispersi koloid dengan cara penguapan, degumming dan pencucian dengan asam; (2) pemisahan asam lemak bebas dengan cara netralisasi; (3) dekolorisasi dengan pemucatan; (4) deodorisasi; dan (5) pemisahan gliserida jenuh (stearin) dengan cara pendinginan (chilling). Winterisasi adalah bagian dari pemurnian minyak hasil ekstraksi. Winterisasi yaitu proses pemisahan bagian gliserida jenuh atau bertitik cair tinggi dari trigliserida bertitik cair rendah. Pada suhu rendah, trigliserida padat tidak dapat larut dalam trigliserida cair (Ketaren, 1986).
Minyak sawit memiliki banyak keunggulan yang dapat dieksploitasi sedemikian rupa untuk produk-produk farmasetikal dan nutrasetikal, di antaranya adalah adanya kandungan komponen-kompenen minor, antara lain karoten dan tokoferol. Kandungan karoten di dalam minyak sawit berkisar antara 400 – 700 µg/g dan tokoferol (vitamin E) berkisar antara 500 – 700 µg/g (Muchtadi, 1992)
Minyak sawit kasar mengandung lebih kurang 1% komponen minor yang terdiri dari karotenoid, tokoferol, tokotrienol, sterol-sterol, fosfolipid dan glikolipid, terpen dan gugus hidrokarbon alifatik, dan elemen sisa lainnya. Komponen terbesar dari karotenoid adalah β-karoten dan α-karoten yang mencapai 90% dari total karotenoid yang terdiri dari 13 jenis (Ong et al.,1990).
B. KAROTENOID
lainnya terletak pada posisi C-1 dan C-5 serta di antaranya terdapat ikatan ganda terkonjugasi.
CH2 = C – CH = CH2
Gambar 1. Struktur molekul isoprena (Lehninger, 1982)
Gugus metil yang terletak pada posisi C-1 dan C-5 terbentuk dari hasil penggabungan dua molekul isoprena, demikian pula gugus metil pada posisi C-1 dan C-6 (Gambar 2). Penggabungan ini terjadi melalui ujung dan pangkal (Choo et al., 1989)
-C=CH-CH=CH-C=CH= = = = = = = = = = = = =CH-CH=C-CH-CH-CH=C-
Gambar 2. Struktur dasar karotenoid (Lehninger, 1982)
Menurut Ranganna (1979), karotenoid dapat digolongkan atas empat golongan, yaitu:
1. Karotenoid hidrokarbon C40H56; yang termasuk golongan ini adalah α-, β-, - karoten dan likopen
2. Xantofil dan derivat-derivat karoten yang mengandung oksigen dan gugus hidroksil (C40H55OH); yang termasuk dalam golongan ini adalah kriptosantin, kapsantin, torularhodin dan lutein (C40H54(OH)2)
3. Ester xantofil yaitu ester xantofil asam lemak, misal zeasantin
4. Asam karotenoid yaitu derivat karotenoid yang mengandung gugus karboksil.
CH3 CH3 CH3 CH3
1 1 5 5 molekul pusat
1 6 CH3
Karotenoid termasuk senyawa lipida yang tidak tersabunkan, larut dengan baik dalam pelarut organik tetapi tidak larut dalam air. Sifat ini penting terutama dalam pemisahan karotenoid dari bahan lain (Ranganna, 1979). Menurut Meyer (1966) sifat fisika dan kimia karotenoid adalah:
1. Larut dalam minyak dan tidak larut dalam air
2. Larut dalam kloroform, benzene, karbon disulfida dan petroleum eter 3. Tidak larut dalam etanol dan metanol dingin
4. Tahan terhadap panas apabila dalam keadaan vakum 5. Peka terhadap oksidasi, autooksidasi dan cahaya 6. Mempunyai ciri khas absorpsi cahaya.
Sifat-sifat di atas penting untuk pemisahan karotenoid dari bahan lain. Adanya ikatan ganda menyebabkan karotenoid peka terhadap oksidasi yang akan lebih cepat dengan adanya sinar dan katalis logam, khususnya tembaga, besi dan mangan (Walfford, 1980).
Karotenoid lebih tahan tersimpan dalam lingkungan asam lemak tidak jenuh jika dibandingkan dengan penyimpanan dalam asam lemak jenuh, karena asam lemak lebih mudah menerima radikal bebas bila dibandingkan dengan karotenoid, sehingga oksidasi yang pertama kali akan terjadi pada asam lemak dan akibatnya karotenoid terlindungi dari oksidasi. Pada suasana asam, karotenoid mengalami isomerisasi dan akan membentuk poli cis-isomer (Chichester et al., 1970). Karena warnanya mempunyai kisaran dari kuning sampai merah, maka deteksi panjang gelombangnya diperkirakan antara 430 – 480 nm (Fennema, 1996).
Tabel 2. Jenis-jenis karotenoid yang mempunyai nilai gizia Jenis Karotenoid Relatif Potensi Biologis
terhadap Vitamin A α-karoten
β-karoten -karoten
53 100
45 aWirahadikusumah (1985)
Karoten merupakan sumber vitamin A yang berasal dari tanaman dalam bentuk β-karoten, α-karoten dan -karoten, sedangkan yang berasal dari hewan berbentuk vitamin A. Senyawa ini sering disebut anti xerophtalmia, karena kekurangan akan senyawa tersebut dapat menimbulkan gejala rabun mata. Provitamin A yang merupakan β-karoten dalam minyak sawit dapat bermanfaat untuk penanggulangan kebutaan karena xerophtalmia, mengurangi peluang terjadinya penyakit kanker, mencegah proses menua yang terlalu dini, meningkatkan imunisasi tubuh dan mengurangi terjadinya penyakit degeneratif. Struktur β-karoten dan retinol dapat dilihat pada Gambar 3.
Gambar 3. Struktur β-karoten dan retinol (Fennema, 1996)
Senyawa β-karoten jauh lebih aman dikonsumsi daripada vitamin A yang dibuat secara sintetis. Pendekatan yang terbaik untuk mencegah defisiensi vitamin A adalah dengan menghimbau agar suplementasi β-karoten dosis tinggi dilakukan pada diet intake. Tubuh manusia mempunyai kemampuan mengubah sejumlah besar karoten menjadi vitamin A (retinol), sehingga karoten ini disebut provitamin A (Winarno 1991). Sekitar 25% dari β-karoten yang
CH2OH
β-karoten
diabsorbsi pada mukosa usus tetap dalam bentuk utuh, sedang 75% sisanya diubah menjadi retinol (vitamin A) dengan bantuan enzim 15, 15’ β-karoten dioksigenase (Fennema, 1996).
Vitamin A dikenal juga dengan nama lain, yaitu: akseroftol (axerophtol), asam retinoat (retinoic acid), retinal, retinol dan dehidroretinol. Sampai tahun 1967, aktifitas vitamin A pada jaringan tanaman/hewan dinyatakan dalam International Unit (IU) atau United States Pharmaopeia (USP), yang nilainya sebanding (1 IU = 1 USP unit, yang sama dengan 0.3 µg retinol) (Sulaswatty, 1998).
Fennema (1996) menyebutkan bahwa β-karoten hanya memiliki seperenam aktifitas retinol ketika dicerna manusia. Satuan Retinol Equivalents (RE) digunakan untuk mengukur aktifitas vitamin A (1 RE = 1 µg retinol). Untuk konversi satuan vitamin A perlu diperhatikan hal-hal sebagai berikut: (a) pada basis berat, keaktifan adalah setengahnya dari retinol sedangkan karotenoid lain seperempatnya dari retinol; dan (b) retinol diserap secara sempurna oleh usus, sedangkan karotenoid hanya sepertiganya. Oleh karena itu, aktifitas β-karoten = 1/6 retinol, sedangkan karotenoid lain = 1/12 retinol.
1 IU = 0.3 µg retinol = 0.6 µg β-karoten 1 RE = 1 µg retinol
= 6 µg β-karoten = 12 µg karotenoid lain
C. METIL ESTER
agen aktif, bahan pembantu dalam pengolahan karet, produk farmasi, dan alternatif pengganti atau pencampur bahan bakar motor diesel (Hui, 1996).
Hui (1996) menyatakan bahwa penggunaan metil ester sebagai bahan baku oleokimia dasar atau turunannya memiliki beberapa keuntungan, seperti produk akhir dengan tingkat kemurnian tinggi, pengaturan kondisi yang lebih mudah selama sintesis dan tidak memerlukan bahan-bahan yang terlalu mahal untuk konstruksi, lebih mudah untuk didistilasi fraksinasi, mudah dalam penanganan dan transportasi, serta mudah didegradasikan.
Metil ester terutama dimanfaatkan dalam industri kosmetika, dan agen pencuci dan pembersih. Selain itu metil ester juga dimanfaatkan sebagai plasticizer, sabun metalik, sabun, keperluan rumah tangga, produk perawatan diri, bahan pembantu dalam pengolahan karet, farmasi dan bahan baku untuk produksi oleokimia dasar lainnya serta biofuel (biodiesel) (Ong et al., 1990).
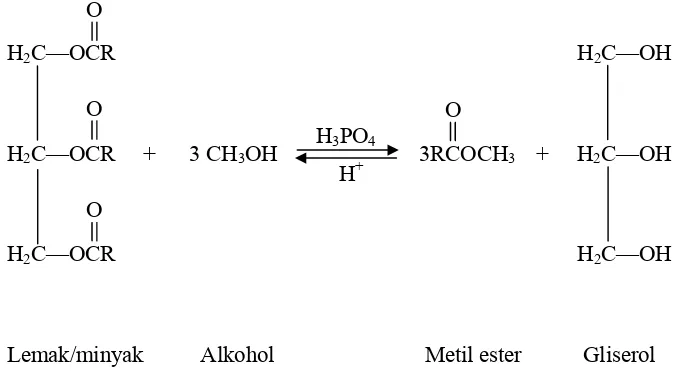
Prinsip pembuatan metil ester adalah interesterifikasi dengan menggunakan alkohol dari suatu ester dengan ester lain dengan dasar proses hidrolisis, kecuali mengganti air dengan alkohol. Proses ini sering disebut alkoholisis atau metanolisis apabila menggunakan metanol dalam prosesnya (Hui, 1996). Proses transesterifikasi minyak atau lemak dipengaruhi oleh beberapa faktor, yaitu suhu, lama hidrolisis, jenis dan konsentrasi katalis, kecepatan pengadukan dan perbandingan metanol-asam lemak (Hui, 1996). Proses transesterifikasi akan berlangsung lebih cepat bila suhu dinaikkan mendekati titik didih metanol. Semakin tinggi kecepatan pengadukan akan meningkatkan pergerakan molekul dan menyebabkan terjadinya tumbukan. Pada awal terjadinya reaksi, pengadukan akan menyebabkan terjadinya difusi antara minyak atau lemak sampai terbentuk metil ester. Dengan semakin banyaknya metil ester yang terbentuk menyebabkan pengaruh pengadukan semakin kecil, hingga terbentuk keseimbangan. Reaksi metanolisis antara lemak atau minyak dengan metanol dapat dilihat pada Gambar 4.
transesterifikasi secara kontinyu yang dilakukan oleh Noureddini dan Zhu (1997) serta Darnoko dan Cheryan (2000) yaitu suhu reaksi 60oC, waktu reaksi 1-2 jam yang diikuti dengan pengadukan, menggunakan katalis KOH 1 persen (w/w) terlarut dalam metanol. Penambahan metanol dilakukan dengan perbandingan reaktan sebesar 6:1.
H2C—OCR H2C—OH
H2C—OCR + 3 CH3OH 3RCOCH3 + H2C—OH
H2C—OCR H2C—OH
Lemak/minyak Alkohol Metil ester Gliserol
Gambar 4. Persamaan reaksi metanolisis (Farris, 1979)
Proses transesterifikasi dapat dilakukan dengan menggunakan katalis ataupun tanpa menggunakan katalis. Biasanya dalam pembuatan metil ester digunakan katalis asam (HCl, H2SO4, H3PO4) atau katalis basa atau alkali (NaOCH3, KOH dan NaOH) (Sonntag, 1982). Menurut Faris (1979), katalis yang paling efektif adalah natrium metoksida.
Reaksi menggunakan katalis basa pada umumnya berlangsung lebih cepat dibandingkan dalam katalis asam dikarenakan reaksi berlangsung searah. Namun pemakaian katalis basa memiliki kelemahan yaitu hanya akan berlangsung sempurna bila minyak atau lemak dalam kondisi netral dan tanpa keberadaan air. Selain itu pemakaian katalis basa dapat menyebabkan terbentuknya sabun, dimana dapat menyebabkan hilangnya katalis basa akibat reaksi penyabunan (proses transesterifikasi berlangsung dalam dua tahap) dan
O H3PO4
H+ O
O
juga menyebabkan terbentuknya struktur gel yang dapat menghambat proses pemisahan (Sonntag, 1982).
Secara stokiometri reaksi metanolisis hanya memerlukan tiga mol metanol untuk satu mol trigliserida. Pemakaian metanol dalam jumlah berlebih diharapkan mendorong reaksi bergeser ke kanan sehingga akan menghasilkan rendemen metil ester yang tinggi dan proses pemisahan salah satu produk dari campuran hasil reaksi lebih mudah (Noureddini dan Zhu, 1997). Rasio metanol-minyak sekitar 6:1 sudah optimal untuk menghasilkan rendemen metil ester sekitar 95%, dimana katalis yang digunakan adalah NaOH 1% (Boocock et al., 1998). Minyak sawit yang digunakan telah mengalami perlakuan pendahuluan berupa proses pemurnian meliputi degumming, netralisasi, bleaching, dan deodorisasi.
Pada proses pemekatan karotenoid, minyak sawit diubah ke dalam bentuk ester metil melalui proses alkoholisis dengan metanol, dilanjutkan dengan mengekstrak metil ester yang terbentuk dengan mencampurkan pelarut organik, sehingga didapatkan lapisan berwarna kaya karoten dan lapisan tidak berwarna, dan jika lapisan berwarna dipekatkan lebih lanjut dengan kromatografi maka karotenoid dapat dipekatkan sampai 95% (Iwasaki dan Murakoshi, 1992). Sedangkan Ooi et al. (1994) melaporkan, bahwa minyak sawit kasar dari spesies tenera yang dialkoholisis dengan metanol atau etanol (pro analisa) pada perbandingan molar minyak sawit kasar terhadap alkohol 2:1 dengan katalis NaOH 0.5% (b/b) setelah asam lemak bebas dinetralkan, dan dilanjutkan dengan distilasi molekuler 2 tahap, dapat memekatkan karotenoid sampai 75%.
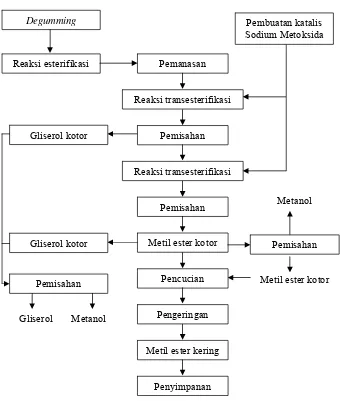
yang cukup tinggi (sekitar 6.5 juta ton pada tahun 2000 meningkat menjadi 15 juta ton pada 2012). Pada proses produksi biodiesel, CPO yang digunakan sebagai minyak mentah dibersihkan terlebih dahulu dengan proses degumming. Proses tersebut tidak perlu mengikuti keseluruhan urutan proses rafinasi CPO menjadi refined oil karena ada pengotor minyak yang dapat dimanfaatkan langsung menjadi biodiesel dan pengotor-pengotor lainnya akan tersingkirkan selama proses pembuatan biodiesel, kecuali pengotor berupa zat warna (Soerawidjaja et al., 2005).
Gambar 5. Diagram alir proses produksi metil ester dari minyak sawit pada industri biodiesel (Soerawidjaja et al., 2005)
Pemanasan
Reaksi transesterifikasi
Pemisahan
Reaksi transesterifikasi
Pemisahan
Metil ester kotor
Pencucian
Pengeringan
Metil ester kering
Penyimpanan Reaksi esterifikasi
Degumming Pembuatan katalis
Sodium Metoksida
Gliserol kotor
Gliserol kotor
Pemisahan
Pemisahan
Metil ester kotor Metanol
D. METODE EKSTRAKSI DAN PEMEKATAN KAROTENOID
Berbagai metode telah dikembangkan untuk melakukan ekstraksi dan pemekatan karotenoid dari minyak sawit antara lain: metode penyabunan, metode adsorpsi, metode urea, proses ekstraksi menggunakan pelarut selektif dan distilasi molekular, transesterifikasi diikuti dengan pemisahan dan distilasi molekuler serta teknik fluida superkritik (Masni, 2004).
Menurut Gross (1991), belum terdapat metode standar untuk ekstraksi karotenoid, namun untuk mendapatkan hasil ekstraksi yang optimal sebaiknya digunakan bahan yang segar, tidak rusak dan contoh yang digunakan harus terwakili. Ekstraksi dilakukan secepat mungkin untuk mencegah terjadinya kerusakan akibat oksidasi.
1. Metode Penyabunan
Proses penyabunan diawali dengan melarutkan minyak sawit kasar dengan KOH dalam metanol. Prinsip dari metode ini adalah memisahkan senyawa karotenoid yang merupakan senyawa yang tidak tersabunkan dengan senyawa-senyawa yang dapat disabunkan. Pemisahan selanjutnya adalah dengan melarutkan karotenoid tersebut dengan menggunakan pelarut organik, akan tetapi bahan yang tersabunkan tidak ikut terlarut (Parker, 1992).
Lemak kasar yang direaksikan dengan basa mengakibatkan lemak, lilin, senyawa lipid, dan asam lemak bebas didalamnya akan membentuk sabun. Persenyawaan sabun ini akan terdispersi dalam lapisan air, hasil lainnya yaitu gliserol, fosfat alkohol dan amina terlarut dalam air, sedangkan golongan sterol, pigmen, hidrokarbon bersifat tidak larut dalam air (Ketaren, 1986).
pekat produk yang diperoleh semakin tinggi konsentrasinya dan semakin besar kelipatan konsentrasinya dibandingkan konsentrasi awal.
2. Metode Ekstraksi Pelarut
Metode ekstraksi pelarut merupakan salah satu metode ekstraksi yang cukup sederhana untuk mengekstrak karotenoid dari minyak sawit dibanding metode lain yang bisa digunakan, antara lain metode distilasi molekuler dan ekstraksi dengan metode fluida superkritis (Masni, 2004). Metode ekstraksi pelarut pertama kali diperkenalkan oleh Freeman (1940), dan pada awalnya metode ini didasarkan pada derajat ketidakjenuhan suatu campuran digliserida (diasilgliserol), namun kemudian dikembangkan untuk memperoleh komponen minor dari minyak seperti β-karoten (Choo et al., 1989; Ooi et al., 1994).
Proses pemisahan pada metode ekstraksi pelarut tergantung pada penggunaan jenis pelarut yang dapat memisahkan fraksi yang diinginkan. Pelarut yang umum digunakan adalah, heksana, metanol, etanol, asetonitril dan furfural. Food and Drug Administration (FDA, 1987) memberikan batasan jumlah sisa pelarut yang masih diperkenankan dalam bahan makanan (Tabel 3).
Tabel 3. Residu pelarut organik yang diijinkan dalam makanana Jenis Pelarut Residu (ppm) Aseton
Etilen klorida Etanol Heksana
Isopropil alkohol Metilen diklorida Metanol
30 30 30 25 50 30 50 a
Metode ekstraksi pelarut telah banyak digunakan oleh beberapa peneliti terdahulu untuk mengekstrak karotenoid, antara lain Taungbodithan (1998) menggunakan metode ini untuk mengekstrak karotenoid dari buah dan sayuran, yaitu tomat, wortel dan daun bayam; Kurilich et al. (1999) mengekstrak karotenoid dari Brassica oleraceae; Lessin, Catigani dan Schwartz (1997) mengekstrak karotenoid dari buah dan sayuran segar antara lain brokoli, cantaloupe, wortel, jeruk, peach, bayam, ubi jalar dan tomat; Konings dan Roomans (1997) menggunakan metode ekstraksi pelarut untuk mengekstrak karotenoid dari buah dan sayuran. Ittah et al. (1993) mengekstrak karotenoid dari cabe merah, paprika dan oleoresin.
Burdick dan Fletcher (1985) mengekstrak pigmen karotenoid dengan menggunakan campuran heksana-aseton-metanol (80:10:10 v/v/v). Schwartz dan Patroni (1985) mengekstrak jaringan tanaman dengan menggunakan campuran aseton-heksana (1:9 v/v), kemudian Ittah et al. (1993) mengekstraksi pigmen karotenoid dari paprica (Capsicum annum L) dengan menggunakan aseton. Masni (2004) yang menggunakan pelarut campuran heksana-aseton (10:1 v/v) berhasil mengekstrak karotenoid dari limbah serat sawit dengan konsentrasi 1283 µg/g. Hasanah (2006) dapat meningkatkan konsentrasi karotenoid minyak sawit kasar dari 498 µg/g menjadi 744 µg/g melalui fraksinasi menggunakan pelarut isopropanol (6:1 v/b minyak sawit kasar).
3. Metode Adsorpsi
Pemisahan karotenoid dari minyak sawit kasar dengan menggunakan adsorben resin sintetis (Diaion HP-20) telah dilaporkan oleh Baharin et al. (1998). Cara ini menghasilkan tingkat perolehan kembali (recovery) karotenoid yang beragam dari 40 – 65%, tergantung pada kondisi kolom kromatografi. Selanjutnya Desai dan Dubash (1994) juga melaporkan bahwa, dengan menggunakan adsorben campuran bentonit dan alumina (4 : 1) dalam bentuk gel untuk menjerap karoten dari CPO, didapatkan tingkat perolehan kembali sebesar 79%. Lessin et al. (1997) menggunakan polimer sintetis untuk menjerap karoten dari beberapa jenis buah segar dan yang telah diproses dan Sahidin et al. (2001) menggunakan adsorben campuran magnesium oksida dan aluminium oksida (1:1) untuk memurnikan β-karoten yang diekstraksi dari CPO dan didapatkan tingkat perolehan kembali sebesar 82.41%.
Masni (2004) melaporkan bahwa konsentrasi karotenoid dari produk konsentrat setelah proses pemisahan dengan menggunakan bahan penjerap abu sekam padi enam kali lebih besar dibandingkan dengan konsentrasi karotenoid ekstrak asalnya dengan tingkat perolehan kembali sebesar 86%. Nilai tersebut lebih tinggi dibandingkan dengan konsentrasi karotenoid dari pekatan yang diperoleh dengan menggunakan bahan penjerap silika gel dan alumina. Hasanah (2006) memperoleh konsentrat karotenoid dari minyak sawit kasar menggunakan kolom kromatografi dengan tingkat pemekatan 15 kali dan perolehan karotenoid sebesar 49%. Perolehan karotenoid adalah persentase total karotenoid produk akhir dibandingkan total karotenoid produk awal.
4. Metode Distilasi Molekuler
kondisi vakum untuk memisahkan suatu komponen dalam suatu campuran. Tekanan yang digunakan dalam metode ini berkisar antara 0.01-0.001 mmHg. Pada distilasi molekuler, jarak antara permukaan penguapan (lapisan cairan yang terbentuk secara mekanis) dengan permukaan kondensasi hanya beberapa cm, sehingga molekul-molekul mempunyai energi yang cukup untuk dapat terpisah dari campuran senyawa ke permukaan kondensasi tanpa bertabrakan dengan molekul lainnya (Ooi et al., 1994).
Dibandingkan dengan metode distilasi vakum, hasil yang diperoleh dengan distilasi molekuler jauh lebih besar. Hal ini disebabkan karena kontak terhadap panas pada waktu distilasi molekuler lebih singkat dibandingkan distilasi vakum. Dari beberapa penelitian yang dilakukan, diketahui bahwa metode distilasi molekuler melalui jalur metil ester cukup efektif dilakukan untuk mendapatkan ekstrak karotenoid dengan kemurnian dan hasil yang tinggi (Masni, 2004). Ooi et al. (1994) berhasil mendapatkan konsentrat karotenoid dengan kemurnian 75% menggunakan metode distilasi molekuler 2 tahap dan perlakuan metanolisis pada bahan bakunya.
5. Metode Ekstraksi dengan Fluida Superkritik
Teknik ekstraksi dengan fluida superkritik merupakan suatu teknik pemisahan yang memanfaatkan daya pelarut dari fluida superkritik pada suhu dan tekanan di sekitar titik kritik. Cara ini sangat efektif terutama untuk mengisolasi senyawa dengan bobot molekul sedang dengan kepolaran rendah. Dengan pemisahan pada suhu rendah, maka sangat berguna untuk mengekstraksi senyawa yang tidak tahan terhadap pemanasan (Sulaswatty, 1998).
teknik fluida superkritik hingga 39 kali tingkat pemekatan dengan rendemen karotenoid sebesar 42%.
Dibandingkan dengan pelarut lain, fluida superkritik mempunyai densitas dan viskositas yang rendah serta difusitas yang tinggi, sehingga memungkinkan untuk ekstraksi dan pemisahan yang cepat. Daya pelarut dari fluida superkritik cukup tinggi terhadap senyawa padat, cair atau gas dan ini dapat diubah dengan memvariasikan tekanan dan suhu. Selanjutnya fluida dapat dipisahkan dari ekstrak dan residu karena perbedaan volatilitas yang cukup tinggi (Sulaswatty, 1998).
E. Kromatografi Kolom Adsorpi
Kromatografi kolom pada dasarnya adalah pemisahan komponen-komponen dalam sampel dengan cara mengalirkan sampel melewati suatu kolom. Sampel dalam hal ini dibawa carrier atau disebut fase gerak (mobile phase). Sedangkan kolom berisi suatu bahan yang disebut fase diam (stationary phase) yang berfungsi memisahkan komponen sampel. Ada komponen yang ditahan lebih kuat dan ada yang ditahan secara lemah. Untuk yang ditahan lebih lemah akan keluar dari kolom lebih dahulu dan yang ditahan lebih kuat akan keluar lebih akhir (Gritter et al., 1991). Komponen-komponen tersebut bergerak pada tingkatan yang berbeda membentuk pita. Kromatografi kolom konvensional biasanya menggunakan adsorben padat yaitu silika gel. Eluen pada kromatografi ini biasanya bergerak lamban (Houghton, 1998).
adsorpsi adalah kompetisi antara zat terlarut (sampel) dan fase gerak dengan permukaan fase diam. Kekuatan adsorpsi terutama bergantung sifat gugus fungsionalnya, dimana gugus-gugus fungsional ini menentukan tingkat kepolaran. Sebagai contoh asam-asam akan diadsorpsi lebih kuat daripada alkohol, alkohol diadsorpsi lebih kuat daripada aldehid, aldehid diadsorpsi lebih kuat daripada hidrokarbon dan sebagainya (Adnan, 1997).
Proses desorpsi terjadi karena adanya interaksi antara pelarut dengan adsorben dan antara sampel dengan adsorben dalam bentuk ikatan yang lemah. Untuk melarutkan molekul non polar yang hanya memiliki interaksi yang lemah dengan adsorben yaitu van der Waals, dibutuhkan pelarut non polar yang juga hanya memiliki interaksi yang lemah. Meskipun solut dan pelarut tidak membentuk interaksi yang kuat satu sama lain (hanya interaksi van der Waals) pelarutan terjadi secara spontan (Casiday dan Frey, 2001). Adanya interaksi antara pelarut dan solut akan menyebabkan solut akan memutuskan ikatannya dengan adsorben. Ikatan yang terjadi ini pun sangat lemah sehingga selanjutnya terjadi lagi interaksi antara solut dengan penjerap. Hal ini terjadi secara berulang-ulang seiring penambahan pelarut yang terus-menerus sehingga terjadi pemisahan komponen dalam solut karena perbedaan kepolaran yang menyebabkan perbedaan waktu terjerap.
F. Abu Sekam Padi
Produksi beras yang tinggi di Indonesia menyebabkan tingginya limbah penggilingan padi yaitu sekam. Sekam padi adalah bagian terluar dari butiran padi, yang merupakan hasil sampingan saat proses penggilingan padi dilakukan. Sekitar 20% dari bobot padi adalah sekam padi dan kurang lebih 15% dari komposisi sekam adalah abu sekam padi yang selalu dihasilkan setiap kali sekam dibakar (Hara, 1986).
Abu sekam padi merupakan sumber biologis dari silika gel yang dapat digunakan dalam proses pemurnian minyak (Proctor dan Pallaniapan, 1989). Pembakaran sekam menggunakan cerealia prossesor akan menghasilkan abu yang mengandung silika 55% dan residu karbon. Pembakaran lebih lanjut di laboratorium pada suhu 500oC dapat menghasilkan abu dengan kandungan silika 97% dan kalium oksida 2%. Silika yang terdapat dalam sekam padi ada dalam bentuk amorf terhidrat. Kalmath dan Proctor (1998) juga melaporkan bahwa dengan proses kimiawi abu sekam padi dapat digunakan untuk memproduksi silika gel.
Peluang penggunaan abu sekam padi sebagai bahan penjerap pemisahan karotenoid menggunakan metode kromatografi kolom adsorpsi mengacu pada temuan beberapa penelitian yang telah menggunakan abu sekam padi sebagai penjerap, dengan pertimbangan bahwa abu sekam padi merupakan sumber silika yang baik. Kemampuan abu sekam padi sebagai penjerap lutein dari minyak kedelai ditunjukkan oleh hasil penelitian Proctor dan Pallaniapan (1989). Pada tahun 1992, Proctor dan Pallaniapan juga menemukan bahwa abu sekam padi dapat berperan sebagai bahan penjerap fosfolipid pada proses pemurnian minyak kacang kedelai (Masni, 2004).
bebas dari minyak goreng. Sedangkan Ping et al. (2001) menemukan bahwa abu sekam padi dapat digunakan sebagai pemucat minyak wijen.
III. METODOLOGI PENELITIAN
A. BAHAN DAN ALAT
Bahan baku utama yang digunakan dalam penelitian ini adalah minyak sawit kasar (crude palm oil) yang diperoleh dari PT Sinar Meadow International Indonesia. Adsorben yang digunakan adalah abu sekam padi dan silika gel. Sedangkan bahan lain yang digunakan yaitu, natrium hidroksida, metanol, heksana, asam asetat glasial, gas nitrogen, metanol, isopropanol, kloroform, kalium hidroksida, dan natrium sulfat anhidrat, serta beberapa bahan kimia lainnya.
Alat yang digunakan pada penelitian ini mencakup orbital thermoshaker, neraca analitik, sentrifuge, penangas air, buret, spektrofotometer UV-Vis, Gas Chromatography (GC), kolom kromatografi, fraction collector, lemari pendingin, rotavapor, oven, vortex, tabung vial, botol semprot dan peralatan gelas lainnya.
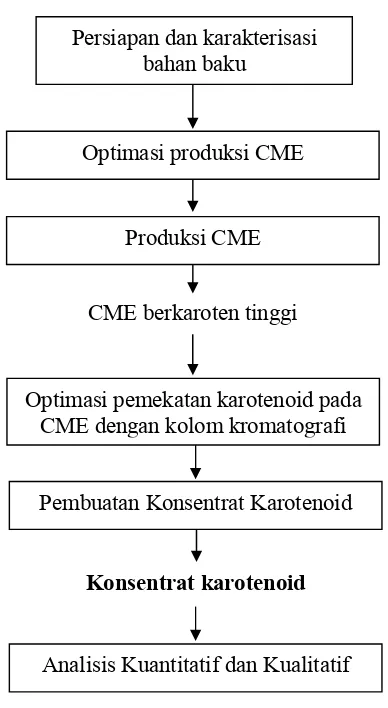
B. METODE PENELITIAN
Gambar 6. Diagram alir penelitian optimasi pemekatan karotenoid dari minyak sawit kasar skala laboratorium
1. Persiapan dan Karakterisasi Bahan Baku
Bahan baku CPO yang digunakan mula-mula dianalisis untuk mengetahui kadar air, kadar asam lemak bebas, konsentrasi karotenoid serta komposisi asam lemaknya. Sedangkan abu sekam padi dibuat dengan cara mengabukan sekam padi dalam tanur pada suhu 1200oC yang selanjutnya diayak menggunakan saringan ukuran 60 mesh agar didapatkan abu sekam yang halus dan bebas kotoran. Diagram alir persiapan bahan abu sekam padi disajikan pada Gambar 7.
Produksi CME
CME berkaroten tinggi
Pembuatan Konsentrat Karotenoid
Analisis Kuantitatif dan Kualitatif Optimasi produksi CME
Optimasi pemekatan karotenoid pada CME dengan kolom kromatografi
Konsentrat karotenoid Persiapan dan karakterisasi
Sekam padi
↓
Pengabuan suhu 1200oC ↓
Pengayakan ↓
Abu sekam padi berukuran 60-100 mesh ↓
Pengaktifan kembali pada suhu 100oC selama dua jam ↓
Abu sekam padi yang siap digunakan
Gambar 7. Diagram alir persiapan bahan abu sekam padi
2. Optimasi Produksi Metil Ester Kasar (Crude Methyl Ester)
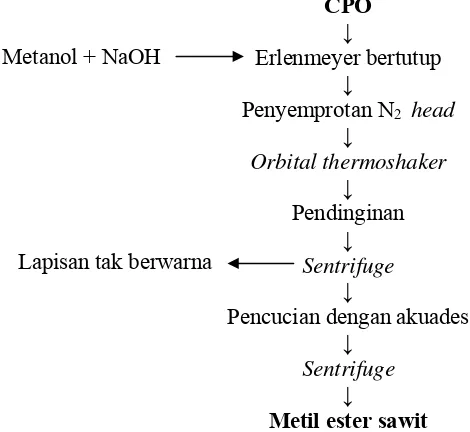
Metanolisis CPO dilakukan berdasarkan metode Ooi et al. (1994) dengan menggunakan katalis NaOH dalam metanol seperti tertera pada Gambar 8. Penentuan kondisi optimum proses produksi CME dilakukan dengan penerapan dua tahap optimasi. Tahap pertama yaitu optimasi proses dengan perlakuan kecepatan pengadukan, sedangkan tahap kedua yaitu optimasi proses dengan kombinasi tiga perlakuan (konsentrasi NaOH, waktu reaksi dan suhu reaksi).
CPO ↓
Erlenmeyer bertutup ↓
Penyemprotan N2 head
↓
Pencucian dengan akuades ↓
Sentrifuge
↓
Metil ester sawit
Gambar 8. Proses produksi metil ester (Ooi et al., 1994) Metanol + NaOH
a. Penentuan kecepatan pengadukan optimum
Reaksi transesterifikasi terjadi antara minyak (CPO) dengan metanol. Proses ini dipengaruhi oleh kecepatan pengadukan saat reaksi terjadi. Kecepatan pengadukan yang menghasilkan CME dengan tingkat ester dan konsentrasi karotenoid yang tinggi diseleksi melalui penerapan empat tingkatan kecepatan yaitu 150, 200, 250 dan 300 putaran per menit (rotation per minute/rpm). Proses transesterifikasi dilakukan pada temperatur 60oC selama 1 jam dalam orbital thermoshaker dengan nisbah CPO/metanol 1:10 (mol/mol) serta konsentrasi NaOH 1% (b/b CPO). Setelah reaksi selesai, campuran reaksi di-sentrifuge sehingga terbentuk dua lapisan. Lapisan atas berwarna merupakan fase ester dengan karotenoid di dalamnya dan lapisan bawah tak berwarna adalah fase air dan gliserol. Lapisan atas dicuci dengan air dan dipisahkan dengan sentrifuge, kemudian dilihat penampakan hasil dan pemisahan lapisannya secara kualitatif serta dianalisis tingkat ester dan kandungan total karotennya.
b. Penentuan konsentrasi NaOH, waktu reaksi dan suhu reaksi
optimum
Reaksi transesterifikasi dapat terjadi dengan adanya katalis, baik berupa asam ataupun basa. Katalis yang digunakan dalam penelitian adalah natrium hidroksida (NaOH). Di samping itu, reaksi transesterifikasi dapat berlangsung dengan baik pada suhu dan waktu reaksi tertentu. Ketiga faktor ini dikombinasikan sebagai perlakuan optimasi proses produksi CME.
reaksi adalah 1: 10 (mol/mol). Kecepatan pengadukan yang digunakan adalah kecepatan pengadukan optimum yang terpilih pada tahap sebelumnya. Metil ester yang terbentuk kemudian dianalisis tingkat ester dan kandungan total karotennya.
3. Pemekatan Karotenoid pada CME
Pemisahan karotenoid pada CME dilakukan dengan menggunakan kolom kromatografi. Bahan penjerap yang digunakan yaitu abu sekam padi dan silika gel. Kolom yang digunakan berdiameter 2.0 cm dan tinggi 40 cm. Setiap kolom diisi dengan bahan penjerap yang telah diaktifkan (dipanaskan dalam oven pada suhu 100oC selama lebih dari 2 jam) sebanyak 40 g dan dicampur dengan pelarut yang digunakan sebagai eluen untuk mengelusi contoh. Eluen yang digunakan yaitu heksana. Diagram alir pemekatan karotenoid pada CME menggunakan kolom kromatografi dapat dilihat pada Gambar 9.
Persiapan kolom kromatografi ↓
Pengisian kolom dengan bahan penjerap ↓
Pelarutan sampel dalam eluen ↓
Pengisian sampel ke dalam kolom ↓
Penyerapan sampel dalam bahan penjerap ↓
Pengelusian menggunakan heksana ↓
Penampungan fraksi eluat yang berwarna ↓
Penghitungan konsentrasi karotenoid dari setiap fraksi menggunakan spektrofotometer pada panjang gelombang 446 nm
↓
Penguapan pelarut dengan rotavapor dan penyemprotan N2
↓
Konsentrat karotenoid
Penentuan kondisi optimum proses produksi konsentrat karotenoid dilakukan dengan penerapan dua tahap optimasi. Tahap pertama yaitu optimasi proses dengan perlakuan nisbah abu sekam padi dan silika gel (b/b), sedangkan tahap kedua yaitu optimasi proses dengan perlakuan jumlah sampel yang dilewatkan dalam kolom.
a. Penentuan nisbah abu sekam padi/silika gel optimum
Abu sekam padi sebagai adsorben bersifat kurang menjerap karotenoid dan mudah melepaskannya kembali. Sedangkan silika gel memiliki kemampuan adsorpsi terhadap senyawa karotenoid yang tinggi tetapi kemampuan desorpsinya rendah (Masni, 2004). Berdasarkan hal tersebut, maka dilakukan pencampuran abu sekam padi dan silika gel sebagai adsorben dalam kromatografi kolom dengan harapan kelemahan dari masing-masing adsorben tersebut dapat tertutupi oleh kelebihan masing-masing adsorben. Nisbah abu sekam/silika gel yang menghasilkan konsentrat dengan konsentrasi karotenoid dan tingkat pemekatan yang tinggi diseleksi melalui penerapan tiga tingkatan nisbah abu sekam padi/silika gel yaitu 35:5, 30:10, dan 25:15 (b/b). Pada proses kromatografi, sampel yang telah dilarutkan dalam eluen dimasukkan ke dalam kolom, dibiarkan terserap dalam penjerap, kemudian dielusi dengan bahan pengelusi yaitu heksana. Jumlah ekstrak yang dilewatkan dalam kolom yaitu sebanyak 1 g. Cairan yang keluar dari kolom ditampung per fraksi sampai eluat yang keluar tidak berwarna lagi dengan volume setiap fraksi adalah 3 ml (Hasanah, 2006).
b. Penentuan jumlah sampel yang dilewatkan dalam kolom optimum
Jumlah sampel yang dilewatkan dalam kolom yang menghasilkan konsentrat dengan konsentrasi karotenoid dan tingkat pemekatan yang tinggi diseleksi melalui penerapan empat tingkatan jumlah sampel yaitu 1, 2, 3, dan 4 g. Nisbah abu sekam/silika gel yang digunakan adalah nisbah abu sekam/silika gel optimum yang terpilih pada tahap sebelumnya. Produk konsentrat karotenoid selanjutnya dikarakterisasi, mencakup analisis konsentrasi karotenoid, kadar ester dan komposisi asam lemak.
C. METODE PENGAMATAN
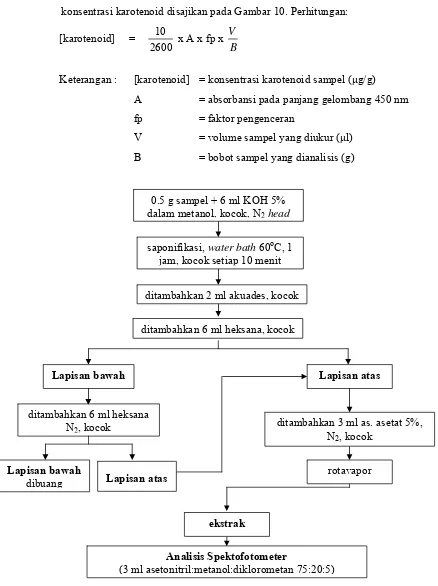
1. Analisis Kandungan Karotenoid, Metode Spektrofotometri (Parker,
1992)
Sampel sebanyak 0.5 g didispersikan dalam 6 ml KOH 5% dalam metanol di dalam tabung reaksi bertutup. Headspace diisi dengan gas nitrogen, kemudian disaponifikasi pada temperatur 60-70oC selama 1 jam di dalam penangas air dengan kondisi gelap. Setiap 10 menit dikocok dengan vortex. Setelah itu didinginkan dan ditambahkan 2 ml air bebas ion dan 6 ml heksana. Headspace diisi nitrogen, ditutup dan dikocok selama 1 menit. Kemudian di- sentrifuge, larutan bagian atas dipindahkan ke tabung reaksi yang bersih. Bagian bawah hasil ekstrak pertama diekstrak ulang dengan 6 ml heksana, di- sentrifuge dan lapisan atas ditambahkan ke ekstrak pertama.