SKRIPSI
MEMPELAJARI PROSES PEMEKATAN KAROTENOID DARI MINYAK SAWIT KASAR DENGAN
METODE FRAKSINASI BERTAHAP
Oleh:
DIAN SUKMA KUSWARDHANI F24103030
2007
FAKULTAS TEKNOLOGI PERTANIAN INSTITUT PERTANIAN BOGOR
Dian Sukma Kuswardhani. F24103030. Mempelajari Proses Pemekatan Karotenoid dari Minyak Sawit Kasar dengan Metode Fraksinasi Bertahap. Di bawah bimbingan Nur Wulandari, S.TP, M.Si..
RINGKASAN
Karotenoid merupakan salah satu komponen gizi dalam minyak sawit kasar atau crude palm oil (CPO) yang berpotensi untuk dijumput dan dibentuk menjadi produk konsentrat. Karena proses pemurnian CPO yang menggunakan panas dan bahan kimiawi merusak komponen karotenoid tersebut, diperlukan upaya penjumputan karotenoid dari CPO sebelum dilakukan pemurnian.
Tujuan penelitian ini adalah untuk mempelajari metode penjumputan karotenoid yang lebih sederhana dibandingkan dengan metode yang telah ada, yaitu dengan cara fraksinasi bertahap pada suhu rendah. Proses pemisahan karotenoid diduga dapat lebih efektif bila dibantu dengan penambahan pelarut organik dan pengadukan.
Penelitian ini terdiri dari 5 tahap, yaitu karakterisasi bahan baku CPO, penentuan waktu pengadukan, penentuan konsentrasi pelarut heksana, fraksinasi bertahap pada suhu rendah, dan perbandingan metode pengambilan fraksi cair. Parameter yang diukur meliputi konsentrasi karotenoid, recovery karotenoid, tingkat pemekatan karotenoid, rendemen konsentrat karotenoid, dan rendemen fraksi padat.
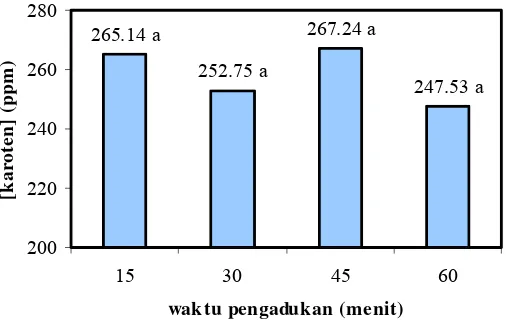
Sampel dengan perbandingan CPO : heksana 1 : 1 diaduk dengan rotary shaker pada kecepatan 200 rpm dan suhu 27°C untuk menentukan waktu pengadukan. Perlakuan waktu pengadukan 15, 30, 45, dan 60 menit tidak memberikan pengaruh nyata terhadap konsentrasi dan recovery karotenoid pekatan. Waktu yang dipilih untuk perlakuan selanjutnya adalah 15 menit.
Pada penentuan konsentrasi pelarut heksana, sampel diaduk dengan rotary shaker pada kecepatan 200 rpm dan suhu 27°C selama 15 menit. Konsentrasi pelarut heksana 0, 20, 40, 50, 55, 60, 65, 70, dan 75% memberikan pengaruh nyata terhadap recovery karotenoid pekatan. Konsentrasi pelarut heksana yang terpilih adalah 50 % (CPO : heksana = 1 : 1). Akan tetapi, konsentrasi ini ternyata tidak dapat diaplikasikan pada fraksinasi suhu rendah karena sampel mengalami pembekuan sehingga dilakukan peningkatan jumlah heksana.
Pada fraksinasi bertahap suhu rendah, jumlah heksana yang dicobakan, yaitu (CPO : heksana) 1 : 2, 1 : 3, 1 : 4, 1 : 5, dan 1 : 6. Pengaruh perbandingan CPO dan heksana terhadap hasil fraksinasi adalah dengan semakin bertambahnya jumlah heksana, maka konsentrasi karotenoid konsentrat menurun, recovery karotenoid konsentrat meningkat, tingkat pemekatan karotenoid konsentrat menurun, rendemen konsentrat meningkat, dan rendemen fraksi padat konsentrat menurun. CPO difraksinasi secara bertahap pada suhu 20, 15, 10, 5, 0, 5, dan -10°C. Pengaruh suhu fraksinasi terhadap hasil fraksinasi adalah dengan semakin rendahnya suhu fraksinasi, maka konsentrasi karotenoid konsentrat meningkat, recovery karotenoid konsentrat menurun, tingkat pemekatan karotenoid konsentrat meningkat, rendemen konsentrat menurun, dan rendemen fraksi padat konsentrat meningkat.
karotenoid paling tinggi pada suhu fraksinasi -10°C dihasilkan pada perbandingan CPO dan heksana 1 : 2 sebesar 1.46 kali dengan recovery karotenoid 17.29 % dan konsentrasi karotenoid 719.9 ppm.
INSTITUT PERTANIAN BOGOR FAKULTAS TEKNOLOGI PERTANIAN
MEMPELAJARI PROSES PEMEKATAN KAROTENOID DARI MINYAK SAWIT KASAR DENGAN
METODE FRAKSINASI BERTAHAP
SKRIPSI
Sebagai salah satu syarat untuk memperoleh gelar SARJANA TEKNOLOGI PERTANIAN pada Departemen Ilmu dan Teknologi Pangan
Fakultas Teknologi Pertanian Institut Pertanian Bogor
Oleh:
DIAN SUKMA KUSWARDHANI F24103030
2007
FAKULTAS TEKNOLOGI PERTANIAN INSTITUT PERTANIAN BOGOR
INSTITUT PERTANIAN BOGOR FAKULTAS TEKNOLOGI PERTANIAN
MEMPELAJARI PROSES PEMEKATAN KAROTENOID DARI MINYAK SAWIT KASAR DENGAN
METODE FRAKSINASI BERTAHAP
SKRIPSI
Sebagai salah satu syarat untuk memperoleh gelar SARJANA TEKNOLOGI PERTANIAN pada Departemen Ilmu dan Teknologi Pangan
Fakultas Teknologi Pertanian Institut Pertanian Bogor
Oleh:
DIAN SUKMA KUSWARDHANI F24103030
Dilahirkan pada tanggal 9 Agustus 1985 di Rembang, Jawa Tengah
Tanggal lulus : 29 November 2007
Menyetujui
Nur Wulandari, STP, Msi Dosen Pembimbing
Mengetahui,
RIWAYAT HIDUP
Nama lengkap penulis adalah Dian Sukma Kuswardhani. Anak pertama dari tiga bersaudara dari pasangan Bapak Suwaji dan Ibu Endang Kusdiningsih ini dilahirkan di Rembang, 9 Agustus 1985. Penulis mengenyam pendidikan SD Negeri Sumberjo 2 Rembang, SLTP Negeri 2 Rembang, SMU Negeri 1 Rembang, dan melanjutkan pendidikan di Departemen Ilmu dan Teknologi Pangan, Fakultas Teknologi Pertanian, IPB melalui jalur USMI.
Semasa kuliah, penulis aktif dalam organisasi dan berbagai kegiatan kemahasiswaan, di antaranya UKM Panahan (2003-2004), UKM FORCES (2004-2005), Tim Kajian Pangan Halal LDF Forum Bina Islami Fateta ((2004-2005), dan OMDA Himpunan Keluarga Rembang Bogor.
Penulis aktif dalam kegiatan Program Kreativitas Mahasiswa. Salah satu proposal PKM bidang Kemasyarakatan yang berjudul ”Peningkatan Kualitas Hidup Anak Putus Sekolah di Kelurahan Sukadamai Tanah Sareal Kota Bogor Melalui Pendidikan Berbasis Pangan” didanai oleh DIKTI. Penulis berkesempatan menjadi finalis PKM Penulisan Ilmiah pada PIMNAS XIX dengan makalah berjudul ”Fortifikasi Fe Organik dari Bayam (Amaranthus tricolor L) dalam Pembuatan Cookies untuk Wanita Menstruasi”. Penulis juga pernah menjadi asisten praktikum mata kuliah Pendidikan Agama Islam (2005) dan mata kuliah Teknologi Penyimpanan Pangan (2007).
KATA PENGANTAR
Assalamu’alaikum warahmatullahi wabarakatuh
Segala puji bagi Allah SWT yang telah memberikan berkah dan karunia-Nya sehingga penulis dapat menyelesaikan kuliah di Departemen Ilmu dan Teknologi Pangan, Fateta, IPB dan menyusun skripsi ini dengan baik. Shalawat dan salam semoga senantiasa tercurah kepada Rasulullah SAW yang menjadi teladan dan inspirasi selama ini.
Skripsi ini disusun setelah penulis melakukan kegiatan penelitian di laboratorium Laboratorium Pengembangan Produk dan Proses Pangan SEAFAST Center IPB, Laboratorium Kimia, dan Laboratorium Biokimia Departemen Ilmu dan Teknologi Pangan. Selama penelitian dan penyusunan skripsi, penulis mendapatkan bantuan dari berbagai pihak. Oleh karena itu, dalam kesempatan ini penulis mengucapkan terimakasih kepada :
1. Ibu, Bapak, Santi dan Satrio atas semua kebaikan yang tak ternilai. Tak lupa keluarga besar Samingun Hardjo Soecipto dan keluarga besar Pawiro Sarkam atas dukungannya selama ini.
2. Ibu Nur Wulandari, STP, MSi selaku dosen pembimbing akademik yang senantiasa memberikan arahan, bimbingan, dan motivasi yang sangat berarti. 3. Dr. Ir. Nuri Andarwulan, MSi. dan Dr. Ir. Nugraha Edhy Suyatma, DEA
selaku dosen penguji yang telah memberikan saran dan masukan untuk penyempurnaan skripsi ini.
4. Guru-guruku yang telah mengajariku a ba ta dan a i u (terutama Bu Rahayu Biologi, Bu Tutik Kimia, Mbak Ika Fisika yang telah banyak menginspirasi). 5. Para dosen dan staf di Departeman Ilmu dan Teknologi Pangan yang telah
banyak membantu penulis dalam menyelesaikan kuliah dan penelitian.
6. Pak Wachid, Abah (Pak Karna), Pak Rojak, Pak Koko, Pak Yahya, Pak Sobirin, Pak Mul, Pak Sidiq, Mas Edi, Bu Rubiyah, Teh Ida, Mbak Ari, Bi’ Cacih dan semua laboran ITP. Terimakasih atas bantuannya.
Ados, Nunu, Arie, Angel, Hani, Ade, Dion, Rina, Bebe. Terimakasih atas persahabatan dan dukungannya selama ini.
8. Teman-teman Kolak, Pagi Anaba 2005, Fafourty, FBI, Ramadhan’ers (M’ Ari, M’ Ummi, M’ Dhenok, M’ Lenni, M’ Siti, Anis, Uyuy, Erven, Irma), HKRB & SMANSA (Nok, Aal, Dian, Deva, Diah, Bunga, Lina), Tim PKMI (Mbak Yani dan Kak Ibot), adik-adikku (Meku, Noku, Siku), saudaraku Dewi Kurnia Sari, Nurul Nufita, dan Yossy Renggo Wardhani.
9. Pihak-pihak yang tidak dapat disebutkan satu per satu. Terimakasih yang sebesar-besarnya atas bantuan yang diberikan.
Skripsi ini tidak luput dari kekurangan dan kesalahan. Meskipun demikian penulis berharap semoga skripsi ini dapat berguna bagi semua pihak yang memerlukannya.
Bogor, Desember 2007
DAFTAR ISI
Halaman
ABSTRAK... ii
HALAMAN PENGESAHAN... iv
RIWAYAT HIDUP... vi
KATA PENGANTAR... vii
DAFTAR ISI………... ix
DAFTAR TABEL... xi
. DAFTAR GAMBAR... xii
DAFTAR LAMPIRAN... xiv
I. PENDAHULUAN... 1
A. LATAR BELAKANG... 1
B. TUJUAN... 3
C. MANFAAT... 3
II. TINJAUAN PUSTAKA... 4
A. TANAMAN SAWIT... 4
B. MINYAK KELAPA SAWIT... 5
C. ASAM LEMAK MINYAK KELAPA SAWIT... 6
D. KRISTALISASI MINYAK... 9
E. KAROTENOID... 10
1. Karakteristik Karotenoid... 10
2. Pemekatan Karotenoid... 13
F. FRAKSINASI... 15
G. PELARUT HEKSANA... 17
III. METODOLOGI PENELITIAN... 19
A. WAKTU DAN TEMPAT... 19
B. BAHAN DAN ALAT... 19
C. METODE PENELITIAN... 19
1. Karakterisasi Bahan Baku CPO... 19
2. Penentuan Waktu Pengadukan... 20
3. Penentuan Konsentrasi Pelarut Heksana... 21
4. Fraksinasi Bertahap Suhu Rendah... 23
D. METODE PENGAMATAN... 27
1. Uji Kadar Air, Metode Oven... 27
2. Bilangan Asam... 28
3. Bilangan Iod, Metode Hanus... 28
4. Analisis Kandungan Karotenoid, Metode Spektrofotometri.. 29
5. Analisis Komposisi Asam Lemak Minyak... 29
IV. HASIL DAN PEMBAHASAN... 32
A. KARAKTERISASI BAHAN BAKU CPO... 32
B. FRAKSINASI CPO... 35
1. Penentuan Waktu Pengadukan... 39
2. Penentuan Konsentrasi Pelarut Heksana... 41
3. Fraksinasi Bertahap Pada Beberapa Suhu... 45
4. Perbandingan Metode Pengambilan Fraksi Cair... 60
V. KESIMPULAN DAN SARAN………. 63
A. KESIMPULAN……… 63
B. SARAN……… 64
DAFTAR PUSTAKA……….. 65
SKRIPSI
MEMPELAJARI PROSES PEMEKATAN KAROTENOID DARI MINYAK SAWIT KASAR DENGAN
METODE FRAKSINASI BERTAHAP
Oleh:
DIAN SUKMA KUSWARDHANI F24103030
2007
FAKULTAS TEKNOLOGI PERTANIAN INSTITUT PERTANIAN BOGOR
Dian Sukma Kuswardhani. F24103030. Mempelajari Proses Pemekatan Karotenoid dari Minyak Sawit Kasar dengan Metode Fraksinasi Bertahap. Di bawah bimbingan Nur Wulandari, S.TP, M.Si..
RINGKASAN
Karotenoid merupakan salah satu komponen gizi dalam minyak sawit kasar atau crude palm oil (CPO) yang berpotensi untuk dijumput dan dibentuk menjadi produk konsentrat. Karena proses pemurnian CPO yang menggunakan panas dan bahan kimiawi merusak komponen karotenoid tersebut, diperlukan upaya penjumputan karotenoid dari CPO sebelum dilakukan pemurnian.
Tujuan penelitian ini adalah untuk mempelajari metode penjumputan karotenoid yang lebih sederhana dibandingkan dengan metode yang telah ada, yaitu dengan cara fraksinasi bertahap pada suhu rendah. Proses pemisahan karotenoid diduga dapat lebih efektif bila dibantu dengan penambahan pelarut organik dan pengadukan.
Penelitian ini terdiri dari 5 tahap, yaitu karakterisasi bahan baku CPO, penentuan waktu pengadukan, penentuan konsentrasi pelarut heksana, fraksinasi bertahap pada suhu rendah, dan perbandingan metode pengambilan fraksi cair. Parameter yang diukur meliputi konsentrasi karotenoid, recovery karotenoid, tingkat pemekatan karotenoid, rendemen konsentrat karotenoid, dan rendemen fraksi padat.
Sampel dengan perbandingan CPO : heksana 1 : 1 diaduk dengan rotary shaker pada kecepatan 200 rpm dan suhu 27°C untuk menentukan waktu pengadukan. Perlakuan waktu pengadukan 15, 30, 45, dan 60 menit tidak memberikan pengaruh nyata terhadap konsentrasi dan recovery karotenoid pekatan. Waktu yang dipilih untuk perlakuan selanjutnya adalah 15 menit.
Pada penentuan konsentrasi pelarut heksana, sampel diaduk dengan rotary shaker pada kecepatan 200 rpm dan suhu 27°C selama 15 menit. Konsentrasi pelarut heksana 0, 20, 40, 50, 55, 60, 65, 70, dan 75% memberikan pengaruh nyata terhadap recovery karotenoid pekatan. Konsentrasi pelarut heksana yang terpilih adalah 50 % (CPO : heksana = 1 : 1). Akan tetapi, konsentrasi ini ternyata tidak dapat diaplikasikan pada fraksinasi suhu rendah karena sampel mengalami pembekuan sehingga dilakukan peningkatan jumlah heksana.
Pada fraksinasi bertahap suhu rendah, jumlah heksana yang dicobakan, yaitu (CPO : heksana) 1 : 2, 1 : 3, 1 : 4, 1 : 5, dan 1 : 6. Pengaruh perbandingan CPO dan heksana terhadap hasil fraksinasi adalah dengan semakin bertambahnya jumlah heksana, maka konsentrasi karotenoid konsentrat menurun, recovery karotenoid konsentrat meningkat, tingkat pemekatan karotenoid konsentrat menurun, rendemen konsentrat meningkat, dan rendemen fraksi padat konsentrat menurun. CPO difraksinasi secara bertahap pada suhu 20, 15, 10, 5, 0, 5, dan -10°C. Pengaruh suhu fraksinasi terhadap hasil fraksinasi adalah dengan semakin rendahnya suhu fraksinasi, maka konsentrasi karotenoid konsentrat meningkat, recovery karotenoid konsentrat menurun, tingkat pemekatan karotenoid konsentrat meningkat, rendemen konsentrat menurun, dan rendemen fraksi padat konsentrat meningkat.
karotenoid paling tinggi pada suhu fraksinasi -10°C dihasilkan pada perbandingan CPO dan heksana 1 : 2 sebesar 1.46 kali dengan recovery karotenoid 17.29 % dan konsentrasi karotenoid 719.9 ppm.
INSTITUT PERTANIAN BOGOR FAKULTAS TEKNOLOGI PERTANIAN
MEMPELAJARI PROSES PEMEKATAN KAROTENOID DARI MINYAK SAWIT KASAR DENGAN
METODE FRAKSINASI BERTAHAP
SKRIPSI
Sebagai salah satu syarat untuk memperoleh gelar SARJANA TEKNOLOGI PERTANIAN pada Departemen Ilmu dan Teknologi Pangan
Fakultas Teknologi Pertanian Institut Pertanian Bogor
Oleh:
DIAN SUKMA KUSWARDHANI F24103030
2007
FAKULTAS TEKNOLOGI PERTANIAN INSTITUT PERTANIAN BOGOR
INSTITUT PERTANIAN BOGOR FAKULTAS TEKNOLOGI PERTANIAN
MEMPELAJARI PROSES PEMEKATAN KAROTENOID DARI MINYAK SAWIT KASAR DENGAN
METODE FRAKSINASI BERTAHAP
SKRIPSI
Sebagai salah satu syarat untuk memperoleh gelar SARJANA TEKNOLOGI PERTANIAN pada Departemen Ilmu dan Teknologi Pangan
Fakultas Teknologi Pertanian Institut Pertanian Bogor
Oleh:
DIAN SUKMA KUSWARDHANI F24103030
Dilahirkan pada tanggal 9 Agustus 1985 di Rembang, Jawa Tengah
Tanggal lulus : 29 November 2007
Menyetujui
Nur Wulandari, STP, Msi Dosen Pembimbing
Mengetahui,
RIWAYAT HIDUP
Nama lengkap penulis adalah Dian Sukma Kuswardhani. Anak pertama dari tiga bersaudara dari pasangan Bapak Suwaji dan Ibu Endang Kusdiningsih ini dilahirkan di Rembang, 9 Agustus 1985. Penulis mengenyam pendidikan SD Negeri Sumberjo 2 Rembang, SLTP Negeri 2 Rembang, SMU Negeri 1 Rembang, dan melanjutkan pendidikan di Departemen Ilmu dan Teknologi Pangan, Fakultas Teknologi Pertanian, IPB melalui jalur USMI.
Semasa kuliah, penulis aktif dalam organisasi dan berbagai kegiatan kemahasiswaan, di antaranya UKM Panahan (2003-2004), UKM FORCES (2004-2005), Tim Kajian Pangan Halal LDF Forum Bina Islami Fateta ((2004-2005), dan OMDA Himpunan Keluarga Rembang Bogor.
Penulis aktif dalam kegiatan Program Kreativitas Mahasiswa. Salah satu proposal PKM bidang Kemasyarakatan yang berjudul ”Peningkatan Kualitas Hidup Anak Putus Sekolah di Kelurahan Sukadamai Tanah Sareal Kota Bogor Melalui Pendidikan Berbasis Pangan” didanai oleh DIKTI. Penulis berkesempatan menjadi finalis PKM Penulisan Ilmiah pada PIMNAS XIX dengan makalah berjudul ”Fortifikasi Fe Organik dari Bayam (Amaranthus tricolor L) dalam Pembuatan Cookies untuk Wanita Menstruasi”. Penulis juga pernah menjadi asisten praktikum mata kuliah Pendidikan Agama Islam (2005) dan mata kuliah Teknologi Penyimpanan Pangan (2007).
KATA PENGANTAR
Assalamu’alaikum warahmatullahi wabarakatuh
Segala puji bagi Allah SWT yang telah memberikan berkah dan karunia-Nya sehingga penulis dapat menyelesaikan kuliah di Departemen Ilmu dan Teknologi Pangan, Fateta, IPB dan menyusun skripsi ini dengan baik. Shalawat dan salam semoga senantiasa tercurah kepada Rasulullah SAW yang menjadi teladan dan inspirasi selama ini.
Skripsi ini disusun setelah penulis melakukan kegiatan penelitian di laboratorium Laboratorium Pengembangan Produk dan Proses Pangan SEAFAST Center IPB, Laboratorium Kimia, dan Laboratorium Biokimia Departemen Ilmu dan Teknologi Pangan. Selama penelitian dan penyusunan skripsi, penulis mendapatkan bantuan dari berbagai pihak. Oleh karena itu, dalam kesempatan ini penulis mengucapkan terimakasih kepada :
1. Ibu, Bapak, Santi dan Satrio atas semua kebaikan yang tak ternilai. Tak lupa keluarga besar Samingun Hardjo Soecipto dan keluarga besar Pawiro Sarkam atas dukungannya selama ini.
2. Ibu Nur Wulandari, STP, MSi selaku dosen pembimbing akademik yang senantiasa memberikan arahan, bimbingan, dan motivasi yang sangat berarti. 3. Dr. Ir. Nuri Andarwulan, MSi. dan Dr. Ir. Nugraha Edhy Suyatma, DEA
selaku dosen penguji yang telah memberikan saran dan masukan untuk penyempurnaan skripsi ini.
4. Guru-guruku yang telah mengajariku a ba ta dan a i u (terutama Bu Rahayu Biologi, Bu Tutik Kimia, Mbak Ika Fisika yang telah banyak menginspirasi). 5. Para dosen dan staf di Departeman Ilmu dan Teknologi Pangan yang telah
banyak membantu penulis dalam menyelesaikan kuliah dan penelitian.
6. Pak Wachid, Abah (Pak Karna), Pak Rojak, Pak Koko, Pak Yahya, Pak Sobirin, Pak Mul, Pak Sidiq, Mas Edi, Bu Rubiyah, Teh Ida, Mbak Ari, Bi’ Cacih dan semua laboran ITP. Terimakasih atas bantuannya.
Ados, Nunu, Arie, Angel, Hani, Ade, Dion, Rina, Bebe. Terimakasih atas persahabatan dan dukungannya selama ini.
8. Teman-teman Kolak, Pagi Anaba 2005, Fafourty, FBI, Ramadhan’ers (M’ Ari, M’ Ummi, M’ Dhenok, M’ Lenni, M’ Siti, Anis, Uyuy, Erven, Irma), HKRB & SMANSA (Nok, Aal, Dian, Deva, Diah, Bunga, Lina), Tim PKMI (Mbak Yani dan Kak Ibot), adik-adikku (Meku, Noku, Siku), saudaraku Dewi Kurnia Sari, Nurul Nufita, dan Yossy Renggo Wardhani.
9. Pihak-pihak yang tidak dapat disebutkan satu per satu. Terimakasih yang sebesar-besarnya atas bantuan yang diberikan.
Skripsi ini tidak luput dari kekurangan dan kesalahan. Meskipun demikian penulis berharap semoga skripsi ini dapat berguna bagi semua pihak yang memerlukannya.
Bogor, Desember 2007
DAFTAR ISI
Halaman
ABSTRAK... ii
HALAMAN PENGESAHAN... iv
RIWAYAT HIDUP... vi
KATA PENGANTAR... vii
DAFTAR ISI………... ix
DAFTAR TABEL... xi
. DAFTAR GAMBAR... xii
DAFTAR LAMPIRAN... xiv
I. PENDAHULUAN... 1
A. LATAR BELAKANG... 1
B. TUJUAN... 3
C. MANFAAT... 3
II. TINJAUAN PUSTAKA... 4
A. TANAMAN SAWIT... 4
B. MINYAK KELAPA SAWIT... 5
C. ASAM LEMAK MINYAK KELAPA SAWIT... 6
D. KRISTALISASI MINYAK... 9
E. KAROTENOID... 10
1. Karakteristik Karotenoid... 10
2. Pemekatan Karotenoid... 13
F. FRAKSINASI... 15
G. PELARUT HEKSANA... 17
III. METODOLOGI PENELITIAN... 19
A. WAKTU DAN TEMPAT... 19
B. BAHAN DAN ALAT... 19
C. METODE PENELITIAN... 19
1. Karakterisasi Bahan Baku CPO... 19
2. Penentuan Waktu Pengadukan... 20
3. Penentuan Konsentrasi Pelarut Heksana... 21
4. Fraksinasi Bertahap Suhu Rendah... 23
D. METODE PENGAMATAN... 27
1. Uji Kadar Air, Metode Oven... 27
2. Bilangan Asam... 28
3. Bilangan Iod, Metode Hanus... 28
4. Analisis Kandungan Karotenoid, Metode Spektrofotometri.. 29
5. Analisis Komposisi Asam Lemak Minyak... 29
IV. HASIL DAN PEMBAHASAN... 32
A. KARAKTERISASI BAHAN BAKU CPO... 32
B. FRAKSINASI CPO... 35
1. Penentuan Waktu Pengadukan... 39
2. Penentuan Konsentrasi Pelarut Heksana... 41
3. Fraksinasi Bertahap Pada Beberapa Suhu... 45
4. Perbandingan Metode Pengambilan Fraksi Cair... 60
V. KESIMPULAN DAN SARAN………. 63
A. KESIMPULAN……… 63
B. SARAN……… 64
DAFTAR PUSTAKA……….. 65
DAFTAR TABEL
Halaman
Tabel 1. Komposisi asam lemak minyak kelapa sawit
dan minyak inti sawit... 7 Tabel 2. Beberapa jenis asam lemak dan titik cairnya... 8 Tabel 3. Beberapa jenis karotenoid dalam tanaman dan
aktivitas provitamin A-nya ... 12 Tabel 4. Metode ekstraksi dan pemekatan karotenoid... 13 Tabel 5. Residu pelarut organik yang diizinkan dalam makanan... 18
Tabel 6. Karakteristik minyak sawit kasar (CPO) yang diukur
berdasarkan beberapa parameter SNI 01-2901-1992... 32 Tabel 7. Kadar asam lemak pada CPO sampel dibandingkan
dengan literatur... 34 Tabel 8. Waktu inkubasi sampel pada berbagai konsentrasi
heksana pada suhu kamar... 42 Tabel 9. Kadar asam lemak pada konsentrat hasil fraksinasi bertahap
pada perbandingan CPO : heksana = 1 : 2 dibandingkan
DAFTAR GAMBAR
Halaman Gambar 1. Pohon dan buah sawit... 5 Gambar 2. Struktur β-karoten... 12 Gambar 3. Diagram alir penentuan waktu pengadukan... 21 Gambar 4. Diagram alir penentuan konsentrasi heksana... 22 Gambar 5. Diagram alir proses fraksinasi bertahap
(Modifikasi Mardawati, 2001)... 24 Gambar 6. Wadah fraksinasi CPO berupa erlenmeyer bertutup... 36 Gambar 7. Kenampakan fraksi cair dan fraksi padat campuran CPO :
heksana = 1 : 3 pada (a) suhu kamar dan (b) suhu -5°C... 37 Gambar 8. Fraksi cair (a) dan fraksi padat (b) minyak yang dipisahkan
setelah proses fraksinasi... 38 Gambar 9. Konsentrat karotenoid dalam minyak hasil fraksinasi... 38 Gambar 10. Konsentrasi karotenoid fraksi cair pada berbagai
waktu pengadukan... 40 Gambar 11. Recovery karotenoid fraksi cair pada berbagai waktu
pengadukan... 40 Gambar 12. Konsentrasi karotenoid fraksi cair pada berbagai
konsentrasi penambahan heksana... 43 Gambar 13. Recovery karotenoid fraksi cair pada berbagai
konsentrasi penambahan heksana... 44 Gambar 14. Fraksi padat hasil fraksinasi... 44
Gambar 15. Pengaruh perbandingan pelarut terhadap konsentrasi
karotenoid sampel pada setiap suhu fraksinasi... 47 Gambar 16. Pengaruh perbandingan pelarut terhadap recovery
karotenoid sampel pada setiap suhu fraksinasi... 49 Gambar 17. Kristal fraksi padat yang terbentuk pada fraksinasi
Gambar 18. Pengaruh perbandingan pelarut terhadap pemekatan
karotenoid sampel pada setiap suhu fraksinasi... 52 Gambar 19. Pengaruh perbandingan pelarut terhadap
rendemen fraksi cair sampel pada setiap suhu fraksinasi... 54 Gambar 20. Kenampakan konsentrat karotenoid sampel... 55 Gambar 21. Pengaruh perbandingan pelarut terhadap
rendemen fraksi padat sampel pada setiap suhu fraksinasi... 56 Gambar 22. Grafik hubungan antara suhu fraksinasi dengan persentase
Fraksi cair dan fraksi padat yang diperoleh... 58 Gambar 23. Recovery karotenoid produk pada suhu 5°C
dengan pemisahan bertahap dan langsung... 61 Gambar 24. Pemekatan karotenoid produk pada suhu 5°C
DAFTAR LAMPIRAN
Halaman Lampiran 1. Hasil analisis komposisi asam lemak CPO... 72 Lampiran 2. Pengaruh waktu pengadukan terhadap konsentrasi
dan recovery karotenoid... 75 Lampiran 3. Hasil sidik ragam konsentrasi karotenoid
fraksi cair minyak sawit pada berbagai
perlakuan waktu pengadukan... 76 Lampiran 4. Hasil sidik ragam recovery karotenoid
fraksi cair minyak sawit pada berbagai
perlakuan waktu pengadukan... 77 Lampiran 5. Pengaruh penambahan heksana terhadap konsentrasi
dan recovery karotenoid... 78 Lampiran 6. Hasil analisis sidik ragam konsentrasi karotenoid
fraksi cair minyak sawit pada berbagai
perlakuan penambahan pelarut... 79 Lampiran 7. Hasil analisis sidik ragam recovery karotenoid
fraksi cair minyak sawit pada berbagai
perlakuan penambahan pelarut... 80 Lampiran 8. Hasil analisis komposisi asam lemak fraksi cair... 81 Lampiran 9. Pengaruh suhu dan perbandingan pelarut terhadap
konsentrasi karotenoid, recovery karotenoid, tingkat pemekatan, berat konsentrat, rendemen fraksi cair,
dan rendemen fraksi padat... 84 Lampiran 10. Pengaruh metode pengambilan fraksi terhadap
recovery karotenoid dan tingkat pemekatan karotenoid... 86 Lampiran 11. Hasil analisis sidik ragam recovery karotenoid
fraksi cair minyak sawit pada pemisahan sampel
secara bertahap dan langsung... 87 Lampiran 12. Hasil analisis sidik ragam pemekatan karotenoid
fraksi cair minyak sawit pada pemisahan sampel
I. PENDAHULUAN
A. LATAR BELAKANG
Indonesia merupakan salah satu negara pensuplai kebutuhan kelapa sawit dunia. Produksi minyak kelapa sawit Indonesia pada tahun 2006 mencapai 11.3 juta ton. Besarnya produksi minyak kelapa sawit ini menjadikan Indonesia sebagai negara pengekspor minyak sawit terbesar di dunia. Pada periode tahun 2002-2005 Indonesia mengusai 67.8% ekspor dunia, sedangkan nilai ekspor Malaysia baru mencapai 20% (Pratomo dan Negara, 2007).
Hasil produksi minyak sawit di Indonesia masih lebih besar dibandingkan dengan kebutuhan domestik (Pratomo dan Negara, 2007). Sementara, industri minyak sawit di Indonesia masih didominasi oleh industri kilang minyak sawit kasar (Crude Palm Oil/CPO) dan minyak inti sawit (Palm Kernel Oil/PKO), serta produk antara berupa Refined Bleached Deodorized (RBD) palm oil dan stearin. Pengembangan industri hilir lainnya belum banyak berkembang hingga saat ini. Akibatnya, produsen kelapa sawit cenderung untuk melempar produksinya ke pasar internasional dalam bentuk komoditas primer CPO. Melihat fenomena demikian, industri kelapa sawit Indonesia perlu diperkuat melalui pengembangan produk-produk hilir minyak sawit yang memiliki nilai tambah yang lebih tinggi.
tubuh, dan dapat menurunkan atheroscleosis (D’Odorico et al., 2000; Muhilal, 1991; Murakoshi et al., 1989, Rodriguez-Amaya dan Kimura, 2004).
Karena sedemikian banyak manfaatnya, karotenoid sangat potensial untuk dijumput dan dibentuk menjadi beberapa produk, seperti minyak kaya karotenoid, konsentrat karotenoid atau zat pewarna yang aman. Di Indonesia, sebagian besar produk olahan dari karotenoid masih diimpor dan harganya relatif mahal.
Dalam proses pengolahan minyak kelapa sawit, karotenoid seringkali mengalami kerusakan dan kandungannya pada produk akhir menjadi sangat rendah. Proses pemurnian kelapa sawit yang menggunakan suhu tinggi dan bahan kimiawi lainnya, menyebabkan kerusakan karotenoid. Kehilangan karotenoid dalam proses pemurnian minyak kurang diperhatikan oleh industri pengolahan sawit karena dipengaruhi juga oleh pasar yang menginginkan minyak goreng dengan warna yang cerah (kuning pucat). Oleh karena itu, perlu dilakukan upaya penjumputan karotenoid sebelum CPO dimurnikan dan diproses menjadi produk lain.
Beberapa peneliti telah melakukan upaya untuk mendapatkan karotenoid dari minyak sawit. Metode ekstraksi karotenoid yang telah dikembangkan, antara lain metode penyabunan/saponifikasi (Sanjaya, 1996), destilasi molekuler (Ooi et al, 1994), supercritical fluid extraction (Sulaswatty, 1998), kromatografi kolom adsorpsi (Hasanah, 2006).
Olein dari crude palm oil (CPO) biasanya diperoleh melalui fraksinasi kering (dry fractionation) atau dengan perlakuan fisik menggunakan perlakuan suhu (pemanasan) dan pengadukan (Moran dan Rajah, 1994). Dengan cara ini, dapat diperoleh olein dalam jumlah cukup banyak, tetapi perlakuan panas menyebabkan kerusakan karotenoid lebih besar.
Oleh karena itu, perlu dikaji metode lain, yaitu metode solvent fractionation, yaitu fraksinasi dengan pelarut dan kristalisasi pada suhu rendah (Moran dan Rajah, 1994). Pelarut heksana digunakan untuk mengoptimalkan permisahan olein dan mengikat lebih banyak karotenoid. Fraksinasi dilakukan secara bertahap pada suhu rendah agar diperoleh konsentrat karotenoid dengan konsentrasi karotenoid yang tinggi. Olein yang ada pada konsentrat karotenoid diharapkan jumlahnya sedikit tetapi kandungan karotenoidnya tinggi (pekat), sementara itu fraksi padat dengan kandungan karotenoid yang rendah dapat diolah lagi menjadi produk turunan lemak lainnya.
B. TUJUAN
Penelitian ini bertujuan untuk:
1. Mempelajari proses penjumputan karotenoid dengan teknik fraksinasi bertahap pada suhu rendah dibantu dengan penambahan pelarut heksana dan pengadukan.
2. Menentukan kondisi optimal pemisahan karotenoid dari minyak sawit kasar dengan metode fraksinasi bertahap pada suhu rendah, untuk memperoleh konsentrat karotenoid dengan konsentrasi karotenoid dan recovery karotenoid yang tinggi.
C. MANFAAT
II. TINJAUAN PUSTAKA
A. TANAMAN SAWIT
Tanaman kelapa sawit (Elais guinensis Jacq.) adalah tanaman berkeping satu yang masuk dalam genus Elais, family Palmae, kelas divisio Monocotyledonae, sub divisio Angiospermae dengan divisio Spermatophyta. Elaeis berasal dari Elaion yang berarti minyak, dalam bahasa Yunani, guinensis berasal dari Guinea (Pantai Barat Afrika). Jacq berasal dari nama botanis Amerika yang menemukannya, yaitu Jacquine. Tanaman ini tumbuh pada iklim tropis dengan curah hujan 2000 mm/tahun dan suhu 22-32°C (Lubis, 1992 dan Harley, 1977).
Kelapa sawit mulai berbuah pada umur 3-4 tahun. Kematangan buah yang optimum adalah pada umur 15-17 minggu setelah pembuahan. Untuk memperoleh kelapa sawit yang baik, panen kelapa sawit dilakukan pada saat kadar minyak mesokarpnya maksimum dan kandungan asam lemak bebasnya minimum, yaitu saat buah mencapai tingkat kematangan tertentu yang dilihat dari warna kulit buah dan jumlah buah yang rontok tiap tandan. Kadar minyak sawit dan minyak inti sawit yang tertinggi diperoleh dari buah sawit yang berumur 16 minggu (Muchtadi, 1992 dan Ketaren, 1986).
Ada beberapa varietas tanaman sawit. Berdasarkan warna kulit buahnya, tanaman sawit dibedakan atas nigriscens (merah kehitaman), virescens (merah terang), dan albescens (hitam). Berdasarkan ketebalan tempurung dan daging buah, varietas sawit dibedakan atas dura (tebal, bentuk buah tidak teratur), delidura (tebal, bentuk buah bulat), tenera (tipis, bentuk buah bulat), dan pisivera (inti buah kecil, bentuk buah bulat) (Ketaren, 1986).
buah dengan kadar minyak sekitar 34-40%, sedangkan biji buah sawit kurang lebih 20% dari total buah sawit (Ketaren, 1986).
Gambar 1. Pohon dan buah sawit
Buah sawit dapat diolah menjadi berbagai macam produk. Produk mentahnya biasanya dalam bentuk CPO (crude palm oil) dan PKO (palm kernel oil). Produk setengah jadinya biasanya dalam bentuk oleokimia, seperti asam lemak dan gliserin serta dalam bentuk oleopangan, seperti minyak goreng, margarin, dan shortening. Sedangkan produk jadi yang biasa ditemui adalah sabun dan kosmetik (Ketaren, 1986).
B. MINYAK KELAPA SAWIT
Minyak kelapa sawit berasal dari buah tanaman kelapa sawit yang diperoleh dengan cara mengekstrak buah sawit. Kelapa sawit menghasilkan dua jenis minyak yang berlainan sifatnya, yaitu minyak yang berasal dari sabut (mesokarp) yang disebut dengan Crude Palm Oilatau CPO, dan minyak yang berasal dari inti (kernel) yang disebut Palm Kernel Oil atau PKO (Somaatmadja, 1981).
Perbedaan minyak sawit dengan minyak inti sawit adalah adanya pigmen karotenoid yang berwarna kuning merah pada minyak sawit. Perbedaan lainnya yaitu dalam kandungan asam lemaknya. Pada minyak inti sawit terdapat adanya asam kaproat dan asam kaprilat yang tidak terdapat dalam minyak sawit (Muchtadi, 1992).
a
b c
d e f
Keterangan a. pohon sawit b. tandan sawit c. epikarpium d. mesokarpium
c dan d perikarpium e. endosperm
CPO mengandung lebih kurang 1% komponen minor yang terdiri dari karotenoid, tokoferol, tokotrienol, sterol-sterol, fosfolipid dan glikolipid, terpen dan gugus hidrokarbon alifatik, dan elemen sisa (trace element) lainnya. Komponen terbesar dari karotenoid adalah -karoten dan α-karoten yang mencapai 90% dari total karotenoid yang terdiri dari 13 jenis (Ong et al.,1990). Kandungan karotenoid pada CPO sekitar 500-700 ppm (Ketaren, 1986)
Ketaren (1986) menggambarkan pengolahan minyak sawit secara umum dengan beberapa tahap, yaitu ekstraksi, pemurnian, dan winterisasi (fraksinasi). Ekstraksi adalah suatu cara untuk mendapatkan minyak atau lemak dari bahan yang diduga mengandung minyak atau lemak. Adapun cara ekstraksi yaitu rendering, mechanical expresion, dan solvent extraction.
Tujuan utama dari proses pemurnian adalah untuk menghilangkan rasa serta bau yang tidak enak, warna yang tidak menarik dan memperpanjang masa simpan minyak sebelum dikonsumsi atau digunakan sebagai bahan mentah dalam industri. Pada umumnya minyak untuk tujuan bahan pangan dimurnikan melalui tahap proses sebagai berikut: (1) pemisahan bahan berupa suspensi dan dispersi koloid dengan cara penguapan, degumming dan pencucian dengan asam; (2) pemisahan asam lemak bebas dengan cara netralisasi; (3) dekolorisasi dengan pemucatan; (4) deodorisasi; dan (5) pemisahan gliserida jenuh (stearin) dengan cara pendinginan (chilling).
C. ASAM LEMAK MINYAK KELAPA SAWIT
Minyak kelapa sawit kasar mengandung asam lemak dalam jumlah cukup besar. Asam lemak tersebut berikatan dengan gliserol membentuk gliserida (Corley, 1979). Karena asam-asam lemak terdapat 95% dari berat total molekul gliserida dan asam-asam lemak tersebut terdiri dari bagian yang reaktif, maka asam-asam lemak sangat mempengaruhi karakteristik minyak (Moolayil, 1977).
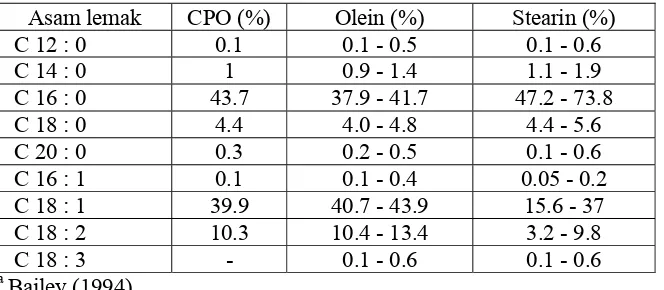
Campuran asam lemak jenuh dan tidak jenuh tersebut dapat dipisahkan dengan cara fraksinasi. Komposisi asam lemak CPO, olein dan stearin minyak sawit dapat dilihat pada Tabel 1.
Tabel 1. Komposisi asam lemak minyak kelapa sawit dan minyak inti sawita Asam lemak CPO (%) Olein (%) Stearin (%)
C 12 : 0 0.1 0.1 - 0.5 0.1 - 0.6
C 14 : 0 1 0.9 - 1.4 1.1 - 1.9
C 16 : 0 43.7 37.9 - 41.7 47.2 - 73.8
C 18 : 0 4.4 4.0 - 4.8 4.4 - 5.6
C 20 : 0 0.3 0.2 - 0.5 0.1 - 0.6
C 16 : 1 0.1 0.1 - 0.4 0.05 - 0.2
C 18 : 1 39.9 40.7 - 43.9 15.6 - 37 C 18 : 2 10.3 10.4 - 13.4 3.2 - 9.8
C 18 : 3 - 0.1 - 0.6 0.1 - 0.6
a
Bailey (1994)
Sifat fisik asam lemak tergantung pada berat molekul dan jenis ikatannya. Salah satu sifat fisik pada asam lemak adalah titik cair. Setiap asam lemak mempunyai titik cair yang berbeda-beda. Faktor yang mempengaruhi titik cair asam lemak, antara lain panjang rantai karbon, jumlah ikatan rangkap, stereoisomerisasi ikatan rangkap, posisi ikatan rangkap, percabangan asam lemak bebas, posisi asam lemak bebas dalam trigliserida, bentuk asimetrik, dan asam lemak dengan jumlah atom karbon ganjil (Walstra, 1987). Selain itu, kombinasi asam lemak dalam bentuk monogliserida, digliserida, maupun trigliserida serta isomer-isomernya juga menyebabkan variasi titik cair dari asam lemak tersebut (Ketaren, 1986).
Minyak sawit memiliki dua komponen asam lemak yang terbesar yaitu asam palmitat dan asam oleat. Asam palmitat merupakan asam lemak rantai panjang yang memiliki titik cair (melting point) yang tinggi, yaitu 64°C. Kandungan asam palmitat yang tinggi ini membuat minyak sawit lebih tahan terhadap oksidasi (ketengikan) dibanding jenis minyak lain. Asam oleat merupakan asam lemak tidak jenuh rantai panjang dengan panjang rantai C18
dan memiliki satu ikatan rangkap. Titik cair asam oleat lebih rendah dibanding asam palmitat yaitu 14°C (Ketaren, 1986). Beberapa jenis asam lemak dan titik cairnya dapat dilihat pada Tabel 2.
Tabel 2. Beberapa jenis asam lemak dan titik cairnya. Jenis Atom
Karbon
Titik cair dalam berbagai bentuk (°C) asam
lemaka
mono- gliseridab
1,3-di gliseridab
Tri- gliseridab Butyric Acid C 4 : 0 -7.9 - - -
Caproic Acid C 6 : 0 -3 - - -
Caprylic Acid C 8 : 0 16-17 - - -
Capric Acid C 10 : 0 31 - - -
Lauric Acid C 12 : 0 44-46 63 57.8 46.4 Myristic Acid C 14 : 0 58.8 70.5 66.8 57 Palmitic Acid C 16 : 0 63-64 77 76.3 63.5 Stearic Acid C 18 : 0 69-70 81.5 79.4 73.1 Oleic acid C 18 : 1 13-14 35.2 21.5 5.5 Linoleic acid C 18 : 2 -6.5 12.3 -2.6 -13.1 Linolenic acid C 18 : 3 -12.8 15.7 -12.3 -24.2 Arachidic Acid C 20 : 0 75.5 - - - Behenic Acid C 22 : 0 74-78 - - - Erucic acid C 22 : 1 33.8 - - -
Oleinc - 18-20 - - -
Stearinc - 48-50 - - -
a
Anonim (2007)
b
Johnson dan Davenport (1971)
c
Gunstone dan Norris (1983)
pelarut organik yang non polar, seperti benzena, eter, kloroform, atau heksana. Asam-asam lemak tidak jenuh lebih mudah larut dalam pelarut organik dibandingkan dengan asam lemak jenuh. Sifat kelarutan ini dapat digunakan sebagai dasar pemisahan asam lemak dengan proses kristalisasi (Fardiaz et al., 1992 dan Ketaren, 1986).
D. KRISTALISASI MINYAK
Minyak dapat mengalami kristalisasi karena penurunan suhu. Sifat ini sangat bermanfaat dalam proses fraksinasi untuk pemisahan olein dan stearin. Faktor yang mempengaruhi pembentukan kristal stearin adalah suhu awal minyak, suhu akhir fraksinasi, kecepatan pendinginan, dan metode separasi. Variabel tersebut mempengaruhi ukuran dan bentuk kristal, kecepatan filtrasi, perolehan olein dan stearin, solid fat content, titil leleh, profil asam lemak dari fraksi cair dan fraksi padat (kristal) (Breeding dan Marshall, 1995).
Mekanisme pembentukan kristal karena penurunan suhu diawali dengan melambatnya gerakan termal molekul-molekul minyak karena hilangnya panas. Kondisi ini menyebabkan jarak antara molekul-molekulnya lebih kecil. Jika jarak antara molekul tersebut mencapai 5 Å, maka akan timbul gaya tarik menarik antarmolekul yang disebut gaya Van der Waalls. Akibatnya, asam-asam lemak dalam molekul minyak akan tersusun berjajar dan saling bertumpuk serta berikatan membentuk kristal. Kristal-kristal yang terbentuk ini berbeda sifat dan titik cairnya (Winarno, 1997). Fardiaz et al. (1992) menambahkan bahwa gaya tarik menarik pada pembentukan kristal minyak tidak hanya oleh gaya Van der Waalls, tetapi juga karena adanya ikatan hidrogen. Ikatan hidrogen dapat menyebabkan molekul-molekul tertarik satu sama lain. Apabila rantai molekul minyak cukup panjang, maka daya tarik kumulatif dapat menyebabkan asam-asam lemak dalam molekul minyak berjejer secara paralel membentuk kristal.
ukuran besar-besar (25-50, kadang-kadang 100μm) dan berkelompok. Kestabilan beta intermediet ada diantara alfa dan beta, bentuk seperti jarum halus dengan ukuran 1μm (Winarno, 1997).
Proses kristalisasi mempunyai tahap yang berlanjut secara simultan. Tahap pertama adalah pembentukan partikel kecil, yang disebut dengan inti (nucleid). Pembentukan inti terjadi saat beberapa molekul lemak berkumpul membentuk agregat dan energi potensialnya turun sampai nilai minimum. Tahap kedua dalam proses kristalisasi adalah pertumbuhan inti. Inti kristal dapat tumbuh menjadi kristal bila probabilitas molekul lemak untuk teradsorpsi di permukaan inti kristal cukup besar. Semakin besar agregat yang terbentuk, semakin rendah energi potensialnya dan probabilitas untuk mengadsorpsi molekul lemak semakin besar. Minyak yang mengalami kristalisasi membentuk molekul yang rigid, beraturan, dan berbentuk tiga dimensi (Coulson dan Ricardson, 1955; Nawar, 1995; dan Fardiaz et al., 1992).
Pendinginan yang relatif cepat akan menghasilkan kristal yang transparan, rapuh, dan pipih. Keadaan ini akan menghasilkan polimorfis bentuk alfa. Pendinginan yang terlalu lama akan memperlambat pembentukan kristal yang disebabkan oleh penurunan energi potensial yang tidak secara tiba-tiba. Bentuk kristal yang dihasilkan adalah bentuk seperti jarum halus dengan bentuk polimorfis beta intermediet (Oh, et al., 1990). Kristal yang terlalu halus dan terlalu kecil dapat mengakibatkan pemisahan tidak efisien (Tirtaux, 1990).
E. KAROTENOID
1. Karakteristik Karotenoid
Karotenoid terdapat dalam kloroplas (0.5%) bersama-sama dengan klorofil (9.3%) terutama pada bagian permukaan atas daun, dekat dengan dinding sel palisade (Winarno, 1997). Karena warnanya mempunyai kisaran dari kuning sampai merah, maka deteksi panjang gelombangnya diperkirakan antara 430 – 480 nm (Schwartz dan Elbe, 1996).
Komponen karotenoid memiliki sifat penyerapan panjang gelombang tertentu. Pada pelarut yang berbeda, karotenoid akan menyerap panjang gelombang yang berbeda secara maksimum. Sifat penyerapan ini dijadikan dasar untuk menentukan jumlah karotenoid secara spektrofotometri (Simpson et al., 1987). PORIM (1995) telah menguji bahwa karotenoid minyak sawit yang dilarutkan pada heksana mempunyai serapan maksimum pada panjang gelombang 446 nm.
Menurut Meyer (1966), karotenoid dibagi atas empat golongan, yaitu: 1) karotenoid hidrokarbon, C40H56 seperti α, , dan karoten dan
likopen; 2) xantofil dan derivat karoten yang mengandung oksigen dan hidroksil antara lain kriptosantin, C40H55OH dan lutein, C40H54(OH)2; 3)
asam karotenoid yang mengandung gugus karboksil; dan 4) ester xantofil asam lemak, misalnya zeasantin.
Karotenoid termasuk senyawa lipida yang tidak tersabunkan, larut dengan baik dalam pelarut organik tetapi tidak larut dalam air (Ranganna, 1979). Menurut Meyer (1966) sifat fisika dan kimia karotenoid adalah larut dalam minyak dan tidak larut dalam air, larut dalam kloroform, benzena, karbon disulfida dan petroleum eter, tidak larut dalam dalam etanol dan metanol dingin, tahan terhadap panas apabila dalam keadaan vakum, peka terhadap oksidasi, autooksidasi dan cahaya, dan mempunyai ciri khas absorpsi cahaya.
Karotenoid lebih tahan disimpan dalam lingkungan asam lemak tidak jenuh jika dibandingkan dengan penyimpanan dalam asam lemak jenuh, karena asam lemak lebih mudah menerima radikal bebas dibandingkan dengan karotenoid. Sehingga apabila ada faktor yang menyebabkan oksidasi, asam lemak akan teroksidasi terlebih dahulu dan karotenoid akan terlindungi lebih lama (Chichester et al., 1970).
Karotenoid merupakan sumber vitamin A yang berasal dari tanaman, sedangkan yang berasal dari hewan berbentuk vitamin A. Beberapa jenis karotenoid dalam tanaman dan aktivitas provitamin A-nya disajikan dalam Tabel 3.
Tabel 3. Beberapa jenis karotenoid dalam tanaman dan aktivitas provitamin A-nyaa
Jenis Karotenoid Aktivitas provitamin A (%)
β-karoten 100
α-karoten 50-54
γ-karoten 42-50
β-zeakaroten 20-40
β-karoten-5,6-monoepoksida 21
3,4 dehidro-β-karoten 75
a
Hasanah (2006)
β-karoten sering juga disebut anti xerophtalmia karena defisiensi β -karoten dapat menimbulkan gejala rabun mata. β-karoten dalam minyak sawit selain merupakan provitamin A juga dapat mengurangi peluang terjadinya penyakit kanker, mencegah proses penuaan dini, meningkatkan imunitas tubuh, dan mengurangi terjadinya penyakit degeneratif (Muhilal, 1991; Murakoshi et al., 1989). Struktur β-karoten dapat dilihat pada Gambar 2.
Gambar 2. Struktur β-karoten
1 2
4
3 5
6 7 8 9 10 11 12 13 14
15 14’ 12’ 10’ 8’ 15’ 13’ 11’ 9’ 7’
4’ 5’
1’ 6’ 2’
3’
Gambar 2. Struktur β-karoten
1 2
4
3 5
6 7 8 9 10 11 12 13 14
15 14’ 12’ 10’ 8’ 15’ 13’ 11’ 9’ 7’
4’ 5’
1’ 6’ 2’
Tubuh manusia mempunyai kemampuan mengubah sejumlah besar -karoten menjadi vitamin A (retinal), sehingga -karoten ini disebut provitamin A. Mengkonsumsi -karoten jauh lebih aman daripada mengkonsumsi vitamin A yang dibuat secara sintetis. Pendekatan yang terbaik untuk mencegah defisiensi vitamin A adalah dengan menghimbau agar suplementasi -karoten dosis tinggi dilakukan pada diet intake (Winarno, 1997).
2. Pemekatan Karotenoid
Menurut Gross (1991), belum terdapat metode standar untuk ekstraksi karotenoid. Namun untuk mendapatkan hasil yang optimal, sebaiknya digunakan bahan yang segar, tidak rusak, dan contoh yang digunakan harus terwakili. Selain itu, ekstraksi dilakukan secepat mungkin untuk mencegah kerusakan akibat oksidasi. Karena itulah dicoba dilakukan ekstraksi sederhana dengan menggunakan teknik fraksinasi. Banyak metode lain yang sudah dilakukan untuk memperoleh konsentrat karotenoid dari minyak kelapa sawit. Diantaranya disajikan dalam Tabel 4. Tabel 4. Metode ekstraksi dan pemekatan karotenoid
Metode Keterangan Capaian Peneliti
Penyabunan
Pada CPO Pemekatan 22 kali Rahayu (1996) Pada CPO, skala
digandakan Pemekatan 54.31 kali Sanjaya (1996) Ekstraksi pelarut
Pada tomat, wortel, bayam
Taungbodithan (1998)
Pada Brassica oleraceae
Kurilich et al.
(1999) Pada brokoli,
cantaloupe, wortel, jeruk, peach, bayam, ubi jalar, tomat
Lessin, Catigani
dan Schwartz (1997) Pada buah dan
sayuran
Konings dan
Roomans (1997) Pada cabe merah,
paprika dengan aseton, oleoresin
Ittah et al. (1993)
Dengan pelarut heksana-aseton-metanol (80:10:10 v/v/v)
Burdick dan
Tabel 4. Metode ekstraksi dan pemekatan karotenoid (lanjutan)
Metode Keterangan Capaian Peneliti
Ekstraksi pelarut
Pada jaringan tanaman, dengan pelarut aseton-heksana (1:9 v/v)
Schwartz dan
Patroni (1985)
Pada limbah serat sawit, dengan pelarut heksana-aseton (10:1 v/v)
Konsentrasi produk 1283 µg/g
Masni (2004)
Pada sawit, dengan pelarut isopropanol (6:1 v/b CPO)
Meningkatkan konsentrasi dari 498 µg/g menjadi 744 µg/g
Hasanah (2006)
Adsorpsi
Pada sawit, adsorben resin sintetis (Diaion HP-20)
Tingkat recovery 40-65 %
Baharin et al. (1998) Pada sawit, adsorben bentonit:alumina (4:1) Tingkat recovery 79 %
Desai dan Dubash (1994)
Pada buah segar dan olahan, adsorben polimer sintetis
Lessin et al.
(1997) Pada sawit,
adsorben MgO2
:AlO3 (1:1)
Tingkat recovery 82.41%
Sahidin et al. ( 2001) Pada sawit,
adsorben abu sekam padi
Pemekatan 6 kali, tingkat recovery 86%
Masni (2004)
Adsorpsi berulang dengan adsorben abu sekam padi dan silika gel Pemekatan 7.44 kali, tingkat recovery 28.8% Zulkipli (2007) CME sawit,
adsorben abu sekam padi dan silika gel
Pemekatan 6 kali, tingkat recovery 70.25%
Widayanto (2007)
Pada sawit Pemekatan 15 kali, tingkat recovery 49%
Tabel 4. Metode ekstraksi dan pemekatan karotenoid (lanjutan)
Metode Keterangan Capaian Peneliti
Destilasi Molekuler
Pada metil ester Kemurnian dan hasil tinggi
Masni (2004) Bahan baku
di-metanolisis, 2 tahap destilasi molekuler
Kemurnian 75% Ooi et al. (1994)
Fluida Superkritik
T 400C, 3000-5000 psi, 4 jam
Penurunan total karotenoid 26.8%
Muchtadi (1992) Pada metil ester
sawit
Pemekatan 39 kali, tingkat recovery 42%
Sulaswatty (1998)
F. FRAKSINASI
Minyak kelapa sawit yang disimpan di tempat dingin pada suhu 5-7ºC dapat terpisah menjadi dua bagian (fraksi), yaitu fraksi cair yang disebut olein dan fraksi semi padat yang disebut stearin (Law dan Thiagarajan, 1989).
Pemisahan olein dan stearin dari CPO dapat dilakukan dengan fraksinasi. Menurut Gunstone dan Padley (1997), fraksinasi merupakan proses thermomechanical di mana bahan dasar dipisahkan menjadi dua atau lebih fraksi. Proses ini dilakukan dalam dua tahap, yaitu proses kristalisasi dengan cara mengatur kondisi suhu dan filtrasi dengan penyaringan. Breeding dan Marshal (1995) melakukan fraksinasi dengan suhu rendah dan menyaringnya dengan membran press filter. Fraksinasi asam lemak dan turunannya menggunakan teknik kristalisasi dengan suhu rendah diperkenalkan oleh Brown dan Kolb. Brown melakukan kristalisasi suhu rendah dari renatang 0°C hingga -75°C menggunakan dry ice (Fogerty, 1971).
Moran dan Rajah (1994) menyebutkan bahwa ada tiga metode yang digunakan dalam proses fraksinasi, yaitu dry fractionation, lanza fractionation, dan solvent fractionation. Dry fractionation biasanya dilakukan secara semi kontinyu terhadap minyak yang dimurnikan. Proses ini tidak membutuhkan bahan kimia atau bahan tambahan lainnya. Minyak dihomogenkan pada suhu 70°C untuk menghilangkan kristal yang telah terbentuk sebelumnya agar tidak terjadi proses yang tidak diinginkan saat pendinginan. Pembentukan dan pertumbuhan kristal terjadi pada minyak yang diaduk dan didinginkan dengan pendinginan sirkulasi air. Dry fractionation biasanya menghasilkan olein sebanyak 70-75%.
Lanza fractionation (fraksinasi deterjen) biasanya dilakukan pada minyak sawit kasar. Pertama, minyak didinginkan pada crystallizer dengan pendingin air untuk mendapatkan kristal dari gliserida dengan titik leleh tinggi. Ketika suhu yang diinginkan tercapai, massa yang mengkristal dicampur dengan larutan deterjen yang mengandung 0.5% natrium lauril sufat dan MgSO4 sebagai elektrolit. Pemisahan berlangsung dalam suspensi cair.
Kemudian dilakukan sentrifugasi agar fraksi olein dan stearin terpisah. Fraksi olein kemudian dicuci dengan air panas untuk menghilangkan sisa deterjen lalu dikeringkan dengan vaccum dryer untuk mendapatkan olein mencapai 80% (Moran dan Rajah, 1994).
Solvent fractionation merupakan fraksinasi menggunakan pelarut, dan proses ini relatif mahal karena terjadi penyusutan jumlah pelarut, memerlukan perlengkapan untuk recovery pelarut, membutuhkan suhu rendah, dan membutuhkan penanganan untuk mencegah bahaya pelarut yang digunakan. Pelarut yang biasanya digunakan adalah heksana atau aseton. Minyak harus dilarutkan dalam pelarut diikuti dengan pendinginan sehingga suhu yang diinginkan tercapai untuk mendapatkan kristal yang diinginkan. Proses ini biasanya digunakan untuk mendapatkan produk bernilai tinggi, seperti mentega coklat atau mendapatkan lemak tertentu berdasarkan titik cairnya (Moran dan Rajah, 1994).
produk sedikit tetapi kandungan karotenoidnya tinggi (pekat) sedangkan fraksi padatnya diharapkan jumlahnya lebih banyak, kandungan karotenoidnya rendah, dan dapat diolah lagi menjadi produk turunan lemak yang lain.
G. PELARUT HEKSANA
Pemilihan pelarut merupakan tahap paling penting dalam proses ekstraksi. Pertimbangan dalam pemilihan pelarut antara lain, pelarut mempunyai daya larut yang tinggi, tidak berbahaya, dan tidak beracun. Selain itu, pelarut dipilih tergantung pada titik didih yang diperlukan, mudah tidaknya terbakar, pengaruh terhadap peralatan ekstraksi, inert terhadap bahan baku, mudah didapat, dan murah harganya (Goldman, 1949). Dalam penelitian ini, dipilih heksana sebagai pelarut dalam proses fraksinasi.
Heksana merupakan campuran beberapa isomer parafin yang terdiri dari enam atom karbon (Mirghani dan Man, 2003). Heksana tergolong dalam hidrokarbon alkana (ikatan tunggal) dengan rumus kimia CH3(CH2)4CH3.
Isomer heksana yang lain, kebanyakan tidak reaktif dan sering digunakan sebagai pelarut inert dalam reaksi-reaksi organik karena sifatnya yang non polar (Institut national de recherche et de sécurité, 2005). Heksana banyak digunakan untuk mengekstrak minyak dari bahan nabati, seperti sawit dan kedelai (ATSDR, 1999).
Heksana memang beracun, tetapi tingkatnya relatif rendah. Menghirup heksana dalam konsentrasi yang tinggi akan menyebabkan efek euforia ringan yang diikuti dengan sakit kepala. Namun efek ini tidak permanen dan biasanya hilang dengan sendirinya setelah beberapa saat menghentikan kontak dengan heksana (Institut national de recherche et de sécurité, 2005). Residu heksana juga tidak terkonsentrasi pada tanaman maupun hewan sehingga tidaklah benar jika dikatakan bahwa heksana dapat menyebabkan kanker pada manusia.
menganjurkan bahwa kandungan heksana di udara dalam ruang kerja tidak lebih dari 50 ppm, sedangkan The Occupational Health and Safety Administration (OSHA) masih memberikan toleransi hingga batas 500 ppm (ATSDR, 1999). Food and Drug Administration (FDA, 1987) memberikan batasan jumlah sisa pelarut yang masih diperkenankan dalam bahan makanan yang ditunjukkan oleh Tabel 5.
Tabel 5. Residu pelarut organik yang diizinkan dalam makanana Jenis Pelarut Residu (ppm)
Aseton 30
Etilen klorida 30
Etanol 30 Heksana 25
Isopropil alkohol 50
Metilen diklorida 30
Metanol 50
a
Food and Drug Administration (1987)
III. METODOLOGI PENELITIAN
A. WAKTU DAN TEMPAT
Penelitian ini dilaksanakan selama 8 bulan mulai dari bulan Februari 2007 sampai dengan bulan September 2007. Tempat pelaksanaan penelitian ini adalah di Laboratorium Pengembangan Produk dan Proses Pangan SEAFAST Center IPB, serta Laboratorium Kimia dan Laboratorium Biokimia Departemen Ilmu dan Teknologi Pangan, FATETA IPB.
B. BAHAN DAN ALAT
Bahan baku utama yang digunakan dalam penelitian ini adalah minyak sawit kasar (CPO) yang diperoleh dari PT. Sinar Meadow, Jakarta dan pelarut heksana. Sedangkan bahan lain yang digunakan, yaitu NaOH, HCl, KI, KIO3,
natrium tiosulfat, asam oksalat, asam asetat, metanol, gas nitrogen, serta beberapa bahan kimia lainnya.
Alat yang digunakan pada penelitian ini mencakup erlenmeyer bertutup ukuran 50 ml, 100 ml, dan 250 ml; pipet volumetrik, pipet tetes, bulb, shaker, timer, neraca analitik, spektrofotometer UV-Vis, Gas Chromatography (GC), lemari pendingin, evaporator vakum berputar (rotary vacum evaporator), tabung bertutup, termometer, dan peralatan gelas lainnya.
C. METODE PENELITIAN
Penelitian ini terdiri dari 5 tahap yaitu (1) tahap karakterisasi bahan baku CPO, (2) penentuan waktu pengadukan, (3) penentuan konsentrasi pelarut heksana, (4) fraksinasi bertahap pada beberapa suhu, dan (5) perbandingan metode pengambilan fraksi cair. Selanjutnya dilakukan karakterisasi produk konsentrat karotenoid yang dihasilkan.
1. Karakterisasi Bahan Baku CPO
terkandung di dalam CPO tidak mengalami degradasi akibat proses pemurnian. Pemisahan hanya dilakukan secara fisik melalui proses fraksinasi pada suhu rendah. Sebelum dilakukan fraksinasi, bahan baku CPO dianalisis kandungan karotenoidnya dengan metode spektrofotometrik (Apriyantono et al., 1989) dan komposisi asam lemaknya dengan kromatografi gas (Gas Chromatography) (AOAC, 1995). Selain itu dianalisis juga karakteristik fisik dan kimianya, meliputi kadar air (SNI 01-3555-1998), bilangan asam (SNI 01-0019-1995), dan bilangan iod (Apriyantono et al., 1989).
2. Penentuan Waktu Pengadukan
Sebelum dilakukan proses fraksinasi terhadap CPO, terlebih dahulu ingin diketahui pengaruh pengadukan terhadap proses fraksinasi. Pengujian waktu pengadukan (shaker) dilakukan selama 15 menit, 30 menit, 45 menit, dan 60 menit. Tujuan pengadukan adalah menghomogenkan minyak dan pelarut heksana. Sampel yang digunakan untuk pengujian ini adalah sampel dengan perbandingan CPO : heksana = 1 : 1. Pengadukan (shaker) dilakukan pada suhu kamar (27°C) dan kecepatan shaker 200 rpm. Setelah itu, sampel diinkubasi pada suhu ruang sampai pemisahan fraksi cair dan fraksi padat optimal. Kondisi pemisahan dinyatakan optimal apabila tidak terdapat penambahan jumlah fraksi padat selama 24 jam. Pengukuran kadar karotenoid dilakukan dengan metode spektrofotometrik (Apriyantono et al., 1989).
Model rancangan percobaan yang digunakan adalah sebagai berikut Yij = μ + τi + εij
Dimana :
Yij = nilai hasil karakterisasi yang dilakukan pada minyak (i = 1, 2, 3, 4 dan j = 1, 2)
μ = rata-rata umum
τi = pengaruh waktu pengadukan ke-i
εij = pengaruh acak (galat) pada perlakuan ke i ulangan ke j
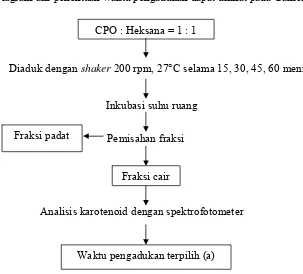
Diagram alir penentuan waktu pengadukan dapat dilihat pada Gambar 3.
3. Penentuan Konsentrasi Pelarut Heksana
Setelah diperoleh waktu yang optimal untuk mendapatkan fraksi cair dengan kandungan karotenoid tertinggi, dilakukan pengujian jumlah pelarut heksana yang dipergunakan. Pelarut heksana digunakan untuk melarutkan fraksi cair dan karotenoid sehingga lebih mudah dibebaskan
CPO : Heksana = 1 : 1
Diaduk dengan shaker 200 rpm, 27°C selama 15, 30, 45, 60 menit
Inkubasi suhu ruang Fraksi padat Pemisahan fraksi
Fraksi cair
Analisis karotenoid dengan spektrofotometer
[image:45.612.173.476.267.541.2]Waktu pengadukan terpilih (a)
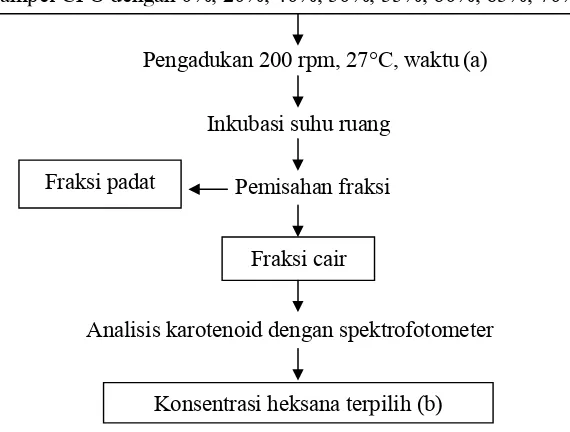
dari fraksi padat. Perlakuan konsentrasi heksana ini adalah penambahan heksana pada CPO sebesar 0%, 20%, 40%, 50%, 55%, 60%, 65%, 70%, dan 75%. Pengadukan (shaker) dilakukan pada suhu kamar (27°C) dan kecepatan shaker 200 rpm selama waktu terpilih hasil penentuan waktu pengadukan (waktu (a)). Setelah itu, sampel diinkubasi pada suhu ruang sampai pemisahan fraksi cair dan fraksi padat optimal. Kondisi pemisahan dinyatakan optimal apabila tidak terdapat penambahan jumlah fraksi padat selama 24 jam. Pengukuran kadar karotenoid dilakukan dengan metode spektrofotometrik (Apriyantono et al., 1989). Diagram alir penentuan konsentrasi heksana dapat dilihat pada Gambar 4.
Pada tahap ini, rancangan percobaan yang digunakan adalah Rancangan Acak Lengkap (RAL) satu faktor. Faktor yang dimaksud adalah persen penambahan heksana dengan tujuh perlakuan, yaitu penambahan heksana pada CPO sebesar 0%, 20%, 40%, 50%, 55%, 60%, 65%, 70%, dan 75%. Masing-masing perlakuan terdiri dari dua ulangan. Pengolahan data menggunakan uji Oneway ANOVA dari program statistik SPSS 10.0. Parameter yang digunakan untuk memilih persen penambahan heksana yang optimal adalah persen recovery karotenoid tertinggi yang
Sampel CPO dengan 0%, 20%, 40%, 50%, 55%, 60%, 65%, 70%, 75% heksana
Pengadukan 200 rpm, 27°C, waktu (a)
Inkubasi suhu ruang Fraksi padat Pemisahan fraksi
Fraksi cair
Analisis karotenoid dengan spektrofotometer
[image:46.612.174.459.299.515.2]Konsentrasi heksana terpilih (b)
terkandung dalam fraksi cair. Model rancangan percobaan yang digunakan adalah sebagai berikut
Yij = μ + τi + εij
Dimana :
Yij = nilai hasil karakterisasi yang dilakukan pada minyak (i = 1, 2, 3, 4, 5, 6, 7 dan j = 1, 2)
μ = rata-rata umum
τi = pengaruh penambahan heksana ke-i
εij = pengaruh acak (galat) pada perlakuan ke i ulangan ke j
4. Fraksinasi Bertahap Pada Suhu Rendah
Pada awal rencana penelitian, fraksinasi bertahap dilakukan terhadap sampel CPO dengan penambahan konsentrasi heksana sesuai hasil optimasi (b) diaduk pada suhu 27°C, 200 rpm, selama waktu (a) menit menggunakan shaker. Akan tetapi, pada kondisi konsentrasi heksana optimal, proses fraksinasi mengalami hambatan, yaitu terjadi pembekuan pada saat pemisahan pada suhu yang lebih rendah. Oleh karena itu, dilakukan perubahan perlakuan dengan penambahan konsentrasi heksana dengan perbandingan CPO : heksana 1 : 2, 1 : 3, 1 : 4, 1 : 5, dan 1 : 6 (gram sampel/ml heksana). Jumlah heksana ditingkatkan agar tidak terjadi lagi pembekuan pada campuran tersebut.
Sejumlah sampel ditimbang dalam erlenmeyer 250 ml bertutup yang sudah dibungkus dengan alufo. Kemudian ditambahkan sejumlah pelarut heksana dan diaduk pada suhu 27°C, kecepatan 200 rpm, selama waktu(a) menit menggunakan shaker. Berikutnya, sampel diinkubasi pada suhu 20°C sampai pemisahan fraksi cair dan fraksi padat optimal. Kondisi dinyatakan pemisahan optimal apabila tidak terdapat penambahan jumlah fraksi padat selama 24 jam. Fraksi padat dihitung jumlah dan persentasenya, sedangkan fraksi cair yang diperoleh dianalisis kandungan karotenoidnya.
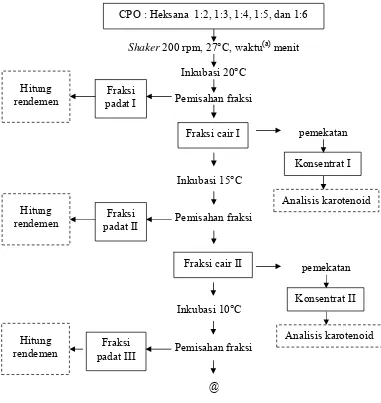
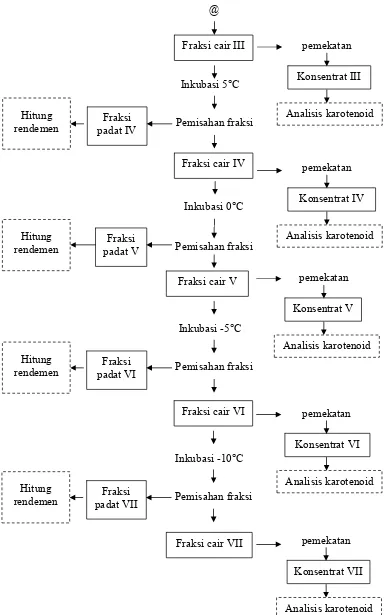
karotenoid dari fraksi cair yang dihasilkan tetap dilakukan. Fraksinasi dilanjutkan secara bertahap terhadap fraksi cair yang dihasilkan dengan tingkatan suhu fraksinasi, yaitu 10°C, 5°C, 0°C, -5°C, dan -10°C. Fraksi cair hasil fraksinasi kemudian dipisahkan dari heksana dengan dengan rotary vacum evaporator dan diukur lagi kandungan karotenoidnya. Fraksi cair dengan hasil paling baik dianalisis komposisi asam lemaknya mengunakan Gas Chromatography. Diagram alir proses fraksinasi bertahap apda suhu rendah dapat dilihat pada Gambar 5.
Inkubasi 20°C
Fraksi cair I Pemisahan fraksi Fraksi
padat I Hitung
rendemen
Shaker 200 rpm, 27°C, waktu(a) menit CPO : Heksana 1:2, 1:3, 1:4, 1:5, dan 1:6
pemekatan Konsentrat I
Analisis karotenoid Inkubasi 15°C
Pemisahan fraksi Fraksi
padat II Hitung
rendemen
Fraksi cair II pemekatan
Konsentrat II
Analisis karotenoid Inkubasi 10°C
Pemisahan fraksi Fraksi
padat III Hitung
rendemen
[image:48.612.131.512.246.649.2]@
Gambar 5. Diagram alir proses fraksinasi bertahap (Modifikasi Mardawati, 2001)(lanjutan) Inkubasi 0°C
Fraksi cair V Pemisahan fraksi Fraksi
padat V Hitung
rendemen
pemekatan Konsentrat V
Analisis karotenoid Inkubasi -5°C
Pemisahan fraksi Fraksi
padat VI Hitung
rendemen
Fraksi cair VI pemekatan
Konsentrat VI
Analisis karotenoid Inkubasi -10°C
Pemisahan fraksi Fraksi
padat VII Hitung
rendemen
Fraksi cair VII pemekatan Konsentrat VII
Analisis karotenoid Fraksi cair III pemekatan
Konsentrat III
Analisis karotenoid Inkubasi 5°C
Pemisahan fraksi Fraksi
padat IV Hitung
rendemen
Fraksi cair IV pemekatan
Konsentrat IV
Beberapa parameter yang diukur pada tahap ini dan cara penghitungannya adalah sebagai berikut :
a. Recovery karotenoid
Recovery karotenoid adalah total karotenoid CPO yang dapat diperoleh kembali setelah proses fraksinasi. Recovery karotenoid dinyatakan dalam persen.
[karotenoid] konsentrat x berat konsentrat Recovery karotenoid =
[karotenoid] CPO x berat sampel CPO
b. Pemekatan karotenoid
Pemekatan karotenoid adalah besarnya peningkatan konsentrasi karotenoid konsentrat dibandingkan dengan konsentrasi CPO awal.
[karotenoid] konsentrat Pemekatan karotenoid =
[karotenoid] sampel CPO
c. Rendemen konsentrat karotenoid
Rendemen konsentrat karotenoid adalah jumlah fraksi olein (cairan) dari CPO yang diperoleh setelah proses fraksinasi bertahap pada suhu rendah. Rendemen konsentrat karotenoid dinyatakan dalam persen.
Berat konsentrat karotenoid
Rendemen konsentrat = x 100 % Berat sampel CPO awal
d. Rendemen fraksi padat
Rendemen fraksi padat adalah jumlah fraksi stearin (padatan) dari CPO yang diperoleh setelah proses fraksinasi bertahap pada suhu rendah. Rendemen fraksi padat dinyatakan dalam persen.
Berat fraksi padat
Rendemen fraksi padat = x 100 %
Berat sampel CPO awal
5. Perbandingan Metode Pengambilan Fraksi Cair
Fraksinasi bertahap dilakukan dengan cara menurunkan suhu fraksinasi secara bertahap mulai dari suhu tinggi ke suhu yang lebih
rendah. Pada proses fraksinasi ini, dalam setiap suhu fraksinasi dilakukan pemisahan antara fraksi padat dan fraksi cair. Kemudian fraksi cair disimpan lagi pada suhu yang lebih rendah untuk difraksinasi lagi.
Pada tahap ini dilakukan fraksinasi dengan penurunan suhu secara bertahap pula, akan tetapi tidak dilakukan pemisahan fraksi cair pada setiap tingkat suhu. Fraksi cair baru dipisahkan pada suhu akhir saat fraksinasi selesai, untuk selanjutnya dianalisis dan dipekatkan. Dengan cara ini ingin di ketahui apakah konsentrat yang dihasilkan berbeda dari segi konsentrasi dan recovery karotenoidnya. Pada uji lanjutan ini, suhu akhir fraksinasi yang digunakan adalah 5oC.
Hasil yang diperoleh dengan pemisahan fraksi cair hanya di suhu akhir (pemisahan langsung) selanjutnya dibandingkan dengan hasil fraksinasi yang fraksi cainnya dipisahkan pada setiap suhu (pemisahan bertahap), dengan uji statistik ANOVA.
D. METODE PENGAMATAN
Karakterisasi produk dilakukan pada bahan baku CPO yang disesuaikan dengan beberapa syarat mutu yang terdapat pada SNI CPO, yaitu SNI 01-2901-1992. Analisis yang dilakukan, meliputi kadar air, bilangan asam, dan bilangan iod. Analisis lain yang dilakukan adalah analisis kadar karoten menggunakan metode spektrofotometri dan analisis kandungan asam lemak menggunakan gas chromatography. Sampel yang dianalisis kandungan karotenoidnya adalah sampel awal (CPO) dan konsentrat yang memberikan hasil yang terbaik. Metode analisis yang dilakukan sebagai berikut.
1. Uji Kadar Air, Metode Oven (SNI 01-3555-1998)
Kadar air (% b/b) = 100%
1 2
1 x
m m m −
Keterangan : m1 = bobot sampel awal (gram)
m2 = bobot sampel setelah pengeringan (gram)
2. Bilangan Asam (SNI 01-0019-1995)
Timbang 2 gram - 5 gram sampel ke dalam erlenmeyer 250 ml. Kemudian tambahkan 50 ml etanol 95% netral. Erlenmeyer dipanaskan di atas penangas air sampai mendidih. Sampel kemudian dititrasi dalam keadaan panas menggunakan larutan standar NaOH 0.1 N dengan menambahkan 2-3 tetes indikator phenolphtalein sehingga terbentuk warna merah muda tetap (tidak berubah selama 15 detik). Penetapan dilakukan duplo dan dilakukan perhitungan sebagai berikut :
Bilangan asam (sebagai asam palmitat, % b/b) = W VxNx2.56
Keterangan : V = Volume NaOH yang terpakai (ml) N = Normalitas aktual NaOH (N) W = Bobot sampel (gram)
3. Bilangan Iod Metode Hanus (Apriyantono et al., 1989)
Sebanyak 0.5 gram sampel minyak ditimbang dalam erlenmeyer 250 ml. Ke dalamnya kemudian ditambahkan 10 ml kloroform dan 25 ml pereaksi Hanus. Pereaksi Hanus dibuat dengan mereaksikan 13.2 gram iod dalam satu liter asam asetat dan ditambah 2 ml brom. Setelah itu, sampel disimpan dalam tempat gelap selama satu jam sambil sesekali dikocok. Setelah itu, ditambahkan 10 ml KI 15% dan dihomogenkan. Sampel kemudian dititrasi dengan larutan Na2S2O3 hingga warna kuning larutan
Bilangan iod = (m1-m2) x N x 12.69
W
Keterangan : m1 = Volume titer blanko (ml)
m2 = Volume titer sampel (ml)
N = Normalitas aktual Na2S2O3 (N)
W = Bobot sampel (gram)
4. Analisis Kandungan Karotenoid, Metode Spektrofotometri (Apriyantono et al., 1989)
Satu gram sampel, ditimbang dalam labu takar 50 ml. Kemudian ditepatkan hingga tanda tera dengan heksana. Pengenceran dilakukan bila absorbansi yang diperoleh nilainya lebih dari 0.700. Absorbansi diukur pada panjang gelombang 446 nm dengan kuvet (lebar 1 cm).
Konsentrasi karotenoid (ppm) = 10 mg/ml x A x fp x V x 1000 E1% 1 cm x W
Keterangan : A = nilai serapan sampel pada 446 nm fp = faktor pengenceran
V = volume sampel yang diukur W = bobot sampel yang dianalisis
E1% 1 cm = koefisien absorbansi
Konsentrasi karotenoid dalam sampel minyak sawit dihitung menggunakan nilai E1% (1 cm) = 2611, yaitu absorbansi dari 1% larutan karotenoid dari minyak sawit (10 mg/ml atau μg/μl) pada panjang gelombang 446 nm menggunakan kuvet 1 cm dengan pelarut heksana (PORIM, 1995)
5. Analisis Komposisi Asam Lemak Minyak (AOAC, 1995)
air yang mendidih (suhu air sekitar 100oC) selama 5 menit, diikuti dengan pendinginan sampai suhu campuran berada pada kisaran suhu 30-40°C. Pereaksi BF3-metanol 14% (b/v) segera ditambahkan ke dalam campuran, dialiri gas nitrogen dan ditutup rapat, kemudian dipanaskan kembali dalam penangas air mendidih selama 30 menit. Campuran didinginkan kemudian ditambahkan 1 ml heksana, dialiri gas nitrogen, ditutup rapat dan dikocok selama 30 detik. Campuran yang dihasilkan selanjutnya ditambahkan 5 ml larutan NaCl jenuh, dihembus gas nitrogen, ditutup rapat dan dikocok. Lapisan heksana dipindahkan ke dalam vial, fase metanol-air diekstrak kembali dengan 1 ml heksana dan hasil ekstraksi digabungkan serta disaring dengan Na2SO4 anhidrat dan telah dipekatkan dengan gas nitrogen
sampai diperoleh volume sekitar 1 ml.
Metil ester asam lemak yang telah dibebaskan dari kandungan air dengan Na2SO4 anhidrat dan telah dipekatkan dengan gas nitrogen,
sebanyak 1 μl disuntikkan ke alat kromatografi gas. Alat kromatografi dilengkapi dengan FID, integrator chromatopac C-R6 dan kolom kapiler DB-23 (30 m x 0,25 mm: J & W Scientific, Folson, CA). Suhu injektor diatur 250oC dan suhu detektornya 260oC. Suhu awal kolom 140oC yang dipertahankan selama 6 menit dengan laju kenaikan suhu 30oC/menit. Suhu akhir kolom diatur 230oC dan dipertahankan selama 25 menit. Gas pembawa yang digunakan adalah gas helium dengan tekanan 1 kg/cm2 dan detektor FID. Tekanan gas hidrogen dan tekanan udara diatur sampai 0.5 kg/cm2. Kromatogram yang diperoleh digunakan untuk menentukan persentase komposisi asam lemak menggunakan persamaan :
a) Penentuan respon faktor (Rf) standar asam lemak:
Area standar internal mg asam lemak X
Rf = x
mg standar internal area asam lemak b) Penentuan kadar asam lemak sampel
WSI (mg) Rf x area X
[asam lemak] (mg/100g) = x
Wminyak (100 g) Area SI
WSI = bobot asam lemak standar internal (SI) yang ditambahkan (mg)
Wminyak = bobot minyak yang dimetilasi (100 gram)
c) Penentuan persen asam lemak
Bobot asam lemak
IV. HASIL DAN PEMBAHASAN
Pembuatan konsentrat karotenoid dari minyak sawit kasar (crude palm oil/CPO) dengan menggunakan teknik fraksinasi bertahap diupayakan melalui 5 tahap, yaitu (1) Karakterisasi bahan baku, (2) Penentuan waktu pengadukan, (3) Penentuan konsentrasi pelarut heksana, dan (4) Fraksinasi bertahap pada beberapa suhu, dan (5) Perbandingan metode pengambilan fraksi cair.
Karakterisasi bahan baku CPO meliputi analisis kadar air, bilanga