OPTIMASI PENINGKATAN KONSENTRASI
KARBONDIOKSIDA (CO2) TERHADAP PERTUMBUHAN DAN POPULASI Chaetoceros sp SKALA LABORATORIUM
NASIRUDDIN
PROGRAM STUDI BUDIDAYA PERAIRAN FAKULTAS PERTANIAN
UNIVERSITAS MUHAMMADIYAH MAKASSAR
2013
i
OPTIMASI PENINGKATAN KONSENTRASI KARBONDIOKSIDA (CO2) TERHADAP PERTUMBUHAN DAN POPULASI Chaetoceros sp
SKALA LABORATORIUM
SKRIPSI
NASIRUDDIN 105 94 281 08
Sebagai Salah Satu Syarat Untuk Memperoleh Gelar Sarjana Perikanan Pada Program Studi Budidaya Perairan Fakultas Pertanian
Universitas Muhammadiyah Makassar
PROGRAM STUDI BUDIDAYA PERAIRAN FAKULTAS PERTANIAN
UNIVERSITAS MUHAMMADIYAH MAKASSAR
2013
ii
OPTIMASI PENINGKATAN KONSENTRASI KARBONDIOKSIDA (CO2) TERHADAP PERTUMBUHAN DAN POPULASI Chaetoceros sp
SKALA LABORATORIUM
Nama : NASIRUDDIN
NIM : 105 94 281 08
Program Studi : Budidaya Perairan Fakultas : Pertanian
Telah Diperiksa dan Disetujui
Komisi Pembimbing
Pembimbing Utama Pembimbing Anggota
(Sahabuddin, S.Pi., M.P) (Ir. Andi Khaeriyah, M.Pd)
Diketahui
Dekan Ketua Program Studi
Fakultas Pertanian Budidaya Perairan
( Ir. H. Saleh Molla, M.M) (Murni, S.Pi., M.Si)
Tanggal Pengesahan :...
iii
HALAMAN PERNYATAAN KEASLIAN
Yang bertanda tangan di bawah ini :
NAMA : NASIRUDDIN
NIM : 105 94 281 08
Program Studi : Budidaya Perairan
Menyatakan dengan sebenarnya bahwa skripsi yang saya tulis ini benar-benar merupakan hasil karya saya sendiri, bukan merupakan pengambilalihan tulisan atau pemikiran orang lain. Apabila dikemudian hari terbukti atau dapat dibuktikan bahwa sebagian atau keseluruhan skripsi ini hasil karya orang lain, saya bersedia menerima sanksi atas perbuatan tersebut.
Makassar, November 2013
Nasiruddin
iv ABSTRAK
NASIRUDDIN. Optimasi Peningkatan Konsentrasi Karbondioksida (CO2) Terhadap Pertumbuhan dan Populasi Chaetoceros sp Skala Laboratorium.
Dibimbing oleh Sahabuddin dan Andi Khaeriyah.
Plankton adalah pakan alami yang utama bagi larva ikan, crustacea seperti udang serta merupakan salah satu faktor pembatas bagi organisme budidaya.
Plankton di kelompokkan atas fitoplankton dan zooplankton. Fitoplankton dibedakan atas fitoplankton coklat (brown algae) dan fitoplankton hijau (green algae). Pakan ini hidup bebas diberbagai perairan, baik perairan tawar, payau maupun laut dan mampu berkembang dengan secara cepat. Pemberian plankton dalam jumlah besar pada larva tidak memungkinkan dilakukan dengan penangkapan atau penyaringan air laut bebas mengingat ketersediaannya di alam sangat terbatas dan membutuhkan waktu yang cukup lama sehingga tidak efisien.
Oleh karena itu, perlu dilakukan budidaya atau kultur plankton untuk mendapatkan plankton dalam jumlah besar.
Penelitian ini bertujuan untuk menentukan Optimasi Peningkatan Konsentrasi Karbondioksida (CO2) Terhadap Pertumbuhan dan Populasi Chaetoceros sp Skala Laboratorium. Sedangkan kegunaannya adalah sebagai bahan informasi bagi usaha pembenihan dalam menyediakan pakan alami.
Penelitian dimulai tahap persiapan alat dan bahan, uji perlakuan dan pelaksanaan penelitian berlangsung dari Bulan Desember 2012 sampai Bulan Mei 2013. Bertempat di Balai Penelitian dan Pengembangan Budidaya Air Payau (BPPBAP) Maros, Lingkungan Marampesu, Kelurahan Boribellaya, Kecematan Turikale, Kabupaten Maros. Perlakuan yang diujikan adalah sebagai berikut:
Perlakuan Konsentrasi Karbondioksida (CO2) 385 ppm, (CO2) 750 ppm, (CO2)1000 ppm selama 9 hari. Selama penelitian berlangsung dilakukan pengamatan sel Chaetoceros sp.
Dari hasil penelitian tersebut bahwa diantara ketiga perlakuan kosentrasi karbondiokasida (CO2) mendapatkan hasil yang terbaik untuk pertumbuhan dan populasi Chaetoceros sp yakni kosentrasi karbondiokasida (CO2) 385 ppm.
Kata Kunci: Kultur algae, Konsentrsasi (CO2) 385 ppm, (CO2)750 ppm, (CO2)1000 ppm, Skala Laboratorium.
v
KATA PENGANTAR
Assalamu’alaikum Wr.Wb.
دـعب اما .نيعمجا هبحصو هـلا ىلعو , نيلسرملاو ءايــبنلأا فرشا ىلع م لاـسلاو ة لاصلاو نيـملاعلا بر لله دمحلا Segala puji syukur dan kehadirat Allah SWT dengan Rahmat dan Magfirah-Nya serta salawat serta salam teruntuk Nabi sepanjang zaman, Nabi Muhammad SAW. Atas Ridho dan doa yang disertai dengan usaha yang semaksimalnya setelah melalui proses yang panjang dan melelahkan akhirnya skripsi ini dapat diselesaikan.
Keberadaan skripsi ini bukan sekedar persyaratan formal bagi mahasiswa untuk mendapat Gelar Sarjana tetapi lebih dari itu merupakan wadah pengembangan ilmu yang didapat dibangku kuliah dan merupakan kegiatan penelitian sebagai unsur Tri Darma Perguruan Tinggi. Dalam mewujudkan ini, penulis memilih judul “OPTIMASI PENINGKATAN KONSENTRASI KARBONDIOKSIDA (CO2) TERHADAP PETUMBUHAN DAN POPULASI Chaetoceros sp SKALA LABORATORIUM” Semoga kehadiran Skripsi ini dapat memberi informasi terhadap pihak-pihak yang menaruh minat pada masalah ini.
Dalam mengisi hari-hari kuliah dan penyusunan skripsi ini, penulis telah banyak mendapat bantuan, motivasi dan bimbingan dari berbagai pihak. Untuk itu patut kiranya diucapkan terima kasih yang tulus dan penghargaan kepada :
vi
1. Penghormatan dan terima kasih yang sebesar-besarnya kepada kedua orang tua yaitu Ayahanda H. HASANUDDIN dan Ibunda HJ HARYANI tercinta yang dengan penuh kasih sayang, pengertian dan iringan doa-nya telah mendidik dan membesarkan serta mendorong penulis hingga sekarang menjadi seperti ini.
2. Bapak Dr. Irwan Akib, M.Pd selaku Rektor Universitas Muhammadiyah Makassar.
3. Bapak Ir. H. M. Saleh Molla, M.M selaku Dekan Fakultas Pertanian.
4. Bapak Sahabuddin, S.Pi., M.P selaku pembimbing I yang telah banyak memberikan bimbingan dan mengarahkan penulis dalam perampungan penulisan skripsi ini.
5. Ibu Ir. Andi Khaeriyah, M.Pd selaku pembimbing II yang juga telah banyak meluangkan waktunya untuk memberi bimbingan kepada penulis sejak persiapan penelitian hingga selesainya skripsi ini.
6. Para Bapak dan Ibu dosen serta seluruh karyawan (i) Fakultas Pertanian Universitas Muhammadiyah Makassar yang telah memberikan pelayanan yang berguna dalam penyelesaian studi pada Fakultas Pertanian Universitas Muhammadiyah Makassar.
7. Seluruh dosen pada Universitas Muhammadiyah Makassar terima kasih atas bantuan dan bekal disiplin ilmu pengetahuan selama menimba ilmu di bangku kuliah.
8. Tidak terkecuali semua rekan-rekan Mahasiswa khususnya Fakultas pertanian dan semua pihak yang tidak mungkin penulis sebutkan satu
vii
persatu, yang telah banyak memberikan bantuannya, baik moril maupun materil dalam penyelesaian skripsi ini.
Akhirnya dengan segala kerendahan hati, penulis mengharapkan semoga skripsi ini dapat bermanfaat bagi semua pihak terutama bagi penulis sendiri.
Wassalam
Makassar, ………. 2013
Nasiruddin
viii DAFTAR ISI
Halaman
Halaman Judul i
Halaman Pengesahan ii
Halaman Pernyataan Keaslian Skripsi iii
Abstrak iv
Kata Pengantar v
Daftar Isi viii
Daftar Tabel x
Daftar Gambar xi
Daftar Lampiran xii
I. PENDAHULUAN 1
1.1 Latar Belakang 1
1.2 Tujuan dan Kegunaan 3
II. TINJAUAN PUSTAKA 4
2.1 Klsifikasi dan Ciri Morfologis 4
2.2 Reproduksi 5
2.3 Pertumbuhan 6
2.4 Konsentrasi Karbondioksida (CO2) 8 2.5 Faktor – Faktor Yang Mempengaruhi Fitoplankton 9
2.6 Pertumbuhan Populasi 12
III. METODE PENELITIAN 14
3.1 Waktu dan Tempat 14
ix
3.2 Organisme Uji 14
3.3 Bahan dan Alat 14
3.4 Prosedur Penelitian 17
3.5 Perlakuan dan Rancangan Percobaan 18
3.6 Pengukuran Kualitas Air 21
3.7 Analisis Data 21
IV. HASIL DAN PEMBAHASAN 22
4.1 Pertumbuhan Populasi Chaetoceros sp 22
4.2 Parameter Kualitas Air 26
V. PENUTUP 28
5.1 Kesimpulan 28
5.2 Saran 28
VI. DAFTAR PUSTAKA 29
VII. LAMPIRAN 32
VIII. RIWAYAT HIDUP 41
x
DAFTAR TABEL
Halaman
1. Bahan yang digunakan dalam penelitian 14
2. Jenis alat dan kegunaannya dalam penelitian 15 3. Parameter Kualitas Air yang Diukur 21 4. Data kepadaan Pertumbuhan Chaetoceros sp 22
5. Parameter kualitas air 26
xi
DAFTAR GAMBAR
Halaman
1. Morfologi Chaertoceros sp 4
2. Tata letak unit penelitian 19
3. Laju pertumbuhan Chaetoceros sp perlakuan CO2 385 ppm 24 4. Laju pertumbuhan Chaetoceros sp perlakuan CO2 750 ppm 25 5. Laju pertumbuhan Chaetoceros sp perlakuan CO2 1000 ppm 25
6. Diagram Kepadatan 26
xii
DAFTAR LAMPIRAN
Halaman
1. Foto-foto kegiatan selama penelitian berlangsung 32
1
PI. PENDAHULUAN 1.1. Latar Belakang
Pengembangan usaha budidaya ikan dan non ikan akhir-akhir ini semakin giat dilaksanakan baik itu secara ekstensif, semi intensif maupun intensif. Usaha pengembangan budidaya, tentunya tidak terlepas dari kegiatan pembenihan yang selama ini menjadi faktor pembatas dalam pengembangan usaha budidaya di Indonesia. Faktor ketersediaan benih baik dari segi jumlah, kualitas maupun kesinambungan merupakan penyebabnya. Selain ketiga faktor tersebut diatas, ketersediaan pakan baik pakan alami maupun pakan buatan juga merupakan salah satu faktor yang menjadi kendala mengapa selama ini usaha budidaya khususnya kegiatan pembenihan tidak berjalan secara optimal.
Pakan alami merupakan unsur terpenting dalam menunjang pertumbuhan dan kelangsungan hidup organisme yang dibudidaya khususnya pada fase larva atau benih. Pakan alami disini mencakup fitoplankton dan zooplankton yang berperan sebagai sumber karbohidrat, lemak, protein dengan susunan asam amino yang lengkap serta mineral yang berperan dalam pertumbuhan larva atau benih ikan. Lebih lanjut dijelaskan bahwa fitoplankton sangat berperan dalam keberhasilan pemeliharaan larva pada unit pembenihan, karena pada umumnya stadia awal pemeliharaan larva baik ikan maupun non ikan menggunakan pakan dari jenis fitoplankton.
2
Dewasa ini telah berhasil dikultur beberapa spesies fitoplankton yang digunakan sebagai pakan larva diantaranya Chlorella sp, Skeletonema costatum, Chaetoceros sp, Tetraselmis dan Isochrysis. Salah satu jenis fitoplankton yang umumnya dibudidayakan sebagai pakan alami terutama untuk larva udang vannamei (litopenaeus vannamei) adalah Chaetoceros sp, (Yunus, 1992). Chaetoceros sp, banyak digunakan sebagai pakan alami pada unit-unit pembenihan karena disamping memiliki kandungan protein yang cukup tinggi, pada kondisi lingkungan yang cocok kepadatan dari pakan alami ini cepat meningkat. Kandungan nutrisi dari Chaetoceros sp, yaitu protein 35%, lemak 6,9%, karbohidrat 6,6% dan kadar abu 28% (Isnansetyo dan Kurniastuty, 1995).
Chaetoceros sp mempunyai lebih dari 160 spesies dan merupakan genus terbesar dari kelas Bacillariophyceae. Mikro alga ini hidup di perairan dingin sampai perairan panas dan merupakan plankton neritik yang mempunyai setae. Mikro alga tersebut membentuk koloni dengan sel-sel terikat dengan setae yang panjang membentuk filament (Lee, 1980).
Fitoplankton secara umum membutuhkan faktor-faktor pendukung untuk membantu proses pertumbuhannya. Faktor-faktor tersebut antara lain suhu, intensitas cahaya dan CO2 (Fogg, 1965). Permasalahan yang timbul pada setiap kultur alga diantaranya adalah populasi alga yang tidak stabil dalam setiap panennya bahkan cendrung mengalami drop sehingga ketersediaannya berkurang dan tidak kotinu lagi.
Hal ini disebabkan faktor-faktor pendukung pertumbuhannya kurang optimal, dalam
3
hal ini adalah CO2. Oleh karena itu, diperlukan kandungan CO2 yang memadai pada media kulturnya selain dari nutriennya.
1.2. Tujuan dan Kegunaan
Tujuan dari penelitian ini adalah untuk menentukan Optimasi Peningkatan Konsentrasi Karbondioksida (CO2) Terhadap Pertumbuhan dan Populasi Chaetoceros sp Skala Laboratorium. Sedangkan kegunaan dari penelitian ini adalah sebagai bahan informasi awal tentang konsentrasi karbondioksida (CO2) pada media kultur yang memberikan pertumbuhan optimal untuk pengembangan budidaya Chaetoceros sp sebagai pakan alami.
4
II. TINJAUAN PUSTAKA
2.1. Klasifikasi dan Ciri Morfologis
Klasifikasi Chaetoceros sp menurut Bougis (1979) dalam Sudjiharno (2002) adalah sebagai berikiut :
Divisi : Bacillariophyta Kelas : Bacillariophyceae Ordo : Centrales
Sub Ordo : Biddulphiinae Famili : Chaetoceraceae Genus : Chaetoceros Species : Chaetoceros sp
Gambar 1. Morfologi Chaetoceros sp.
Diatom merupakan organisme/ganggang bersel tunggal yang tergolong dalam divisi Bacillariophyta, ganggang jenis ini memiliki dua ordo yakni centrales dan pennales. Kedua ordo ini dapat dibedakan berdasarkan bentuk fisik tubuh dan habitanya. Diatom dari ordo centrales memiliki ciri bentuk tubuh silinder dan hidup
5
di air laut sedangkan ordo pennales memiliki bentuk tubuh lonjong dan hidup di air tawar. Chaetoceros sp, merupakan diatom dari ordo centrales (Bachtiar, 2003).
Chaetoceros sp, ada yang memiliki bentuk tubuh bulat dengan ukuran tubuh yang sangat kecil yakni berkisar antara 4-6 mikron dan ada yang berbentuk segi empat dengan ukuran 8-12 dan 7-18 mikron. Sama seperti diatom pada umumnya, Chaetoceros sp memiliki dinding sel yang dibentuk dari silika (Isnansetyo dan Kurniastuty, 1995). Lebih lanjut ditambahkan oleh Sumeru dan Anna (2005), bahwa pada setiap sel Chaetoceros sp dipenuhi oleh cytoplasma.
Menurut Isnansetyo dan Kurniastuty (1995) bahwa Chaetoceros sp, merupakan diatom yang bersifat eurythermal dan euryhaline. Daerah penyebarannya meliputi muara sungai, pantai dan laut pada daerah tropis dan subtropis. Diatom ini dapat hidup pada kisaran suhu yang tinggi, pada suhu air 400C fitoplankton ini masih dapat bertahan hidup namun tidak berkembang. Pertumbuhan optimumnya memerlukan suhu pada kisaran antara 25-300C. Salinitas optimal untuk pertumbuhan optimal dari Chaetoceros sp adalah 17-25 ‰. Selanjutnya dikemukakan bahwa seperti halnya fitoplankton pada umumnya, pertumbuhan dari Chaetoceros sp ini juga dipengaruhi oleh intensitas cahaya.
2.2. Reproduksi
Chaetoceros sp bereproduksi secara aseksual yakni dengan pembelahan sel dan seksual dengan pembentukan auxospora, silikat memiliki peranan penting dalam proses reproduksi fitoplankton ini sebagai bahan pembentuk cangkang. Pembelahan
6
sel pada diatom ini sama seperti pembelahan sel diatom pada umumnya, dimana satu sel induk yang membelah akan menghasilkan dua sel anak. Satu sel anak mendapatkan tutup kotak (epiteka) akan berkembang menyerupai ukuran sel induknya, sedangkan sel anak yang mendapatkan dasar kotak (hipoteka) akan tumbuh lebih kecil dari sel induk. Pembelahan sel ini akan terus berlanjut sampai ukuran sel semakin kecil (Djarijah, 2006).
Menurut Isnansetyo dan Kurniastuty (1995), pembelahan sel Chaetoceros sp yang dilakukan secara terus menerus akan menyebabkan ukuran sel menjadi semakin kecil dan sampai batas ukuran tertentu, pembelahan sel ini akan berhenti sebentar dan berganti menjadi reproduksi secara seksual melalui pembentukan auxospora dimana isi sel (sel anak) akan keluar dari cangkang dan akan tumbuh membesar hingga ukurannya sama dengan ukuran sel induk semula dan kemudian sel ini akan melakukan reproduksi secara aseksual kembali yakni melalui pembelahan sel.
2.3 Pertumbuhan
Menurut Effendie (1997), bahwa pertumbuhan dipengaruhi oleh beberapa faktor baik itu faktor yang berasal dari individu itu sendiri maupun berasal dari faktor luar atau faktor lingkungan. Faktor dalam umumnya adalah yang sulit dikontrol seperti keturunan, sex, umur, parasit dan penyakit, sedangkan faktor luar meliputi makanan dan lingkungan perairan. Serta kekeruhan yang tinggi mengakibatkan pertumbuhan organisme yang menyesuaikan diri pada air yang jernih menjadi
7
terhambat dan dapat pula menyebabkan kematian karena mengganggu proses respirasi (Hutagalung et al., 1997).
Cahyaningsih, dkk (2005), menyatakan bahwa selama masa inkubasi fitoplankton mengalami proses pertumbuhan yang di bagi menjadi 4 fase yaitu :
1. Fase Adaptasi 2. Fase Logaritmik 3. Fase Stasioner 4. Fase Kematian - Fase Adaptasi
Disebut juga lag fase yakni pada fase ini sel melakukan adaptasi terhadap lingkungannya dan mulai melakukan metabolisme namun belum terjadi pertambahan sel.
- Fase Logaritmik/eksponensial
Fase ini merupakan fase dimana pertumbuhan fitoplankton terjadi dengan cepat sehingga terjadi pertambahan jumlah sel yang sangat signifikan.
- Fase Stasioner
Fase stasioner atau yang sering disebut fase pertumbuhan tetap ialah fase dimana laju reproduksi seimbang dengan laju kematian. Fase ini merupakan puncak pertumbuhan populasi fitoplankton.
- Fase Kematian
Fase kematian ialah fase dimana laju pertumbuhan lebih kecil dari pada laju kematian, karena disebabkan oleh penurunan kemampuan metabolisme dari fitoplankton.
8 2.4. Konsentrasi Karbondioksida (CO2)
Karbondioksida merupakan unsur utama dalam proses fotosintesis yang dibutuhkan oleh fitoplankton dan tumbuhan air. Keberadaan karbondioksida diperairan sangat dibutuhkan oleh tumbuhan baik yang besar maupun yang kecil untuk proses fotosintesis (Kordi, 2004). Oleh karena itu, perbedaan perlakuan konsentrasi karbondioksida (CO2) tersebut dikarenakan untuk menjadikan suatu bahan percobaan dalam hal untuk mengetahui atau membandingkan pengaruh pertumbuhan terhadap kepadatan, produksi proses fotosintesis, dan perubahan kualitas air dalam membudidayakan pakan alami utamanya Chaetoceros sp.
Karbondioksida (CO2) merupakan salah satu parameter kimia yang sangat menentukan dalam kegiatan budidaya organisme. Karbondioksida yang dianalisis dalam kegiatan budidaya adalah karbondioksida dalam bentuk gas yang terkandung di dalam air. Gas karbondioksida (CO2) memegang peranan sebagai unsur makanan bagi semua tumbuhan yang mempunyai chlorophil, baik tumbuh-tumbuhan renik maupun tumbuhan tingkat tinggi.
Tinggi dan rendahnya suatu karbondioksida (CO2) dalam perairan tidak lepas dari pengaruh parameter lain seperti oksigen, alkalinitas, kesadahan, suhu, cahaya dan sebagainya. Di mana semakin tinggi karbondioksida, maka oksigen yang diperlukan bertambah. Konsentrasi karbondioksida (CO2) sangat erat hubungannya dengan konsentrasi oksigen terlarut dalam perairan, karena kandungan karbondioksida
9
mempunyai konsentrasi yang hampir sama dengan konsentrasi oksigen terlarut (Soeyasa, 2001).
Untuk melakukan proses fotosintesis, alga membutuhkan karbondioksida yang merupakan gas yang bersifat asam, tidak berbau, tak terasa, tidak berwarna, tidak beracun, tidak terbakar, dan tidak meninggalkan sisa endapan (Jalil, 1989 dalam Nainggolan, 1993). Karbondioksida adalah sumber karbon yang lebih disukai oleh tumbuhan akuatik seperti alga dibandikan bikarbonat dan karbonat. Bikarbonat sebenarnya dapat dijadikan sebagai sumber karbon akan tetapi didalam kloroplas, bikarbonat dikonversi menjadi karbondiksida dengan bantuan enzim karbonik anhidrase (Boney, 1989 dalam Effendi 2003).
2.5. Faktor-faktor yang Mempengaruhi Pertumbuhan Fitoplankton a. Suhu
Suhu merupakan salah satu faktor fisik yang sangat menentukan tingkat kulaitas air suatu perairan khususnya media budidaya. Suhu secara tidak langsung merupakan faktor pembatas bagi organisme yang dibudidayakan. Baik suhu tinggi maupun suhu rendah mempengaruhi pertumbuhan dari organisme yang dibudidaya (Lesmana, 2005). Lebih lanjut ditambahkan bahwa suhu lingkungan sangat mempengruhi metabolisme organisme.
Suhu memberikan peranan penting dalam kultur fitoplankton, karena sangat mempengaruhi aktifitas enzim dalam metabolisme sel (Graffith, 1983 dalam Nurliati,
10
1995). Selanjutnya dikemukakan bahwa semua spesies Chaetoceros sp toleran terhadap suhu tinggi.
Menurut Cahyaningsih, dkk (2005), Chaetoceros sp toleran terhadap suhu tinggi. Pada suhu 40 0C spesies ini dapat hidup tetapi tidak dapat berkembang.
Chaetoceros sp tumbuh normal pada kisaran suhu 20 – 30 0C dan tumbuh optimum pada kisaran suhu 25 – 30 0C.
b. Derajat keasaman (pH)
Menurut Kordi (2004) pH air mempengaruhi tingkat kesuburan perairan karena mempengaruhi kehidupan jasad renik. Perairan asam akan kurang produktif pada pH rendah (keasaman tinggi) karena kandungan oksigen terlarut (DO) akan berkurang dan akibatnya konsumsi oksigen menurun, aktifitas pernapasan naik dan selera makan organisme akuatik akan berkurang.
Derajat keasaman (pH) merupakan salah satu faktor yang berpengaruh langsung terhadap pertumbuhan dan produksi diatom. Pada saat peningkatan pH melewati titik ambang maksimum maka kecepatan tumbuh diatom akan menurun (Angka dkk, 1976 dalam Nurliati, 1995).
Menurut Sutomo (2005), batas pH untuk petumbuhan jasad merupakan suatu gambaran dari batas pH bagi kegiatan enzim, dan ion H+ sangat berpengaruh terhadap kegiatan enzim. Jika suatu enzim menunjukan kegiatannya pada pH tertentu, kenaikan atau penurunan pH tertentu suatu enzim substrat menjadi hasil akhir, lebih lanjut disampaikan bahwa umumnya fitoplankton dapat tumbuh dengan baik pada
11
kisaran optimum 8,0–8,5, ini sesuai dengan pendapatnya Lavens dan Sargeloos (1986), mengatakan bahwa kisaran pH secara umum untuk beberapa spesies alga yaitu antara 7–9 dengan kisaran optimal 8,2–8,7. Menurut Ari, dkk (2002), persyaratan kualitas air yang terbaik untuk pertumbuhan Chaetoceros sp adalah pada pH 7–8.
c. Oksigen Terlarut (DO)
Oksigen terarut (DO) merupakan parameter penting untuk mengukur pencemaran air. Walaupun oksigen(O2) sulit larut, tapi dibutuhkan banyak oleh semua jenis organism air. Tahap adanya oksigen tidak ada kehidupan tanaman dan binatang diperairan (Sutrisno,2009).
Oksigen terlarut dalah gas untuk respirasi yang sering menjadi faktor pembatas dalam lingkungan perairan. Ditinjau dari segi ekosistem, kadar oksigen terlarut menentukan kecepatan metabolisme dan respirasi serta sangat penting bagi kelangsungan dan pertumbuhan organisme air. Kandungan oksigen terlarut akan berkurang dengan naiknya suhu dan salinitas (Sachlan, 1982; Nybakken, 1988).
Menurut Raymont (1963).
d. Salinitas
Salinitas merupakan salah satu faktor pembatas pertumbuhan dan perkembangan fitoplankton. Perubahan salinitas secara langsung menyebabkan perubahan tekanan osmose di dalam sel fitoplankton sehingga aktifitas sel menjadi
12
terganggu. Fluktuasi salinitas juga dapat mempengaruhi pH sitoplasma sel dan menurunkan kegiatan enzim (Sudjiharno, 2002).
Menurut Isnansetyo dan kurniastuty (1995), Chaetoceros sp tergolong spesies yang euryhaline. Toleransi salinitasnya sangat lebar yakni 6 – 50‰. Salinitas optimal untuk pertumbuhan optimal dari Chaetoceros sp adalah 17 - 25 ‰.
2.6. Pertumbuhan populasi
Pertumbuhan pada fitoplankton didefinisikan sebagai suatu peningkatan berat disertai dengan peningkatan ukuran sel yang disebabkan oleh sintesis makromolekul, sehingga terbentuklah struktur yang baru (Becker 1994). Penentuan pola pertumbuhan pada Chaetoceros sp dilakukan dengan perhitungan sel secara langsung menggunakan haemocitometer yang diamati di bawah mikroskop Olympus BX 40.
Menurut Effendi (1979), pertumbuhan populasi adalah pertambahan jumlah individu. Selanjutnya dikatakan pula bahwa pertumbuhan merupakan proses biologis yang kompleks dimana banyak faktor yang mempengaruhinya. Ismail, dkk (1999) mengatakan bahwa pertumbuhan populasi dipengaruhi oleh faktor internal dan eksternal. Faktor internal antara lain adalah kelamin, umur, genetis ketahanan penyakit, dan kemampuan memanfaatkan pakan. Sedangkan faktor eksternal meliputi kualitas air, pakan, kepadatan, predator, dan kompetitor.
Peningkatan atau penambahan CO2 dalam media kultur, selain mempengaruhi pertumbuhan alga Chaetoceros sp, penambahan itu juga dapat menyebabkan perubahan kualitas air dari media kultur antara lain: suhu, salinitas,
13
dan derajad keasaman (pH). Dengan demikian perubahan yang terjadi diharapkan masih mendukung pertumbuhan populasi alga tersebut. (Boney, 1989 dalam Effendy 2003).
Ketersediaan pakan dan kemampuan organisme memanfaatkan atau daya mencerna pakan akan menentukan pertumbuhan populasi organisme karena bagian pakan yang dikomsumsi dan yang dapat diterima dicerna adalah sebagai sumber energi untuk kebutuhan metabolisme dan pertumbuhan, Gerking (1978) dalam Erlina dan Hastuti (1986).
Lebih lanjut Iagler et. Al (1962) dalam Yusuf (1994) menjelaskan pertumbuhan populasi tidak hanya dipengaruhi oleh nilai gizi pakan seperti protein, lemak dan vitamin tetapi juga kegemaran dan daya cerna suatu organisme yang akan berpengaruh terhadap pertumbuhan.
Stickney (1979) dalam Yusuf (1994) menjelaskan bahwa energi yang terkandung didalam pakan yang berasal dari non protein dapat mempengaruhi jumlah protein yang digunakan untuk pertumbuhan. Jika pakan kekurangan energi yang berasal dari non protein, maka sebahagian besar protein yang seharusnya digunakan untuk pertumbuhan akan dimanfaatkan sebagai sumber energi, lemak dalam pakan berperan sebagai sumber energi dan media perantara dalam penyerapan vitamin-vitamin yang dapat larut didalamnya.
14
III. METODE PENELITIAN
3.1. Waktu dan Tempat
Penelitian dimulai tahap persiapan alat dan bahan, uji perlakuan dan pelaksanaan penelitian berlangsung dari Desember 2012 sampai Mei 2013.
Pelaksanaan penelitian di Laboratorium Balai Penelitian dan Pengembangan Budidaya Air Payau (BPPBAP), Kabupaten Maros.
3.2. Organisme Uji
Organisme uji yang digunakan dalam penelitian ini adalah diatom jenis Chaetoceros sp.
3.3. Bahan dan Alat
Bahan dan alat yang digunakan dalam penelitian dapat dilihat pada Tabel 1 dan Tabel 2:
Tabel 1. Bahan yang digunakan dalam penelitian.
No Jenis bahan Kegunaan 1.
2.
3.
4.
Chaetoceros sp Air laut steril 30 ‰ Air tawar / aquades Etanol
Sebagai organisme uji Media kultur Chaetoceros sp Untuk mencuci alat
Untuk mengawetkan Chaetoceros sp
15
Tabel 2. Jenis alat dan kegunaan yang digunakan dalam penelitian.
No Jenis alat Kegunaan 1.
2.
3.
4.
5.
6.
7.
8.
9.
10.
11.
12.
13.
14.
15.
16.
17.
18.
19.
Spidol snowman Witeboard Blower
Tabung karbondioksida (CO2) konsentrasi 750 ppm dan 1000 ppm
Kabel listrik
Toples kaca / plastik Stiropoam
Slang aerasi Batu aerasi Krang aerasi Spoit
Lakban warna kuning Gunting
DO meter pH meter Thermometer
Automatic aquarium heater Talenan
Gelas ukur
Alat penanda label
Papan untuk menulis penjelasan penelitian
Menyuplai oksigen Menyuplai CO2
Penyambung listrik untuk blower Wadah pemeliharaan Chaetoceros sp Tempat penyimpanan wadah/toples Penyuplai aerator
Penghasil gelembung CO2
Untuk mengatur besar kecilnya aerator Alat untuk mengambil sampel
Sebagai label setiap toples Untuk memotong alat
Untuk mengukur konsentrasi oksigen terlarut
Untuk mengukur derajat keasaman Mengukur suhu
Untuk menaikkan suhu Untuk menyipan botol sampel
Tempat air pembilas haemocytometer
16 20.
21.
22.
23.
24.
25.
26.
27.
28.
29.
30.
31.
32.
33.
Cover glas Mikropipet Botol sampel
Mikroskop Olympus BX 40 Stapol
Adaptor
Haemocytometer
Kaca preparat kecil Tissue
Kanebo Buku Pensil
Hand caunter (alat hitung) Calculator
Gelas penutup sampel Alat pengambil sampel Alat menyimpan sampel
Alat untuk mengamati Chaetoceros sp Alat bantu monitor mikroskop
Alat bantu monitor mikroskop
Alat menghitung kepadatan Chaetoceros sp
Penutup haemocymeter
Untuk membersihkan haemocytometer Untuk membersihkan alat
Tempat untuk mencatat hasil Untuk mencatat hasil
Sebagai alat menghitung kepadatan Chaetceros sp
Alat untuk menghitung hasil akhir kepadatan Chaetceros sp
17 3.4. Prosedur Penelitian
a). Persiapan Wadah Kultur
Wadah dan peralatan yang digunakan disterilisasi dengan menggunakan kaporit 100 ppm dan detergen dilanjutkan dengan pembersihan dan pembilasan dengan menggunakan air tawar, kemudian dikeringkan. Wadah yang sudah disterilkan diatur tata letaknya sesuai dengan rancangan yang digunakan.
Langkah awal kultur Chaetoceros sp, skala Laboratorium sebelum dilakukan penelitian dengan beberapa tahapan yakni tahap isolasi, dan kultur murni serta dilakukan dengan kultur bertingkat dimulai dari kultur dalam tabung reaksi volume 10 ml (test tube) sampai kultur pada wadah yang lebih besar mulai dari 100 ml – 5 liter (Isnansetyo dan kurniastuty, 1995).
b). Kultur Chaetoceros sp
Wadah yang telah disiapkan diisi dengan air laut steril sebanyak 1000 ml.
Setelah itu dilakukan penebaran bibit Chaetoceros sp, sebanyak 105 sel/ml untuk setiap wadah penelitian. Hal ini sesuai dengan pendapat Nukiyama (1976) dalam Muhaimin (2008) bahwa dalam kultur Chaetoceros sp, digunakan air laut sebanyak 80–90% dengan padat penebaran awal 100.000 sel/ml. Wadah tersebut kemudian diletakkan pada rak-rak (styropoam) kultur lalu diberi pencahayaan dengan lampu 20 watt sebanyak 2 buah untuk setiap perlakuan. Selama kultur berlangsung wadah ditutup dan air medianya diberi aerasi terus menerus untuk menghindari pengendapan Chaetoceros sp, dan juga untuk menyuplai CO2.
18
Menurut Sudjiharno (2002), kultur fitoplankton memerlukan kondisi lingkungan yang terkendali, olehnya itu perlu dilengkapi dengan AC (Air Conditioner) agar suhu ruangan selalu terkendali dan ruangan terisolasi dari lingkungan luar yang dapat menyebabkan kontaminasi. Lebih lanjut ditambahkan bahwa dalam kultur skala Laboratorium, kesterilan alat, bahan dan air media yang akan digunakan sangat dibutuhkan sehingga bebas dari kontaminasi organisme lain seperti jenis fitoplankton lainnya, zooplankton, protozoa dan bakteri yang bisa menjadi kompetitor dan predator bagi fitoplankton yang dikultur.
Menurut Gusrina (2008), penebaran bibit fitoplankton harus dilakukan secara tepat, dimana bibit yang akan ditebar ke dalam media harus yang sudah dewasa.
Volume bibit atau jumlah bibit yang yang dibutuhkan untuk penebaran dapat dihitung dengan rumus : V1N1= V2N2;
Dimana : V1 : Volume bibit yang diperlukan (ml)
V2 : Volume kultur yang dibuat dalam gelas erlemeyer (ml) N1 : Jumlah bibit per cc yang ditebar (sel/ml)
N2 : Jumlah bibit yang dikehendaki (sel/ml).
3.5. Perlakuan dan Rancangan Percobaan
Optimasi peningkatan konsentrasi karbondioksida (C02) terhadap pertumbuhan dan populasi Chaetoceros sp skala Laboratorium. Rancangan yang digunakan dalam penelitian ini adalah Rancangan Acak Lengkap dengan tiga perlakuan dan tiga ulangan, perlakuan yang diujikan adalah sebagai berikut;
19
Konsentrasi Karbondioksida (CO2) 385 ppm Konsentrasi Karbondoksida (CO2) 750 ppm Konsentrasi Karbondoksida (CO2) 1000 ppm
Gambar 2. Tata letak unit penelitian setelah pengacakan.
a). Cara Kerja
Hal yang pertama dilakukan adalah menyiapkan wadah dan peralatan yang akan digunakan. Wadah yang digunakan berupa toples plastik berkapasitas 2 liter, wadah dan peralatan yang akan digunakan terlebih dahulu disucihamakan dengan menggunakan detergen. Selanjutnya wadah dan peralatan tersebut disterilkan. Alat dan bahan penelitian yang steril dipersiapkan untuk pemasangan stalasi yang dimulai dari tabung karbondioksida (CO2) yang dilengkapi dengan slank aerasi, krang aerasi dan batu aerasi disambungkan kedalam toples yang sudah diatur dengan perlakuan tersebut, setelah itu toples tersebut diisi air laut steril 30‰ sebanyak satu liter, kemudian dilakukan penebaran bibit Chaetoceros sp yang telah dikultur, lalu kemudian organisme atau Chaetoceros sp yang ada dalam wadah atau toples tersebut
385-1 385-3 385-2
750-3 750-1
750-2
1000-1 1000-2
1000-3
20
setiap harinya disemprotkan atau diberi karbondioksida (CO2) sebelum pengambilan sampel guna untuk mengetahui reaksi atau pengaruh pertumbuhan populasi Chaetoceros sp pada peningkatan konsentrasi karbondioksida (CO2) tersebut. Namun penyemprotan CO2 dilakukan tiga kali sehari hal tersebut dilakukan untuk mengetahui pengaruh kualitas air yang diukur seperti pH, suhu, dan oksigen terlarut (DO).
b). Pengambilan Sampel Chaetoceros sp.
Pertumbuhan fitoplankton dalam kultur dapat ditandai dengan bertambah banyaknya jumlah sel (kepadatan sel) (Takdir, 1990). Pertumbuhan populasi Chaetoceros sp pada penelitian ini dilakukan sekali 24 jam yakni pada pagi hari sekitar jam 07:00 dengan mengambil air sampel sebanyak 1 ml/unit perlakuan.
Untuk menghitung kepadatan sel Chaetoceros sp, digunakan haemocytometer. Mula-mula air sampel atau plankton tersebut diambil dengan menggunakan pipet kemudian diberi etanol untuk mengawetkan atau mematikan sel Chaetoceros sp sebelum diteteskan diatas haemocytometer untuk memudahkan perhitungan, selanjutnya kepadatan sel dihitung dibawah mikroskop Olimpus BX40 yang dilengkapi monitor dengan bantuan alat penghitung (hand counter). Kepadatan sel populasi Chaetoceros sp, untuk setiap ml nya dihitung dengan menggunakan rumus menurut Mudjiman (2007).
∑Sel/ml = N x 104
Dimana : N = jumlah rata-rata sel.
21
3.6. Pengukuran Kualitas Air
Parameter kualitas air yang diamati dalam penelitian ini adalah Suhu, pH, dan DO meter. Parameter kualitas air, alat yang digunakan, dan waktu pengamatan tercantum pada Tabel 3. berikut :
Tabel 3. Parameter Kualitas Air yang Diukur
Alat/Metode yang Digunakan, dan Waktu Pengamatan Selama Penelitian
No Parameter Metode Satuan Alat ukur
1. Suhu Pembaca skala ºC Termometer
2. pH Pembaca skala - pH Meter
3. DO Pembaca skala mg/l DO meter
4. Suhu termometer Pembaca skala mg/l -
3.7. Analisa Data
Data yang diperoleh dianalisis dengan statistik Excel kemudian ditampilkan dalam bentuk tabel, grafik, histogran dan anova secara deskriptif.
22
IV. HASIL DAN PEMBAHASAN
4.1. Pertumbuhan Populasi Chaetoceros sp
Berdasarkan hasil peningkatan konsentrasi karbondioksida (CO2) terhadap petumbuhan dan populasi Chaetoceros sp skala laboratorium setiap perlakuan dapat dilihat pada tabel dibawah ini.
Tabel 4. Data kepadatan Chaeotceros cp, pada penelitian selama sembilan hari dalam 3 perlakuan dan masing-masing 3 ulangan.
Tabel 4 menunjukkan bahwa kepadatan pertumbuhan dan populasi Chaetoceros sp, pada penelitian tersebut, memberikan hasil cukup berbeda antara perlakuan konsentrasi karbondioksida (CO2) 385 ppm, (CO2) 750 ppm dan (CO2) 1000 ppm, serta rata-rata kepadatan maksimun terjadi pada hari ke-7 dan hari ke-8 dari masing-masing perlakuan dan ulangan.
Dari setiap perlakuan konsentrasi karbondioksida (CO2), untuk fase adaptasi berlangsung hampir sama yakni pada hari 1 sampai 3.
23
Fase eksponensial pada setiap perlakuan berkisar pada hari ke 4 sampai ke 6.
Adanya kecendrungan bahwa fase eksponensial cukup lama dikarenakan unsur hara yang cukup tersedia pada saat timbulnya fase eksponensial. Menurut Fogg (1975).
Laju pertumbuhan menggambarkan kecepatan pertambahan individu algae per satuan waktu. Nilai laju pertumbuhan dapat digunakan untuk mengetahui adanya daya dukung media terhadap pertumbuhan algae. Semakin tinggi nilai laju pertumbuhan, menunjukkan daya dukung media terhadap pertumbuhan algae semakin baik (Myers, 1955 dalam massenreng, 2002).
Laju perumbuhan Chaetoceros sp, perlakuan konsentrasi karbondioksida (CO2) 385 ppm terlihat bahwa kepadatan Chaetoceros sp, yang paling tinggi pada hari ke-8 yaitu 3.240.000 sel/ml, dan disusul Gambar 3 CO2 750 ppm pada hari ke-6 yaitu 1.472.500 sel/ml, serta Gambar 4 CO2 1000 ppm pada hari ke-6 yaitu 1.375.000 sel/ml. Dari ke-3 perlakuan konsentrasi karbindioksida (CO2) tersebut merupakan laju kepadatan pertumbuhan populasi Chaetoceros sp, yang lebih baik disetiap atau masing-masing perlakuan konsentrasi karbindioksida (CO2). Hal ini dikarenakan atau bertanda alga lebih menyukai karbondiksida (CO2) yang lebih rendah (Boney, 1989 dalam effendi, 2003). Karbondioksida (CO2) merupakan gas yang dibutuhkan oleh tumbuhan air renik maupun untuk melakukan fotosintesis. Meskipun peranan karbondioksida (CO2) sangat besar bagi kehidupan organisme air namun kandungannya yang berlebihan sangat menganggu, bahkan dapat menjadi racun secara langsung bagi organisme tersebut (M. Ghufran H. Kordi K 2002).
24
Ini bertanda bahwa memberikan dampak buruk pada pertumbuhan Chaetoceros sp, jika konsentrasi karbondioksida (CO2) semakin tinggi.
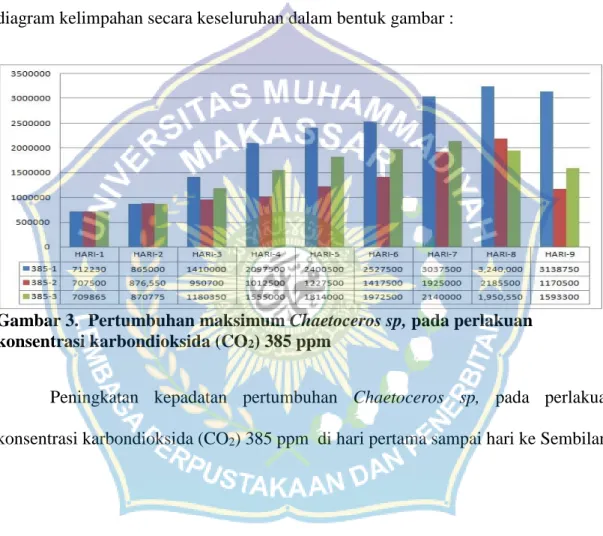
Agar lebih mudah dipahami peningkatan karbondioksida (CO2) Terhadap Pertumbuhan dan populasi Chaetoceros sp, penulis menyajikan diagram harian dan diagram kelimpahan secara keseluruhan dalam bentuk gambar :
Gambar 3. Pertumbuhan maksimum Chaetoceros sp, pada perlakuan konsentrasi karbondioksida (CO2) 385 ppm
Peningkatan kepadatan pertumbuhan Chaetoceros sp, pada perlakuan konsentrasi karbondioksida (CO2) 385 ppm di hari pertama sampai hari ke Sembilan.
25
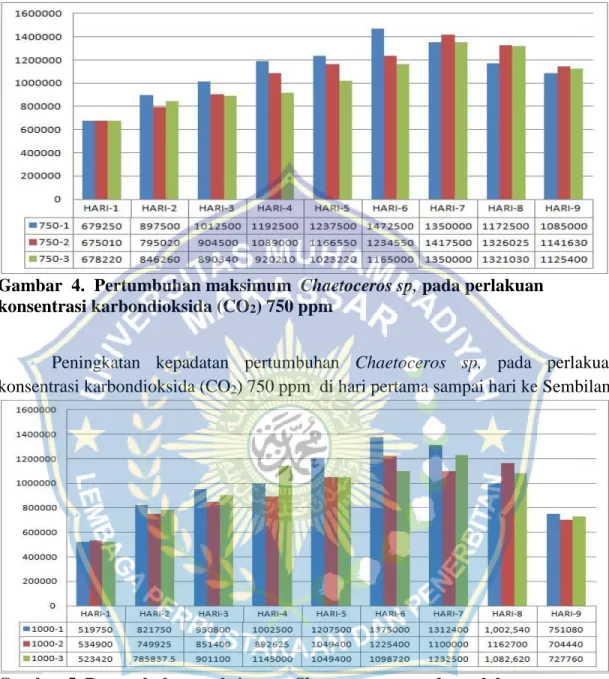
Gambar 4. Pertumbuhan maksimum Chaetoceros sp, pada perlakuan konsentrasi karbondioksida (CO2) 750 ppm
Peningkatan kepadatan pertumbuhan Chaetoceros sp, pada perlakuan konsentrasi karbondioksida (CO2) 750 ppm di hari pertama sampai hari ke Sembilan.
Gambar 5. Pertumbuhan maksimum Chaetoceros sp, pada perlakuan konsentrasi karbondioksida (CO2) 1000 ppm
Peningkatan kepadatan pertumbuhan Chaetoceros sp, pada perlakuan konsentrasi karbondioksida (CO2) 1000 ppm di hari pertama sampai hari ke sembilan.
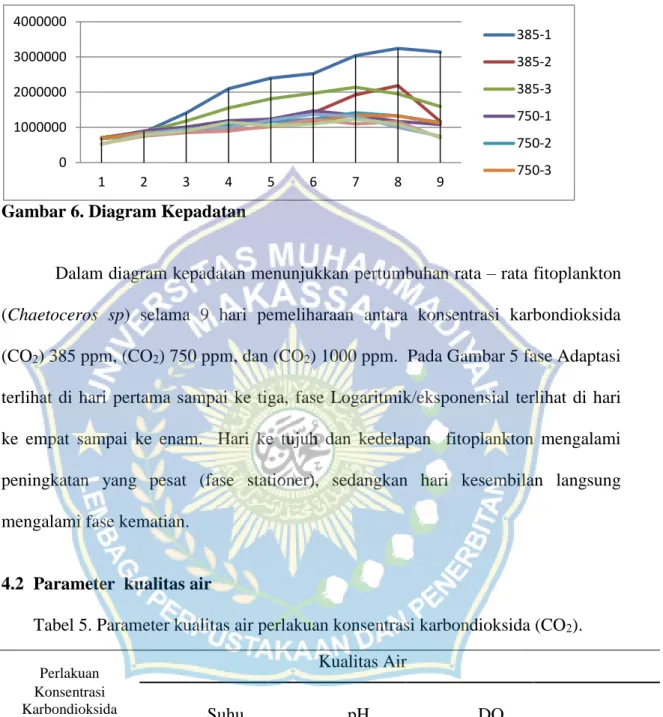
26 Gambar 6. Diagram Kepadatan
Dalam diagram kepadatan menunjukkan pertumbuhan rata – rata fitoplankton (Chaetoceros sp) selama 9 hari pemeliharaan antara konsentrasi karbondioksida (CO2) 385 ppm, (CO2) 750 ppm, dan (CO2) 1000 ppm. Pada Gambar 5 fase Adaptasi terlihat di hari pertama sampai ke tiga, fase Logaritmik/eksponensial terlihat di hari ke empat sampai ke enam. Hari ke tujuh dan kedelapan fitoplankton mengalami peningkatan yang pesat (fase stationer), sedangkan hari kesembilan langsung mengalami fase kematian.
4.2 Parameter kualitas air
Tabel 5. Parameter kualitas air perlakuan konsentrasi karbondioksida (CO2).
Perlakuan Kualitas Air
Konsentrasi Karbondioksida
(CO2) Suhu pH DO 385 ppm 28 – 30 8,08 – 8,73 2,35 – 8,25 750 ppm 27 – 30 7,78 – 8,92 2,14 – 7,44 1000 ppm 24 – 30 8,16 – 8,88 2,09 – 8,17
Sumber : Laboratorium Uji BPPBAP Maros
0 1000000 2000000 3000000 4000000
1 2 3 4 5 6 7 8 9
385-1 385-2 385-3 750-1 750-2 750-3
27 a). Suhu
Suhu memberikan peranan penting dalam kultur fitoplankton, karena sangat mempengaruhi aktifitas enzim dalam metabolisme sel (Graffith, 1983 dalam Nurliati, 1995). Selanjutnya dikemukakan bahwa semua spesies Chaetoceros sp, Toleran terhadap suhu tinggi.
Menurut Cahyaningsih, dkk (2005), Chaetoceros sp, toleran terhadap suhu tinggi. Pada suhu 40 0C spesies ini dapat hidup tetapi tidak dapat berkembang.
Chaetoceros sp. Tumbuh normal pada kisaran suhu 20 – 30 0C dan tumbuh optimum pada kisaran suhu 25 – 30 0C.
b). pH
Fitoplankton dapat tumbuh dengan baik pada kisaran optimum 8,0 – 8,5, ini sesuai dengan pendapatnya Lavens dan Sargeloos (1986), mengatakan bahwa kisaran pH secara umum untuk beberapa spesies alga yaitu antara 7 – 9 dengan kisaran optimal 8,2 – 8,7. Menurut Ari, dkk (2002), persyaratan kualitas air yang terbaik untuk pertumbuhan Chaetoceros sp, adalah pada pH 7–8.
c). DO
Kadar oksigen terlarut pada perairan alami biasanya kurang dari 10 mg/L (Effendi, 2003). Kandungan oksigen terlarut akan berkurang dengan naiknya suhu dan salinitas (Sachlan, 1982; Nybakken, 1988). Menurut Raymont (1963), konsentrasi dari oksigen terlarut paling rendah yang dibutuhkan oleh organisme perairan adalah 1 ppm.
28 V. PENUTUP
5.1. KESIMPULAN
Dari hasil penelitian tersebut bahwa diantara ketiga perlakuan konsentrasi karbondiokasida (CO2) mendapatkan hasil yang terbaik untuk pertumbuhan dan populasi Chaetoceros sp, yakni konsentrasi karbondioksida (CO2) 385 ppm dengan total populasi tertinggi 3.240.0004 pada hari ke – 8.
5.2. SARAN
Peneliti menyarankan bahwa untuk meningkatkan pertumbuhan dan populasi Chaetoceros sp skala laboratorium, dibutuhkan karbondioksida (CO2) 385 ppm.
29
DAFTAR PUSTAKA
Angka, S. L., Sumantadinata, K., Harris, E., Darnas, Chaeruddin, A., 1976. Kultur Laboratories Diatomae Laut (Pengaruh Salinitas dan Inoculums Terhadap Pertumbuhan Populasi Monocultur Skeletonema Costatum dan Nitzschia Closterium Pelagis dan Benthis Dari Laut Jawa). Proyek Pengembangan Perguruan Tinggi Institut Pertanian Bogor.
Ari K. W., Sudjiharno dan Anjar S. 2000. Pasca Panen Fitoplankton dan Pemanfaatannya. DKP. Direktorat Jenderal Perikanan Bala Budidaya Laut Lampung.
Bachtiar, Y., 2003. Menghasilkan Pakan Alami Untuk Ikan Hias. Agromedia Pustaka, Jakarta.
Becker, EW. 1994. Microalgae Biotechnology and Microbiology. Britain: Cambridge University Press. 279 hal.
Cahyaningsih, S., Achmad, N.,Sugeng, J.P., 2005. Kultur Murni Fitoplankton.
Departemen kelautan dan Perikanan Direktorat Jenderal Perikanan Budidaya, Balai Budidaya Air Payau Situbondo.
Cahyaningsih, S., 2006. Petunjuk Teknis Produksi Pakan Alami. Departemen kelautan dan Perikanan Direktorat Jenderal Perikanan Budidaya, Balai Budidaya Air Payau Situbondo.
Djarijah, A.S., 1995. Pakan Ikan Alami. Kanisius, Yogyakarta.
Djarijah, A.S., 2006. Budidaya Chaeotceros sp. Kanisius, Yogyakarta.
Effendie, M. I., 1997. Biologi Perikanan. Yayasan Pustaka Nusatama, Yogyakarta.
Effendie, M. I., 2003. Managemenagribisnis Perikanan Yayasan Pustaka Nusatama, Yogyakarta.
Foog, G. F, 1965. Algal Cultures and Phytoplankton Ecology. The University of Wisconsin Press, London. 126 hal.
Gusrina, 2008. Budidaya Ikan Jilid II. Direktorat Pembinaan Sekolah Menengah Kejuruan Departemen Pendidikan Nasional, Jakarta.
Haryati, 1980. Percobaan Penggunaan Beberapa Macam Komposisi Media Terhadap Pertumbuhan populasi monokultur Skeletonema costatum Greville. UNDIP- Press. Semarang.
30 Hastuti, 1986. Planktologi. Semarang UNDIP.
Hutagalung H. P. 1984. Logam Berat dalam Lingkungan Laut. Oseana. IX(1) : 12-14.
Ismail A, Wedjatmiko, Sastrawijaya dan Sindu S. 1999. Kajian Teknis Paktor Pertumbuhan dan Populasi Plankton. Pusat Penelitian dan Pengembangan Eksplorasi Laut dan Perikanan. Departemen Perikanan dan Kelautan Bekerjasama dengan Japan International Corporation Agency. Jakarta.
Isnansetyo, A & Kurniastuti, 1995. Teknik Kultur Fitoplankton dan Zooplankton Pakan Alami Untuk Pembenihan Organisme Laut. Kanisius. Yogyakarta.
Kordi, G. H., 2004. Penanggulangan Hama dan Penyakit Ikan. Rineka Cipta, Jakarta.
Lavens, P dan Sorgeloos, P. 1996. Manual on The Production and Use For Live Food For Aquakulture. F.A.O. Tecnichal Paper.
Lee, R. E. 1980. Phyciology. Cambrige Universitas Press. Cambrige, Canada. 478 hal.
Lesmana, D. S., 2005. Kualitas Air . Penebar Swadaya, Jakarta.
Messenreng, 2002. Komposisi dan kelimpahan fitoplankton Crysophyta
(Phaeodactylom sp., Chaetoceros sp., Pavlova sp.) pada berbagaitingkat kandungan unsur hara nitrogen, fospat, dan Salikat. Skripsi. Jurusan MSP.
FPIK IPB, Bogor. 54 hal.
Mudjiman, A., 2007. Makanan Ikan Edisi Revisi. Penebar Swadaya, Jakarta.
Muhaimin, M. I., 2008. Pengaruh Konsentrasi Posfat pada Formula Pupuk Conway terhadap Pertumbuhan Chaetoceros sp., Skripsi Fakultas Perikanan dan Ilmu Kelautan Universitas Muslim Indonesia, Makassar.
Nainggolan, R. F. 1993. Penggunaan karbondioksida dan propionate dalam kemasan plastik plesibel kedap udara untuk menghambat perkembangan serangga dan kapan pada ransun petelur komersil. Tesis. Sekolah pasca sarjana, IPB, Bogor. Hal 18.
Nurliati, A., 1995. Pengaruh Dosis Abu Sekam Padi Terhadap Pertumbuhan
Chaetoceros sp. Skripsi. Fakultas Perikanan dan Ilmu Kelautan Universitas Muslim Indonesia, Makassar.
31
Raymont, J. E. E. 1963. Plankton and Productivity in the Ocean. 2nd edition.
Pergamon Press, Oxford. 770 pp.
Soeyasa, 2001. Ekologi Perairan. Departemen Kelautan dan Perikanan Dirjen.
Pendidikan Menengah Atas, JakartA.
Sudjiharno, 2002. Budidaya Fitoplankton dan Zooplankton. Departemen kelautan dan Perikanan Direktorat Jenderal Perikanan Budidaya, Balai Budidaya Laut Lampung.
Sumeru, S.U. dan Anna, S., 1992. Pakan Udang Windu (Penaeus monodon).
Kanisius, Yogyakarta.
Sutomo, 2005. Kultur Tiga Jenis Mikroalga (Tetraselmis sp, Chlorella sp Dan Chaetoceros Gracilis) Dan Pengaruh Kepadatan Awal Terhadap Pertumbuhan C. Gracilis Di Laboratorium. Oseanologi dan Limnologi di Indonesia. ISSN 0125-9830.
Takdir, 1990. Pengaruh Abu Sekam Padi Terhadap Pertumbuhan Chaetoceros sp.
Jurnal Penelitian Budidaya Pantai, Balai Penelitian Perikanan Budidaya Pantai Maros.
Yunus, 1992. Pengaruh Salinitas yang Berbeda terhadap Pertumbuhan Chaetoceros ceratosporum di Laboraturium. Jurnal Penelitian Budidaya Pantai, Balai Penelitian Perikanan Budidaya Pantai Maros.
Yusuf, Trianingsih, E. Asnaryanti dan S. H. Riono. 1994. Kisaran Kelimpahan dan Komposisi Plankton Predominan diperairan Kawasan Timur Indonesia. P3O- LIPI. Jakarta.
32
33 Dokumentasi penelitian
Laboratorium tempat penelitian pakan alami
34
Gambar pH meter, DO meter, thermometer, blower, heater.
35
Alat dan bahan yang digunakan pada saat penelitian
36 Kultur pakan alami
37 Penebaran Chaetoceros sp dan pengukuran pH
38 Pengukuran pH dan Chaetoceros sp dalam toples
39 Pengambilan sampel sel Chaetoceros sp
40 Perhitungan sel fitopalnkton atau Chetoceros sp
41
RIWAYAT HIDUP
NASIRUDDIN, lahir di Bantaeng pada tanggal 13 Maret 1988, dari pasangan H. Hasanuddin dan Hj Haryani.
merupakan anak ke dua dari 3 bersaudara. Pendidikan formal yang pernah ditempuh adalah Sekolah Dasar 49 Erasaya, Desa Kaloling, Kecamatan Gantarang Keke, Kabupaten Bantaeng
dan tamat pada tahun 2001, Sekolah Menengah Pertama Negeri 4 Tompo’bulu Kabupaten Bantaeng dan Tamat pada tahun 2004, Sekolah Menengah Kejuruan Negeri 2 Perikanan dan Kelautan Bantaeng Program Studi Budidaya Perairan Laut dan tamat pada tahun 2008. Pada tahun 2008 diterima di Fakultas Pertanian Universitas Muhammadiyah Makassar (Unismuh) dan memilih jurusan Budidaya Perairan. Selama menjadi mahasiswa, penulis pernah aktif dalam Himpunan Mahasiswa Perikanan Unismuh dan juga sebagai pengurus Organisasi Daerah (ORGANDA) Kabupaten Bantaeng yakni Kelompok Studi dan Karya Putra Putri Bantaeng (KOSKAR PPB).
Pada tanggal 28 November 2013 menyelesaikan pendidikan Strata satu dan meraih Gelar Sarjana Perikanan, setelah mempertahankan karya ilmiah didepan team penguji dengan judul : Optimasi Peningkatan Konsentrasi Karbondioksida (CO2) Terhadap Pertumbuhan dan Populasi Chaetoceros sp Skala Laboratorium.