i
OBAT HERBAL TERSTANDAR (OHT) RHEUMAKUR® YANG BEREDAR DI PASARAN MENGGUNAKAN METODE
KROMATOGRAFI CAIR KINERJA TINGGI (KCKT) FASE TERBALIK
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm)
Program Studi Farmasi
Oleh:
Dian Prahara Florentino Wara NIM: 078114107
FAKULTAS FARMASI UNIVERSITAS SANATA DHARMA
ii
Persetujuan Pembimbing
PENETAPAN KADAR KURKUMIN DALAM SEDIAAN KAPSUL LUNAK OBAT HERBAL TERSTANDAR (OHT) RHEUMAKUR® YANG
BEREDAR DI PASARAN MENGGUNAKAN METODE
KROMATOGRAFI CAIR KINERJA TINGGI (KCKT) FASE TERBALIK
Skripsi yang diajukan oleh: Dian Prahara Florentino Wara
NIM: 078114107
telah disetujui oleh
iii
PENETAPAN KADAR KURKUMIN DALAM SEDIAAN KAPSUL LUNAK OBAT HERBAL TERSTANDAR (OHT) RHEUMAKUR® YANG
BEREDAR DI PASARAN MENGGUNAKAN METODE
KROMATOGRAFI CAIR KINERJA TINGGI (KCKT) FASE TERBALIK
Oleh:
Dian Prahara Florentino Wara NIM: 078114107
Dipertahankan di hadapan Panitia Penguji Skripsi Fakultas Farmasi
iv
HALAMAN PERSEMBAHAN
Bukan Manusia yang berusaha dan
Tuhan yang menentukan, namun
Tuhan yang memberi pilihan dan
manusia yang memilih, berusaha
dan bertanggung jawab atas pilihan
hidupnya…..
manusia berhenti makan karena kenyang, berhenti berjalan karena lelah namun tidak berhenti mengejar ilmu dan kesenangan…
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
v
Saya menyatakan dengan sesungguhnya bahwa skripsi yang saya tulis ini tidak memuat karya atau bagian karya orang lain, kecuali yang telah disebutkan dalam kutipan dan daftar pustaka, sebagaiman layaknya karya ilmiah.
Apabila di kemudian hari ditemukan indikasi plagiarisme dalam naskah ini, maka saya bersedia menanggung segala sanksi sesuai peraturan perundang-undangan yang berlaku.
vi
LEMBAR PERNYATAAN PERSETUJUAN
PUBLIKASI KARYA ILMIAH UNTUK KEPENTINGAN AKADEMIS
Yang bertanda tangan di bawah ini, saya mahasiswa Universitas Sanata Dharma: Nama : Dian Prahara Florentino Wara
Nomor Mahasiswa : 078114107
Demi pengembangan ilmu pengetahuan, saya memberikan kepada Perpustakaan Universitas Sanata Dharma karya ilmiah saya yang berjudul:
“PENETAPAN KADAR KURKUMIN DALAM SEDIAAN KAPSUL LUNAK OBAT HERBAL TERSTANDAR (OHT) RHEUMAKUR® YANG
BEREDAR DI PASARAN MENGGUNAKAN METODE
KROMATOGRAFI CAIR KINERJA TINGGI (KCKT) FASE TERBALIK
“
beserta perangkat yang diperlukan (bila ada). Dengan demikian saya memberikan kepada Perpustakaan Universitas Sanata Dharma hak untuk menyimpan, mengalihkan dalam bentuk media lain, mengelolanya dalam bentuk pangkalan data, mendistribusikannya secara terbatas, dan mempublikasikannya di internet atau media lain untuk kepentingan akademis tanpa perlu meminta ijin dari saya maupun memberikan royalti kepada saya selama tetap mencantumkan nama saya sebagai penulis.
Demikian pernyataan ini saya buat dengan sebenarnya. Dibuat di Yogyakarta
Pada tanggal : 3 Juni 2011
vii
Puji dan syukur kepada Tuhan Yang Maha Esa, yang telah melimpahkan berkat rahmat-Nya sehingga penulis dapat menyelesaikan skripsi yang berjudul “Penetapan Kadar Kurkumin Dalam Sediaan Kapsul Lunak Obat Herbal Terstandar (OHT) Rheumakur® Yang Beredar Di Pasaran Menggunakan Metode Kromatografi Cair Kinerja Tinggi (KCKT) Fase Terbalik” sebagai salah satu syarat memperoleh gelar Sarjana Farmasi (S. Farm) di Fakultas Farmasi Universitas Sanata Dharma.
Penulis mengucapkan terima kasih kepada semua pihak yang mendorong, memotivasi dan memberikan saran hingga selesainya skripsi ini, terutama kepada: 1. Bapak Ipang Djunarko M.Sc, Apt., selaku Dekan Fakultas Farmasi
Universitas Sanata Dharma Yogyakarta.
2. Ibu Christine Patramurti, M.Si, Apt. selaku Dosen Pembimbing yang telah membimbing penulis, memberikan masukan, kritik, solusi, dan memberikan dukungan kepada penulis selama penyusunan skripsi ini.
3. Bapak Jeffry Julianus, M.Si. selaku Dosen Penguji yang memberikan kritik dan saran untuk skripsi ini.
4. Bapak Prof. Dr. C.J. Soegihardjo, Apt. selaku Dosen Penguji yang memberikan kritik dan saran untuk skripsi ini
viii
6. Ibu Rini Dwi Astuti, M.Sc, Apt. selaku Kepala Laboratorium Fakultas Farmasi Universitas Sanata Dharma Yogyakarta.
7. Segenap dosen dan karyawan atas ilmu dan pengalaman yang berharga sehingga berguna dalam proses penyusunan skripsi.
8. Seluruh staff laboratorium, staff keamanan, dan kebersihan di Fakultas Farmasi Universitas Sanata Dharma Yogyakarta.
9. Perpustakaan Universitas Sanata Dharma atas koleksi buku-buku serta akses internetnya sehingga penulis memperoleh bahan-bahan yang cukup lengkap dalam penulisan skripsi ini
10. Keluargaku tercinta, Papa Bernadus Wara, Mama Monica, Mbak Maria Emyrensiana dan adikku tersayang Daniela.
11. Katarina Kusmiyanti yang selalu mendukung dan menyemangati penulis untuk menyelesaikan skripsi.
12. Benny Nugroho selaku teman seperjuangan selama penelitian dan penyusunan skripsi.
13. Teman-teman skripsi satu tema kurkumin atas kerjasama dan dukungannya selama penyusunan skripsi.
14. Teman-teman FST dan FKK 2007 atas pengalaman, keceriaan, dan kebersamaan yang tak kan terlupakan.
15. Semua teman-teman Farmasi, terima kasih atas kebersamaannya.
16. Teman-teman jaman TK, SD dan SMP yang sekarang sedang mengejar cita-citanya masing-masing atas kenangan sedih, ceria dan gila serta dukungannya pada penulis selama mengerjakan skripsi
ix
Penulis menyadari bahwa skripsi ini masih terdapat banyak kekurangan. Oleh karena itu penulis mengharapkan kritik dan saran untuk membantu penulis dalam perkembangan selanjutnya. Akhir kata, semoga skripsi ini berguna bagi pembaca.
x
DAFTAR ISI
Hal
HALAMAN JUDUL ... i
HALAMAN PERSETUJUAN PEMBIMBING ... ii
HALAMAN PENGESAHAN ... iii
HALAMAN PERSEMBAHAN ... iv
xi
C. Kapsul lunak ... 9 D. Obat herbal terstandar ...
E. Cara Pembuatan Obat Tradisional yang Baik ... F. Standardisasi ekstrak ... H. Kromatografi Cair Kinerja Tinggi ...
1. Definisi dan instrumentasi KCKT ... 2. Kromatografi partisi fase terbalik ... 3. Waktu retensi dan resolusi ... 4. Analisis kulitatif dan analisis kuantitatif ...
18 BAB III. METODE PENELITIAN ...
A. Jenis dan Rancangan Penelitian ... B. Variabel Penelitian ... 1. Variabel bebas ... 2. Variabel tergantung ... 3. Variabel pengacau terkendali ... C. Defisnisi Operasional ... D. Bahan Penelitian ... E. Alat Penelitian ... F. Tata Cara Penelitian ...
xii
1. Pemilihan dan pengambilan sampel ... 2. Pembuatan asam asetat glasial 2% ... 3. Pembuatan metanol pH 4 sebagai pelarut ... 4. Pembuatan fase gerak ... 5. Pembuatan larutan baku kurkumin ... 6. Penentuan panjang gelombang maksimum kurkumin ... 7. Pembuatan kurva baku kurkumin ... 8. Optimasi waktu ekstraksi kurkumin dalam sampel
Rheumakur® ... 9. Penetapan kadar ... G. Analisis hasil ... BAB IV. HASIL DAN PEMBAHASAN ... A. Pemilihan Sampel …... B. Pembuatan Pelarut... C. Pembuatan Fase Gerak ... D. Penentuan Panjang Gelombang Maksimal Kurkumin dengan
xiii
DAFTAR PUSTAKA ... LAMPIRAN ... BIOGRAFI PENULIS ...
xiv Tabel IV. Hasil perhitungan kadar kurkumin dalam masing-masing
xv
Gambar 1. Struktur dari kurkuminoid ... Gambar 2. Reaksi degradasi kurkumin pada pH basa ... Gambar 3. Produk fotodegradasi kurkumin ... Gambar 4. Produk Rheumakur® ... Gambar 5. Logo Obat Herbal Terstandar …... Gambar 6. Aspek dan tahapan skematik standardisasi ... Gambar 7. Peralatan KCKT ... Gambar 8. Reaksi pembuatan kolom oktadesilsilan... Gambar 9. Pemisahan dua senyawa ... Gambar 10. Reaksi degradasi kolom C18 pada pH asam ≤ 2 ... Gambar 11. Spektra serapan kurkumin dengan pelarut campuran metanol
p.a dan asam asetat glasial 2% pada pH 4 ... Gambar 12. Gugus kromofor dan auksokrom kurkumin ... Gambar 13. Kurva baku kurkumin ... Gambar 14. Kromatogram baku kurkumin (a) dan kurkumin dalam sampel (b) ... Gambar 15. Gugus nonpolar dari kurkumin ... Gambar 16. Interaksi kurkumin dengan fase gerak metanol p.a:asam
asetat glasial 2% membentuk ikatan hidrogen ... Gambar 17. Interaksi kurkumin dengan fase diam oktadesilsilan ... Gambar 18. Kromatogram ekstraksi sampel menggunakan ultrasonikator
xvi
selama 5; 10; 15; 20; 25; dan 30 menit ... Gambar 19. Kurva optimasi waktu ekstraksi sampel Rheumakur® ...
xvii
Lampiran 1. Jaminan Keaslian Baku Kurkumin Hasil Sintesis ... Lampiran 2. Hasil Uji Stabilitas Kurkumin pada pH 3-5 dengan Spektrofotometer Visibel pada rentang 200-500 nm ... Lampiran 3. Perhitungan Kepolaran Fase Gerak ... Lampiran 4. Spektra Serapan Kurkumin dengan Pelarut Campuran Metanol p.a dan Asam Asetat Glasial 2% pada pH 4... Lampiran 5. Hasil Uji Keseragaman Bobot dan Contoh Perhitungannya ... Lampiran 6. Data Kurva Baku Kurkumin ... Lampiran 7. Kromatogram Ekstraksi Sampel Menggunakan
Ultrasonikator ... Lampiran 8. Kromatogram Penetapan Kadar Kurkumin dalam Sampel... Lampiran 9. Data Hasil Perhitungan Penetapan Kadar Kurkumin dalam Sampel Rheumakur®... Lampiran 10. Data Uji Statistik ...
xviii
INTISARI
Kurkumin diketahui memiliki efek farmakologi sebagai antiinflamasi, hepatoprotektor, antioksidan serta antikanker sehingga banyak digunakan sebagai komponen utama obat tradisional golongan obat herbal terstandar (OHT). Aktifitas farmakologi kurkumin tergantung pada ketepatan dan keseragaman dosis. Berdasarkan penjelasan di atas, dibutuhkan adanya penelitian untuk menetapkan kadar kurkumin dalam suatu sediaan OHT Rheumakur® untuk menjamin mutu dan kualitas sediaan OHT.
Penelitian ini bersifat non eksperimental deskriptif. Kromatografi Cair Kinerja Tinggi (KCKT) fase terbalik yang digunakan adalah kondisi sistem yang optimal dan memenuhi parameter validasi. Sistem KCKT fase terbalik yang optimal menggunakan fase diam oktadesilsilan (C18), fase gerak metanol : asam asetat glasial 2% (95:5 v/v), kecepatan alir 1,0 ml/menit dengan detektor visible
pada panjang gelombang 432 nm. Parameter validitas metode yang digunakan adalah selektivitas, linearitas, akurasi, presisi, dan rentang pada kadar 6,5 ppm.
Hasil penelitian menunjukkan bahwa kadar rata-rata kurkumin yang terdapat dalam sediaan padat OHT merk Rheumakur® yang beredar dipasaran untuk setiap apoteknya masing-masing 39,6350 ± 1,5242; 39,5934 ± 0,3594; dan 47,2658 ± 0,8192 % (b/b) dengan nilai CV masing-masing 3,8456%; 0,9078%; dan 1,7331%. Reprodusibilitas kadar tiap apotek menunjukkan bahwa terdapat perbedaan bermakna apotek 1 dengan apotek 3 serta apotek 2 dan apotek 3. Pada apotek 1 dan 2 tidak memiliki perbedaan bermakna.
Kata kunci: kurkumin, KCKT, penetapan kadar, Rheumakur®
xix
Curcumin is known to have pharmacological effects as an anti-inflammatory, hepatoprotector, antioxidant and anticancer so widely used as a major component of traditional medicine standardized herbal drug classes (OHT). Pharmacological activity of curcumin depends on the accuracy and uniformity of dosage. Based on the explanation above, it takes a study to determine levels of curcumin in a preparation OHT Rheumakur ® to ensure the quality and the quality of preparations OHT.
This was a non-experimental descriptive. High Performance Liquid Chromatography (HPLC) reversed phase system used was the optimal condition and meet the validation parameters. Reversed phase HPLC system using the optimal stationary phase octadecylsylane (C18), mobile phase methanol: glacial acetic acid 2% (95:5 v / v), flow rate 1.0 ml / min with visible detector at wavelength 432 nm. Parameter validity of the method used is the selectivity, linearity, accuracy, precision, and range in levels of 6.5 ppm.
The results showed that the average content of curcumin contained in solid dosage OHT Rheumakur ® brand in the market for each respective apoteknya 39.6350 ± 1.5242, 39.5934 ± 0.3594, and 47.2658 ± 0, 8192% (w / w) with each CV value 3.8456%, 0.9078% and 1.7331%. The reproducibility levels of each pharmacy showed that there were significant differences pharmacy pharmacy 1 with 3 and 2 and pharmacy 3. At pharmacy 1 and 2 do not have significant differences.
1
BAB I
PENGANTAR
A. Latar Belakang
Penggunaan obat tradisional untuk menyembuhkan berbagai macam penyakit saat ini sudah cukup banyak digunakan di masyarakat. Menurut data WHO (World Health Organization), sebanyak 80% dari populasi masyarakat di negara-negara yang berada di benua Asia dan Afrika, menggunakan obat tradisional untuk terapi (WHO, 2005). Obat tradisional yang banyak digunakan dan beredar di pasaran adalah kunyit yang kandungan zat aktifnya kurkumin. Salah satu contoh produk obat tradisional yang mengandung kurkumin adalah Obat Herbal Terstandar (OHT) Rheumakur®.
Kurkumin merupakan senyawa berwarna kuning-orange yang terkandung di dalam tanaman bergenus Curcuma sp. Senyawa ini diketahui memiliki efek farmakologi sebagai antiinflamasi, hepatoprotektor, antioksidan serta antikanker (Anonim, 2002). Dalam penggunaannya sebagai obat yang berkhasiat menyembuhkan reumatik, maka efek farmakologi kurkumin yang diinginkan ialah sebagai antiinflamasi. Kurkumin sebagai antiinflamasi memiliki mekanisme kerja dengan menghambat lipooksigenase dan siklooksigenase 2 (Anonim, 2002).
Produk OHT Rheumakur® yang beredar di pasaran dalam bentuk sediaan kapsul lunak diproduksi oleh PT Phytochemindo. Dalam produk Rheumakur® terdapat kandungan kurkuminoid 10 mg dan minyak atsiri dari ekstrak kunyit dan temulawak sebesar 100 mg. Rheumakur® diklaim berkhasiat membantu mengatasi
timbulnya rasa nyeri yang sering dikeluhkan penderita penyakit reumatik (Anonim, 2011).
Pada kemasan sampel OHT Rheumakur® tertulis bahwa kadar kurkumin dalam bentuk kurkuminoid adalah 10 mg. Dosis kurkumin tersebut dapat berkurang akibat suhu yang tidak dijaga selama proses distribusi maupun penyimpanan di setiap apotek. Suhu dapat mempengaruhi kestabilan kurkumin. Perubahan kestabilan kurkumin dapat mempengaruhi kadar kurkumin yang ada di dalam kapsul. Berkurangnya kadar kurkumin ini dapat mempengaruhi efek farmakologi yang diinginkan.
Berdasarkan penjelasan di atas, dibutuhkan adanya penelitian untuk menetapkan kadar kurkumin dalam suatu sediaan OHT Rheumakur® untuk menjamin mutu dan kualitas sediaan OHT. Penjaminan mutu berguna untuk menjamin khasiat dan keamanan produk OHT Rheumakur®.
Penelitian mengenai penetapan kadar kurkumin dalam sediaan OHT dengan menggunakan metode KCKT fase terbalik selektif karena metode ini dapat memisahkan senyawa dalam campuran multikomponen dengan sensitifitas yang tinggi sehingga diperoleh pemisahan yang baik. Metode KCKT juga merupakan metode yang cocok untuk analisis kuantitatif senyawa dalam campuran karena tidak perlu dilakukan proses pemisahan senyawa tersebut terlebih dahulu (Johnson dan Stevenson, 1978).
3
menggunakan metode KCKT fase terbalik. Pada penelitian tentang optimasi metode penetapan kadar kurkumin dalam sediaan padat OHT dengan metode KCKT fase terbalik, didapatkan kondisi KCKT yang optimal, yaitu fase gerak metanol p.a : asam asetat glasial 2% (95:5, pH 4,0) dan flow rate 1,0 mL/menit serta nilai resolusi ≥ 1,5 (Kusmiyanti, 2011). Sedangkan pada tahap validasi penetapan kadar kurkumin dalam sediaan padat OHT dengan metode KCKT fase terbalik telah memenuhi parameter akurasi, presisi, linearitas dan spesifisitas pada kadar 6,5 ppm (Nugroho, 2011).
1. Permasalahan
a. Berapakah kadar kurkumin dalam sediaan kapsul lunak OHT Rheumakur® yang beredar di pasaran?
b. Apakah terdapat perbedaan kadar kurkumin pada sediaan kapsul lunak OHT Rheumakur® yang diperoleh dari apotek yang berbeda dengan nomor batch yang sama?
2. Keaslian penelitian
Berbagai penelitian terhadap kurkumin telah dilakukan dari ekstraksi, sintesis, aktivitas farmakologisnya hingga penetapan kadarnya dalam suatu sediaan obat. Pemisahan kurkumin dengan RP-HPLC pernah dilakukan dengan komposisi fase gerak asetonitril:asam asetat 7,6% (55:45) (Yang, Pan, and Xu, 2006). Penelitian dengan judul “Curcumin Quantification in Dosage Forms using High Performance Liquid Chromatography” juga pernah dilakukan menggunakan fase diam C18 dengan komposisi fase gerak asetonitril:asam asetat 2% (45:55)
(Musfiroh, Indriyati, Susilawati, dan Percekawati, 2007). Namun penetapan kadar kurkumin dalam sediaan OHT merk Rheumakur® dengan metode KCKT fase terbalik dengan fase gerak campuran metanol p.a:asam asetat glasial 2% (95:5),
flow rate 1,0 ml/menit belum pernah dilakukan.
3. Manfaat penelitian
a. Manfaat praktis. Penelitian ini dapat memberikan pengetahuan mengenai kualitas dan mutu sediaan OHT yang berhubungan dengan keamanan dan khasiat penggunaannya.
b. Manfaat metodologis. Penelitian ini dapat dijadikan salah satu acuan untuk analisis penetapan kadar kurkumin dalam sampel OHT dengan metode KCKT fase terbalik.
B. Tujuan Penelitian
1. Melakukan penetapan kadar kurkumin pada sediaan kapsul lunak OHT Rheumakur® yang beredar di pasaran dengan metode KCKT fase terbalik. 2. Menganalisis hasil penetapan kadar kurkumin pada sediaan kapsul lunak
5
BAB II
PENELAAHAN PUSTAKA
A. Kurkumin
Kurkumin merupakan senyawa fitokimia yang berwarna kuning-orange yang secara praktis tidak larut dalam air. Kurkumin atau diferuloilmetan merupakan senyawa yang terdapat dari ekstrak tanaman bergenus Curcuma sp.
Senyawa ini diperoleh dengan ekstraksi menggunakan etanol. Struktur dari Kurkumin (C21H20O6) pertama kali ditemukan pada tahun 1815 oleh Vogel dan Pellatier dan pada tahun 1910 disebut diferuloilmetan (Aggarwal, Kumar, Shishodia, 2005). Kurkumin tidak larut dalam air namun larut dalam etanol atau dimetilsulfoksida. Kurkumin memiliki melting point 183°C, dengan rumus molekul C21H20O6 dan memiliki berat molekul 368,37 g/mol (Kiswanto, 2005).
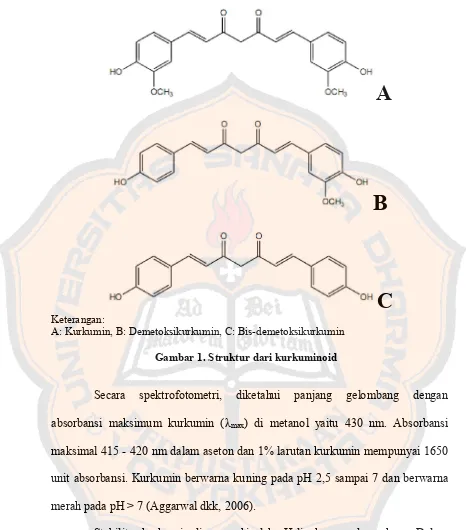
Selain kurkumin, terdapat juga senyawa derivat yang lain dan senyawa derivat ini dinamakan "Kurkuminoid". Kurkuminoid ini meliputi kurkumin, demetoksikurkumin, bis-demetoksikurkumin, dan komponen lainnya. Dalam kurkuminoid komersial itu mengandung kurkumin (77%), demetoksikurkumin (18%), dan bis-demetoksikurkumin (5%).
A
B
C
Keterangan:A: Kurkumin, B: Demetoksikurkumin, C: Bis-demetoksikurkumin
Gambar 1. Struktur dari kurkuminoid
Secara spektrofotometri, diketahui panjang gelombang dengan absorbansi maksimum kurkumin (λmax) di metanol yaitu 430 nm. Absorbansi maksimal 415 - 420 nm dalam aseton dan 1% larutan kurkumin mempunyai 1650 unit absorbansi. Kurkumin berwarna kuning pada pH 2,5 sampai 7 dan berwarna merah pada pH > 7 (Aggarwal dkk, 2006).
7
lebih lambat dibanding pH >7. Ketidakstabilan kurkumin pada pH alkali disebabkan oleh gugus metilen aktif (Tonnasen dan Karlsen, 1985).
O O
Gambar 2. Reaksi degradasi kurkumin pada pH basa (Stankovic, 2004)
O O
Gambar 3. Produk degradasi kurkumin oleh cahaya (Sudaryono, Nourmamode, Gardrat, Grelier, Bravic, Chasseau, Castellan, 2003)
B. Rheumakur®
Rheumakur® merupakan obat herbal terstandar yang diproduksi oleh PT Phytochemindo dengan sediaan berbentuk kapsul lunak. Komposisi Rheumakur® sendiri terdiri atas 10 mg ekstrak kurkuminoid yang telah distandardisasi dan 100 mg minyak atsiri kunyit dan temulawak. Rheumakur® berkhasiat membantu mengatasi timbulnya rasa nyeri yang sering dikeluhkan penderita penyakit rheumatik. Selain itu, Rheumakur® dapat mencegah peradangan akibat peroksidasi lemak (Anonim, 2011).
Melalui penelitian farmakologi dan kimia telah membuktikan bahwa minyak atsiri Curcuma xanthorhiza (temulawak) yang mengandung xanthorrhizol dan kurkumin memiliki aktivitas anti-inflamasi. Dalam minyak atsiri Curcuma domestica mengadung tumerone dan tumerole yang juga memiliki aktivitas inflamasi. Adanya kurkuminoid akan memperpanjang dan memperkuat daya anti-inflamasi minyak atsiri kunyit dan temulawak. Selain itu, kombinasi kurkuminoid dan minyak atsiri temulawak, kunyit juga membantu melarutkan lemak sehingga dapat mencegah peradangan akibat peroksidasi lemak (Anonim, 2011).
9
C. Kapsul Lunak
Kapsul cangkang lunak terbuat dari gelatin. Bentuknya sedikit lebih tebal daripada kapsul cangkang keras dan dapat diplastisasi dengan penambahan senyawa poliol, seperti sorbitol atau gliserin. Kapsul lunak dapat mengandung pigmen atau pewarna, bahan opak seperti titanium dioksida, pengawet,pengharum dan pemanis/sukrosa 5 %. Cangkang gelatin lunak umumnya mengandung air 6-13 % (Direktorat Jendral Pengawasan Obat dan Makanan Republik Indonesia, 1995).
Keseragaman bobot pada kapsul lunak dapat dilakukan dengan menimbang 10 kapsul utuh satu per satu. Kemudian buka kapsul dengan alat pemotong yang bersih dan kering seperti pisau atau gunting yang tajam, keluarkan isinya, lalu cuci cangkang kapsul dengan eter. Biarkan sisa pelarut cuci menguap pada suhu kamar dalam waktu 30 menit, cegah adanya penarikan atau kehilangan lembab. Timbang seluruh bagian cangkang kapsul dan hitung bobot netto isi kapsul dan bobot rata-rata tiap isi kapsul. Hitung jumlah zat aktif dalam tiap kapsul dengan anggapan semua zat aktif terdistribusi homogen dalam kapsul (Direktorat Jendral Pengawasan Obat dan Makanan Republik Indonesia, 1995).
D. Obat Herbal Terstandar
Menurut BPOM (Badan Pengawas Obat dan Makanan), OHT adalah sediaan obat bahan alam yang telah dibuktikan keamanan dan khasiatnya secara ilmiah dengan uji praklinik dan bahan bakunya telah distandardisasi. Setiap OHT yang beredar di wilayah Indonesia wajib memiliki izin edar dari Kepala Badan
POM yang diperoleh melalui pendaftaran. Oleh karena itu, agar dapat beredar di masyarakat OHT harus memiliki syarat sebagai berikut:
1. Menggunakan bahan berkhasiat dan bahan tambahan yang memenuhi persyaratan mutu, keamanan dan kemanfaatan/khasiat;
2. Dibuat sesuai dengan ketentuan Pedoman Cara Pembuatan Obat Tradisional yang Baik (CPOTB) atau Cara Pembuatan Obat yang Baik (CPOB) yang berlaku;
3. Penandaan berisi informasi lengkap dan obyektif yang dapat menjamin penggunaan obat tradisional, obat herbal terstandar dan fitofarmaka secara tepat, rasional dan aman sesuai hasil evaluasi dalam rangka pendaftaran (Badan Pengawas Obat dan Makanan RI, 2005).
Obat Herbal Terstandar dilarang mengandung bahan kimia hasil isolasi atau sintetik berkhasiat, narkotika atau psikotropika, bahan yang dilarang sesuai dalam lampiran yang ditetapkan BPOM serta hewan atau tumbuhan yang dilindungi oleh peraturan perundang-undangan yang berlaku. Larangan lainnya adalah obat tradisional dilarang dalam bentuk sediaan intravaginal, tetes mata, parenteral dan suppositoria (kecuali untuk wasir). Penggunaan etil alkohol dalam sediaan obat tradisional juga tidak boleh lebih besar dari 1% kecuali dalam bentuk sediaan tingtur yang pemakaiannya dengan pengenceran (Badan Pengawas Obat dan Makanan RI, 2005).
11
E. Cara Pembuatan Obat Tradisional yang Baik
Cara Pembuatan Obat Tradisional yang Baik (CPOTB) bertujuan untuk menjamin agar produk yang dihasilkan senantiasa memenuhi persyaratan yang berlaku. Dilakukan langkah-langkah agar obat tradisional yang dihasilkan aman, bermanfaat, dan bermutu; keamanan dan mutu obat tradisional tergantung pada bahan baku, bangunan, prosedur dan pelaksanaan proses pembuatan, peralatan yang digunakan, pengemas termasuk bahannya serta personalia yang terlibat dalam pembuatan obat tradisional; dan CPOTB merupakan cara pembuatan obat tradisional yang diikuti dengan pengawasan menyeluruh, dan bertujuan untuk menyediakan obat tradisional yang memenuhi persyaratan berlaku (Kementrian Kesehatan Republik Indonesia, 1994).
Penerapan CPOTB merupakan persyaratan kelayakan dasar untuk menerapkan sistem jaminan mutu yang diakui dunia internasional. Untuk itu sistem mutu hendaklah dibangun, dimantapkan, dan diterapkan sehingga kebijakan yang ditetapkan dan tujuan yang diinginkan dapat dicapai (Kepala Badan Pengawas Obat dan Makanan Republik Indonesia, 2005).
1. Personalia
Personalia diharapkan memiliki pengetahuan, pengalaman, ketrampilan dan kemampuan yang sesuai dengan tugas dan fungsinya serta tersedia dalam jumlah yang cukup. Personalia diharapkan dapat menangani tugas yang dibebankan kepadanya dalam keadaan sehat. Personil yang terlibat dalam kegiatan pembuatan hendaklah dilatih sesuai prinsip-prinsip CPOTB (Kepala Badan Pengawas Obat dan Makanan Republik Indonesia, 2005).
2. Bangunan
Bangunan untuk industri obat tradisional menjamin aktifitas industri agar dapat berlangsung aman. Bangunan industri obat tradisional hendaklah memenuhi persyaratan: higiene dan sanitasi; tahan terhadap pengaruh cuaca, serta dapat mencegah masuknya rembesan dan masuk bersarangnya serangga, binatang pengerat, burung atau binatang lainnya; memudahkan dalam pelaksanaan kerja, pembersihan dan pemeliharaan; dan memiliki ruangan-ruangan pembuatan yang rancang bangun dan luasnya sesuai dengan bentuk, sifat dan jumlah produk yang dibuat, jenis dan jumlah peralatan yangdigunakan, jumlah karyawan yang bekerja serta fungsi ruangan (Kepala Badan Pengawas Obat dan Makanan Republik Indonesia, 2005).
3. Peralatan
Peralatan yang digunakan dalam pembuatan produk hendaklah memiliki rancang bangun konstruksi yang tepat, ukuran yang memadai serta ditempatkan dengan tepat, sehingga mutu yang dirancang bagi tiap produk terjamin secara seragam dari bets ke bets, serta untuk memudahkan pembersihan dan perawatannya (Kepala Badan Pengawas Obat dan Makanan Republik Indonesia, 2005).
4. Sanitasi dan higiene
13
5. Pengolahan dan pengemasan
Pengolahan dan pengemasan hendaklah mengikuti cara yang telah ditetapkan oleh industri sehingga dapat menjamin produk yang dihasilkan senantiasa memenuhi persyaratan yang berlaku. Hal-hal yang termasuk dalam pengolahan dan pengemasan yaitu verifikasi, pencemaran, sistem penomoran kode produksi, penimbangan dan penyerahan, pengolahan, pengemasan, dan penyimpanan (Kepala Badan Pengawas Obat dan Makanan Republik Indonesia, 2005).
6. Pengawasan mutu
Pengawasan mutu merupakan bagian yang essensial dari CPOTB. Rasa ketertarikan dan tanggung jawab semua unsur dalam semua rangkaian pembuatan adalah mutlak untuk menghasilkan produk yang bermutu mulai dari bahan awal sampai pada produk jadi. Untuk keperluan tersebut bagian pengawasan mutu hendaklah merupakan bagian yang tersendiri (Kepala Badan Pengawas Obat dan Makanan Republik Indonesia, 2005).
7. Inspeksi diri
Program inspeksi diri hendaklah dirancang untuk mengevaluasi pelaksanaan CPOTB dan untuk menetapkan tindak lanjut. Inspeksi diri ini hendaklah dilakukan secara teratur. Tindakan perbaikan yang disarankan hendaklah dilaksanakan. Untuk pelaksanaan inspeksi diri hendaklah ditunjuk tim inspeksi yang mampu menilai secara obyektif pelaksanaan CPOTB. Hendaklah dibuat prosedur dan catatan mengenai inspeksi diri (Kepala Badan Pengawas Obatdan Makanan Republik Indonesia, 2005).
8. Dokumentasi
Dokumentasi pembuatan produk merupakan bagian dari sistem informasi manajemen yang meliputi spesifikasi, label/etiket, prosedur, metoda dan instruksi, catatan dan laporan serta jenis dokumentasi lain yang diperlukan dalam perencanaan, pelaksanaan, pengendalian serta evaluasi seluruh rangkaian kegiatan pembuatan produk. Dokumentasi sangat penting untuk memastikan bahwa setidap petugas mendapat instruksi secara rinci dan jelas mengenai bidang tugas yang harus dilaksanakannya, sehingga memperkecil risiko terjadinya salah tafsir dan kekeliruan yang biasanya timbul karena hanya mengandalkan komunikasi lisan (Kepala Badan Pengawas Obat dan Makanan Republik Indonesia, 2005).
9. Penanganan terhadap produk diperedaran
Penarikan kembali produk yang berupa penarikan kembali satu atau beberapa bets atau seluruh produk tertentu dari semua mata rantai distribusi. Penarikan kembali dilakukan apabila ditemukan adanya produk yang tidak memenuhi persyaratan atau atas dasar pertimbangan adanya efek yang tidak diperhitungkan yang merugikan kesehatan. Penarikan kembali seluruh produk tertentu dapat merupakan tindak lanjut penghentian pembuatan satu jenis produk yang bersangkutan (Kepala Badan Pengawas Obat dan Makanan Republik Indonesia, 2005).
F. Standardisasi Ekstrak
15
pelarut yang sesuai. Ekstrak tumbuhan obat yang dibuat dari simplisia nabati dapat digunakan sebagai bahan awal, bahan antara, atau bahan produk jadi (Badan Pengawas Obat dan Makanan Republik Indonesia, 2005).
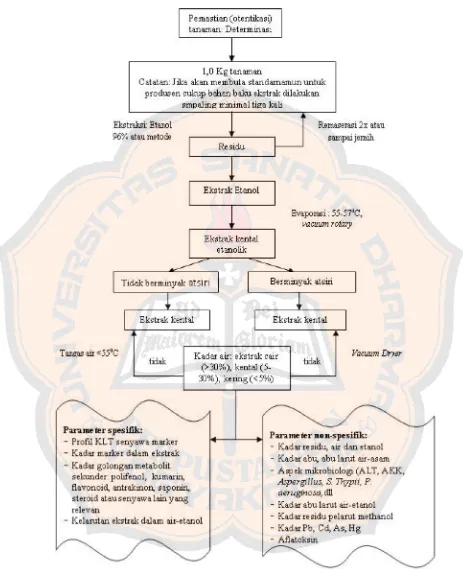
Mayoritas penggunaan bahan obat berbasis herbal di Indonesia masih bersifat tidak terukur baik kepastian tanaman, takaran, cara penyiapan sehingga tidak menjamin konsistensi khasiat. Tujuan standardisasi adalah menjaga konsistensi dan keseragaman khasiat dari obat herbal. Standardisasi melibatkan pemastian kadar senyawa aktif farmakologis melalui analisis kuantitatif yang akan menjamin keseraagaman khasiat (Saifudin, Rahayu, Teruna, 2011).
Standardisasi obat herbal meliputi 2 aspek, yaitu aspek parameter spesifik dan non-spesifik. Aspek parameter spesifik berfokus pada senyawa atau golongan senyawa yang bertanggung jawab terhadap aktivitas farmakologi. Aspek parameter non-spesifik berfokus pada aspek kimia, mikrobiologi dan fisis yang mempengaruhi keamanan konsumen dan stabilitas, misalnya kadar logam berat, aflatoksin, kadar air dan lain-lain (Saifudin dkk, 2011)
17
G. Spektrofotometri Visibel
Spektrofotometri visibel merupakan suatu teknik spektroskopik menggunakan sumber radiasi elektromagnetik sinar tampak (380-780 nm) dengan menggunakan spektrofotometer. Pengukuran absorbansi dalam spektrofotometri sinar tampak digunakan untuk analisis kualitatif dan kuantitatif (Khopkar, 1990). Sinar tampak memberikan energi yang cukup untuk terjadinya transisi elektronik. Transisi yang terjadi pada suatu molekul dengan struktur yang berbeda adalah tidak sama satu dengan molekul lain sehingga spektra absorpsinya juga berbeda. Dengan demikian dapat bermanfaat sebagai analisis kualitatif. Banyaknya sinar yang diabsorpsi pada panjang gelombang tertentu sebanding dengan banyaknya molekul yang menyerap radiasi sehingga dapat juga digunakan sebagai analisis kuantitatif (Rohman dan Gandjar, 2007).
Suatu molekul dapat memberikan serapan REM jika memiliki gugus kromofor yaitu gugus penyerap dalam molekul. Pada senyawa organik dikenal pula gugus auksokrom yaitu gugus tidak jenuh yang terikat langsung pada kromofor. Gugus auksokrom dapat mengubah panjang gelombang serapan dan intensitas serapan maksimum (Sastrohamidjojo, 2002).
Ikatan terkonjugasi merupakan ikatan rangkap yang berselang-seling dengan satu ikatan tunggal. Dalam orbital molekul, elektron π mengalami delokalisasi lanjut dengan adanya ikatan terkonjugasi. Adanya efek delokalisasi ini akan menyebabkan penurunan tingkat energi π* dan memberikan pengurangan karakter antiikatan. Sebagai konsekuensinya, panjang gelombang molekul yang
mempunyai ikatan rangkap terkonjugasi akan mengalami pergeseran batokromik (Rohman dan Gandjar, 2007).
Besarnya REM yang dapat diserap oleh kromofor dapat digambarkan oleh dua hukum yaitu hukum Lambert dan Beer. Hukum Lambert menyatakan bahwa bila cahaya monokromatik melewati medium tembus cahaya, laju berkurangnya intensitas oleh bertambahnya ketebalan berbanding lurus dengan intensitas cahaya. Hukum Beer menyatakan bahwa intensitas berkas cahaya monokromatik berkurang secara eksponensial dengan bertambahnya konsentrasi zat penyerap linier (Bassett, Denney, Jeffery, dan Medham, 1994).
H. Kromatografi Cair Kinerja Tinggi (KCKT)
1. Definisi dan instrumentasi KCKT
19
dapat memisahkan zat-zat yang tidak menguap atau tidak tahan panas tanpa perlu membuat derivat yang mudah menguap (Direktorat Jenderal Pengawasan Obat dan Makanan RI, 1995).
Pada KCKT menggunakan sistem kromatografi partisi dengan polaritas yang berbeda dari fase diam dan fase geraknya. Bila fase gerak bersifat polar dan fase diam bersifat non-polar maka dikenal dengan kromatografi fase balik (Direktorat Jenderal Pengawasan Obat dan Makanan RI, 1995). Peralatan KCKT dapat dilihat pada gambar 7.
Gambar 7. Peralatan KCKT (Kazakevich and Nair, 1996)
Hal-hal yang harus diperhatikan dalam analisis menggunakan KCKT, yaitu fase gerak, kolom, dan detektor.
a. Fase gerak
Fase gerak pada sistem KCKT sangat berpengaruh pada tambatan sampel dan pemisahan komponen dalam campuran zat. Bila digunakan sistem kromatografi fase terbalik maka kandungan utama fase geraknya ialah air (Munson, 1994).
b. Kolom
Kolom yang digunakan pada KCKT ialah kolom kemasan fase terikat. Fase diam yang biasanya digunakan pada sistem kromatografi fase terbalik ialah oktadesilsilan (ODS) (Munson, 1984)
c. Detektor
Persyaratan detektor KCKT adalah sensitifitas harus tinggi (10-8 – 10-15 g analit/detik); kestabilan dan reprodusibilitas yang baik; memberikan respon yang linier terhadap konsentrasi analit; dapat bekerja pada temperatur kamar sampai 400°C; tidak terpengaruh oleh perubahan temperatur dan kecepatan fase gerak; mudah didapat dan mudah dioperasikan; selektif terhadap berbagai macam analit di dalam fase gerak; tidak merusak analit; dapat menghilangkan “zone broadening” dengan adanya pengaruh minimal internal volume (Mulja dan Suharman, 1995).
2. Kromatografi Partisi Fase Terbalik
21
Dalam kromatografi, K didefinisikan sebagai perbandingan konsentrasi analit dalam fase diam (Cs) dan dalam fase gerak (Cm) (Rohman dan Gandjar, 2007).
(1)
Kolom yang biasa digunakan dalam kromatografi partisi fase terbalik adalah kolom dengan kemasan fase terikat yang memiliki sifat stabil karena fase diamnya terikat secara kimia pada penyangga, sehingga tidak mudah terelusi oleh fase gerak. Penyangga pada fase terikat biasanya terbuat dari silika yang sudah diseragamkan, berpori, dan umumnya mempunyai diameter 3,5 atau 10 µm (Skogg dkk., 1998).
Pada KCKT partisi fase terbalik biasanya mengandung bagian organik yang terikat secara kimia dengan gugus silanol pada permukaan silika. Bagian organik tersebut umumnya hidrokarbon rantai panjang, sehingga fase gerak umumnya polar. Gugus silanol permukaan dapat direaksikan dengan berbagai cara menempelkan berbagai jenis gugus organik. Kemasan fase terikat dengan tipe ikatan siloksan (Si-O-Si-O) dibuat dengan mereaksikan organoklorosilan dengan gugus silanol pada permukaan silika gel. Reaksi pembuatan kolom oktadesilsilan (ODS) gugus silanol dan oktadesilklorosilan dapat dilihat pada gambar 8.
Si OH Cl Si (CH2)17CH3 Si O Si (CH2)17CH3 HCl
Gambar 8. Reaksi pembuatan kolom oktadesilsilan
Gugus yang ditempelkan pada silanol pada umumnya adalah hidrokarbon rantai panjang. Panjang pendeknya rantai karbon mempengaruhi tertambatnya senyawa pada fase diam.
Gugus silanol yang tidak bereaksi karena adanya halangan sterik dapat memberikan kepolaran yang tidak dikehendaki dan menyebabkan pengekoran pada puncak kromatogram. Untuk mengurangi jumlah gugus silanol yang masih bebas, reaksi dilanjutkan dengan penambahan trimetilklorosilan yang dapat mencapai gugus silanol karena ukurannya yang lebih kecil dibandingkan organoklorosilan lain. Penambahan trimetilklorosilan dapat menutupi banyak gugus silanol yang masih bebas, namun tidak semua gugus tersebut dapat tertutupi (Skoog dkk., 1998).
Fase gerak yang sering digunakan adalah campuran metanol atau asetonotril dengan air atau dengan larutan buffer. Untuk analit yang bersifat asam atau basa lemah, peranan pH sangat penting karena jika pH fase gerak tidak diatur maka analit akan mengalami ionisasi sehingga ikatan dengan fase diam akan menjadi lemah jika dibandingkan dengan bentuk tidak terionisasi, spesies yang terionisasi akan terelusi lebih cepat (Rohman dan Ganjar, 2007).
3. Waktu retensi dan resolusi
23
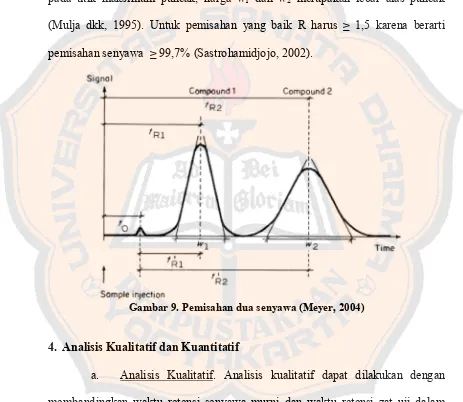
Resolusi (Rs) adalah jarak antara dua puncak dibagi dengan rata-rata lebar dasar puncak dapat diukur dengan persamaan:
(2)
Harga tR1 dan tR2 merupakan waktu retensi senyawa yang dapat diukur pada titik maksimum puncak, harga w1 dan w2 merupakan lebar alas puncak (Mulja dkk, 1995). Untuk pemisahan yang baik R harus ≥ 1,5 karena berarti pemisahan senyawa ≥ 99,7% (Sastrohamidjojo, 2002).
Gambar 9. Pemisahan dua senyawa (Meyer, 2004)
4. Analisis Kualitatif dan Kuantitatif
a. Analisis Kualitatif. Analisis kualitatif dapat dilakukan dengan membandingkan waktu retensi senyawa murni dan waktu retensi zat uji dalam sampel. Respon yang dihasilkan berupa tinggi peak maupun luas area peak
b. Analisis Kuantitatif. Analisis kuantitatif menggunakan kromatogram yang dihasilkan dari pemisahan KCKT. Cara analisis kuantitatif KCKT yang digunakan yaitu dapat berdasarkan tinggi puncak dan berdasarkan luas puncak. Tinggi dan luas puncak berkaitan secara proporsional atas kadar ataupun jumlah analit tertentu yang terdapat dalam sampel. Apabila kromatogram yang dihasilkan mengalami pelebaran puncak maka analisis berdasarkan tinggi puncak menjadi tidak teliti lagi. Cara yang tepat dalam perhitungan kuantitatif yaitu berdasarkan luas pucak. Analisis kuantitatif berdasarkan luas puncak lebih disukai karena tidak dipengaruhi oleh pelebaran pita (Noegrohati, 1994).
I. Landasan Teori
25
Cara Pembuatan Obat Tradisional yang Baik (CPOTB) bertujuan untuk menjamin agar produk yang dihasilkan senantiasa memenuhi persyaratan yang berlaku. Dilakukan langkah-langkah agar obat tradisional yang dihasilkan aman, bermanfaat, dan bermutu; keamanan dan mutu obat tradisional tergantung pada bahan baku, bangunan, prosedur dan pelaksanaan proses pembuatan, peralatan yang digunakan, pengemas termasuk bahannya serta personalia yang terlibat
Metode KCKT digunakan untuk menetapkan kadar kurkumin dalam sediaan obat herbal terstandar (OHT) karena memiliki sensitifitas dan selektifitas yang tinggi. Metode KCKT dapat digunakan sebagai analisis kualitatif dan kuantitatif.
J. Hipotesis
1. Kadar kurkumin dalam sediaan kapsul lunak OHT merk Rheumakur® yang terukur sesuai dengan yang tertera dalam kemasan.
2. Kadar kurkumin dalam sediaan kapsul lunak OHT merk Rheumakur® yang terukur dari masing-masing apotek reprodusibel.
26
METODE PENELITIAN
A. Jenis dan Rancangan Penelitian
Penelitian ini termasuk dalam penelitian noneksperimental dengan rancangan penelitian deskriptif, karena tidak ada perlakuan terhadap subyek uji yaitu sediaan kapsul lunak OHT merk Rheumakur®.
B. Variabel Penelitian
1. Variabel bebas
Variabel bebas dalam penelitian ini adalah tempat pengambilan sampel OHT merk Rheumakur®.
2. Variabel tergantung
Variabel tergantung dalam penelitian ini adalah kadar kurkumin yang dihasilkan sampel OHT Rheumakur® pada masing-masing apotek.
3. Variabel pengacau terkendali
Variabel pengacau terkendali pada percobaan ini adalah kemurnian pelarut, cahaya, dan pH. Untuk mengatasinya digunakan pelarut yang pro analysis
27
C. Definisi Operasional
1. Kurkumin merupakan senyawa yang terdapat dalam sampel kapsul lunak OHT merk Rheumakur®.
2. Sistem Kromatografi Cair Kinerja Tinggi(KCKT) yang digunakan adalah seperangkat alat KCKT fase terbalik dengan fase diam kolom reversed phase
C18 dan fase gerak campuran metanol p.a : asam asetat glasial 2% (95:5) dengan kecepatan alir 1,0 ml/menit.
3. Kadar kurkumin dalam kapsul lunak OHT merk Rheumakur® dinyatakan dalam % b/b.
D. Bahan Penelitian
Bahan-bahan yang digunakan dalam penelitian adalah baku kurkumin (hasil sintesis Prof. Dr. Sudibyo Martono, M.Si., Apt. yang telah melalui konfirmasi struktur dengan metode spektroskopi 1H-NMR dan Mass Spectra, kurkumin ini memiliki titik lebur 181,20-182,40C), metanol p.a (E. Merck), asam asetat glasial p.a (E. Merck), aquabidestilata, kapsul Obat Herbal Terstandar merk Rheumakur® yang mengandung kurkumin.
E. Alat Penelitian
Seperangkat alat spektrofotometri UV-Vis merk Milton Ray Spectronic
3000 Array dengan printer Epson LQ-1170, seperangkat alat KCKT fase terbalik dengan sistem gradien dengan detektor visibel, Shimadzu LC-2010C, kolom oktadesilsilan (C18) merk KNAUER C18 No. 25EE181KSJ (B115Y620) dengan
panjang 250 x 4,6 mm, packing KROMASIL 100-5 C18, seperangkat komputer merk Dell B6RDZ1S Connexant System RD01-D850 A03-0382 JP France S.A.S, printer HP Deskjet D2566 HP-024-000 625 730, ultrasonikator merk Retsch tipe T460 No V935922013 EY, syringe, neraca kasar, neraca analitik Ohaus Carat Series PAJ 1003 (max 60/120 g, min 0,001g, d = 0,01/0,1 mg), penyaring millipore, mikropipet Socorex, vakum, organic solvent membrane filter
(Whatman) ukuran pori (0,45 µm; diameter 47 mm), seperangkat alat gelas (Pyrex), indikator pH universal (kertas pH).
F. Tata Cara Penelitian
1. Pemilihan dan pengambilan sampel
Sampel yang dipilih adalah kapsul lunak OHT merk Rheumakur® dengan nomor batch yang sama dari 3 apotek berbeda dengan expired date Agustus 2013. Dari masing-masing apotek diambil sebanyak 10 buah kapsul untuk uji keseragaman bobot (FI IV).
2. Pembuatan asam asetat 2%
Sebanyak 2,0 ml asam asetat glasial dimasukkan ke dalam labu takar 100,0 ml, ditambahkan aquabidest sampai batas tanda.
3. Pembuatan metanol pH 4 sebagai pelarut
29
4. Pembuatan fase gerak
Fase gerak yang digunakan dalam penelitian ini yaitu campuran metanol
p.a : asam asetat glasial 2% (95:5). Masing-masing komponen fase gerak disaring dengan menggunakan kertas Whatman yang dibantu dengan pompa vaccum dan di degassing menggunakan ultrasonikator selama 15 menit. Pencampuran fase gerak dilakukan di dalam sistem KCKT.
5. Pembuatan larutan baku kurkumin
a. Pembuatan larutan stok kurkumin. Menimbang seksama lebih kurang 10,0 mg serbuk kurkumin dan dimasukkan dalam labu 10,0 ml lalu ditambah dengan metanol p.a pH 4 sampai tanda.
b. Pembuatan larutan intermediet kurkumin. Sebanyak 1,0 ml diambil dari larutan stok kurkumin dan dimasukkan dalam labu 10,0 ml diencerkan dengan metanol p.a pH 4 sampai tanda.
c. Pembuatan seri larutan baku kurkumin. Sebanyak 0,15 ml; 0,25 ml; 0,35 ml; 0,45 ml; 0,55 ml; dan 0,65 ml diambil dari larutan intermediet kurkumin. Masing-masing larutan kemudian diencerkan dengan metanol p.a pH 4 dalam labu ukur 10,0 ml sampai tanda sehingga diperoleh 6 seri larutan baku kurkumin (1,5 ppm; 2,5 ppm; 3,5 ppm; 4,5 ppm; 5,5 ppm; 6,5 ppm). Masing-masing larutan disaring dengan millipore dan di degassing menggunakan ultrasonikator selama 15 menit.
6. Penentuan panjang gelombang maksimum kurkumin
Penentuan panjang gelombang maksimum dilakukan dengan merekam spektra larutan baku kurkumin 1 ppm; 3,5 ppm; dan 6 ppm pada rentang panjang
gelombang 400-500 nm dengan menggunakan spektrofotometer UV-Vis terhadap blanko metanol p.a pH 4. Dari spektra serapan dapat diketahui panjang gelombang yang dihasilkan dari tiap konsentrasi. Tentukan panjang gelombang yang akan digunakan pada sistem KCKT yaitu panjang gelombang dimana ketiga konsentrasi tersebut menghasilkan serapan yang maksimum. Pengerjaan larutan kurkumin dilakukan di tempat yang terlindungi dari cahaya.
7. Pembuatan kurva baku kurkumin
Tiap baku dengan konsentrasi 2,5 ppm; 3,5 ppm; 4 ppm; 4,5 ppm; 5,0 ppm; dan 5,5 ppm diinjeksikan sebanyak 10,0 µl dengan kecepatan alir 1,0 ml/menit dan detektor KCKT yang diatur pada panjang gelombang maksimum. Amati luas area di bawah kurva (AUC) yang dihasilkan oleh masing-masing konsentrasi.
8. Optimasi waktu ekstraksi kurkumin dalam sampel Rheumakur®
31
dioptimasi. Amati respon AUC yang dihasilkan dari masing-masing waktu ekstraksi.
9. Penetapan kadar
Masing-masing kapsul lunak dari setiap apotek diambil sebanyak 10 buah dan timbang secara seksama bobotnya. Keluarkan semua isi kapsulnya dan kemudian dihomogenkan. Isi kapsul yang sudah homogen ditimbang dengan seksama lebih kurang 50,0 mg. Larutkan dengan 10,0 mL metanol p.a pH 4 dan diekstraksi menggunakan ultrasonikator dengan waktu ekstraksi yang optimal. Sebanyak 185 µL larutan dimasukkan ke labu ukur 10,0 mL dan tambahkan metanol p.a pH 4 hingga tanda. Larutan sampel disaring menggunakan millipore
kemudian di-degassing dengan menggunakan ultrasonikator selama 15 menit. Larutan sampel sebanyak 10,0 µL diinjeksikan ke dalam sistem KCKT yang telah dioptimasi. Amati nilai AUC yang dihasilkan. Sampel setiap apotek direplikasi lima kali. Setiap larutan yang mengandung kurkumin harus terlindung dari cahaya.
G. Analisis hasil
Hasil dari penetapan kadar kurkumin dalam kapsul OHT merk Rheumakur® dapat dilihat dari AUC kromatogram yang dihasilkan. Nilai AUC sampel yang diperoleh dimasukkan ke dalam persamaan regresi linier yang diperoleh dari kurva baku. Data AUC yang diperoleh dimasukkan ke dalam persamaan sebagai nilai y dan kemudian kadar kurkumin dalam sampel
Rheumakur® dinyatakan sebagai x. Kadar kurkumin dalam tiap kapsul lunak OHT merk Rheumakur® dari masing-masing apotek dinyatakan dalam % (b/b).
Reprodusibilitas kadar dalam masing-masing batch yang diperoleh dari 3 apotek yang berbeda dapat dilihat dari nilai CV.
Selain itu, diperlukan uji statistik untuk mendukung reprodusibilitas kadar kurkumin dalam sampel OHT Rheumakur® yang diperoleh dari 3 apotek berbeda untuk melihat adanya perbedaan kadar yang bermakna atau tidak. Uji statistik yang dilakukan ialah uji normalitas data Shapiro-Wilk, one way Annova dan uji
53
BAB IV
HASIL DAN PEMBAHASAN
Penetapan kadar kurkumin pada sediaan kapsul lunak Rheumakur® dapat dilakukan dengan menggunakan metode kromatografi cair kinerja tinggi (KCKT) fase terbalik. Metode KCKT yang digunakan telah dioptimasi dan divalidasi sebelum dilakukan proses penetapan kadar.
A. Pemilihan Sampel
Penelitian ini memiliki tujuan untuk penjaminan mutu sampel sediaan OHT yang mengandung kurkumin. Melalui proses penetapan kadar sebagai penjaminan mutu nantinya dapat dijadikan gambaran stabilitas kurkumin selama distribusi dan penyimpanan. Sampel sediaan OHT yang digunakan diambil dari tiga apotek berbeda dengan nomor batch yang sama. Sampel OHT yang digunakan dalam penelitian ini adalah sediaan kapsul lunak merk Rheumakur®.
Sampel diambil dengan menggunakan teknik probabiliy sampling: simple random. Teknik probability sampling merupakan cara yang paling ideal dalam pengambilan sampel karena setiap anggota populasi memiliki peluang yang sama untuk dipilih menjadi sampel. Syarat digunakannya probability sampling adalah dengan adanya daftar subjek dan karakteristiknya yang terdapat pada populasi penelitian. Secara khusus, digunakan simple random karena karakteristik subjek diasumsikan homogen (Dahlan, 2009).
Pengambilan sampel dilakukan dengan mengontak distributor OHT Rheumakur® untuk mengetahui jalur distribusi OHT Rheumakur® di apotek yang terdapat di Jakarta. Setelah didapatkan informasi mengenai apotek-apotek yang terdistribusi OHT Rheumakur®, maka dilakukan pengundian untuk mendapatkan 3 kandidat apotek sebagai tempat pengambilan sampel. Produk OHT Rheumakur® berasal dari nomor batch yang sama untuk mengkondisikan proses produksi dalam keadaan yang sama. Pemilihan dari 3 apotek yang berbeda adalah untuk melihat perbedaan kadar sampel OHT Rheumakur® yang dipengaruhi kondisi penyimpanan dari masing-masing apotek.
35
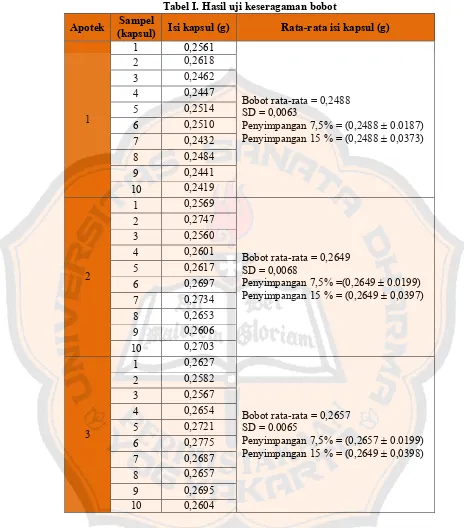
Tabel I. Hasil uji keseragaman bobot
Apotek Sampel (kapsul) Isi kapsul (g) Rata-rata isi kapsul (g)
1
1 0,2561
Bobot rata-rata = 0,2488 SD = 0,0063
Penyimpangan 7,5% = (0,2488 ± 0.0187) Penyimpangan 15 % = (0,2488 ± 0,0373)
2 0,2618
Penyimpangan 7,5% =(0,2649 ± 0.0199) Penyimpangan 15 % = (0,2649 ± 0,0397)
2 0,2747
Penyimpangan 7,5% = (0,2657 ± 0.0199) Penyimpangan 15 % = (0,2649 ± 0,0398)
2 0,2582
Tabel di atas menunjukkan data keseragaman bobot dalam kapsul dengan rata-rata untuk masing-masing apotek yaitu 0,2488; 0,2648; dan 0,2657. Menurut Farmakope Indonesia IV (1995) keseragaman bobot untuk kapsul yang berisi obat tradisional cair tidak lebih dari satu kapsul yang masing-masing bobot isinya
menyimpang dari bobot isi rata-rata lebih besar dari 7,5% dan tidak satu kapsulpun yang bobot isinya menyimpang dari bobot isi rata-rata lebih besar dari 15%. Data keseragaman bobot pada tabel I menunjukkan bahwa pada apotek 1, 2 dan 3 tidak terdapat penyimpangan keseragaman bobot dimana tidak terdapat satupun bobot yang menyimpang sebanyak 7,5% maupun 15%.
B. Pembuatan Pelarut
Metanol p.a pH 4 digunakan sebagai pelarut kurkumin. Menurut hasil orientasi penelitian, kurkumin stabil pada pH 4. Metanol pH 4 dibuat dengan menambahkan asam asetat glasial 2% ke dalam metanol p.a. Penggunaan asam asetat glasial 2% bertujuan mengatur pH untuk menjaga stabilitas dari kurkumin agar tidak terdegradasi. Menurut Tonnesen dan Karlsen (1985), kurkumin dapat terdegradasi menjadi asam ferulat dan vanilin pada pH basa.
C. Pembuatan Fase Gerak
Jenis dan komposisi fase gerak yang digunakan dalam penelitian ini adalah campuran metanol p.a. dan asam asetat glasial 2% dengan perbandingan 95:5 (v/v) dengan indeks polaritas sebesar 5,351. Komposisi fase gerak ini berdasarkan atas penelitian yang dilakukan oleh Kusmiyanti (2011). Dipilih metanol p.a. dan asam asetat glasial 2% sebagai fase gerak karena keduanya dapat melarutkan kurkumin dengan baik.
Komponen fase gerak terlebih dahulu disaring menggunakan penyaring
37
yang dapat menyumbat kolom KCKT. Selanjutnya fase gerak di-degassing
menggunakan ultrasonikator untuk menghilangkan gelembung udara yang dapat mengakibatkan tekanan pada pompa tidak stabil sehingga mempengaruhi proses pembacaan sinyal dalam instrumen KCKT.
Sistem gradien digunakan dalam instrumen KCKT dimana proses pencampuran fase gerak dilakukan di dalam sistem KCKT. Sistem gradien dipilih karena proses kerja menjadi lebih cepat dan efisien. Campuran fase gerak metanol
p.a. dan asam asetat glasial 2% (95:5 v/v) memiliki nilai pH 4 sehingga tidak akan merusak kolom oktadesilsilan (C18) pada instrumen KCKT. Pada pH terlalu asam (pH ≤ 2), C18 bereaksi dengan asam sehingga oktadesilsilan kembali ke bentuk silanol (Gambar 10).
Si O Si (CH2)17CH3 Si OH + Cl Si (CH2)17CH3
silanol
H2O / H+ H+
Gambar 10. Reaksi degradasi kolom C18 pada pH asam ≤ 2
D. Penetapan Panjang Gelombang Maksimal Kurkumin dengan
Spektrofotometri Visibel
Penentuan panjang gelombang maksimal bertujuan untuk memperoleh panjang gelombang dimana kurkumin memberikan serapan yang maksimal untuk dapat dibaca oleh sistem detektor KCKT. Dilakukan scanning λmaks dengan menggunakan spektrofotometer visibel untuk menentukan λmaks kurkumin.
Scanning λmaks dilakukan dengan menggunakan 3 seri kadar dengan tujuan agar hasil yang diperoleh benar-benar panjang gelombang serapan
maksimum dari kurkumin. Pembacaan serapan dilakukan pada rentang panjang gelombang 400-500 nm karena panjang gelombang kurkumin berada pada rentang panjang gelombang tersebut. Dapat dilihat hasil pengukuran λmaks pada gambar 11.
Gambar 11. Spektra serapan kurkumin dengan pelarut campuran metanol p.a dan asam asetat glasial 2% pada pH 4
39
Panjang gelombang yang dipilih sebagai panjang gelombang maksimum detektor dalam sistem KCKT fase terbalik yaitu 432 nm. Dipilih panjang gelombang 432 nm karena paling sering muncul dari ketiga level konsentrasi, khususnya pada konsentrasi rendah dan tinggi.
Syarat suatu senyawa dapat ditetapkan kadarnya secara spektrofotometri visibel yaitu memiliki gugus kromofor, mempunyai auksokrom, atau merupakan senyawa berwarna. Kurkumin memiliki gugus kromofor yang bertanggung jawab dalam penyerapan radiasi sinar. Gugus auksokrom yang dimiliki oleh kurkumin terikat langsung pada gugus kromofor. Gugus auksokrom memiliki peran dalam pergeseran panjang gelombang dan intensitas serapan maksimum dari kurkumin. Gugus kromofor dan auksokrom dari kurkumin ditunjukkan pada gambar 12.
Gambar 12. Gugus kromofor dan auksokrom kurkumin. Keterangan = gugus kromofor, = gugus auksokrom
E. Pembuatan Seri Larutan Baku Kurkumin
Baku kurkumin yang digunakan, yaitu baku kurkumin hasil sintesis Prof. Dr. Sudibyo Martono, M.S., Apt. yang telah dikonfirmasi strukturnya dengan metode spektroskopi 1H-NMR dan Mass Spectra, kurkumin hasil sintesis ini memiliki titik lebur 181,2-182,40C.
Pembuatan kurva baku ini telah dilakukan oleh pada tahap validasi sebelumnya untuk mendapatkan persamaan regresi linear. Persamaan regresi linear ini digunakan untuk menghitung kadar kurkumin dalam sampel Rheumakur®. Penentuan kurva baku kurkumin dengan mengukur AUC kromatogram kurkumin pada 6 konsentrasi kurkumin (1,5; 2,5; 3,5; 4,5; 5,5; dan 6,5 ppm) dan direplikasi sebanyak 3 kali. Persamaan regresi linear disebut baik jika memiliki koefisien korelasi 0,999.
Tabel II. Data kurva baku kurkumin
Replikasi C (ppm) 60.000.000) C (mg/ml x AUC Perhitungan regresi linier
1
41
yang dihasilkan baik. Modifikasi kurva baku dilakukan dengan cara mengalikan kadar terukur dengan bilangan tertentu (60.000.000). Hasilnya diperoleh persamaan y= 1,0358x + 1711,5 dengan nilai r = 0,9996 dan α = 46,01°.
Gambar 13. Kurva baku kurkumin
F. Analisis Kualitatif Kurkumin
Analisis kualitatif bertujuan untuk membuktikan bahwa dalam sampel OHT merk Rheumakur® yang diteliti mengandung kurkumin. Analisis kualitatif dalam penelitian ini dilakukan dengan membandingkan waktu retensi pada baku kurkumin dengan waktu retensi yang dimaksud pada sampel Rheumakur®. Hasil uji kualitatif sampel OHT merk Rheumakur® terhadap baku kurkumin dapat dilihat pada gambar 14.
Gambar 14. Kromatogram baku kurkumin (a) dan kurkumin dalam sampel (b)
Pada kromatogram yang ditunjukkan gambar 14, diketahui bahwa baku kurkumin memiliki waktu retensi 2,682 menit dan kurkumin dalam sampel kapsul lunak OHT merek Rheumakur® memiliki waktu retensi 2,680 menit. Berdasarkan
waktu retensi yang diperoleh, dapat dipastikan bahwa dalam sampel kapsul OHT merek Rheumakur® terdapat kandungan kurkumin.
43
Keterangan: = gugus polar, = gugus nonpolar
Gambar 15. Gugus polar dan non-polar kurkumin
Gugus polar dari kurkumin berinteraksi dengan fase gerak melalui interaksi hidrogen, sedangkan bagian gugus non-polar dari kurkumin berinteraksi dengan fase diam melalui interaksi Van Der Waals. Interaksi antara kurkumin dengan fase diam oktadesilsilan dan fase gerak metanol p.a. : asam asetat glasial 2% (95:5 v/v) dapat dilihat pada gambar 16 dan 17.
Gambar 16. Interaksi kurkumin dengan fase gerak metanol p.a:asam asetat glasial 2% membentuk interaksi hidrogen
Gambar 17. Interaksi kurkumin dengan fase diam oktadesilsilan
Pada gambar 16 dan 17 menunjukkan bahwa interaksi kurkumin dengan fase gerak lebih kuat dibandingkan dengan fase diam. Hal ini disebabkan oleh adanya interaksi hidrogen antara kurkumin dengan fase gerak yang lebih kuat dibandingkan interaksi Van Der Waals antara kurkumin dengan fase diam. Interaksi antara kurkumin dengan fase gerak yang lebih kuat dibandingkan antara kurkumin dengan fase diam menyebabkan kurkumin semakin cepat terelusi keluar dari kolom. Hal tersebut dapat dilihat dari waktu retensi baku kurkumin pada 2,682 menit dan sampel OHT Rheumakur® pada 2,680 menit (gambar 14).
G. Optimasi Waktu Ekstraksi Kurkumin dalam Rheumakur®
45
A
B
D
E
F
Keterangan:A: 5 menit, B: 10 menit, C: 15 menit, D: 20 menit, E: 25 menit, F: 30 menit
47
Hasil kromatogram untuk ekstraksi menggunakan ultrasonikator pada gambar 18 dan tabel III menunjukkan bahwa semakin bertambahnya waktu, respon yang dihasilkan semakin tinggi. Hal ini ditunjukkan dengan bentuk peak
dan nilai AUC yang semakin tinggi. Dengan demikian, dapat disimpulkan bahwa peningkatan waktu ekstraksi akan meningkatkan jumlah kurkumin yang terekstraksi.
Tabel III . Hasil pengukuran AUC sampel dengan variasi waktu menggunakan ultrasonikator
Berdasarkan data yang diperoleh maka dipilih metode ekstraksi menggunakan ultrasonikator selama 30 menit. Alasan dipilih waktu ekstraksi 30 menit karena waktu ekstraksi 30 menit menghasilkan respon AUC paling tinggi yang artinya kurkumin yang terekstraksi paling optimal. Selain alasan bahwa kurkumin terekstraksi optimal pada menit ke-30, jumlah peak yang dihasilkan kromatogram menit ke-30 ternyata lebih banyak dari waktu ekstraksi antara 5 sampai 25 menit. Penambahan jumlah peak ini disebabkan oleh terbentuknya produk degradasi kurkumin. Adanya produk degradasi kurkumin tersebut dapat mempengaruhi besarnya respon AUC yang dihasilkan sehingga tidak menunjukkan kadar kurkumin yang sebenarnya. Bila proses ekstraksi tetap dilanjutkan lebih lama dikhawatirkan kadar kurkumin akan menurun sedangkan kadar produk degradasinya akan meningkat.
Gambar 19. Kurva optimasi waktu ekstraksi sampel Rheumakur®
H. Penetapan Kadar Kurkumin dalam Sampel Rheumakur®
Kadar kurkumin dalam kapsul lunak OHT Rheumakur® dapat dihitung berdasarkan kromatogram yang memiliki nilai AUC menggunakan persamaan kurva baku yang telah diperoleh. Parameter analisis yang digunakan untuk melihat reprodusibiltas yaitu nilai CV. Dari data pada tabel IV dapat dilihat kadar rata-rata kurkumin dalam sampel.
Tabel IV. Hasil perhitungan kadar kurkumin dalam masing-masing apotek Apotek Replikasi AUC Kadar Kurkumin
(% b/b) Keterangan
1
1 454.994 38,4768
Kadar rata-rata = 39,6350 % b/b SD = 1,5242
Kadar rata-rata = 39,5934 % b/b SD = 0,3594
49
Kadar Rheumakur®untuk masing-masing apotek yaitu 39,6350; 39,5934; dan 47,2658 % b/b. Pada label tercantum kadar kurkuminoid tiap kapsul sebesar 10 mg. Menurut Aggarwal dkk (2006), kandungan kurkumin dalam kurkuminoid adalah 77%, sehingga dalam 10 mg kurkuminoid terdapat kurang lebih 2,7500 % b/b kurkumin. Kadar kurkumin setiap sampel dari masing-masing apotek ternyata jauh lebih besar (±10-20 kali) dibandingkan kadar kurkumin yang terdapat dalam 10 mg kurkuminoid. Nilai CV masing-masing sampel dari tiap-tiap apotek yaitu 3,8456%; 0,9078%; dan 1,7331%. Nilai CV pada apotek 1 ternyata tidak memenuhi syarat CV yang baik (CV < 2), yaitu CV = 3,8456% sehingga kadar kurkumin dalam sampel OHT Rheumakur® yang diperoleh dari apotek 1 tidak reprodusibel.
Sebelum membandingkan data kadar kurkumin pada masing-masing apotek, perlu dilakukan uji normalitas data. Analisis normalitas data yang digunakan ialah Shapiro-Wilk dengan nilai kemaknaan (p) > 0,05. Alasan digunakan metode Shapiro-Wilk karena jumlah sampel ≤ 50.
Tabel V. Nilai normalitas data apotek 1, 2, dan 3 Tests of Normality
*. This is a lower bound of the true significance.
Dari tabel V didapatkan bahwa data kadar apotek 2 ternyata tidak terdistribusi normal karena pada tabel Sig. menunjukkan nilai kemaknaan (p) =
0.025 dimana p < 0,05. Dengan demikian, uji analisis komparatif yang digunakan untuk mengetahui reprodusibilitas kadar sampel Rheumakur® masing-masing apotek adalah uji Kruskall-Wallis kemudian dilanjutkan analisis Post Hoc dengan uji Mann Whitney. Analisis Post Hoc dengan uji Mann Whitney bertujuan untuk mengetahui kadar sampel Rheumakur® dari apotek mana sajakah yang memiliki perbedaan bermakna.
Tabel VI. Nilai uji Kruskall-Wallis data apotek 1, 2, dan 3 Test Statisticsa,b
Hasil uji Kruskall-Wallis menunjukkan adanya perbedaan bermakna dari sampel Rheumakur® yang berasal dari ketiga apotek tersebut. Diperoleh nilai p = 0,009 dimana p < 0,05. Setelah uji Kruskall-Wallis kemudian diteruskan dengan analisis Post Hoc dengan uji Mann-Whitney.
Tabel VII. Nilai uji Mann-Whitney data apotek 1 dan 2 Test Statisticsb
Asymp. Sig. (2-tailed) .602
Exact Sig. [2*(1-tailed
Sig.)] .690a
a. Not corrected for ties.
51
Tabel VIII . Nilai uji Mann-Whitney data apotek 1 dan 3 Test Statisticsb
Asymp. Sig. (2-tailed) .009
Exact Sig. [2*(1-tailed
Sig.)] .008a
a. Not corrected for ties.
b. Grouping Variable: Kelompok
Tabel IX . Nilai uji Mann-Whitney data apotek 2 dan 3 Test Statisticsb
Asymp. Sig. (2-tailed) .009
Exact Sig. [2*(1-tailed
Sig.)] .008a
a. Not corrected for ties.
b. Grouping Variable: Kelompok
Dari hasil analisis Post Hoc dengan uji Mann-Whitney didapatkan data sebagai berikut:
a. Nilai p untuk apotek 1 dan apotek 2, yaitu 0,602 b. Nilai p untuk apotek 2 dan apotek 3, yaitu 0,009 c. Nilai p untuk apotek 1 dan apotek 3, yaitu 0,009
Dari data di atas dapat diketahui bahwa antara apotek 1 dan apotek 2 memiliki kadar yang tidak berbeda bermakna. Hal tersebut ditunjukkan dengan nilai p > 0,05 (p = 0,602). Sedangkan antara apotek 1 dan apotek 3 serta apotek 2 dan 3
53
BAB V
KESIMPULAN DAN SARAN
A. Kesimpulan
1. Dari hasil penelitian yang telah diperoleh, dapat disimpulkan bahwa kadar rata-rata kurkumin yang terdapat dalam sediaan padat OHT merk Rheumakur® yang beredar dipasaran untuk setiap apoteknya masing-masing 39,6350 ± 1,5242; 39,5934 ± 0,3594; dan 47,2658 ± 0,8192 % (b/b) dengan nilai CV
masing-masing 3,8456%; 0,9078%; dan 1,7331%.
2. Kadar kurkumin setiap sampel dari masing-masing apotek ternyata tidak masuk dalam rentang kadar kurkumin yang terdapat dalam 10 mg kurkuminoid. Kadar kurkumin dalam sediaan kapsul lunak Rheumakur® antara apotek 1 dan 2 tidak berbeda bermakna secara statistik, sedangkan antara apotek 1 dan 3 serta apotek 2 dan 3 ternyata memiliki perbedaan bermakna.
B. Saran
Perlu dilakukan analisis terhadap sampel obat tradisional lain yang mengandung kurkumin dengan menggunakan metode penelitian ini.
54
DAFTAR PUSTAKA
Anonim, 2002, Curcuma longa: Alternative Medicine Review Monographs, http://www.thorne.com/media/alternative_medicine_review/monographs/ CurcumaMono.pdf, diakses tanggal 30 September 2010.
Anonim, 2011, Rheumakur, http://phytochemindo.indonetwork.net/1167963/ rheumakur-kombinasi-minyak-kunyit-dan-temulawak.htm, diakses tanggal 28 Januari 2011.
Aggarwal, B.B., Kumar, A., Anggarwal, M.S., Shishodia, S., 2003, Curcumin Derived from Turmeric (Curcuma longa)- a Spice for All Seasons, http://www.curcumin.co.nz/pdf/Curcumin_A_Spice_For_All_Seasons.pd f, diakses tanggal 5 September 2010.
Aggarwal, B.B., Bhatt, I.D., Ichikawa, H., Ahn, K.S., Sethi, G., Sandur, S.K., 2006, Curcumin- Biological and Medicinal Properties, diakses tanggal 5 September 2010.
Badan Pengawas Obat dan Makanan Republik Indonesia, 2005, Peraturan Kepala Badan Pengawas Obat dan Makanan Republik Indonesia Nomor HK.00.05.4.2411 tentang Penggolongan Obat Bahan Alam Indonesia, Badan Pengawas Obat dana Makanan Republik Indonesia, Jakarta. Badan Pengawas Obat Dan Makanan RI, 2005, Lampiran Peraturan Kepala
Badan Pengawas Obat dan Makanan Republik Indonesia Nomor HK 00.05.4.1380 tentang Pedoman Cara Pembuatan Obat Tradisional Yang Baik, Badan Pengawas Obat dan Makanan Republik Indonesia, Jakarta. Badan Pengawas Obat dan Makanan Republik Indonesia, 2005, Standarisasi
Ekstrak Tumbuhan Obat Indonesia, Salah Satu Tahapan Penting dalam Pengembangan Obat Asli Indonesia, InfoPOM, 6(4), 1-5.
Bassett, J., Denney, R. C., Jeffery, G. H., Mendham, J., 1994, Vogel’s Textbook of Quantitative Inorganic Analysis Including Elementary Instrumental Analysis, diterjemahkan oleh Pudjaatmaka, A. H., hal. 863-866, Penerbit Buku Kedokteran EGC, Jakarta.
Direktorat Jenderal Pengawasan Obat dan Makanan RI, 1995, Farmakope Indonesia, jilid IV, Departemen Kesehatan Republik Indonesia, Jakarta. Johnson, E. L., and Stevenson, R., 1978, Basic Liquid Chromatography,