OPTIMASI GELLING AGENTCMC-Na DAN HUMEKTAN POLIETILEN GLIKOL 400 DALAM SEDIAAN GEL ANTIINFLAMASI EKSTRAK
LIDAH BUAYA (Aloe barbadensis Mill.) DENGAN APLIKASI DESAIN FAKTORIAL
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
Oleh :
Enggar Nugraheni Putri NIM : 108114027
FAKULTAS FARMASI UNIVERSITAS SANATA DHARMA
i
OPTIMASI GELLING AGENTCMC-Na DAN HUMEKTAN POLIETILEN GLIKOL 400 DALAM SEDIAAN GEL ANTIINFLAMASI EKSTRAK
LIDAH BUAYA (Aloe barbadensis Mill.) DENGAN APLIKASI DESAIN FAKTORIAL
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
Oleh :
Enggar Nugraheni Putri NIM : 108114027
FAKULTAS FARMASI UNIVERSITAS SANATA DHARMA
iv
HALAMAN PERSEMBAHAN
Janganlah takut, sebab Aku menyertai engkau,
janganlah bimbang, sebab Aku ini Allahmu;
Aku akan meneguhkan, bahkan akan menolong
engkau;
Aku akan memegang engkau dengan tangan
kanan- Ku yang membawa kemenangan.
(Yesaya 41 : 10 )
K a r y a i n i k u p e r se m b a h k a n u n t u k :
Tu h a n Y e su s K r i st u s Ju r u Se l a m a t k u y a n g H i d u p
P a p a h d a n M a m a h
A a d , Ti t i e s, Ch r i st i n , Lu c k y
Sa h a b a t -sa h a b a t k u
vii PRAKATA
Puji syukur penulis panjatkan kepada Tuhan Yang Maha Esa berkat dan rahmatNya, sehingga penulis dapat menyelesaikan skripsi berjudul “Optimasi Gelling Agent CMC Na dan Humektan Polietilen Glikol 400 Dalam Sediaan Gel Antiinflamasi Ekstrak Lidah Buaya (Aloe barbadensisMill.) dengan Aplikasi Desain Faktorial” ini dengan baik. Skripsi ini disusun guna memenuhi salah satu syarat memperoleh gelar sarjana farmasi (S.Farm.) di Fakultas Farmasi Universitas Sanata Dharma Yogyakarta.
Selama proses masa perkuliahan studi S1 hingga penyusunan skripsi ini selesai, penulis menerima bantuan, sarana, dukungan, nasehat, bimbingan, saran, dan kritik dari berbagai pihak. Oleh karena itu, penulis ingin mengucapakan terima kasih yang sebesar-besarnya kepada :
1. Orang tua, kakak, adik, dan keluarga besar penulis atas doa dan dukungan yang telah diberikan baik secara moril maupun materiil
2. Bapak Ipang Djunarko, M.Sc., Apt., selaku Dekan Fakultas Farmasi Universitas Sanata Dharma Yogyakarta
3. Bapak Septimawanto Dwi Prasetyo, M.Si., Apt. selaku dosen pembimbing atas bantuan, kesabaran, perhatian, dan semangat selama penyusunan proposal hingga selesainya skripsi ini
viii
5. Segenap dosen atas kesabarannya dalam mengajar dan membimbing penulis selama perkuliahan di fakultas farmasi Universitas Sanata Dharma
6. Pak Musrifin, Pak Agung, Pak Wagiran, Pak Heru, serta laboran-laboran lain yang telah membantu penulis selama penelitian
7. Rekan kerja selama penelitian dan selama perkuliahan, Skolastika Ruth Maharani dan Daniel Pradipta atas kerja samanya.
8. Priskila Agnes Salviana, Agustinus Hendy Larsen, Oswaldine Heraolia Pramesthi atas bantuan yang sudah diberikan selama penelitian.
9. Teman-teman skripsi lantai I, Via, Sita, Juli, Cilla, Aries, Niken, dan teman-teman lain atas kebersamaan yang telah diberikan
10. Teman-teman angkatan 2010 atas kebersamaan yang tidak terlupakan dan kekompakannya
11. Sahabat dahsyat “KONYIL” Mae, Adit, Renni, Hendy, Pras, Vincent, Wisnu atas keceriaan semangat, dan doa yang diberikan ditengah-tengah pengerjaan penelitian
12. Semua pihak yang tidak dapat disebutkan satu per satu karena keterbatasan penulis, terima kasih untuk bantuan yang telah diberikan kepada penulis
Penulis menyadari bahwa skripsi ini masih jauh dari kata sempurna. Penulis mengharapkan kritik dan saran yang membangun dari seluruh pihak. Akhir kata, semoga penelitian ini dapat berguna bagi semua pihak terutama dalam bidang farmasi.
Yogyakarta, Juli 2014
xi 2. Pengumpulan dan Penyiapan Tanaman Lidah Buaya
(Aloe barbadensisMill.)... 3. Pembuatan Jus Lidah Buaya... 4. Isolasi Polisakarida Acemannan dari Lidah
Buaya... 5. Formula Gel Antiinflamasi... 6. Pembuatan Gel Antiinflamasi... 7. Uji Sifat Fisik dan Stabilitas gel Antiinflamasi
Ekstrak Lidah Buaya (Aloe barbadensisMill.)... 8. Orientasi Waktu Pengolesan Sediaan... 9. Uji Kemampuan Antiinflamasi Gel Antiinflamasi
Ekstrak Lidah Buaya (Aloe barbadensisMill.)... G. Analisis Hasil... BAB IV HASIL DAN PEMBAHASAN... A. Determinasi dan Ekstraksi Lidah Buaya... B. Pembuatan Gel Antiinflamasi Ekstrak Lidah Buaya...
xii
C. Uji pH Gel Antiinflamasi Ekstrak Lidah Buaya... D. Karakteristik Sifat Fisik dan Stabilitas Gel Antiinflamasi
Ekstrak Lidah Buaya... 1. Uji Daya Sebar... 2. Uji Viskositas dan Pergeseran Viskositas... E. Efek Penambahan CMC-Na dan PEG 400 serta
xiii
DAFTAR TABEL
Tabel I Formula Aloe veraGel... 27 Tabel II Formula Gel Hasil Modifikasi... 27 Tabel III Level Rendah dan level Tinggi CMC-Na dan PEG 400
pada Formula Gel Antiinflamasi ekstrak Lidah Buaya... 28 Tabel IV Formula Gel Antiinflamasi... 28 Tabel V Uji pH Gel Antiinflamasi Ekstrak Lidah Buaya... 38 Tabel VI Daya Sebar Gel Antiinflamasi Ekstrak Lidah Buaya 48 Jam
setelah Pembuatan... 40 Tabel VII Daya Sebar Gel Antiinflamasi Ekstrak Lidah Buaya setelah
1 Bulan Penyimpanan... 40 Tabel VIII Viskositas Gel Antiinflamasi Ekstrak Lidah Buaya 48 Jam
setelah Pembuatan (dPa.s)... 41 Tabel IX Viskositas Gel Antiinflamasi Ekstrak Lidah Buaya setelah
1 Bulan Penyimpanan (dPa.s)... 41 Tabel X Pergeseran Viskositas Gel Antiinflamasi Ekstrak Lidah
Buaya... 42 Tabel XI Uji Normalitas Data Viskositas dan Daya Sebar Sediaan
Gel Antiinflamasi Ekstrak Lidah Buaya... 44 Tabel XII Uji Variansi Data Viskositas dan Daya Sebar... 45 Tabel XIII Analisis ANOVA Efek CMC-Na dan PEG 400 dan
xiv
Tabel XIV Analisis ANOVA Efek CMC-Na dan PEG 400 dan Interaksinya dalam Menentukan Respon Daya Sebar... 48 Tabel XV Pergeseran Viskositas tiap Formula setelah 1 Bulan
Penyimpanan (x± SD)... 51 Tabel XVI Hasil Uji t Berpasangan Sediaan Gel Antiinflamasi Ekstrak
Lidah Buaya terhadap Viskositas... 51 Tabel XVII Hasil Uji Aktivitas Antiinflamasi Gel Antiinflamasi
Ekstrak Lidah Buaya... 54 Tabel XVIII Uji Normalitas Data Aktivitas Antiinflamasi Gel
Antiinflamasi Ekstrak Lidah Buaya... 55 Tabe XIX Uji t Independent Nilai Persentase Inhibisi Kontrol (-)
xv
DAFTAR GAMBAR
Gambar 1 Struktur CMC-Na... 9
Gambar 2 Struktur PEG... 11
Gambar 3 Struktur Natrium Benzoat... 11
Gambar 4 Tanaman Lidah Buaya... 12
Gambar 5 Struktur Acemannan... 14
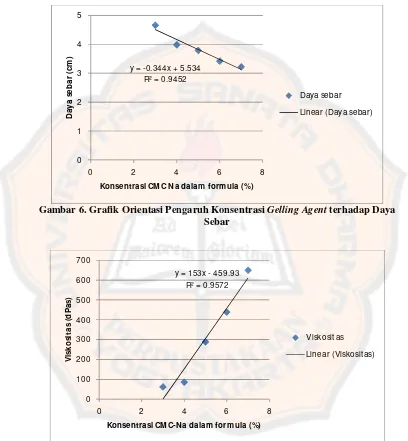
Gambar 6 Grafik Orientasi Pengaruh Konsentrasi Gelling Agent terhadap Daya Sebar... 36
Gambar 7 Grafik Orientasi Pengaruh Konsentrasi Gelling Agent terhadap Viskositas... 36
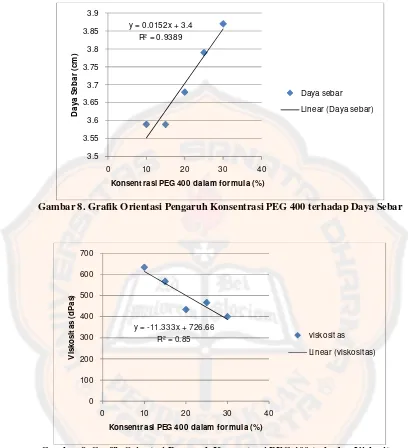
Gambar 8 Grafik Orientasi Pengaruh Konsentrasi PEG 400 terhadap Daya Sebar... 37
Gambar 9 Grafik Orientasi Pengaruh Konsentrasi PEG 400 terhadap Viskositas... 37
Gambar 10 Grafik Viskositas Gel tiap Minggu... 43
Gambar 11 Grafik Hubungan CMC-Na terhadap Respon Viskositas setelah 48 jam... 46
Gambar 12 Grafik Hubungan PEG 400 terhadap Respon Viskositas setelah 48 jam... 47
xvi
setelah 48 jam... 49 Gambar 15 Contour plotViskositas Gel Antiinflamasi Ekstrak Lidah
Buaya... 52 Gambar 16 Contour plotDaya Sebar Gel Antiinflamasi Ekstrak Lidah
Buaya... 52 Gambar 17 Contour plotViskositas dan Daya Sebar Gel Antiinflamasi
Ekstrak Lidah Buaya... 53 Gambar 18 Persentase Inhibisi Kontrol (-) dan Gel Antiinflamasi
xvii
DAFTAR LAMPIRAN
Lampiran 1 Lembar Determinasi Tanaman Lidah Buaya... 63
Lampiran 2 Data Hasil Uji pH... 64
Lampiran 3 Hasil Uji Sifat Fisik dan Stabilitas Gel Antiinflamasi Ekstrak Lidah Buaya... 64
Lampiran 4 Hasil Analisis Data Menggunakan R.2.14.1... 66
Lampiran 5 Uji Statistik Aktivitas Antiinflamasi... 72
Lampiran 6 Dokumentasi... 76
xviii INTISARI
Inflamasi merupakan respon jaringan protektif terhadap cedera atau kerusakan jaringan yang berfungsi menghancurkan, mengurangi, atau mengurung baik agen yang menyebabkan cedera maupun jaringan yang cedera itu. Lidah buaya banyak mengandung polisakarida, salah satunya adalah acemannan. Acemannan ditemukan mayoritas dalam gel daun lidah buaya yang diidentifikasi sebagai bahan aktif utama dalam gel daun lidah buaya. Acemannan memiliki mekanisme aksi sebagai antiinflamasi dengan cara mengeblok pembentukan histamin dan bradikinin, serta menghambat aktivitas bradikinin dan histamin.
Tujuan penelitian ini untuk mengetahui dan mendapatkan komposisi optimum sebagai formula optimum gel dari gelling agentCMC Na dan humektan PEG 400 serta mengetahui aktivitas antiinflamasi yang diberikan oleh ekstrak lidah buaya (Aloe barbadensis Mill.). Penelitian ini merupakan eksperimental murni yang bersifat eksploratif. Bahan aktif yang digunakan adalah acemannan yang terdapat didalam daging daun tanaman lidah buaya dan diketahui memiliki aktivitas antiinflamasi. Isolasi polisakarida acemannan diperoleh dengan cara mengendapkan kandungan polisakarida didalam jus lidah buaya dengan menggunakan pelarut etanol 96% pada suhu 10ºC selama 10 jam. Bahan yang akan dioptimasi dalam penelitian ini adalah CMC-Na sebagai gelling agent dan PEG 400 sebagai humektan. Pada penelitian akan dilakukan pedekatan desain faktorial dengan membuat beberapa variasi komposisi CMC-Na dan PEG 400. Optimasi dilakukan terhadap parameter sifat fisik gel (daya sebar, viskositas, dan pergeseran viskositas). Dilakukan uji kemampuan antiinflamasi gel antiinflamasi ekstrak lidah buaya menggunakan hewan uji tikus galur Wistar yang diinduksi karagenan untuk masing-masing formula yang dibuat.
Hasil penelitian menujukkan bahwa CMC-Na, PEG 400, dan interaksi keduanya memberikan respon yang signifikan terhadap viskositas dan daya sebar. Tidak ditemukan area komposisi optimum yang diprediksi sebagai formula optimum gel dari gelling agent dan humektan yang memenuhi persyaratan sifat fisik gel (viskositas serta daya sebar) dan stabilitas gel (pergeseran viskositas). Gel antiinflamasi ekstrak lidah buaya memberikan efek farmakologis berupa antiinflamasi terhadap kaki tikus yang diinduksi karagenan.
xix ABSTRACT
Inflammation is a protective tissue response to injury or tissue damage which serves destroy, reduce, or confine both agents that cause injury or tissue injury. Aloe vera contains many polysaccharides, one of which is acemannan. Acemannan found in the majority of the leaves of aloe vera gel which is identified as the main active ingredient in the gel of aloe vera leaves. Acemannan has as anti-inflammatory mechanism of action by blocking the formation of histamine and bradykinin, as well as inhibit the activity of bradykinin and histamine.
The purpose of this study to determine the optimum composition and obtain optimum formula gel as a gelling agent of CMC Na and humectant PEG 400 and know that given by the anti-inflammatory activity of extracts of aloe vera (Aloe barbadensis Mill.). This study is purely explorative experimental. The active ingredient used is acemannan contained in leaf aloe vera plant and is known to have anti-inflammatory activity. Isolation of acemannan obtained by precipitation of polysaccharides content in aloe vera juice using 96 % ethanol at 10ºC during 10 hours. Materials to be optimized in this study is CMC - Na as a gelling agent and PEG 400 as a humectant. In the research will be conducted factorial design to make several variations of the composition of CMC - Na and PEG 400. The parameter optimization is physical properties of the gel (dispersive power, viscosity, and viscosity shift). Tested the ability of anti-inflammatory of aloe vera gel using test animals Wistar rats induced carrageenan for each formula are made.
The results showed that CMC - Na, PEG 400, and the interaction of the two gives a significant response to the viscosity and dispersive power. Not found the optimum composition of the area predicted as optimum gel formula of a gelling agent and a humectant that meets the requirements of the physical properties of the gel (viscosity and dispersive power) and stability of the gel (viscosity shift). Aloe vera gel in the form of anti-inflammatory pharmacological effect against carrageenan -induced mice.
Keywords : Aloe barbadensis Mill., Anti-inflammatory gel, CMC - Na, PEG 400, Acemannan, factorial design
1 BAB I PENDAHULUAN
A. Latar Belakang
Fungsi utama kulit adalah sebagai organ pelindung terhadap lingkungan. Hilangnya integritas kulit akan menimbulkan cedera atau nyeri yang mengakibatkan sakit. Nyeri muncul jika integritas kulit rusak. Luka atau nyeri adalah keadaanya hilangnya kontinuitas jaringan tubuh, dapat disebabkan oleh diantaranya sengatan listrik, ledakan, gigitan hewan, atau trauma yang disebabkan oleh benda tumpul ataupun benda tajam.
Inflamasi merupakan respon jaringan protektif terhadap cedera atau kerusakan jaringan yang berfungsi menghancurkan, mengurangi, atau mengurung baik agen yang menyebabkan cedera maupun jaringan yang cedera itu. Ketika tubuh mendapatkan stimulus dari luar maka tanda awal yang muncul adalah rubor (memerah) disertai dengan kalor (panas), dolor (nyeri) dan pada akhirnya terjadi tumor (bengkak) dan functio laesa (hilangnya fungsi) (Anonim, 1996). Sebenarnya inflamasi merupakan respon normal dari tubuh ketika tubuh diinvasi oleh benda asing. Namun inflamasi dapat juga mengakibatkan kerusakan pada jaringan. Kerusakan sel akibat stimulus dari luar akan membebaskan mediator seperti histamin, bradikinin, prostaglandin dan leukotrien dimana mediator-mediator tersebut berperan dalam proses inflamasi (Katzung, 2001).
luar tubuh). Faktor eksternal yang dapat mempercepat penyembuhan inflamasi yaitu dengan cara irigasi luka menggunakan larutan fisiologis (NaCl 0,9%) dan penggunaan obat-obatan sintetik dan alami (Rahayu, 2012).
Lidah buaya menurut sejarah banyak digunakan sebagai obat konstipasi, luka terbuka, serta luka terbakar (Gaby dkk., 2006). Lidah buaya biasanya dimanfaatkan sebagai bahan pangan atau dijadikan obat dan bahan kosmetik. (Sudarto, 1997). Lidah buaya banyak mengandung polisakarida, salah satunya adalah acemannan (Hamman, 2008). Acemannan ditemukan mayoritas dalam gel daun lidah buaya yang diidentifikasi sebagai bahan aktif utama dalam gel daun lidah buaya (Cowsert, 2010). Acemannan memiliki mekanisme aksi sebagai antiinflamasi dengan cara mengeblok pembentukan histamin dan bradikinin, serta menghambat aktivitas bradikinin dan histamin (Cowsert, 2010).
Bentuk sediaan antiinflamasi sebaiknya mampu memberikan lingkungan yang lembab. Lingkungan yang lembab akan mencegah dehidrasi jaringan dan kematian sel, mempercepat angiogenesis dan meningkatkan pecahnya fibrin dan jaringan mati (Yuliani, 2012). Berbagai bentuk sediaan yang ditujukan untuk inflamasi salah satunya adalah gel.
dengan daya lekat tinggi, yang tidak menyumbat pori kulit dan dapat dengan mudah dicuci dengan air (Voight, 1994). Tipe gel yang dibuat dalam penelitian ini adalah hidrogel, karena memiliki kompatibilitas yang relatif baik terhadap jaringan biologi sehingga meminimalkan timbulnya iritasi (Swarbrick dan Boylan, 1992).
Sediaan kosmetik yang baik adalah sediaan yang optimum dalam komposisi bahan yang digunakan. Untuk mendapatkan sediaan gel antiinflamasi yang baik perlu dilakukan optimasi terhadap bahan yang memegang peranan penting di dalam sediaan tersebut, yaitu gelling agentdan humektan.
B. Perumusan Masalah
1. Apakah ditemukan area komposisi optimum yang diprediksi sebagai formula optimum gel dari gelling agentdan humektan yang memenuhi persyaratan sifat fisik gel (viskositas serta daya sebar) dan stabilitas gel (pergeseran viskositas) ?
2. Apakah ekstrak lidah buaya memberikan aktivitas antiinflamasi?
C. Keaslian Penelitian
Sejauh penelusuran pustaka yang dilakukan penulis, penelitian tentang optimasi gelling agent CMC-Na dan humektan polietilen glikol 400 dalam sediaan gel antiinflamasi ekstrak lidah buaya dengan aplikasi desain faktorial belum pernah dilakukan. Adapun penelitian terkait yang pernah dilakukan :
1. Kurniawan (2013) yaitu “Optimasi Natrium Alginat dan CMC-Na sebagai Gelling Agent pada Sediaan Gel Antiinflamasi Ekstrak Daun Petai Cina (Leucaena leucocephala (Lam.) de Wit.) dengan Aplikasi Desain Faktorial”. Dalam penelitian ini dilakukan optimasi gelling agent yaitu natrium alginat dan CMC-Na pada sediaan gel antinflamasi dengan ekstrak daun petai cina.
agent dan propilenglikol sebagai humektan dalam sediaan cooling gel dengan ekstrak daun petai cina.
D. Manfaat Penelitian 1. Manfaat Teoritis
Menambah ilmu pengetahuan bagi perkembangan dunia farmasi mengenai optimasi gelling agentCMC-Na dan humektan Polietilen glikol 400 pada pembuatan gel antiinflamasi dari bahan alam.
2. Manfaat Metodologis
Hasil penelitian diharapkan dapat memberikan informasi tentang komposisi optimum dari gelling agent dan humektan dengan metode desain faktorial.
3. Manfaat praktis
Dengan adanya sediaan gel antiinflamasi ini diharapkan dapat menjadi alternatif pilihan obat dari bahan alam dan masyarakat dapat mengembangkan potensi lidah buaya sebagai antiinflamasi.
E. Tujuan Penelitian 1. Tujuan Umum
2. Tujuan Khusus
a. Mengetahui perbandingan gelling agent CMC-Na dan humektan Polietilen glikol 400 agar didapat sediaan gel antiinflamasi ekstrak lidah buaya yang memenuhi persyaratan sifat fisik gel.
7 BAB II
TINJAUAN PUSTAKA A. Gel
Gel merupakan bentuk sediaan semisolid yang mengandung larutan bahan aktif tunggal maupun campuran dengan pembawa senyawa hidrofilik dan hidrofobik. Gel juga dirumuskan sebagai sistem dispersi, yang minimal terdiri dari dua fase yaitu sebuah fase padat dan sebuah fase cair (gel liofil) atau terdiri dari sebuah fase padat dan fase berbentuk gas (gel kserofil). Gel mengandung basis senyawa hidrofilik sehingga memiliki konsistensi lembut dan memberikan rasa dingin pada kulit. Rasa dingin tersebut merupakan efek evaporasi air (Voight, 1994).
Hidrogel adalah sediaan semisolid yang mengandung material polimer yang mempunyai kemampuan untuk mengembang dalam air tanpa larut dan bisa menyimpan air dalam strukturnya. Hidrogel secara umum terdiri dari 2 komponen sistem, satu komponen bersifat hidrofilik, tidak larut, merupakan jaringan polimer tiga dimensi, dan komponen yang lain merupakan air. Sifat hidrogel yaitu kandungan airnya relatif tinggi dan bersifat lembut, konsistensinya elastis sehingga kuat (Swarbrick dan Boylan, 1992). Hidrogel adalah sistem yang menjebak air karena adanya polimer-polimer tidak larut yang membentuk jaringan. Alasan digunakannya hidrogel sebagai komponen dari sistem penghantaran dan pelepasan obat adalah kompatibilitasnya dengan jaringan biologis relatif baik (Zats dan Kushla, 1996).
pandang yang elastis dengan daya lekat tinggi, yang tidak menyumbat pori kulit, dan mudah dicuci dengan air (Voight, 1994). Sediaan gel hidrofilik memiliki sifat daya sebar yang baik pada kulit, pelepasan obat yang baik, tidak menghambat fungsi fisiologis kulit, efek dingin yang ditimbulkan, dan mudah dicuci dengan air (Voight, 1995).
Karekteristik gel yang digunakan harus sesuai dengan tujuan penggunaan gel. Gel topikal tidak boleh terlalu liat, dan konsentrasi bahan pembentuk gel yang terlalu tinggi atau penggunaan bahan pembentuk gel dengan berat molekul yang terlalu besar yang dapat mengakibatkan sediaan sulit dioleskan dan sulit pula didispersikan (Zats dan Kushla, 1989). Kemampuan menembus permeabilitas kulit merupakan salah satu penghalang dalam sistem penghantaran topikal. Upaya dalam meningkatkan penetrasi zat aktif ke dalam kulit dapat dilakukan dengan beberapa cara, antara lain dengan memodifikasi lapisan stratum corneum seperti pada penggunaan enhancerdan dengan menggunakan sistem
pembawa (Benson, 2005).
B. Gelling Agent
Gelling agentadalah gum alam atau sintetis, resin, atau hidrokoloid lain yang digunakan di dalam formulasi gel untuk menjaga konstituen cairan dan padatan dalam suatu bentuk gel yang halus. Gelling agent yang sering digunakan antara lain Carpobol dan Sodium Carboxy Methyl Cellulose (CMC-Na) (Lieberman dan Martin, 1996).
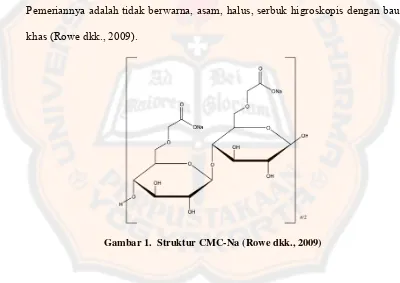
Pada penelitian ini digunakan CMC-Na sebagai gelling agent. CMC-Na adalah polimer sintetik dengan berat molekul besar yang terdiri atas rantai silang antara asam akrilat dengan alil selulosa atau alil eter dari pentaerythritol. Pemeriannya adalah tidak berwarna, asam, halus, serbuk higroskopis dengan bau khas (Rowe dkk., 2009).
Gambar 1. Struktur CMC-Na (Rowe dkk., 2009)
berfungsi sebagai gelling agent. Solusi CMC-Na stabil pada pH 2 – 10. Jika pH kurang dari 2 maka dapat terjadi presipitasi sedangkan bila pH lebih dari 10 dapat menyebabkan penurunan viskositas (Rowe dkk., 2009).
C. Humektan
Humektan adalah bahan dalam produk kosmetik yang dimaksudkan untuk mencegah hilangnya lembab dari produk dan meningkatkan jumlah air (kelembaban) pada lapisan kulit terluar saat produk digunakan (Loden, 2001). Gliserol, propilen glikol, sorbitol, dan polyethylene glycol biasa digunakan sebagai humektan dalam sediaan untuk mencegah penguapan dan pembentukan lapisan kering pada permukaan produk (Zocchi, 2001). Gel transparan diformulasikan dengan konsentrasi humektan maksimal sebesar 80% (Lieberman dan Martin, 1996).
Pada penelitian ini digunakan Polietilen glikol 400. Polietilen glikol 400 adalah polimer dari etilen oksida dan air. Pemeriannya adalah cairan kental, jernih, tidak berwarna, memiliki bau khas, dan agak higroskopis. PEG 400 memiliki sifat larut dalam air, dalam etanol, dalam aseton, dalam glikol lain, dan dalam hidrokarbon aromatik, praktis tidak larut dalam eter dan bahan hidrokarbon alifatik (Dirjen POM, 1995). PEG dapat berfungsi sebagai humektan bila diformulasikan dalam sediaan gel (Lieberman dan Martin, 1996). Polyethylene glycol 400 disebut juga dengan makrogol 400 atau PEG 400 adalah polimer dari etilen oksida dan air, dinyatakan dengan rumus H(OCH2CH2)nOH dengan harga
memiliki suatu tingkat
berat molekul 144,11 (Rowe dkk., 2009). Natrium benzoat
makanan, dan obat. Natrium 0,02% - 0,5%; untuk produk kosmetik (Rowe dkk., 2009).
Gambar 3. Struk
tingkat polimerasi lebih dari 10 menunjukkan struktur belok, rantai pendek yang berbentuk zig-zag (Voight, 1994).
Gambar 2. Struktur PEG (Rowe dkk., 2009)
D. Natrium Benzoat
benzoat merupakan butiran atau kristal putih, sedikit higroskopis. tidak berbau, atau dengan sedikit bau kapur barus dan
garam. Natrium benzoat memiliki rumus empiris C7H5NaO
molekul 144,11 (Rowe dkk., 2009).
benzoat digunakan sebagai bahan antimikroba dalam kosmetik, obat. Natrium benzoat dalam obat oral digunakan pada konsentra
untuk produk parenteral sebesar 0,5%; dan 0,1% - 0,5% tik (Rowe dkk., 2009).
r 3. Struktur natrium benzoat (Rowe dkk., 2009)
E. Lidah Buaya
Tanaman lidah buaya berbatang pendek. Batangnya tidak kelihatan karena tertutup oleh daun-daun yang rapat dan sebagian terbenam dalam tanah. Daun tanaman lidah buaya berbentuk pita dengan helaian yang memanjang. Daunnya berdaging tebal, tidak bertulang, berwarna hijau keabu-abuan, bersifat sukulen (banyak mengandung air) dan banyak mengandung getah atau lendir (Sudarto, 1997).
Bunga lidah buaya berwarna kuning atau kemerahan berupa pipa yang mengumpul, keluar dari ketiak daun. Bunga berukuran kecil, tersusun dalam rangkaian berbentuk tandan. Akar tanaman lidah buaya berupa akar serabut yang pendek dan berada di sekitar permukaan tanah. Panjang akar berkisar antara 50 cm - 100 cm (Sudarto, 1997).
Gambar 4. Tanaman lidah buaya (Bassetti dan Sala, 2005)
khasiat purgatif, yang termasuk dalam senyawa resin adalah senyawa kromon glukosil-C aloesin (aloeresin B). Antrakuinon adalah metabolit di dalam aloe yang kadarnya bergantung pada aktivitas metabolisme secara keseluruhan (Wiryowidagdo, 2008).
Acemannan ditemukan mayoritas dalam gel daun lidah buaya yang diidentifikasi sebagai bahan aktif utama dalam gel daun lidah buaya (Cowsert, 2010). Acemannan memiliki mekanisme aksi sebagai antiinflamasi dengan cara mengeblok pembentukan histamin dan bradikinin, serta menghambat aktivitas bradikinin dan histamin (Cowsert, 2010).
Khasiat dari lidah buaya diantaranya untuk melembabkan kulit, melegakan tenggorokan, meluruhkan cacing, mendinginkan dan mengurangi rasa sakit. Lidah buaya menurut sejarah banyak digunakan sebagai obat konstipasi, luka terbuka, serta luka terbakar (Gaby dkk., 2006). Aloe vera dapat bersifat sebagai antibakteri yang membantu penyembuhan dari sunburn. Hal ini dikarenakan adanya kandungan aloectin B yang merangsang sistem kekebalan (Anonim, 2012).
F. Acemannan
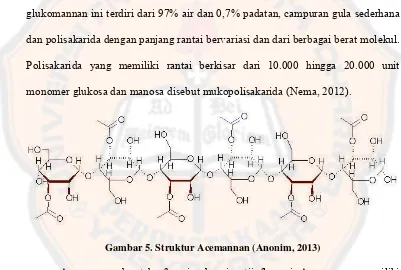
Acemannan adalah mukopolisakarida D-isomer dalam gel daun lidah buaya. Senyawa ini dikenal memiliki imunostimulan, antivirus, dan antineoplastik (Anonim, 2013). Kelompok sakarida berfungsi untuk menghasilkan energi. Aloe memiliki dua kategori gula, glukosa dan manosa sebagai monosakarida dan acemannan serta selulosa sebagai polisakarida. Di dalam gel daun lidah buaya, prekursor beta-(1,4)-asetil-polymannose lebih dikenal sebagai acemannan. Dalam glukomannan ini terdiri dari 97% air dan 0,7% padatan, campuran gula sederhana dan polisakarida dengan panjang rantai bervariasi dan dari berbagai berat molekul. Polisakarida yang memiliki rantai berkisar dari 10.000 hingga 20.000 unit monomer glukosa dan manosa disebut mukopolisakarida (Nema, 2012).
Gambar 5. Struktur Acemannan (Anonim, 2013)
memiliki aktivitas sebagai penyembuh luka dan antiinflamasi (Choi dan Chung, 2005).
G. Inflamasi
jaringan dan karena rasa nyeri yang mengurangi mobilitas pada daerah yang terkena (Kee dan Hayes, 1996).
Inflamasi biasanya dibagi dalam 3 fase : inflamasi akut, respons imun, dan inflamasi kronis. Inflamasi akut merupakan respon awal terhadap cedera jaringan, hal tersebut terjadi melalui autacoid serta pada umumnya didahului oleh pembentukan respon imun. Sejumlah autocoid yang terlibat seperti histamin, serotonin, bradikinin, prostaglandin, dan leukotrien (Katzung, 2001). Respon imun terjadi bila sejumlah sel yang mampu menimbulkan kekebalan diaktifkan merespon organisme asing atau susbtansi antigenik yang terlepas selama respon terhadap inflamasi akut serta kronis.
H. Isolasi Polisakarida
Isolasi polisakarida dapat dilakukan dengan 2 tahap, yaitu ekstraksi dan pengendapan. Tahap yang pertama adalah ekstraksi dengan penambahan solvent yang dapat melarutkan polisakarida, umumnya air. Polisakarida memiliki kelarutan dalam air murni yaitu sekitar 0,133 sampai 0,769 g/g (Bouchard, 2007). Faktor yang berpengaruh pada proses ekstraksi antara lain, waktu pasca panen, perbandingan gel lidah buaya dan solvent, jenis solvent, suhu waktu kontak, ukuran partikel dan pengadukan. Tahap selanjutnya adalah pengendapan polisakarida dari filtrat lidah buaya menggunakan co-solvent berupa alkohol. Faktor yang berpengaruh dalam proses pengendapan antara lain, jenis co-solvent, perbandingan co-solvent dan solute yang akan diendapkan, suhu, kecepatan pengadukan, kecepatan penambahan co-solvent, pengaruh ion sejenis dan ion kompleks, serta pH (Ayuningsih dan Setyaningrum, 2011). Sebagai pengendap polisakarida dalam tanaman lidah buaya, etanol memiliki kemampuan melarutkan polisakarida yang relatif kecil, meskipun kemampuan dalam melarutkan zat-zat lain yang relatif besar. Etanol dapat digunakan dalam proses pengendapan polisakarida penyusun karbohidrat dalam jaringan tanaman lidah buaya yang membentuk endapan polisakarida (Kusmawati dan Pratiwi, 2009).
I. Viskositas
formulasi yang penting dalam produk akhir ssediaan semosolid. Viskositas sediaan ditingkatkan oleh bahan baku yang digunakan secara umum, misalnya polimer yang memiliki tingkat viskositas tertentu. Semakin tinggi viskositas, maka tahanan suatu cairan untuk dapat mengalir semakin besar pula. Rheology sangat berperan dalam aplikasi formulasi sediaan farmasi seperti emulsi, pasta, suppositoria, dan tablet salut (Liebermann dan Martin, 1996). Peningkatan viskositas akan memperngaruhi daya sebar (Garg dkk., 2002). Pergeseran viskositas yang kecil terjadi pada temperatur penyimpanan normal (Zats dan Kushla, 1996).
J. Daya Sebar
Daya sebar dipengaruhi oleh beberapa faktor yaitu karakteristik formula, kekuatan dan lama tekanan yang menghasilkan kelengketan dan temperatur tempat aksi. Kecepatan penyebaran suatu sediaan bergantung pada viskositas formula, kecepatan evaporasi, dan kecepatan peningkatan viskositas karena evaporasi. Efikasi sediaan topikal bergantung pada daya sebar formulasi untuk menghantarkan dosis. Penghantaran dosis obat bergantung pada daya sebar suatu formula (Garg dkk., 2002).
K. Pergeseran Viskositas
tersebut dengan sistem dispersi, sedangkan faktor lainnya yang ikut berpengaruh yaitu agregasi partikel yang tidak tergantung pada kandungan polimer, meskipun polimer dapat mengurangi kecepatan perubahan ukuran partikel (Zatz dkk., 1996).
L. Metode Desain Faktorial
Desain faktorial merupakan cara yang digunakan untuk mengevaluasi efek faktor yang dipelajari secara stimultan dan efek yang relatif penting dapat dinilai (Armstrong dan James, 1996). Desain faktorial merupakan aplikasi persamaan regresi yaitu teknik untuk memberikan model hubungan antara variabel-respon dengan satu atau lebih variabel bebas. Model yang diperoleh dari analisa tersebut berupa persamaan matematika (Bolton, 1997). Penelitian desain faktorial dimulai dengan menentukan faktor dan aras yang akan diteliti, serta respon yang akan diukur. Desain faktorial merupakan desain yang dipilih untuk mendeterminasi efek-efek secara simultan dan interaksi dari efek-efek tersebut. Dengan desain faktorial, dapat didesain suatu percobaan untuk mengetahui faktor yang dominan berpengaruh secara signifikan terhadap respon. Juga memungkinkan untuk mengetahui interaksi antara faktor-faktor tersebut (Bolton, 1997).
Desain faktorial memiliki beberapa keuntungan. Metode ini memiliki efisiensi yang maksimum untuk memperkirakan efek yang dominan dalam menentukan respon. Keuntungan utama desain faktorial adalah bahwa metode ini memungkinkan untuk mengidentifikasi efek masing-masing faktor, maupun efek interaksi antar faktor (Bolton, 1997).
M. Landasan Teori
CMC-Na memiliki rentang pH 5-10 sehingga dalam pencampuran di dalam formula tidak dibutuhkan agen pembasa. Selain itu dalam penelitian juga digunakan humektan untuk mempertahankan kelembaban pada gel antiinflamasi, humektan yang digunakan adalah PEG 400. Polietilen glikol 400 berperan dalam meningkatkan ikatan struktur gel yang terbentuk, karena memiliki gugus hidrofilik yang dapat berikatan dengan struktur gel yang sebagian besar penyusunnya adalah air. Sifat fisik gel yang meliputi daya sebar dan viskositas berpengaruh pada acceptability dan penghantaran zat aktif, oleh karena itu diperlukan konsistensi formula yang optimum agar formula dapat menghantarkan zat aktif dengan baik.
Pada penelitian ini, dilakukan model percobaan dengan menggunakan metode desain faktorial dua aras 2 faktor. Dengan menggunakan metode ini, akan diketahui efek dari interaksi kedua faktor yang digunakan.
N. Hipotesis
22 BAB III
METODOLOGI PENELITIAN
A. Jenis Rancangan Penelitian
Penelitian ini merupakan rancangan eksperimental murni menggunakan Desain Faktorial dan bersifat eksploratif, yaitu mencari range formula gel antiinflamasi ekstrak lidah buaya yang memenuhi uji fisik
B. Variabel Penelitian 1. Variabel bebas
Variabel bebas pada penelitian ini adalah komposisi CMC-Na dan Polietilen glikol 400 dalam formula gel antiinflamasi ekstrak lidah buaya (Aloe barbadensis Mill.).
2. Variabel tergantung
Variabel tergantung pada penelitian ini adalah sifat fisik gel (meliputi daya sebar, viskositas, pergeseran viskositas) dan efek antiinflamasi yang dihasilkan.
3. Variabel pengacau terkendali
Variabel pengacau terkendali pada penelitian ini adalah kecepatan dan lama pengadukan, metode pembuatan gel yang digunakan, dan wadah penyimpanan gel.
4. Variabel pengacau tak terkendali
C. Definisi Operasional
a. Ekstrak lidah buaya adalah endapan polisakarida yang didapatkan dengan cara mencampur jus lidah buaya dengan etanol 96% (1:4) pada suhu 10ºC selama 10 jam.
b. Efek antiinflamasi adalah kemampuan zat aktif dalam sediaan antiinflamasi untuk meredakan nyeri, menurunkan suhu tubuh yang naik dan menghambat agregasi platelet (antikoagulan).
c. Gelling agent adalah bahan pembentuk sediaan gel yang membentuk matriks. CMC-Na digunakan sebagai gelling agentdalam penelitian ini. d. Humektan adalah bahan yang berfungsi untuk menarik lembab dari
lingkungan sehingga kelembaban kulit dapat dipertahankan. Polietilen glikol 400 digunakan sebagai humektan dalam penelitian ini.
e. Sifat fisik gel adalah parameter untuk mengetahui kualitas fisik gel yang meliputi daya sebar, viskositas, dan pergeseran viskositas setelah penyimpanan selama 1 bulan.
f. Daya sebar adalah kemampuan menyebar dari gel ekstrak lidah buaya yang diukur menggunakan kaca bulat dan diberi pemberat dimana berat kaca pembulat dan pemberat adalah 125 gram, kemudian diukur diameter penyebarannya. Daya sebar gel diukur 48 jam setelah formulasi.
h. Pergeseran viskositas adalah persentase perubahan viskositas gel setelah penyimpanan 1 bulan. Viskositas gel setelah 1 bulan diketahui dengan mengamati gerakan jarum penunjuk viskositas menggunakan viscotester. i. Formula gel optimum adalah formula gel yang memenuhi standar sediaan
semisolid yang ditetapkan (daya sebar 3-5 cm, viskositas 250 - 440 dPas, dan pergeseran viskositas kurang dari atau sama dengan 10%).
j. Desain faktorial adalah metode yang memungkinkan untuk mengetahui efek yang dominan dalam menentukan sifat fisik dan stabilitas sediaan gel antiinflamasi.
k. Faktor adalah variabel yang diteliti dalam penelitian (CMC-Na dan PEG 400).
l. Respon adalah besaran yang diamati, perubahan efek dan besarnya dapat dinyatakan secara kuantitatif. Dalam penelitian ini adalah sifat fisik dan stabilitas gel.
m. Level adalah tetapan atau nilai dari suatu faktor yang dinyatakan secara numerik.
n. Efek adalah perubahan respon yang disebabkan oleh variasi level dan faktor.
D. Bahan Penelitian
Bahan-bahan yang digunakan dalam penelitian ini adalah lidah buaya, etanol 96% (kualitas teknis), CMC-Na (kualitas farmasetis), PEG 400 (kualitas farmasetis), Natrium benzoat (kualitas farmasetis), Asam sitrat (kualitas farmasetis), Oleum menthae piperita (kualitas farmasetis), Akuades, Hewan uji tikus galur Wistar yang berusia 2-3 bulan dengan berat badan 200-300 gram, ketamin-xilazine, karagenan.
E. Alat Penelitian
Alat-alat gelas (PYREX-GERMANY), neraca analitik, mixer (Phillips), pH universal, viscometer seri VT 04 (RION-JAPAN), stopwatch, alat uji daya sebar, corong Buchner, jangka sorong, spuit injeksi, wadah plastik (net @200 g).
F. Tata Cara Penelitian 1. Determinasi tanaman lidah buaya
2. Pengumpulan dan penyiapan tanaman lidah buaya
Tanaman lidah buaya diperoleh dari kawasan Daerah Istimewa Yogyakarta. Tanaman diambil daunnya yang berwarna hijau, utuh, dan segar tetapi tidak terlalu tua (umur 8-10 bulan) kemudian dicuci dengan air mengalir. Setelah itu dilakukan sortasi basah, dan kulit daun dikupas kemudian diambil daging daunnya.
3. Pembuatan jus lidah buaya
Lidah buaya yang telah dipanen dikupas kulit luarnya hingga didapat daging daunnya. Daging daun tersebut dibersihkan dengan menggunakan air mengalir untuk menghilangkan cairan kuning (eksudat) dan kotoran yang menempel pada daging lidah buaya, kemudian daging dipotong kecil-kecil. Potongan daging lidah buaya yang telah dibersihkan kemudian dimasukkan ke dalam blender, kemudian disaring untuk memisahkan padatan dan cairannya kemudian disaring.
4. Isolasi polisakarida acemannan dari lidah buaya
larutannya dengan menggunakan saringan penghisap (Kusmawati dan Pratiwi, 2009).
5. Formula gel antiinflamasi
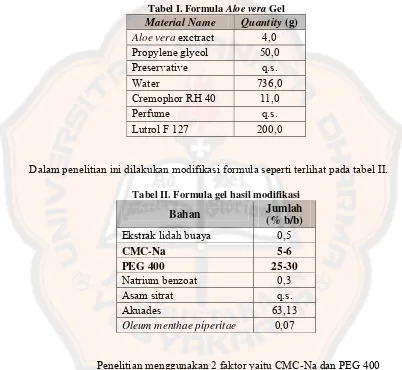
Formula standar : Aloe veraGel (Niazi, 2004) Tabel I. Formula Aloe veraGel Material Name Quantity (g)
Dalam penelitian ini dilakukan modifikasi formula seperti terlihat pada tabel II. Tabel II. Formula gel hasil modifikasi
Bahan Jumlah
Tabel III. Level rendah dan level tinggi CMC-Na dan PEG 400 pada formula gel
Berdasarkan formula yang akan dibuat dapat dilakukan perhitungan untuk menentukan besarnya sampel yang akan digunakan, yaitu :
(n-1)(p-1) > 15
Keterangan : n = jumlah sampel p = jumlah perlakuan
p = 4 (4 formula kombinasi komposisi CMC-Na dan PEG 400) Dari rumus perhitungan tersebut didapatkan hasil jumlah sampel n ≥ 2 sehingga pada penelitian ini dipergunakan jumlah sampel sebanyak 3 replikasi
untuk masing-masing formula yang digunakan (Bolton, 1997). 6. Pembuatan gel antiinflamasi
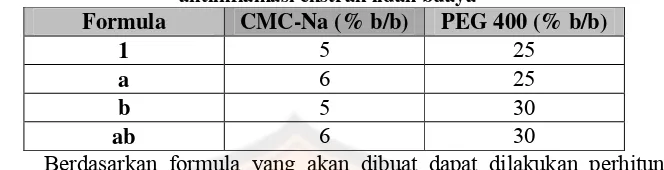
Berdasarkan tabel III, dibuat 4 formula gel antiinflamasi ekstrak lidah buaya menjadi seperti dalam tabel IV.
Tabel IV. Formula gel antiinflamasi ekstrak lidah buaya (200 gram)
Bahan F1 Fa Fb Fab
Ekstrak Lidah Buaya 1 1 1 1
CMC-Na 10 12 10 12
PEG 400 50 50 60 60
Natrium Benzoat 0,6 0,6 0,6 0,6
Akuadest 126,26 126,26 126,26 126,26
Asam Sitrat q.s. q.s. q.s. q.s.
Oleum menthae piperita 0,14 0,14 0,14 0,14 *semua formula dalam gram
level 1 selama 2 menit. PEG 400 dimasukkan kedalam wadah yang berisi CMC-Na diaduk menggunakan mixer dengan kecepatan putar level 1 selama 3 menit. Ekstrak Aloe barbadensis Mill. ditambahkan dan terus diaduk selama 2 menit dengan kecepatan putar level 2, kemudian ditambahkan natrium benzoat diikuti asam sitrat sedikit demi sedikit dan oleum menthae piperita sambil terus diaduk selama 2 menit pada kecepatan putar level 1 hingga pH yang didapat 4-6. Setelah itu dilakukan uji pH dengan kertas pH universal, pH sediaan yang diharapkan pH sediaan antara 4-6.
7. Uji sifat fisik dan stabilitas gel antiinflamasi ekstrak lidah buaya
Uji sifat fisik gel dilakukan dengan menguji daya sebar dan viskositas, untuk uji stabilitas dilakukan dengan menguji viskositas gel setelah penyimpanan selama 1 bulan.
Uji sifat fisik : 1. Uji daya sebar
2. Uji viskositas
Pengukuran viskositas menggunakan alat viscotester. Cara pengujiannya yaitu gel dimasukkan dalam wadah dan dipasang pada portable viscotester. Viskositas gel diketahui dengan mengamati gerakan jarum penunjuk viskositas. Pengukuran viskositas gel dilakukan 48 jam setelah formulasi. 3. Uji pergeseran viskositas
Pergeseran viskositas gel ekstrak lidah buaya diketahui dengan menghitung persentase perubahan viskositas gel setelah penyimpanan selama 1 bulan. Viskositas gel setelah penyimpanan 1 bulan diukur menggunakan alat viscotester. Cara pengujiannya yaitu gel dimasukkan dalam wadah dan dipasang pada portable viscotester. Viskositas gel setelah 1 bulan diketahui dengan mengamati gerakan jarum penunjuk viskositas.
8. Orientasi waktu pengolesan sediaan gel antiinflamasi ekstrak lidah buaya
9. Uji kemampuan antiinflamasi gel antiinflamasi ekstrak lidah buaya Hewan percobaan dibagi secara acak menjadi 5 kelompok yang masing-masing-masing berjumlah 3 ekor, terdiri dari 4 kelompok untuk masing-masing-masing formula dan 1 kelompok kontrol negatif. Sebelum perlakuan semua tikus dianastesi menggunakan ketamin-xilazine, lalu pada kaki kiri tiap tikus diinjeksi 0,05 ml keraganin-saline 1%. Setelah menunjukkan pembengkakan optimum (waktu hasil orientasi), masing-masing kelompok perlakuan diberi formula-formula gel antiinflamasi secara topikal, dan satu kelompok kontrol yang tidak diberi formula gel antiinflamasi. Pengukuran dilakukan setiap 1 jam selama 4 jam. Presentase inflamasi masing-masing tikus dihitung dengan rumus :
% ℎ = − 100
(Kharat dkk., 2010). G. Analisis Hasil
32 BAB IV
HASIL DAN PEMBAHASAN
A. Determinasi dan Ekstraksi Lidah Buaya
Tanaman lidah buaya yang digunakan dalam penelitian ini didapatkan dari daerah kota Yogyakarta dan digunakan tanaman yang berumur 8-10 bulan karena pada usia ini tanaman memiliki kandungan metabolit yang optimum (Sudarto, 1997). Selain itu juga dipilih tanaman lidah buaya yang memiliki daun segar, utuh dan berwarna hijau untuk menghindari kemungkinan berkurangnya atau rusaknya kandungan kimia di dalamnya yang diakibatkan oleh hama ataupun lingkungan sekitarnya. Sebelum digunakan tanaman lidah buaya diuji terlebih dahulu kebenaran tanaman yang dimaksud adalah benar tanaman lidah buaya. Maka dilakukan determinasi pada tanaman lidah buaya yang akan digunakan. Determinasi bertujuan untuk mendapatkan informasi apakah tanaman yang digunakan dalam penelitian adalah benar tanaman yang dimaksud. Determinasi dilakukan dengan mencocokkan morfologi tanaman lidah buaya dengan kunci determinasi yang ditulis oleh Backer dan Van Den Brink (1965) (lampiran 1). Hasil determinasi menunjukkan bahwa tanaman yang diambil merupakan Aloe barbadensisMill.
nantinya akan didapatkan daging daun lidah buaya yang berwarna bening, transparan, dan agak berlendir. Dalam proses pengupasan, bagian bergerigi pada tepi daun dihilangkan terlebih dahulu untuk mempermudah proses pengupasan. Daging daun lidah buaya tersebut kemudian direndam dalam air untuk mengilangkan eksudat cairan yang menempel.
Daging daun lidah buaya yang telah bersih dari eksudat, kemudian dihaluskan dengan blender sehingga didapatkan jus lidah buaya. Jus lidah buaya ini selanjutnya disaring untuk memisahkan sari dengan padatannya sehingga didapatkan filtrat lidah buaya yang bening dan sedikit kental. Jus lidah buaya yang disaring kemudian ditambah dengan etanol 96% dengan perbandingan 1 : 4, dalam hal ini 50 mL jus lidah buaya ditambah dengan 200 mL etanol 96%. Campuran jus lidah buaya tersebut diaduk selama 10 menit dengan menggunakan magnetic stirer, agar filtrat dan etanol bercampur homogen dan didapatkan hasil yang optimum. Kemudian didiamkan untuk proses pengendapan selama 10 jam pada suhu 10oC. Endapan yang terbentuk dipisahkan dari larutannya dengan menggunakan saringan penghisap. Sebagai pengendap polisakarida dalam tanaman lidah buaya, etanol memiliki kemampuan melarutkan polisakarida yang relatif kecil, meskipun kemampuan dalam melarutkan zat-zat lain yang relatif besar dengan demikian etanol dapat digunakan dalam proses pengendapan polisakarida penyusun karbohidrat dalam jaringan tanaman lidah buaya yang membentuk endapan polisakarida (Kusmawati dan Pratiwi, 2009).
pengekstrak bersifat lebih selektif, tidak beracun, dapat bercampur dengan air pada berbagai perbandingan serta kapang dan bakteri tidak dapat tumbuh di dalamnya.
B. Pembuatan Gel Antiinflamasi Ekstrak Lidah Buaya
Bentuk sediaan yang dibuat pada penelitian ini adalah hidrogel. Hidrogel adalah sediaan semisolid yang mengandung material polimer yang mempunyai kemampuan untuk mengembang dalam air tanpa larut dan bisa menyimpan air dalam strukturnya. Sifat hidrogel yaitu kandungan airnya relatif tinggi dan bersifat lembut, konsistensinya elastis sehingga kuat (Swarbrick dan Boylan, 1992). Dipilih hidrogel sebagai bentuk sediaan karena zat aktif yang larut dalam air, selain itu hidrogel memiliki kompatibilitas dengan jaringan biologis relatif baik, setelah kering akan meninggalkan suatu film tembus pandang yang elastis dengan daya lekat tinggi, yang tidak menyumbat pori kulit (Voight, 1994), memiliki sifat daya sebar yang baik pada kulit, pelepasan obat yang baik, tidak menghambat fungsi fisiologis kulit, efek dingin yang ditimbulkan, dan mudah dicuci dengan air (Voight, 1995).
digunakan adalah CMC-Na, menurut Rowe dkk. (2009), sebagai gelling agent CMC-Na berada pada range 3% - 6%. CMC-Na aman digunakan baik secara oral maupun topikal dan stabil pada pH 4 – 10. Untuk mencegah hilangnya lembab dari produk dan meningkatkan jumlah air (kelembaban) pada lapisan kulit terluar saat produk digunakan maka dalam sediaan gel ditambahkan humektan (Loden, 2001). Humektan yang digunakan dalam penelitian ini adalah polietilen glikol 400 (PEG 400). PEG 400 dapat berfungsi sebagai humektan bila diformulasikan dalam sediaan gel (Lieberman dan Martin, 1996) dan memiliki sifat larut dalam air, sehingga cocok untuk sediaan hidrogel. Pengawet yang digunakan dalam formula ini adalah natrium benzoat, karena relatif aman digunakan untuk sediaan topikal.
Sebelum dilakukan pembuatan gel, terlebih dahulu dilakukan orientasi gelling agentdan humektan untuk menentukan level rendah dan leveltinggi yang akan digunakan dalam penelitian. Grafik hasil orientasi pengaruh konsentrasi CMC-Na sebagai gelling agent terhadap daya sebar dan viskositas dapat dilihat pada gambar 6 dan 7.
formula sejumlah 200 gram, sehingga CMC-Na yang digunakan sebanyak 10-12 gram.
Gambar 6. Grafik Orientasi Pengaruh Konsentrasi Gelling Agentterhadap Daya Sebar
Gambar 7. Grafik Orientasi Pengaruh Konsentrasi Gelling Agentterhadap Viskositas
Konsentrasi CM C Na dalam formula (%)
Daya sebar
Konsentrasi CM C-Na dalam form ula (%)
Viskosit as
Gambar 8. Grafik Orientasi Pengaruh Konsentrasi PEG 400 terhadap Daya Sebar
Gambar 9. Grafik Orientasi Pengaruh Konsentrasi PEG 400 terhadap Viskositas
Dari gambar 8 dan 9 dapat diketahui bahwa pada konsentrasi PEG 400 10%, 15%, 25% dan 30% memberikan efek yang besar terhadap viskositas gel dan konsentrasi PEG 400 25% dan 30% memberikan efek yang besar pada daya sebar gel. Oleh karena itu, didapat daerah irisan dari kedua grafik tersebut, yakni konsentrasi PEG 400 25% dan 30%. Pada daerah tersebut juga sudah memenuhi
y = 0.0152x + 3.4
Konsentrasi PEG 400 dalam formula (%)
Daya sebar
Konsentrasi PEG 400 dalam formula (%)
viskosit as
viskositas yang diinginkan (250-440 dPa.s) serta daya sebar yang diinginkan (3-5 cm), sehingga dipilih level rendah PEG 400 25% dan level tingginya 30%. Gel yang dibuat tiap formula sejumlah 200 gram, sehingga PEG 400 yang digunakan sebanyak 50-60 gram. Setelah didapatkan level tinggi dan level rendah dari gelling agent CMC-Na dan humektan PEG 400 maka dilanjutkan dengan pembuatan sediaan gel.
C. Uji pH Gel Antiinflamasi Ekstrak Lidah Buaya
Uji pH pada gel antiinflamasi ekstrak lidah buaya dilakukan dengan pH stik atau kertas pH universal. Uji pH bertujuan untuk mengetahui pH sediaan sesaat setelah dibuat, setelah 48 jam, dan pada penyimpanan 1 bulan. Hasil uji pH pada sediaan gel antiinflamasi ekstrak lidah buaya dapat dilihat pada tabel V.
Tabel V. Uji pH gel antiinflamasi ekstrak lidah buaya
Formula
D. Karakterisasi Sifat Fisik dan Stabilitas Gel Antiinflamasi Ekstrak Lidah Buaya
Sifat fisik dan stabilitas berfungsi untuk mengetahui kualitas dari suatu sediaan. Sediaan obat yang baik adalah sediaan yang memenuhi persyaratan sifat fisik dan stabil dalam penyimpanan. Untuk sediaan gel, sifat fisik yang dapat diukur adalah daya sebar dan viskositas, sedangkan untuk stabilitas dapat dilakukan uji pergeseran viskositas. Untuk mengetahui sifat fisik sediaan gel, pengukuran daya sebar dan viskositas sediaan gel antiinflamasi ekstrak lidah buaya dilakukan 48 jam setelah pembuatan, sedangkan untuk mengetahui stabilitasnya dilakukan uji pergeseran vikositas setelah 1 bulan penyimpanan. 1. Uji daya sebar
Uji daya sebar dilakukan 48 jam setelah sediaan gel dibuat. Uji daya sebar bertujuan untuk mengetahui luas area gel dapat menyebar dan merata saat digunakan. Cara ujinya yaitu dengan gel ditimbang seberat 1 gram, diletakkan ditengah kaca bulat berskala. Diatas gel diletakkan kaca bulat lain dan pemberat dengan berat total 125 gram, didiamkan selama 1 menit, kemudian dicatat diameter penyebarannya (Garg dkk., 2002). Daya sebar merupakan karakteristik yang bertanggungjawab terhadap penghantaran obat ke tempat aksi, kemudahan dalam mengeluarkan sediaan dari wadah, dan penerimaan konsumen (Garg dkk., 2002).
yang tidak terlalu kecil ataupun terlalu besar. Besarnya daya sebar yang dituju pada penelitian ini adalah 3 – 5 cm. Berikut hasil uji daya sebar yang dilakukan 48 jam setelah pembuataan sediaan dan 1 bulan setelah penyimpanan.
Tabel VI. Daya sebar gel antiinflamasi ekstrak lidah buaya 48 jam setelah pembuatan
Replikasi F1 Fa Fb Fab
1 3,58 cm 3,4 cm 3,9 cm 3,45 cm
2 3,53 cm 3,5 cm 4,05 cm 3,63 cm
3 3,55 cm 3,55 cm 3,93 cm 3,3 cm
rata-rata 3,55 cm 3,48 cm 3,96 cm 3,46 cm
SD 0,025 0,076 0,079 0,165
Tabel VII. Daya sebar gel antiinflamasi ekstrak lidah buaya setelah 1 bulan penyimpanan
Replikasi F1 Fa Fb Fab
1 4,08 cm 3,65 cm 4,18 cm 3,50 cm
2 4,20 cm 3,80 cm 3,95 cm 3,63 cm
3 3,95 cm 3,38 cm 4,10 cm 3,55 cm
rata-rata 4,08 cm 3,61 cm 4,07 cm 3,56 cm
SD 0,125 0,212 0,116 0,065
Hasil uji daya sebar tabel VI menunjukkan bahwa sediaan gel yang dibuat memenuhi persyaratan daya sebar yaitu memiliki daya sebar diantara 3 – 5 cm.
2. Uji viskositas dan pergeseran viskositas
dengan pergeseran viskositas kurang dari 10%. Hasil uji viskositas 48 jam setelah pembuatan dan 1 bulan setelah penyimpanan dapat dilihat pada tabel VIII.
Tabel VIII. Viskositas gel antiinflamasi ekstrak lidah buaya 48 jam setelah pembuatan (dPa.s)
Tabel IX. Viskositas gel antiinflamasi ekstrak lidah buaya 1 bulan setelah penyimpanan (dPa.s)
Dari hasil yang didapat (tabel VIII) menunjukkan hanya formula F1 yang memiliki viskositas seperti yang dikehendaki, yaitu diantara 250 – 440 dPa.s, sedangkan formula lainnya tidak masuk kedalam rentang, hal ini kemungkinan disebabkan adanya interaksi antara bahan yang satu dengan yang lain sehingga mempengaruhi viskositas sediaan.
Tabel X. Pergeseran viskositas gel antiinflamasi ekstrak lidah buaya Formula Replikasi Viskositas (dPa.s) Pergeseran
viskositas (%)
rata-rata ± SD 6,000 ±10,392
viskositas menunjukkan bahwa sediaan yang dibuat memiliki nilai pergeseran viskositas kurang dari 10%. Hal ini menunjukkan bahwa sediaan yang dibuat memiliki stabilitas yang baik.
Gambar 10. Grafik Viskositas Gel setiap Minggu
E. Efek Penambahan CMC-Na dan PEG 400 serta Interaksinya dalam Menentukan Sifat Fisik Gel Antiinflamasi Ekstrak Lidah Buaya
Perbedaan level dan faktor menyebabkan perubahan respon yang disebut dengan efek. Efek dari CMC-Na, PEG 400, dan interaksi keduanya terhadap sifat fisik sediaan gel dapat diketahui dengan menggunakan analisis statistik program R.-2.14.1 dengan uji two way ANOVA pada taraf kepercayaan 95%. Dilakukan juga analisis signifikansi pada masing-masing faktor dalam menimbulkan efek. Penelitian ini menggunakan rancangan desain faktorial dengan 2 faktor pada 2 level yaitu level tinggi dan rendah.
1. Uji normalitas data
Uji normalitas data pada penelitian ini dilakukan dengan melihat distribusi data yang dihasilkan dalam penelitian yang diharapkan distribusi datanya adalah normal (Mario dan Sujarweni, 2006). Distribusi data dikatakan normal jika memiliki p-value > 0,05 (Istyastono, 2012). Uji Shapiro-Wilk digunakan untuk menguji normalitas data. Hasil pengujian yang dilakukan, menunjukkan bahwa data memilki p-value lebih dari 0,05 yang berarti data memiliki distribusi normal.
Untuk dapat melakukan uji ANOVA, data yang dihasilkan haruslah memiliki kesamaan varian, yang dapat dilihat dari besarnya p-value. Data dikatakan tidak menunjukkan perbedaan varian jika memiliki p-value> 0,05 (Suhartono, 2008).
Tabel XII. Uji variansi data viskositas dan daya sebar
Data p-value
Viskositas 0,2024 Daya sebar 0,3905
Hasil uji variansi data menunjukkan bahwa semua data baik viskositas ataupun daya sebar memiliki p-value > 0,05 sehingga data yang ada tidak menunjukkan perbedaan varian dan dapat dilakukan uji ANOVA dan parametrik.
3. Respon viskositas
Pengukuran respon viskositas dilakukan setelah 48 jam sediaan gel dibuat. Analisis hasil dilakukan dengan menggunakan perangkat lunak R-2.14.1.
Tabel XIII. Analisis ANOVA efek CMC-Na dan PEG 400 dan interaksinya dalam menentukan respon viskositas CMC-Na -653,333 254,25 15052 15052,1 1 0,015181 PEG 400 -125 50,85 29502 29502,1 1 0,002587 Interaksi 26,333 9,207 13002 13002,1 1 0,021152
faktor dan interkasinya, memiliki p-value < 0,05 sehingga dapat disimpulkan ketiganya memiliki efek yang signifikan terhadap respon viskositas sediaan. Faktor yang paling berpengaruh terhadap viskositas sediaan adalah CMC-Na karena memiliki nilai efek yang lebih besar jika dibandingkan dengan faktor lainnya.
Persamaan desain faktorial untuk respon viskositas adalah y = 3513,33 (± 1404,141) – 653,33 (± 254,250) (X1) – 125,00 (± 50,850) (X2) + 26,333 (±9,207) (X1X2) dengan p-value0,00244; X1 adalah CMC-Na, X2 adalah PEG 400, serta X1X2 adalah interaksi antar keduanya. Gambar 11 dan 12 menunjukkan pengaruh CMC-Na dan PEG 400 terhadap viskositas sediaan gel antiinflamasi ekstrak lidah buaya.
Gambar 12. Grafik hubungan PEG 400 terhadap respon viskositas setelah 48 jam
Pada gambar 11 dapat dilihat bahwa pada penambahan CMC-Na pada level rendah PEG 400 tidak memberikan respon viskositas. Sedangkan pada level tinggi PEG 400 penambahan CMC-Na memberikan respon viskositas yang cukup besar. Hal ini disebabkan karena PEG 400 selain sebagai humektan juga dapat berfungsi sebagai binding dan juga thickening agent (Rowe,2009). PEG 400 merupakan cairan yang memiliki sifat yang hidrofilik, sehingga bila dicampurkan dengan CMC-Na akan meningkatkan ikatan struktur gel yang terbentuk sehingga matriks gel yang telah terbentuk akan semakin kuat dan dapat memperangkap bahan-bahan lain di dalam matriks gel tersebut. Hal ini akan menyebabkan sediaan gel yang terbentuk akan semakin stabil tingkat kekentalannya. Gambar 12 juga menunjukkan hasil yang hampir sama dengan gambar 11 yaitu penambahan PEG 400 sebagai humektan pada level tinggi CMC-Na memberikan respon viskositas. Sehingga dapat disimpulkan bahwa keduanya memiliki pengaruh terhadap respon viskositas, namun faktor CMC-Na yang dianggap memiliki
pengaruh signifikan karena pada analisis statistik memiliki nilai efek yang besar jika dibandingkan dengn faktor PEG 400 ataupun interaksi keduanya.
4. Respon daya sebar
Pengukuran respon daya sebar dilakukan setelah 48 jam sediaan gel dibuat. Analisis ANOVA dilakukan dengan menggunakan perangkat lunak R-2.14.1. Dari hasil analisis didapatkan data seperti terlihat dalam tabel XIV.
Tabel XIV. Analisis ANOVA efek CMC-Na dan PEG 400 dan interaksinya dalam menentukan respon daya sebar CMC-Na 2,08000 0,63824 0,243675 0,243675 1 0,001146 PEG 400 0,51133 0,12765 0,110208 0,110208 1 0,010587 Interaksi -0,08600 0,02311 0,138675 0,138675 1 0,005865
Sama seperti pada respon viskositas, jika p-value yang dimiliki oleh suatu faktor < 0,05 maka dapat dikatakan faktor tersebut memberikan efek yang signifikan terhadap respon. Dari data yang didapat menunjukkan bahwa kedua faktor dan interkasinya, memiliki p-value < 0,05 sehingga dapat disimpulkan ketiganya memiliki efek yang signifikan terhadap respon daya sebar sediaan. Dari tabel hasil analisis ANOVA pada tabel XIV dapat dilihat bahwa CMC-Na memiliki nilai efek paling besar yaitu 2,08000 jika dibandingkan dengan faktor lainnya, hal ini menunjukkan bahwa untuk respon daya sebar, CMC-Na yang mempunyai pengaruh yang signifikan.
0,086 (±0,02311) (X1X2) dengan p-value 8,889 x 10-4; X1 adalah CMC-Na, X2 adalah PEG 400, serta X1X2 adalah interaksi antar keduanya. Gambar 13 dan 14 menunjukkan pengaruh CMC-Na dan PEG 400 terhadap daya sebar sediaan gel antiinflamasi ekstrak lidah buaya.
Gambar 13. Grafik hubungan CMC-Na terhadap respon daya sebar setelah 48 jam
Gambar 14. Grafik hubungan PEG 400 terhadap respon daya sebar setelah 48 jam Gambar 13 menunjukkan pada level rendah PEG 400 penambahan CMC-Na tidak meberikan respon daya sebar ditandai dengan grafik yang terlihat lurus. Sedangkan pada level tinggi PEG 400, penambahan CMC-Na berpengaruh
signifikan, dimana penambahan CMC-Na akan menurunkan respon daya sebar. Pada gambar 14 menunjukkan bahwa pada level tinggi CMC-Na penambahan PEG 400 tidak memberikan respon daya sebar, grafik yang dihasilkan juga berupa garis lurus. Sedangkan pada level rendah CMC-Na, penambahan PEG 400 memberikan respon daya sebar yang signifikan, dimana daya sebar akan naik seiring penambahan PEG 400. Sehingga dapat disimpulkan bahwa CMC-Na memiliki pengaruh signifikan karena pada analisis statistik memiliki nilai efek yang besar terhadap daya sebar jika dibandingkan dengn faktor PEG 400 ataupun interaksi keduanya.
F. Stabilitas Gel Antiinflamasi Ekstrak Lidah Buaya
Tabel XV. Pergeseran viskositas tiap formula setelah 1 bulan penyimpanan (x± SD)
Hasil yang didapat menunjukkan bahwa sediaan memiliki pergeseran viskositas < 10%. Hal ini berarti sediaan gel antiinflamasi ekstrak lidah buaya yang dibuat stabil. Selain itu juga dilakukan uji t berpasangan terhadap hasil pengukuran viskositas yang didapat pada hari ke 2 setelah sediaan dibuat dan 1 bulan setelah penyimpanan. Uji t berpasangan dilakukan untuk mengetahui kestabilan gel yang dibuat, jika hasil menunjukkan p-value> 0,05 maka sediaan yang dibuat stabil, dan jika sebaliknya yaitu p-value < 0,05 maka sediaan tidak stabil. Hasil dari pengujian dengan menggunakan Uji t berpasangan dapat dilihat pada tabel XVI.
G. Contour PlotGel Antiinflamasi Ekstrak Lidah Buaya
Persamaan desain faktorial yang didapat dari hasil viskositas dan daya sebar dapat dibuat contour plot. Contour plot adalah grafik yang merupakan area optimum dari formula yang menunjukkan parameter sediaan gel yang baik. Dari grafik contour plot yang dibuat dapat diketahui daerah yang memiliki kriteria yang diinginkan.
Gambar 15. Contour plotviskositas gel antiinflamasi ekstrak lidah buaya
Gambar 17. Contour plotviskositas dan daya sebar gel antiinflamasi ekstrak lidah buaya
Gambar 17 menunjukkan bahwa contour plot viskositas dan daya sebar gel antiinflamasi ekstrak lidah buaya tidak saling tumpang tindih sehingga tidak ditemukan area optimum yang memenuhi karakteristik fisik yang diinginkan. Hal ini kemungkinan disebabkan karena pengaruh suhu ruangan pada saat pembuatan dan penyimpanan gel, kecepatan putar mixer pada saat pembuatan serta lama pengadukan yang belum dioptimasi.
H. Uji Aktivitas Gel Antiinflamasi Ekstrak Lidah Buaya
Tabel XVII. Hasil uji aktivitas antiinflamasi gel antiinflamasi ekstrak lidah buaya mengalami penurunan inflamasi berdasarkan perhitungan persentase inhibisinya dengan hasil perhitungan persentase inhibisinya untuk semua formula lebih besar dibandingkan dengan kontrol negatif. Hal ini menujukkan bahwa sediaan yang dibuat memiliki aktivitas antiinflamasi. Hasil tersebut kemudian diperkuat dengan analisis statistik.
Gambar 18. Persentase Inhibisi kontrol (-) dan gel antiinflamasi ekstrak lidah buaya
Tabel XVIII. Uji normalitas data aktivitas antiinflamasi Data p-value
Data terdistribusi normal dan memiliki kesamaan varian, maka analisis data dapat dilanjutkan dengan uji t independentantara kontrol (-) dengan semua formula gel. Hasil dari uji t independent(tabel XIX) menunjukkan bahwa semua formula yaitu F1, Fa, Fb, dan Fab memiliki p-value< 0,05 yang berarti kelompok perlakuan tersebut memiliki persentase inhibisi lebih besar daripada kontrol (-) dan berbeda secara signifikan serta memiliki aktivitas antiinflamasi.
Tabel XIX. Uji t independentnilai persentase inhibisi kontrol (-) dengan gel antiinflamasi ekstrak lidah buaya
Data p-value F1 0,0419 Fa 0,0181 Fb 0,0232 Fab 0,0224
Tanaman lidah buaya sebagian besar terdiri dari polisakarida, dan acemannan merupakan senyawa yang paling banyak terkandung di dalam lidah buaya dan diidentifikasi sebagai bahan aktif utama dalam gel daun lidah buaya (Cowsert, 2010). Mekanisme acemannan sebagai antiinflamasi yakni dengan cara mengeblok pembentukan histamin dan bradikinin, serta menghambat aktivitas keduanya (Cowsert, 2010).
57 BAB V
KESIMPULAN DAN SARAN
A. Kesimpulan
1. CMC-Na merupakan faktor yang paling dominan dalam menentukan viskositas dan daya sebar gel antiinflamasi ekstrak lidah buaya.
2. Tidak ditemukan area komposisi optimum yang diprediksi sebagai formula optimum gel dari gelling agentdan humektan yang memenuhi persyaratan sifat fisik gel (viskositas serta daya sebar) dan stabilitas gel (pergeseran viskositas).
3. Gel antiinflamasi ekstrak lidah buaya memberikan efek farmakologis berupa antiinflamasi pada kaki tikus yang diinduksi karagenan.
B. Saran
1. Perlu dilakukan standardisasi ekstrak lidah buaya untuk menjamin kualitas sediaan.
2. Perlu dilakukan optimasi lama pencampuran, kecepatan pengadukan, serta suhu penyimpanan untuk mendapatkan sediaan gel antiinflamasi ekstrak lidah buaya yang memenuhi kriteria.
DAFTAR PUSTAKA
Anonim, 2012, Mengapa Aloe vera Salep Salah Satu Pengobatan Terbaik untuk Sunburns, Prmob Free Articel Directory, http://id.prmob.net/aloe-vera/kulit/terbakar-sinar-matahari-458678.html, diakses tanggal 13 Mei 2013.
Anonim, 2013, Acemannan, http://en.wikipedia.org/wiki/Acemannan, diakses tanggal 31 Agustus 2013.
Armstrong, N.A., dan James, K.C., 1996, Pharmaceutical Experimental Design and Interpretation, Tylor and Francis, USA, pp. 131-165.
Ayuningsih, L.N., dan Setyaningrum, W., 2011, Salting OutMannan Lidah Buaya (Aloe vera) Menggunakan Co-Solvent Metanol, Etanol, dan Isopropanol, , Laporan Penelitian, Jurusan Teknik Kimia, Fakultas Teknik, Universitas Diponegoro, Semarang.
Backer, C.A., dan Van Den Brink, R.C.B., 1965, Flora of Java, Vol. 3, N.V.P Noordhoff-Groningen, Netherlands, pp. 82-83, 88-89.
Bassettti, A., dan Sala, 2005, The Great Aloe Book, Zuccari Pty Ltd., United State of America, pp. 27.
Benson, H.A.E., 2005, Transdermal Drug Delivery : Penetration Enhancement Technique current drug delivery, National Center for Biotechnology Information, 2(1), 23-33.
Bolton, 1997, Pharmaceutical Statistics Practical and Clinical Applications, 3rd Ed., Marcel Dekker, Inc., New York, pp. 610-619.
Bouchard, A., 2007, Properties of Sugar, Polyol, and Polisaccharide Water-Etanol Solution, J. Chem. Eng. Data 52, pp. 1838-1842.
Choi, S., dan Chung, M.,H., 2003, Review on The Relationship Between Aloe Vera Componennts and Their Biologic Effects, Seminar in Integrative Medicine, vol. 1 (1), 54-56.