PENGARUH UKURAN PARTIKEL TERHADAP OPTIMASI
DERAJAT REDUKSI Fe PADA BIJIH LATERIT LOW GRADE
SKRIPSI
EKO MULIA PUTRA 0806455692
FAKULTAS TEKNIK
DEPARTEMEN METALURGI DAN MATERIAL DEPOK
UNIVERSITAS INDONESIA
PENGARUH UKURAN PARTIKEL TERHADAP OPTIMASI
DERAJAT REDUKSI Fe PADA BIJIH LATERIT LOW GRADE
SKRIPSI
Diajukan sebagai salah satu syarat untuk memperoleh gelar Sarjana Teknik
EKO MULIA PUTRA 0806455692
FAKULTAS TEKNIK
DEPARTEMEN METALURGI DAN MATERIAL DEPOK
Skripsi ini adalah hasil karya saya sendiri, dan semua sumber baik yang dikutip maupun dirujuk telah saya nyatakan dengan benar.
Nama : Eko Mulia Putra
NPM : 0806455692
Tanda Tangan :
Puji dan syukur senantiasa saya panjatkan kehadirat Allah SWT karena dengan berkat dan rahmat-Nya, saya dapat menyelesaikan skripsi ini dengan sebaik-baiknya. Skripsi yang berjudul “Pengaruh Ukuran Partikel Terhadap Optimasi Derajat Reduksi Fe pada Bijih Laterit Low Grade” ini disusun untuk memenuhi sebagian persyaratan akademis dalam meraih gelar Sarjana Teknik di Departemen Metalurgi dan Material Fakultas Teknik Universitas Indonesia. Saya menyadari bahwa, tanpa bantuan dan bimbingan dari berbagai pihak, dari masa perkuliahan sampai penyusunan skripsi ini, sangatlah sulit bagi saya untuk menyelesaikan skripsi ini. Oleh karena itu saya mengucapkan terima kasih kepada:
1. Prof. Dr. Ir. Johny Wahyuadi Soedarsono, DEA, selaku dosen pembimbing yang telah menyediakan waktu, tenaga, dan pikiran untuk mengarahkan saya dalam penyusunan skripsi ini.
2. Prof. Dr-Ing. Ir. Bambang Suharno, selaku Kepala Departemen Teknik Metalurgi dan Material FTUI.
3. Dr. Ir. Donanta Daneswara, M.Si selaku Pembimbing Akademis penulis. 4. Kedua orang tua tercinta Dasmawati dan Ir. Kasmis yang senantiasa
mendukung, mendoakan, dan selalu ada untuk saya, serta adik saya Kurnia Dwi Putra.
5. Teman-teman seperjuangan dan seperjalanan di Metalurgi dan Material FTUI: a. Jenifer Gunawan yang telah membimbing saya selama penelitian ini b. Teman seperjuangan dalam penelitian ini: Prabu Binsar Setiawan dan
Patrick Siregar
c. Teman Penelitian dan tugas akhir dengan tema ekstraksi : Achmad Taufiq, Suprayogi, Nova Listyanto, Frendy Lumban Bantu, Doni Johansyah, Gana Damar, David, dan Erwin
d. Teman-teman angkatan 2008 yang mengerjakan skripsi bersama-sama di Lab Metalografi dan Lab Korosi : Ardiles Jeremia Sitorus, Rendi Fajar
Yudi Prasetyo, Brian Hermawan, Indra Septiawan, Yosia Samuel, Wali Riansyah, M Fahmi Haddar, Rulliansyah, Vicky Indrafusa, Abdullah Nirmolo, Fuad Hakim Nofec Budiarto, dan Allam Putra.
e. Teman-teman Kantek Zona Hijau.
f. Serta untuk teman-teman seperjalanan di Metalurgi dan Material angkatan 2008 yang memulai kekeluargaan sejak dikumpulkan di masa PPAM hingga saat ini dan membuat kenangan indah dan pengalaman tidak terlupakan. Semoga ikatan keluarga ini akan bertahan terus hingga kita tua nanti.
Akhir kata, saya berharap Allah SWT berkenan membalas segala kebaikan semua pihak yang telah membantu. Semoga skripsi ini membawa manfaat bagi pengembangan ilmu metalurgi dan material ke depannya.
Depok, Juli 2012
Sebagai sivitas akademik Universitas Indonesia, saya yang bertanda tangan di bawah ini, :
Nama : Eko Mulia Putra
NPM : 0806455692
Program Studi : Teknik Metalurgi dan Material Departemen : Metalurgi dan Material
Fakultas : Teknik Jenis Karya : Skripsi
Demi pengembangan ilmu pengetahuan, menyetujui untuk memberikan kepada Universitas Indonesia Hak Bebas Royalti Noneksklusif (Non-exclusive
Royalty-Free Right) atas karya ilmiah saya yang berjudul :
Pengaruh Ukuran Partikel Terhadap Optimasi Derajat Reduksi Fe pada Bijih Laterit Low Grade
beserta perangkat yang ada (jika diperlukan). Dengan Hak Bebas Royalti Nonekslusif ini, Universitas Indonesia berhak menyimpan, mengalihmedia atau formatkan, mengelola dalam bentuk pangkalan data (database), merawat, dan mempublikasikan tugas akhir saya selama tetap mencantumkan nama saya sebagai penulis atau pencipta dan sebagai pemilik Hak Cipta.
Demikian pernyataan ini saya buat dengan sebenarnya. Dibuat di : Depok Pada Tanggal : Juli 2012
Yang menyatakan
ABSTRAK
Nama : Eko Mulia Putra
NPM : 0806455692
Program Studi : Teknik Metalurgi dan Material
Judul Skripsi : Pengaruh Ukuran Partikel Terhadap Optimasi Derajat Reduksi Fe pada Bijih Laterit Low Grade
Laterit yang ada di Indonesia memiliki kandungan Fe sekitar 50 %,. Walaupun bijih laterit memiliki kandungan Fe yang besar tapi belum ada pemanfaatan bijih laterit untuk di pengolahan sebagai bahan baku pembuatan pig
iron atau iron nugget. Agar bijih laterit dapat digunakan, bijih besi laterit yang
banyak mengandung Fe2O3 harus direduksi untuk mendapatkan besi Fe sehingga
kandungan kadar Fe dalam laterit meningkat. Penelitian ini dilakukan pada bijih laterit dengan jenis saprolit dengan menggunakan parameter ukuran partikel untuk mengetahui ukuran partikel dengan kandungan Fe yang optimum. Ukuran partikel yang digunakan adalah ukuran mesh 120, 170, 200, dan 270. Reduksi yang dilakukan adalah dengan cara memanaskan Bijih yang telah dicampur dengan batubara dalam oven dengan suhu 1100OC selama 60 menit. Setelah itu, bijih tersebut dilakukan dengan pengujian karakterisasi kuantitatif dengan EDAX dan karakterisasi kualitatif dengan XRD. Ukuran partikel mempengaruhi kadar peningkatan Fe pada bijih laterit. Semakin besar ukuran partikel maka kadar Fe yang terkandung dalam bijih laterit setelah proses roasting semakin besar. Peningkatan Kadar Fe terbesar terdapat pada ukuran partikel mesh 120 yaitu sebesar 12,54%. Akan tetapi, kadar Fe yang terbesar terdapat pada ukuran partikel mesh 170 sebesar 46,7%.
Name : Eko Mulia Putra
NPM : Eko Mulia Putra
Major : Metallurgy and Material Engineering
Title : Effect of Particle Size on The Optimization Degree Reduction of Fe in Low Grade Laterite ores
Laterite in Indonesia has about 50% Fe content. Although laterite ore contains a large Fe but utilization of lateritic ore for processing as the raw material to make pig iron is rarely. Laterite ore contains Fe2O3 should be reduced to obtain
Fe. So that, Fe content in laterite increases. The research was conducted on lateritic ore, saprolite type, use the parameters of particle size to determine the optimum size of the content. The research was carried out using the particle size parameter. Particle size which used are 120, 170, 200 and 270 mesh. The reduction is done by heating the laterite ore mixed with coal in the oven with a temperature of 1100 OC for 60 min. Then, the characterization tests for laterite ore by EDAX and XRD. Particle size affect Fe content in laterite ores. Elevated contents of Fe increases as increasing particle size after reduction process. The largest elavated content of Fe occur on 120 mesh particle size that is equal to 12.54%.. In other side, the largest Fe content occur on 170 mesh particle size of 46.7%.
DAFTAR ISI
HALAMAN JUDUL ... i
HALAMAN PERNYATAAN ORISINILITAS ... iii
HALAMAN PENGESAHAN ... iv
KATA PENGANTAR ... v
HALAMAN PERNYATAAN PERSETUJUAN PUBLIKASI TUGAS AKHIR UNTUK KEPENTINGAN AKADEMIS ... vii
ABSTRAK ... viii
ABSTRACT ... ix
DAFTAR ISI ... x
DAFTAR TABEL ... xii
DAFTAR GAMBAR ... xiii
DAFTAR LAMPIRAN ... xiv
Bab 1 PENDAHULUAN ... 1
1.1. Latar Belakang ... 1
1.2. Perumusan Masalah ... 3
1.3. Tujuan Penelitian ... 3
1.4. Ruang Lingkup dan Batasan Masalah ... 3
1.5. Sistematika Penulisan ... 4
Bab2 TEORI PENUNJANG ... 6
2.1. Bijih Laterit ... 6
2.2. Reduksi Oksida ... 7
2.2.1 Prinsip Dasar Proses Reduksi ... 8
2.2.1.1 Termokimia ... 9
2.2.1.2 Energi Bebas ... 10
2.2.1.3 Reaksi Boudouard... 13
2.2.2 Mekanisme Reduksi Langsung ... 15
2.2.2.1 Pembentukan Gas Reduktor ... 15
2.2.2.2 Adsorpsi Gas pada Besi Oksida ... 18
2.2.2.3 Proses Difusi Dalam Besi Oksida ... 19
2.4 Energy Dispersive X-Ray Alnalysis (EDAX) ... 21
2.5 X-Ray Diffraction (XRD) ... 22
3. METODOLOGI PENELITIAN ... 24
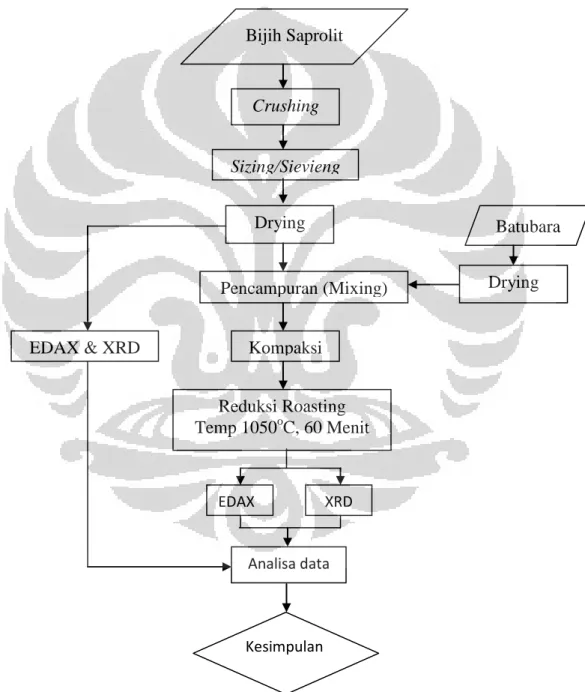
3.1. Diagram Alir Penelitian... 24
3.2. Alat dan Bahan ... 25
3.3. Prosedur Penelitian... 25
3.3.1. Preparasi Sampel ... 25
3.3.1.1 Crushing & Sievieng ... 25
3.3.1.2 Drying dan Kompaksi ... 25
3.3.2. Roasting ... 26
3.3.3. Uji Karakterisasi... 26
3.3.3.1 Uji EDAX... 26
4.3 Pengujian EDAX ... 32
5. KESIMPULAN ... 37
DAFTAR PUSTAKA ... 38
DAFTAR TABEL
Tabel 2.1 Presentation of average value of laboratory analysis of Nickel laterite ore during year’s 2008, 2009 and 2010 – Indonesia ... 7 Tabel 4.1 Data massa sample sebelum dan sesudah reduksi roasting ... 28 Tabel 4.2 Data Hasil Pengujian EDAX pada bijih laterit sebelum proses reduksi ... 32
Gambar 2.3. Diagram Bauer Glassner dan Boudouard ... 14
Gambar 2.4 Gasifikasi Karbon ... 16
Gambar 2.5 Mekanisme reduksi langsung pada pellet berporos ... 20
Gambar 2.6 Prinsip Energy Dispersive X-Ray Analysis (EDAX) ... 21
Gambar 2.7 Contoh Hasil Pengujian Energy Dispersive X-Ray Analysis ... 22
Gambar 2.8 Contoh grafik hasil pengujian XRD ... 23
Gambar 3.1 Diagram alir penelitian ... 24
Gambar 4.1 Gambar hasil pengujian XRD sampel awal bijih saprolit ... 29
Gambar 4.2 Gambar hasil pengujian XRD pada ukuran partikel mesh 120 setelah reduksi ... 30
Gambar 4.2 Gambar hasil pengujian XRD pada ukuran partikel mesh 120 setelah reduksi ... 30
Gambar 4.4 Gambar hasil pengujian XRD pada ukuran partikel mesh 200 setelah reduksi ... 31
Gambar 4.5 Gambar hasil pengujian XRD pada ukuran partikel mesh 170 setelah reduksi ... 32
Gambar 4.6 Grafik Perubahan Kadar Fe sebelum dan setelah reduksi Roasting pada setiap ukuran partikel ... 32
Gambar 4.7 Grafik Perubahan Kadar O sebelum dan setelah reduksi Roasting pada setiap ukuran partikel... 36
DAFTAR LAMPIRAN Lampiran 1 Hasil Pengujian EDAX
BAB 1 PENDAHULUAN
1.1 LATAR BELAKANG
Sebagian besar sumber nikel dunia yang telah diketahui terkandung dalam tipe deposit laterit. Mineral nikel terdapat dalam bentuk baik laterit maupun sulfida, namun mayoritas cadangan nikel dunia (65%) terdapat dalam bentuk bijih laterit. Sekitar 55% produksi nikel dunia berasal dari bijih sulfida sedangkan sumber nikel baru berasal dari cadangan laterit.
Sekitar 72% sumber nikel dunia ditemukan terutama di daerah tropis seperti Indonesia, Kuba, Kaledonia Baru, Filipina dan Australia. Sisanya sebesar 28% adalah tipe deposit sulfida terutama terdapat di Kanada dan Rusia. Walaupun mayoritas sumber nikel dunia yang diketahui terkandung dalam laterit, produksi nikel dari sulfida lebih dominan karena kadar nikel yang lebih tinggi dan pengolahan yang lebih mudahdibandingkan dengan tipe deposit laterit. Kadar nikel dalam tipe deposit sulfida secara komersial bervariasi antara 0,5-8,0%, sedangkan dari tipe deposit laterit sekitar 1,0-2,0%.[1]
Besarnya cadangan nikel dalam bijih laterit di Indonesia diduga mencapai 12 % dari cadangan dunia. Meskipun cadangan nikel Indonesia bukanlah yang terbesar di dunia, namun Indonesia merupakan salah satu produsen pertambangan nikel terbesar di dunia. Penambangan dan pengolahan laterit nikel di Indonesia didominasi oleh PT INCO Tbk.dan PT Aneka Tambang Tbk (PT Antam). Pada saat ini PT INCO mengolah laterit nikel untuk memproduksi nikel dalam bentuk nickel matte (Ni3S2) yang seluruh produksinya diekspor ke Jepang, sedangkan PT
Antam mengolah laterit nikel untuk memproduksi nikel dalam bentuk fero-nikel (logam paduan FeNi).
Sejak tahun 1938, bijih laterit yang tidak memenuhi persyaratan yang biasa disebut bijih laterit off grade, dieskpor keluar negeri [2]. Beberapa perusahan lain yang memiliki luas pertambangan lebih kecil di Sulawesi dan Maluku hanya
2
pembuatan nickel pig iron. Kenyataan ini menunjukan bahwa potensi laterit di indonesia yang sangat besar belum dimanfaatkan secara maksimal. Selain itu, dengan adanya UU Minerba yang melarang mengeskpor bahan baku menjadi suatu keharusan untuk menolahnya di Indonesia.
Laterit yang ada di Indonesia memiliki kandungan Fe sekitar 50 %, Mg dan Si berkisar pada besaran 20 - 25 %, agar dapat dimanfaatkan menjadi bahan baku iron nugget atau pig iron maka perlu dilakukan peningkatan konsentrasi Fe dan penurunan kadar Si. Selanjutnya dilakukan reduksi menggunakan coal/ batu bara dengan kadar C yang cukup tinggi. Oleh karena itu perlu dilakukan proses konsentrasi / benefisiasi kemudian dilakukan proses reduksi dengan kondisi yang paling optimum. Dari data uraian diatas sangat menarik untuk dikembangkan pembuatan pig iron menggunakan bahan baku lokal karena bahan baku dengan kandungan Fe yang relatif cukup tinggi tersedia masih cukup banyak dan juga bahan baku industri besi baja nasional sampai saat ini masih import. Proses reduksi untuk mendapatkan Fe dari senyawanya ditentukan oleh beberapa faktor, antara lain temperatur, waktu reduksi, kadar karbon, dan ukuran partikel .
Nickel pig iron adalah logam besi wantah yang merupakan hasil dari
proses peleburan bijih nikel kadar rendah di bawah 1.8% Ni. Pada saat ini NPI dihasilkan dari proses peleburan bijih nikel kadar rendah dengan menggunakan tungku tegak. NPI digunakan sebagai bahan baku pembuatan stainless stell.
1.2 Perumusan Masalah
Sejak tahun 1938, bijih laterit yang tidak memenuhi persyaratan yang biasa disebut bijih laterit off grade atau bijih laterit buangan dieskpor ke negara Australia. Ini menunjukan bahwa belum adanya pemanfaatan bijih laterit buangan ini. Kenyataan ini menunjukan bahwa potensi laterit di indonesia yang sangat besar belum dimanfaatkan secara maksimal. Selain itu, dengan adanya UU Minerba yang melarang mengeskpor bahan baku menjadi suatu keharusan untuk menolahnya di Indonesia[2].
Agar dapat dimanfaatkan bijih laterit buangan menjadi bahan baku pig
variabel optimum. Menurut literatur[3], selain kenaikan temperatur reduksi, ukuran partikel reduksi dapat mempengaruhi pula proses reduksi. Hal yang perlu diperhatikan adalah ukuran partikel sangat mempengaruhi kecepatan pemanasan partikel sehinga dapat berpengaruh kepada pasokan energi. Pasokan energi ini juga sangat mempengaruhi ongkos produksi.
Mengingat pentingnya aspek-aspek tersebut, maka pada penelitian ini akan dilakukan variasi ukuran partikel bijih saprolit. Variasi ukuran bijih saprolit ini dilakukan untuk melihat derajat reduksi besi yang terjadi sehingga selanjutnya dapat dicari titik optimum reduksi Fe. Sebagai reduktor, digunakan batubara yang memiliki nilai kalor tertentu dengan ukuran partikkel yang beragam. Kemudian proses kompaksi batubara dan mineral nikel dilakukan dengan metode Heckel untuk menghindari fenomena springback yang dapat menurunkan kualitas (densitas, porositas, dan kekuatan) sampel.
1.3 Tujuan Penelitian
Penelitian ini bertujuan untuk:
1. Mengetahui efek perbedaan ukuran partikel bijih saprolit terhadap derajat reduksi oksida besi.
2. Mengetahui ukuran partikel bijih saprolit yang tepat untuk mendapatkan nilai optimal reduksi Oksida besi.
1.4 Sistematika Penulisan
Dalam penulisan ini, sistematika penulisan disusun agar konsep dalam penulisan skripsi menjadi berurutan sehingga akan didapat kerangka alur pemikiran yang mudah dan praktis. Sistematika tersebut dapat diartikan dalam bentuk banyak bab-bab yang saling berkaitan dengan yang lain. Bab-bab tersebut diantaranya :
4
Bab 1 Pendahuluan
Membahas mengenai latar belakang penulisan, perumusan masalah, tujuan penelitian, ruang lingkung penelitian, dan sistematika penulisan. Bab 2 Teori Penunjang
Membahas mengenai teori korosi secara umum mengenai bijih laterit di indonesia, reduksi Fe, pengaruh ukuran partikel terhadap reduksi, dan pengujian karakterisasi.
Bab 3 Metodologi Penelitian
Membahas mengenai diagram alir penelitian, alat dan bahan yang diperlukan untuk penelitian, dan prosedur penelitian.
Bab 4 Hasil Penelitian dan Pembahasan
Membahas mengenai pengolahan data yang didapat dari penelitian serta menganalisa hasil penelitian baik berupa angka, gambar, dan grafik, serta membandingkan dengan teori dan literatur.
Bab 5 Kesimpulan
Membahas mengenai kesimpulan dari hasil penelitian yang telah dilakukan serta saran-saran yang bisa dimanfaatkan berdasarkan hasil penelitian.
1.5 Ruang Lingkup Penelitian
a. Sampel yang digunakan pada penelitian ini berasal dari daerah Pomala, Sulawesi Tenggara, Indonesia. Sampel merupakan mineral nikel jenis saprolite. Sedangkan, batubara didapatkan dari penjual lokal.
b. Metode crushing dan sieving yang dilakukan dengan metode mekanik sederhana.
c. Kompaksi mengunakan mesin kompaksi di labotarium TPB, Departemen Metalurgi dan Material UI.
d. Reduksi dilakukan dengan metode roasting dengan suhu 1100oC menggunakan oven Carbolite di Labotarium Teknologi Pengubahan Bentuk, Departemen Metalurgi dan Material UI.
e. Pemeriksaan atau pengujian Karakterisasi dengan menggunakan alat uji EDAX Leo 420i di Departemen Metalurgi dan Material UI dan alat uji XRD shimadzu-7000 di Labotarium Terpadu, UIN Syarif Hidayatullah.
BAB II
TEORI PENUNJANG 2.1 BIJIH LATERIT
Bijih laterit merupakan tipe bijih yang biasa digunakan dalam praktik industri untuk produksi nikel. Penanganan bijih laterite masih dibatasi oleh faktor ekonomi, yaitu biaya energi yang mencapai hingga 2-3 kali dibandingkan dengan bijih sulfida. Di sisi lain, laterite dapat dieksploitasi dengan mudah menggunakan
open pit methods di mana bijih sulfida biasanya membutuhkan ekspolitasi bawah
tanah yang lebih mahal. Tren industri masa depan diperkirakan akan lebih melibatkan pengolahan laterite dengan teknologi proses yang lebih ekonomis.
Indonesia mengandung sekitar 16% cadangan nikel dunia dan cadangan tersebut memiliki profil yang dapat ditunjukan pada Gambar 2.1, sebagai berikut:
- Red Laterite (Hematite)
- Yellow Laterite (Limonite), biasanya mengandung goethite (FeO(OH)) dan bervariasi dalam kandungan air
- Saprolit, kaya akan magnesium (10-20% Mg), dengan terdapat kandungan besi yang mensubstitusi magnesium dalam serpentine (Mg3Si2O5(OH)4),
Tabel berikut menunjukkan analisa kimia terhadap komposisi bijih laterit Indonesia selama kurun waktu beberapa tahun terakhir.
Tabel 2.1 Persentase rata-rata komposisi bijih laterit Indonesia selama tahun 2008, 2009, dan 2010[1]
Pengotor sampingan yang dibawa oleh bijih nikel, seperti tampak dalam tabel di atas, didominasi oleh oksida Fe, Mg, Si, Co, dan Cr. Bergantung pada jenis lapisan laterisasinya, kadar elemen pengotor ini bervariasi seperti ditunjukkan dalam Tabel 2.1 .
Bijih laterit diklasifikasikan dalam tiga kelas berdasarkan konten Fe dan MgO mereka[4]: i) Kelas A-garnieritik jenis laterit (Fe <12% dan MgO >25%). ii) Kelas B-Limonit jenis laterit (tinggi kandungan Fe, 15-32% atau >32% dan MgO <10%) dan iii) Kelas C-menengah jenis laterit, yang terletak antara bijih tipe garnieritik dan Limonit (Fe 12-15% dan MgO 25-35% atau 10-25%).
2.2 REDUKSI OKSIDA
Pembelajaran tentang proses pengolahan besi merupakan hal yang penting untuk dipelajari, mengingat logam tersebut digunakan pada berbagai macam aplikasi. Teknik yang paling umum digunakan secara komersial yaitu dengan menggunakan blast furnace dan juga converter. Pada blast furnace reaksi yang terjadi yaitu sebagai berikut [5] :
8 3Fe2O3+C→ 2 Fe3O4+CO • Fe3O4+CO → 3FeO+CO2 Fe3O4+ C → 3FeO+CO • FeO+CO → Fe+CO2 FeO+C → Fe+CO
Dari persamaan reaksi diatas terlihat bahwa bijih besi dapat direduksi secara langsung dengan menggunakan karbon padat, namun reduksi dengan menggunakan gas CO mengindikasikan reaksi utama yang terjadi pada beberapa reduksi bijih besi.
Pemrosesan reduksi bijih besi dengan menggunakan blast furnace memiliki kelemahan utama, yaitu karena temperatur proses yang terlalu tinggi maka logam lain ( Si, Mn, dll.) akan banyak yang ikut melebur bersama dengan Fe sehingga akan sulit untuk dipisahkan. Oleh karena itu dikembangkan suatu metode baru untuk mengatasi hal tersebut dengan menggunakan proses reduksi langsung.
Proses reduksi langsung adalah proses pengurangan oksigen dari besi oksida dimana besi oksida tersebut tidak mengalami perubahan fasa, yaitu fasa padat. Proses reduksi langsung menggunakan zat pereduksi yang afinitas terhadap oksigen lebih besar daripada besi oksida. Proses ini dilakukan dengan menggunakan temperatur tinggi, namun lebih rendah dari temperatur yang digunakan pada pemrosesan dengan menggunakan blast furnace.
Banyak studi yang dilakukan untuk mempelajari proses reduksi langsung, Usui et al. mempelajari tentang proses prereduksi pada besi oksida dengan menggunakan batu bara dan juga gas dengan reaksi utama yang terjadi antara besi oksida dan hidrogen [6]. Ishikawa et al. secara sukses mempelajari tentang reduksi pada wustit (Fe1)xO dengan menggunakan karbon padat [7] .
2.2.1 Prinsip Dasar Proses Reduksi
Proses reduksi langsung merupakan reduksi bijih besi dengan menghindari fasa cair. Proses ini dilakukan dengan menggunakan pereduktor seperti karbon (coal), minyak bumi dan juga gas metana (CH4). Prinsip dasar proses ini adalah
mengurangi kadar oksigen dengan menggunakan unsur yang afinitas terhadap O (oksigen) lebih besar daripada Fe (besi). Proses ini dilakukan tanpa mengubah fasa, yaitu fasa padat. Hasil akhir proses ini menghasilkan bijih besi yang didalamnya masih terdapat oksida. Proses reduksi langsung digunakan dengan beberapa alasan sebagai berikut :
a. Menggunakan batu bara/ gas bumi sebagai pengganti kokas b. Produk berkualitas tinggi
c. Kapasitas produksi bisa rendah, sesuai dengan permintaan pasar d. Emisi CO2 rendah sehingga lebih ramah terhadap lingkungan
2.2.1.1 Termokimia
Reaksi kimia selalu melibatkan pelepasan maupun penyerapan energi. Hal tersebut menunjukkan bahwa setiap material memiliki energi. Energi dilepaskan apabila dalam suatu reaksi produk memiliki energi yang lebih rendah daripada pereaktan, sedangkan suatu reaksi dikatakan menyerap energi apabila produk memiliki energi yang lebih tinggi daripada pereaktan [8].
Panas merupakan bentuk energi yang umum pada suatu reaksi. Derajat panas juga dapat diukur dengan suhu. Panas yang dimiliki oleh suatu material merupakan entalpi dari material tersebut yang diberi lambang H.
Ketika suatu unsur bereaksi dengan unsur lain membentuk suatu senyawa, energi panas yang digunakan pada reaksi tersebut disebut sebagai energi panas pembentukan (entalpi pembentukan) yang diberi lambang ΔHf.
Ketika suatu senyawa bereaksi dengan senyawa lain membentuk suatu senyawa baru maka ΔHf berubah menjadi ΔH penguraian, oleh karena itu besar ΔHf harus dibalik. Contohnya sebagai berikut :
Fe3O4 + CO → 3FeO + CO2 ΔH = + 30664
Apabila ΔH reaksi bernilai positif maka reaksi merupakan reaksi endotermik (menyerap panas). Apabila ΔH bernilai negatif maka reaksi
10
2.2.1.2 Energi Bebas
Energi bebas merupakan selisih antara total energi pada sistem dengan energi ikatan, TS. Energi bebas reaksi kimia pada temperatur konstan dirumuskan pada Persamaan 2.1 [10] sebagai berikut:
(2.1)
Keterangan :
ΔF = Energi bebas cal/mol ΔH = Entalpi cal/mol T = Temperatur K ΔS = Perubahan entropi
Apabila ΔF bernilai negatif maka reaksi tersebut dapat berjalan secara spontan, namun apabila suatu reaksi ΔF bernilai positif maka reaksi tersebut tidak dapat berjalan secara spontan. Contoh energi bebas beberapa reaksi sebagai berikut [10] :
2Fe + O2→ 2FeO ΔFTo = -124.100 + 29.90T cal/molO2 (298 – 1642oK)
6FeO + O2→2Fe3O4 ΔFTo = -149.240 + 59.80T cal/molO2 (298 – 1642oK)
4Fe3O4 + O2→6Fe2O3 ΔFTo = -119.240 + 67.24T cal/molO2 (298 – 1460oK)
2C + O2→ 2CO ΔFTo = -53.400 - 42.0 T cal/molO2 (298 – 2500oK)
C + O2→ CO2 ΔFTo = -94.200 - 0.2 T cal/molO2 (298 – 2000oK)
2CO + O2→2 CO2 ΔFTo = -135.000 + 41.6 T cal/molO2 (298 – 2000oK)
C + CO2 →2CO ΔFTo = +40.800 + 41.8 T cal/molO2 (298 – 2000oK)
2H2 + O2→2H2O ΔFTo = -117.800 + 26.2 T cal/molO2 (298 – 2500oK)
Energi bebas suatu reaksi juga dapat ditentukan dengan menggunakan prinsip kesetimbangan kimia. Pada reaksi kimia :
A + B → C + D
Kecepatan reaksi pereaktan sama dengan kecepatan pereaksi produk (Vpereaktan = Vproduk). Energi bebas dapat ditentukan dengan Persamaan 2.2.
(2.2) Keterangan :
ΔFo
= Energi bebas cal/mol R = konstanta gas
T = Temperatur K a = aktivitas
Aktivitas pada gas sama dengan tekanan parsial yang dimiliki oleh gas tersebut. Untuk material padat dan cair, sama dengan konsentrasi yang dimiliki. Energi bebas yang dimiliki oleh suatu reaksi dapat diplot kedalam suatu grafik bersama dengan temperatur. Grafik yang memuat energi bebas versus temperatur disebut sebagai Diagram Ellingham seperti ditunjukkan pada Gambar 2.2. Pada diagram Ellingham, logam yang aktif secara kimia memiliki energi bebas yang paling tinggi (negatif) dalam membentuk oksida terletak pada diagram dibagian paling bawah. Sedangkan untuk logam yang memiliki energi bebas terkecil (positif) dalam membentuk oksida terletak pada diagram dibagian paling atas. Nilai dari ΔFo untuk reaksi oksidasi merupakan ukuran afinitas kimia suatu logam terhadap oksigen. Semakin negatif nilai ΔFo suatu logam menunjukkan logam tersebut semakin stabil dalam bentuk oksida.
Dari diagram Ellingham pada Gambar 2.2, kita dapat mengetahui temperatur minimal yang dibutuhkan agar reaksi tersebut dapat terjadi. Hal tersebut dapat ditunjukkan oleh perpotongan antara kurva oksidasi dan reduksi. Termodinamika hanya dapat digunakan untuk menentukan apakah suatu reaksi dapat berjalan spontan ataukah tidak pada temperatur tertentu berdasarkan energi bebas yang dimiliki. Namun tidak dapat digunakan untuk menentukan laju
reaksi. Perpotongan antara garis reaksi oksidasi dan reduksi secara termodinamika menunjukkan bahwa reaksi tersebut dapat berjalan pada temperatur tertentu. Selain menggunakan diagram Ellingham, kita juga dapat menentukan termodinamika suatu reaksi melalui perhitungan energi bebas ΔF dari reaksi
12
Hasil perhitungan energi bebas diatas menunjukkan bahwa ketiga reaksi tersebut dapat berjalan spontan. Secara termodinamika menunjukkan ketiga reaksi tersebut feasible untuk dilakukan.
2.2.1.3 Reaksi Boudouard
Proses reduksi langsung menggunakan kesetimbangan antara besi, hematite, magnetit, wustit, karbonmonoksida, karbondioksida, serta karbon padat pada tekanan 1 atm seperti ditunjukkan dalam diagram Bauer Glassner dan Boudouard pada Gambar 2.3. Kesetimbangan tersebut merupakan dasar dilakukannya proses reduksi langsung dengan menggunakan karbon padat.
14
Gambar 2.3. Diagram Bauer Glassner dan Boudouard [8]
Dalam diagram tersebut terdapat kesetimbangan besi oksida dengan campuran gas CO/ CO2, antara lain :
• Garis kesetimbangan Boudouard : CO2 + C = 2CO
• Garis kesetimbangan : 3Fe2O3 + CO = 2Fe3O4+ CO2
• Garis kesetimbangan : Fe3O4 + CO = 3FeO + CO2
• Garis kesetimbangan : FeO + CO = Fe + CO2
Dari garis kesetimbangan Boudouard, pada temperatur 10000C terdapat 100 % gas CO. Apabila temperatur diturunkan maka kesetimbangan tersebut tidak tercapai sehingga terjadi penguraian dari gas CO menjadi CO2 dan C. Sehingga
jumlah gas CO (pereduktor) akan berkurang.
Pada daerah disebelah kiri garis kesetimbangan boudouard maka gas CO2 akan lebih stabil sehingga gas CO yang ada akan terurai menjadi CO2. Pada daerah disebelah kanan garis kesetimbangan boudouard gas CO lebih stabil sehingga gas CO2 akan mengalami reaksi boudouard membentuk gas CO.Hal tersebut merupakan contoh dari prinsip Le Chatelier, reaksi boudouard merupakan
reaksi yang endotermik sehingga membutuhkan temperatur tinggi untuk dapat berjalan.
Dari Diagram Bauer Glassner dan Boudouard pada Gambar 2.3 , senyawa yang terbentuk sangat dipengaruhi oleh perbandingan antara CO/CO2 dan juga
temperatur operasi. Misal pada temperatur 7000C dengan perbandingan CO/CO2
adalah 60:40, maka senyawa yang paling stabil adalah wustit. Magnetit akan tereduksi menjadi wustit, sedangkan Fe akan mengalami oksidasi menjadi wustit.
Hal penting yang dapat disimpulkan dari kesetimbangan Boudouard antara garis kesetimbangan wustit/Fe dan garis kesetimbangan boudouard berpotongan pada temperatur 7000C. Hal tersebut menunjukkan bahwa temperatur minimum yang dibutuhkan untuk mereduksi wustit menjadi Fe adalah 7000C. Antara garis kesetimbangan Magnetit/wustit dan garis kesetimbangan boudouard berpotongan pada temperatur 6500C. Hal tersebut menunjukkan bahwa temperatur minimum yang dibutuhkan untuk mereduksi magnetit menjadi wustit adalah 6500C.
Temperatur minimum diatas pada tekanam 1 atm. Sangat tidak mungkin reaksi dapat berjalan dibawah temperatur minimum karena karbonmonoksida terurai menjadi karbondioksida.
2.2.2 Mekanisme Reduksi Langsung
Mekanisme reduksi langsung besi oksida dengan karbon padat terdiri dari : 1. Pembentukan gas reduktor
2. Adsorbsi gas pada besi oksida 3. Proses difusi dalam besi oksida
2.2.2.1 Pembentukan Gas Reduktor
Bila karbon dengan adanya oksigen pada temperatur tertinggi akan terbentuk gas CO menurut reaksi :
C + O2 → CO2
CO2 + C → 2CO
Karbondioksida yang dibentuk dapat bereaksi kembali dengan karbon sehingga terbentuk karbonmonoksida sesuai dengan reaksi boudouard. Karbon
16
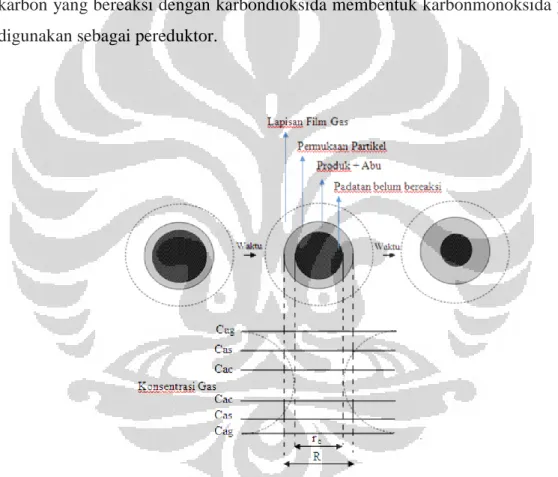
mereduksi besi oksida. Pada proses pembakaran karbon terjadi pembentukan lapisan film. Gas CO yang terbentuk konsentrasinya lebih rendah bila dibandingkan dengan konsentrasi gas CO pada fraksi padat. Selain gas CO sebagai reduktor yang terbentuk dari pembakaran tadi, dihasilkan juga abu yang mempengaruhi jumlah molekul gas reduktor tiap satuan volume. Gas-gas yang terjadi dipengaruhi oleh kecepatan molar transformasi karbon padat tiap satuan waktu dan satuan volume.
Proses pembentukan gas CO berjalan dengan seiring waktu, seperti ditunjukkan pada Gambar 2.4 . Semakin lama waktu reaksi maka semakin banyak karbon yang bereaksi dengan karbondioksida membentuk karbonmonoksida yang digunakan sebagai pereduktor.
Gambar 2.4 Gasifikasi Karbon
Keterangan :
Cag = konsentrasi gas reaktan pada fasa gas
Cas = konsentrasi gas reaktan pada permukaan partikel padat
Cac = konsentrasi gas reaktan pada permukaan padatan yang belum tereaksi Crc = konsentrasi gas produk pada permukaan padatan yang belum tereaksi
Crg = konsentrasi gas produk pada fasa gas R = jari-jari partikel padat
rc = jari-jari padatan yang belum tereaksi
Reaksi gasifikasi karbon dengan CO2 merupakan reaksi endotermik, oleh
karena itu reaksi ini terjadi pada temperatur tinggi. Pada temperatur 10000C akan dihasilkan 100% CO pada tekanan 1 atm. Laju reaksi secara keseluruhan dikendalikan oleh laju gasifikasi karbon [5]. Laju gasifikasi karbon ditentukan oleh beberapa faktor yaitu reaktivitas karbon, temperatur dan juga ketersediaan panas yang digunakan untuk mempertahankan reaksi hingga mencapai temperatur operasi [8].
Reaktivitas yang dimiliki oleh material yang mengandung karbon (carbonaceous material) sangat bervariasi. Luas permukaan karbon yang memungkinkan terjadinya reaksi antara karbon dengan CO2 merupakan hal yang
penting, yang ditentukan oleh ukuran partikel material dan juga porositas yang dimiliki oleh material. Charcoal, arang dan juga kokas memiliki porositas dan reaktivitas yang lebih tinggi daripada material karbon alami seperti kayu, karbon, dan grafit. Charcoal lebih reaktif daripada kokas pada temperatur rendah.Kokas yang dibuat dengan tipe karbon yang berbeda-beda (lignit, bituminous, anthracite) juga akan memberikan reaktivitas yang berbeda-beda.
Pada banyak kasus, laju reaksi serta produktivitas dari proses reduksi langsung ditentukan oleh beberapa faktor yang saling terhubung yaitu :
Transfer panas (heat transfer)
Reaktivitas karbon (carbon reactivity)
Reducibility besi oksida (iron oxide reducibility)
Ukuran partikel karbon, jumlah karbon yang tersedia, serta tipe karbon yang digunakan sangat berpengaruh terhadap laju gasifikasi. Ukuran partikel yang kecil dan ketersediaan dalam jumlah banyak akan meningkatkan luas permukaan yang mungkin untuk terjadi reaksi gasifikasi karbon sehingga dapat meningkatkan laju reaksi[10].
18
2.2.2.2 Adsorpsi Gas pada Besi Oksida
Proses bereaksinya molekul-molekul gas reduktor dengan permukaan besi oksida yang disebabkan oleh adanya kekuatan fisika dan kimia disebut sebagai reaksi adsorpsi.
Fisika adsorpsi merupakan pengikatan yang terjadi oleh bergeraknya masing-masing molekul gas. Proses adsopsi gas reduktor ke permukaan besi oksida secara fisika dipengaruhi oleh jumlah molekul gas reduktor yang menumbuk permukaan besi oksida dalam periode waktu tertentu.
Kimia adsopsi merupakan reaksi antara gas reduktor dengan padatan, di mana gas melingkupi dan berinteraksi dengan permukaan padatan. Proses adsopsi gas reduktor besi oksida ke permukaan besi oksida bergantung pada kemampuan dan kecenderungan antara gas dengan besi oksida dalam bertukar ion elektron atau memberi orbitnya.
Gambar 2.5 Skema arah pergerakan gas CO dan reduksi [5]
Dalam wustit (Fe1-yO), di mana y adalah bagian dari tempat kosong ion besi terhadap kisi-kisi besi atau mole fraksi dari tempat kosong ion besi. Dengan adanya gas CO akan terjadi pengurangan oksigen yang bersamaan terbentuknya ion bervalensi 2 dalam posisi kisi normal. Produk akhir dari reaksi ini adalah Fe yang berada pada daerah luar sampel. Pada permukaan besi oksida akan terjadi bentuk ikatan baru, dari wustit berupa ikatan kovalen menjadi besi metalik. Sedangkan di sisi lain, terjadi desorpsi di mana ion oksigen dari kisi oksida akan keluar dalam bentuk gas CO2. Pengurangan oksigen dalam besi oksida dapat
ditunjukkan dengan adanya beda konsentrasi gas CO2 antara fasa gas dengan fasa
2.2.2.3 Proses Difusi Dalam Besi Oksida
Difusi didefinisikan sebagai pergerakan atom didalam suatu material dengan fasa padat, cair ataupun gas. Fokus pada pembahasan disini adalah pada material denga fasa padat, yaitu besi oksida pada temperatur tinggi.
Pada temperatur tinggi tempat atom kosong akan bergerak semakin cepat dengan meningkatnya temperatur. Diperlukan energi untuk menggerakkan sebuah tempat atom kosong dari suatu keadaan setimbang ke keadaan setimbang yang lain. Selain itu juga diperlukan juga energi untuk membentuk tempat atom kosong. Sehingga difusi tidak hanya tergantung pada pergerakan tempat kosong termasuk pada pergerakan atom tetapi juga pada fraksi kedudukan tempat yang atomnya kosong. Konsekuensi dengan bertambahnya tempat atom kosong yaitu meningkatkan kecepatan difusi atau meningkatnya difusifitas dengan meningkatnya temperatur.
Reduciability dari besi oksida sangat dipengaruhi oleh porositas yang
dimiliki oleh besi oksida tersebut. Semakin tinggi porositas maka akan mempermudah difusi gas pereduktor CO pada besi oksida sehingga akan
meningkatkan laju reduksi. Pellet hasil aglomerisasi memiliki porositas yang jauh lebih tinggi daripada pellet yang disinter, sehingga reduciability pellet hasil aglomerisasi jauh lebih tinggi daripada pellet hasil sinter.
Ukuran partikel pereaksi seperti karbon juga sangat berpengaruh. Semakin kecil partikel karbon maka semakin luas permukaan yang memungkinkan terjadi reaksi, sehingga laju pembentukan CO semakin tinggi. Mekanisme reaksi reduksi langsung pada pellet berpori sangat tergantung dari difusi CO untuk menyentuh permukaan besi oksida dan bereaksi. Semakin banyak pori-pori, semakin mudah CO berdifusi kedalam pellet sehingga laju reaksi reduksi akan berjalan semakin cepat. Semakin sedikit pori-pori, semakin sulit CO untuk bereduksi sehingga laju reaksi reduksi akan berjalan semakin lambat. Mekanisme reduksi langsung seperti ditunjukkan pada Gambar 2.5 .
20
Gambar 2.5 Mekanisme reduksi langsung pada pellet berporos [8]
Pada material yang bebas poros maka reaksi reduksi menggunakan mekanisme solid state difffusion of ferrous ion.
2.3 Efek Ukuran Partikel
Ukuran partikel merupakan salah satu faktor yang dapat mempengaruhi proses reduksi selain batubara, temperatur reduksi, jenis dan kadar reduktor, dan waktu reduksi. Menurut Standish et al, ukuran partikel juga sangat penting walaupun tidak selalu konsisten dalam faktor pemanasan material granular[9]..
Penelitian efek ukuran partikel pada material granular dengan pemanasan microwave yang dilakukan oleh Standish et al[9] dalam penelitian tersebut menunjukan adanya perbedaan pengaruh ukuran partikel antara partikel Fe3O4 dan
Al2O3. Dalam proses pemanasan microwave butir alumina dan mangnetit, terlihat
bahwa proses pemanasan Al2O3 halus lebih cepat dari pada yang kasar sedangkan
Fe3O4 sebaliknya.
Penelitian lain yang dilakukan Bhyung-Su Kim et al [10], menyatahan bahwa derajat oksidatif roasting meningkat pada peningkatan temperatur reaksi dan kecepatan roasting meningkat pada penurunan ukuran partikel. Partikel molybdenite berukuran 53μm hanya membutuhkan 40 menit pada 1058o
C oksida roasting untuk mengkonversi menjadi molybdenum triokside.
mineral sulfat. Dari penelitian tersebut, diketahui bahwa adanya pengaruh ukuran partikel pada suhu pengapian sulfida, dinilai dengan metode TG. Ukuran partikel yang lebih kecil maka temperatur pengapian semakin rendah. Semakin rendah suhu pengapian maka proses oksidasi roasting semakin cepat.
Dari penelitian standish, dapat disimpulkan bahwa semakin besar ukuran partikel maka kecepatan reduksi Fe semakin cepat. Kecepatan reduksi dapat mempengaruhi efektifitas reduksi sehingga akan ada peningkatan kadar Fe pada partikel yang besar.
2.4. Energy Dispersive X-Ray Alnalysis (EDAX)
Energy Dispersive X-Ray Analysis (EDAX) adalah sebuah teknik analisis
yang digunakan untuk karakterisasi kimia elemental dari sebuah sample padatan. EDAX merupakan salah satu varian dari X-Ray Fluorosense (XRF). Dinamakan spektroskopi karena investigasi sampel dilakukan berdasarkan interaksi radiasi elektromagnetik, membuat sinar x-ray teremitasi dan menumbuk partikel. Proses karakterisasi didasari oleh prinsip bahwa semua elemen memiliki struktur atom yang unik dan tersendiri.
Simulasi emisi dari karakterisasi x-ray dilakukan dengan ledakan berkekuatan tinggi (high energy beam) berisi muatan – muatan elektron dan proton Ledakan ini akan menyebabkan electron pada lingkar dalam tereksitasi, menuju lingkar yang lebih luar dan menciptakan lubang electron (electron hole) [13], Gambar 3.2. Perbedaan energi dari hasil emisi elektron tersebut kemudian diukur oleh energy dispersive spectrometer. Karena energi tiap elemen berbeda, maka pengujian dapat menghasilkan komposisi elemental dari sampel uji.
22
Hasil EDAX memiliki beberapa keterbatasan, salah satunya adalah detektor EDAX tidak mampu mendeteksi keberadaan elemen dengan nomor atom kurang dari 5, artinya EDAX tidak dapat mendeteksi H, HE, LI, ataupun Be. Selain itu, EDAX tidak mampu mendeteksi elemen dengan titik puncak yang terlampau besar energinya (overlapping peaks) misalnya Ti Kβ and V Kα, Mn Kβ and Fe Kα. Gambar 3.3 menunjukkan salah satu contoh hasil pengujian EDAX.
Gambar 2.7 Contoh Hasil Pengujian Energy Dispersive X-Ray Analysis (EDAX) [9]
2.5 X-Ray Diffraction (XRD)
XRD merupakan alat difraktometer yang menggunakan prinsip difraksi. XRD adalah suatu metode analisa nondestruktif yang didasarkan pada pengukuran radiasi sinar-X yang terdifraksi oleh bidang kristal ketika terjadi interaksi antara suatu materi dengan radiasi elektromagnetik sinar X. Suatu kristal memiliki kisi kristal tertentu dengan jarak antar bidang kristal (d) spesifik juga sehingga bidang kristal tersebut akan memantulkan radiasi sinar X dengan sudut-sudut tertentu.
Alat ini digunakan untuk mengidentifikasi fasa kristalin dalam material dengan cara menentukan parameter struktur kisi serta untuk mendapatkan ukuran partikel.
Dengan alat ini kita melihat senyawa yang terbentuk. Dengan kata lain, kita dapat melihat transformasi fasa yang terjadi pada suatu sampel akibat suatu
proses atau treatment yang dilakukan. Tetapi dengan pemakaian alat XRD ini, kita tidak bisa mendapatkan kadar atau persentase dari unsur yang terdapat pada sampel mineral.
Bijih Saprolit Crushing Sizing/Sievieng Pencampuran (Mixing) Batubara Drying Kompaksi Drying Reduksi Roasting Temp 1050oC, 60 Menit EDAX & XRD EDAX XRD Analisa data Kesimpulan BAB 3 METODOLOGI PENELITIAN
3.1 Diagram Alir Penelitian
Untuk memudahkan dalam membaca alir penelitian maka dibuat sebuah diagram alir seperti pada Gambar 3.1.
3.2 Alat dan Bahan
Sampel yang digunakan pada penelitian merupakan bijih laterit jenis saprolit yang berasal dari daerah Pomala, Sulawesi Tenggara, Indonesia. Sedangkan batubara didapatkan dari penjual lokal.
Peralatan yang digunakan antara lain : a. Mortar dan tumbukan
b. Wadah penyimpanan sampel c. Alat sieving otomatis
d. Piring ayakan ukuran mesh 70, 120, 170, 200, dan 270
e. Mesin kompaksi
f. Cetakan sampel kompaksi berbentuk silinder
g. Alat ukur (caliper, penggaris)
h. Timbangan
i. Dapur microwave
3.3 Prosedur Penelitian 3.3.1 Preparasi Sampel
Sebelum dilakukan reduksi roasting sampel terlebih dahulu dilakukan preparasi seperti crushing, svievieng/sizing, drying, dan kompaksi.
3.3.1.1 Crushing & Sievieng/Sizing
Proses crushing dilakukan manual menggunakan mortar. Lalu, sampel yang telah dihancurkan dan dihaluskan dengan meggunakan palu setelah itu dilanjutkan dengan proses sieving (pengayakan). Pada proses ini dilakukan untuk pengelompokan ukuran partikel (sizing) berdasarkan ukuran partikel yang digunakan yaitu mesh 120, 170, 200, dan 270.
3.3.1.2 Drying dan Kompaksi
26
memastikan hilangnya keseluruhan moisture dalam batubara maupun bijih saprolit.
Setelah bijih saprolit dicampurkan dengan batubara dengan perbandingan 1:1, kompaksi dilakukan menggunakan cetakan silinder dengan diameter 22mm dan ketinggian sampel +/- 16mm. Besarnya gaya tekan kompaksi yang diberikan adalah 150 bar.
3.3.2 Roasting
Reduksi dilakukan pada bijih saprolit dengan menggunakan reduktan karbon (batubara) yang telah dicampurkan dengan perbandingan 1:1. Proses reduksi dilakukan pada temperatur 11000C selama 60 menit. Reduksi melalui proses roasting menggunakan menggunakan oven Carbolite di Labotarium Metalografi, Departemen Teknik Metalurgi dan Material Universitas Indonesia.
3.3.3 Uji Karakterisasi
Setelah reduksi, dilakukan pengujian karakterisasi. Pengujian karakterisasi yang dilakukan adalah pengujian EDAX dan XRD.
3.3.3.1 Uji EDAX
Pengujian EDAX dilakukan untuk mengetahui kadar unsur untuk mendapatkan perbandingan kadar kandungan Fe pada saprolit awal dengan bijih saprolit hasil reduksi. Pengujian ini dilakukan menggunakan alat uji EDAX Leo 420i di Labotarium SEM, Departemen Teknik Metalurgi dan Material Universitas Indonesia.
3.3.3.2 Uji XRD
Pengujian XRD dilakukan untuk mengetahui struktur kristal dari sampel reduksi. Pengujian XRD dilakukan untuk melihat senyawa pada sampel awal dan hasil reduksi. Pengujian XRD ini dilakukan menggunakan alat uji XRD
Shimadzu 7000 di Labotarium Terpadu, Universitas Islam Negeri Syarif Hidayatullah.
BAB 4
HASIL DAN PEMBAHASAN 4.1 Data Berat Sampel
Tabel 4.1 Data massa sample sebelum dan sesudah reduksi roasting
Mesh Massa (gr) dW Awal Akhir #120 7.92 3.96 3.96 #170 7.86 3.93 3.93 #200 7.71 3.855 3.855 #270 7.88 3.94 3.94
Massa awal merupakan massa bijih laterit yang telah dicampur dengan batubara dengan perbandingan 1:1 antara bijih laterit dan batubara, lalu dikompaksi dengan tekanan 150 bar dengan bentuk silinder. Sedangkan berat akhir adalah berat sampel yang telah direduksi dengan proses reduksi pada temperatur 1100oC selama 60 menit.
Pada Tabel 4.1, terlihat bahwa massa akhir lebih kecil dari pada massa awal dan selisih berat sampel awal dan akhir di setiap ukuran partikel cenderung stabil. Ini membuktikan bahwa selama proses reduksi, batubara terdekomposisi secara sempurna.
4.2 Pengujian XRD
Pengujian hasil dengan menggunakan XRD akan memberikan hasil secara kualitatif akan setiap senyawa yang terkandung di dalam bijih laterit setelah mengalami proses reduksi. Pengujian secara XRD tidak dapat memberikan hasil secara kuantitatif. Oleh karena itu, hasil penelitian data dengan menggunakan XRD hanya akan dianalisa senyawa yang terbentuk dari proses reduksi dengan melihat grafik yang dihasilkan dengan melihat 2Ө pada grafik yang terbentuk.
Gambar 4.1 Gambar hasil pengujian XRD sampel awal bijih laterit
Gambar 4.1 adalah gambar hasil pengujian XRD bijih laterit awal sebelum proses reduksi. Pengujian XRD ini tidak dikelompokan bedasarkan ukuran partikel karena untuk setiap partikel dianggap mempunyai senyawa yang sama di setiap ukuran partikel. Dari gambar tersebut, dapat dilihat bahwa mineral laterit ini didominasi oleh αFeOOH (geothite) , Fe2O3 (hematite), Fe3O4 (magnetite),
NiO dan SiO2.
Gambar 4.2, Gambar 4.3, Gambar 4.4, dan Gambar 4.5 adalah hasil pengujian XRD pada bijih laterit untuk setiap ukuran partikel setelah proses reduksi. Berbeda dengan Gambar 4.1, untuk pengujian XRD pada sampel laterit yang telah direduksi pengujian dilakukan bedasarkan ukuran partikel yaitu mesh 120, 170, 200, dan 270.
Jika dibandingkan dengan hasil XRD sampel sebelum dengan sesudah reduksi, adanya kemungkinan kenaikan kadar Fe yang diiringan dengan kenaikan kadar Ni. Fe berikatan dengan Ni membentuk feronikel [Fe,Ni]. Selain itu, adanya proses reduksi dari Fe2O3 (hematite) menjadi Fe3O4 (magnetite) juga dapat
meningkatkan kadar Fe. Adapun senyawa yang dihasilkan pada grafik hasil reduksi adalah terbentuk senyawa Fe-Ni hal ini dibandingkan dengan data XRD dengan nomor 47-1417, yaitu Fe-Ni .
30
Gambar 4.2 Gambar hasil pengujian XRD pada ukuran partikel mesh120 setelah reduksi
Gambar 4.2 Gambar hasil pengujian XRD pada ukuran partikel #120 setelah reduksi
Selain itu, hasil pengujian XRD juga menunjukkan pada hasil reduksi terbentuk senyawa FeNi, Fe3O4, dan Fe2O3, yang memilki nilai peak yang besar
dari grafik hasil XRD, Hal ini dapat diamati pada perbandingan kurva hasil pengujian XRD sebelum mengalami proses reduksi dan setelah mengalami proses reduksi. Hal ini menunjukkan bahwa proses reaksi reduksi pada temperatur 1100
°C merupakan temperatur dimana suatu proses dapat membentuk senyawa FeNi, , Fe3O4, dan Fe2O3.
Bijih laterit tergolong bijih kompleks, yang mengandung NiO, Fe2O3,
Fe3O4, dsb, sehingga reaksi-reaksi lain berlangsung serempak dalam proses
reduksi sebagai berikut [14]:
32
Gambar 4.5 Gambar hasil pengujian XRD pada ukuran partikel #170 setelah reduksi Roasting
4.3 Pengujian EDAX
Pengujian hasil dengan menggunakan EDAX akan memberikan hasil secara kuantitatif akan setiap unsur yang terkandung di dalam bijih laterit setelah mengalami proses reduksi. Pengujian nilai kadar unsur yang dilakukan bertujuan untuk melihat perubahan kadar unsur sebelum dan sesudah proses reduksi. Hasil pengujian EDAX untuk bijih laterite sebelum direduksi pada setiap ukuran partikel dapat dilihat pada Tabel 4.2.
Tabel 4.2 Data Hasil Pengujian EDAX pada bijih laterit sebelum proses reduksi setiap ukuran partikel Ukuran Partikel (Mesh) Unsur Fe Mg Al Si C O 120 28.42 9.70 2.21 20.38 3.42 38.87 170 35.92 9.33 1.81 18.59 2.25 32.10 200 36.03 9.11 1.64 17.13 2.10 33.73 270 39.45 7.17 2.27 15.85 1.80 33.49
Dari tabel tersebut dapat dilihat kadar unsur di setiap ukuran partikel yang terkandung dalam bijih laterit sebelum proses reduksi. Analisa dari hasil pengujian EDAX bijih laterit yang terdapat pada tabel 4.2 sebagai berikut:
1 kadar Fe merupakan kadar unsur logam yang tertinggi pada bijih laterit ini yaitu berkisar 28.4% sampai 39,4%, diikuti Mg berkisar 7% sampai 9,7% dan Al 1,5% sampai 2,5%. Sedangkan Kadar kandungan pengotor seperti Si berkisar 15,8% sampai 20,3%, C berkisar 1,80% sampai 3,42%, dan O berkisar 33,49% sampai 38,87%. Ini menunjukan kandungan laterit di dominasi oleh unsur Fe dan Si.
2 Semakin kecil ukuran partikel, kandungan unsur Fe pada bijih cenderung meningkat dari 28,4% pada partikel bijih dengan ukuran mesh 170 hingga 3,94% pada partikel bijih dengan ukuran mesh 270. Sedangkan pada unsur pengotor seperti unsur Al, Mg, Si, O dan C cenderung menurun. Hal ini menunjukan bahwa semakin kecil ukuran partikel menyebabkan kandungan pengotor menurun.
Gambar 4.6 Grafik Perubahan Kadar Fe sebelum dan setelah reduksi
Gambar 4.6 adalah grafik kadar Fe dari hasil pengujian EDAX pada bijih laterit sebelum dan sesudah direduksi dengan parameter ukuran partikel mesh 120, 170, 200, dan 270. Fe awal merupakan kandungan unsur Fe pada bijih laterit sebelum proses reduksi sedangan Fe akhir adalah kandungan unsur Fe pada bijih laterit setelah proses reduksi.
28.42 35.92 36.03 39.45 40.96 46.07 42.11 40.25 0.00 10.00 20.00 30.00 40.00 50.00 120 170 200 270 P er sen tase (% ) Ukuran Mesh
Grafik Perubahan Kadar Fe
Fe Awal Fe Akhir
34
Pada Gambar 4.6 terlihat bahwa terjadi peningkatan kadar Fe pada bijih laterit setelah roasting di setiap ukuran partikel. Hal ini menunjukan terjadinya proses reduksi Fe. [Fe,Ni]O(OH) pada laterit tereduksi atau terjadi pemutusan ikatan OOH dan terbentuklah feronikel FeNi. Selain itu, terbentuknya magnetite (Fe3O4) sebagai produk reduksi hematite (Fe2O3) karena pengikatan unsur O pada
hematite oleh gas CO Hal ini dibuktikan pada Gambar 4.8 yang menunjukan adanya penuruna kandungan unsur O pada bijih laterit ssebelum dan sesudah dilakukan reduksi.
Gambar 4.8 Grafik Perubahan Kadar O sebelum dan setelah reduksi.
Gambar 4.7 adalah grafik perubahan kadar O pada bijih laterit sebelum dan sesudah reduksi dengan parameter ukuran partikel. Pada gambar tersebut, O awal adalah kandungan unsur O pada bijih laterit sebelum dilakukan proses reduksi sedangan O akhir adalah kandungan unsur O setelah direduksi.
Pada Gambar 4.7 terlihat kandungan unsur O pada bijih laterit setelah dilakukan proses reduksi cenderung menurun jika dibandingkan dengan kandungan O pada bijih laterit sebelum dilakukan reduksi. Hal ini dikarenakan terjadinya reaksi reduksi atau pengikatan unsur O yang terdapat pada senyawa Fe2O3 (hematite) , NiO dan FeOOH (geothite) oleh gas monoksida (CO) selama
proses reduksi berlangsung sehingga karbon monoksida tergenerasi menjadi 38.87 32.10 33.73 33.49 27.59 25.37 27.99 28.07 0.00 10.00 20.00 30.00 40.00 50.00 120 170 200 270 P er sen tase (% ) Ukuran Mesh
Grafik Perubahan Kadar O
O Awal O Akhir
Ukuran partikel pada mesh 170 memiliki kadar yang paling tinggi setelah reduksi yaitu sebesar 46,07% dibandingkan ukuran partikel lain dengan mesh 120, 170, 200 dan 270 yang memiliki kadar sebesar 40,96%, 40,11 %, dan 40,25%. Walaupun demikian, peningkatan kadar Fe yang paling tertinggi terdapat ukuran partikel mesh 120. Peningkatan tersebut dapat dilihat pada Gambar 4.8 yang menunjukan grafik peningkatan kadar Fe pada bijih laterit sebelum dan sesudah reduksi.
Gambar 4.8 adalah grafik perubahan kadar Fe pada ukuran partikel mesh 120, 170, 200, dan 270. Perubahan kadar di dapat dari selisih antara kadar unsur Fe pada bijih sebelum reduksi dengan kadar unsur Fe setelah reduksi pada ukaran partikel mesh 120, 170, 200, dan 270.
Gambar 4.7 Grafik pengaruh ukuran partikel terhadap peningkatan kadar Fe
Pada Gambar 4.8 terlihat bahwa terjadi penurunan kadar peningkatan Fe seiring peningkatan ukuran partikel. Kandungan Fe pada bijih pada ukuran partikel yang besar dengan ukuran mesh #120 meningkat sebesar 11,58% sedangkan ukuran partikel yang lebih kecil dengan ukuran mesh #270 hanya meningkat sebesar 0.80%.
Peningkatan kandungan Fe ini sesuai dengan penelitian standish et al[9] 0.00 2.00 4.00 6.00 8.00 10.00 12.00 14.00 120 170 200 270 Pen in gkat an K ad ar ( % )
Ukuran Partikel (Mesh)
Grafik Pengaruh Ukuran Partikel
terhadap Peningkatan Kadar Fe
36
panas dari pada ukuran partikel yang lebih kecil karena luas permukaan ukuran partikel yang kecil lebih luas dibandingkan dengan ukuran partikel yang besar. Permukaan partikel yang luas memudahkan hilangnya lapisan atmosfer CO selama pemanasan. Bertambahnya kandungan gas karbon monoksida, maka kecenderungan terbentuknya Fe akan semakin tinggi. Namun harus diperhatikan juga, periode pemanasan yang berlebihan akan berdampak sebaliknya. Fe yang telah terbentuk akan tereduksi kembali menjadi Fe3O4 dan Fe2O3.
Selain itu, Porositas pada sampel merupakan salah satu faktor yang sangat berpengaruh terhadap laju reduksi. Semakin besar partikel membuat porositas semakin banyak pada sampel. Hal ini dapat meningkatkan laju difusi CO pada sampel. Peningkatan laju difusi memungkinkan peningkatan jumlah reaksi reduksi yang terjadi antara CO dan besi oksida. Oleh karena itu, kandungan unsur Fe yang dihasilkan setelah reduksi pada sampel meningkat.
BAB 5 KESIMPULAN
5.1. Kesimpulan
Berdasarkan hasil pengujian penangaruh ukuran partikel terhadap reduksi Fe pada bijih laterit low grade, maka didapatkan kesimpulan sebagai berikut :
1. Ukuran partikel sangat mempengaruhi peningkatan kadar peningkatan Fe pada bijih saprolit. Ukuran partikel yang besar mempunyai nilai kenaikan kadar Fe yang semakin besar. Peningkatan Kadar Fe yang paling besar terdapat pada ukuran partikel mesh 120 yaitu sebesar 12,54%. Sedangkan peningkatan yang terendah terdapat pada ukuran partikel mesh 270 yaitu sebesar 0.8%.
2. Akan tetapi, kadar Fe sampel hasil reduksi yang paling terbesar terdapat pada ukuran partikel mesh 170 sebesar 46,7%. Hal ini disebabkan kandungan unsur Fe pada ukuran partikel bijih laterit ini mempunyai kandungan awal atau bijih laterit sebelum reduksi yang tinggi.
3. Kadar optimal Fe setelah reduksi melalui roasting adalah sebesar 46,7% dengan ukuran partikel mesh 170. Sedangkan kenaikan kadar Fe optimal adalah sebesar 12,54% dengan ukuran partikel mesh 270.
DAFTAR PUSTAKA
[1] Elias, Mick. 2002. Nickel laterite deposit –geological overview,
resources and exploitation. Tasmania\
[2] Prasetyo, Paguh. 2008. “Pemanfaatan Bijih Nikel Indonesia Pada Saat Ini dan Saat Mendatang”. Metalurgi, Volume 23, No 3. Pusat Penelitian Metalurgi LIPI; hal 1-3.
[3] Kazie E Haque. 1999. “Microwave energy for mineral treatment processes
—a brief review”. Int J Miner Process, 57 ; 1–24.
[4] Zevgolis EN. 2000. Extractive metallurgy of nickel: part I.
Pyrometallurgical methods. Athens: National Technical University
of Athens, editors.
[5] Toru Yamashita, Tomoya Nakada, Kazuhiro Nagata. 2007. “ In-Situ Observation of Fe0.94O Reduction at High Temperature with the Use of Optical Microscopy”. Metallurgical and Materials
Transactions B. vol 38B: hal. 185-191.
[6] T. Usui, N. Inoue, T. Watanabe, T. Yokoyama, T. Oyama, and M. Morita. 2006. ”Prereduction of Iron Oxide with Coal Carbonization Gas“,
Ironmaking Steelmaking, vol. 31: pp. 479–84.
[7] N. Ishikawa, K. Furuya, N. Mitsuoka, and T. Inami. 2006. “Reduction Wustite by Solid Carbon”, ISIJ Int., vol. 46 : pp. 1106–7.
[8] Robert .L.Stepershon, et al. 1980. “Direct Reduction Iron/Technology and
Economic of Production ad Use”. U.S.A : The Iron Steel Society
of AIME
[9] N Standish, H. K. Worner, and D. Y. ObucHowski. 1990. ”Particle Size
Effect in Microwave Heating of Granular Material”. Powder Metallurgy, 66: 225-230.
[10] J.G. Dunn. 1996. ” The oxidation of sulphide minerals”. Thermochimica
Acta 300 :127-139
Kinetics of the Oxidative Roasting of Low Grade Mongolian Molybdenite Concentrate”. Materials Transactions, Vol. 50 No.
10: 2669 -2674
[12] Fandrich, R., Ying Gu, Debra Burrows, Kurt Moeller. 2006. Modern
SEMbased mineral liberation analysis. Elsevier
[13] Azároff, L. V.; R. Kaplow, N. Kato, R. J. Weiss, A. J. C. Wilson, R. A. Young. 1974. X-ray diffraction. McGraw-Hill.
[14] Li, B., Wang, H. And Wei, Y . 2011. “The reduction of nickel from low- grade nickel laterite ore using a solid-state deoxidisation method.” International Journal of Minerals Engineering 24: 1556-1562.
Lampiran 1 Lampiran 2
Lampiran 1 Lampiran 2
Lampiran 1 Lampiran 2
Lampiran 1 Lampiran 2
Lampiran 1 Lampiran 2
Lampiran 1 Lampiran 2
Lampiran 1 Lampiran 2



![Gambar 2.3. Diagram Bauer Glassner dan Boudouard [8]](https://thumb-ap.123doks.com/thumbv2/123dok/4085953.3045013/28.892.184.760.127.814/gambar-diagram-bauer-glassner-dan-boudouard.webp)
![Gambar 2.5 Skema arah pergerakan gas CO dan reduksi [5]](https://thumb-ap.123doks.com/thumbv2/123dok/4085953.3045013/32.892.172.747.407.813/gambar-skema-arah-pergerakan-gas-co-reduksi.webp)
![Gambar 2.5 Mekanisme reduksi langsung pada pellet berporos [8]](https://thumb-ap.123doks.com/thumbv2/123dok/4085953.3045013/34.892.193.727.137.738/gambar-mekanisme-reduksi-langsung-pada-pellet-berporos.webp)
![Gambar 2.7 Contoh Hasil Pengujian Energy Dispersive X-Ray Analysis (EDAX) [9]](https://thumb-ap.123doks.com/thumbv2/123dok/4085953.3045013/36.892.178.733.359.768/gambar-contoh-hasil-pengujian-energy-dispersive-analysis-edax.webp)
![Gambar 2.8 Contoh grafik hasil pengujian XRD [10]](https://thumb-ap.123doks.com/thumbv2/123dok/4085953.3045013/37.892.182.707.224.914/gambar-contoh-grafik-hasil-pengujian-xrd.webp)