Pembimbing : Dr. Ir. Kuswandi,DEA
Disusun oleh :
Adi Kurnia
2306 100 016
Aditya Widyadhana
2306 100 021
Laboratorium Thermodinamika Teknik Kimia
Jurusan Teknik Kimia
Fakultas Teknik Industri
Institut Teknologi Sepuluh Nopember
K e s e t i m b a n g a n c a i r - c a i r
s i s t e m E u g e n o l -
β
- c a r y o p h y l l e n e - e t a n o l - a i r
Latar Belakang
Dalam industri rokok, kosmetik, dll.
Minyak atsiri harus memilki syarat
tertentu yang nantinya dijadikan standart
baku mutu dari minyak atsiri itu sendiri
antara lain: minyak atsiri harus mampu
larut dalam alkohol 60-70% dalam hal ini
adalah etanol. Untuk itu diperlukan
pemurnian minyak atsiri dari
terpen-terpennya agar minyak atsiri dari daun
cengkeh mampu larut dalam alkohol
60-70%.
Page 3
Eugenol
Β-Caryophyllene
Ethanol
Tinjauan Penelitian
Yang dkk (2007) melakukan eksperimen untuk memprediksikan
komposisi kesetimbangan sistem kuarterner metil isobutil
keton-air-phenol-hidroquinone. Parameter kesetimbangan yang digunakan adalah
model persamaan UNIQUAC dan NRTL.
Chen dkk (2000) melakukan eksperimen untuk memprediksikan
komposisi kesetimbangan sistem kuaterner n-hexane, n-octane, benzene,
sulfolane pada suhu 298,15K. Parameter kesetimbangan yang digunakan
adalah model persamaan NRTL
Gomis dkk (1995) melakukan eksperimen untuk memprediksikan
komposisi kesetimbangan sistem kuaterner air, asam asetat, 2-butanon dan
cyclohexane pada suhu 25
0
C . Parameter kesetimbangan yang digunakan
Page 5
Li dan Tamura (2005) melakukan eksperimen untuk memprediksikan komposisi
kesetimbangan sistem kuaterner air, etanol, α-pinene,β-pinene pada suhu 298.15
K. Parameter kesetimbangan yang digunakan adalah model persamaan modifikasi
UNIQUAC.
Kuswandi, dkk melakukan eksperimen untuk memprediksikan komposisi
kesetimbangan system β
-Caryophyllene
+Etanol+Air pada Rentang Temperatur
303-323 K . Parameter kesetimbangan yang digunakan adalah model persamaan
UNIQUAC dan NRTL.
Naryono.E dan Kuswandi melakukan eksperimen untuk mempredisiksikan
komposisi kesetimbangan system Eugenol+Etanol+Air pada Rentang Temperatur
303-333 K
Page 7
Tujuan
Memperoleh data kesetimbangan cair-cair (LLE) dari
eksperimen untuk sistem kuaterner, yaitu Eugenol +
β
-Caryophyllene
+ etanol + air pada rentang
temperatur 303K-323K
Mengkorelasikan data yang didapatkan dengan
menggunakan persamaan NRTL dan UNIQUAC
Manfaat
Hasil dari penelitian ini dapat dipakai untuk mengembangkan
proses ekstraksi terpen dari minyak cengkeh yang ke
depannya dapat dijadikan acuan dalam pengembangan
teknologi pengolahan minyak cengkeh dan referensi
perancangan alat serta operasi ekstraksi minyak cengkeh.
Page 9
Pada kondisi kesetimbangan harga
ΔG sistem mencapai minimum. Dalam
perhitungan, fungsi
ΔG lebih mudah dinyatakan dalam bentuk tak berdimensi,
(ΔG/RT) karena bisa dihubungkan langsung dengan besaran tak berdimensi
energy gibbs ekses, (GE/RT) menurut hubungan:
(2.6)
Ekspresi yang menghubungkan
(ΔG/RT) dengan komposisi kesetimbangan
khususnya LLE dapat dirumuskan dalam berbagai model persamaan antara
lain UNIQUAC dan NRTL.
Persamaan Korelasi koefisien aktivitas
Model persamaan UNIQUAC (Universal Quasi Chemical), Model
persamaan UNIQUAC dikemukakan oleh abrams dan prauznitz
pada tahun 1975. Persamaan ini diaplikasikan pada larutan yang
memilki molekul-molekul yang berbeda baik ukuran maupun
bentuknya.
R
c
g
g
g
R i c i i
ln
ln
ln
j j j i i i i i i i i c ix
l
x
l
q
z
x
ln
2
ln
ln
j j ij j i i Rs
s
q
1
ln
ln
Page 11
τ
ij
= exp
−
𝑅×𝑇
𝑢
𝑖𝑗
τ
ji
= exp
−
𝑅×𝑇
𝑢
𝑗𝑖
𝑙
𝑖
=
𝑧
2
𝑟
𝑖
− 𝑞
𝑖
− 𝑟
𝑖
− 1
𝜃
𝑖
=
𝑞
𝑖
𝑥
𝑖
𝑞
𝑗
𝑗
𝑥
𝑗
∅
𝑖
=
𝑟
𝑖
𝑥
𝑖
𝑟
𝑗
𝑗
𝑥
𝑗
ln 𝛾
𝑖
= 𝑙𝑛
∅
𝑖𝑥
𝑖+
𝑧
2
𝑞
𝑖
𝑙𝑛
𝜃
𝑖∅
𝑖+ 𝑙
𝑖
−
∅
𝑖𝑥
𝑖𝑥
𝑗
𝑗
𝑙
𝑗
+ 𝑞
𝑖
1 − 𝑙𝑛
𝜃
𝑗
𝜏
𝑗𝑖
𝑚
𝑗=1
−
𝜃
𝑗𝜏
𝑗𝑖𝜃
𝑘𝜏
𝑘𝑗 𝑚 𝑘=1𝑚
𝑗=1
Model Persamaan NRTL (Non-Random-Two-Liquid), Persamaan
NRTL di kemukakan oleh H.Renon dan J.M Prausnitz (1968).
Persamaan tersebut dinyatakan dengan :
12
1
2
12
12
21
2
1
21
21
2
1
G
x
x
G
G
x
x
G
x
x
RT
G
E
2 12 2 2 12 12 2 21 2 1 21 21 2 2 1ln
G
x
x
G
G
x
x
G
x
2 21 2 1 21 21 2 12 1 2 12 21 2 1 2ln
G
x
x
G
G
x
x
G
x
Page 13
τij =
𝑅×𝑇
𝑔
𝑖𝑗
τji =
𝑅×𝑇
𝑔
𝑗𝑖
G
ij
= exp(-ατ
ij
)
G
ji
= exp(-ατ
ji
)
ln γ
i
=
𝜏
𝑗𝑖
𝐺
𝑗𝑖
𝑥
𝑗
𝑚
𝑗=1
𝐺
𝑙𝑖
𝑥
𝑙
𝑚
𝑙=1
+
𝑥
𝑗
𝐺
𝑗𝑖
𝐺
𝑙𝑗
𝑥
𝑙
𝑚
𝑙=1
𝜏
𝑖𝑗
−
𝑥
𝑛
𝜏
𝑛𝑗
𝐺
𝑛𝑗
𝑚
𝑛=1
𝐺
𝑙𝑗
𝑥
𝑙
𝑚
𝑙=1
𝑚
𝑗=1
Page 15
Peralatan
Keterangan Gambar:
1. Tabung sampel
2. Baffle
3. Magnetic stirrer
4. Pengeluaran
sampel
5. Jacket pemanas
Keterangan Gambar:
1.Termometer
6. Pompa
11. Corong Pemisah
2.Kondensor
7. Fuse Waterbath
12. Water Bath
3.Pipa Kran
8. Termokopel
4.Stirrer
9. Display
Page 17
Analisa
Sampel dianalisa memakai GC HP 5890 series II menggunakan kolom HP-5(cross
linket 5% phenyl methyl siloxane) sebagai carrier gas adalah helium dengan laju
alir 30 ml/menit. Temperatur oven dipertahankan 120
o
C selama 1 menit,
selanjutnya dinaikkan secara bertahap sampai mencapai 240
o
C dengan
kecepatan kenaikkan 10
o
C/menit. Temperatur ini dibiarkan stabil selama 5
menit, kemudian sampel sebesar 1 microliter diinjeksikan ke dalam kolom. Hasil
kuantitatif sampel dideteksi memakai detector FID.
Prosedur Percobaan
Pencampuran bahan kedalam equilibrium cell
Pengadukkan campuran pada temperatur konstan 303-323 K
selama 2 jam
Campuran dibiarkan hingga mencapai kesetimbangan selama 20
jam kemudian dipisahkan dengan corong pemisah
Page 19
Bahan yang digunakan
Bahan yang digunakan
Etanol Absolut 99,99%
-Caryophillene 98%
Aquabidest
Variabel percobaan
Temperatur 303 K, 313 K, 323K pada tekanan atmosferis
Persen berat ethanol 0%-50%
RUN Suhu(K) % Massa Etanol terhadap Air Massa (gram) TOTAL (gram) Etanol air eugenol caryophyllene
1 303,313,323 50 5 5 9 1 20 2 45 4.5 5.5 9 1 20 3 4 40 35 4 3.5 6 6.5 9 9 1 1 20 20 5 25 2.5 7.5 9 1 20 6 7 15 10 1.5 1 8.5 9 9 9 1 1 20 20 8 5 0.5 9.5 9 1 20 9 0 0 10 9 1 20
Page 21
RUN
Persen massa
etanol terhadap air
(%)
z
i(% mol)
z
1z
2z
3z
41
50
0.2334
0.5964
0.1177
0.0526
2
45
0.2027
0.6330
0.1136
0.0508
3
40
0.1740
0.6672
0.1097
0.0491
4
35
0.1473
0.6991
0.1061
0.0475
5
25
0.0988
0.7571
0.0996
0.0445
6
15
0.0558
0.8084
0.0938
0.0420
7
10
0.0362
0.8319
0.0912
0.0408
8
5
0.0176
0.8541
0.0887
0.0397
9
0
0.0000
0.8751
0.0863
0.0386
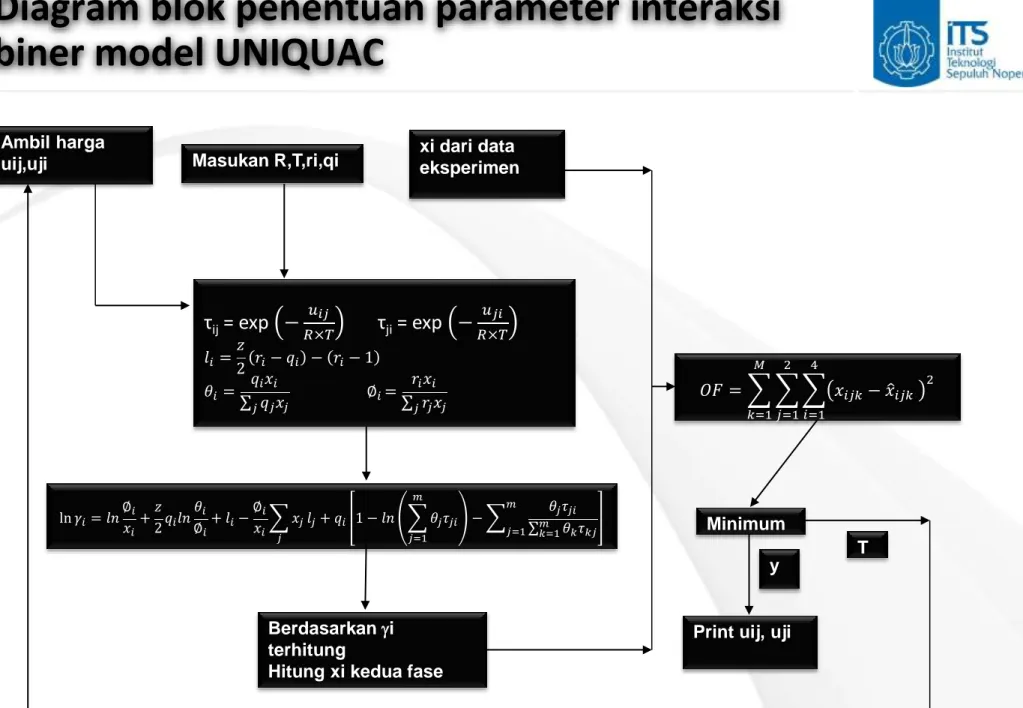
Diagram blok penentuan parameter interaksi
biner model UNIQUAC
Ambil harga
uij,uji
Masukan R,T,ri,qi
xi dari data
eksperimen
τ
ij= exp
−
𝑅×𝑇𝑢𝑖𝑗τ
ji= exp
−
𝑅×𝑇𝑢𝑗𝑖 𝑙𝑖 = 𝑧 2 𝑟𝑖− 𝑞𝑖 − 𝑟𝑖− 1 𝜃𝑖 = 𝑞𝑖𝑥𝑖 𝑞𝑗 𝑗𝑥𝑗 ∅𝑖= 𝑟𝑖𝑥𝑖 𝑟𝑗 𝑗𝑥𝑗 ln 𝛾𝑖= 𝑙𝑛∅𝑥𝑖 𝑖+ 𝑧 2𝑞𝑖𝑙𝑛 𝜃𝑖 ∅𝑖+ 𝑙𝑖− ∅𝑖 𝑥𝑖 𝑥𝑗 𝑗𝑙𝑗+ 𝑞𝑖 1 − 𝑙𝑛 𝜃𝑗𝜏𝑗𝑖 𝑚 𝑗=1 − 𝜃𝑗𝜏𝑗𝑖 𝜃𝑘𝜏𝑘𝑗 𝑚 𝑘=1 𝑚 𝑗=1Berdasarkan i
terhitung
Minimum
Print uij, uji
y
T
𝑂𝐹 = 𝑥
𝑖𝑗𝑘− 𝑥
𝑖𝑗𝑘 2 4 𝑖=1 2 𝑗=1 𝑀 𝑘=1Page 23
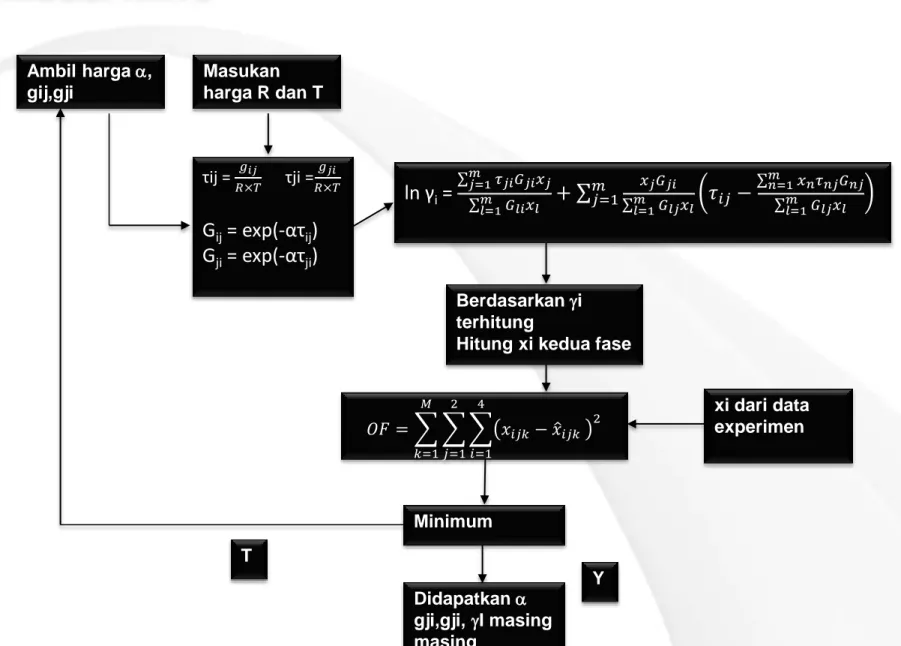
Diagram blok penentuan parameter interaksi
biner model NRTL
Ambil harga ,
gij,gji
Masukan
harga R dan T
τij =
𝑅×𝑇𝑔𝑖𝑗τji =
𝑅×𝑇𝑔𝑗𝑖G
ij= exp(-ατ
ij)
G
ji= exp(-ατ
ji)
xi dari data
experimen
ln γ
i=
𝜏𝑗𝑖𝐺𝑗𝑖𝑥𝑗 𝑚 𝑗=1 𝐺𝑙𝑖𝑥𝑙 𝑚 𝑙=1+
𝑥𝑗𝐺𝑗𝑖 𝐺𝑙𝑗𝑥𝑙 𝑚 𝑙=1𝜏
𝑖𝑗−
𝑥𝑛𝜏𝑛𝑗𝐺𝑛𝑗 𝑚 𝑛=1 𝐺𝑙𝑗𝑥𝑙 𝑚 𝑙=1 𝑚 𝑗=1Berdasarkan i
terhitung
Hitung xi kedua fase
𝑂𝐹 = 𝑥
𝑖𝑗𝑘− 𝑥
𝑖𝑗𝑘 2 4 𝑖=1 2 𝑗=1 𝑀 𝑘=1Didapatkan
gji,gji, I masing
masing
Minimum
Y
T
Hasil Percobaan
No sampel
%etanol terhadap air(%)
fase atas fase bawah
x1 x2 x3 x4 x1 x2 x3 x4 1 50 0.0092 0 0.1527 0.8381 0.2882 0.0190 0.4249 0.2679 2 40 0.0046 0 0.1439 0.8515 0.2665 0.0200 0.3167 0.3968 3 35 0.0024 0 0.1528 0.8448 0.2979 0.0243 0.2982 0.3797 4 25 0.0018 0 0.1341 0.8641 0.3314 0.0257 0.3028 0.3401 5 10 0.0012 0 0.0968 0.9020 0.2189 0.0187 0.2421 0.5203 6 0 0.0001 0 0 0.9999 0.3007 0.0274 0 0.6719 No sampel %etanol terhadap air(%)
fase atas fase bawah
x1 x2 x3 x4 x1 x2 x3 x4 1 50 0.0005 0 0.3676 0.6319 0.1422 0.0169 0.1874 0.6535 2 45 0.0011 0 0.4701 0.5288 0.1885 0.0206 0.2016 0.5893 3 35 0.0005 0 0.7310 0.2686 0.3306 0.0373 0.1793 0.4528 4 25 0.0011 0 0.1193 0.8796 0.2892 0.0308 0.0836 0.5964 5 10 0.0001 0 0.0435 0.9565 0.0019 0.0004 0.0652 0.9324
Suhu 303 K
Suhu 313 K
Page 25
No sampel
%etanol terhadap air(%)
fase atas fase bawah
x1 x2 x3 x4 x1 x2 x3 x4 1 50 0.0004 0 0.3556 0.6440 0.1589 0.0186 0.1300 0.6925 2 40 0.0004 0 0.4214 0.5781 0.1962 0.0200 0.0883 0.6954 3 35 0.0001 0 0.2720 0.7279 0.3926 0.0392 0.0415 0.5267 4 25 0.0001 0 0.0961 0.9038 0.3001 0.0315 0.0817 0.5867 5 10 0 0 0.0820 0.9180 0.4496 0.0470 0.0478 0.4557 6 0 0.0001 0 0 0.9999 0.5162 0.0531 0 0.4257
Suhu 323 K
Parameter interaksi NRTL dan UNIQUAC
suhu (K) komp NRTL parameter RMSD UNIQUAC parameter RMSD
gij gji uij uji 303 1-2 74.7762 84.6383 0.1164 58.9228 284.5346 0.0916 1-3 0.0629 152.9515 4270.1050 4068.9418 1-4 149.2712 67.4961 41.7040 730.9369 2-3 169.2697 42.5436 1360.0510 0.1349 2-4 107.4750 174.4906 1162.5530 3193.3668 3-4 126.5016 136.5694 0.0034 0.0672 313 1-2 0.3100 727.4791 0.0927 2.0423 1.2789 0.1062 1-3 0.6831 56.7355 0.0969 0.0833 1-4 0.0029 0.0022 0.0024 0.0012 2-3 122.6748 1.0023 0.0024 1002.0663 2-4 2.6126 96.5466 0.0022 3142.5434 3-4 0.9554 9.9495 1.1214 0.1661 323 1-2 0.9841 95153.2850 0.1276 1002.0060 0.0024 0.1154 1-3 0.4732 1.3713 3142.5430 1.0022 1-4 0.0034 0.0035 0.1661 3.1319 2-3 0.0099 11.9455 0.0024 1.2775
Page 27
Parameter Secara Simultan
Komp
NRTL parameter
RMSD
UNIQUAC parameter
RMSD
g
ijg
jiu
iju
ji1-2
116.6867
14.4053
0.1041
786.3166 116.9571
0.0875
1-3
52.4619
68.7972
88.8051
66.4551
1-4
112.3189
10.6422
119.6105 349.8787
2-3
7.337288
153.4714
87.1750
59.0801
2-4
98.3025
222.6869
21346.71 19226.68
3-4
70.9184
67.2916
223.4177
27.0947
Hasil prediksi kesetimbangan (NRTL)
suhu (K) fase atas fase bawah
x1 x2 x3 x4 x1 x2 x3 x4 303 0.5347 0.0405 0.0480 0.3768 0.5468 0.0182 0.0452 0.3898 0.1892 0.0712 0.0742 0.6654 0.1903 0.0298 0.0717 0.7083 0.1669 0.0714 0.0778 0.6840 0.1682 0.0278 0.0758 0.7282 0.1169 0.0716 0.0714 0.7402 0.1180 0.0267 0.0696 0.7857 0.0352 0.0856 0.0602 0.8189 0.0352 0.0350 0.0581 0.8717 0 0.0404 0.0691 0.8905 0 0.0065 0.0684 0.9251
suhu (K) fase atas fase bawah
x1 x2 x3 x4 x1 x2 x3 x4 313 0.4974 0.0039 0.1884 0.3103 0.4984 0.0016 0.1887 0.3113 0.1803 0.0135 0.1655 0.6406 0.1800 0.0051 0.1662 0.6487 0.2597 0.0229 0.1062 0.6112 0.2625 0.0065 0.1062 0.6249 0.0770 0.0207 0.1459 0.7564 0.0766 0.0053 0.1469 0.7712 0.0003 0.0034 0.0042 0.9921 0.0003 0.0028 0.0041 0.9928 0 0.0610 0.0327 0.9063 0 0.0597 0.0326 0.9078
suhu (K) fase atas fase bawah
x1 x2 x3 x4 x1 x2 x3 x4
0.4858 0.0004 0.1866 0.3272 0.4860 0 0.1866 0.3274 0.3008 0.0008 0.1090 0.5894 0.3009 0 0.1090 0.5901
Page 29
Prediksi kesetimbangan UNIQUAC
suhu (K) fase atas fase bawah
x1 x2 x3 x4 x1 x2 x3 x4 303 0.1144 0.0000 0.0296 0.8559 0.0216 0.0000 0.4892 0.4892 0.0360 0.0568 0.5161 0.3911 0.0140 0.0778 0.2896 0.6186 0.0442 0.0771 0.6169 0.2618 0.0015 0.0043 0.2668 0.7274 0.0288 0.0715 0.4745 0.4251 0.0276 0.0790 0.4208 0.4725 0.0316 0.0974 0.3225 0.5486 0.0314 0.1188 0.4806 0.3691 0.0432 0.0823 0.1805 0.6940 0.0327 0.1866 0.4881 0.2926
suhu (K) fase atas fase bawah
x1 x2 x3 x4 x1 x2 x3 x4 313 0.0006 0.0000016 0.4071 0.5923 0.0005 0.0000016 0.3913 0.6082 0.0012 0.0000006 0.5213 0.4775 0.0012 0.0000006 0.5061 0.4927 0.0005 0.0000020 0.8118 0.1877 0.3379 0.0000010 0.5713 0.0907 0.0012 0.0000015 0.1306 0.8681 0.0018 0.0000014 0.1538 0.8444 0.0001 0.0000016 0.0462 0.9537 0.0001 0.0000016 0.0432 0.9567 0 0.0000016 0.0010 0.9990 0 0.0000016 0.0009 0.9991
suhu (K) fase atas fase bawah
x1 x2 x3 x4 x1 x2 x3 x4 323 0.0004 0.0009 0.3553 0.6435 0.0004 0.0009 0.3564 0.6423 0.0004 0.0008 0.4211 0.5777 0.0004 0.0008 0.4162 0.5826 0.0001 0.0009 0.2718 0.7273 0.0002 0.0008 0.3253 0.6737 0.0001 0.0009 0.0960 0.9031 0.0002 0.0008 0.1256 0.8734 0.0000 0.0008 0.0819 0.9173 0.4534 0.0004 0.0695 0.4766 0 0.0008 0.0008 0.9983 0 0.0008 0.0017 0.9975
Kesimpulan
Dari eksperimen dan prediksi yang telah dilakukan dapat ditarik kesimpulan sebagai berikut:
1.
Didapatkan hasil kesetimbangan cair-cair sistem
Eugenol(1) + β
-Caryophyllene
(2) + Etanol(3) + Air (4).
2.
Secara keseluruhan berdasarkan perhitungan %RMSD secara simultan yang berkisar dari
0,0875-0,1041 lebih baik daripada %RMSD yang dihitung tiap suhu yang berkisar dari
0,0916-0,1276
» Pada suhu 303 K perhitungan untuk sistem ini lebih baik model UNIQUAC dengan RMSD 0,0916
sedangkan untuk model NRTL RMSD didapatkan 0,1164.
» Pada suhu 313 K perhitungan untuk sistem ini lebih baik model NRTL dengan RMSD 0,0927
sedangkan untuk model UNIQUAC RMSD didapatkan 0,1062.
» Pada suhu 323 K perhitungan untuk sistem ini lebih baik model UNIQUAC dengan RMSD 0,1154
sedangkan untuk model NRTL RMSD didapatkan 0,1276.
» Secara simultan didapatkan perhitungan untuk sistem ini lebih baik model UNIQUAC dengan RMSD
0,0875 sedangkan untuk model NRTL RMSD didapatkan 0,1041.
Data komposisi sample berdasarkan lama pengambilan sampel
(sebagai dasar lamanya pengambilan sample ketika telah mencapai kesetimbangan)
No sampel Waktu
(jam )
Komposisi (% area)
Eugenol Etanol Air
2a top 20 0 2,61 95,63 2c top 24 0 3,23 95,29 3a top 22 0 6,20 92.28 3c top 44 0 5,60 92.31 7a top 22 0.85 15,59 82,62 7c top 46 0.65 15,77 83.23 8a top 20 0.94 18,54 80,19 8c top 44 0,93 18,24 79,60 21a top 20 0.36 10,59 87.95 21c top 24 0.33 10,48 88.17 22 top 20 0.33 10,50 88.23 22 top 24 0.38 9.910 88.73 2b bot 20 93,57 2,37 3,57 2d bot 24 92.9 2.32 3.26 3b bot 22 92.63 4.79 1.24 3d bot 44 92.92 5.42 1.29
Page 33
Carrier Gas
Harus inert : N2, He, Ar, CO
2
Pemilihan berdasarkan tipe detektor yang digunakan
Terdapat MS yang menyaring impurities
Untuk efisiensi kolom, sampel tidak boleh terlalu banyak dan harus masuk ke dalam
kolom dalam bentuk gas
Sampel yang terlalu banyak dapat menyebabkan bond broodening dan lost of resolution
Metode injeksi yang paling umum adalah dengan menggunakan microsyringe untuk
menginjeksikan sampel melalui rubber septum kedalam flash vaporizer spot pada bagian
atas kolom
Temperatur sampel port biasanya 50
o
C dari titik didih komponen volatile paling sedikit
pada sampel
Column
Untuk hasil yang presisi
temperatur kolom harus dikontrol dalam 10
o
Temperatur optimum kolom bergantung pada titik didih sampel sebagai acuan
rule of thumb = temperatur sedikit diatas titik didih rata-rata sampel dalam
elution time
Temperatur minimum memberikan hasil yang baik tetapi menaikkan elution
time
Jika sampel mempunyai jangkauan titik didih yang besar, pengontrolan atau
Page 35
Detector
Different detector
different type selectivity
– Non selective detector
merespon semua senyawa kecuali carrier gas
– Selective Detector
merespon banyak komponen yang sifat fisika dan kimia sama
– Specific Detector
merespon 1 komponen saja
Concentration dependent detector
tidak menghancurkan sampel
Mass flow dependent detector
manghancurkan sampel
FID (Flame Ionization Detector)
Keluaran dari kolom dicampur dengan Hidrogen kemudian dibakar. Komponen
organic dibakar dalam api menghasilkan ion dari elektron yang menghasilkan
listrik. Potensial listrik yang dihasilkan dikumpulkan dengan electrode collector
letaknya ada diatas api.
FID
– mass sensitive bukan konsentrasi sensitive
– Keuntungannya perubahan pada flow rate mobile phase tidak mempengaruhi
respon detektor
– Detector yang memiliki sensitivitas tinggi, sering digunakan
– Mudah digunakan, tetapi menghancurkan sampel
– Diletakkan dibelakang karena sifat yang menghancurkan sampel biasanya
didepannya ada detektor lagi seperti TCD(Thermal Conductivity Detector)
Page 37
Rumus Umum NRTL :
ln γ
i
=
𝜏
𝑗𝑖
𝐺
𝑗𝑖
𝑥
𝑗
𝑚
𝑗=1
𝐺
𝑙𝑖
𝑥
𝑙
𝑚
𝑙=1
+
𝑥
𝑗
𝐺
𝑗𝑖
𝐺
𝑙𝑗
𝑥
𝑙
𝑚
𝑙=1
𝜏
𝑖𝑗
−
𝑥
𝑛
𝜏
𝑛𝑗
𝐺
𝑛𝑗
𝑚
𝑛=1
𝐺
𝑙𝑗
𝑥
𝑙
𝑚
𝑙=1
𝑚
𝑗=1
Penjabaran NRTL 4 komponen
𝑙𝑛𝛾
1=
𝜏
21𝐺
21𝑥
2+ 𝜏
31𝐺
31𝑥
3+ 𝜏
41𝐺
41𝑥
4𝑥
1+ 𝐺
21𝑥
2+ 𝐺
31𝑥
3+ 𝐺
41𝑥
4+
𝑥
1𝑥
1+ 𝐺
21𝑥
2+ 𝐺
31𝑥
3+ 𝐺
41𝑥
4−
𝜏
21𝐺
21𝑥
2+ 𝜏
31𝐺
31𝑥
3+ 𝜏
41𝐺
41𝑥
4𝑥
1+ 𝐺
21𝑥
2+ 𝐺
31𝑥
3+ 𝐺
41𝑥
4+
𝑥
2𝐺
21𝑥
1𝐺
12+ 𝑥
2+ 𝐺
32𝑥
3+ 𝐺
42𝑥
4𝜏
12−
𝜏
12𝐺
12𝑥
1+ 𝜏
32𝐺
32𝑥
3+ 𝜏
42𝐺
42𝑥
4𝑥
1𝐺
12+ 𝑥
2+ 𝐺
32𝑥
3+ 𝐺
42𝑥
4+
𝑥
3𝐺
31𝑥
1𝐺
13+ 𝐺
23𝑥
2+ 𝑥
3+ 𝐺
43𝑥
4𝜏
13−
𝜏
13𝐺
13𝑥
1+ 𝜏
23𝐺
23𝑥
2+ 𝜏
43𝐺
43𝑥
4𝑥
1𝐺
13+ 𝐺
23𝑥
2+ 𝑥
3+ 𝐺
43𝑥
4+
𝑥
4𝐺
41𝑥
1𝐺
14+ 𝐺
24𝑥
2+ 𝐺
34𝑥
3+ 𝑥
4𝜏
14−
𝜏
14𝐺
14𝑥
1+ 𝜏
24𝐺
24𝑥
2+ 𝜏
34𝐺
34𝑥
3𝑥
1𝐺
14+ 𝐺
24𝑥
2+ 𝐺
34𝑥
3+ 𝑥
4
Rumus Umum UNIQUAC
ln 𝛾
𝑖= 𝑙𝑛
∅𝑖 𝑥𝑖+
𝑧 2𝑞
𝑖𝑙𝑛
𝜃𝑖 ∅𝑖+ 𝑙
𝑖−
∅𝑖 𝑥𝑖𝑥
𝑗 𝑗𝑙
𝑗+ 𝑞
𝑖1 − 𝑙𝑛
𝜃
𝑗𝜏
𝑗𝑖 𝑚 𝑗=1−
𝜃𝑗𝜏𝑗𝑖 𝜃𝑘𝜏𝑘𝑗 𝑚 𝑘=1 𝑚 𝑗=1
Penjabaran UNIQUAC 4 komponen
𝑙𝑛𝛾
1= 𝑙𝑛
∅
1𝑥
1+
𝑧
2
𝑞
1𝑙𝑛
𝜃
1∅
1+ 𝑙
1−
∅
1𝑥
1𝑙
1𝑥
1+ 𝑙
2𝑥
2+ 𝑙
3𝑥
3+ 𝑙
4𝑥
4+ 𝑞
11 − 𝑙𝑛 𝜃
1𝜏
11+ 𝜃
2𝜏
21+ 𝜃
3𝜏
31+ 𝜃
4𝜏
41−
𝜃
1𝜏
11𝜃
1𝜏
11+ 𝜃
2𝜏
21+ 𝜃
3𝜏
31+ 𝜃
4𝜏
41+
𝜃
2𝜏
21𝜃
1𝜏
12+ 𝜃
2𝜏
22+ 𝜃
3𝜏
32+ 𝜃
4𝜏
42+
𝜃
3𝜏
31𝜃
1𝜏
13+ 𝜃
2𝜏
23+ 𝜃
3𝜏
33+ 𝜃
4𝜏
43+
𝜃
4𝜏
41𝜃
1𝜏
14+ 𝜃
2𝜏
24+ 𝜃
3𝜏
34+ 𝜃
4𝜏
44Page 39
Penyimpangan hasil eksperimen dan prediksi model NRTL
% etanol terhadap air(%) atas bawah Δx1 Δx2 Δx3 Δx4 Δx1 Δx2 Δx3 Δx4 50 0.6606 0.0058 0.0671 0.0116 0.5210 0.0140 0.1140 0.0070 45 0.1250 0.0085 0.3547 0.0284 0.0630 0.0167 0.0862 0.0284 35 0.1700 0.0155 0.6482 0.0909 0.1598 0.0316 0.0969 0.0888 25 0.0507 0.0127 0.0253 0.1464 0.2378 0.0265 0.0104 0.1445 10 0.0001 0.0018 0.0412 0.0122 0.0018 0.0011 0.0629 0.0121 0 0.0000 0.0350 0.0189 0.0002 0.0016 0.0248 0.0187 0.0122 % etanol terhadap air(%) atas bawah Δx1 Δx2 Δx3 Δx4 Δx1 Δx2 Δx3 Δx4 50 0.5255 0.0595 0.1048 0.2149 0.2728 0.0818 0.4594 0.1943 40 0.1846 0.0288 0.0697 0.0040 0.0048 0.0702 0.0679 0.0637 35 0.1645 0.0286 0.0751 0.3140 0.0636 0.0722 0.0189 0.0805 25 0.1150 0.0284 0.0627 0.0150 0.1635 0.0733 0.0196 0.1853 10 0.0340 0.0144 0.0366 0.1270 0.1092 0.0650 0.0136 0.1063 0 0.0001 0.0596 0.0309 0.1086 0.4690 0.0935 0.0638 0.4512 % etanol terhadap air(%) atas bawah Δx1 Δx2 Δx3 Δx4 Δx1 Δx2 Δx3 Δx4 50 0.5977 0.0005 0.1349 0.0315 0.4395 0.0186 0.0909 0.0165 40 0.1919 0.0005 0.3532 0.0588 0.0039 0.0200 0.0201 0.0580 35 0.1432 0.0009 0.2188 0.0955 0.2493 0.0392 0.0117 0.1064 25 0.0875 0.0012 0.0458 0.1528 0.2125 0.0315 0.0603 0.1654 10 0.0344 0.0015 0.0035 0.2385 0.4151 0.0470 0.0306 0.2250 0 0.0000 0.0018 0.0710 0.2832 0.5162 0.0531 0.0669 0.2915
Suhu
313 K
303 K
323 K
% etanol terhadap air(%) atas bawah Δx1 Δx2 Δx3 Δx4 Δx1 Δx2 Δx3 Δx4 50 0.5255 0.0595 0.1048 0.2149 0.0431 0.0818 0.4594 0.1943 40 0.1846 0.0288 0.0697 0.0040 0.0008 0.0702 0.0679 0.0637 35 0.1645 0.0286 0.0751 0.3140 0.0101 0.0722 0.0189 0.0805 25 0.1150 0.0284 0.0627 0.0150 0.0258 0.0733 0.0196 0.1853 10 0.0340 0.0144 0.0366 0.1270 0.0173 0.0650 0.0136 0.1063 0 0.0001 0.0596 0.0309 0.1086 0.0742 0.0935 0.0638 0.4512
Penyimpangan hasil eksperimen dan prediksi model UNIQUAC
% etanol terhadap air(%) atas bawah Δx1 Δx2 Δx3 Δx4 Δx1 Δx2 Δx3 Δx4 50 0.6454 0.0081 0.0404 0.0106 0.0800 0.0124 0.0288 0.0074 45 0.0212 0.0139 0.0512 0.0451 0.0265 0.0124 0.0301 0.0106 35 0.0230 0.0351 0.0315 0.0290 0.0489 0.0145 0.0437 0.0435 25 0.0078 0.0182 0.0120 0.1200 0.0445 0.0230 0.0115 0.0632 10 0.0143 0.0006 0.0048 0.1347 0.0020 0.0001 0.0103 0.1038 0 0.0000 0.0012 0.0000 0.1408 0.0016 0.0093 0.0002 0.1101 % etanol terhadap air(%) atas bawah Δx1 Δx2 Δx3 Δx4 Δx1 Δx2 Δx3 Δx4 50 0.0290 0.0011 0.3546 0.0086 0.1297 0.0180 0.1291 0.0179 40 0.0010 0.0012 0.4197 0.0168 0.1950 0.0194 0.0867 0.0423 35 0.0012 0.0019 0.2678 0.0132 0.3915 0.0382 0.0374 0.0597 25 0.0009 0.0021 0.0949 0.0323 0.0546 0.0307 0.0806 0.0641
Suhu
313 K
303 K
323 K
Page 41
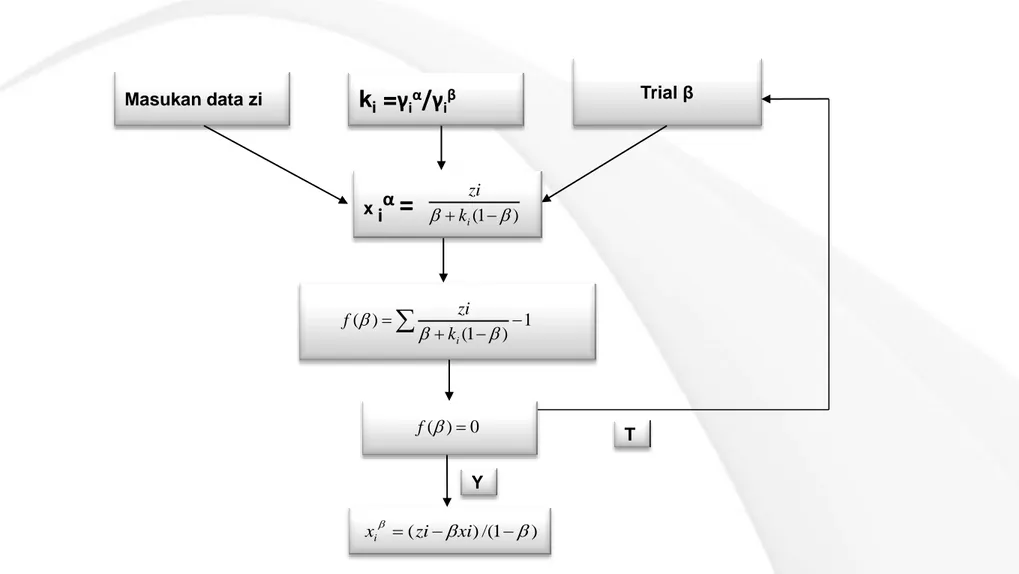
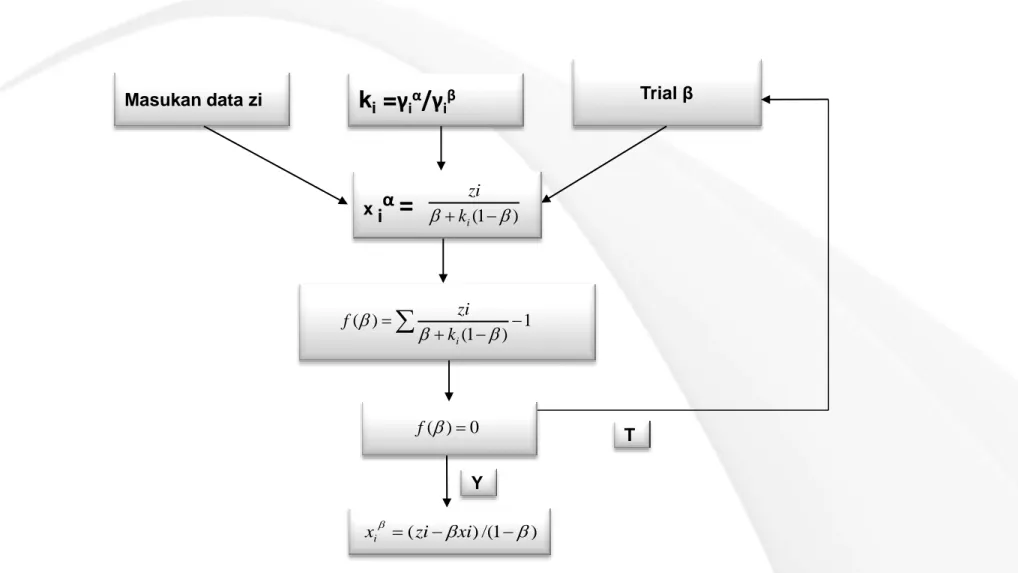
Diagram blok perhitungan komposisi
Masukan data zi
Trial β
1 ) 1 ( ) (
i k zi f ) 1 /( ) (
zi xi xi0
)
(
f
Y
T
k
i=
γ
iα/γ
iβx
i
α
=
(
1
)
ik
zi
Diagram blok perhitungan komposisi
Masukan data zi
Trial β
1 ) 1 ( ) (