TUGAS AKHIR
PRARANCANGAN PABRIK KAPROLAKTAM DARI
SIKLOHEKSANON DAN HIDROKSILAMIN SULFAT
KAPASITAS 60.000 TON PER TAHUN
DISUSUN OLEH :
NUR ERIKA LAILA M. I 0507048
ARDIENA NOORLYTA I 0507063
JURUSAN TEKNIK KIMIA FAKULTAS TEKNIK
UNIVERSITAS SEBELAS MARET
commit to user
BAB I
PENDAHULUAN
1.1. Latar Belakang Pendirian Pabrik
Perkembangan ilmu pengetahuan dan teknologi serta kemajuan sektor industri menuntut bangsa Indonesia menuju ke arah industrialisasi. Untuk pencapaian kemajuan di bidang industri terfokus pada bidang industri kimia, maka kebutuhan akan bahan-bahan kimia di dalam negeri perlu ditumbuhkan dan dikembangkan. Sampai saat ini pembangunan sektor industri di Indonesia mengalami peningkatan, salah satunya adalah pembangunan sub sektor industri kimia. Namun, ketergantungan impor luar negeri masih lebih besar dibandingkan ekspornya. Indonesia masih banyak mengimpor bahan baku atau produk - produk suatu industri kimia dari luar negeri.
Kaprolaktam merupakan senyawa organik dengan rumus kimia C6H11NO
yang dapat diperoleh dari reaksi oksimasi antara sikloheksanon, hidroksilamin sulfat, dan Amonia. Penggunaan utama kaprolaktam adalah sebagai bahan baku nilon-6. Kaprolaktam juga digunakan secara luas pada industri plastik asam amino kaproat, poliuretan, dan cat mobil.
Berdasarkan pertimbangan hal-hal diatas, pendirian pabrik kaprolaktam sangat diperlukan dalam mengurangi impor dan meningkatkan ekspor. Selain itu, pendirian pabrik kaprolaktam juga akan membuka lapangan kerja sehingga dapat mengurangi pengangguran dan akan memacu tumbuhnya pabrik baru yang menggunakan kaprolaktam sebagai bahan bakunya.
1.2. Kapasitas Prarancangan
Kapasitas produksi mempengaruhi perhitungan secara teknis maupun ekonomis dalam perancangan pabrik. Pada prarancangan pabrik kaprolaktam dari sikloheksanon dan hidroksilamin sulfat yang direncanakan berkapasitas 60.000 ton per tahun. Kapasitas rancangan pabrik kaprolaktam ditentukan dengan didasarkan pada beberapa pertimbangan sebagai berikut :
1.Prediksi kebutuhan pasar 2.Ketersediaan bahan baku
3.Kapasitas pabrik yang menguntungkan
1. Prediksi Kebutuhan Pasar
commit to user
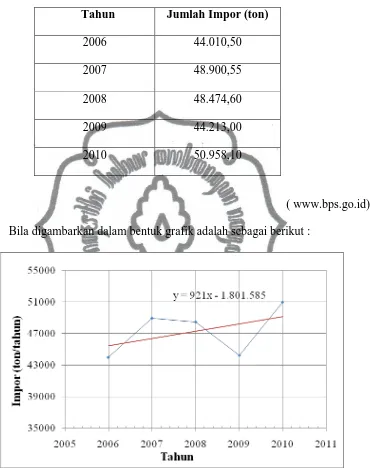
Tabel 1.1. Kebutuhan Kaprolaktam di Indonesia
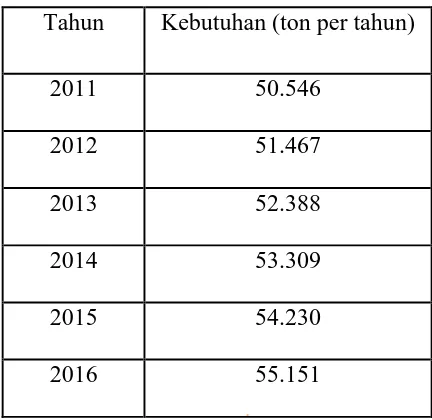
( www.bps.go.id) Bila digambarkan dalam bentuk grafik adalah sebagai berikut :
Gambar 1.1 Kebutuhan Kaprolaktam Indonesia
Grafik diatas menunjukkan bahwa impor kaprolaktam pada tahun 2006 sampai 2007 mengalami kenaikan kemudian mengalami penurunan pada tahun 2008 kemudian mengalami kenaikan lagi pada tahun 2010. Angka impor kaprolaktam cukup tinggi di Indonesia. Pendirian pabrik kaprolaktam penting
Tahun Jumlah Impor (ton)
untuk pemenuhan kebutuhan kaprolaktam Indonesia dan akan memenuhi kebutuhan impor kaprolaktam Indonesia sehingga merupakan peluang yang besar dalam memberikan keuntungan sekaligus meningkatkan devisa negara karena akan menekan laju angka impor dan meningkatkan laju angka ekspor.
Kebutuhan kaprolaktam yang diperkirakan meningkat pada tahun-tahun mendatang dapat dihitung dengan membuat grafik linier kebutuhan kaprolaktam 2006 - 2010 dan diperoleh persamaan kapasitas = 921x - 1.801.585. Berdasarkan perhitungan diperkirakan kebutuhan kaprolaktam pada tahun 2016 sekitar 50.000 ton per tahun. Berdasarkan pertimbangan diatas maka direncanakan didirikan pabrik kaprolaktam dengan kapasitas 60.000 ton per tahun untuk membantu memenuhi kebutuhan kaprolaktam tersebut.
Dari persamaan tersebut diperoleh prediksi kebutuhan kaprolaktam pada tahun-tahun mendatang (Tabel 1.2.), yang digunakan sebagai bahan pertimbangan untuk penentuan kapasitas produksi pabrik.
Tabel 1.2. Prediksi Kebutuhan Kaprolaktam Tahun Kebutuhan (ton per tahun)
commit to user
Kaprolaktam sangat dibutuhkan di Indonesia, karena di Indonesia terdapat beberapa perusahaan yang sudah mengembangkan produk nilon-6, asam amino kaproat, dan poliuretan yang menggunakan kaprolaktam sebagai bahan bakunya. Industri yang membutuhkan kaprolaktam dapat dilihat pada Tabel 1.3.
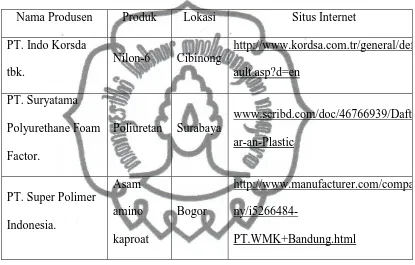
Tabel 1.3. Industri Indonesia yang Menggunakan Kaprolaktam
Nama Produsen Produk Lokasi Situs Internet PT. Indo Korsda
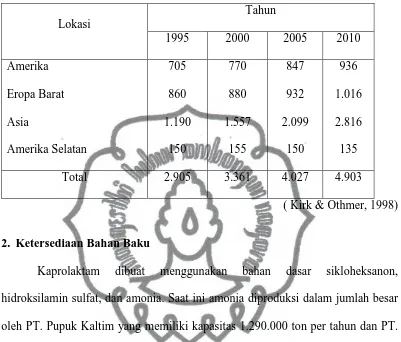
Tabel 1.4. Perkiraan Kapasitas Kaprolaktam Dunia ( x 103 ton)
commit to user
3. Kapasitas pabrik yang menguntungkan
Kapasitas pabrik yang didirikan harus diatas kapasitas minimum pabrik, atau minimal sama dengan pabrik yang berjalan. Untuk pertimbangan kapasitas, dapat dilihat dari beberapa pabrik yang sudah berdiri pada Tabel 1.5.
Tabel 1.5. Industri Penghasil Kaprolaktam di Luar Negeri
Nama Perusahaan Lokasi Kapasitas (ton per tahun) Hanook Kaprolaktam Ulsan, Korea 80.000
Hanhua Kaprolaktam Korea 80.000 Chung Tai Taipei, Taiwan 110.000 Mitstubishi Chem Kurosaki, Japan 100.000 Toray Ind. Nagoya, Japan 145.000 Nitrocarbono Camacan, Brazil 55.000 Monomers Colombia 25.000 SNIA Montedipe Torviscosa, Italia 15.000
(Kirk & Othmer, 1998) Berdasarkan data aktual dan prediksi kebutuhan kaprolaktam, maka penentuan kapasitas rancangan harus lebih dari kapasitas minimal pabrik yang sudah ada agar dapat mendatangkan keuntungan dan memenuhi kebutuhan dalam negeri. Oleh karena itu pendirian pabrik kaprolaktam dengan kapasitas 60.000 ton per tahun pada tahun 2016 dipilih dengan pertimbangan :
a. Diperkirakan dapat memenuhi kebutuhan dalam negeri.
kapasitas minimal.
1.3. Lokasi Pabrik
Pemilihan lokasi pabrik sangat penting dalam menentukan keberhasilan dan kelangsungan hidup suatu pabrik. Pada dasarnya terdapat dua faktor yang menentukan lokasi pabrik, yaitu:
1. Faktor primer, antara lain :
a. Letak pabrik terhadap pasar dan bahan baku
Pabrik didirikan dekat bahan baku, agar suplai bahan baku terjamin dan biaya transportasi bahan baku lebih murah.
b. Pemasaran
c. Tersedianya tenaga kerja
d. Tersedianya utilitas (sumber air dan tenaga listrik) 2. Faktor sekunder antara lain:
a. Kondisi masyarakat setempat b. Jenis transportasi
c. Kebijakan pemerintah setempat d. Iklim
commit to user
a. Letak Bahan Baku
Suatu pabrik dapat beroperasi sangat tergantung pada ketersediaan bahan baku. Pabrik kaprolaktam akan didirikan di Gresik, Jawa Timur karena letaknya berdekatan dengan sumber bahan baku yaitu amonia dan asam sulfat yang diperoleh dari PT. Petrokimia Gresik yang masing-masing memiliki kapasitas produksi sebesar 445.000 ton per tahun dan 570.000 ton per tahun.
b. Pemasaran
Daerah pemasaran kaprolaktam tersebar di pulau Jawa, diantaranya Tanggerang, Bogor dan Surabaya. Pemasaran kaprolaktam tidak sulit karena sarana transportasi yang tersedia cukup lengkap. Sehingga dengan berdirinya pabrik kaprolaktam juga akan membuka kesempatan berdirinya industri-industri lain yang menggunakan bahan baku kaprolaktam di kawasan Jawa.
c. Tenaga Kerja
Tenaga kerja dapat diperoleh dari masyarakat sekitar pabrik, mengingat masyarakat sudah terbiasa adanya pabrik serta dekat dengan pusat pendidikan daerah tersebut yang mendukung.
d. Sarana Transportasi
e. Utilitas
Kebutuhan pabrik akan air sangat besar, untuk itu diperlukan lokasi yang cukup. Gresik merupakan daerah yang memiliki kadar air yang relatif besar jika dibandingkan dengan daerah-daerah lainnya. Kebutuhan akan air dapat diperoleh dari air sungai Bengawan Solo. Kebutuhan listrik diperoleh dari PLN dengan gardu-gardu utama disekitar pabrik dan diesel generator sebagai cadangan. Kebutuhan bahan bakar yakni IDO (Industrial Diesel Oil) yang digunakan untuk generator diperoleh dari Pertamina.
f. Iklim
Iklim yang terlalu panas akan mengakibatkan diperlukannya peralatan pendingin yang lebih banyak sedangkan iklim yang terlalu dingin atau lembab akan berakibat bertambahnya biaya konstruksi pabrik karena diperlukan perlindungan khusus pada alat-alat proses. Di daerah Gresik merupakan daerah tropis sehingga memiliki iklim yang kering dengan curah hujan yang cukup tinggi. Sehingga Gresik sangat cocok untuk dijadikan lokasi pabrik kaprolaktam.
g. Kebijakan pemerintah setempat
commit to user
Gambar 1.2 Peta lokasi pendirian pabrik
1.4. Tinjauan Pustaka
Kaprolaktam (C6H11NO) atau yang dikenal sebagai Aminocaproic lactam,
merupakan senyawa organik yang larut dalam air, pelarut-pelarut terklorinasi, dan destilat petroleum. Kaprolaktam merupakan senyawa yang terbentuk dari reaksi oksimasi antara sikloheksanon, hidroksilamin sulfat, dan amonia.
Di pasaran, kaprolaktam beredar dalam bentuk flake maupun kristal atau
priil serta dijual dalam kemasan kantong plastik dan drum. Kaprolaktam yang mengalami peningkatan dari tahun ke tahun dijadikan pertimbangan dalam pendirian pabrik. Impor kaprolaktam selama ini hampir seluruhnya diserap oleh sektor nilon-6, asam amino kaproat, dan poliuretan. Namun pada tahun 2008
impor kaprolaktam mangalami penurunan. Impor tersebut terutama yang berasal dari Jepang, Jerman, Belgia, Swiss, dan Polandia.
(Kirk & Othmer,1998)
1.4.1. Macam-macam Proses Pembuatan Kaprolaktam
Pemilihan proses bertujuan untuk penentuan proses yang tepat yang akan digunakan, sehingga menguntungkan baik secara teknis maupun ekonomis. Proses pembuatan kaprolaktam bermacam-macam tergantung dari bahan baku yang digunakan, saat ini ada 3 proses reaksi yang berbeda secara mendasar, yaitu:
1. BASF Process
BASF Process disebut juga Allied Chemical Process. Pembuatan kaprolaktam dengan proses ini menggunakan bahan baku sikloheksanon, hidroksilamin sulfat, amonia, dan dengan penambahan asam sulfat. Proses pembuatan kaprolaktam ini terdiri dari 2 tahap, yaitu reaksi oksimasi dan penyusunan Beckman. Tahap pertama bertujuan untuk pembentukkan oksim dan tahap kedua bertujuan untuk pembentukkan kaprolaktam.
Pada tahap pertama umpan sikloheksanon, hidroksilamin sulfat, amonia direaksikan pada fase cair dengan perbandingan 1 : 5 : 1. Reaksi berlangsung secara eksotemis pada suhu 150°C dan tekanan 5 atm. Pada tahap pertama ini terjadi reaksi oksimasi pembentukkan sikloheksanon oksim dengan produk samping berupa amonium sulfat (1.1).
commit to user
reaksi 2 yang bersifat basa dinetralisasi dengan penambahan asam sulfat yang bersifat asam sehingga membentuk hasil samping berupa amonium sulfat. Produk utama berupa kaprolaktam dan produk samping berupa amonium sulfat dengan perbandingan 1 : 1,5. Reaksi yang terjadi adalah :
C
Dutch Statemines Process disebut juga Hydroxylamine Phosphate to Oksim (HPO Process). Pembuatan kaprolaktam dengan proses ini menggunakan bahan baku fenol, amonia, asam fosfat, dan katalis palladium. Proses ini terbagi menjadi dua tahap, tahap pertama adalah hidrogenasi fenol menjadi sikloheksanol dengan katalis palladium yang menghasilkan 95% yield. Kemudian dilanjutkan dengan hidrogenasi sikloheksanol menjadi sikloheksanon (1.3). Proses ini berlangsung secara endotermis dengan temperatur 400oC - 600oC.
Beckmann agar menjadi kaprolaktam seperti dalam proses fenol (1.5). Proses ini berlangsung pada temperatur 145oC - 165oC dengan tekanan 10 atm.
HNO3 + H2PO4- NO3- + H3PO4...(1.3)
3. Toyo Rayon Photonitrosation
Pembuatan kaprolaktam dengan proses ini menggunakan bahan baku sikloheksan, amonia, dengan katalis Pt-Rh. Proses ini dikembangkan oleh Toyo Rayon Co. dari Jepang. Proses fotonisasi ini secara keseluruhan ditujukan agar sikloheksan berubah menjadi sikloheksanon oksim.
commit to user kelebihan serta kekurangannya, maka pada prarancangan pabrik kaprolaktam dipilih proses BASF, karena :
2. Proses BASF perancangan reaktor akan lebih murah dan sederhana dibandingkan dengan proses yang lainnya karena dapat menggunakan reaktor RATB.
3. Kondisi operasi pada tekanan dan temperatur yang lebih rendah daripada proses lain.
1.4.2. Kegunaan Produk
Kegunaan kaprolaktam sebagai bahan mentah untuk produksi serat-serat nilon-6. Selain itu, digunakan juga pada industri plastik, asam amino kaproat, poliuretan, dan cat mobil. Sedangkan produk samping yang berupa ammonium sulfat dapat digunakan sebagai pupuk.
(Kirk & Othmer, 1998)
1.4.3. Sifat Fisika dan Kimia
1.4.3.1. Sifat Fisika dan Kimia Bahan Baku
a. Sikloheksanon 1) Sifat Fisika
Rumus bangun :
C O
CH2
CH2 CH2
CH2
CH2
commit to user
Warna : Bening tak berwarna
Titik didih : 156,7°C
Titik lebur : -31,15°C
Densitas : 1,05 g/mL
Kemurnian : 99,9% berat
Impuritas : 0,1% H2O Kelarutan : Larut dalam air
(Yaws, 1999) 2) Sifat Kimia
Reaksi Oksidasi
Oksidasi fase cair dengan udara menggunakan katalis kobalt atau asam borak menghasilkan sikloheksanol.
(Kirk & Othmer, 1998) b. Hidroksilamin sulfat
1) Sifat Fisika
Rumus molekul : (NH2OH)2 H2SO4 Berat molekul : 164,14 g/gmol
Wujud : Padat
Warna : Putih
Densitas : 1,463 g/mL
Ukuran Kristal :
- Øavg : 0,356 mm
Kemurnian : 99,5% berat
Impuritas : 0,5% H2O Titik lebur : 170°C
(Yaws, 1999) 2) Sifat Kimia
Sangat larut dalam air
(Kirk & Othmer, 1998) c. Amonia
1) Sifat Fisika
Rumus molekul : NH3
Berat molekul : 17,03 g/gmol
Wujud : Cair
Warna : Bening tak berwarna
Titik didih : -33,43°C
Titik lebur : -77,74°C
Densitas : 0,7708 g/mL
Kemurnian : 29,4% berat
Impuritas : 70,6% H2O Kelarutan : Larut dalam air
commit to user
2) Sifat Kimia
Pada suhu tinggi bila dioksidasi dengan KMnO4 menghasilkan
nitrogen dan air.
2 NH3 + 2 KMnO4 2 KOH + 2 MnO2 + 2 H2O + N2...(1.12) Klorinasi.
8 NH3 + 3 Cl2 N2 + 6 NH4Cl...(1.13) Dioksidasi menjadi nitrogen oksida dan air untuk menghasilkan
asam nitrat dengan katalis Pt-Rhodium.
4 NH3 + 5 O3 4 NO + 6 H2O...(1.14)
2 NO + O2 2 NO2...(1.15)
3 NO2 + 2 H2O 2 HNO3 + NO...(1.16) Amonia cair dan garamnya akan membentuk ion kompleks dalam
larutan amoniak berlebih.
CuSO4 + 2 NH3 Cu(OH)2 + (NH4)2SO4...(1.17)
Cu(OH)2 Cu2+ + 2 OH-...(1.18)
4 NH3 + Cu2+ [Cu(NH3)4] 2+...(1.19) Amonia dengan logam aktif, seperti magnesium akan menghasilkan
nitrit.
3 Mg + 2 NH3 Mg3N2 + 3 H2...(1.20) Bereaksi dengan halogen :
NCl3NH3 + 3 NH3 N2 + 3 NH4Cl...(1.21)
NCl3Cl + 3 Cl2 NCl3 + 3 HCl...(1.22)
Bereaksi dengan phosphorus akan menghasilkan nitrogen dan phospin.
2 NH3 + 2 P 2 PH3 + N2...(1.24) Sedangkan dengan sulfur vapor akan menghasilkan ammonium sulfida dan nitrogen. Sulfur juga bereaksi dengan amoniak anhidrit cair akan terbentuk nitrogen sulfida .
10 S + 4 NH3 6 H2S + N4S4...(1.25) Apabila bereaksi dengan karbondioksida akan membentuk
ammonium karbonat yang kemudian akan terdekomposisi menjadi urea dan air .
2 NH3 + CO2 NH2CO2NH4...(1.26)
NH2CO2NH4 NH2CO2NH2 + H2O...(1.27)
(Kirk & Othmer, 1998) d. Toluen
1) Sifat Fisika
Rumus bangun :
C
CH CH3
CH
CH CH
CH
Rumus molekul : C7H8
commit to user
Warna : Bening tak berwarna
Titik didih : 111°C
Titik lebur : -94,97°C
Densitas : 0,866 g/mL
Kemurnian : 99,5% berat
Impuritas : 0,5% H2O Kelarutan : Larut dalam air
(Kirk & Othmer, 1998)
2) Sifat Kimia
Reaksi Oksidasi
Oksigen pada fase cair dengan adanya katalis kobalt yang di dukung oleh bromindan mangan, sangat baik untuk menghasilkan asam benzoik.
Reaksi Substitusi
Klorinasi pada 100oC atau dengan adanya sinar ultraviolet dan initiator radikal bebas lainnya memberikan hasil benzyl chloride, benzal chloride, dan benzotri chloride.
Reaksi Adisi pada senyawa aromatik
Toluene dapat terhidrogenasi menjadi methylcyclohexane.
(Kirk & Othmer, 1998) e. Asam Sulfat
1) Sifat Fisika
Berat molekul : 98,08 g/gmol
Wujud : Cair
Warna : Bening tak berwarna
Titik didih : 337ºC
Titik lebur : 10,46ºC
Densitas : 1,837 g/cm3
(Yaws, 1999) 2) Sifat Kimia
Dengan basa akan membentuk garam dan air
H2SO4 (l) + 2NaOH (s) Na2SO4(s) + H2O (l)...(1.28) Dengan alkohol membentuk eter dan air
2C2H5OH(l) + H2SO4(l) C2H5OC2H5(l) + H2O(l) + H2SO4(l)....(1.29) Korosif terhadap semua logam
Bereaksi dengan NaCl membentuk NaSO4
NaCl + H2SO4(l) NaSO4 + 2HCl(l)...(1.30) Bereaksi dengan MgCO3 membentuk MgSO4
MgCO3(s) + H2SO4(l) MgSO4(s) + H2O (l) + CO2(g)...(1.31)
(Kirk & Othmer 1998)
1.4.3.2. Sifat Fisika dan Kimia Bahan Baku Pembantu
a. Air
1) Sifat Fisika
commit to user Wujud : Cair
Warna : Bening tak berwarna
Titik didih : 100oC
Titik lebur : 0ºC
Kemurnian : 100% berat
(Yaws, 1999) 2) Sifat Kimia
Pelarut kimia yang baik (paling sering digunakan)
Merupakan reagen penghidrolisa pada reaksi hidrolisa
Memiliki sifat netral (pH 7)
(www.uk.airliquid.com, 2012)
1.4.3.3. Sifat Fisika dan Kimia Produk
a. Kaprolaktam 1) Sifat Fisika
Rumus bangun :
C H2C
H2C
H2C
NH
CH2
CH2
O
Rumus molekul : C6H11NO Berat molekul : 113,16 g/gmol
Wujud : Padat
Warna : Bening tak berwarna
Titik lebur : 69,21oC
Kemurnian : 99% berat
Impuritas : 1% H2O
Kelarutan : Tidak larut dalam air
(Yaws, 1999) 2) Sifat Kimia
Dapat larut dalam pelarut klorin, benzena, kloroform, etanol, metanol, dan pelarut petroleum
(www.pom.go.id, 2012) b. Amonium Sulfat
1) Sifat Fisika
Rumus molekul : (NH4)2SO4 Berat molekul : 132,14 g/gmol
Wujud : Padat
Warna : Bening tak berwarna
Kemurnian : 99% berat
Impuritas : 1% H2O Densitas : 1,577 g/mL
(Yaws, 1999) 2) Sifat Kimia
Larutan dengan konsentrasi 0,1 M memiliki pH 5,5
commit to user
2NH4OH + H2SO4 (NH4)2.SO4 + H2O...(1.32)
(digilib.its.ac.id, 2012)
1.4.4. Tinjauan Proses Secara Umum
Proses pembuatan kaprolaktam mempunyai 2 tahap reaksi. Proses pertama adalah pembuatan sikloheksanon oksim. Hidroksilamin sulfat yang berfase padat dilarutkan terlebih dahulu dengan menggunakan pelarut toluen di dalam mixer (M-01). Sikloheksanon oksim merupakan reaksi antara sikloheksanon, hidroksilamin sulfat, dan penambahan amonia dan terjadi pada reaktor 1 (R-01). Proses kedua yang terjadi pada reaktor 2 adalah penyusunan Beckman yang mengubah sikloheksanon oksim menjadi kaprolaktam. Kedua proses ini dilakukan dalam reaktor alir tangki berpengaduk (RATB). Reaksi berlangsung pada fase cair-cair, eksotermis, non adiabatis, isothermal pada suhu 150C dan tekanan 5 atm. Perbandingan mol reaktan antara sikloheksanon, hidroksilamin sulfat, Amonia adalah 1 : 5 : 1.
Reaksi yang terjadi adalah sebagai berikut : Reaksi I :
2C6H10O + (NH2OH)2.H2SO4 + 2NH3 2C6H11NO + (NH4)2SO4 + 2H2O....(1.33)
Sikloheksanon Hidroksilamin Amonia Sikloheksanon Amonium Air Sulfat Oksim Sulfat
Reaksi II :
C6H11NO
H2SO4 C
6H11NO
Sikloheksanon Kaprolaktam
Oksim