BAB 3
- Asam Asetat p.a (E.Merck)
- HNO3 p.a (E.Merck)
- Seperangkat alat spektrofotometer FTIR Shimadzu
- Beaker Glass Pyrex
- Neraca Analitik (presisi±0,0001g) Mettler
- Spatula Kaca
- Pipet ukur
3.3. Cara Pengambilan Sampel
Teknik lokasi pengambilan sampling menggunakan teknik ”purpose random
sampling”. Pada pengambilan sampel menggunakan cara point sampler dimana
sampel di ambil pada 3 (tiga) titik (SNI 6989.57:2008)
Titik I di ambil di wilayah pasar sunggal yang merupakan wilayah padat
penduduk dengan aktifitas yang padat, titik II di ambil di sekitar PDAM Tirtanadi
yang menggunakan sungai Belawan sebagai sumber air, dan titik III di ambil di
wilayah pasar I sunggal. Pengambilan sampel air dilakukan di lapisan permukaan
kemudian dimasukkan ke dalam satu botol yang berukuran 600 ml. kemudian Sampel
air ditambahkan HNO3 sebagai pengawet.
3.4. Prosedur Penelitian
3.4.1. preparasi sampel
Sebanyak 100 mL Air Sungai dimasukkan kedalam Beaker glass, ditambahkan 5 mL
HNO3 pekat dipanaskan hingga setengah volume awal diatas hotplate, kemudian didinginkan dan disaring dengan kertas saring dan diencerkan kedalam labu takar 100
mL. Selanjutnya dianalisa logam Fe, Mn dan Zn dengan menggunakan ICP-OES.
3.4.2. Pembuatan Pereaksi
3.4.2.1. Pembuatan Larutan Asetat 1%(v/v)
Sebanyak 10 mL asam asetat glasial dimasukkan ke dalam labu ukur 1000 mL,
kemudian diencerkan dengan aqua steril sampai garis tanda, dan dihomogenkan.
3.4.2.2. Pembuatan Larutan NaOH 2 M (b/v)
Sebanyak 40 g NaOH pelet dimasukkan kedalam Beaker glass. Dilarutkan dengan
aquadest, dimasukkan kedalam labu takar 500 mL kemudian diukur hingga garis tanda
3.4.2.3. Pembuatan Larutan Cu(NO3)2.5H2O 0,5 M
Sebanyak 34.6875 g Kristal Cu(NO3)2.5H2O dimasukkan ke dalam Beaker glass. Dilarutkan dengan aquadest, dimasukkan kedalam labu takar 500 mL kemudian
diukur hingga garis tanda sehingga diperoleh larutan Cu(NO3)2 0,5 M.
3.4.3. Pembuatan Larutan Kitosan
Sebanyak 10 g kitosan dilarutkan kedalam larutan asetat 1% (b/v) sebanyak 1000 mL,
lalu diaduk sampai homogen sehingga diperoleh larutan kitosan kental,
3.4.4. Pembuatan Kitosan CuO
Larutan kitosan dimasukkan kedalam Beaker glass, kemudian ditambahkan dengan
larutan Cu(NO3)2 0,5 M dengan rasio (2:1) hingga diperoleh larutan kental Larutan kental dimasukkan kedalam pompa injeksi dan diteteskan kedalam larutan NaOH 2 M
hingga terbentuk butiran hitam. Selanjutnya didiamkan selama 1 malam, kemudian
disaring dicuci dengan akuades dan dikeringkan.
3.4.5. Proses Adsorpsi Logam pada Air Sungai Sunggal dengan Kitosan CuO Sebanyak 50 mL Air belawan Sunggal setelah didestruksi dimasukkan kedalam kolom
yang telah berisi 15 g kitosan CuO, didiamkan selama 15, 30, 45, 60, dan 75 menit,
kemudian dibuka tutup kolom dan ditampung dengan botol vial, Selanjutnya dianalisa
logam Fe, Mn dan Zn dengan menggunakan ICP.
Gambar 3.1 preparasi sampel 100 mL air sungai
dimasukkan kedalam Beaker glass,
ditambahkan 5 mL HNO3 pekat dipanaskan hingga setengah volume awal diatas hotplate,
didinginkan dan disaring dengan kertas saring diencerkan kedalam labu takar 100 mL.
dianalisa logam Fe, Mn dan Zn
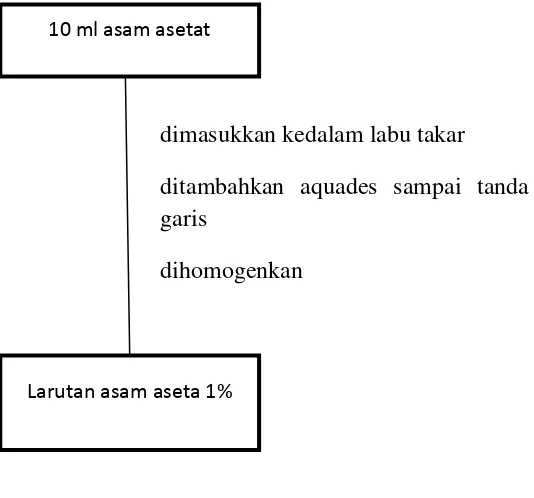
3.5.2. Pembuatan Larutan Asetat 1%(v/v)
Gambar 3.2 Pembuatan Larutan Asetat 1% 10 ml asam asetat
Larutan asam aseta 1%
dimasukkan kedalam labu takar
ditambahkan aquades sampai tanda garis
3.5.3. Pembuatan Larutan NaOH 2M
Gambar 3.3 Pembuatan Larutan NaOH 2M 4 g NaOH
Larutan NaOH 2M
Dilarutkan dengan aquadest, dimasukkan kedalam labu takar 500 mL
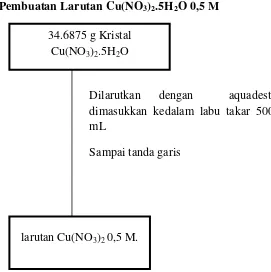
3.5.4. Pembuatan Larutan Cu(NO3)2.5H2O 0,5 M
Gambar 3.4 Pembuatan Larutan Cu(NO3)2.5H2O 0,5 M
3.5.5. Pembuatan Larutan Kitosan
Gambar 3.5 Pembuatan Larutan Kitosan 34.6875 g Kristal
Cu(NO3)2.5H2O
larutan Cu(NO3)2 0,5 M.
Dilarutkan dengan aquadest, dimasukkan kedalam labu takar 500 mL
Sampai tanda garis
10 g kitosan
larutan kitosan kental
dilarutkan kedalam larutan asetat 1% (b/v) sebanyak 1000mL
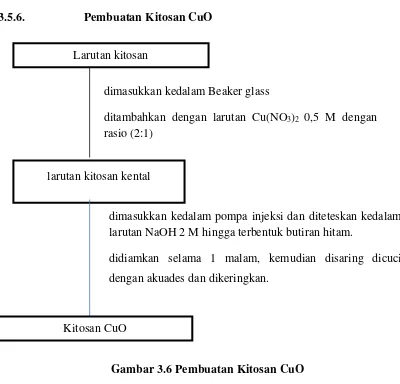
3.5.6. Pembuatan Kitosan CuO
Gambar 3.6 Pembuatan Kitosan CuO Larutan kitosan
larutan kitosan kental
dimasukkan kedalam Beaker glass
ditambahkan dengan larutan Cu(NO3)2 0,5 M dengan rasio (2:1)
dimasukkan kedalam pompa injeksi dan diteteskan kedalam larutan NaOH 2 M hingga terbentuk butiran hitam.
didiamkan selama 1 malam, kemudian disaring dicuci
dengan akuades dan dikeringkan.
3.5.7. Preparasi Air Sungai Belawan dengan Metode Destruksi Basah
Gambar 3.7 Preparasi Air Sungai Belawan dengan Metode Destruksi Basah 100 mL Air Sungai Belawan
dimasukkan kedalam Beaker glass,
ditambahkan 5 mL HNO3 pekat
dipanaskan hingga setengah volume awal diatas hotplate
didinginkan dan disaring dengan kertas saring diencerkan kedalam labu takar 100 mL
3.5.8. Proses Adsorpsi Logam pada Air Sungai Belawan dengan Kitosan CuO
Gambar 3.8 Proses Adsorpsi Logam Pada Air Sungai Belawan dengan Komposit Kitosan CuO
BAB 4 50mL Air Sungai Belawan setelah
didestruksi
dimasukkan kedalam kolom yang telah berisi 15 g kitosan CuO,
didiamkan selama 15, 30, 45, 60, 75 menit, kemudian dibuka tutup kolom dan ditampung dengan botol vial
HASIL DAN PEMBAHASAN
4.1. Hasil Penelitian 4.1.1. Preparasi sampel
Pada penelitian ini air sungai belawan sebagai sampel memiliki warna kuning
kecoklatan agak keruh di distruksikan dengan larutan HNO3. Kemudia mengukur absorbansi dengan menggunaka ICP-OES pada panjang gelombang tertentu.
Konsentrasi sampel yang baku yang didapat kemudian dibandingkan dengan
konsentrasi sampel air yang menggunakan kitosan CuO.
4.1.2. Pembuatan Kitosan CuO
Larutan kitosan dalam beaker gelas ditambah kan Cu(NO3)2 0,5 M larutan dengan rasio (2:1) maka dlarutan kitosan mengental kemudian dimasukkan kedalam pompa
injeksi diteteskan kelarutan NaOH 2M hingga terbentuk butiran hitam.
Cu(NO3)2 (aq) + 2NaOH(aq)→ Cu(OH)2 + 2 NaNO3(aq)
Cu(OH)2 (l)→ CuO (s) + H2O (l)
Kemudian didiamkan selama 24 jam kemudian disaring dan dicuci dengan aquades
3
Gambar 4.1. Spektrum FT-IR Kitosan Komersil
Tabel 4.1. Data FT-IR Kitosan Komersil
Bilangan Gelombang ( cm-1) Gugus Fungsi
3
Spektrum dan data FT-IR pada kitosan CuO dapat dilihat pada gambar 4.2 dan tabel
4.2 berikut.
Gambar 4.2 Spektrum FT-IR Kitosan CuO
Tabel 4.2. Data Spektrum FT-IR Kitosan CuO
Bilangan Gelombang ( cm-1) Gugus Fungsi
3443,83
1635,61
1458,99
1095,95
O-H tumpang tindih dengan N-H
C=O stretching
N-Cu
4.1.4. Data Konsentrasi Logam Pada Air Sungai belawan Dengan Menggunakan ICP-OES
Data konsentrasi logam pada air sungai dapat dilihat pada tabel 4.1 dibawah ini
Tabel 4.3. Data konsentrasi logam pada air sungai Belawan
4.1.5. Data Konsentrasi Logam Pada Air Sungai Sunggal Setelah Penambahan Kitosan CuO Dengan Menggunakan ICP-OES
Data konsentrasi logam pada air sungai sunggal setelah penambahan kitosan CuO
dapat dilihat pada tabel dibawah ini
Tabel 4.4. Data Konsentrasi Logam Pada Air Sungai Belawan Setalah
0,03981 0,10518 0,01976
30 0,02875 0,07464 0,00525
45 0,01530 0,03136 0,00509
60 0,01846 0,04137 0,00513
75 0,02071 0,04009 0,00811
No Parameter Konsentrasi(mg/L) Baku Mutu
1. Besi(Fe) 0,05051 0,3
2. Mangan (Mn) 0,3251 0,1
4.1.6. Data Persentase Penurunan Konsentrasi Logam Pada Air Sungai Sebelum Dan Setelah Penambahan Kitosan CuO dengan Menggunakan ICP-OES (Penentuan Persen (%) Adsorpsi)
Persentasi penurunan konsentrasi logam pada air sungai sebelum dan setelah di
adsorpsi dapat ditentukan dengan menggunakan persamaan berikut:
%Adsorpsi =
Dari data hasil pengukuran yang terdapat pada tabel 4.1 dan 4.2 maka penentuan %
adsorpsi dapat dihitung sebagai berikut:
%Adsorpsi =
= 91,799%
Berdasarkan perhitungan diatas dapat diproleh persentasi penurunan sebagai berikut :
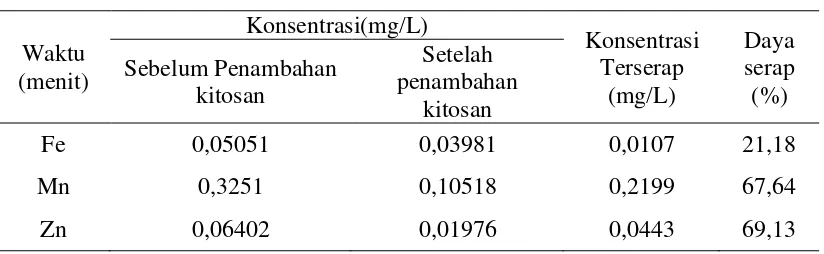
Tabel 4.5. Data Penurunan Persentase Konsentrasi Logam Pada Air Sungai Sebelum Dan Setelah Di Adsorpsi Pada Waktu 15 Menit
Logam
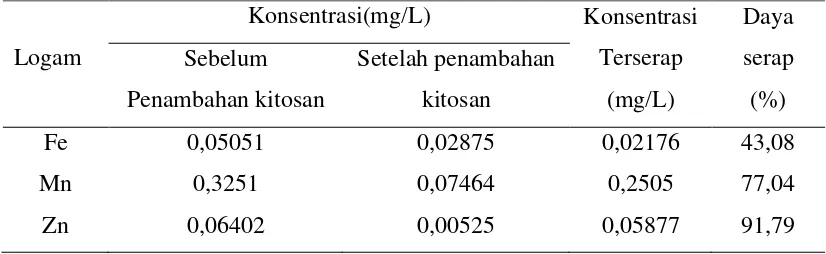
Tabel 4.8. Data Penurunan Persentase Penurunan Konsentrasi Logam Pada Air Sungai Sebelum Dan Setelah Di Adsorpsi Pada Waktu 60 Menit
Logam
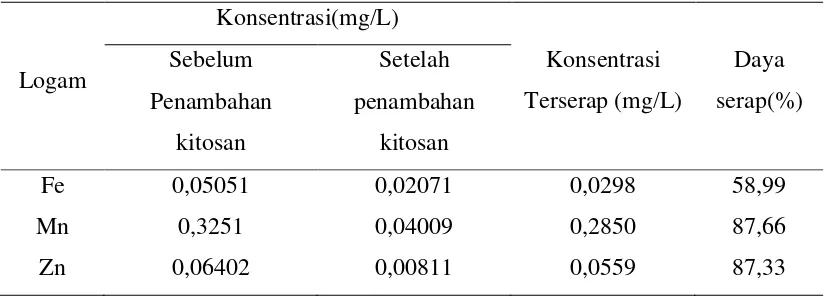
Tabel 4.9. Data Penurunan Persentase Penurunan Konsentrasi Logam Pada Air Sungai Sebelum Dan Setelah Di Adsorpsi Pada Waktu 75 Menit
0
Gambar 4.3 Kurva Hubungan Antara Waktu Kontak Dengan Daya Serap
Kitosan CuO yang berwana hitam berbentuk butiran-butiran pasir di masukkan
ke dalam kolom sebanyak 15 g dan kemudian ditambahkan sampel terjadi gelembung-
gelumbung dan air sampel menjadi berwarna biru muda dan terbentuk endapan
kecoklatan kemudian setalah 15 menit disaring dan menghasilkan filtrat berwarna biru
muda bening dilakukan pengulangan yang sama pada rentang waktu 30 menit, 45
menit, 60 menit dan 75 menit. Kemudia di analisa dengan menggunakan ICP-OES.
Maka diperoleh absorbansi dan persen daya serap seperti pada 15 menit pertama data
tabel 4.9, pada menit 30 pada data table 4.10, pada menit 45 menit pada tabel 4.11,
menit ke 60 pada tabel 4.12 dan menit ke 75 pada tabel 4.13 . dapat dilihat hubungan
antara waktu kontak dan persen daya sarap yang dapat dlihat pada gambar 4.5 dimana
pada waktu kontak selama 45 menit mengalami kenaikan daya serap yang sangat
signifikan, sedangkan antara kontak waktu 45 menit menuju 60 dan 75 menit daya
serap menurun. terdapat perbedaan sedikit sedangkan pada logam Fe mengalami
4.2. Pembahasan 4.2.1. Analisa FTIR
FT-IR digunakan untuk memberikan informasi mengenai adanya perubahan gugus
fungsi yang terbentuk pada suatu senyawa tertentu yang menandakan telah terjadi
interaksi secara kimia. Hasil analisis spektrum infra merah dari kitosan komersil
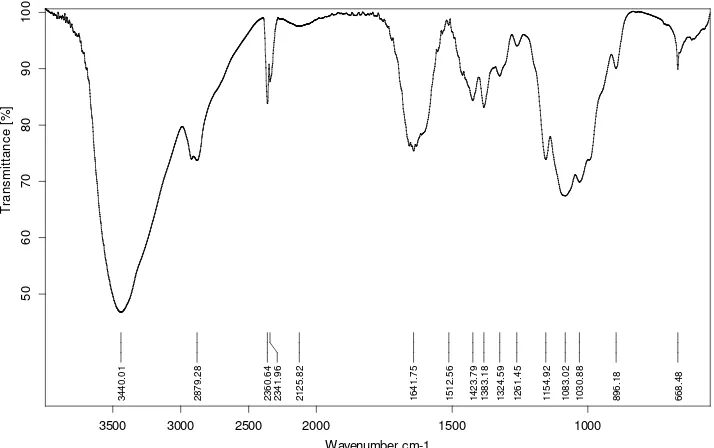
seperti pada gambar 4.3 diatas. Spektra FTIR dari kitin dan kitosan menunjukkan
gugus-gugus yang ada pada polimer-polimer tersebut. Pada kitosan terdapat ulur OH
pada bilangan gelombang 3440,01 cm-1 yang memunculkan pita lebar dengan intentitas yang kuat. Pada daerah bilangan gelombang ini seharusnya ulur N-H juga
muncul, tetapi karena tertutup oleh uluran OH yang lebih lebar maka ulur N-H tidak
dapat diamati. Adanya ulur N-H dapat diperjelas dengan adanya tekukan N-H pada
bilangan gelombang 1512,58 cm-1 . Serapan pada bilangan gelombang 2879,82 cm-1 merupakan rentang C-H dari metilen (-CH2) dari rantai utama kitin yang berbentuk
tembaga. Adanya uluran N-H yang terikat dengan tembaga diperjelas dengan adanya
tekukan yang mengalami pergeseran ke bilangan gelombang yang lebih kecil yaitu
4.2.2. Penyerapan Logam Dengan Kitosan CuO
Air sungai belawan yang di ambil dari kecamatan medan sunggal memiliki kadar
logam berat Fe 0,05051 mg/l, Mn 0,3252 mg/l dan Zn 0,06402 hasil menunjukkan
kadar logam Mn dan Zn berada diatas batas standar baku mutu SNI 7387-2009, pada
logam Fe tidak melebihi standar baku mutu. Namun pada uji pendahuluan pada air
PDAM Fe dan Zn berada diatas batas standar baku mutu. Pada pengolahan air PDAM
dengan menggunakan chlorin dan kaporit masih belum akurat untuk menurunkan
kadar logam Fe dan Zn.
Kitosan dipilih sebagai bahan pengikat untuk logam tembaga karena
ketersediaannya yang sangat berlimpah di alam serta karakteristiknya yang merupakan
hidrophilik, biokompatibel, biodegredabel, non toksik dan sifat adsorben yang sangat
baik untuk logam berat dimana gugus amino dan hidroksil pada kitosan dapat berperan
sebagai gugus aktif untuk proses adsorbsi. Digunakan kitosan dari cangkang
belangkas hal ini dikarenakan cangkang belangkas memiliki derajat deasetilasi sebesar
99,31 % dimana derajat deasetilasi kitosan dari cangkang belangkas ini dapat dihitung
dari data FTIR yang diperoleh dengan menggunakan metode base line dengan berat
molekul kitosan 1048000 g/mol. Semakin tinggi derajat deasetilasi kitosan maka
semakin baik material yang dibentuk.
Dalam adsorbsi logam dengan komposit kitosan CuO pada air sungai diperoleh Fe
69,71%, Mn 90,35%, Zn 92,05%. Dengan memvariasikan waktu , karena Lamanya
perendaman merupakan lama kontak larutan kitosan dengan air sungai yang juga
sangat mempengaruhi proses adsorbsi logam. Lama perendaman memberikan waktu
gugus amino dalam mengikat logam Fe, Mn dan Zn . Semakin lama waktu
perendaman dengan larutan kitosan, maka semakin banyak kadar ion logam berat yang
diikat gugus amino. Namun berdasarkan hasil penelitian menunjukkan jika pada lama
perendaman 45 menit lebih efektif daya serap yang dihasilkan pada Mn 90,35% dan
Zn 92,05%. Pada logam Fe daya serap yang dihasil 69,71% namun tetap terjadi
penurun kadar logam. Larutan kitosan mencapai titik optimum pada lama perendaman
mengalami penurunan. Jika Dalam adsorpsi telah tercapai massa optimum, maka
selanjutnya tidak akan terjadi kenaikan atau penurunan adsorpsi, akan tetapi bersifat
statis dan relatif konstan.
Pada proses adsorpsi dengan waktu 60 menit dan 75 menit, terjadi penurunan
persentase adsorpsi, diduga karena gugus amin dan hidroksil yang terdapat pada
kitosan sudah penuh mengikat komponen lain (H+ ) atau sudah jenuh. Pada kondisi adsorpsi yang terlalu lama, kemungkinan ion logam yang sudah terikat oleh adsorben
(kitosan) dapat terlepas lagi atau terjadi desorpsi (Khotimah dkk, 2010). Atau
kemungkinan lain disebabkan juga oleh suhu percobaan yang rendah (suhu kamar),
sehingga ikatan yang terjadi bersifat ikatan lemah. Selain itu perubahan pH larutan
menjadi naik kemungkinan dapat terjadi karena kontak dengan kitosan. Semakin lama
proses adsorpsi berlangsung, maka larutan akan semakin basa, sehingga daya adsorpsi
kitosan menurun dan semakin tidak efektif.
Pada hasil penelitian diperoleh logam Zn memiliki daya serap yang paling
besar, dikarekana Berdasarkan sifat sistem periodik unsur Tembaga, Besi, mangan
dan zink berada dalam periode yang sama yaitu periode empat. Sifat dari unsur logam
Zn dibandingkan dengan unsur logam Cu, Fe dan mangan sifat unsur Zn memiliki
energi ionisasi lebih besar, karena semakin ke kanan gaya tarik inti makin kuat, sifat
keelektronegatifan Zn lebih besar dan kereaktifannya lebih reaktif dibandingkan unsur
logam Mn dan Fe, sehingga Zn mudah bereaksi dengan kitosan CuO.
Pada logam Mn dan Fe diperoleh adsorbsi Mn lebih tinggi dibandingkan Fe.
Jika berdasarkan sifat unsur logam seharusnya unsur logam Fe lebih tinggi
dibandingkan Mn. Karena posisi unur logam Fe terletak disebalah kanan unsur
logam Mn dimana energi ionisasi unsur logam Fe lebih besar, karena semakin ke
kanan gaya tarik inti makin kuat, sifat keelektronegatifan lebih besar dan
kereaktifannya lebih reaktif dibandingkan unsur logam Mn . Namun pada hasil
O
Gambar 4.4 (a) Bentuk Ikatan Kitosan Komposit CuO (b) Bentuk Ikatan Antara Kitosan Komposit CuO dengan Air
Reaksi diatas merupakan reaksi ion logam Cu2+ yang terikat dengan kitosan. Dimana
pada reaksi (a) merupakan bentuk “jembatan” yang menggambarkan koordinasi ion
logam dengan beberapa kelompok amino dengan rantai polimer yang sama ataupun
yang berbeda. Pada gambar 4.4 (b) yaitu bentuk “liontin” dimana ion logam hanya
beraksi dengan satu kelompok amino.
Menurut Hirano (1986) dalam Meriatna (2008) kemampuan kitosan sebagai
adsorben logam- logam berat karena adanya sifat-sifat kitosan yang dihubungkan
dengan gugus amino dan hidroksil yang terikat, sehingga menyebabkan kitosan
mempunyai reaktivitas kimia yang tinggi dan menyebabkan sifat polielektrolit kation.
Akibatnya kitosan dapat berperan sebagai penukar ion (ion exchanger) dan dapat
berperan sebagai adsorben terhadap logam berat Fe, Mn dan Zn. Gugus amino
merupakan kation yang mampu berikatan dengan logam berat . Gugus amino sebagai
chealating agent akan mengikat logam berat Fe, Mn dan Zn yang terdapat pada air
sungai. Logam berat yang terikat dengan gugus amino (NH2), yang mana pada kondisi tersebut logam berat bersifat stabil. Sehingga sifat toksik logam Fe, Mn dan Zn akan
berkurang. Menurut Negm and Hanan (2010), menyebutkan jika sifat elektronegatif
Interaksi kitosan dengan ion logam terjadi karena proses pengkompleksan dimana
penukaran ion, penyerapan dan pengkhelatan terjadi selama proses berlangsung. Ketiga
proses tersebut tergantung dari ion logam masing-masing. Kitosan menunjukkan afinitas
yang tinggi pada logam transisi golongan 3 (Muzzarelli, 1973). Kitosan memiliki
kemampuan mengikat logam dengan membentuk kompleks logam- kitosan. Elektron dari
nitrogen yang terdapat pada gugus aminanya dapat membentuk ikatan kovalen koordinasi
dengan ion-ion logam transisi. Kitosan berperan sebagai donor elektron pada ion-ion
logam transisi ( E. Guibal,2004).
Kitosan dapat digunakan ketika tingginya kadar logam yang akan diserap
seperti pada limbah-limbah industri. Dan adsorben dari kitosan termodifikasi mampu
digunakan kembali sampai berulang kali dengan kemampuan adsorpsi yang tidak
berubah. Namun, pada penyerapan logam berat menggunakan kitosan membutuhkan
BAB 5
KESIMPULAN DAN SARAN
5.1. Kesimpulan
Dari penelitian ini dapat disimpulkan bahwa
1. Kadar logam berat yang terdapat pada air sungai Belawan yaitu logam Fe diperoleh 0,05051 mg/l, logam Mn 0,3251 mg/l, dan logam Zn 0,06402. Setelah menggunakan
kitosan kadar logam menurun dengan daya serap Fe 69,71%, Mn 90,35%, Zn 92,05%. 2. Lama perendaman kitosan CuO berpengaruh nyata terhadap penurunan kadar
logam berat Fe, Zn dan Mn air sungai Belawan. Untuk perlakuan perendaman
terbaik, yaitu 45 menit dengan daya serap Fe 69,71%, Mn 90,35%, Zn 92,05%.
5.2. Saran
1. Dapat diteliti lebih lanjut terhadap efisiensi penyerapan adsorben kitosan CuO pada