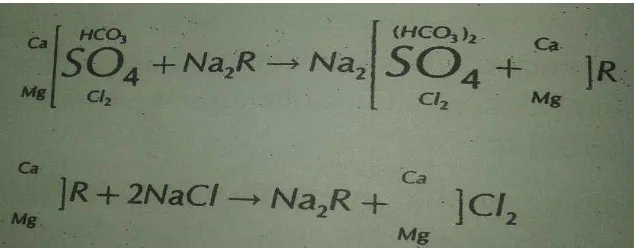TUGAS UTS TAKE HOME
MK PENGOLAHAN AIR MINUM
(3 SKS)
Disusun Oleh :
Achmad Rizki Azhari
NIM. 25010113140258
FAKULTAS KESEHATAN MASYARAKAT
UNIVERSITAS DIPONEGORO
1. Karakteristik Sumber Air Baku dan Permasalahannya
Beberapa masalah kualitas air baku adalah sebagai berikut: (Tri Joko, 2010) a. Masalah kualitas dari parameter bau:
Bau tanah Bau besi Bau sulfur Bau lainnya
b. Masalah kualitas dari parameter rasa: Rasa asin atau payau
Rasa besi
Rasa tanah tanpa kekeruhan Rasa lainnya
c. Masalah kualitas dari parameter kekeruhan: Kekeruhan sedang, coklat dari lumpur Kekeruhan tinggi, coklat dari lumpur Kekeruhan berwarna putih
Kekeruhan berwarna sedikit kuning setelah air berada sebentar di dalam ember
d. Masalah kualitas dari parameter warna: Cokelat tanpa kekeruhan
Cokelat bersama dengan kekeruhan Warna utih
Warna lainnya
A. Karakteristik dan Permasalahan Sumber Air Baku Permukaan
Karakteristik dan permasalahan air baku permukaan yang ada di Indonesia secara umum digolongkan menjadi: (Tri Joko, 2010)
A. Air permukaan dengan tingkat kekeruhan tinggi
Air permukaan ini telah mengalir pada permukaan tanah yang rentan terhadap erosi atau ditutupi dengan vegetasi yang rendah kerapatannya. B. Air permukaan dengan tingkat kekeruhan rendah sampai sedang
Air ini pada umumnya mempunyai sifat stabil di danau atau waduk yang sedikit mengandung gulma atau tanaman air seperti halnya air pada golongan pertama, hanya saja telah mengalami pengendapan yang cukup lama dengan waktu tinggal lebih dari satu minggu.
C. Air permukaan dengan tingkat kekeruhan yang sifatnya temporer Air yang mengalir di atas permukaan yang tertutup vegetasi cukup rapat dan curam akan mengahsilkan air keruh ssat musim hujan dan jernih saat tidak hujan. Saat hujan terjadi erosi sedimentasi setelah debit dan kecepatan air meningkat tajam. Tingkat kekeruhan yang tinggi hanya terjadi beberapa saat, 2-3 jam setelah hujan reda air
kembali ke aliran dasar “base flow” dan air kembali jernih. Air sungai
D. Air permukaan dengan kandungan warna yang sedang sampai tinggi Air ini umumnya telah mengalir pada daerah dengan tingkat humus tinggi atau gambut. Pada umumnya air mempunyai tingkat warna di atas 20 PtCo sebagai akibat terlarutnya zat tannin dari sisa-sisa humus. Biasanya pH air bersifat asam (4-7). Air ini mempunyai tingkat kekeruhan dan warna tinggi.
E. Air permukaan dengan tingkat kesadahan tinggi
Kesadahan pada prinsipnya adalah terkontaminasinya air oleh unsur kation seperti Ca, Mg, Na dan sebagainya. Air sadah tinggi mengalir pada daerah bebatuan kapur. Kesadahan dapat dikatakan tinggi dan mulai berakibat pada alat-alat masak adalah di atas 100 mg/l CaCO3. Kesadahan di atas 300 mg/l bila dikonsumsi secara terus menerus akan merusak ginjal manusia.
F. Air permukaan dengan kekeruhan sangat rendah
Air permukaan dengan tingkat kekeruhan sangat rendah dapat dijumpai pada danau-danau yang masih belum tercemar atau air yang baru keluar dari mata air.
B. Karakteristik dan Permasalahan Sumber Air Tanah
Permasalahan pada air tanah (dangkal dan dalam) yaitu: (Tri Joko, 2016) Jumlah sumur yang berkualitas buruk sedikit dan lokasi tersebar Hampir semua sumur pedesaan berkualitas buruk
Rasa asin atau payau pada air
Kekeruhan tinggi pada sumur gali dan sumur pompa tangan (SPT) Air mengandung kadar besi dan atau mangan
Air berwarna dan berbau
2. Kategori Partikel dalam Air dan Sifat-Sifatnya
Jenis-jenis partikel yang dapat ditemukan pada air permukaan dan air tanah yaitu inorganik, organic, dan partikel biologis. (AWWARF dan IWSA, 1997). Gambaran dari tiga komposisi utama partikel tersedia di bawah ini: (AWWA, 2011)
Mayoritas partikel organik dalam air alami adalah hasil dari degradasi tanaman dan hewan bahan. Kandungan organic tersebut dapat diklasifikasikan sebagai bahan organik alami/Natural Organic Matter
(NOM). NOM dalam air alami/natural water terdiri dari lebih banyak partikel tersuspensi dan molekul NOM larut.
Partikel biologis termasuk mikroorganisme seperti virus, bakteri, dan protozoa. Mikroorganisme ini masuk air melalui debit langsung dari air limbah, limpasan dari daerah aliran sungai, atau kotoran hewan, dan beberapa dapat tumbuh dan berkembang dalam badan air. Mikroorganisme juga dapat melekat pada partikel bahan tersuspensi. Tipe lain dari partikel biologis adalah ganggang, yang menggunakan nutrisi mineral (nitrogen dan fosfor) dan fotosintesis untuk tumbuh.
3. Prinsip-Prinsip Pengolahan Air Minum
Prinsip-prinsip pengolahan air minum secara umum, yaitu: (WHO, 2006) a) Menghilangkan atau menonaktifkan kontaminan mikroba (bakteri, virus,
protozoa)
b) Menghilangkan kontaminan kimia (inorganic dan organic)
c) Menghilangkan kontaminan estetis (rasa yang tidak diinginkan, bau, warna, kekeruhan)
Prinsip-prinsip tujuan pengolahan air minum secara proses, yaitu: (Tri Joko, 2010)
a) Pengolahan fisik
Bertujuan untuk mengurangi/menghilangkan kotoran-kotoran besar, penyisihan lumpur dan pasir, mengurangi zat-zat organic yang ada pada air yang akan diolah, dan mengolah air tanpa zat kimia
b) Pengolahan kimia
Bertujuan untuk membantu proses pengolahan selanjutnya, misalnya pembubuhan tawas membantu mengurahi kekeruhan air.
c) Pengolahan biologi
Bertujuan untuk membunuh/memusnakan bakteri-bakteri terutama bakteri penyebab penyakit yang terkandung dalam air.
4. Contoh Data Kualitas Air Baku
Tabel 1. Kualitas air salah satu muara sungai Tallo, Makassar (Latif, 2012)
(TSS)
5. Pengolahan Air Minum Sumber Air Baku Sungai Tallo A. TDS Melebihi Batas Maksimum
Pengolahan air dengan TDS yang tinggi dapat dilakukan dengan metode destilasi dan reverse osmosis.(Extension, 2010a)
Destilasi (Extension, 2010b)
Destilasi adalah salah satu proses pengolahan air tertua. Air direbus dan uap yang dihasilkan dikumpulkan dan didinginkan dalam wadah (chamber) terpisah. Air hasil olahan disebut air suling yang relatif bebas dari banyak kontaminan. Distilasi biasanya menghilangkan lebih dari 99,9 persen dari bahan terlarut, sehingga membuat air bersifat korosif dan tanpa mineral. (Extension, 2010b)
Metode ini efektif menangani beberapa logam berat, padatan terlarut, beberapa bakteri dan virus, bahan anorganik seperti nitrat, natrium, fluoride, dan sulfat, dan beberapa bahan kimia organik beracun yang terdapat dalam air baku. Tetapi tidak efektif untuk mengolah air yang mengandung kebanyakan senyawa volatil dan semivolatile organik (VOC), dan beberapa bakteri. (Extension, 2010b)
Reverse Osmosis
Reverse osmosis memerlukan tekanan tinggi sekitar 10-60 bar dalam pengoperasiannya sehingga dapat mengatasi tekanan osmotic dan tekanan hidrolik membrane. (Tri Joko, 2010).
Reverse osmosis efektif untuk menangani kontaminan anorganik dalam air seperti: garam terlarut dari natrium, besi terlarut (ferrous), nitrat, lead, fluoride, sulfat, kalium, mangan, aluminium, silika, klorida, total padatan terlarut, kromium, dan ortofosfat. Juga efektif dalam menghilangkan beberapa deterjen, beberapa rasa, warna dan bau akibat bahan kimia, kontaminan organik tertentu, dan beberapa pestisida. Tetapi metode ini tidak efektif menangani gas-gas terlarut, kebanyakan kontaminan organik yang mudah menguap dan semi-volatile termasuk beberapa pestisida dan pelarut. Unit reverse osmosis tidak dianjurkan secara tunggal untuk treatment bakteri dan organisme mikroskopis lainnya. (Extension, 2010c)
B. DO Tidak Mencapai Batas Minimum
Metode yang digunakan untuk mengatasi kekurangan O2 terlarut dalam air adalah aerasi. Aerasi merupakan proses pengolahan air dengan cara mengontakkan air dengan udara. Proses aerasi pada dasarnya adalah untuk memberikan oksigen ke dalam air atau meningkatkan kandungan oksigen terlarut dalam air. (Tri Joko, 2010).
C. Fecal Coliform ataupun Total Coliform Melebihi Batas Maksimum Disinfeksi adalah usaha untuk mematika mikroorganisme yang masih tersisa dalam proses, terutama ditjukan kepada mikroorganisme yang bersifat pathogen. Terdapat bermacam-macam cara desinfeksi: (Tri Joko, 2010)
Kimia : Larutan kaporit, gas chloor, dan gas ozon Fisika : Gelombang mikro, ultraviolet
Untuk membunuh mikroorganisme yang bersifat pathogen tekandung di dalam air, misalnya adalah mikroba E. Colli (tergolong jenis bakteri coliform fecal). Bahan berupa kaporit, bromin klorida, gas klor, gas iod, ozon, dan kalium permanganate. Desinfektan yang sering digunakan adalah kaporit, gas klor, dan sinar ultra. (Tri Joko, 2010).
6. Pengolahan Air Minum Terhadap Beberapa Indikator A. Pengolahan Terhadap Kesadahan
Kesadahan disebabkan oleh ion-ion bervalensi +2 terutama ion calcium dan magnesium. Ion calcium dan magnesium terlarut dari batuan kapur, dolomite, dan mineral-mineral lainnya. Efek dari kesadahan meningkatkan pemakaian sabun, tertutupnya pori kulit, merubah warna porcelain. (Tri Joko, 2010).
kalsium, dan magnesium, sedangkan kesadahan sementara disebabkan oleh karbonat dan bikarbonat.
Proses ini bertujuan untuk menghilangkan kesadahan air. Kesadahan dalam air disebabkan oleh ion calcium dan magnesium hasil kontak air dengan system dengan susunan geologi. (Tri Joko, 2010).
Dua metode dasar yang digunakan yaitu proses kapur soda dan proses pertukaran ion. Pelunakan presipitasi menggunakan kapur (CaO) dan soda abu (Na2CO3) untuk menghilangkan calcium dan magnesium dari larutan. Pelenuakan dengan memakai ion penukar (ion exchange) menggunakan rezin untuk menghilangkan ion bivalen dan menggantikannya dengan ion sodium. (Tri Joko, 2010).
1. Proses kapur soda
Pada proses kapur soda, kapur [Ca(OH2)] dan abu soda (NaCO3) ditambahkan ke air, akan bereaksi dengan garam calcium dan magnesium membentuk endapan kalsium karbonat (CaCO3) dan magnesium hidroksida [Mg(OH)2], reaksi kimiawi yang umum adalah: Ca(HCO3)2 + Ca(OH)2 2CaCO3 + 2H2O
Mg(HCO3)2 + 2Ca(OH)2 2CaCO3 + Mg(OH)2 + 2H2O MgSO4 + Ca(OH)2 Mg(OH)2 + CaSO4
CaSO4 + NaCO3 CaCO3 + Na2SO4 2. Proses pertukaran ion (ion exchange)
Suatu perangkat pertukaran ion mirip dengan suatu filter pasir yang medium filternya berupa suatu getah pertukaran ion R, yang dapat bersifat alamiah (zeolite) atau sintesis. Bila air sudah melewati filter penukar ion tersebut maka akan terjadi suatu pertukaran kation: kalsium dan magnesium di dalam air diperuntukkan dengan sodium di dalam getah tesebut. (Tri Joko, 2010).
Gambar 1. Reaksi Pertukaran Ion R, Ca, dan Mg (Tri Joko, 2010)
Terdapat beberapa proses yang termasuk pertukasin ion: Kation exchange: pertukaran antara ion positif Anion exchange: pertukaran antara ion negative
Keleman dari metode penghilangan kesadahan ini adalah menghasilkan konsentrasi sodium yang mungkin berbahaya bagi orang yang sakit jantung. (Tri Joko, 2010).
B. Pengolahan Terhadap Besi dan Mangan
Metode yang sering digunakan untuk menghilangkan besi dan mangan, yaitu: 1) Oksidasi dan presipitasi; 2) Penambahan bahan-bahan kimia serta filtrasi; dan 3) Pertukaran ion. (Tri Joko, 2010).
Diantara reaksi tersebut yang sering digunakan yaitu reaksi oksidasi: 4Fe (HCO3)2 + O2 + 2H2O 4Fe(OH)3 + 8CO2
Besi dalam bentuk ferrous (+2) dioksidasi menjadi ferric hidroksida terlarut yang dapat dihilangkan melalui presipitasi.
Besi ferro (Fe++) dan mangan manganous (Mn++) adalah terlarut, bentuk yang tidak terlihat, mungkin terdapat dalam air sumur atau air yang anaerobic. Apabila kontak dengan udara, bentuk ini teroksidasi berubah perlahan menjadi bentuk yang tidak larut, bentuk kelihatan nyata, besi teroksidasi, ferri (Fe++++) dan mangan manganic (Mn++++). Besi dan mangan teroksidasi tersebut dapat seluruhnya dihilangkan dengan proses pengendapan dan penyaringan. (Tri Joko, 2010).
Sementara besi dan mangan teroksidasi secara kimiawi oleh system chlor bebas atau potassium permanganate pada tingkat oksidasi, lebih besar dari pada oksigen terlarut. (Tri Joko, 2010).
Apabila chlor digunakan, sisa chlor bebas yang ada dipertahankan melalui proses pengolahan. Penyaringan yang efektif mengikuti aerasi atau oksidasi kimiawi adalah penting bila sejumlah floculant oksida metal tidak cukup berat untuk mengendap dengan cara gravitasi. (Tri Joko, 2010).
C. Pengolahan Terhadap CO2 Agresif
CO2 agresif merupakan bentuk karbondioksida yang paling berbahaya kadar CO2 agresif yang tinggi dapat menyebabkan kerusakan pada logam-logam dan beton. (Tri Joko, 2010). Cara yang dilakukan untuk menghilangkan CO2 di dalam air yaitu dengan metode oksidasi dengan udara (aerasi).
Aerasi merupakan proses pengolahan air dengan cara mengontakkan air dengan udara. Aerasi secara luas telah digunakan untuk mengurangi kandungan zat padat dan gas terlarut dalam air. Aerasi adalah pencampuran udara dengan air sehingga terjadi perubahan konsentrasi zat-zat yang mudah menguap di dalam air. Dengan tersedianya oksigen terlarut dapat meningkatkan karateristik fisik dan kimia air. (Tri Joko, 2010).
Proses aerasi pada dasarnya adalah untuk memberikan oksigen ke dalam air atau meningkatkan kandungan oksigen terlarut dalam air, diantaranya bertujuan untuk: (Tri Joko, 2010)
Menghilangkan CO2 yang terlarut dalam air, dengan cara melepaskan CO2 ke udara, dengan proses ini sekaligus menaikkan pH air
Menghilangkan gas amoniak (NH3); H2S dengan kondisi tertentu b) Proses oksidasi, contoh pada proses penghilangan besi dan mangan
terlarut menjadi besi endapan (tersuspensi halus) dengan proses oksidasi dengan oksigen
7. Fungsi Unit-Unit Pengolahan Air A. Screening
Tahap awal unit pemurnian yaitu air baku (air permukaan) melewati layar/screen logam untuk mencegah organisme hidup berukuran besar dan puing-puing mengambang seperti tongkat, daun dan sampah masuk ke dalam sistem pengolahan, tetapi memungkinkan air baku (air permukaan) untuk melewati screen tersebut. (Waterwise, 2011)
Gambar 2. Screening Air Permukaan (Waterwise, 2011)
B. Pra-Sedimentasi
Pra-sedimentasi dimaksudkan untuk menangkap benda kasar yang mudah mengendap yang terkandung dalam air baku seperti pasir atau dapat juga disebut partikel diskret. Partikel diskret merupakan partikel yang tidak mengalami perubahan bentuk selama proses pengendapan. Unit ini dapat dilengkapi penangkap minyak dan lemak bila diperlukan. (Tri Joko, 2010).
Gambar 3. Bak Pra Sedimentasi
(Sumber: http://www.panoramio.com/photo/37650485)
C. Koagulasi
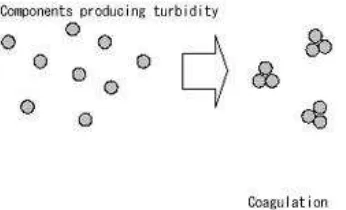
Koagulasi adalah penambahan koagulan (aluminium sulfat/tawas, natrium aluminat, ferro sulfat, ferri chlorida) ke dalam air baku diikuti dengan pengadukan cepat yang bertujuan untuk mencampur antara koagulan dengan koloid. Koagulasi berfungsi untuk mempermudah butiran ukuran halus (missal berdiameter 0,06 mm) yang sangat lama mengendap dalam unit sedimentasi dan koloid-kolid yang bermuatan listrik yang selalu bergerak-gerak serta tidak dapat diendapkan secara gravitasi untuk mengendap. (Tri Joko, 2010).
Partikel-partikel yang sangat halus atau koloid bersifat stabil dalam air dinon satabilkan muatan permukaannya dengan zat koagulan sehingga terjadi gaya tarik-menarik membentuk flok-flok yang dapat dipisahkan dengan air melalui proses sedimentasi. Untuk meratakan pencampuran zat koagulan dan pembentukan flok (mikrofloak) dilakukan proses pengadukan cepat dan pengadukan lambat. (Tri Joko, 2010).
Pengadukan yang memanfaatkan gaya hidrolisis air (biasa disebut pengadukan hidrolisis) yang biasa dipakai untuk debit air di atas 50 liter/detik adalah dengan terjunan air. Pembubuhan koagulan dilakukan sesaat sebelum air diterjunkan sehingga air yang terjun sudah mengandung koagulan yang siap diaduk. (Tri Joko, 2010).
(Sumber: http://apec-vc.or.jp/e/modules/tinyd00/?id=57&kh_open_cid_00=8)
Gambar 5. Ilustrasi Koagulasi
(Sumber: http://apec-vc.or.jp/e/modules/tinyd00/?id=57&kh_open_cid_00=8)
D. Flokulasi
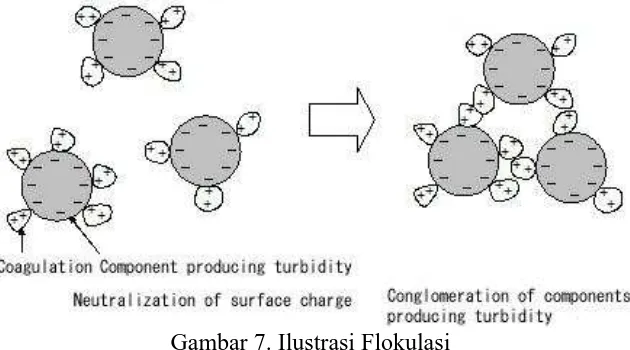
Flokulasi secara umum disebut juga pengadukan lambat, dimana dalam unit ini berlangsung proses terbentuknya penggumpalan flok-flok yang lebih besar dan akibat adanya perbedaan berat jenis terhadap air, maka flok-flok tersebut dapat dengan mudah mengendap di bak sedimentasi. (Tri Joko, 2010).
Flokulasi dilakukan setelah proses koagulasi. Flokulator berjalan dengan kecepatan lambat dengan maksud terjadi pembentukkan flok besar. Kecepatan air dalam bak pengaduk dijaga pada harga 15-30 cm/detik, agar tidak terjadi pengendapan maupun kerusakan flok yang telah terbentuk. (Tri Joko, 2010).
Gambar 6.Ilustrasi Perubahan Ukuran Partikel Sebelum dan Setelah Proses Flokulasi
Gambar 7. Ilustrasi Flokulasi
(Sumber: http://apec-vc.or.jp/e/modules/tinyd00/?id=57&kh_open_cid_00=8)
E. Sedimentasi
Proses sedimentasi secara umum diartikan sebagai proses pengendapan, dimana akibat gaya gravitasi, partikel yang mempunyai berat jenis lebih besar dari berat jenis air akan mengendap ke bawah dan jika lebih kecil berat jenisnya maka akan mengapung. Kecepatan pengendapan partikel akan bertambah sesuai dengan pertambahan ukuran partikel dan berat jenisnya. (Tri Joko, 2010).
Fungsi dari bangunan sedimentasi adalah untuk menyingkirkan beberapa macam partikel yang terkandung di dalam air yaitu: (Tri Joko, 2010)
1. Partikel terendapkan.
2. Partikel yang telah terkoagulasi seperti kekeruhan dan warna.
3. Hasil endapan dari proses presipitasi seperti hardness (CaCO3), besi, dan mangan.
4. Untuk memisahkan flok yang telah terbentuk dari sub unit flokulator sehingga mudah dibuang.
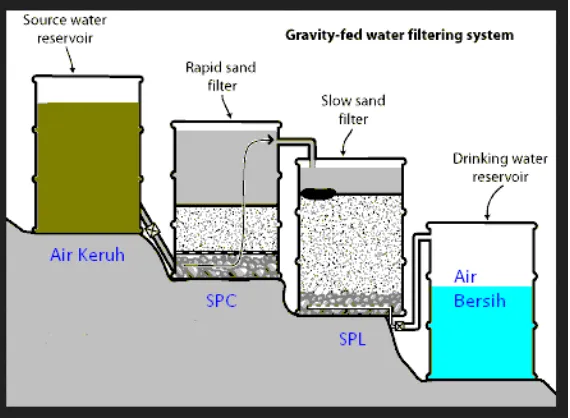
F. Saringan Pasir Cepat
Saringan pasir dapat menghasilkan air bersih sejumlah 1,3 – 2,7 liter/m3/detik, Diameter pasir yang digunakan 0,4 mm – 0,8 mm dengan ketebalan 0,4 – 0,7 m. Saringan pasir hanya mampu berfungsi untuk menahan bahan padat terapung dan tidak bias menyaring mikroorganisme seperti virus atau bakteri pathogen, sehingga diperlukan unit disinfeksi setelah pengolahan air dengan saringan pasir cepat. (Untung, 2008)
Gambar 8. Ilustrasi Arah Aliran Saringan Pasir Cepat dan Lambat (Sumber:http://www.nicofilter.co.id/sistem-dan-teknik-penjernihan-air-sederhana.html)
G. Desinfeksi
Desinfeksi adalah usaha untuk memetikan mikroorganisme yang masih tersisa dalam proses pengolahan air minum, terutama ditujukan kepada mikroorganisme pathogen. Terdapat bermacam-macam cara desinfeksi: (Tri Joko, 2010)
Kimia : Larutan kaporit, gas chloor, dan gas ozon. Fisika : Gelombang mikro, ultraviolet.
Untuk membunuh mikroorganisme yang bersifat pathogen tekandung di dalam air, misalnya adalah mikroba E. Colli (tergolong jenis bakteri coliform fecal). Bahan atau media desinfeksi berupa kaporit, bromin klorida, gas klor, gas iod, ozon, dan kalium permanganate. Desinfektan yang sering digunakan adalah kaporit, gas klor, dan sinar ultra. (Tri Joko, 2010).
Kemampuan dari desinfektan ini adalah sebagai berikut: (Tri Joko, 2010)
Menghilangkan bau Mematikan alga
Mengoksidasi Fe (II) menjadi Fe (III) sehingga konsentrasi di air turun.
Mengoksidasi Mn.
Mengoksidasi H2S menjadi H2SO4. Mengoksidasi nitrit menjadi nitrat
Mengoksidasi ammonia menjadi senyawa amin
Mengoksidasi phenol menjadi senyawa yang tidak berbahaya.
Klorin (Cl2) Kaliumpermanganate (KMnO4) Fenols
Alkohol
Sabun dan deterjen
Garam Kwartair amonium Hidrogen peroksida Beberapa asam dan basa
Untuk desinfeksi air secara fisik, desinfektan berikut dapat digunakan: (Lenntech, 2004)
Kesadahan disebabkan oleh ion-ion bervalensi +2 terutama ion calcium dan magnesium. Ion calcium dan magnesium terlarut dari batuan kapur, dolomite, dan mineral-mineral lainnya. Efek dari kesadahan meningkatkan pemakaian sabun, tertutupnya pori kulit, merubah warna porcelain. (Tri Joko, 2010).
Jenis-jenis kesadahan yaitu kesadahan tetap dan kesadahan sementara. Kesadahan tetap disebabkan sulfat, klorida, nitrat, silikat, kalsium, dan magnesium, sedangkan kesadahan sementara disebabkan oleh karbonat dan bikarbonat.
Water softening atau pelunakan air berfungsi untuk menghilangkan kesadahan air. Kesadahan dalam air disebabkan oleh ion calcium dan magnesium hasil kontak air dengan system dengan susunan geologi. (Tri Joko, 2010).
I. Oksidasi
Oksidasi berfungsi untuk menghilangkan besi dan atau mangan. Oksidasi yaitu menaikkan tingkat oksidasi oleh suatu oksidator (udara, khlorin, dan permanganat/KMnO4) dengan tujuan mengubah bentuk besi dan atau mangan terlarut menjadi besi dan atau mangan tidak terlarut (endapan). Endapan yang terbentuk dihilangkan dengan proses sedimentasi dan atau filtrasi. (Tri Joko, 2010).
Contoh reaksi oksidasi besi dan mangan dalam pengolahan air minum dengan oksidator berupa udara (O2) adalah sebagai berikut:
4Fe(HCO3)2 + O2 + 2H2O = 4Fe(OH)3- + 8CO2
Ferrous bicarbonate dan manganese bicarbonate merupakan bentuk besi dan mangan yang larut dalam air. Sehingga dengan penambahan O2 dalam air, dapat mengubah kedua bentuk tersebut menjadi ferric hidroksida dan manganese dioksida yang bersifat tidak larut air dan dapat dihilangkan dengan sedimentasi atau filtrasi. (GE Power, 2007).
J. Reduksi
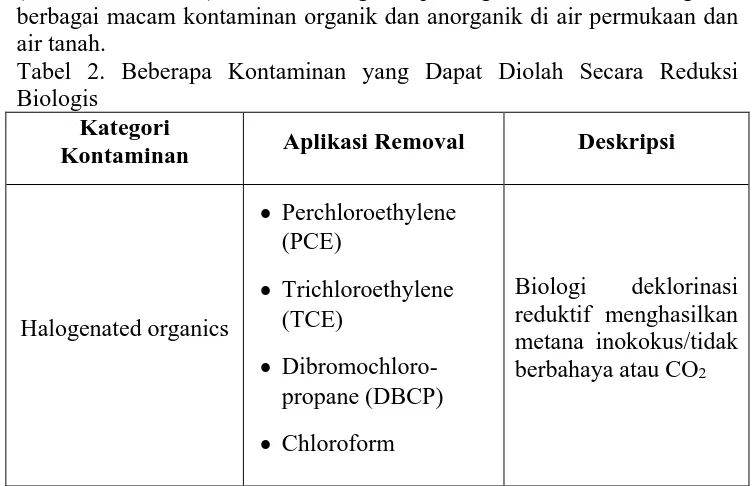
Reduksi digunakan untuk pengolahan air minum secara biologis (microbial biomass). Proses biologis dapat digunakan untuk mengatasi berbagai macam kontaminan organik dan anorganik di air permukaan dan air tanah.
Tabel 2. Beberapa Kontaminan yang Dapat Diolah Secara Reduksi Biologis
Kategori
Kontaminan Aplikasi Removal Deskripsi
Inorganics dapat mudah disaring atau diendapkan,
Bakteri memperoleh energi dan bereproduksi dengan mediasi transfer elektron dari senyawa pendonor (yaitu, senyawa yang mudah menyumbangkan elektron) ke senyawa teroksidasi (yaitu, senyawa yang siap menerima elektron). Sekali senyawa pendonor menyumbangkan elektron, maka electron tersebut melakukan perjalanan bolak-balik melintasi membran mitokondria sel dalam serangkaian reaksi oksidasi-reduksi internal. Pada akhirnya, elektron disumbangkan untuk senyawa penerima elektron terminal. Rangkaian reaksi, yang secara kumulatif dikenal sebagai rantai transpor elektron, menciptakan gradien elektrokimia di membran sel yang digunakan bakteri untuk menghasilkan adenosin trifosfat atau juga dikenal sebagai energi. (Brown, 2007).
Sebagai senyawa yang mendapatkan atau kehilangan elektron, mereka akan dikonversi ke bentuk yang berbeda, sering tidak berbahaya, yang termodinamikanya lebih stabil daripada senyawa aslinya. Contoh di bawah ini menggambarkan reaksi oksidasi-reduksi mikroba dimediasi antara asetat (donor elektron) dan oksigen terlarut dan nitrat (dua elektron lingkungan akseptor).
Proses pengolahan air minum biologis didasarkan pada pertumbuhan komunitas bakteri yang mampu menengahi reaksi oksidasi-reduksi yang melibatkan setidaknya satu sasaran kontaminan (Gambar 9). Proses biologis heterotrofik menggunakan donor elektron organik (misalnya, asam asetat), sedangkan proses biologis autotrophic menggunakan donor elektron anorganik (misalnya, hidrogen). (Brown, 2007).
Gambar 9. Mikroba Sebagai Mediasi Reaksi Oksidasi-Reduksi (Brown, 2007)
K. Preklorinasi
Pra-klorinasi adalah ketika klorin diterapkan untuk air segera setelah memasuki fasilitas pengolahan. Pada langkah pra-klorinasi, klorin biasanya ditambahkan langsung ke air baku (air untreatment yang memasuki fasilitas pengolahan), atau ditambahkan di flash mixer (mesin pencampuran yang cepat, dispersi seragam dari klorin). Klorin ditambahkan ke air baku untuk menghilangkan ganggang dan bentuk lain dari kehidupan aquatic dari air sehingga tidak akan menimbulkan masalah pada tahap selanjutnya dari pengolahan air. Pra-klorinasi di flash mixer dilakukan untuk menghilangkan rasa dan bau, dan mengendalikan pertumbuhan biologis seluruh sistem pengolahan air, sehingga mencegah pertumbuhannya dalam tangki sedimentasi dan media filtrasi. Penambahan klorin juga akan mengoksidasi besi apapun, mangan dan / atau hidrogen sulfida yang hadir, sehingga mereka juga dapat dihilangkan dalam sedimentasi dan filtrasi. (SDWF, 2008).
L. Netralisasi
Netralisasi adalah salah satu upaya agar pH air menjadi normal. Netralisasi dalam mengolah air gambut adalah mengatur pH air gambut yang bersifat asam (pH < 7) menjadi netral (pH 7-8) dengan cara pembubuhan alkali. Cara yang paling mudah dan murah adalah dengan membubuhkan CaO (kapur tohor) atau CaCO3 (batu gamping). Tujuan proses netralisasi adalah untuk membantu efektivitas proses selanjutnya, antara lain: (Said dan Widayat, 2010)
Pada proses oksisdasi dengan chlorine reaksi efektif pada pH 7–8,5 (80%), sedangkan pada pH <6 dan >8,5 hanya bereaksi < 40%.
Pada proses koagulasi dengan menggunakan alum akan afektif pada
pH ≥ 6.
Pengendapan semua logam akan terjadi pada pH ≥ 8,3; Fe pada pH 8 – 9 dan Mn pada pH 11.
Zat alkali dipakai untuk mengolah air dengan tujuan mengatur pH agar pH air menjadi netral agar proses flokulasi dan koagulasi dapat berjalan baik dan efektif. Zat-zat alkali yang sering digunakan adalah batu kapur (slake lime), soda abu, Na (HCO3). Batu kapur (slake lime) banyak digunakan karena harganya murah dan hasilnya baik. Tetapi mempunyai beberapa kekurangan yaitu kelarutan kecil dan dapat memperbesar kesadahan. (Said dan Widayat, 2010).
M.Aerasi
Aerasi adalah suatu bentuk perpindahan gas dan dipergunakan dalam berbagai bentuk variasi operasi meliputi: (Tri Joko, 2010)
1. Tambahan oksigen untuk mengoksidasi besi dan mangan terlarut 2. Pembuangan carbon dioksida
3. Pembuangan hydrogen sulfide untuk menghilangkan baud an rasa 4. Pembungan minyak yang mudah menguap dan bahan-bahan penyebab
bau dan rasa serupa yang dikeluarkan oleh ganggang serta mekroorganisme lain
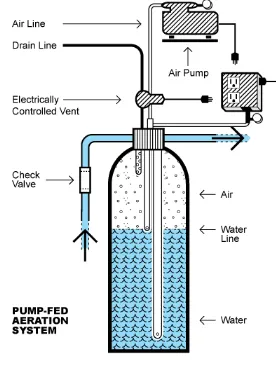
Aerator merupakan nama alat yang digunakan dalam proses aerasi. Aerator dibagi dalam dua kategori. Aerator memasukkan udara ke air, atau air ke udara. Metode air-dalam-udara yang dirancang untuk menghasilkan tetesan kecil air yang jatuh melalui udara. Metode udara-dalam-air menciptakan gelembung kecil udara yang disuntikkan ke dalam aliran air. Semua aerator dirancang untuk menciptakan sejumlah besar kontak antara udara dan air untuk meningkatkan transfer gas dan meningkatkan oksidasi. (MRWA, 2011)
Gambar 10. Aerator Udara-dalam-Air
Gambar 11. Aerator Air-dalam-udara
(Sumber: http://www.unh.edu/research/blog/2014/04/seeking-trial-participants-new-system-treat-drinking-water-disinfectant-products)
N. Saringan Pasir Lambat
Saringan pasir lambat adalah saringan yang menggunakan pasir sebagai media filter dengan ukuran butiran sangat kecil, namun mempunyai kandungan kuarsa yang tinggi. (Taweel dan Ali, 2000).
Proses filtrasi yang terjadi pada saringan pasir lambat, terjadi dengan memisahkan air dari kandungan kontaminan berupa partikel tersuspensi dan koloid, serta bakteri, dengan cara melewatkan air pada suatu media berpori. Pada prinsipnya material ini dapat berupa material apa saja, seperti lapisan granular pasir, batu yang dihancurkan, antrachite, kaca, sisa arang, dan lain-lain. Pada prakteknya di lapangan, media berpori yang paling sering digunakan adalah pasir, karena pasir mudah ditemui dalam jumlah banyak, biaya yang murah, dan hasil pengolahan yang diberikan juga sangat memuaskan. Effective size (ES) dari media pasir berkisar antara 0,15 mm – 0.35 mm. Kecepatan filtrasi dari saringan pasir lambat biasanya berkisar antara 0,1 – 0,3 m/jam (Longsdon et al., 2002). Secara keseluruhan penyisihan kontaminan dengan proses filtrasi merupakan kombinasi dari beberapa proses yang berbeda – beda, dan yang terpenting adalah mechanical straining, sedimentasi, dan adsorpsi, dan aktivitas biologi (Huisman, 1974).
Pengolahan dengan saringan pasir lambat pada umumnya tidak menggunakan bahan kimia sebagai pengolahan pendahuluan, sehingga air baku yang digunakan haruslah dalam kondisi yang sudah baik. Di bawah ini merupakan beberapa rekomendasi untuk air baku yang akan diolah dengan saringan pasir lambat tanpa menggunakan pengolahan pendahuluan berupa saringan pasir cepat: (Longsdon et al., 2002)
• Kekeruhan rendah, kurang dari 5 NTU
• Konsentrasi maksimum besi 0,3 mg/L, dan konsentrasi maksimum mangan 0,05 mg/L.
• Hindari air baku yang mengandung logam berat.
• Hindari air baku dengan kandungan pestisida dan herbisida kecuali digunakan karbon aktif.
• Hindari air baku dengan warna tinggi kecuali apabila digunakan pengolahan pendahuluan ozone.
• Tidak ada residu oksidan, misalnya chlorine yang digunakan sebelum saringan pasir lambat.
Beberapa parameter yang dapat disisihkan dengan menggunakan unit ini antara lain: (Astari dan Iqbal, 2009)
kekeruhan dengan efisiensi penyisihan hingga 92,6%,
besi dengan efisiensi penyisihan sebesar 91,5%, mangan dengan efisiensi 93%,
zat organic dengan efisiensi penyisihan sebesar 23.5%, total solid terlarut dengan efisiensi penyisihan 7.7%, kesadahan total dengan efisiensi penyisihan 4.7%, nitrit hingga 80%, dan
nitrat hingga 69%.
Gambar 12. Ilustrasi Saringan Pasir Lambat