PENGARUH PEMBERIAN VITAMIN C
TERHADAP AKTIVITAS ENZIM DELTA AMINOLEVULINIC
ACID DEHYDRATASE ( -ALAD), KADAR HEMOGLOBIN DAN
BASOPHILIC STIPPLING PADA MENCIT
YANG DIPAPAR PLUMBUM
TESIS
Oleh
NELMA
067008008/BM
SEKOLAH PASCASARJANA
UNIVERSITAS SUMATERA UTARA
PENGARUH PEMBERIAN VITAMIN C
TERHADAP AKTIVITAS ENZIM DELTA AMINOLEVULINIC
ACID DEHYDRATASE ( -ALAD), KADAR HEMOGLOBIN DAN
BASOPHILIC STIPPLING PADA MENCIT
YANG DIPAPAR PLUMBUM
TESIS
Untuk Memperoleh Gelar Magister Kesehatan
dalam Program Studi Ilmu Biomedik
pada Sekolah Pascasarjana Universitas Sumatera Utara
Oleh
NELMA
067008008/BM
SEKOLAH PASCASARJANA
UNIVERSITAS SUMATERA UTARA
Judul Tesis : PENGARUH PEMBERIAN VITAMIN C TERHADAP AKTIVITAS ENZIM AMINOLEVULINIC ACID DEHYDRATASE, KADAR HEMOGLOBIN DAN BASOPHILIC STIPPLING PADA MENCIT YANG DIPAPAPAR PLUMBUM
Nama Mahasiswa : Nelma Nomor Pokok : 067008008 Program Studi : Biomedik
Menyetujui Komisi Pembimbing
(Dr. Ramlan Silaban, M.Si) (Prof.dr.Azmi S.Kar,SpPD KHOM) Ketua Anggota
Ketua Program Studi, Direktur
(dr. Yahwardiah Siregar, PhD) (Prof. Dr. Ir. T. Chairun Nisa B, M.Sc)
Telah diuji pada
Tanggal : 25 Agustus 2008
____________________________________________________________________
PANITIA PENGUJI TESIS
Ketua : Dr. Ramlan Silaban, M.Si
Anggota : 1. Prof.dr.Azmi S.Kar,SpPD.KHOM
2. dr. T.Azhar Djohan, SpPK
ABSTRAK
Plumbum dalam darah pada kadar tertentu dapat menimbulkan gangguan kesehatan, Plumbum berkemampuan berikatan dalam gugus–SH dalam molekul protein dan menyebabkan hambatan sintesis Hemoglobin dengan menghambat konversi aminolevulinic asid menjadi forfobilinogen dan juga menghambat korporasi dari Fe kedalam proforfirin IX untuk membentuk hemoglobin. Untuk mengatasi permasalahan keracunan Plumbum dapat dilakukan terapi dengan pemberian antioksidan yaitu untuk mengatasi radikal bebas yang disebabkan oleh plumbum. Salah satu antioksidan yang dapat diberikan adalah vitamin c yaitu merupakan antioksidan pemutus rantai akan memutus rantai reaksi menjadi senyawa non radikal atau radikal yang lebih stabil. Penelitian ini bertujuan untuk mengetahui sampai sejauh mana efek pemberian vitamin c secara oral selama 1 minggu terhadap aktivitas enzim amino leuvelenic acid dehydratase, kadar hemoglobin dan basophilic stippling pada mencit percobaan.
Penelitian ini adalah eksperimental laboratorik dengan rancangan acak lengkap (RAL). Jumlah sample terdiri dari 32 ekor mencit jantan (Mus musculus L) yang dibagi ke dalam 5 kelompok yang masing-masing terdiri dari 7 ekor mencit. Pemeriksaan hemoglobin dilakukan dengan metoda cyanmethemoglobin, aktivitas enzim ALAD dilakukan dengan pemeriksaan Wigfield and Farant dan basophilic stipling dihitung pada hapusan darah yang diwarnai dengan Giemsa. Pengolahan data dilakukan dengan analisis uji Anova dan Kruskall Wallis serta Mann- Whitney.
Hasil dari uji Anova didapatkan bahwa pemberian plumbum dapat menurunkan aktifitas enzim alad pada kelompok perlakuan (p= 0.010), Namun pada kelompok mencit yang diberikan Plumbum + vitamin c 1000mg/oral/kgBB ternyata dapat meningkatkan aktifitas enzim ALAD (p= 0.077). Ditemukan basophilic stippling pada mencit yang di beri Pb 20mg/kgBB, dan terjadi penurunan jumlah basophilic stipling pada mencit yang diberi vitamin c (p= 0,001)
Hasil dari uji Anova pemberian vitamin c 1000mg/kgBB secara oral selama 7 hari dapat meningkatkan enzim Amino leuvelenic acid dehydratase dan uji Mann- Whitney menurunkan jumlah basophilic stippling pada hewan coba.
ABSTRACT
Lead in the blood at high concentrations can cause health problems such as binding the SH group in globin molecules which disrupts Hemoglobin synthesis, The conversion of Aminoleuvilinic acid ( ALAD) to phorphobilinogen is disrupted as well as the in corporation of Fe into phorphirin IX to form the Hemoglobin. Antioxidant teraphy is used to treat lead poisoning because lead causes free radical production. An antioxidant that can be given is Vitamin C breaks down the free radical molecule a non-radical form or to a more stable radical. The present was carnet out to find out the of adsministration effect oral Vitamin C for a week, an the activity of Amino leuvelenic acid dehydratase, the hemoglobin concentration and total basophilic stippling observed in the experimental mice.
This research was conducted with randomised groups of male mice (Mus musculus L). The mice were divided into 5 groups of 7 mice each. The hemoglobin concentration was determined using the cyanmethemoglobin method. The activity of the ALAD was measured according to the method of Wigfield and Farant The basophilic stippling was counted on blood smear dyed with Giemsa. The data was analysed with Anova then Kruskal Walis and Mann- Whitney tests.
The results of the Anova test showed that lead decreased the ALAD activity in the treatment group (p=0,010). However, in the group which was given lead + Vitamin C at a dose of 1000mg/kg, the activity ALAD increased (p=0,077). Basophilic Stippling was found in all treatment groups (lead dose of 20 mg/kg) but there was a significant decrease observed in the group reserving 1000mg/kg Vitamin C (p=0,001).
The conclusions of this study are Vitamin C 1000mg/kg for seven days increases the Aminoleuvelenic acid dehydratase activity and decreases the basophilic stippling in the experimental animals.
RIWAYAT HIDUP
1. Nama : Nelma
2. Tempat/Tanggal Lahir : Medan, 4 Nopember 1962
3. Agama : Islam
4. Status : Menikah
5. Alamat : Jl. Karya Mesjid Gg.Padi No.10 Medan 6. Telp/HP : (061)6625353/085296238500
7. Pendidikan :
SD Negeri No 32 : 1969 - 1975
SMP Negeri 1 Medan : 1975 - 1979
SMAK Depkes Medan : 1979 – 1982
AAK Depkes Bandung : 1992 – 1995
Sarjana (S1) Fakultas Biologi UMA : 1995 – 1999 Pascasarjana (S2) Biomedik SPS USU : 2006 - 2008 8. Riwayat Pekerjaan :
Staf Pengajar Tetap di :
SMAK Depkes Medan : 1984 – 1996
DAFTAR ISI
Halaman
ABSTRAK ... i
ABSTRACT... ii
KATA PENGANTAR ... iii
RIWAYAT HIDUP... vi
DAFTAR ISI... vii
DAFTAR TABEL... ix
DAFTAR GAMBAR ... x
DAFTAR LAMPIRAN... xi
BAB 1 PENDAHULUAN ... 1
1.1Latar Belakang ... 1
1.2 Perumusan Masalah ... 4
1.3 Kerangka Teori... 5
1.4 Tujuan Penelitian ... 6
1.5 Hipotesis... 7
1.6 Manfaat Penelitian ... 7
BAB 2 TINJAUAN PUSTAKA ... 8
2.1Plumbum (Pb) ... 8
2.2Biosintesis Haemoglobin ... 13
2.4Oksidan ... 16
2.5Antioksidan ... 18
2.6Dampak Oksidan Terhadap Tubuh ... 19
2.7Vitamin C ... 22
BAB 3 METODOLOGI PENELITIAN... 24
3.1Desain Penelitian... 24
3.2Tempat dan Waktu Penelitian ... 24
3.3Populasi Penelitian ... 24
3.4Variabel Penelitian ... 24
3.5Bahan ... 25
3.6Alat ... 25
3.7Pelaksanaan Penelitian ... 25
3.8Prosedur Pemeriksaan ... 27
3.9Analisa Data ... 31
BAB 4 HASIL DAN PEMBAHASAN ... 32
4.1Pengaruh Perlakuan terhadap Aktivitas Enzim ALAD... 32
4.2Pengaruh Perlakuan terhadap Kadar Hemoglobin ... 38
4.3Pengaruh Perlakuan terhadap Jumlah Basophilic Stippling... 43
BAB 5 KESIMPULAN DAN SARAN ... 48
5.1Kesimpulan ... 48
5.2Saran... 49
DAFTAR TABEL
No. Judul Hal 1. Data Penelitian Enzim ALAD pada Kelompok Kontrol dan Berbagai
Kelompok Perlakuan (n=32) ... 32
2. Distribusi Rata-rata Aktivitas Enzim ALAD terhadap Kelompok Kontrol
dan Berbagai Kelompok Perlakuan (n=32)... 33
3. Hasil Uji LSD Aktivitas Enzim ALAD pada Kelompok Perlakuan
(n=32)... 34
4. Data Penelitian Kadar Hemoglobin pada Kelompok Kontrol dan Berbagai
Kelompok Perlakuan (n=32) ... 39
5. Distribusi Rata-rata Kadar Hemoglobin pada Kelompok Kontrol
dan Berbagai Kelompok Perlakuan (n=32)... 39
6. Distribusi Basophilic Stippling pada Kelompok Perlakuan (n=32)... 43
7. Hasil Kruskal Walis Basophilic Stippling pada Kelompok Perlakuan
(n=32)... 44
8. Hasil Uji Mann-Whitney Basophilic Stippling pada Kelompok Perlakuan
DAFTAR GAMBAR
DAFTAR LAMPIRAN
No Judul Hal 1. Persetujuan Komite Etik Tentang Pelaksanaan Penelitian Bidang Kesehatan . 53 2. Pernyataan Melakukan Penelitian dari Kepala Balai Penyidikan dan Pengujian
Veteriner Regional I Medan ... 54
BAB 1
PENDAHULUAN
1.1. Latar Belakang
Timbal disebut juga Pb, merupakan logam berat yang terdapat di dalam kerak bumi dan tersebar ke alam dalam jumlah kecil melalui proses alamiah. Apabila Pb terhirup atau tertelan oleh manusia maka di dalam tubuh, akan beredar mengikuti aliran darah, diserap kembali di dalam ginjal dan disimpan di dalam tulang dan gigi. Manusia menyerap plumbum melalui udara, debu, air dan makanan. Salah satu penyebab kehadiran plumbum adalah pencemaran udara, yaitu akibat kegiatan transportasi darat yang menghasilkan bahan pencemar seperti gas CO3, NOx,
hidrokarbon, SO2, dan tetraethyl lead, yang merupakan bahan logam timah hitam
(timbal) yang ditambahkan ke dalam bahan bakar (Palar, 1994).
Sel-sel darah merah merupakan suatu bentuk kompleks khelat yang dibentuk oleh logam Fe (besi) dengan gugus haem dan globin sintesa dari kompleks tersebut melibatkan 2 enzim, yaitu enzim ALAD (Amino Levulinic Acid Dehidrase) atau asam amino levulinat dehidrase dan enzim ferrokhelatase. Enzim ALAD adalah enzim jenis sitoplasma. Enzim ini akan bereaksi secara aktif pada tahap awal sintesa dan selama sirkulasi sel darah merah berlangsung. Sistim haematopoetik sangat peka terhadap efek Pb. Efek hematoksisitas Pb adalah menghambat sebagian besar enzim yang berperan dalam biosintesa heme. Diantara enzim yang terlibat dalam pembentukan heme adalah enzim aminolevulinic acid dehydrogenase (ALAD) dan ferrochelatase termasuk enzim yang paling rentan terhadap efek penghambatan Pb. Sedangkan enzim aminolevulinic acid synthetase (ALAS) uroporphyrinogen decarboxylase (UROD) dan coproporphyri nogen oxidase (COPROD) tidak begitu peka terhadap penghambatan Pb (Goldstein and Kipen, 1994).
Inhibisi pada ALAD berhubungan dengan konsentrasi Pb dalam darah. Hampir 50% aktivitas enzim ini dihambat pada kadar Pb darah 15 g/dL. Efek yang paling berperan adalah hambatan pada reaksi enzimatik terakhir dalam sintetis heme, dimana ferrochelatase mengkatalisis penggabungan besi ferro ke dalam cincin heme. Inhibisi pada ferrochelatase mengakibatkan akumulasi free erythrosyt protoporpyrin (FEP) atau zinc protoporphyrin (ZPP) dan coproporphiryn dalam urine (Child, 1990)
hidup eritrosit. Patogenesis terjadinya hemolisis pada keracunan Pb diperkirakan berhubungan dengan inhibisi pada pyrimidine–5’ nucleotidase. Defisiensi enzim ini secara herediter ditandai dengan basophilic stippling pada eritrosit, hemolisis kronik, dan akumulasi nukleotida pirimidin di intra eritrosit. Nukleotida pirimidin ini berkompetensi dengan nukleotida adenin pada sisi aktif kinase pada glycolitic pathway yang mengubah stabilitas membran sel darah merah. Defisiensi enzim yang disebabkan oleh Pb dan penemuan klinis yang ditemukan sama dengan kelainan herediter karena defisiensi enzim pyrimidine–5’nucleotidase, oleh karenanya keracunan Pb yang berat dihubungkan dengan penyakit herediter ini.(Palar, 1994) Penelitian tentang efek plumbum terhadap aktivitas enzim ALAD pada hewan percobaan telah banyak dilakukan. Pemberian Pb selama 14 hari pada tikus albino menyebabkan penurunan aktivitas enzim ALAD secara signifikan dibandingkan dengan kontrol (Hasan and Seth, 1981). Penelitian pada rattus norvegicus dengan pemberian 0,5 g/kg/BB/oral/hari/tikus selama 16 minggu mengakibatkan peningkatan aktivitas enzim ALAD dan anemia (Hariono, 2008). Keracunan Pb dapat menyebabkan terjadinya anemi akibat penurunan sintesis globin walaupun tak tampak adanya penurunan kadar zat besi dalam serum dan terjadi anemi ringan disertai dengan sedikit peningkatan kadar Amino Levulinic Acid di urin (Sudarmaji et al., 2006).
C yaitu merupakan antioksidan pemutus rantai (chain breaking antioksidans) akan memutus rantai reaksi menjadi senyawa non radikal atau radikal yang lebih stabil. Vitamin C senyawa alami yang dengan mengikat zat-zat radikal seperti superoksida dismutase dan radikal hidroksil, juga bereaksi langsung dengan hidrogen peroksida, oleh karena itu mencegah berbagai radikal bebas bersifat toksik yang menyebabkan oksidasi (Gajawat et al., 2006). Banyak penelitian yang telah dilakukan menunjukkan bahwa Vitamin C sangat bermanfaat dan pengobatan penyakit antara lain: menurunkan tekanan darah dan kolesterol, mencegah terjadinya resiko terjadinya serangan jantung, bekerja sebagai antioksidan, melindungi sistim immun dalam melawan virus (Klenner, 1997)
Berdasarkan latar belakang tersebut diatas, maka peneliti menganggap perlu melakukan penelitian mengenai pengaruh pemberian suplementasi viatamin C terhadap enzim ALAD (Aminolevulinic Acid Dehydrogenase), Kadar Hemoglobin Dan Basophilic Stippling pada tikus yang terpapar dengan Pb.
1.2. Perumusan Masalah
1.3. Kerangka Teori
Plumbum dapat merangsang aktivitas enzim delta aminolevulinic acid syntetase (ALAS) dalam mitokondria, dan dapat menghambat aktivitas enzim ALAD dalam sitoplasma(WHO, 1977).
Gangguan sintesis heme pada manusia ditunjukkan dengan peningkatan kadar prekusor heme yang tidak normal dalam darah dan urin. Penghambatan enzim ALAD dibuktikan dengan akumulasi ALA dan eritrosit protoporfirin dalam darah dan urin. Terjadinya peningkatan ekskresi ALA dalam urin, menunjukkan bahwa terjadi penurunan ALA, yang disebabkan oleh penghambatan aktivitas enzim ALAD (WHO, 1977). Keracunan plumbum menyebabkan protobilinogen (PBG), dan uroporfirin meningkat dalam darah. Besi non-heme seperti ferritin diakumulasi dalam eritrosit (Scinicariello et al., 2007)
Pemberian antioksidan diharapkan dapat mengatasi radikal bebas yang disebabkan oleh Pb. Salah satu antioksidan yang dapat diberikan adalah vitamin C yaitu merupakan antioksidan pemutus rantai (chain breaking antioksidans) akan memutus rantai reaksi menjadi senyawa non radikal atau radikal yang lebih stabil. Vitamin C senyawa alami yang dengan mengikat zat-zat radikal seperti superoksida dismutase dan radikal hidroksil, juga bereaksi langsung dengan hidrogen peroksida, oleh karena itu mencegah berbagai radikal bebas bersifat toksik yang menyebabkan oksidasi.
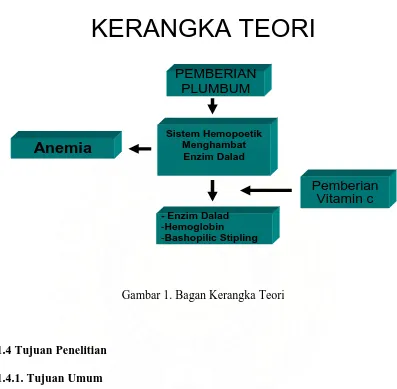
KERANGKA TEORI
PEMBERIAN PLUMBUM
Sistem Hemopoetik Menghambat
Enzim Dalad
- Enzim Dalad -Hemoglobin -Bashopilic Stipling
Anemia
Pemberian Vitamin c
Gambar 1. Bagan Kerangka Teori
1.4 Tujuan Penelitian
1.4.1. Tujuan Umum
Untuk mengetahui efek pemberian Vitamin C secara oral terhadap kadar enzim ALAD (Amino Levulinic Acid Dehydrase), Kadar Hemoglobin dan Basophilic Stippling akibat paparan plumbum.
1.4.2. Tujuan Khusus
b. Untuk mengetahui bagaimana pengaruh pemberian Vitamin C terhadap kadar hemoglobin dan basophilic stippling pada darah yang dipaparkan dengan Plumbum 1.5. Hipotesis
Pemberian suplemen Vitamin C secara oral dapat menghambat penurunan aktivitas enzim ALAD, kadar hemoglobin dan terbentuknya basophilic stippling pada darah yang dipaparkan Plumbum.
1.6. Manfaat Penelitian
a. Memberikan informasi tentang penggunaan vitamin c sebagai antioksidan khususnya terhadap pengaruh plumbum
b. Informasi tambahan untuk dunia pendidikan khususnya bidang kesehatan c. Dasar penyuluhan/konseling untuk mencegah timbulnya anemi kronis oleh plumbum
d. Penelitian ini dapat dipakai sebagai acuan untuk peneliti selanjutnya tentang pengaruh Pb pada manusia.
BAB 2
TINJAUAN PUSTAKA
2.1. Plumbum (Pb)
2.1.1. Sifat Fisika dan Kimia Plumbum
Plumbum biasa juga disebut timbal atau Timah Hitam dalam susunan berkala
merupakan logam berat yang terdapat secara alami dan tersebar kealam dalam jumlah kecil melalui proses alami. Apabila timbal terhirup atau tertelan oleh manusia, didalam tubuh akan beredar mengikuti aliran darah, diserap kembali didalam ginjal, dan disimpan dalam tulang dan gigi. Manusia menyerap timbal melalui udara, debu, air dan makanan (Bartik, 1981)
Timbal (Pb) adalah logam berat, dengan nomor atom 82, berat atom 207,19 dan berat jenis 11,34, bersifat lunak dan berwarna biru keabu-abuan dengan kilau logam yang khas sesaat setelah dipotong. Kilaunya akan segera hilang sejalan dengan pembentukan lapisan oksida pada permukaannya, mempunyai titik leleh 327,50C dan titik didih 17400C. (Palar,1994)
2.1.2. Keracunan Plumbum
Ukuran keracunan suatu zat ditemukan oleh kadar dan lamanya paparan. Keracunan dibedakan menjadi keracunan akut dan keracunan kronis. Keracunan yang disebabkan oleh Pb dalam tubuh mempengaruhi berbagai jaringan dan organ tubuh. Organ-organ tubuh yang menjadi sasaran dari keracunan timbal adalah sistem peredaran darah, sistem saraf, sistem urinaria, sistem reproduksi, sistem endokrin, dan jantung.(WHO,1977)
Pada orang dewasa kadar Pb darah 10 µg/dl, akan mempengaruhi perkembangan sel darah, kadar Pb darah 40µg/dl akan mempengaruhi beberapa fungsi dari kemampuan darah untuk membentuk hemoglobin, gangguan system syaraf menyebabkan kelelahan, irritability, kehilangan ingatan dan reaksi lambat. Pada ginjal menyebabkan penyakit ginjal yang kronis dan gagal ginjal. Pada sistem reproduksi mengakibatkan berkurangnya jumlah sperma dan meningkatnya jumlah sperma yang abnormal. Jumlah yang sangat tinggi pada wanita akan mengakibatkan keguguran. Tingginya level Pb didarah juga meningkatkan tekanan darah (Shannon, 1998).
2.1.3. Metabolisme Plumbum
Masukan Pb 100 hingga 350 g/hari dan 20 g diabsorbsi melalui inhalasi uap Pb dan partikel dari udara lingkungan kota yang polutif. Timah hitam dan senyawanya masuk ke dalam tubuh manusia melalui saluran pernafasan dan saluran pencernaan, sedangkan absorpsi melalui kulit sangat kecil sehingga dapat diabaikan. Bahaya yang ditimbulkan oleh Pb tergantung oleh ukuran partikelnya. Partikel yang lebih kecil dari 10 g dapat tertahan di paru-paru, sedangkan partikel yang lebih besar mengendap di saluran nafas bagian atas (Ardyanto,2005)
Absorpsi Pb melalui saluran pernafasan dipengaruhi oleh tiga proses yaitu deposisi, pembersihan mukosiliar, dan pembersihan alveolar. Deposisi terjadi di nasofaring, saluran trakeobronkhial, dan alveolus. Deposisi tergantung pada ukuran partikel Pb, volume pernafasan dan daya larut. Partikel yang lebih besar banyak di deposit pada saluran pernafasan bagian atas dibanding partikel yang lebih kecil. Pembersihan mukosiliar membawa partikel di saluran pernafasan bagian atas ke nasofaring kemudian di telan. Rata-rata 10 – 30% Pb yang terinhalasi diabsorpsi melalui paru-paru, dan sekitar 5-10% dari yang tertelan diabsorbsi melalui saluran cerna (Palar,1994)
2.1.4. Distribusi dan Penyimpanan Plumbum
Plumbum yang diabsorpsi diangkut oleh darah ke organ-organ tubuh sebanyak 95% Pb dalam darah diikat oleh eritrosit. Sebagian Pb plasma dalam bentuk yang dapat berdifusi ke jaringan lunak (sum-sum tulang, sistem saraf, ginjal, hati ) dan kejaringan keras ( tulang, kuku, rambut, gigi ). Gigi dan tulang panjang mengandung Pb yang lebih banyak dibandingkan tulang lainnya. Pada gusi dapat terlihat lead line yaitu berupa pigmen yang berwarna abu-abu pada perbatasan antara gigi dan gusi. Hal ini merupakan ciri khas dari keracunan Pb. Pada jaringan lunak sebagian Pb disimpan dalam aorta, hati, ginjal, otak dan kulit (Ardyanto, 2005)
2.1.5. Ekskresi Plumbum
Ekskresi Pb melalui beberapa cara, yang terpenting adalah melalui ginjal dan saluran cerna. Ekskresi Pb melalui urine sebanyak 75 – 80%, melalui feces 15% dan lainnya melalui empedu, keringat, rambut, dan kuku. Ekskresi Pb melalui saluran cerna dipengaruhi oleh saluran aktif dan pasif kelenjar saliva, pankreas dan kelenjar lainnya di dinding usus, regenerasi sel epitel, dan ekskresi empedu. Sedangkan Proses eksresi Pb melalui ginjal adalah melalui filtrasiglomerulus (Ardyanto,2005)
2.1.6. Pengaruh Plumbum pada Sistem Peredaran Darah
Kira-kira 90% Pb yang masuk kedalam sirkulasi darah menuju ke eritrosit, ada juga yang ke albumin darah, -globulin dan protein lain. Plumbum mempengaruhi sistem peredaran darah dengan berbagai cara:
a. Dengan memperlambat pematangan normal sel darah merah (eritrosit) dalam sum-sum tulang, hal ini menyebabkan terjadinya anemia.
b. Mempengaruhi kelangsungan hidup sel darah merah. Sel darah merah yang diberi perlakuan dengan timbal, memperlihatkan peningkatan tekanan osmosis dan kelemahan pergerakan. Selain itu juga memperlihatkan penghambatan Na-K-ATP ase yang meningkatkan kehilangan kalium, intraseluler. Pengaruh ini menjelaskan bahwa kejadian anemia pada peristiwa keracunan plumbum disertai oleh penyusutan waktu hidup sel darah merah.
c. Menghambat biosintesis hemoglobin dengan cara menghambat aktivitas enzim ALAD dengan enzim ferroketalase (WHO, 1977)
2.1.7. Deteksi Plumbum dalam tubuh manusia
Untuk mengetahui seberapa besar kandungan plumbum yang diabsorbsi dapat
dilakukan dengan pemeriksaan kadar plumbum dalam darah juga dapat dilakukan dengan: Pengujian kadar koproporfirin dalam urin, Pengujian kadar ALA dalam urin, Pengujian kadar ALA dan aktivitas enzim ALAD dalam darah.
Pengujian kadar ALA dan aktivitas enzim ALAD dalam darah biasanya dipakai untuk mengetahui kadar plumbum pada orang yang terpapar plumbum. Pengukuran yang paling sensitif adalah pengukuran yang dilakukan terhadap penurunan aktivitas enzim ALAD dalam darah (Habal, 2006)
2.2. Biosintesis Haemoglobin
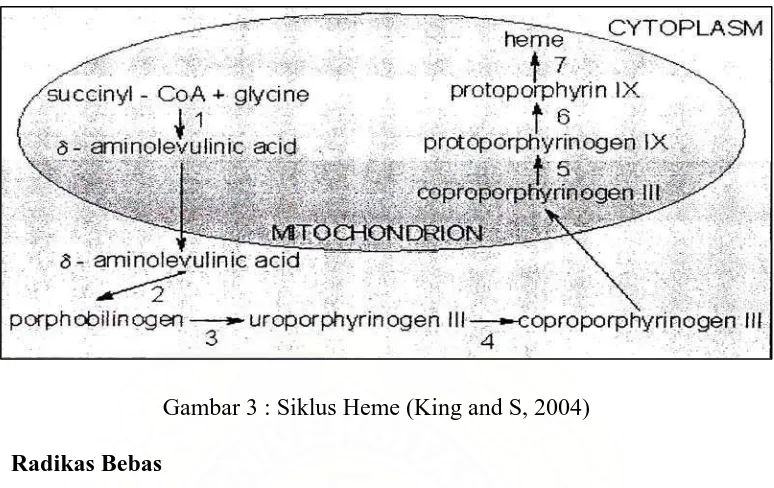
molekul porfobilinogen. Masih dalam sitoplasma, 4 unit porfobilinogen mengalami kondensasi membentuk polimer siklik yaitu uroporfobilinogen. Ada 2 isomer uroporfobilinogen, yaitu isomer I dan isomer tipe III. Heme berasal dari isomer tipe III. Uroporfibilinogen III diubah menjadi koproporfirinogen III. Reaksi ini dikalisis oleh uroporfirinogen dekarboksilase. Kemudian koproporfirinogen III memasuki mitokondria, selanjutnya diubah menjadi protoporfirinogen. Dari 15 kemungkinan isomer hanya satu yang dibentuk, yaitu protoporfirinogen IX. Protoporfirinogen IX dioksidasi oleh enzim protoporfirinogen oksidasi menghasilkan proforfirin IX. Oksidasi ini menghasilkan ikatan rangkap terkonjugasi yang merupakan ciri porfirin. Tahap ahir pembentukan heme adalah pemasukan ion ferro ke dalam proporfirin yang dikatalisis oleh enzim ferrokhelatase (Murray et al., 2003) .
Gambar 3 : Siklus Heme (King and S, 2004) 2.3. Radikas Bebas
Pb merupakan unsur yang dapat meningkatkan pembentukan radikal bebas dan menurunkan kemampuan antioksidan tubuh sehingga dapat menyebabkan kerusakan organ, Suatu radikal bebas dapat dinyatakan sebagai spesies yang terdiri satu atau lebih elektron yang tidak berpasangan. Radikal bebas ini dapat bereaksi dengan berbagai cara. Salah satunya adalah apabila dua radikal bertemu maka elektron yang tidak berpasangan tadi akan bergabung membentuk ikatan kovalen (Halliwel, 1987).
Radikal bebas ditemukan baik melalui faktor eksogen maupun endogen serta mempengaruhi kehidupan sel. Radikal terpenting dalam tubuh adalah radikal derivad dari oksigen yang disebut kelompok oksigen reaktif (reactive oxygen species /ROS) (Arief, 2006).
rangsangan. Secara rutin adalah superokside yang dihasilkan melalui aktifasi fagosit dan reaksi katalisa seperti ribonucleotida reductase. Sedang pembentukan melalui rangsangan adalah kebocoran superoksida, hidrogen peroksida dan kelompok oksigen reaktif (ROS) lainnya pada saat bertemunya bakteri dengan fagosit teraktifasi. Pada keadaan normal sumber utama radikal bebas adalah kebocoran elektron yang terjadi dari rantai transpot elektron, misalnya yang ada dalam mitokondria dan endoplasma retikulum dan molekul oksigen yang menghasilkan superoksida (RetnoGitawati, 1995)
Apabila ada ketidakseimbangan antara radikal bebas dengan antioksidan maka akan terjadi suatu keadaan yang disebut stres oksidatif. Stres oksidatif adalah suatu keadaan dimana tingkat kelompok oksigen reaktif (ROS) yang toksik melebihi pertahanan antioksidan endogen. Keadaan ini mengakibatkan kelebihan radikal bebas yang akan bereaksi dengan lemak, protein, dan asam nucleat seluler sehingga terjadi kerusakan lokal dan disfungsi organ tertentu. (Arief, 2006)
2.4. Oksidan
Dalam pengertian ilmu kimia, oksidan adalah senyawa penerima elektron, yaitu senyawa-senyawa yang dapat menarik elektron, sedangkan radikal bebas adalah atom atau molekul (sekumpulan atom) yang memiliki elektron yang tak berpasangan ( unpaired electron ) (Suryohudoyo, 2003).
(HOO) dan singlet oksigen (O2). Radikal yang terahir merupakan molekul yang
reaktif dan dapat bereaksi dengan protein, asam nukleat, lipid dan molekul lainnya untuk mengubah strukturnya serta menimbulkan kerusakan jaringan.
Superoksida terbentuk karena adanya proses auto oksidasi Hb ( yang besarnya
3% auto oksidasi per hari ) menjadi methemoglobin. Superoksida secara spontan mengalami dismutasi sehingga terbentuk H2O2 dan O2 , akan tetapi kecepatan reaksi
yang sama akan mengalami peningkatan yang luar biasa akibat kerja enzim superoksid dismutase (SOD).Ion Fe2+ pada Hb rentan terhadap oksidasi oleh oksidan.(ion superoksid ), dimana terbentuk metHb yang tidak mampu mengangkut oksigen. Pada keadaan normal hanya dijumpai sedikit metHb didalam darah, karena eritrosit memiliki sistem yang efektif untuk mereduksi kembali Fe3+ menjadi Fe2. Ion superoksida terbentuk melalui beberapa cara, antara lain :
a. Sebagai reaksi samping yang melibatkan Fe2+ , misalnya : pada proses fosforilasi oksidatif, proses oksigenasi hemoglobin, proses hidroksilasi oleh enzim monooksigenase ( sitokrom p 450 dan sitokrom b4 ), dan ion Fe2+ b. Reaksi yang dikatalisis oleh NADPH / NADH oksidase yang terdapat dalam
mitokondria
c. Reaksi yang dikatalisis olehenzim xantin oksidase
Pada eritrosit dan beberapa jaringan, enzim glutation peroksidase yang mengandung silenium ( Se ) mengkatalisis H2O2, sehingga mencegah peroksidasi
lipid dan menghambat terjadinya oksidasi Hb menjadi metHb. Daya rusak hidrogen peroksida bukan hanya karena senyawa tersebut merupakan oksidan yang kuat, tetapi H2O2 juga dapat menghasilkan radikal hidroksil bila H2O2 bereaksi dengan logam
transisi seperti Fe 2+ dan Cu +.
Radikal hidroksil dapat juga terbentuk dari reaksi ion superoksida dan hidrogen
peroksida (reaksi Haber Weiss).
Reaksi ini memerlukan ion Fe3+ dan Cu 2+ dan diperkirakan melalui 2 tahap, yaiu: Radikal peroksil terbentuk dari ion superoksida dengan asam. Radikal ini
sangat reaktif dan akan membentuk radikal baru serta H2O2
Singlet Oksigen, merupakan bentuk oksigen yang jauh lebih reaktif dibandingkan
oksigen biasa. Singlet oksigen ini terbentuk dari reaksi-reaksi yang dikatalis oleh enzim-enzim tertentu.
2.5. Antioksidan
Senyawa antioksidan adalah senyawa-senyawa pemberi elektron, dalam arti yang lebih luas adalah : senyawa-senyawa yang dapat meredam dampak negatif oksidan, termasuk diantaranya enzim-enzim dan protein pengikat logam. Dalam meredam dampak negatif oksidan diterapkan dua strategi :
Berdasarkan dua mekanisme pencegahan dampak negatif oksidan, antioksidan dapat dibagi menjadi dua golongan yaitu :
a. Antioksidan pencegah b. Antioksidan pemutus rantai
Eritrosit dilengkapi antioksidan berupa enzim seperti copper-zink-superoxide dismutase (CuZn-SOD), glutation peroksidase (GSH-Px), katalase (Cat) dan glutation reduktase (Suryohudoyo, 2000)
Sintesis antioksidan yang berupa enzim dalam eritrosit ini terjadi selama erytropoesis, Sedangkan pada eritrosit dewasa, enzim-enzim ini tidak disintesis lagi, hal ini berkaitan dengan hilangnya inti sel pada eritrosit dewasa sebagai peredam dampak negatif ROS (Suryohudoyo, 2000)
2.6 Dampak Oksidan Terhadap Tubuh
2.6.1. Dampak negatif
Dampak negatif timbul karena senyawa ROS merupakan oksidan yang kuat dan mempunyai reaktifitas yang dapat merusak komponen-komponen sel yang penting untuk mempertahankan integritas dan kehidupan sel. Diantara senyawa ROS yang lain, radikal hidroksil merupakan senyawa yang paling berbahaya karena reaktifitasnya sangat tinggi. Radikal hidroksil dapat merusak tiga jenis senyawa yang penting untuk mempertahankan integritas sel yaitu :
a. Terhadap membran sel
dan arakidonat) yang sangat rawan terhadap serangan-serangan radikal, terutama radikal hidroksil. Radikal hidroksil dapat menimbulkan reaksi rantai yang dikenal dengan nama peroksidasi lipid. Akibat dari rantai reaksi ini adalah terputusnya rantai asam lemak menjadi berbagai senyawa yang bersifat toksik terhadap sel, antara lain berbagai macam aldehida seperti, malondialdehida (MDA), 9-hidroksil-nonenal serta bermacam-macam hidrokarbon seperti hidrokarbon etana (C2 H6) dan pentane
(C5H12).
Selain reaksi diatas dapat pula terjadi ikatan silang antara dua rantai asam lemak atau antara asam lemak dan rantai peptida (protein) yang timbul karena reaksi dua radikal. Semua ini menyebabkan kerusakan parah membran sel yang membahayakan kehidupan sel (Suryohudoyo, 2000).
b. Terhadap protein
Oksidan dapat merusak protein karena dapat mengadakan reaksi dengan asam-asam amino yang menyusun protein. Diantara asam-asam-asam-asam amino penyusun protein yang paling rawan adalah sistein. Sistein mengandung gugus sulfhidril (SH) dan justru gugus inilah yang paling peka terhadap serangan radikal bebas seperti radikal hidroksil.
c. Terhadap DNA
Radikal bebas dapat menimbulkan berbagai perubahan pada DNA yang antara lain berupa : hidroksilasi basa timin dan sitosin, pembukaan inti purin dan pirimidin serta terputusnya rantai fosfodiester DNA. Bila kerusakan tak terlalu parah, maka masih bisa diperbaiki oleh sistem perbaikan DNA. Namun apabila kerusakan terlalu parah, misalnya rantai DNA terputus diberbagai tempat, maka kerusakan tersebut tak dapat diperbaiki dan replikasi sel terganggu. Susahnya, perbaikan DNA ini justru menimbulkan mutasi, karena dalam memperbaiki DNA sistem perbaikan DNA cendrung membuat kesalahan, dan apabila mutasi ini mengenai gen-gen tertentu, maka mutasi tersebut dapat menimbulkan kanker (Suryohudoyo, 2000)
2.6.2. Dampak positif
2.7. Vitamin C
2.7.1. Struktur vitamin C
Vitamin C merupakan vitamin yang larut dalam air, banyak didapatkan dalam buah-buahan segar dan sayur-sayuran terutama sitrus, berri dan dari famili kubis. Ditemukan pertama kali oleh Sir Richard Hawkins pada abad 16 yang melaporkan bahwa jeruk dan lemon adalah yang paling efektif dalam menyembuhkan pelaut-pelaut Inggris dari penyakit scorbut (LindeCM, 1992).
Vitamin C mempunyai 2 bentuk, yaitu asam askorbat (bentuk reduksi) dan asam dehidroaskorbat ( bentuk Oksida ). Vitamin ini sangat tidak stabil pada pH netral atau alkali, juga terhadap panas tetapi sangat stabil terhadap asam dan selama penyimpanan sementara dalam keadaan dingin dan segar (Almatsier, 2003).
2.7.2. Fungsi Vitamin C
Pada level molekuler, askorbat dan dehidroaskorbat mempunyai sifat pereduksi dan juga mempunyai sifat penting lainnya sebagai antioksidan yang mempengaruhi redoks-potensial tubuh (sebagai sumberreducing equivalent di seluruh tubuh). Pada proses hidroksilasi yang menggunakan molekul oksigen dan sering mempunyai kofaktor Fe++ atau Cu++, vitamin C ikut berperan sebagai :
a. Sumber elektron untuk mereduksi oksigen ( misalnya sebagai kosubstrat )
Reaksi hidroksilasi tersebut misalnya pada :
a. Reaksi pembentukan hidroksiprolin dan hidroksilisin dalam sintesis prokolagen pada endoplasmik retikulum sel.
b. Sintesis karnitin dari lisin yang penting dalam proses pengangkutan asam-asam lemak ke dalam mitokondria untuk mendapat proses oksidasi.
c. Hidroksilasi tirosin dan mungkin pada pembentukan katekolamin dan serotonon 5-OH triptamin atau mungkin proses hidroksilasi hormon steroid, obat-obatan aromatik dan karsinogen melalui sistem mikrosomal oksigenasi endoplasmik retikulum hati (LindeCM, 1992).
Penelitian tentang pemberian vitamin c 500 mg dan 1000 mg dapat mengatasi beberapa infeksi virus serta pemberian vitamin c 200 mg dan 500 mg dapat mengatasi kerusakan jaringan yang diakibatkan oleh berbagai logam berat. Penelitian yang dilakukan oleh Dawson dkk telah membuktikan bahwa vitamin c dengan dosis 1000 mg secara signifikan dapat menurunkan kadar Pb darah pada perokok(Dawson et al., 1999)
BAB 3
METODOLOGI PENELITIAN
3.1. Desain Penelitian
Penelitian yang dilakukan pada penelitian ini adalah eksperimental laboratorik dengan Rancangan Acak Lengkap (RAL). Sebanyak 34 ekor mencit jantan (Mus musculus L) dibagi dalam 5 kelompok percobaan. Masing-masing kelompok terdiri dari 7 ekor mencit. Adapun penentuan jumlah ulangan dengan menggunakan Rancangan Acak Lengkap adalah sebagai berikut :
t(r-1) ≥ 20 t : Jumlah Perlakuan
r : Jumlah Ulangan(Sugandi and Sugiharto, 1994) 3.2. Tempat dan Waktu Penelitian
Tempat : Penelitian dilakukan di Laboratorium Balai Penyidikan dan Pengujian Veteriner (BPPV) Medan, dalam waktu 12 minggu
3.3. Populasi Penelitian
Populasi adalah Mencit jantan Mus musculus L. Strain Balb c, berumur 6-8 minggu dengan berat badan 20-50 gram, yang diperoleh dari Badan Penyidikan dan Pengujian Veteriner (BPPV) Medan.
3.4. Variabel Penelitian
3.4.1. Variabel Indipenden, yaitu Pb asetat dan Vitamin C
3.4.3 Variabel kendali, yaitu jenis kelamin, umur, berat badan, kesehatan dan lingkungan
3.5.Bahan
a. Sediaan Plumbum Aceticum (Lead acetate) dalam bentuk kristal (CH3COO)2Pb
3H2O made in Germany diencerkan dengan aquadest
b. L(+) Ascorbic Acid produk PT.Merck c. Pellet produksi PT.Mabar Feed Medan 3.6. Alat
a. Peralatan untuk pemeriksaan aktivitas enzim ALAD (Spectro Fotometer Genesis Tm20) yang terkalibrasi dengan baik
b. Peralatan untuk pemeriksaan kadar hemoglobin (Spectro Fotometer Genesis
Tm
20) yang terkalibrasi dengan baik
c. Peralatan untuk pemeriksaan hapusan darah (Pewarnaan Menurut Giemsa) d. Timbangan hewan
e. Termometer ruangan f. Spuit 1ml merek Trumo 3.7. Pelaksanaan Penelitian
3.7.1 Pemeliharaan Hewan Coba
dimasukkan kedalam tiap kandang terpisah, setiap kandang diberi tanda sesuai dengan perlakuan(Kusumawati)
3.7.2. Perlakuan Hewan Coba
a. Sampel dibagi menjadi lima kelompok masing-masing kelompok terdiri dari tujuh ekor mencit, kecuali kelompok kontrol 6 ekor mencit
b. Kelompok 1 adalah kelompok kontrol yang diberi aquadest
c. Kelompok 2 adalah kelompok yang diberi perlakuan dengan timbal acetat dosis 20 mg/kgBB secara intraperitoneal selama 2 hari (Gajawat et al., 2006) d. Kelompok 3 adalah kelompok yang diberi perlakuan Vitamin C dosis 200
mg/kgBB secara oral selama 7 hari. Satu jam setelah pemberian Vitamin C pada hari ketujuh dilanjutkan dengan pemberian timbal acetat 20mg/kgBB secara intraperitoneal selama 2 hari (Klenner, 1997)
e. Kelompok 4 adalah kelompok yang diberi perlakuan Vitamin C dosis 500mg/kgBB secara oral selama 7 hari. Satu jam setelah pemberian Vitamin C pada hari ketujuh dilanjutkan dengan pemberian timbal acetat 20mg/kgBB secara intraperitoneal selama 2 hari
g. Dilakukan pemeriksaan kadar enzim ALAD, kadar hemoglobin,dan basophilic stippling pada mencit pada tiap kelompok penelitian, setelah itu mencit dibunuh secara dislokasi leher.
3.8. Prosedur Pemeriksaan
3.8.1. Pemeriksaam enzim ALAD
a. Pembuatan larutan pereaksi untuk pemeriksaan enzim ALAD
Alat dan Bahan
Alat yang digunakan dalam pembuatan larutan pereaksi yaitu : timbangan analitik, labu ukur 100ml, pH meter, baker glas 250ml, gelas ukur 500ml dan 100ml.
Bahan kimia yang digunakan adalah : Na2HPO412H2O, NaH2PO42H2O, ALA,
Trichloro asetat (TCA), HgCl2, Triton X 100, p-dimethylaminobenzaldehyd, asam
acetat glacial, asam perclorat, aquadest. Cara kerja
a. Larutan triton X-100
0,5 ml troton x 100 dicampur denga 500ml aquadest
b. Larutan buffer natrium fosfat pH 6,2
Sebanyak 53,72 g Na2HPO412H2O ditimbang dilarutkan didalam 500 ml
aquadest (larutan A), NaH2PO42H2O 23,4 dilarutkan dalam 500 ml aquadest (larutan
c. Larutan ALA 125mmol/L
Sebanyak 209,5 mg ALA dilarutkan hingga 100mL dan disimpan dalam 40C d. Larutan Trichloro asetat(TCA) 60g/L yang mengandung HgCl2 60mmol /L
15g TCA dan 4g HgCl2 dilarutkan dengan aquadest hingga 250 mL aquadest
e. Larutan pereaksi Erlich
Timbang 2,0 g p-dimethylaminobenzaldehyd kemudian larutkan dalam 60 mL asam acetat glacial, selanjutnya tambahkan 32 mL asam perclorat 70% sambil diaduk tambahkan asam acetat hingga 100 mL (Wigfield & Farant,1981)
Prosedur penentuan aktivitas enzim ALAD dalam darah
Aktivitas enzim ALAD dilakukan sesuai metode (Wigfield&Farant, 1981),yaitu:
400 µL aquadest. Setelah 5 menit, absorbansi diukur pada panjang gelombang 555 nm (Wigfield and Farrant, 1981)
3.8.2. Penentuan Hematokrit
Digunakan untuk menentukan aktivitas enzim ALAD a. Alat dan Bahan
Alat dan Bahan yang digunakan adalah: pipet hematolrit, centrifuger hematokrit, skala hematokrit, lilin(wax)
b. Cara Kerja
Sampel darah dimasukkan dimasukkan kedalam pipet hematokrit hingga hampir penuh(2/3 dari panjang pipet), tutup salah satu ujung pipet dengan lilin centrifuger selama 5 menit dengan kecepatan 16.000 rpm, persentase hematokrit dibaca dengan skala khusus.
3.8.3. Pemeriksaan Kadar Hemoglobin
Kadar Hemoglobin ditentukan dengan metode Fotoelektrik
Cyanmethemoglobin (Gandasoebrata,1992) a. Alat dan Bahan
Alat yang digunakan : mikro pipet, spectrofotometer, tabung reaksi
Bahan yang digunakan : sampel darah dan reagen hemoglobin berupa kit dari PT. Human
b. Cara Kerja
tersebut Diamkan kurang lebih selama 10 menit pada suhu kamar, kemudian diukur serapannya dengan spektrofotometer pada panjang gelombang 540 nm. (SoebrataGanda, 1992)
3.8.5 Pemeriksaan Hapusan Darah
Pemeriksaan hapusan darah dilakukan dengan metode Giemsa (Gandasoebrata ,1992) a. Alat dan Bahan
Alat yang digunakan : Objec glass, kaca pendorong(untuk membuat hapusan darah)
Bahan yang digunakan : Sampel darah dan reagen Giemsa dari PT.Merck, aquadest serta metanol.
b. Cara Kerja
Letakkan satu tetes kecil darah, pada 2-3 mm dari ujung kaca objek. Letakkan kaca penghapus dengan sudut 30-450 terhadap kaca objek didepan tetesan darah. Tarik kaca pengahapus kebelakang huingga menyentuh tetesan darah, tunggu hingga darah menyebar pada sudut tersebut. Dengan gerakan yang cepat dorong kaca penghapus hingga terbentuk hapusan darah sepanjang 3-4 cm pada kaca objek. Biarkan hapusan darah mengering diudara lalu warnai dengan pewarnaan Giemsa (SoebrataGanda, 1992)
Cara Pemeriksaan Hapusan Darah
basophilik stipling yang tampak secara zig zag per lapangan pandang dalam 1000 eritrosit.
3.9. Analisa Data
BAB 4
HASIL DAN PEMBAHASAN
4.1. Pengaruh perlakuan terhadap aktivitas enzim ALAD
Pengaruh pemberian Pb terhadap aktivitas enzim ALAD dan pengaruh pemberian Pb dengan vitamin c 200mg/kgBB, vitamin c 500mg/kgBB dan 1000mg/kgBB dapat dilihat pada tabel berikut ini :
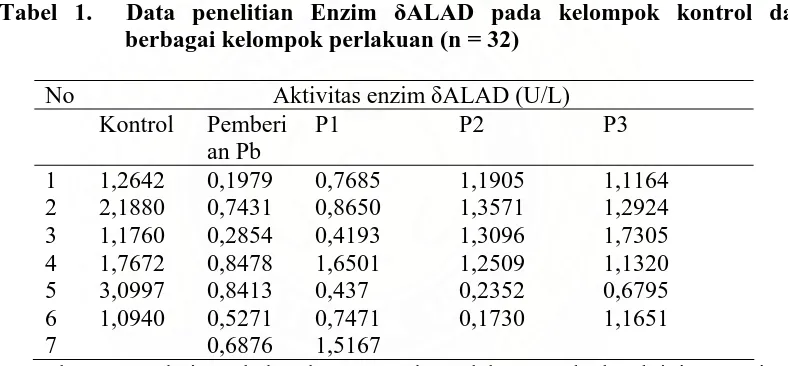
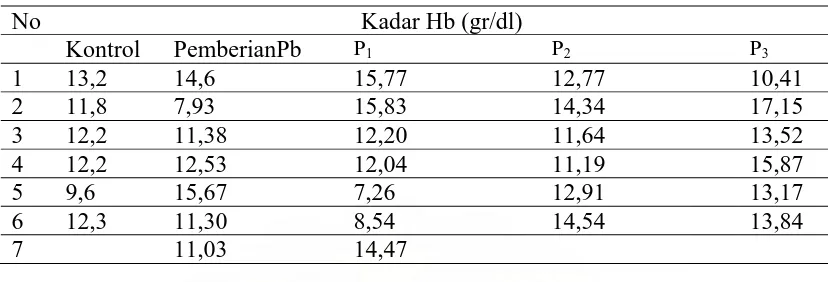
Tabel 1. Data penelitian Enzim ALAD pada kelompok kontrol dan berbagai kelompok perlakuan (n = 32)
No Aktivitas enzim ALAD (U/L)
Kontrol Pemberi an Pb
P1 P2 P3
1 1,2642 0,1979 0,7685 1,1905 1,1164 2 2,1880 0,7431 0,8650 1,3571 1,2924 3 1,1760 0,2854 0,4193 1,3096 1,7305 4 1,7672 0,8478 1,6501 1,2509 1,1320
5 3,0997 0,8413 0,437 0,2352 0,6795
6 1,0940 0,5271 0,7471 0,1730 1,1651
7 0,6876 1,5167
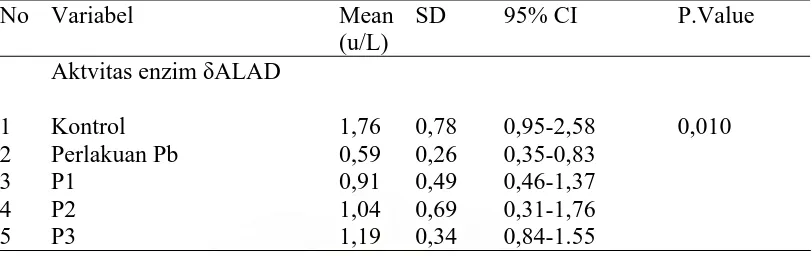
Tabel 2. Distribusi rata-rata Aktivitas Enzin ALAD terhadap kelompok kontrol dan berbagai kelompok perlakuan (n=32)
No Variabel Mean
Aktvitas enzim ALAD Kontrol
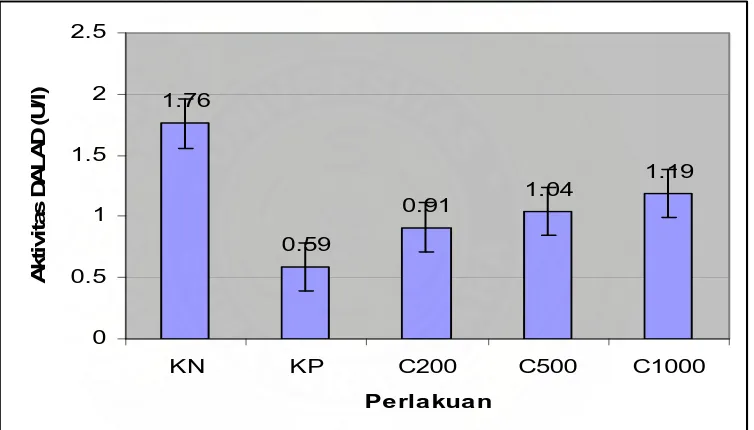
Berdasarkan hasil perhitungan uji anova untuk rata-rata enzim ALAD pada
kontrol yaitu mencit yang tanpa perlakuan adalah 1,76u/L, dengan standar deviasi 0,78. Pada mencit yang diberikan hanya Pb secara intraperitoneal selama 2 hari didapatkan enzim ALAD 0,59u/L dengan standar deviasi 0,26. Pada mencit yang diberikan Vitamin C 200mg/kg BB secara oral selama 1 minggu dan kemudian diberikan Pb secara intraperitonial selama 2 hari ternyata didapatkan enzim ALAD 0,91 /L dengan standar deviasi 0,49. Sedangkan mencit yang diberikan Vitamin C 500mg/kg BB secara oral selama 1 minggu dan kemudian diberikan Pb secara intraperitonial selama 2 hari ternyata enzim, ALAD 1,04µ/L dengan standar deviasi 0,69. Sedangkan mencit yang diberikan Vitamin C 1000mg/kg BB secara oral selama 1 minggu dan kemudian diberikan Pb secara intraperitonial selama 2 hari ternyata didapatkan enzim ALAD 1,19 /Ldengan standar deviasi 0,34.
Dari rangkaian penelitian yang telah dilaksanakan diperoleh hasil uji statistik nilai p = 0,010. Berarti pada alpha 5% ( 0,05) maka H0 ditolak, sehingga dapat
perlakuan. Karena nilai rata-rata Aktivitas enzim ALAD berbeda nyata pada 5 kelompok maka analisis dilanjutkan ke uji LSD, untuk mengetahui kelompok mana yang berbeda secara signifikan yang hasilya seperi tabel dibawa ini :
Tabel 3 Hasil uji LSD Aktivitas enzim ALAD pada kelompok perlakuan (n=32)
Variabel P Value
Aktv Enzim DALAD Kontrol - Perlakuan Pb
Kontrol –Vit C 200mg/kgBB +Perlakuan Pb Kontrol –Vit C 500mg/kgBB +Perlakuan Pb Kontrol –Vit C 1000m/kgBBg +Perlakuan Pb
0,001 0,008 0,027 0,077
Berdasarkan analisis uji LSD didapatkan kelompok yang terdapat perbedaan signifikan adalah antar kelompok kontrol (mencit tanpa perlakuan) dan mencit dengan perlakuan Pb didapatkan p = 0,001, maka H0 ditolak, berarti dapat
disimpulkan bahwa terdapat perbedaan yang signifikan rata-rata nilai aktivitas enzim ALAD pada kedua kelompok perlakuan tersebut. Sementara itu antara kelompok kontrol dengan mencit yang diberikan vitamin C 200mg/kgBB ( secara oral selama 1 minggu) dan diberikan perlakuan Pb (secara intraperitoneal selama 2 hari), dari hasil uji statistik didapatkan p= 0,008 maka H0 ditolak, oleh karena itu dapat disimpulkan
yang signifikan nilai rata-rata aktivitas enzim ALAD pada dua kelompok tersebut. Selanjutnya pada kelompok kontrol dengan kelompok mencit yang diberikan vitamin C 1000 mg/kg BB (secara oral selama 1 minggu) dan pemberian Pb (secara intraperitoneal selama 2hari), didapatkan hasil uji statistik nilai p = 0.077, maka H0
diterima. Berarti dapat disimpulkan bahwa tidak terdapat perbedaan rata-rata nilai aktivitas enzim ALAD pada kedua kelompok perlakuan.
1.76
KN KP C200 C500 C1000
Perlakuan
Gambar 4. Perbandingan Aktivitas enzim ALAD pada Seluruh Kelompok Percobaan
Keterangan:
KN : Kelompok yang hanya diberi aquadest
KP : Kelompok yang diberikan Pb asetat dosis 20 mg/kgBB secara intraperitoneal
C200 : Kelompok yang diberikan vitamin C 200 mg/kgBB/hari selama tujuh hari sebelum diberikan Pb asetat 20 mg/kgBB secara intraperitoneal
C500 : Kelompok yang diberikan vitamin C 500 mg/kgBB/hari selama tujuh hari sebelum diberikan Pb asetat 20 mg/kgBB secara intraperitoneal
C1000 : Kelompok yang diberikan vitamin C 1000 mg/kgBB/hari selama tujuh hari sebelum diberikan Pb asetat 20 mg/kgBB secara intraperitoneal
(1995) yang menyatakan bahwa enzim yang terlibat dalam sintesis hemoglobin terutama enzim ALAD paling rentan terhadap keracunan Pb.
Penurunan enzim tersebut adalah dikarenakan : Toksisitas Pb disebabkan adanya interaksi antara Pb dengan senyawa ligand yang ada didalam tubuh misalnya gugus enzim –SH dari ALAD (yang mengakibatkan penumpukan ALA) dan hem sintetase (mengakibatkan penumpukan protoporfirin) sehingga terjadi hambatan sintesis hemoglobin. Pb juga dapat menghambat enzim ferokelatase yang menyebabkan ion fe tidak dapat berikatan dengan cincin proporpirin, oleh karena terjadi kompetisi antara Pb dengan Fe akibat dari hal tersebut diatas maka Pb dapat mengakibatkan penurunan enzim ALAD (Ganiswara et al., 1995). Keadaan ini sesuai dengan penelitian (Sugiharto and W, 2004) yang menyebutkan bahwa pemberian larutan Pb nitrat [(PbNO3)2] dengan dosis 12 ppm dan 50 ppm selama 30
hari secara oral pada tikus putih memberikan hasil terjadinya penurunan enzim ALAD dan kadar Hb.
C 500mg/kgBB tidak dapat menaikkan nilai aktivitas enzim ALAD, walaupun nilai rata-rata antara kelompok yang diberikan Pb saja, vitamin C 200mg/kgBB + Pb, vitamin C 500 mg/kg BB + Pb didapatkan ada kenaikan aktivitas enzim ALAD, namun kenaikan tersebut masih di bawah nilai kelompok kontrol, dan hal ini dibuktikan hasil uji statistik tidak terdapat perbedaan nilai rata-rata antara kelompok tersebut secara bermakna yang artinya dalam penelitian ini terjadi peningkatan aktivitas enzim ALAD dengan pemberian vitamin C 1000mg/kgBB tetapi tidak dapat memperbaiki hingga sama seperti kontrol.Dalam penelitian ini vitamin C 1000mg/kgBB dapat berperan sebagai zat antioksidan dan detoksikasi dengan cara meningkatkan aktivitas enzim gluthatione S-transferase (GST) serta kelompok enzim gluthatione yang lain (GS-x) yang berperan dalam melenyapkan oksidator kuat (dalam hal ini ion Pb) pada eritrosit dan melindungi gugus enzim-SH eritrosit.
4.2. Pengaruh perlakuan terhadap kadar hemoglobin
Tabel 4. Data penelitian kadar Hemoglobin pada kelompok kontrol dan berbagai kelompok perlakuan (n = 32)
No Kadar Hb (gr/dl)
Untuk mengetahui apakah ada pengaruh perlakuan terhadap kadar Hemoglobin dilakukan uji ANOVA
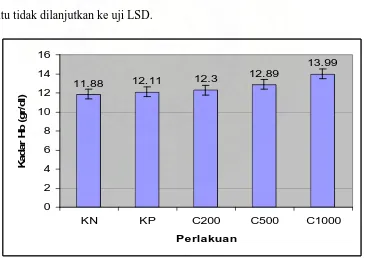
Tabel 5. Distribusi rata-rata kadar Hemoglobin pada kelompok kontrol dan berbagai kelompok perlakuan (n = 32)
No Variabel Mean
dengan standar deviasi 3,39. Sedangkan mencit yang diberikan vitamin C 500mg/kg BB(P2) secara oral selama 1 minggu dan kemudian diberikan Pb secara intraperitoneal selama 2 hari ternyata didapatkan kadar Hb 12,89gr/dl dengan standar deviasi 1,36. Sedangkan mencit yang diberikan vitamin C 1000mg/kg BB (P3) secara oral selama 1 minggu dan kemudian diberikan Pb secara intraperitonial selama 2 hari ternyata didapatkan kadar Hb 13,99gr/dl dengan standar deviasi 2,33.
Dari rangkaian penelitian yang telah dilaksanakan diperoleh hasil uji statistik nilai p = 0,554. Berarti pada alpha 5% ( 0,05) maka H0 diterima, sehingga dapat
disimpulkan tidak ada perbedaan kadar Hb diantara 5 kelompok perlakuan, oleh karena itu tidak dilanjutkan ke uji LSD.
11.88 12.11 12.3
KN KP C200 C500 C1000
Keterangan:
KN : Kelompok yang hanya diberi aquadest
KP : Kelompok yang diberikan Pb asetat dosis 20 mg/kgBB secara intraperitoneal
C200 : Kelompok yang diberikan vitamin C 200 mg/kgBB/hari selama tujuh hari sebelum diberikan Pb asetat 20 mg/kgBB secara intraperitoneal
C500 : Kelompok yang diberikan vitamin C 500 mg/kgBB/hari selama tujuh hari sebelum diberikan Pb asetat 20 mg/kgBB secara intraperitoneal
C1000 : Kelompok yang diberikan vitamin C 1000 mg/kgBB/hari selama tujuh hari sebelum diberikan Pb asetat 20 mg/kgBB secara intraperitoneal
Gambar tersebut menunjukkan peningkatan kadar Hemoglobin antara kelompok kontrol dengan kelompok perlakuan, Hal ini tidak sesuai dengan teori yang mengemukakan Berdasarkan penelitian yang telah dilakukan, diketahui bahwa tingginya kadar Pb dalam tubuh dapat mengakibatkan terganggunya sistem metabolisme tubuh. Salah satu jalur matabolisme yang sangat rentan terhadap Pb adalah sistem hemopoetik, sebab hampir 90 % Pb terikat eritrosit. (WHO, 1977)
Gambaran anemia adalah karakteristik untuk penderita keracunan Pb kronis. Ini adalah akibat menurunnya masa hidup (lifesfan) eritrosit disebabkan interfensi logam Pb dalam sintesis haem. Pb menghambat enzim -aminolevulinic acid dehydratase dan ferrochelatase dalam eritrosit, akibatnya terjadi anemia (Hariono, 2008).
dehydratase dan ferokelatase (Jeffe.1991). Menurut Darmono (1995) pemberian Pb dosis tinggi dapat menyebabkan penurunan ion Fe dan mengakibatkan gejala anemia sebab terdapat penurunan daya absorbsi ion Fe dari sel epitel usus, sehingga terjadi kompetisi antara Pb dan Fe pada protein carier logam (terutama protein ferritin). Kadar ferritin yang rendah merupakan indikator spesifik defisiensi Fe baik untuk terjadi anemi atau tidak. Hal ini dapat mengakibatkan penurunan nilai hematokrit dan mean corpuscular, serta kadar Hb.
didalam ruangan. Keracunan yang kronis yaitu keracunan yang terjadi karena absorbsi Pb dalam jumlah kecil, tetapi terjadi dalam jangka waktu yang lama dan terakumulasi didalam tubuh. Durasi waktu dari permulaan terkontaminasi sampai terjadi gejala atau tanda-tanda keraacunan mungkin dalam beberapa bulan bahkan sampai beberapa tahun(Ariens, 1978)
4.3. Pengaruh perlakuan terhadap jumlah Basophilic Stippling
Pengaruh pemberian Pb terhadap jumlah Basophilic Stippling dan pengaruh pemberian Pb dengan vitamin C 200mg/kgBB, vitamin C 500mg/kgBB dan 1000mg/kgBB dapat dilihat pada tabel berikut ini :
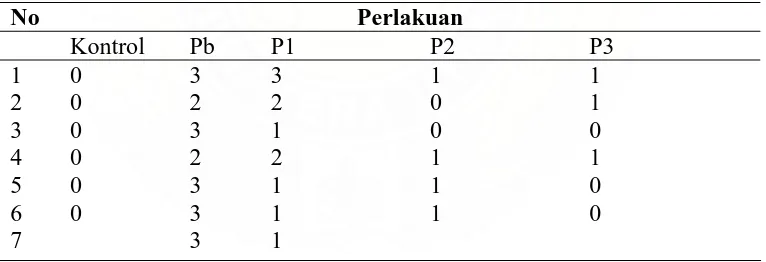
Tabel 6. Distribusi basophilic stippling pada kelompok perlakuan (n = 32)
No Perlakuan
Tabel 7. Hasil Kruskal Walis Basophilic Stpipling pada kelompok perlakuan (n=32)
Variabel Mean SD Kruskal
Wallis
P value Basophilic Stipling
Perlakuan 2,97 1,40 24.274 0.000
Berdasarkan data di atas didapatkan nilai rata-rata basophilic stipling kelompok perlakuan adalah 2.97 dengan standar deviasi 1.40. Dari hasil perhitungan Kurskal Wallis H didapat nilai 24.274, sedang harga X2 tabel dengan tingkat
kepercayaan ( ) 0.05 dengan dk = 4, dapat harga = 9.488. Karena X2 hitung 24.274 >
X2tabel 9.488, maka H0 ditolak. Dengan demikian dapat disimpulkan bahwa terdapat
perbedaan yang significan nilai Basophilic stippling pada kelima kelompok perlakuan.
Hasil analisis statistik penelitian ini menunjukkan terdapat perbedaan nilai rata-rata yang bermakna antara kelompok kontrol dengan perlakuan, akan tetapi pada uji Kruskal Wallis ini tidak diketahui kelompok mana yang memiliki perbedaan tersebut secara signifikan, maka dilanjutkan dengan uji Mann-Whitney untuk menentukan kelompok mana yang berbeda.
0
KN KP C200 C500 C1000
Perlakuan
Gambar 6. Jumlah Basophilic Stippling Pada Kelompok Kontrol dan Perlakuan
Keterangan:
KN : Kelompok yang hanya diberi aquadest
KP : Kelompok yang diberikan Pb asetat dosis 20 mg/kgBB secara intraperitoneal
C200 : Kelompok yang diberikan vitamin C 200 mg/kgBB/hari selama tujuh hari sebelum diberikan Pb asetat 20 mg/kgBB secara intraperitoneal
C500 : Kelompok yang diberikan vitamin C 500 mg/kgBB/hari selama tujuh hari sebelum diberikan Pb asetat 20 mg/kgBB secara intraperitoneal
C1000 : Kelompok yang diberikan vitamin C 1000 mg/kgBB/hari selama tujuh hari sebelum diberikan Pb asetat 20 mg/kgBB secara intraperitoneal
Pada uji Mann-Whitney didapatkan kelompok yang terdapat perbedaan signifikan adalah antar kelompok kontrol (mencit tanpa perlakuan) dan mencit dengan perlakuan Pb didapatkan p = 0,001, maka H0 ditolak, berarti dapat disimpulkan
terdapat perbedaan yang signifikan jumlah rata-rata basophilic stipling pada kedua kelompok perlakuan. Pada kelompok kontrol dengan kelompok mencit diberikan vitamin C 500mg/kgBB ( secara oral selama 1 minggu) dan diberikan perlakuan Pb (secara intraperitoneal selama 2 hari), dari hasil uji statistik Mann -Whytney didapatkan p = 0,019, maka H0 ditolak. Berarti dapat disimpulkan terdapat perbedaan
yang signifikan jumlah rata-rata basophilic stipling pada dua kelompok tersebut. Selanjutnya pada kelompok kontrol dengan kelompok mencit yang diberikan vitamin C 1000 mg/kg BB (secara oral selama 1 minggu) dan pemberian Pb (secara intraperitoneal selama 2 hari), didapatkan hasil uji statistik nilai p = 0.056, maka H0
diterima. Berarti dapat disimpulkan bahwa tidak terdapat perbedaan jumlah rata-rata basophilic stipling pada kedua kelompok perlakuan Pb dengan vitamin C 1000mg/kgBB dengan kelompok kontrol. Dengan demikian pada penelitian ini dapat diketahui bahwa pemberian vitamin C 1000mg/kgBB dapat menurunkan jumlah basophilic stippling di dalam darah mencit yang diberikan Pb.
Kurniawati (1996) menyebutkan bahwa pemberian larutan timbal dapat menyebabkan kerusakan eritrosit (Kurniawati, 1996). Hal ini juga didukung oleh penelitian (Wahyuni, 2000) yang menyatakan pemberian larutan timbal dapat menurunkan nilai volume padat eritrosit (PCV/packed cell volume).
Selain itu, Pb juga memberikan dampak negatif bagi proses eritropoesis maupun pematangan eritrosit. Pb yang berikatan dengan eritrosit menyebabkan eritrosit menjadi rapuh (terjadi kerusakan membran sel), mengurangi eritropoesis, mengurangi masa hidup eritrosit matang, dan menyebabkan terjadinya anemia hemolitik (Lu, 1995).
BAB 5
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Berdasarkan hasil penelitian yang telah dilakukan dan pembahasan yang telah diuraikan, penulis berkesimpulan bahwa :
1. Pada rentang dosis perlakuan, Pb tidak mematikan terhadap hewan coba. 2. Terdapat penurunan aktivitas enzim ALAD pada mencit yang diberi Pb
3. Pemberian Vitamin C 1000 mg/kgBB/oral selama 1 minggu dapat meningkatkan aktivitas enzim ALAD
4. Terjadi peningkatan kadar Hb antara kelompok kontrol dengan kelompok perlakuan namun tidak significan.
5 Terdapat basophilic stippling pada kelompok mencit yang diberi Pb
5.2 Saran
1. Perlu diadakan penelitian lebih lanjut tentang pemeriksan hematologi lainnya. 2. Perlu dilakukan penelitian lebih lanjut dengan menggunakan hewan uji lebih
banyak sehingga hasil yang didapatkan lebih sempurna.
DAFTAR PUSTAKA
ALMATSIER (2003) Prinsip Dasar Ilmu Gizi, Jakarta.
ARDYANTO, D. (2005) Deteksi Pencemaran Timah Hitam(Pb) Dalam Darah Masyarakat Yang Terpajan Timbal(Pb). J Kes Ling, 2.
ARIEF, R. (2006) Radikal Bebas, Surabaya. ARIENS, E. J. (1978) Toksokologi Umum.
BARTIK, M. (1981) Veterinary Toksicology. Elsevier Scientific Publishing Company.
CHILD, J. A. (1990) Hematologi Klinik, Jakarta.
DARMONO (2005) Toksikologi Logam Berat, Surabaya.
DAWSON, E. B., EVANS, D. R., HARRIS, W. A., CTETER, M. & MCGANITY, W. J. (1999) The Effect of Ascorbit Acid Suplementation on the Blood Lead Levels of Smokers. Journal of the American College of Nutrition, 18, 166-70. EMA, A. R. (2006) Pengaruh Suplementasi vitamin C dan E Terhadap Profil Lipid
Pada Pasien Penyakit Jantung Koroner di Poliklinik Kardiologi Ruamah Sakit Umum Dokter Slamet Garut. J Sains Kesehatan, 2.
GAJAWAT , S., SANCHETI, G. & K, G. P. (2006) Protection Against Lead Induced Hepatic Lesion in Swiss Albino Mice by Ascorbic Acid.
Pharmacologyonline, 1, 140-9.
GANISWARA, S., SEIIABUDU, R., SYAMSUDIN, U. & BUSTAM, Z. (1995) Farmakologi dan Terapi. Fakultas Kedokteran Indonesia Jakarta.
GOLDSTEIN, B. D. & KIPEN, H. M. (1994) Hematologic Disolder In Levy and Wegmen. Occupational Health Recognizing and Preventing Work-Realted Deseases 3 rd.
HABAL, M. R. (2006) Toxicity, Lead. American college, 1-10.
HARIONO, B. (2008) Polusi Logam Berat Plumbum di Lingkungan Perubahan Patologik dan Pemantauannya. Universitas Gajah Mada. Yogyakarta. HASAN, M. Z. & SETH, T. D. (1981) Effect of Lead and Zinc Administration of
Liver,Kidney and Brain Levels of Copper, Lead,Manganes and Zinc on Erithrocyte ALA-D Activity In Rats. Toxicology, 353-58.
KING, M. & S, M. (2004) Heme and Porphyrin Metabolism. University of Brescia. KLENNER, F. (1997) Significance of High Daily Intake of Ascorbic Acid in
Preventive Medicine Medicine, 1 .
KURNIAWATI, H. (1996) Pengaruh pemberian Larutan Timbel Anorganik Per Oral Terhadap Inklusi Eritrosit Pada Mencit. FMIPA. Surabaya
.
KUSUMAWATI, S. U. D. Bersahabat Dengan Hewan Coba. Gajah Mada University Press. Surabaya.
LINDECM (1992) Nutritional Biochemistry and Metabolism. Elsevier Scientific Publishing Company, 167-177.
LU, F. (1995) Toksikologi Dasar. UI Press Jakarta.
MAYES (1995) Harper's Review of Biochemistry. Lange Medical Publication, 370-376.
MUGAHI, NM, H. & Z, H. (2000) Effect of Chronic Lead Acetate Intoxication on Blood Indices of Male Adul Rats. Medical Science.
MURRAY, K., KD.GRENNER, MAYES, A. & WV.RODWEL (2003) Biokimia Harper, Jakarta.
PALAR, H. (1994) Pencemaran dan Toksikologi Logam Berat, Jakarta. RETNOGITAWATI (1995) Radikal Bebas-Sifat dan Peran dalam
SCINICARIELLO, FRANCO, MURRAY, EDWARD, H., MOFFETT, B, D., ABADIN, G, H., SEXTON, J, M., FOWLER & A, B. (2007) Lead and delta-aminolevulinic acid dehydratase polymorphism. Environmental Health Perspectives.
SHANNON, M. W. (1998) Clinical Managemen of Poisoning and Drug Overdose. Sponsorhip of the United Nation Enviroment Program and The World Health, 3 rd, 767-784.
SOEBRATAGANDA, R. (1992) Penuntun Laboratorium Klinik. Dian Rakyat Jakarta.
SUDARMAJI, J, M. & IP, C. (2006) Toksikologi Logam Berat B3 dan Dampaknya Terhadap Kesehatan. J Kes Ling, 2.
SUGANDI, E. & SUGIHARTO (1994) Rancangan Percobaan Teori dan Aplikasi, Jakarta.
SUGIHARTO & W, D. (2004) Uji Toksisitas antara Timbal dan Kadmium pada pemeriksaan Kadar Hb,Jumlah Eritrosit dan nilai PCV Tikus Putih. Unair Surabaya.
SURYOHUDOYO, P. (2003) Kapita Selecta:Ilmu Kedokteran Molekuler, Surabaya. TMARTIANA (2007) Use of Hematological and Immunological Biomarker As
indicator of Pb Intoxication. Folia Medica Indonesia, 43, 148-152. WAHYUNI, A. (2000) Pengaruh Pemberian Ekstrak Akar Ginseng Terhadap
Volume padat eritrosit dan Kadar Timbal Darah Tikus Putih Yang Diberi Perlakuan Larutan Timbal. Unair Erlangga.
WHO (1977) Lead Enviromenmental Health. Published Under The Joint Organization Ganeva, 3.
HASIL PENGOLAHAN PENELITIAN SECARA STATISTIK
Blank 6 11.8833 1.21065 .49424 10.6128 13.1538 Kontrol Pb 7 12.1143 2.60769 .98561 9.7026 14.5260
Blank 6 1.764854 .7756539
.316659
4 .950855 2.578853 Kontrol Pb
7 .590042 .2623909 .099174
4 .347371 .832713 P1
7 .914825 .4879860 .184441
4 .463513 1.366137 P2
6 1.038467 .6877962 .280791
6 .316669 1.760265 P3
6 1.193927 .3369777 .137570
6 .840290 1.547563 Total
32 1.078674 .6364436 .112508
Multiple Comparisons
Kontrol Pb -.2310 1.32654 .863 -2.9528 2.4909 P1 -.4181 1.32654 .755 -3.1399 2.3037 P2 -1.0150 1.37661 .467 -3.8396 1.8096 Kontrol BlankP3 -2.1100 1.37661 .137 -4.9346 .7146 Kontrol Pb Kontrol Blank .2310 1.32654 .863 -2.4909 2.9528 P1 -.1871 1.27450 .884 -2.8022 2.4279 P2 -.7840 1.32654 .559 -3.5059 1.9378 P3 -1.8790 1.32654 .168 -4.6009 .8428 P1 Kontrol Blank .4181 1.32654 .755 -2.3037 3.1399 Kontrol Pb .1871 1.27450 .884 -2.4279 2.8022 P2 -.5969 1.32654 .656 -3.3187 2.1249 P3 -1.6919 1.32654 .213 -4.4137 1.0299 P2 Kontrol Blank 1.0150 1.37661 .467 -1.8096 3.8396 Kontrol Pb .7840 1.32654 .559 -1.9378 3.5059 P1 .5969 1.32654 .656 -2.1249 3.3187 P3 -1.0950 1.37661 .433 -3.9196 1.7296 P3 Kontrol Blank 2.1100 1.37661 .137 -.7146 4.9346 Kontrol Pb 1.8790 1.32654 .168 -.8428 4.6009 P1 1.6919 1.32654 .213 -1.0299 4.4137 KADARHB
P2 1.0950 1.37661 .433 -1.7296 3.9196 AKTENZIM Kontrol Blank Kontrol Pb 1.174813
(*)
.298705
4 .001 .561920 1.787705 P1 .850029(
*)
.298705
4 .008 .237136 1.462922 P2 .726388(
*)
.309981
3 .027 .090359 1.362417 P3
.570927 .309981
3 .077 -.065102 1.206956 Kontrol Pb Kontrol Blank
-1.174813 (*)
.298705
4 .001 -1.787705 -.561920 P1
-.324783 .286986
9 .268 -.913632 .264065 P2
-.448425 .298705
4 .145 -1.061318 .164468 P3
-.603885 .298705
4 .053 -1.216778 .009008 P1 Kontrol Blank
*) Kontrol Pb
.324783 .286986
9 .268 -.264065 .913632 P2
-.123642 .298705
4 .682 -.736535 .489251 P3
-.279102 .298705
4 .358 -.891995 .333791 P2 Kontrol Blank
-.726388( *)
.309981
3 .027 -1.362417 -.090359 Kontrol Pb
.448425 .298705
4 .145 -.164468 1.061318 P1
.123642 .298705
4 .682 -.489251 .736535 P3
-.155460 .309981
3 .620 -.791489 .480569 P3 Kontrol Blank
-.570927 .309981
3 .077 -1.206956 .065102 Kontrol Pb
.603885 .298705
4 .053 -.009008 1.216778 P1
.279102 .298705
4 .358 -.333791 .891995 P2
.155460 .309981
3 .620 -.480569 .791489
Kruskal-Wallis Tes
PERLAKUA N
Mean
N Mean Rank Sum of Ranks
Ranks
N Mean Rank Sum of Ranks
Test Statisticsb
N Mean Rank Sum of Ranks