PENGARUH TEKANAN DAN SUHU PADA KONDISI
EVAPORASI EKSTRAK DAUN TEH HIJAU
DODO HANDOKO
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
ABSTRAK
DODO HANDOKO. Pengaruh Tekanan dan Suhu pada Kondisi Evaporasi Ekstrak Daun Teh Hijau. Dibimbing oleh DUDI TOHIR dan BAMBANG SRIJANTO.
Pemanfaatan bahan-bahan alami sebagai sarana penunjang kesehatan sebenarnya telah diterapkan oleh manusia sejak lama, terutama tanaman teh (Camellia sinensis). Teh hijau merupakan salah satu jenis produk teh yang diperoleh tanpa mekanisme fermentasi. Teh hijau berkhasiat untuk menyembuhkan berbagai penyakit terutama penyakit kanker, karena kandungan senyawa polifenol yang melimpah, terutama epigalokatekin, epigalokatekin-galat, epikatekin, dan epikatekin-galat. Berbagai macam perlakuan telah digunakan untuk mengoptimumkan ekstraksi polifenol yang terdapat dalam teh hijau, tetapi perlakuan kondisi evaporasi pelarut belum banyak dilaporkan.
Dalam penelitian ini, 80 gram serbuk teh hijau berukuran 18 mesh dimaserasi dalam 800 ml air bebas ion, selama 20 menit pada suhu konstan, yaitu 80 °C. Setelah itu, larutan diuapkan dengan 3 variasi tekanan dalam labu (80, 90, dan 100 mBar) dan 3 variasi suhu penangas (50, 60, dan 70 °C), selanjutnya ditentukan kondisi optimumnya berdasarkan laju penguapan tertinggi. Kondisi optimum evaporasi diperoleh pada saat tekanan dalam labu dan suhu penangas berturut-turut adalah 90 mBar dan 70oC, dengan waktu dan laju penguapan sebesar 0,7425 jam dan 0,0707 (g/det). Kadar polifenol dari 80 gram serbuk teh hijau ditentukan dengan spektrofotometri sinar tampak pada panjang gelombang 725 nm, perolehannya sebesar 25,4136 ppm atau 3,63% (b/b).
ABSTRACT
DODO HANDOKO. Effect of Pressure and Temperature on Evaporation Condition of Green Tea Extract. Supervised by DUDI TOHIR and BAMBANG SRIJANTO.
Natural substances have been studied and applied as health supplements by human being for long ago, especially tea crop (Camellia sinensis). Green tea represents one of type of tea products that is obtained by nonfermentation mechanism. It is useful to heal various diseases especially cancer, caused by the excess of polyphenols substances, such as epigallocatechin, epigallocatechin-gallate, epicatechin, and epicatechin-gallate. Many treatments have been used to optimized green tea polyphenols extraction, but solvent evaporation condition treatments have not been reported.
ii
PENGARUH TEKANAN DAN SUHU PADA KONDISI
EVAPORASI EKSTRAK DAUN TEH HIJAU
DODO HANDOKO
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Sains pada
Departemen Kimia
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
Judul : Pengaruh Tekanan dan Suhu pada Kondisi Evaporasi Ekstrak Daun Teh Hijau
Nama : Dodo Handoko NIM : G01499074
Pembimbing I,
Drs. Dudi Tohir, MS.
NIP 131 851 277
Menyetujui,
Pembimbing II,
Ir. Bambang Srijanto
NIP 680 003 303
Mengetahui,
Dekan Fakultas Matematika dan Ilmu Pengetahuan Alam Institut Pertanian Bogor
Prof. Dr. Ir. Yonny Koesmaryono, MS
NIP 131 473 999
PRAKATA
Puji dan syukur penulis panjatkan kepada Allah SWT yang telah memberikan rahmat dan karunia-Nya sehingga penulis dapat menyelesaikan laporan penelitian yang berjudul
Pengaruh Tekanan dan Suhu pada Kondisi Evaporasi Ekstrak Daun Teh Hijau.
Penulis mengucapkan terima kasih kepada Bapak Drs. Dudi Tohir, MS dan Bapak Ir. Bambang Srijanto, selaku pembimbing yang telah memberikan masukan dan pengarahan kepada penulis. Terima kasih tak terhingga kepada kedua orangtua tercinta, Ibu Prof. Dr. Ir. Tun Tedja Irawadi, MS selaku ketua Departemen Kimia, Bapak Prof. Dr. Ir. Yonny Koesmaryono, MS selaku Dekan FMIPA IPB, Bapak Kusnata, mas Pipit, dan Agung serta adikku tercinta Wulandari yang selalu memberikan doa, dorongan semangat, bantuan materi, kesabaran, dan kasih sayang serta kepercayaan kepada penulis.
Terima kasih juga penulis ucapkan kepada staf dan laboran di Laboratorium Teknologi Farmasi dan Medika, sahabatku Wakhid Lukas S. Si,Budi Arifin S.Si, Mas Herry, Pak Sabur, Ibu Yenni, Ibu AA, Teh Nung, Marudut serta teman-teman Mexindo 18 atas bantuan, masukan dan kerja samanya selama penelitian dan penulisan karya ilmiah ini
Semoga karya ilmiah ini dapat bermanfaat bagi dunia ilmu pengetahuan.
Bogor, Mei 2007
v
RIWAYAT HIDUP
Penulis dilahirkan di Jakarta pada tanggal 11 Juni 1981 sebagai anak kedua dari tiga bersaudara, anak pasangan Soerodjo HS dan Tjitjih.
Pendidikan formal penulis sampai tingkat SMU diselesaikan di Jakarta, yaitu SD Negeri 04 Petang Pondok Pinang, SMP Negeri 87 Pondok Pinang, dan SMU Negeri 29 Jakarta dari tahun 1987-1999. Penulis diterima di Program Studi Kimia, Departemen Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor melalui jalur Seleksi Penerimaan Mahasiswa Baru (SPMB) pada tahun 1999. Bidang yang diminati ialah Kimia Organik.
DAFTAR ISI
Halaman
DAFTAR TABEL... vii
DAFTAR GAMBAR ... vii
DAFTAR LAMPIRAN... vii
PENDAHULUAN ... 1
TINJAUAN PUSTAKA Tanaman Teh... 1
Kandungan Polifenol Teh Hijau... 2
Optimalisasi Metode Ekstraksi Teh Hijau ... 3
Penguapan Pelarut ... 3
Analisis Kuantitatif Polifenol... 4
BAHAN DAN METODE Bahan dan Alat... 4
Metode Penelitian... 4
Ekstraksi... 4
Analisis Kuantitatif Total Polifenol ... 5
HASIL DAN PEMBAHASAN Ekstraksi Serbuk Daun Teh Hijau... 5
Optimalisasi Kondisi Evaporasi Ekstrak Cair Teh Hijau ... 6
Analisis Kadar Polifenol Ekstrak Teh Hijau ... 7
SIMPULAN DAN SARAN Simpulan ... 8
Saran ... 8
DAFTAR PUSTAKA ... 8
DAFTAR TABEL
Halaman
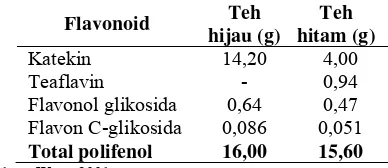
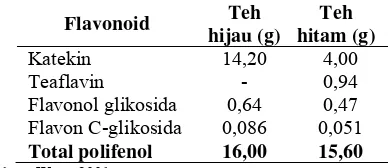
1 Kandungan flavonoid daun teh hijau dan teh hitam tiap 100 g bobot ... 2
2 Peubah evaporasi ekstrak cair yang digunakan pada penelitian ... 4
DAFTAR GAMBAR
Halaman 1 Daun tanaman teh ... 12 Struktur polifenol terbesar pada daun teh hijau... 3
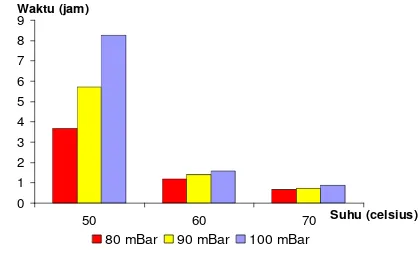
3 Pengaruh tekanan dan suhu terhadap waktu evaporasi ... 6
4 Pengaruh tekanan dan suhu evaporasi terhadap laju penguapan air... 7
5 Pengaruh suhu dan tekanan terhadap konsentrasi polifenol ... 7
DAFTAR LAMPIRAN
Halaman 1 Jenis-jenis kelompok teh ... 112 Kandungan senyawa kimia teh hijau ... 11
3 Diagram alir penelitian ... 12
4 Kadar air serbuk teh hijau (AOAC 1984)... 13
5 Kadar abu serbuk teh hijau (AOAC 1984) ... 13
6 Hasil evaporasi ekstrak cair daun teh ... 14
7 Hasil pemetaan kehomogenan laju penguapan air ... 15
8 Hasil analisis dengan metode GLM ... 16
9 Analisis ragam pengaruh tekanan labu dan suhu terhadap penguapan air ... 18
10 Hasil analisis laju penguapan air ... 18
11 Kurva larutan standar ... 18
12 Kadar polifenol ekstrak daun teh... 19
PENDAHULUAN
Beragam cara untuk mendapatkan kesehatan yang optimal seperti berolah raga, mengkonsumsi makanan yang bernutrisi tinggi, dan mengkonsumsi obat-obatan. Namun, penggunaan obat-obatan perlu diwaspadai terutama jika obat tersebut berasal dari bahan sintetik. Hal ini disebabkan karena obat sintetik memiliki efek samping terhadap organ tubuh seperti pada ginjal. Oleh karena itu, seiring dengan kemajuan di bidang kesehatan, saat ini mulai dikembangkan obat-obatan yang berasal dari alam. Pemanfaatan bahan-bahan alami sebagai sarana penunjang kesehatan sebenarnya telah diterapkan oleh manusia sejak lama, terutama tanaman teh. Teh (Camellia sinensis) pertama kali diperkenalkan oleh kaisar Cina Shen Nung (2737 SM) karena mempunyai aroma yang khas dan sekaligus dapat menjaga kesehatan tubuh (Trevisanato 2000). Sejak saat itu, teh telah mulai merebak ke seluruh penjuru dunia karena dapat memberikan perasaan nyaman dan segar ketika meminumnya.
Saat ini telah dikenal ada empat jenis teh dan salah satunya adalah teh hijau yang telah menunjukkan banyak manfaatnya dalam kesehatan. Beberapa penelitian sebelumnya menunjukkan bahwa teh hijau bermanfaat sebagai antibakteri, antioksidan, antiradang, dan antikanker (Miller 2005). Zat aktif dalam teh hijau menurut Picard (1996) antara lain adalah katekin, epikatekin (EC), galokatekin (GC), epigalokatekin (EGC), epigalokatekin galat (EGCG), epikatekin galat (ECG). Senyawa tersebut dikelompokkan dalam senyawa polifenol.
Ekstraksi teh hijau telah dilakukan sebelumnya di antaranya oleh Song (2001), menggunakan metode maserasi dengan ragam suhu, waktu, dan nisbah bahan baku-pelarut. Diperoleh bahwa ekstraksi menggunakan pelarut air pada suhu 90ºC selama 10 menit secara signifikan meningkatkan rendemen ekstrak polifenol dibandingkan dengan pada suhu yang lebih rendah. Namun, untuk mutu ekstrak yang lebih baik digunakan suhu 80ºC karena beberapa senyawa yang tidak diinginkan turut terekstrak pada suhu 90ºC atau lebih.
Selama ini proses penguapan pelarut pada ekstraksi teh hijau belum mendapat perhatian
lebih lanjut sehingga perlu dilakukan optimalisasi pada kondisi evaporasi dengan mengatur suhu penangas dan tekanan dalam labu rotavapor.
Penelitian ini bertujuan untuk mengetahui pengaruh suhu dan tekanan dalam evaporasi pelarut dan konsentrasi polifenol. Selain itu, diharapkan dapat memperoleh kondisi optimum proses penguapan pada pengolahan ekstrak cair teh hijau. Dengan cara tersebut diharapkan proses pengambilan zat aktif menjadi lebih efektif dan efisien sehingga biaya produksi menjadi lebih rendah dengan kualitas yang lebih tinggi.
TINJAUAN PUSTAKA
Tanaman Teh
Tanaman teh termasuk jenis tanaman semak yang umumnya dapat tumbuh dengan baik di daerah beriklim tropis dan sub tropis dengan ketinggian antara 200 dan 2000 meter di atas permukaan laut dengan suhu kelembaban berkisar 14-25°C. Ketinggian tanaman teh jenis assamica
dapat mencapai 6-20 meter. Perkebunan teh umumnya selalu menjaga pertumbuhan tanaman dengan cara melakukan pemotongan sehingga akan mempermudah pemetikan pucuk daun teh. Ketinggian tanaman teh selalu dipelihara agar kurang dari 2 meter. Bunga teh berwarna putih kekuningan dengan diameter 2,5-4 cm, daun teh berukuran panjang sekitar 4-15 cm dengan lebar 2-5 cm dapat dilihat pada Gambar 1 (Wikipedia 2007).
Gambar 1 Daun tanaman teh.
2
fermentasi. Bentuk dan warna keempat kelompok teh dapat dilihat pada Lampiran 1.
Menurut Mukhtar (2000), tahap awal memproduksi teh hitam dan oolong adalah dengan melayukan daun teh segar sehingga bobotnya menjadi 55% dari bobot awalnya. Tahapan proses pembuatan teh hitam menurut Tuminah (2004) adalah dengan melalui proses fermentasi. Proses tersebut dilakukan pada suhu sekitar 22–28°C dengan kelembaban sekitar 90%. Waktu fermentasi biasanya dilakukan selama 2–4 jam. Selanjutnya dilakukan pengeringan sampai kadar air teh kering mencapai 4–6%.
Fermentasi teh hitam tidak menggunakan mikrob sebagai sumber enzim, melainkan dilakukan oleh enzim polifenol oksidase yang terdapat dalam daun teh itu sendiri. Pada proses ini, katekin teroksidasi menjadi teaflavin dan tearubigin.
Teh oolong diproses secara semi fermentasi. Daun teh segar dilayukan lebih dahulu, kemudian dipanaskan pada suhu 160– 240°C selama 3–7 menit untuk inaktivasi enzim, sebelum digulung dan dikeringkan.
Teh hijau dan teh putih diperoleh tanpa fermentasi, daun teh hanya melalui tahap pemanasan, pengeringan dan penggilingan (Wikipedia 2007). Pemanasan daun teh dapat dilakukan dengan dua metode, dengan udara kering (pemanggangan) atau uap panas (steaming). Pemanggangan daun teh akan memberikan aroma dan cita rasa yang lebih kuat dibandingkan dengan pemberian uap panas. Sementara dengan cara pemberian uap panas, warna teh dan seduhannya lebih hijau terang. (Tuminah 2004)
Perbedaan utama antara teh hijau dan teh putih adalah dari bagian tanaman yang diambil. Jika teh hijau umumnya berasal dari daun teh muda dan dewasa, maka teh putih hanya berasal dari pucuk dan daun teh muda. Oleh karena itu, teh putih memiliki kandungan katekin dan kafein yang lebih banyak daripada teh hijau (Wikipedia 2007).
Kandungan Polifenol Teh Hijau
Beberapa tahun terakhir, senyawa polifenol menarik banyak perhatian peneliti karena kemampuannya sebagai antioksidan, antikanker, antiperadangan, termogenik, probiotik, dan antimikrob pada manusia dan hewan. Selain itu juga karena polifenol
merupakan senyawa aktif yang banyak terkandung pada tanaman obat. Senyawa polifenol telah banyak diidentifikasi bentuk strukturnya bahkan telah dibedakan menjadi beberapa kelompok seperti flavonoid, asam fenolat, dan lignin.
Komponen flavonoid yang banyak terdapat di dalam daun teh adalah katekin, flavonol glikosida, dan flavon C-glikosida. Komposisi kandungan flavonoid rata-rata dalam 100 g teh hijau secara signifikan sebesar 16,00 g (Wang 2001). Menurut Tuminah (2004), masih terdapat beberapa komponen senyawa kimia lain yang ditemukan pada daun teh hijau, seperti kafein yang umumnya terdapat dalam kopi. Senyawa kimia yang lain dapat dilihat pada Lampiran 2.
Tabel 1 Kandungan flavonoid daun teh hijau dan teh hitam tiap 100 g bobot
Flavonoid Teh
hijau (g)
Teh hitam (g)
Katekin 14,20 4,00 Teaflavin - 0,94 Flavonol glikosida 0,64 0,47 Flavon C-glikosida 0,086 0,051
Total polifenol 16,00 15,60
Sumber : Wang 2001
Menurut Youying (2005), kebanyakan polifenol merupakan turunan flavonol dan sekarang dikenal sebagai katekin, epikatekin, dan turunannya.
Polifenol katekin memiliki aktivitas antioksidan yang tinggi, seperti epigalokatekin galat (EGCG), epikatekin galat, epigalokatekin dan epikatekin. Daya antioksidannya lebih besar jika dibandingkan dengan vitamin C atau β– karoten. EGCG memiliki konsentrasi tertinggi, dalam 240 ml ekstrak cair daun teh dengan pelarut air terdapat 200 mg EGCG (Mukhtar 2000) dan terdapat lebih dari 61% turunan epikatekin yang ada di dalam daun teh hijau (Youying 2005).
PENGARUH TEKANAN DAN SUHU PADA KONDISI
EVAPORASI EKSTRAK DAUN TEH HIJAU
DODO HANDOKO
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
ABSTRAK
DODO HANDOKO. Pengaruh Tekanan dan Suhu pada Kondisi Evaporasi Ekstrak Daun Teh Hijau. Dibimbing oleh DUDI TOHIR dan BAMBANG SRIJANTO.
Pemanfaatan bahan-bahan alami sebagai sarana penunjang kesehatan sebenarnya telah diterapkan oleh manusia sejak lama, terutama tanaman teh (Camellia sinensis). Teh hijau merupakan salah satu jenis produk teh yang diperoleh tanpa mekanisme fermentasi. Teh hijau berkhasiat untuk menyembuhkan berbagai penyakit terutama penyakit kanker, karena kandungan senyawa polifenol yang melimpah, terutama epigalokatekin, epigalokatekin-galat, epikatekin, dan epikatekin-galat. Berbagai macam perlakuan telah digunakan untuk mengoptimumkan ekstraksi polifenol yang terdapat dalam teh hijau, tetapi perlakuan kondisi evaporasi pelarut belum banyak dilaporkan.
Dalam penelitian ini, 80 gram serbuk teh hijau berukuran 18 mesh dimaserasi dalam 800 ml air bebas ion, selama 20 menit pada suhu konstan, yaitu 80 °C. Setelah itu, larutan diuapkan dengan 3 variasi tekanan dalam labu (80, 90, dan 100 mBar) dan 3 variasi suhu penangas (50, 60, dan 70 °C), selanjutnya ditentukan kondisi optimumnya berdasarkan laju penguapan tertinggi. Kondisi optimum evaporasi diperoleh pada saat tekanan dalam labu dan suhu penangas berturut-turut adalah 90 mBar dan 70oC, dengan waktu dan laju penguapan sebesar 0,7425 jam dan 0,0707 (g/det). Kadar polifenol dari 80 gram serbuk teh hijau ditentukan dengan spektrofotometri sinar tampak pada panjang gelombang 725 nm, perolehannya sebesar 25,4136 ppm atau 3,63% (b/b).
ABSTRACT
DODO HANDOKO. Effect of Pressure and Temperature on Evaporation Condition of Green Tea Extract. Supervised by DUDI TOHIR and BAMBANG SRIJANTO.
Natural substances have been studied and applied as health supplements by human being for long ago, especially tea crop (Camellia sinensis). Green tea represents one of type of tea products that is obtained by nonfermentation mechanism. It is useful to heal various diseases especially cancer, caused by the excess of polyphenols substances, such as epigallocatechin, epigallocatechin-gallate, epicatechin, and epicatechin-gallate. Many treatments have been used to optimized green tea polyphenols extraction, but solvent evaporation condition treatments have not been reported.
ii
PENGARUH TEKANAN DAN SUHU PADA KONDISI
EVAPORASI EKSTRAK DAUN TEH HIJAU
DODO HANDOKO
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Sains pada
Departemen Kimia
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
Judul : Pengaruh Tekanan dan Suhu pada Kondisi Evaporasi Ekstrak Daun Teh Hijau
Nama : Dodo Handoko NIM : G01499074
Pembimbing I,
Drs. Dudi Tohir, MS.
NIP 131 851 277
Menyetujui,
Pembimbing II,
Ir. Bambang Srijanto
NIP 680 003 303
Mengetahui,
Dekan Fakultas Matematika dan Ilmu Pengetahuan Alam Institut Pertanian Bogor
Prof. Dr. Ir. Yonny Koesmaryono, MS
NIP 131 473 999
PRAKATA
Puji dan syukur penulis panjatkan kepada Allah SWT yang telah memberikan rahmat dan karunia-Nya sehingga penulis dapat menyelesaikan laporan penelitian yang berjudul
Pengaruh Tekanan dan Suhu pada Kondisi Evaporasi Ekstrak Daun Teh Hijau.
Penulis mengucapkan terima kasih kepada Bapak Drs. Dudi Tohir, MS dan Bapak Ir. Bambang Srijanto, selaku pembimbing yang telah memberikan masukan dan pengarahan kepada penulis. Terima kasih tak terhingga kepada kedua orangtua tercinta, Ibu Prof. Dr. Ir. Tun Tedja Irawadi, MS selaku ketua Departemen Kimia, Bapak Prof. Dr. Ir. Yonny Koesmaryono, MS selaku Dekan FMIPA IPB, Bapak Kusnata, mas Pipit, dan Agung serta adikku tercinta Wulandari yang selalu memberikan doa, dorongan semangat, bantuan materi, kesabaran, dan kasih sayang serta kepercayaan kepada penulis.
Terima kasih juga penulis ucapkan kepada staf dan laboran di Laboratorium Teknologi Farmasi dan Medika, sahabatku Wakhid Lukas S. Si,Budi Arifin S.Si, Mas Herry, Pak Sabur, Ibu Yenni, Ibu AA, Teh Nung, Marudut serta teman-teman Mexindo 18 atas bantuan, masukan dan kerja samanya selama penelitian dan penulisan karya ilmiah ini
Semoga karya ilmiah ini dapat bermanfaat bagi dunia ilmu pengetahuan.
Bogor, Mei 2007
v
RIWAYAT HIDUP
Penulis dilahirkan di Jakarta pada tanggal 11 Juni 1981 sebagai anak kedua dari tiga bersaudara, anak pasangan Soerodjo HS dan Tjitjih.
Pendidikan formal penulis sampai tingkat SMU diselesaikan di Jakarta, yaitu SD Negeri 04 Petang Pondok Pinang, SMP Negeri 87 Pondok Pinang, dan SMU Negeri 29 Jakarta dari tahun 1987-1999. Penulis diterima di Program Studi Kimia, Departemen Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor melalui jalur Seleksi Penerimaan Mahasiswa Baru (SPMB) pada tahun 1999. Bidang yang diminati ialah Kimia Organik.
DAFTAR ISI
Halaman
DAFTAR TABEL... vii
DAFTAR GAMBAR ... vii
DAFTAR LAMPIRAN... vii
PENDAHULUAN ... 1
TINJAUAN PUSTAKA Tanaman Teh... 1
Kandungan Polifenol Teh Hijau... 2
Optimalisasi Metode Ekstraksi Teh Hijau ... 3
Penguapan Pelarut ... 3
Analisis Kuantitatif Polifenol... 4
BAHAN DAN METODE Bahan dan Alat... 4
Metode Penelitian... 4
Ekstraksi... 4
Analisis Kuantitatif Total Polifenol ... 5
HASIL DAN PEMBAHASAN Ekstraksi Serbuk Daun Teh Hijau... 5
Optimalisasi Kondisi Evaporasi Ekstrak Cair Teh Hijau ... 6
Analisis Kadar Polifenol Ekstrak Teh Hijau ... 7
SIMPULAN DAN SARAN Simpulan ... 8
Saran ... 8
DAFTAR PUSTAKA ... 8
DAFTAR TABEL
Halaman
1 Kandungan flavonoid daun teh hijau dan teh hitam tiap 100 g bobot ... 2
2 Peubah evaporasi ekstrak cair yang digunakan pada penelitian ... 4
DAFTAR GAMBAR
Halaman 1 Daun tanaman teh ... 12 Struktur polifenol terbesar pada daun teh hijau... 3
3 Pengaruh tekanan dan suhu terhadap waktu evaporasi ... 6
4 Pengaruh tekanan dan suhu evaporasi terhadap laju penguapan air... 7
5 Pengaruh suhu dan tekanan terhadap konsentrasi polifenol ... 7
DAFTAR LAMPIRAN
Halaman 1 Jenis-jenis kelompok teh ... 112 Kandungan senyawa kimia teh hijau ... 11
3 Diagram alir penelitian ... 12
4 Kadar air serbuk teh hijau (AOAC 1984)... 13
5 Kadar abu serbuk teh hijau (AOAC 1984) ... 13
6 Hasil evaporasi ekstrak cair daun teh ... 14
7 Hasil pemetaan kehomogenan laju penguapan air ... 15
8 Hasil analisis dengan metode GLM ... 16
9 Analisis ragam pengaruh tekanan labu dan suhu terhadap penguapan air ... 18
10 Hasil analisis laju penguapan air ... 18
11 Kurva larutan standar ... 18
12 Kadar polifenol ekstrak daun teh... 19
PENDAHULUAN
Beragam cara untuk mendapatkan kesehatan yang optimal seperti berolah raga, mengkonsumsi makanan yang bernutrisi tinggi, dan mengkonsumsi obat-obatan. Namun, penggunaan obat-obatan perlu diwaspadai terutama jika obat tersebut berasal dari bahan sintetik. Hal ini disebabkan karena obat sintetik memiliki efek samping terhadap organ tubuh seperti pada ginjal. Oleh karena itu, seiring dengan kemajuan di bidang kesehatan, saat ini mulai dikembangkan obat-obatan yang berasal dari alam. Pemanfaatan bahan-bahan alami sebagai sarana penunjang kesehatan sebenarnya telah diterapkan oleh manusia sejak lama, terutama tanaman teh. Teh (Camellia sinensis) pertama kali diperkenalkan oleh kaisar Cina Shen Nung (2737 SM) karena mempunyai aroma yang khas dan sekaligus dapat menjaga kesehatan tubuh (Trevisanato 2000). Sejak saat itu, teh telah mulai merebak ke seluruh penjuru dunia karena dapat memberikan perasaan nyaman dan segar ketika meminumnya.
Saat ini telah dikenal ada empat jenis teh dan salah satunya adalah teh hijau yang telah menunjukkan banyak manfaatnya dalam kesehatan. Beberapa penelitian sebelumnya menunjukkan bahwa teh hijau bermanfaat sebagai antibakteri, antioksidan, antiradang, dan antikanker (Miller 2005). Zat aktif dalam teh hijau menurut Picard (1996) antara lain adalah katekin, epikatekin (EC), galokatekin (GC), epigalokatekin (EGC), epigalokatekin galat (EGCG), epikatekin galat (ECG). Senyawa tersebut dikelompokkan dalam senyawa polifenol.
Ekstraksi teh hijau telah dilakukan sebelumnya di antaranya oleh Song (2001), menggunakan metode maserasi dengan ragam suhu, waktu, dan nisbah bahan baku-pelarut. Diperoleh bahwa ekstraksi menggunakan pelarut air pada suhu 90ºC selama 10 menit secara signifikan meningkatkan rendemen ekstrak polifenol dibandingkan dengan pada suhu yang lebih rendah. Namun, untuk mutu ekstrak yang lebih baik digunakan suhu 80ºC karena beberapa senyawa yang tidak diinginkan turut terekstrak pada suhu 90ºC atau lebih.
Selama ini proses penguapan pelarut pada ekstraksi teh hijau belum mendapat perhatian
lebih lanjut sehingga perlu dilakukan optimalisasi pada kondisi evaporasi dengan mengatur suhu penangas dan tekanan dalam labu rotavapor.
Penelitian ini bertujuan untuk mengetahui pengaruh suhu dan tekanan dalam evaporasi pelarut dan konsentrasi polifenol. Selain itu, diharapkan dapat memperoleh kondisi optimum proses penguapan pada pengolahan ekstrak cair teh hijau. Dengan cara tersebut diharapkan proses pengambilan zat aktif menjadi lebih efektif dan efisien sehingga biaya produksi menjadi lebih rendah dengan kualitas yang lebih tinggi.
TINJAUAN PUSTAKA
Tanaman Teh
Tanaman teh termasuk jenis tanaman semak yang umumnya dapat tumbuh dengan baik di daerah beriklim tropis dan sub tropis dengan ketinggian antara 200 dan 2000 meter di atas permukaan laut dengan suhu kelembaban berkisar 14-25°C. Ketinggian tanaman teh jenis assamica
dapat mencapai 6-20 meter. Perkebunan teh umumnya selalu menjaga pertumbuhan tanaman dengan cara melakukan pemotongan sehingga akan mempermudah pemetikan pucuk daun teh. Ketinggian tanaman teh selalu dipelihara agar kurang dari 2 meter. Bunga teh berwarna putih kekuningan dengan diameter 2,5-4 cm, daun teh berukuran panjang sekitar 4-15 cm dengan lebar 2-5 cm dapat dilihat pada Gambar 1 (Wikipedia 2007).
Gambar 1 Daun tanaman teh.
2
fermentasi. Bentuk dan warna keempat kelompok teh dapat dilihat pada Lampiran 1.
Menurut Mukhtar (2000), tahap awal memproduksi teh hitam dan oolong adalah dengan melayukan daun teh segar sehingga bobotnya menjadi 55% dari bobot awalnya. Tahapan proses pembuatan teh hitam menurut Tuminah (2004) adalah dengan melalui proses fermentasi. Proses tersebut dilakukan pada suhu sekitar 22–28°C dengan kelembaban sekitar 90%. Waktu fermentasi biasanya dilakukan selama 2–4 jam. Selanjutnya dilakukan pengeringan sampai kadar air teh kering mencapai 4–6%.
Fermentasi teh hitam tidak menggunakan mikrob sebagai sumber enzim, melainkan dilakukan oleh enzim polifenol oksidase yang terdapat dalam daun teh itu sendiri. Pada proses ini, katekin teroksidasi menjadi teaflavin dan tearubigin.
Teh oolong diproses secara semi fermentasi. Daun teh segar dilayukan lebih dahulu, kemudian dipanaskan pada suhu 160– 240°C selama 3–7 menit untuk inaktivasi enzim, sebelum digulung dan dikeringkan.
Teh hijau dan teh putih diperoleh tanpa fermentasi, daun teh hanya melalui tahap pemanasan, pengeringan dan penggilingan (Wikipedia 2007). Pemanasan daun teh dapat dilakukan dengan dua metode, dengan udara kering (pemanggangan) atau uap panas (steaming). Pemanggangan daun teh akan memberikan aroma dan cita rasa yang lebih kuat dibandingkan dengan pemberian uap panas. Sementara dengan cara pemberian uap panas, warna teh dan seduhannya lebih hijau terang. (Tuminah 2004)
Perbedaan utama antara teh hijau dan teh putih adalah dari bagian tanaman yang diambil. Jika teh hijau umumnya berasal dari daun teh muda dan dewasa, maka teh putih hanya berasal dari pucuk dan daun teh muda. Oleh karena itu, teh putih memiliki kandungan katekin dan kafein yang lebih banyak daripada teh hijau (Wikipedia 2007).
Kandungan Polifenol Teh Hijau
Beberapa tahun terakhir, senyawa polifenol menarik banyak perhatian peneliti karena kemampuannya sebagai antioksidan, antikanker, antiperadangan, termogenik, probiotik, dan antimikrob pada manusia dan hewan. Selain itu juga karena polifenol
merupakan senyawa aktif yang banyak terkandung pada tanaman obat. Senyawa polifenol telah banyak diidentifikasi bentuk strukturnya bahkan telah dibedakan menjadi beberapa kelompok seperti flavonoid, asam fenolat, dan lignin.
Komponen flavonoid yang banyak terdapat di dalam daun teh adalah katekin, flavonol glikosida, dan flavon C-glikosida. Komposisi kandungan flavonoid rata-rata dalam 100 g teh hijau secara signifikan sebesar 16,00 g (Wang 2001). Menurut Tuminah (2004), masih terdapat beberapa komponen senyawa kimia lain yang ditemukan pada daun teh hijau, seperti kafein yang umumnya terdapat dalam kopi. Senyawa kimia yang lain dapat dilihat pada Lampiran 2.
Tabel 1 Kandungan flavonoid daun teh hijau dan teh hitam tiap 100 g bobot
Flavonoid Teh
hijau (g)
Teh hitam (g)
Katekin 14,20 4,00 Teaflavin - 0,94 Flavonol glikosida 0,64 0,47 Flavon C-glikosida 0,086 0,051
Total polifenol 16,00 15,60
Sumber : Wang 2001
Menurut Youying (2005), kebanyakan polifenol merupakan turunan flavonol dan sekarang dikenal sebagai katekin, epikatekin, dan turunannya.
Polifenol katekin memiliki aktivitas antioksidan yang tinggi, seperti epigalokatekin galat (EGCG), epikatekin galat, epigalokatekin dan epikatekin. Daya antioksidannya lebih besar jika dibandingkan dengan vitamin C atau β– karoten. EGCG memiliki konsentrasi tertinggi, dalam 240 ml ekstrak cair daun teh dengan pelarut air terdapat 200 mg EGCG (Mukhtar 2000) dan terdapat lebih dari 61% turunan epikatekin yang ada di dalam daun teh hijau (Youying 2005).
3
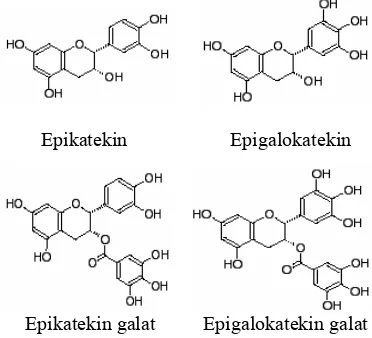
Epikatekin Epigalokatekin
Epikatekin galat Epigalokatekin galat
Gambar 2 Struktur polifenol terbesar pada daun teh hijau.
Optimalisasi Metode Ekstraksi Teh Hijau
Song (2001) dalam penelitiannya melakukan optimalisasi ekstraksi teh hijau dengan metode maserasi menggunakan pelarut air dengan variasi suhu, waktu, dan nisbah bahan baku-pelarut. Maserasi dengan suhu 90ºC selama 10 menit secara signifikan meningkatkan rendemen ekstrak polifenol dibandingkan dengan suhu yang lebih rendah. Namun, agar mendapatkan mutu ekstrak yang lebih baik, digunakan suhu 80ºC karena beberapa senyawa yang tidak diinginkan akan ikut terekstrak pada suhu 90ºC atau lebih.
Beberapa penelitian sebelumnya menunjukkan bahwa pelarut yang efektif untuk ekstraksi polifenol dari bahan makanan ialah etanol dan air mendidih (Shi et al. 2003). Hal ini karena polifenol memiliki gugus hidroksil yang polar, sehingga terekstraksi sempurna dengan air. Akan tetapi, air sendiri dapat melarutkan protein dan polisakarida yang tidak diinginkan, terutama pada suhu tinggi.
Lu et al. (2006) melakukan optimalisasi kondisi ekstraksi katekin dan polifenol dari teh hijau menggunakan pelarut etanol dengan variasi suhu, waktu, dan nisbah bahan baku-pelarut. Indeks polifenol pada nisbah bahan baku-pelarut 1:15 dengan suhu 70oC diperoleh rendemen dan konsentrasi maksimum berturut-turut sebesar 8,5% (b/b) dan 24,9% (b/v).
Sharief (2006) melakukan optimalisasi ekstraksi teh dengan ukuran butir 32 mesh. Metode yang digunakan maserasi dengan ragam suhu (75, 85 dan 95°C), nisbah bahan baku-pelarut (10:100, 15:100 dan 20:100 b/v), dan waktu (2, 4, 6, 8, 10, 15 dan 20) menit. Rendemen yang diperoleh pada suhu 85 dan 95°C mencapai optimal pada menit ke-8 dengan rendemen rata-rata sebesar 20,33% (b/v), sedangkan pada suhu 75°C dan menit ke-10 rendemen ekstrak tertinggi dihasilkan pada nisbah bahan baku-pelarut 10:100 (b/v), yaitu sebesar 13,92% (b/b).
Siringo-ringo (2006) telah melakukan optimalisasi ekstraksi polifenol teh hijau berdasarkan ukuran butir (18, 32, dan 60 mesh), nisbah bahan baku-pelarut (1:10; 1:1,25; dan 1:15 b/v), dan waktu (10, 20, dan 20 menit) dengan metode refluks dan pelarut air. Nilai optimum kadar polifenol teh hijau diperoleh pada ukuran 18 mesh, nisbah bahan baku-pelarut 1:10 dan waktu ekstraksi 23 menit 14 detik sebesar 857,70 ppm.
Nisbah bahan baku dan pelarut yang optimum menurut Siringo-ringo (2006) dan Sharief (2006) adalah 1:10, walaupun metode yang digunakan oleh keduanya berbeda.
Optimasi dilakukan dengan tujuan untuk mencari atau menemukan nilai peubah-peubah yang digunakan dalam proses agar menghasilkan nilai terbaik (Edgar 1988). Optimasi proses ekstraksi teh hijau dengan beragam variasi metode saat ini telah banyak dilakukan, sedangkan optimalisasi pada saat evaporasi ekstrak cair teh hijau belum ditelaah lebih lanjut.
Penguapan Pelarut
Destilasi merupakan teknik pemisahan campuran yang berwujud cair dengan berdasarkan pada perbedaan titik didih. Destilasi dapat pula digunakan untuk mendapatkan zat padat yang terlarut dalam pelarutnya, sehingga dapat diperoleh suatu padatan dengan tingkat kemurnian yang lebih baik.
4
memungkinkan probabilitas kerusakan akan semakin besar dengan pertambahan suhu.
Tekanan uap pelarut dapat pula dipengaruhi dengan melakukan pemampatan pada saat proses destilasi. Karena selain peningkatan temperatur yang mempengaruhi tekanan uap, pemberian tekanan juga dapat memberikan dampak pada tekanan uap pelarut. Jika tekanan diberikan pada suatu campuran berwujud cair, maka tekanan uap pelarutnya akan meningkat. Hal yang sebenarnya terjadi adalah molekul-molekul pelarut akan keluar dari campuran sebagai gas.
Clausius-Clapeyron menunjukkan bahwa dengan menurunkan tekanan sebesar setengah dari tekanan awal akan menurunkan titik didih pelarut sekitar 15%. Hal ini sesuai dengan persamaan : 2 1 1 2 1
2
(
)
ln
T
T
R
T
T
H
P
P
=
Δ
vap−
Analisis Kuantitatif Polifenol
Menurut Makkar (1989), penentuan total polifenol dapat dilakukan dengan berbagai metode. Analisis kuantitatif dapat dilakukan dengan metode kolorimetri, yaitu dengan penambahan reagen diantaranya menggunakan reagen Folin-Denis, Folin Ciocalteu, formaldehida-HCl, biru Prussia, Titanium dan fero amonium sitrat yang diukur dengan spektrofotometer sinar tampak pada panjang gelombang maksimum (λmaks). Metode lain
yang dapat digunakan yaitu gravimetri, dan kromatografi cair kinerja tinggi (HPLC).
Kadar polifenol dapat ditentukan dengan reagen Folin-Ciocalteu. Reagen Folin umumnya digunakan pada metode Lowry, untuk menentukan konsentrasi protein. Walaupun reagen Folin tidak mengandung gugus fenol, tetapi bersifat sensitif untuk mengoksidasi senyawa-senyawa fenol. Reaksi antara reagen dan senyawa-senyawa fenol akan menghasilkan sebuah senyawa kompleks yang berwarna biru, sehingga dapat diukur dengan spektrofotometer pada panjang gelombang 725 nm (Roura 2006).
BAHAN DAN METODE
Bahan dan Alat
Bahan yang digunakan ialah serbuk daun teh hijau dari pabrik teh di daerah Pasir Sarongge Cipanas-Cianjur, air bebas ion, asam galat (Sigma), Na2CO3 25% dan reagen
Folin-Ciocalteu.
Alat yang digunakan ialah Alat-alat kaca, pengaduk listrik, penguap putar Laborota 4003
control vario, dan spektrofotometer spectronic-20D+.
Metode Penelitian
Penelitian ini dilakukan di Laboratorium Teknologi Farmasi dan Medika, BPPT Serpong. Diagram alir penelitian ini dapat dilihat pada Lampiran 3.
Ekstraksi
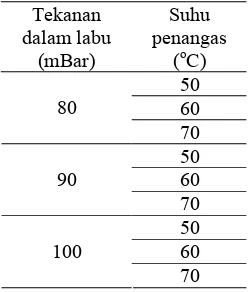
Serbuk daun teh hijau kering ditimbang sebanyak 80 g dan dimaserasi menggunakan 800 ml air bebas ion selama 20 menit pada suhu 80ºC. Hasil maserasi kemudian disaring dan volume ekstrak cair dicatat dan selanjutnya diuapkan dengan peubah evaporasi yang digunakan seperti pada Tabel 2 berikut ini.
Tabel 2 Peubah evaporasi ekstrak cair yang digunakan pada penelitian
Tekanan dalam labu
(mBar)
Suhu penangas
(oC) 50 60 80 70 50 60 90 70 50 60 100 70
5
Analisis Kuantitatif Total Polifenol
Standar polifenol dibuat dengan cara melarutkan asam galat sebagai standar polifenol ke dalam air bebas ion dengan konsentrasi 1000 ppm, kemudian dilakukan pengenceran hingga didapatkan konsentrasi 25, 50, 100, 150, dan 200 ppm. Setelah itu dilakukan pengukuran absorbansinya pada panjang gelombang 725 nm dengan spektrofotometer UV-Vis.
Ekstrak ditimbang sebanyak 0,01 g dan diencerkan dalam labu takar 100 ml dengan air bebas ion sampai tanda tera. Sebanyak 0,5 ml ekstrak hasil pengenceran dipipet ke dalam tabung reaksi, ditambahkan 4,3 ml air bebas ion, 0,2 ml reagen Folin-Ciocalteu, 0,5 ml Na2CO3 25% (b/v), dan divorteks. Kemudian
ditambahkan lagi 4,5 ml air bebas ion dan diukur absorbansinya menggunakan spektro-fotometer pada λ 725 nm.
HASIL DAN PEMBAHASAN
Ekstraksi Serbuk Daun Teh Hijau
Ukuran serbuk daun yang digunakan sebesar 18 mesh karena menurut Siringo-ringo (2006) ukuran butir optimum untuk ekstraksi polifenol teh hijau adalah 18 mesh. Menurut Purseglove et al (1981) sebaiknya bahan yang digunakan memiliki ukuran yang seragam karena proses difusi zat pelarut ke dalam zat terlarut akan lebih mudah. Hal ini disebabkan oleh semakin kecilnya ukuran bahan maka akan membantu penetrasi pelarut ke dalam sel tumbuhan sehingga mempercepat pelarutan komponen bioaktif dan meningkatkan rendemen ekstraksi. Semakin kecil ukuran bahan akan menyebabkan permukaan bidang sentuh bahan dengan pelarut akan semakin besar.
Serbuk daun yang dipakai memiliki kadar air dan kadar abu rata-rata beturut-turut sebesar 3,79% (b/b) (Lampiran 4) dan 5,11% (b/b) (Lampiran 5). Teh pada umumnya memiliki kadar air sebesar 7% (Anonim 2007). Hal ini berarti serbuk daun teh yang digunakan lebih kering dan jika disimpan akan lebih tahan lama.
Pengukuran kadar air penting untuk dilakukan sebagai koreksi terhadap hasil,
karena contoh daun yang sama dengan kadar air yang berbeda akan memberikan hasil yang berbeda pula. Selain itu pengukuran kadar air dan kadar abu juga dapat digunakan sebagai acuan untuk kondisi penyimpanan terutama dalam hal kelembaban ruang penyimpanan. Apabila serbuk makin kering, pada umumnya akan makin awet pada saat penyimpanan.
Metode ekstraksi yang digunakan adalah maserasi dengan pelarut air dan disertai pemanasan. Maserasi menyebabkan serbuk daun akan terendam semua dan berinteraksi langsung dengan pelarut. Adanya pengaturan suhu pada saat maserasi bahan, diperkirakan akan meningkatkan jumlah rendemen, sebab mempengaruhi efektivitas dari pelarut untuk melarutkan bahan. Semakin tinggi suhu yang digunakan maka proses difusi pelarut ke dalam bahan akan lebih cepat.
Maserasi serbuk daun teh dilakukan pada kondisi suhu 80oC, kecepatan putar pengaduk sebesar 90 rpm, dan waktu rendam 20 menit. Pemilihan kondisi ini didasarkan pada kondisi optimum yang diperoleh peneliti sebelumnya. Dari 80 gram serbuk daun yang diekstraksi dengan 800 ml air bebas ion diperoleh rendemen ekstrak sebesar 14,25% (b/b). Rendemen yang diperoleh lebih rendah dari rendemen yang diperoleh Siringo-ringo (2006) dengan metode refluks, yaitu 22,87% pada perlakuan nisbah bahan baku-pelarut 1:10, waktu ekstraksi 20 menit, ukuran partikel 18 mesh, dan suhu 80oC. Hal ini kemungkinan disebabkan karena perbedaan metode ekstraksi yang digunakan. Berbeda dengan hasil yang didapatkan oleh Sharief (2006) yang menggunakan metode sama memperoleh rendemen 20,33% dengan perlakuan nisbah bahan baku-pelarut 1:10, waktu ekstraksi 20 menit, ukuran partikel 32 mesh, dan suhu 85oC. Hal ini diperkirakan karena perbedaan ukuran butir partikel dan suhu ekstraksi.
6
Pengadukan diperkirakan dapat pula meningkatkan efektivitas ekstraksi, karena dapat menyeragamkan kondisi pada saat mengekstrak bahan. Maserasi dengan disertai dengan pemanasan dan pengadukan kemungkinan akan lebih sempurna dalam mengekstrak bahan aktif, karena panas akan terdistribusi dengan baik pada pelarut maupun bahan sehingga senyawa yang berdifusi keluar bahan akan semakin cepat dan melimpah.
Optimalisasi Kondisi Evaporasi Ekstrak Cair Teh Hijau
Evaporasi ekstrak bertujuan untuk mendapatkan ekstrak yang lebih murni tanpa adanya pelarut. Penguapan pelarut dilakukan dengan memanaskan ekstrak pada suhu yang sesuai dengan titik didih pelarut. Namun, tindakan pemanasan yang berlebihan akan dapat merusak bahan aktif senyawa yang diinginkan. Oleh karena itu, penguapan ekstrak cair dilakukan dengan suhu di bawah titik didih pelarutnya dengan cara menurunkan tekanan.
Dari beberapa penelitian sebelumnya belum dilaporkan mengenai kondisi evaporasi yang optimal. Optimalisasi ini dilakukan untuk mencari atau menemukan nilai peubah-peubah yang digunakan dalam proses agar menghasilkan nilai terbaik (Edgar 1988).
Evaporasi dihentikan saat bobot akhir yang diperoleh mempunyai rendemen yang seragam. Hal ini dimaksudkan untuk mengetahui jumlah waktu yang dibutuhkan agar memperoleh jumlah rendemen yang sama pada setiap perlakuan evaporasi. Rendemen ekstrak kental yang diperoleh setelah evaporasi berkisar antara 14,25-14,38% (b/b). Menurut Lu etal. (2006), Sharief (2006) dan Siringo-ringo (2006) rendemen ekstrak dipengaruhi oleh nisbah bahan baku dan pelarutnya serta suhu perlakuan eksraksi. Data hasil evaporasi dapat dilihat di Lampiran 6.
Gambar 3 menjelaskan hubungan antara tekanan dalam labu dan suhu penangas yang digunakan pada evaporasi ekstrak cair terhadap lamanya waktu evaporasi. Grafik tersebut menjelaskan bahwa penurunan tekanan dalam labu akan menyebabkan kondisi dalam labu yang mendekati tekanan 0 atm, sehingga mempercepat waktu penguapan pelarut. Peningkatan suhu penangas turut membantu mempercepat penguapan air.
0 1 2 3 4 5 6 7 8 9
50 60 70 Suhu (celsius)
Waktu (jam)
80 mBar 90 mBar 100 mBar
Gambar 3 Pengaruh tekanan dan suhu
terhadap waktu evaporasi
Apabila faktor tekanan diperkecil, maka waktu evaporasi akan lebih cepat, terutama terlihat secara signifikan pada kondisi suhu 50oC. Peningkatan suhu dari 50-60oC pada kondisi tekanan yang sama memperlihatkan penurunan waktu evaporasi secara signifikan, sedangkan pada peningkatan suhu dari 60-70oC dengan kondisi tekanan yanga sama, tidak memperlihatkan penurunan yang tidak terlalu besar. Dari data tersebut diperoleh waktu penguapan air tercepat diperoleh pada kondisi evaporasi dengan suhu 70oC dan tekanan dalam labu 80 mBar selama 0,6632 jam.
Evaporasi pelarut sebaiknya tidak terlalu lama dan menggunakan suhu yang rendah karena diperkirakan komponen senyawa bioaktif yang tidak tahan panas akan rusak atau terdegradasi akibat pemanasan. Hal ini akan menyebabkan penurunan rendemen dan penurunan kadar polifenol. Kasus penurunan kadar polifenol telah dilaporkan Siringo-ringo (2006), akibat lamanya waktu pemanasan.
Gambar 4 menjelaskan hubungan antara tekanan dalam labu dan suhu penangas terhadap laju penguapan air. Dapat dikatakan laju penguapan air berbanding lurus dengan suhu dan berbanding terbalik dengan tekanan dalam labu. Pada tekanan yang sama, kenaikan suhu akan meningkatkan laju penguapan, sedangkan kenaikan tekanan dalam labu akan menurunkan laju penguapan.
7
sedangkan faktor suhu mempengaruhi dari sisi penguapan pelarut. Pada evaporasi pelarut, yang berperan aktif dalam penguapan pelarut adalah faktor suhu.
0 0.01 0.02 0.03 0.04 0.05 0.06 0.07 0.08 0.09
50 60 70Suhu (celsius)
L a ju p e n g u a p a n (g /d e t)
80 mBar 90 mBar 100 mBar
Gambar 4 Pengaruh tekanan dan suhu evaporasi terhadap laju penguapan air
Dari hasil pemetaan kehomogenan laju Pengujian (Lampiran 7), dapat dikatakan bahwa pengujian optimalisasi dilakukan dengan melihat variabel suhu penangas dan tekanan dalam labu terhadap laju evaporasi air, karena laju evaporasi memiliki data yang menyebar normal
Pengolahan data dilakukan dengan metode GLM dan menggunakan perangkat lunak SAS, sebelumnya data diubah ke dalam bentuk laju transformasi untuk mendapatkan data yang homogen dan menyebar normal. Data pengolahan disajikan pada Lampiran 8.
Gambar 4 menunjukkan laju penguapan tertinggi pada kondisi tekanan dalam labu 80 mBar, suhu 70oC. Namun, menurut Uji Duncan kondisi tersebut tidak berbeda nyata dengan kondisi tekanan 90 mBar, suhu 70oC. Dari uji beda nyata, diperoleh bahwa pada kondisi tekanan dalam labu 90 mBar, suhu 70oC lebih efektif digunakan untuk proses evaporasi pelarut dari hasil ekstraksi. Data hasil analisis berdasarkan uji Duncan dapat dilihat pada Lampiran 9 dan 10.
Dasar pemilihan ini adalah waktu proses dan suhu yang rendah, sehingga kemungkinan rusaknya komponen senyawa yang tidak tahan panas atau terdegradasi akibat pemanasan dapat diperkecil. Pemanasan yang terlalu tinggi, juga waktu kontak sampel dengan panas yang terlalu lama mampu menurunkan
rendemen kadar polifenol (Song 2001, Siringo-ringo 2006).
Analisis Kadar Polifenol Ekstrak Teh Hijau
Asam galat digunakan sebagai larutan standar karena metode kuantitatif ini berdasarkan pada oksidasi ion fenolat. Dari larutan standar, diperoleh persamaan garis y = 0.0054x + 0.021 dengan nilai ketelitian R2= 0.99. Data penentuan kurva larutan standar dapat dilihat pada Lampiran 11.
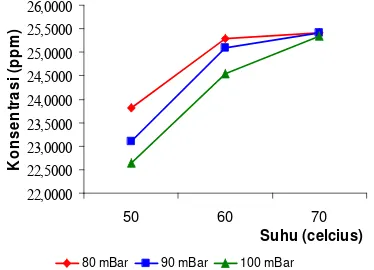
Gambar 5 memperlihatkan hubungan antara suhu, tekanan, dan konsentrasi polifenol dalam ekstrak. Pada perubahan tekanan 80-100 mBar dan perubahan suhu 50-70oC, menunjukkan bahwa faktor suhu dan tekanan berpengaruh dalam penurunan konsentrasi polifenol, sebab faktor suhu mempengaruhi dari sisi penguapan pelarut, sedangkan tekanan mempengaruhi dari sisi penurunan titik didih pelarut. Data konsentrasi polifenol dapat dilihat pada Lampiran 12.
22,0000 22,5000 23,0000 23,5000 24,0000 24,5000 25,0000 25,5000 26,0000
50 60 70
Suhu (celcius) Ko ns ent ras i ( p p m )
80 mBar 90 mBar 100 mBar
Gambar 5 Pengaruh suhu dan tekanan
terhadap konsentrasi polifenol
Penurunan konsentrasi polifenol terlihat secara jelas pada kenaikan tekanan 80-100 mBar dengan kondisi suhu tetap sebesar 50oC. Hal ini diperkirakan karena tekanan yang semakin meningkat menyebabkan evaporasi pelarut berjalan tidak sempurna, sehingga rendemen yang diperoleh kemungkinan masih terdapat sejumlah pelarut.
8
konsentrasi polifenol. Kontak sampel dengan panas yang terlalu lama diperkirakan menyebabkan rusaknya beberapa senyawa yang akan dianalisis.
Penurunan konsentrasi polifenol tidak terlihat pada peningkatan tekanan 80-100 mBar dengan kondisi suhu tetap sebesar 70oC. Menurut Clasius-Clapeyron, penurunan tekanan sebesar setengahnya akan menurun-kan titik didih pelarut sebesar 15%. Pada suhu tetap 70oC, peningkatan tekanan 80-100 mBar tidak mempengaruhi evaporasi pelarut. Hal ini menandakan bahwa suhu penangas sebesar 70oC kemungkinan lebih tinggi daripada titik didih pelarut pada kondisi tekanan 80-100 mBar.
Pada kondisi tersebut, pengaruh suhu diperkirakan lebih dominan daripada pengaruh peningkatan tekanan. Hal ini kemungkinan menyebabkan rendemen yang dihasilkan pada kondisi tersebut seragam, sehingga penurunan konsentrasi polifenol tidak terlihat secara signifikan.
Penentuan polifenol dengan reagen Folin, menurut Roura (2006) dipengaruhi oleh beberapa senyawa yang turut bereaksi dengan reagen tersebut, seperti gula, amina aromatik, sulfur dioksida, asam askorbat, asam organik, dan Fe(II). Hal ini berarti, bahwa kadar polifenol yang diperoleh kemungkinan bukan hanya berasal dari senyawa polifenol saja, tetapi juga berasal dari senyawa lain yang turut bereaksi dengan reagen tersebut. Menurut Tuminah (2004), daun teh hijau memiliki kandungan senyawa kimia selain polifenol, seperti gula, beberapa asam amino, dan teanin.
Berdasarkan kondisi efektif evaporasi pelarut pada tekanan dalam labu 90 mBar dan suhu penangas 70oC, diperoleh konsentrasi polifenol sebesar 25,4136 ppm (3,63% b/b). Hasil ini lebih kecil bila dibandingkan dengan Wang (2001) dan Tuminah (2004) yang berturut-turut sebesar 16% (b/b) dan 35,89% (b/b). Perbedaan ini kemungkinan disebabkan oleh perbedaan bahan teh yang digunakan, metode ekstraksi, dan metode analisis senyawa polifenol.
SIMPULAN DAN SARAN
Simpulan
Peningkatan suhu penangas akan mempercepat waktu evaporasi, sedangkan peningkatan tekanan mengakibatkan waktu evaporasi semakin lama. Perubahan suhu dan tekanan juga turut mempengaruhi konsentrasi polifenol.
Kondisi optimum evaporasi yang diperoleh pada saat tekanan dalam labu 90 mBar dan suhu penangas 70oC. Kadar polifenol yang diperoleh dalam 80 gram serbuk daun teh pada kondisi tersebut sebesar 25,4136 ppm atau 3,63 % (b/b).
Saran
Perlu pengkajian lebih dalam mengenai penurunan kadar polifenol selama proses ekstraksi. Selain itu, perlu adanya penelitian lebih lanjut mengenai perbandingan teknik ekstraksi teh hijau.
Penelitian lebih lanjut juga diperlukan untuk perbandingan kandungan teh hijau dan teh putih.
DAFTAR PUSTAKA
[Anonim]. 2007. Tea/Caffeine Content, Water Content, Pesticides, Fumigants, Ingridients and Declaration. State Laboratory of The Canton Basel City. http://www. kantonslabor-bs.ch/content.cfm?nav=17& content=23&Command=details&year=2003 &kat=all&ID=63.[21 Maret 2007]
AOAC. 1984. Official Methods of Analysis of The Association of Official Analytical Chemist. Virginia: AOAC
Edgar TF, Himmelblau DM. 1988. Optimization of chemical processes. Chemical engineering series. New York: McGraw-Hill.
9
Lu YP, He Q, Yao K, Zen FJ, Lin LH. 2006. Optimization Conditions for the Extraction of Catechin. http://www.ceps.com.tw/
ec/ecjnlarticle.[2 Januari 2007]
Makkar HPS. 1989. Protein Precipitation Methods for Quantitation of Tannins: A Review. J Agric Food Chem 37:1197-1202.
Miller AL. 2005. Antioxidant Flavonoid: Stucture, Function and Clinical Usage.
Mukhtar H, Nihal Ahmad. 2000. Tea Polyphenols: Prevention of Cancer and Optimizing Health. Am J Clin Nutr
71:1698s-1702s.
Picard D. 1996. The Biochemistry of Green Tea Polyphenols and Their Potential Application in Human Skin Cancer.
Alternat Med Rev 1: 31-42.
Purseglove JW, Brown EG, Green GL, Robbins SRG. 1981. Spices Vol. II. New York: Longman.
Roura E, Cristina AL, Ramon E, Rosa MLR. 2006. Total Polyphenol Intake Estimated by a Modified Folin-Ciocalteu Assay of Urine. J Clin Chem 52: 749-751.
Sharief DA. 2006. Optimasi Proses Ekstraksi dan Pengeringan Semprot pada Teh Hijau Instan [skripsi]. Bogor: Institut Pertanian Bogor.
Shi J et al. 2003. Optimization of the extraction of polyphenols from grape seed meal by aqueous ethanol solution. J Food Agric & Environ 1:42-47.
Siringo-ringo MP. 2003. Optimalisasi Ekstraksi Polifenol Teh Hijau Berdasarkan Ukuran Butir, Nisbah Bahan Baku-Pelarut, Dan Waktu [skripsi]. Bogor: Institut Pertanian Bogor.
Song HB. 2001. Study on green tea extraction technology. J Chin Institute of Food Sci and Technol 1: 19-23.
Trevisanato S, Kim Y. 2000. Tea and Health. Int. Life Science Institute 58: 1-10.
Tuminah S. 2004. Teh [Camellia sinensis
O.Kvar.Assamica (Mast)] sebagai salah satu sumber antioksidan. J Cermin Dunia Kedokteran 144:52-54.
Wang H. 2001. Determination of flavonols in green and black tea leaves and green tea infusions by high performance liquid chromatography. Food Res Int 34:223-227
Wikipedia. 2007. Tea. http://en.wikipedia.org/ wiki/Tea.html. [10 Januari 2007].
10
11
Lampiran 1 Jenis-jenis kelompok teh
teh hitam
teh oolong
teh hijau
teh putih
Sumber: Anonim (2007)
Lampiran 2 Kandungan senyawa kimia teh hijau
No. Komponen % (b/b)
Bobot kering
1. Kafein 7,43
2. (-) Epikatekin 1,98 3. (-) Epikatekin galat 5,20 4. (-) Epigalokatekin 8,42 5. (-) Epigalokatekin galat 20,29
6. Flavonol 2,23
7. Teanin 4,70
8. Asam glutamate 0,50 9. Asam aspartat 0,50
10. Arginin 0,74
11. Asam amino lain 0,74
12. Gula 6,68
13. Bahan yang dapat mengendapkan alkohol 12,13
14. Kalium 3,96
12
Lampiran 3 Diagram alir penelitian
Serbuk teh hijau 80 g
Maserasi Parameter :
• Suhu 80oC
• Kecepatan pengaduk 90 rpm • Waktu 20 menit
Evaporasi pelarut (Rotavapor) Penyaringan
Filtrat
Kondisi Optimal
Variasi evaporasi disajikan dalam Tabel 2. • Evaporasi dilakukan sebanyak 3 ulangan
Penentuan kadar polifenol berdasarkan kondisi
evaporasi optimum
13
Lampiran 4 Kadar air serbuk teh hijau (AOAC 1984)
Ulangan a B Kadar air (%)
1 2,0022 1,9248 3,86
2 2,0016 1,9283 3,66
3 2,0034 1,9262 3,85
Rerata 3,79 + 0,11
Keterangan:
a : bobot sampel sebelum dikeringkan (g) b : bobot sampel setelah dikeringkan (g)
Contoh perhitungan: Kadar air = a – b x 100% a
= 2,0022 – 1,9248 x 100% 2,0022
= 3,86%
Lampiran 5 Kadar abu serbuk teh hijau (AOAC 1984)
Ulangan a B Kadar abu (%)
1 2,0040 0,1031 5,14
2 2,0051 0,1025 5,11
3 2,0036 0,1018 5,08
Rerata 5,11 + 0,03
Keterangan:
a : bobot sampel sebelum ditanur (g) b : bobot abu (g)
Contoh perhitungan: Kadar abu = b x 100% a
= 0,1031 x 100%
2,0040
14
Lampiran 6 Hasil evaporasi ekstrak cair daun teh
Bobot ekstrak (g) Tekanan
dalam labu (mBar)
Suhu penangas
(oC)
Jenis ulangan
Bobot serbuk
(g) Awal Akhir % Rendemen
Bobot air teruapkan
(g)
Waktu (jam)
Laju evaporasi
air (g/detik) 80 50 1 80 200,4 11,4 14,25 189,0 3,6483 0,0144
2 80 200,4 11,5 14,38 188,9 3,6756 0,0143 3 80 200,6 11,4 14,25 189,2 3,7183 0,0141 60 1 80 200,4 11,4 14,25 189,0 1,1808 0,0445 2 80 200,6 11,5 14,38 189,1 1,1906 0,0441 3 80 200,6 11,5 14,38 189,1 1,1942 0,0440 70 1 80 200,8 11,5 14,38 189,3 0,6719 0,0783 2 80 200,2 11,4 14,25 188,8 0,6453 0,0813 3 80 200,6 11,4 14,25 189,2 0,6725 0,0781 90 50 1 80 200,7 11,5 14,38 189,2 5,7231 0,0092
2 80 200,6 11,4 14,25 189,2 5,7544 0,0091 3 80 200,2 11,4 14,25 188,8 5,7214 0,0092 60 1 80 199,7 11,4 14,25 188,3 1,4061 0,0372 2 80 200,3 11,4 14,25 188,9 1,3961 0,0376 3 80 200,4 11,4 14,25 189,0 1,4114 0,0372 70 1 80 200,0 11,4 14,25 188,6 0,7381 0,0710 2 80 200,8 11,5 14,38 189,3 0,7439 0,0707 3 80 200,4 11,4 14,25 189,0 0,7456 0,0704 100 50 1 80 199,7 21,9 27,38 177,8 8,2628 0,0060
15
Lampiran 7 Hasil pemetaan kehomogenan laju penguapan air
C6 P e rc e n t 0,35 0,30 0,25 0,20 0,15 0,10 0,05 0,00 99 95 90 80 70 60 50 40 30 20 10 5 1 Mean 0,127 0,1910 StDev 0,06730 N 27 KS 0,149 P- Value
Probability Plot of C6 Normal
95% Bonferroni Confidence I nt ervals for St Devs
t_pompa s_penangas 100 90 80 70 60 50 70 60 50 70 60 50 0,04 0,03 0,02 0,01 0,00 Bartlett's Test 0,582
Test Statistic 12,47
P- Value 0,132
Lev ene's Test
Test Statistic 0,84
P- Value
Test for Equal Variances for C6
Residual P e r c e n t 0,002 0,001 0,000 - 0,001 - 0,002 99 90 50 10 1 Fitted Value R e s id u a l 0,30 0,25 0,20 0,15 0,10 0,002 0,001 0,000 - 0,001 - 0,002 Residual F r e q u e n c y 0,002 0,001 0,000 - 0,001 - 0,002 8 6 4 2 0
Obser vation Or der
R e s id u a l 26 24 22 20 18 16 14 12 10 8 6 4 2 0,002 0,001 0,000 - 0,001 - 0,002
Normal Probabilit y Plot of t he Residuals Residuals Versus t he Fit t ed Values
16
Lampiran 8 Hasil analisis dengan metode GLM
The SAS Sy s t em 22: 33 Sunday , Mar c h 13, 2005 14
The GLM Pr oc edur e
Cl as s Lev el I nf or mat i on
Cl as s Lev el s Val ues
t _s 9 8050 8060 8070 9050 9060 9070 10050 10060 10070
Number of Obs er v at i ons Read 26 Number of Obs er v at i ons Us ed 26
The SAS Sy s t em 22: 33 Sunday , Mar c h 13, 2005 15
The GLM Pr oc edur e
Dependent Var i abl e: t r ans
Sum of
Sour c e DF Squar es Mean Squar e F Val ue Pr > F
Model 8 0. 10652880 0. 01331610 60. 01 <. 0001
Er r or 17 0. 00377253 0. 00022191
Cor r ec t ed Tot al 25 0. 11030133
R- Squar e Coef f Var Root MSE t r ans Mean
0. 965798 7. 667329 0. 014897 0. 194289
Sour c e DF Ty pe I SS Mean Squar e F Val ue Pr > F
t _s 8 0. 10652880 0. 01331610 60. 01 <. 0001
Sour c e DF Ty pe I I I SS Mean Squar e F Val ue Pr > F
17
Hasil analisis dengan metode GLM (lanjutan)
The SAS Sy s t em 22: 33 Sunday , Mar c h 13, 2005 16
The GLM Pr oc edur e
Dunc an' s Mul t i pl e Range Tes t f or t r ans
NOTE: Thi s t es t c ont r ol s t he Ty pe I c ompar i s onwi s e er r or r at e, not t he ex per i ment wi s e er r or
r at e.
Al pha 0. 05 Er r or Degr ees of Fr eedom 17 Er r or Mean Squar e 0. 000222 Har moni c Mean of Cel l Si z es 2. 769231
NOTE: Cel l s i z es ar e not equal .
Number
of Means 2 3 4 5 6 7 8 9
Cr i t i c al
Range . 02671 . 02802 . 02884 . 02941 . 02982 . 03013 . 03036 . 03055
Means wi t h t he s ame l et t er ar e not s i gni f i c ant l y di f f er ent .
Dunc an Gr oupi ng Mean N t _s
A 0. 28285 2 8070 A
B A 0. 26920 3 9070 B
B C 0. 24702 3 10070 C
C 0. 23231 4 8060
D 0. 19421 3 9060 D
D 0. 18235 3 10060
E 0. 13052 3 8050 E
F E 0. 10605 2 9050 F
18
Lampiran 9 Analisis ragam pengaruh tekanan labu dan suhu terhadap laju penguapan air
Sumber keragaman
Jumlah kuadrat
Derajat bebas (dF)
Kuadrat
tengah Fhitung
Probabilitas (P) Model terkoreksi 0,10653 8 0,01332 60,01 0,0001 Tekanan * suhu 0,10653 8 0,01332 60,01 0,0001
Galat 0,00377 17 0,00022 - -
Total terkoreksi 0,11030 25 - - -
Lampiran 10 Hasil analisis laju penguapan air
Laju penguapan air (g/det) + SD Tekanan dalam labu
(mBar) 50 oC 60oC 70oC 80 0,0143 + 0,0001 e 0,0442 + 0,0002 c 0,0792 + 0,0018 a 90 0,00916 + 0,00003 ef 0,0373 + 0,0002 d 0,0707 + 0,0003 ab 100 0,00598 + 0,00003 f 0,0330 + 0,0002 d 0,0597 + 0,0011 bc
Keterangan: SD: simpangan baku. Rerata yang diikuti oleh huruf yang sama
menyatakan tidak berbeda nyata berdasarkan analisis GLM (uji Duncan,
α
= 0,05).
Lampiran 11 Kurva larutan standar
Konsentrasi
standar (ppm) Absorban
0 0 25 0,1459 50 0,3298 100 0,5469 150 0,8397 200 1,0784
y = 0.0054x + 0.021 R2 = 0.99
0 0.2 0.4 0.6 0.8 1 1.2
0 50 100 150 200 250
Konsentrasi (ppm)
A
b
sor
b
an
19
Lampiran 12 Kadar polifenol ekstrak daun teh
Absorbans/ ulangan Tekanan dalam labu (mBar) Suhu penangas
(oC) A1 A2 A3 Rerata
Konsentrasi dalam kurva standar (ppm) Kadar polifenol dalam 80 g serbuk daun
(%) 80 50 0,1478 0,1516 0,1494 0,1496 23,8148 3,40
60 0,1588 0,1556 0,1582 0,1576 25,2840 3,63 70 0,1580 0,1592 0,1576 0,1583 25,4198 3,63 90 50 0,1464 0,1456 0,1453 0,1458 23,1049 3,30
60 0,1567 0,1572 0,1557 0,1565 25,0988 3,58 70 0,1591 0,1574 0,1582 0,1582 25,4136 3,63 100 50 0,1426 0,1436 0,1437 0,1433 22,6481 6,22
60 0,1546 0,1503 0,1558 0,1536 24,5494 3,52 70 0,1569 0,1581 0,1584 0,1578 25,3333 3,62
Contoh perhitungan :
Kadar (%) =
)
(
)
(
1000
1
)
(
)
/
(
g
serbuk
bobot
g
analisis
ekstrak
bobot
mg
g
g
kental
ekstrak
bobot
F
V
ml
mg
ppm
analisis konversi×
×
×
×
×
=g
g
mg
g
g
ml
ml
mg
80
01
,
0
1000
1
43
,
11
5
,
0
100
5
,
0
1000
8148
,
23
×
×
×
×
×
20
Lampiran 13 Alat penguap putar Laborota 4003 control vario
a
b
Keterangan : a) pompa vakum