PENENTUAN KONVERSI CO YANG MENJADI METANOL
PADA METANOL REAKTOR DI PT. KALTIM
METANOL INDUSTRI
BONTANG
KARYA ILMIAH
MUHAMMAD MARDUANSYAH
102401052
PROGRAM STUDI DIPLOMA 3 KIMIA
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
PENENTUAN KONVERSI CO YANG MENJADI METANOL
PADA METANOL REAKTOR DI PT. KALTIM
METANOL INDUSTRI
BONTANG
KARYA ILMIAH
Diajukan untuk melengkapi tugas dan memenuhi syarat memperoleh Ahli Madya
MUHAMMAD MARDUANSYAH
NIM : 102401052
PROGRAM STUDI DIPLOMA 3 KIMIA
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
PERSETUJUAN
Judul : Penentuan Konversi CO Yang Menjadi Metanol Pada Metanol Reaktor di PT. Kaltim Metanol Industri
Kategori : Karya Ilmiah
Nama : Muhammad Marduansyah Nomor Induk Mahasiswa : 102401052
Program Studi : Diploma 3 Kimia Departemen : Kimia
Fakultas : Matematika Dan Ilmu Pengetahuan Alam Universitas Sumatera Utara
Disetujui di Medan, Juni 2013
Program Studi D3 Kimia
Ketua, Pembimbing,
Dra. Emma Zaidar Nasution, M.Si Dr. Andriayani,M.Si NIP.195512181987012001 NIP.196903051999032001
Departemen Kimia FMIPA USU Ketua,
PERNYATAAN
PENENTUAN KONVERSI CO YANG MENJADI METANOL PADA METANOL REAKTOR DI PT. KALTIM
METANOL INDUSTRI BONTANG
KARYA ILMIAH
Saya mengakui bahwa tugas akhir ini adalah hasil karya sendiri. Kecuali beberapa kutipan dan ringkasan yang masing-masing disebutkan sumbernya.
Medan, Juni 2013
PENGHARGAAN
Bismillaahhirrohmaanirrohiim.
Alhamdulillahi Robbil Alamin Penulis ucapkan sebagai suatu ungkapan rasa syukur kepada Allah SWT yang Maha Esa atas kuasanya yang tetap mencurahkan berkah, rahmat, nikmat kesehatan jasmani dan rohani, serta taufiq dan hidayahnya sehingga penulis dapat menjalani hidup dengan penuh makna dan insyaallah akan lebih bermakna lagi. Shalawat dan salam penulis hantarkan kepada Nabi Muhammad SAW yang telah mengemban risalah dan mengalirkan nilai-nilai islam dalam rangkaian tarbiah kepada seluruh umat. Alhamdulillah tidak habisnya penulis ucapkan rasa syukur, atas ridho Allah SWT penulis dapat menyelesaikan Karya Ilmiah ini sebagai salah satu syarat untuk meraih gelar Ahli Madya (AMD) pada program studi Kimia Industri Diploma III di Fakultas Matematika Dan Ilmu Pengetahuan Alam Universitas Sumatera Utara.
Karya Ilmiah ini ditulis berdasarkan pengamatan dan pengalaman penulis selama menjalani Praktek Kerja Lapangan (PKL) di PT. Kaltim Methanol Industri dari tangal 11 Februari 2013 sampai dengan 1 Maret 2013. Penulis menyadari sepenuhnya bahwa Karya Ilmiah ini masih jauh dari kesempurnaan karena adanya keterbatasan pada penulis, baik dari segi pengetahuan, waktu, maupun keterbatasan penulis. Meski demikian penulis mengharapkan karya ilmiah ini dapat bermanfaat bagi penulis dan semua pihak yang telah membaca karya ilmiah ini serta dapat bermanfaat bagi Universitas Sumatera Utara.
Pada masa penyelesaian karya ilmiah ini, Penulis telah banyak mendapatkan dukungan, bantuan dan juga arahan dari berbagai pihak yang terlibat. Oleh karena itu, dengan rasa keikhlasan dan kerendahan hati penulis ingin menyampaikan rasa terima kasih dan penghargaan kepada :
2. Andryani,S.Pd.,M.Si selaku dosen pembimbing yang dengan sabar membimbing dan meluangkan waktunya kepada penulis dalam penyusunan Karya Ilmiah ini.
3. Dr. Sutarman, M.Sc, selaku Dekan Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Sumatera Utara.
4. Dr. Rumondang Bulan, M.S, selaku ketua Departemen Kimia Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Sumatera Utara.
5. Dra. Emma Zaidar, M.Sc, selaku ketua Program Studi D-III Kimia Industri Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Sumatera Utara.
6. Seluruh staf pengajar Fakultas Matematika dan Ilmu Pengetahuan Alam khususnya jurusan Kimia yang telah mendidik penulis dalam menyelesaikan karya ilmiah ini.
7. Pak Dedy Rahmat Utomo ST selaku Pembimbing saya selama melakukan kerja praktek di PT. Kaltim Methanol Industri.
Penulis sudah berupaya semaksimal mungkin dalam menyusun dan menyelesaika karya ilmiah ini, namun penulis mengharapkan kritik dan saran yang bersifat membangun dari pembaca.
Akhir kata penulis mengucapkan Terima Kasih kepada semua pihak yang telah banyak membantu demi selesainya karya ilmiah ini dan penulis berharap semoga karya ilmiah ini dapat bermanfaat bagi kita semua.
Medan, Juli 2013 Penulis,
PENENTUAN KONVERSI CO YANG MENJADI METANOL PADA METANOL REAKTOR DI PT. KALTIM
METANOL INDUSTRI BONTANG
ABSTRAK
PENENTUAN KONVERSI CO YANG MENJADI METANOL PADA METANOL REAKTOR DI PT. KALTIM
METANOL INDUSTRI BONTANG
ABSTRACT
BAB 3. Metode Penelitian
3.1 Alat-Alat 19 3.2 Bahan – Bahan 19 3.3 Prosedur Percobaan 19
BAB 4. Hasil dan Pembahasan
4.1 Hasil Perhitungan 22 4.2 Pembahasan 31
BAB 5. Kesimpulan dan Saran
5.1 Kesimpulan 33 5.2 Saran 33
DAFTAR TABEL
Nomor Judul Halaman Tabel
DAFTAR GAMBAR
Nomor Judul Halaman Gambar
PENENTUAN KONVERSI CO YANG MENJADI METANOL PADA METANOL REAKTOR DI PT. KALTIM
METANOL INDUSTRI BONTANG
ABSTRAK
PENENTUAN KONVERSI CO YANG MENJADI METANOL PADA METANOL REAKTOR DI PT. KALTIM
METANOL INDUSTRI BONTANG
ABSTRACT
BAB 1
PENDAHULUAN
1.1 Latar Belakang
Mengingat perkembangan teknologi yang semakin pesat pada sekarang ini, maka
permintaan akan produk serta mutu produk yang dihasilkan tentu harus semakin baik
pula. Karena itu setiap perusahaan harus memperhatikan atau meningkatkan mutu
barang yang dihasilkan sesuai keinginan pasar, karena mutu produk merupakan
ukuran penting bagi konsumen dan dapat menentukan kemajuan suatu perusahaan.
Untuk menghasilkan mutu yang baik, maka perusahaan harus menata dan
memperhatikan proses pengolahan pada setiap unit operasi sehingga dapat
menghasilkan produk yang baik dan dapat juga diterima oleh pasar lokal maupun
pasar internasional.
Indonesia adalah Negara dengan kekayaan alam yang sangat banyak, minyak,
batu bara, emas dan juga gas alam. Gas alam yang dikandung dibumi Indonesia ini
dapat memberikan kontribusi yang besar terhadap pemasukan Negara. Salah satu
industri yang memanfaatkan gas alam sebagai bahan baku pembuatan metanol adalah
PT. Kaltim Methanol Industri (KMI). Prospek metanol dimasa yang akan datang
terutama untuk industri bahan perekat kayu lapis atau bahan dasar pembuatan
formaldehid. Peningkatan permintaan tersebut akan terus bertambah seiring dengan
semakin berkembangnya industri hilir yang memanfaatkan metanol. Produk PT. KMI
telah mampu menembus pasar diberbagai wilayah baik dalam maupun luar negeri
seperti Korea, Malaysia, Amerika, Cina, Jepang, Bangkok, Singapura, Taiwan,
Australia, Filipina dan India.
Ada tiga proses tahap utama yang terjadi pada pembuatan metanol di PT.
KMI yaitu: yang pertama, unit reforming (unit-100) berfungsi untuk mempersiapkan
bahan baku yang akan masuk kedalam reaktor metanol pada unit sintesis agar sesuai
dengan kondisi reaktor dan dapat beroperasi dengan optimal. Pada unit ini terdapat
beberapa bagian antara lain : desulphurisasi, pre-reforming, steam reforming,
autothermal reforming.
Yang kedua, unit reaktor sintesis metanol (unit-200) adalah unit pembentukan
metanol yang berasal dari gas sintesis reformer. Berdasarkan cara kerjanya biasanya
reaktor menggunakan katalis Cu/ZnO/Al2O3 sesuai dengan jenis dan reaksi yang
terjadi didalam reaktor tersebut. Reaktor ini merupakan reaktor tubular dengan tube
yang diisi katalis khusus yaitu CuO yang dikelilingi oleh boiling water. Katalis
diletakkan diatas bed inert ball yang ditampung di antara tube sheet bagian bawah
dan penahan berlubang berbentuk kerucut. Reaksi yang terjadi didalam reaktor
metanol (020-R01A/B) adalah reaksi kesetimbangan, reaksi ini bersifat eksotermis.
Reaktor dirancang agar reaksi berlangsung pada tekanan sekitar ± 80 bar dan
temperatur sekitar 250oC. Selain itu juga perlu diperhatikan kinerja dari katalis,
Salah satu parameter untuk melihat baik atau tidaknya kinerja dari reaktor metanol
dapat dilihat dari konversi CO pada pembentukan metanol.
Yang ketiga, unit destilasi metanol (unit 300) berfungsi untuk memurnikan
metanol dari zat pengotor agar mendapatkan kualitas metanol tertinggi grade AA
dengan kandungan metanol minimal 99,85% (KMI,1997)
Berdasarkan uraian diatas, Penulis tertarik mengambil judul “Menentukan
Konversi CO Yang Menjadi Metanol Pada Reaktor Metanol Di PT. Kaltim Metanol
Industri”.
1.2 Perumusan Masalah
Reaktor metanol merupakan salah satu alat utama dan memegang peranan yang
sangat penting dalam industri pembuatan metanol, pada metanol reaktor ini terjadi
pembentukan metanol. Oleh karena itu, sangatlah penting untuk mengetahui kinerja
dari metanol reaktor ini. Kinerja dari metanol reaktor dapat ditunjukkan dengan cara
membandingkan profil konversi CO dari waktu ke waktu. Untuk mengetahui
konversi CO ini perlu mengkaji distribusi komponen masuk dan keluar dari metanol
reaktor dari peneracaan massa.
Perhitungan neraca massa dilakukan untuk mengevaluasi beberapa variabel
antara lain laju alir massa, laju alir volumetrik, laju alir molar dan komposisi
komponen aliran. Perhitungan neraca massa tersebut tidak hanya dilakukan disekitar
metanol reaktor tetapi juga perlu dilakukan disekitar metanol separator (020-F02),
tersebut akan menunjang peneracaan massa disekitar metanol reaktor. perhitungan
dapat dilakukan dengan bantuan program komputer sehingga dapat mempermudah
dan mempersingkat waktu.
1.3 Tujuan Percobaan
1. Untuk menentukan konversi CO yang menjadi metanol
2. Untuk menentukan komposisi gas CO sisa yang keluar dari metanol reaktor
(020-R01 A/B).
1.4 Manfaat Percobaan
1. Dapat menambah ilmu pengetahuan bagi pembaca dalam proses
pengolahan industri metanol.
2. Sebagai masukan dan sumber inspirasi baru bagi pembaca dalam proses
pengolahan industri metanol.
3. Dapat mengetahui berapa lama aktivitas katalis dalam reaktor metanol
BAB 2
TINJAUAN PUSTAKA
2.1. Metanol
Metanol merupakan cairan polar yang dapat bercampur dengan air, alkohol – alkohol
lain seperti, ester, keton, eter, dan sebagian besar pelarut organik. Metanol sedikit
larut dalam lemak dan minyak. Titik didih metanol berada pada 64,7oC dengan panas
pembentukan (cairan) –239,03 kJ/mol pada suhu 25oC. Metanol mempunyai panas
fusi 103 J/g dan panas pembakaran pada 25oC sebesar 22,662 J/g. Tegangan
permukaan metanol adalah 22,1 dyne/cm sedangkan panas jenis uapnya pada 25 oC
sebesar 1,370 J/(gK) dan panas jenis cairannya pada suhu yang sama adalah 2,533
J/(gK) (Winarso,1998).
Metanol dapat dibuat dari proses penyulingan kayu, gasifikasi batu bara muda
dan sintesis gas alam. Sintesis metanol dari gas alam saat ini tekhnologinya di pakai
pada pembuatan metanol skala industri di mana di Indonesia sendiri baru ada 2 pabrik
yang mengolahnya yaitu kilang metanol Bunyu di Tarakan, Kaltim dengan kapasitas
produksi 1000 MT/day dan kilang metanol Kaltim Metanol Industri di Bontang juga
Adapun secara ringkas, tahapan proses pembuatan metanol adalah sebagai berikut (di
pakai di kilang KMI Bontang) :
2.2. Unit 100 – Reforming
Unit ini berfungsi untuk mempersiapkan bahan baku yang masuk menuju reaktor
metanol agar sesuai dengan kondisi operasi reaktor metanol tersebut. Pada unit ini
terdapat beberapa bagian pula, antara lain:
2.2.1. Desulfurisasi
Tahap desulfurisasi bertujuan menurunkan kandungan sulfur dalam bahan baku gas
alam sampai kadar yang diijinkan dalam proses. Proses ini menjadi penting karena
katalis yang digunakan pada unit pre-reforming dan sintesis metanol sensitif terhadap
keracunan sulfur.
2.2.2. Pre-Reporming
Gas alam setelah keluar dari desulfurizer direaksikan dengan steam superheated,
reaksi yang terjadi sebagai berikut:
CnHm + n H2O ⇌ nCO + ( m
2+ n) H2 - panas CO + 3 H2 ⇌ CH4 + H2O + panas
2.2.3. Steam Reforming
Reaksi pemecahan metana
CH4 + H2O ⇌ CO + 3 H2 – panas
Komposisi gas yang keluar selanjutnya ditentukan oleh reaksi kesetimbangan
peruraian yang sangat eksotermis.
CO + H2O ⇌ CO2 + H2 + panas
2.2.4. Autotermal Reforming
Merubah sisa-sisa CH4 dengan steam dan O2 untuk mendapatkan sintesis gas pada
rasio stoikiometri yang optimum untuk proses sintesis metanol , di mana reaksi
parsial dan sempurna berlangsung sekaligus. Prinsip reaksi kimia meliputi proses
penyempurnaan pembakaran metana, oksidasi parsial metana dan reformasi metana.
CH4 + 2O2 ⇌ CO2 + 2H2O + panas CH4 + O2 ⇌ CO + H2 + H2O + panas CH4 + H2O ⇌ CO+ 3H2 - panas CO + H2O ⇌ CO2 + H2 + panas 2.3. Sintesis Metanol
Gas-gas CO, CO2, dan H2 menjadi CH3OH dan H2O lalu disintesis dalam reaktor
reaktor kemurniannya masih berkisar 70 %, maka dilakukan tahap akhir yaitu
destilasi untuk mendapatkan metanol dengan kemurnian tinggi.
Menurut standard International Methanol Producers and Consumer
Assocation (IMPCA) kualitas metanol tertinggi adalah grade AA dengan kandungan
metanol minimal 99,85 %, dan kandungan etanol maksimal 10 ppm (KMI,1997).
2.4. Reaktor
Jika tidak ada pertukaran panas yang berlebihan maka reaktor tersebut adalah
adiabatik. Jika reaktor beropresi sangat baik antara hubungan termal dengan
lingkungan sekitar maka temperatur menjadi konstan. (dalam kedua waktu dan posisi
dalam reaktor) dan dengan demikian reaksi yang terjadi didalam reaktor tersebut
adalah reaksi isotermal. Waktu yang dihabiskan dalam reaktor oleh setiap volume
cairan sama (Westerterp,1963).
Reaktor adalah salah satu unit proses yang paling penting dalam proses kimia.
Beberapa pertimbangan yang harus diperhatikan pada sebuah reaktor agar dapat
berjalan secara optimal antara lain kondisi operasi, reaksi yang terjadi dalam reaktor,
jenis reaktor dan katalis yang digunakan pada reaktor. Reaktor ideal berdasarkan
kerjanya bisa dibagi menjadi dua macam yaitu reaktor batch dan reaktor alir
kontinyu. Reaktor alir kontinyu sendiri dibagi menjadi dua macam, yaitu: Reaktor
2.4.1. Reaktor Batch
Reaktor batch sering digunakan untuk tingkat produksi kecil dan waktu reaksi
yang lama. Reaktor fleksibel dan kondisi reaksi dapat disesuaikan, berguna dalam
produksi berbagai bahan kimia yang berbeda. Operasi batch sering ditakutkan dimana
fouling atau kontaminasi cepat terjadi didalam reaktor. Biaya investasi reaktor batch
termasuk peralatan bantu umum yang relatif rendah. disisi lain, operasi manual
diperlukan pengawasan yang relatif luas, sementara operasi otomatis seringkali sulit
dan mahal. Berkenaan dengan kapasitas reaktor, telah ditunjukkan pada bagian
sebelumnya kapasitas tangki reaktor selalu lebih kecil dibandingkan tabung reaktor
(Westerterp,1987).
Reaktor batch berdasarkan sifatnya adalah transisi dari sistem tertutup.
Sementara reaktor batch dapat menjadi sederhana baik diaduk dalam botol batch
temperatur konstan, atau laboratorium reaktor batch skala pabrik. Diamati dari jenis
tingkat konsentrasi dapat disimpulkan bahwa percobaan dalam tipe batch, konsetrasi
dari reaktan dan produk diukur sebagai fungsi dari waktu. Seperti yang ditunjukan
sebelumnya, penggunaan reaktor memungkinkan untuk pengukuran langsung dari
laju reaksi. Dikondisi steady state (berada dalam reaktor batch), skala waktu
digunakan untuk teknik analitik dan pemisahan reaksi. Selain itu karena banyak
contoh dapat menjadi hasil dikondisi yang sama. Meningkatkan akurasi dari data
2.4.2. Reaktor Alir Tangki Berpengaduk
Pengukuran langsung harga reaksi untuk reaktor ideal adalah isotermal, tekanan
operasi reaktor aliran konstan di kondisi steady state dengan pencampuran yang
lengkap diseluruh reaktor sehingga komposisi seragam. Reaksi ideal ini sering
disebut reaktor alir tangki berpengaduk atau aliran kontinyu, reaktor tipe ini adalah
asumsi bahwa komposisi aliran buangan didalam reaktor terjadi pada komposisi
konstan (Davis,2003)
2.4.3. Reaktor Alir Pipa
Tipe lain dari reaktor ideal adalah operasi reaktor aliran tubular dengan reaksi
isotermal ditekanan konstan dan pada kondisi steady state dengan waktu tinggal yang
khusus. Tipe reaktor ini tetap normal karena pipa silinder penampang konstan.
Dengan demikian, aliran sebuah pengisi berjalan disepanjang tabung dan campuran
sebagai pengisi berjalan lancar di sepanjang tabung. Karena itu diberi nama plug flow
reactor (PFR). Asumsi ini tidak ada terjadi pencampuran antara volume cairan
dengan elemen radial (aliran normal) atau aksial (arah aliran) yang berdekatan.
Artinya setiap elemen volume memasuki reaktor memiliki jarak waktu yang sama
karena pertukaran massa tidak pada massa yang lain (Devis,2003).
2.5. Fixed Bed Reaktor
Merupakan suatu reaktor yang mana katalis berdiam di dalam reaktor bed, didalam
reaktor, katalis ditopang oleh suatu struktur penyangga katalis berupa penampang
bervariasi sesuai dengan ukuran partikel katalis baik disisi terbawah maupun
dilapisan teratas bed katalisator.
Secara spesifik, fixed bed reaktor yang ada di unit pengolahan minyak bumi
dirancang berdasarkan kebutuhan proses. Struktur internal reaktor pun berbeda dari
satu dengan lainnya. Karena sifatnya yang sangat spesifik, perancangan reaktor itu
sendiri biasanya juga terkait dengan lisensi prosesnya. Hal ini terkait dengan
kebutuhan proses, terutama terkait dengan kebutuhan katalis yang sangat spesifik
tergantung pada fungsinya masing-masing. Meskipun demikian, secara umum
bagian-bagian internal reaktor tetap sama, hanya saja tiap lisensi proses maupun
reaktor tersebut memiliki tipe desain masing-masing yang diharapkan mampu
mengoptimalkan fungsi dari reaktor tersebut.
Bagian utama dari sebuah fixed bed reaktor adalah reaktor vessel, reaktor
internal, katalisator, inert balls dan tingkat katalisator. Reaktor vessel merupakan
bagian yang menyediakan tempat bagi katalis dan tempat berlangsungnya kontak
antara minyak umpan dan katalis yang kemudian terjadi reaksi. Reaktor vessel
dirancang dengan dasar perancangan pressure vessel (ASME BPVC Section VIII
Division 2). Kunci dari perancangan reaktor vessel ini adalah pemilihan material,
tekanan kerja yang diinginkan (allowable working pressure), dimensi dan ketebalan
dinding vessel (Howard, 1957).
2.6. Konversi
Untuk mengurangi efek CO terhadap lingkungan, dibutuhkan usaha memanfaatkan
adalah hidrogenasi katalitik gas CO menjadi metanol. CO dapat dikonversi menjadi
metanol. Konversi tersebut dapat ditingkatkan dengan penggunaan katalis yang
berperan mempercepat jalannya reaksi dan mengarahkan reaksi sesuai yang
diinginkan agar reaksi tetap berlangsung secara konstan.
Dilihat dari maafaat cukup bervariasi penggunaan metanol, maka perlu dilakukan
pelajaran mengenai konversi gas CO menjadi metanol. Kendala yang dihadapi dalam
sintesis metanol melalui reaksi hidrogenasi katalitik CO diantaranya yaitu:
a. Kondisi operasi tekanan dan temperatur sintesis metanol relatif tinggi. Hal ini
menyebabkan tingginya biaya investasi dan operasional.
b. Konversi CO2 dan selektivitas yang rendah sehingga membutuhkan investasi besar
untuk mendaur ulang umpan CO2 yang tidak terkonversi.
c. Belum ditemukannya katalis yang optimal untuk mengkonversi CO2 dengan
selektivitas yang tinggi terhadap metanol.
Untuk mengatasi kendala tersebut, harus terfokus pada pengembangan katalis
berbasis Cu dan Zn karena kedua komponen tersebut telah dinyatakan aktif dalam
sintesis metanol (Zenta,2009).
2.7. Katalis
Katalis merupakan suatu zat yang dapat mempercepat suatu reaksi serta dapat
mempertahankan suatu reaksi agar tetap berlangsung secara tetap atau konstan.
dapat bertumbukan, sehingga kesetimbangan reaksi cepat tercapai. Katalis yang baik
dapat menginduksi transformasi molekul-molekul reaktan dengan cepat tanpa
mengalami penurunan kualitas yang berarti. Katalis hanya dapat mempercepat
tercapainya kesetimbangan reaksi dan tidak dapat menggesernya (Twigg,1970).
Katalis yang memiliki fasa yang sama dengan reaktan disebut dengan katalis
homogen, sedangkan apabila fasanya berbeda disebut heterogen. Didalam industri
katalis memiliki kemampuan kerja bergantung pada tiga karakter yaitu :
1. Aktivitas katalis.
Kemampuan katalis untuk mempercepat konversi umpan menjadi produk per
satuan berat atau volume katalis pada kondisi tertentu. Aktivitas katalis per satuan
volume menjadi hal penting secara ekonomi karena berpengaruh terhadap ukuran
dan harga reaktor. Penurunan aktivitas katalis akan menyebabkan konversi reaksi
akan turun pada waktu tinggal yang tetap.
Umumnya kerusakan katalis (deaktivasi katalis) dibagi menjadi:
a. Pengerakan (fouling)
Deaktivasi katalis akibat pengerakan, pada umumnya berlangsung cepat.
Pengerakan terjadi jika ada zat-zat dalam reaktor terdeposit diatas permukaan
katalis dan menutup pori-pori katalis secara fisik. Karbon merupakan bentuk
kerak yang paling umum dan bentuk pengerakannya disebut coking. Misalnya
pembentukan coke (C) pada reaksi pemecahan hidrokarbon.
CH4 C + 2H2
Reaksi pembentukan deposit karbon terjadi pada rentan temperatur antara
650-800oC.
b. Peracunan (poisoning)
Deaktivasi katalis akibat peracun, umumnya berlangsung lambat, peracunan
disebabkan oleh penyerapan zat kimia. Zat-zat dalam aliran proses ini
kemudian menutup atau memodifikasi aktif sintesis pada katalis racun dapat
menyebabkan perubahan morfologi permukaan katalis baik melalui
rekonstruksi permukaan maupun relaksasi permukaan.
c. Kerusakan (sintering)
Deaktivasi katalis yang disebabkan oleh pertumbuhan atau aglomerasi
kristal yang akan merubah struktur kimia katalis atau kemampuan kerja
optimum katalis.
2. Selektivitas katalis
Kemampuan katalis untuk mengarahkan reaksi spesifik untuk menghasilkan
produk yang diinginkan sehingga berlangsung reaksi pembentukan produk yang
lain dapat dihambat.
3. Umur katalis
Periode dimana katalis dapat mempercepat reaksi pada rentang waktu yang telah
ditentukan. Umur katalis berkaitan erat dengan aktivitas dan selektivitas. Apabila
katalis yang telah mengalami penurunan kekuatan mekanik, aktivitas dan
selektivitas yang berakibat penurunan konversi secara drastis maka dikatakan
bahwa katalis telah berumur dan harus segera diregenerasi atau diganti
2.8. Neraca Massa
Neraca massa adalah suatu perhitungan bahan yang masuk dan keluar dalam suatu
sistem. Perhitungan ini sangat diperlukan dalam rancangan bangun alat, evaluasi dan
efisiensi kerja alat serta kebutuhan bahan baku dari suatu produk. Perhitungan neraca
massa berdasarkan hukum kekekalan massa, dimana tidak akan pernah terjadi massa
yang hilang, akan tetapi massa yang masuk hanya berubah bentuk, sehingga massa
yang masuk selalu sama dengan massa yang keluar. Untuk sebuah sistem yang
diamati, neraca massa total dinyatakan sebagai berikut :
[Laju Akumulasi Massa] = [Laju Massa Masuk] – [Laju Massa Keluar]
����� �= mmasuk - mkeluar ………. 2.1
Pada saat kondisi Sready State (tunak) tercapai laju akumulasi adalah nol. Maka pada
kondisi tunak persamaan 2.1 menjadi
0 = ������- �������
0 = ������� ………. 2.2
Untuk proses yang berjalan steady state (kondisi tunak), laju aliran massa
yang memasuki sistem aliran harus sama dengan yang meninggalkan sistem itu,
karena dalam sistem aliran yang berada pada kondisi steady state massa tidak
bertambah atau berkurang.
Neraca massa berlaku untuk keseluruhan proses atau alat, dan juga untuk
bagian proses atau alat tersebut. Oleh karena itu, berlaku untuk keseluruhan bahan
yang masuk dan keluar dari proses tersebut atau untuk salah satu bahan (komponen)
2.9. Konsep Kesetimbangan
Pada umumnya reaksi kimia terjadi secara bolak-balik (reversible). Reaksi yang
berjalan secara searah (irreversible) relatif lebih sedikit dibanding yang bolak-balik.
Kesetimbangan kimia terjadi untuk reaksi yang bersifat reversible. Kesetimbangan
kimia adalah keadaan di mana reaksi kecepatan pembentukan produk dan peruraian
produk adalah sama. Secara makroskopis sudah tidak terlihat lagi perubahan kuantitas
reaktan maupun produk. Kesetimbangan kimia pada suatu reaksi melibatkan dua
senyawa berbeda yang bertindak masing-masing sebagai reaktan dan produk.
Untuk reaksi aA + bB ⇌ cC + dD, konstanta kesetimbangan dituliskan sebagai:
Kc
[C]c[D]d
[A]a[B]b
Kc dikenal sebagai tetapan kesetimbangan, (c menunjukan konsentrasi yang
dinyatakan dalam mol per liter, seperti dinyatakan dalam penggunaa kurung siku ([ ]).
Ada beberapa hal yang dapat dijadikan acuan ringkas kaitannya dengan Kc pada suatu
reaksi, yaitu:
1. Jika persamaan reaksi dibalik, maka persamaan reaksi kesetimbangan yang
baru mempunyai tetapan kesetimbangan yang besarnya merupakan kebalikan
dari tetapan kesetimbangan semula, yaitu 1 Kc.
2. Jika persamaan kimia dikalikan factor n, maka persamaan faktor
kesetimbangan yang baru mempunyai tetapan kesetimbangan yang besarnya
adalah tetapan kesetimbangan semula dipangkatkan dengan faktor n tersebut,
2.9.1. Meramalkan Arah Reaksi
Tetapan kesetimbangan dapat membantu untuk meramalkan arah dari suatu reaksi
hingga tercapai kesetimbangannya, serta dapat untuk menghitung konsentrasi dari
reaktan dan produk pada keadaan kesetimbangan.
Jika dalam persamaan tetapan kesetimbangan, konsentrasi produk dan reaktan yang
dimasukkan bukan pada keadaan kesetimbangan, maka harga yang diperoleh disebut
koefisien reaksi (Q). Dari besaran Q ini, dapat meramalkan arah dari reaksi yang akan
terjadi yaitu dengan membandingkan nilai dari Q dan K. ada tiga kemungkinan yang
mungkin terjadi, yaitu:
1. Q < K, perbandingan konsentrasi awal dari produk terhadap reaktan terlalu
kecil sehingga untuk mencapai kesetimbangan, reaktan harus berubah menjadi
produk. Dengan kata lain, reaksi akan bergeser ke arah pembentukan produk.
2. Q = K, konsetrasi awal sudah setimbang. Maka sistem dalam keadaan
setimbang.
3. Q >K, perbandingan konsentrasi awal dari produk terhadap reaktan terlalu
besar, sehingga untuk mencapai kesetimbangan, produk harus terurai menjadi
reaktan. Dengan kata lain, reaksi akan bergeser ke arah pembentukan reaktan.
2.9.2. Prinsip Le Chatellier
Kesetimbangan kimia menggambarkan neraca suatu reaksi bolak-balik. Dalam
banyak kasus, neraca kesetimbangan merupakan hal yang cukup penting dalam suatu
proses kimia. Merubah kondisi operasi akan dapat mengganggu neraca
kesetimbangan dan arah kesetimbangan akan bergeser sehingga akan mempengaruhi
tersebut diantaranya adalah perubahan suhu, tekanan, volume dan konsentrasi.
Komposisi zat-zat dalam suatu reaksi setelah tercapainya kesetimbangan pada suhu
tertentu adalah konstan. Factor volume merupakan kebalikan dari tekanan, jika
tekanan diperbesar maka volume akan mengecil, begitu juga sebaliknya.
Pada tahun 1888 Henri Louis Le Chatelier mengenalkan suatu asas yang
kemudian dikenal sebagai asas Le Chatelier (prinsip Le Chatelier) yang berbunyi,
“jika pada suatu sistem kesetimbangan dilakukan aksi tertentu, sistem akan
mengadakan reaksi untuk mengurangi pengaruh aksi tersebut”. Aksi yang dimaksud
dalam pernyataan di atas adalah melakukan tindakan dengan mengubah konsentrasi,
tekanan, volume dan suhu. Prinsip Le Chatelier membantu untuk dapat memprediksi
arah kesetimbangan baru jika sistem tersebut dikenal aksi. Lebih penting lagi, sistem
ini membantu industri kimia untuk menciptakan kondisi optimum yang dapat
BAB 3
METODE PENELITIAN
3.1. Alat – Alat
- Metanol Separator (020-F02)
- Metanol Reaktor (020-R01 A/B)
- Expansion Vessel (030-F01)
- Prerun Column (030-D01)
3.2. Bahan – Bahan
- Gas CO (karbon monoksida)
- Gas CO2 (karbon dioksida)
- Gas H2 (hidrogen)
- Gas CH4 (metana)
- Gas N2 (nitrogen) - Katalis CuO
- Bola keramik (bed inert ball)
3.3. Prosedur
Untuk menyelesaikan tugas ini, dibutuhkan data yang meliputi laju alir volumetrik
(flow rate) dan komposisi aliran disekitar Metanol Reaktor (020-R01 A/B), Metanol
Separator (020-F02), Expansion Vessel (030-F01) dan Prerun Column (030-D01).
System (DCS) unit 100, 200 dan 300 serta untuk membandingkan hasil perhitungan
dibutuhkan data desainnya. Dalam beberapa hal diperlukan asumsi untuk dapat
menyelesaikan neraca massa, asumsi tersebut diambil untuk mempermudah
perhitungan.
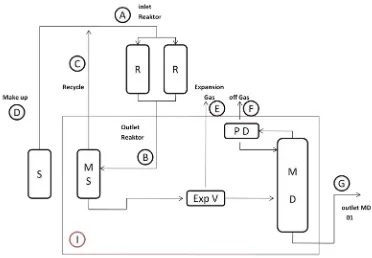
Dalam perhitungan dibutuhkan bagan alir proses sintesis metanol dapat dilihat
pada gambar 3.1.
Keterangan Gambar : S = Separator
MS = Metanol Separator
R = Reaktor
MD = Menara Destilasi
Exp V = Expansion Vessel
Merubah satuan massa
Massa gas = % vol gas x laju alir volumetrik x BM
% massa = massa gas
massa total x 100
Neraca massa komponen CO blok I
Laju Alir Massa Outlet Reaktor (B) = Laju alir Massa Recycle (C) + Laju alir Massa
Expansion Gas (E) + Laju Alir Massa Off
gas (F) + Laju Alir Massa Outlet Menara
Distilasi (G)
Atau
Neraca Massa Total Blok I
Laju Alir Massa CO Outlet Reaktor = Laju alir Massa CO Recycle + Laju Alir
Massa CO Expansion Gas + Laju AlirMassa
CO Off Gas + Laju Alir Massa CO Outlet
Menara Distilasi
Atau
B ZCO = C YCO + E X CO + F W CO + G V CO ……..……… 3.2
Dimana :
B, C, E, F dan G = laju alir massa masing-masing arus (Kg/Jam)
BAB 4
HASIL DAN PEMBAHASAN
4.1 Hasil Perhitungan Basis : 1 jam Operasi
Asumsi yang diambil :
1. Kondisi tunak (steady state), sehingga akumulasi = 0
2. Data diambil pada tanggal 25 Februari 2013
Data – data yang diketahui adalah sebagai berikut :
1. Arus C (Recycle gas)
Laju alir volumetrik = 595783 Nm3
Komposisi gas : CO2 = 7,17% vol
CO = 2,70% vol
H2 = 66,26% vol
CH4 = 2,70% vol
N2 = 2,70% vol
2. Arus E (Expansion Gas)
Laju alir volumetrik = 2017 Nm3
Komposisi gas : CO2 = 44,47 % vol
CO = 2,43 % vol
CH4 = 26,17 % vol
N2 = 1,40 % vol
3. Arus F (Off gas)
Laju alir volumetrik = 798 Nm3
Komposisi gas : CO2 = 44,47 % vol
CO = 2,43 % vol
H2 = 25,51 % vol
CH4 = 26,17 % vol
N2 = 1,40 % vol
4. Arus G (keluaran menara destilasi)
Laju alir massa = 67,9 ton
= 67900 kg
Komposisi gas (CO2,CO,H2,CH4 dan N2) = 0
5. Arus D (Make Up)
Laju alir volumetrik = 225470 Nm3
Data – data yang diketahui secara teori atau desain adalah sebagai berikut :
Make-up Gas
Laju alir : 9380 kmol/jam
Komposisi CO 21,70 % mol
Recycle Gas
Laju alir : 30953 kmol/jam
Masukkan Reaktor
1. Untuk peneracaan massa arus C (Recycle gas) maka laju alir dan komposisi
gas diubah dalam satuan massa.
Massa CO2 = % vol CO2 x laju alir volumetrik x BM
90034,478 kg + 20095,083 kg
% massa CO2 =
Analog perhitungan diatas sehingga diperoleh :
Laju alir massa arus C = 249306,618 kg
2. Untuk peneracaan massa arus E (expansion gas) maka laju alir dan komposisi
gas diubah dalam satuan massa.
Massa CO = 61,137002 kg
Analog dengan perhitungan diatas sehingga diperoleh :
Laju alir massa arus E = 2276,6075 kg
Komposisi gas : CO2 = 77,228 %
CO = 2,685 %
H2 = 2,013 %
CH4 = 16,526 %
3. Untuk peneracaan massa arus F (off gas) maka laju alir dan komposisi gas
diubah dalam satuan massa.
Analog dengan perhitungan diatas sehingga diperoleh:
Laju alir massa arus F = 901,8817 kg
Komposisi gas: CO2 = 77,242 % vol
CO = 2,686 % vol
H2 = 2,014 % vol
CH4 = 16,510 % vol
N2 = 1,548 % vol
a. Menghitung laju alir massa dan mol CO masukkan reaktor (arus A)
laju volumetrik = laju alir volumetrik arus C + laju alir volumetrik arus D
= 595782 Nm3 + 225470 Nm3
b. Menghitung laju alir massa dan komposisi gas CO keluaran Reaktor (Arus B)
Dari persamaan (4.1)
B = C + E + F + G
B = 249306,618 kg + 2276,6075 kg + 901,8817 kg + 67900 kg
= 320385,1072 kg
Dari persamaan (4.2)
B ZCO = C YCO + E XCO + F WCO + G VCO
Z
CO=
C YCO + E XCO + F WCO + G VCO
B
�249306,618 kg�8,060
100��+�2276,6075 kg �
Komposisi gas CO keluaran reaktor = 6,30 % massa
Laju alir massa CO keluaran R = (laju alir massa total)(KomposisiCO keluaranR)
= (320604,532 Kg)(0,063)
= 20167,077 Kg
Untuk menghitung konversi CO yang menjadi metanol, maka lajualir massa CO
keluaran reaktor diubah kedalam satuan mol.
Mol CO keluaran reaktor
=
(Laju alir Massa CO Outlet R)c. Menghitung konversi CO aktual yang menjadi metanol
d. Menghitung konversi CO desain yang menjadi metanol
konversi CO desain =
�
(Mol CO Inlet R−Mol CO Outlet R)Mol CO Inlet R
�
x 100 %konversi CO desain =
�
�7,86
100 x 40333 kmol�−� 3,3
100 x 35065�
�7,86100 x 40333 kmol�
�
x 100 %= 63,5 %
Hasil perhitungan konversi CO aktual dan desain untuk data yang lainnya dapat
dilihat pada table 4.1 berikut :
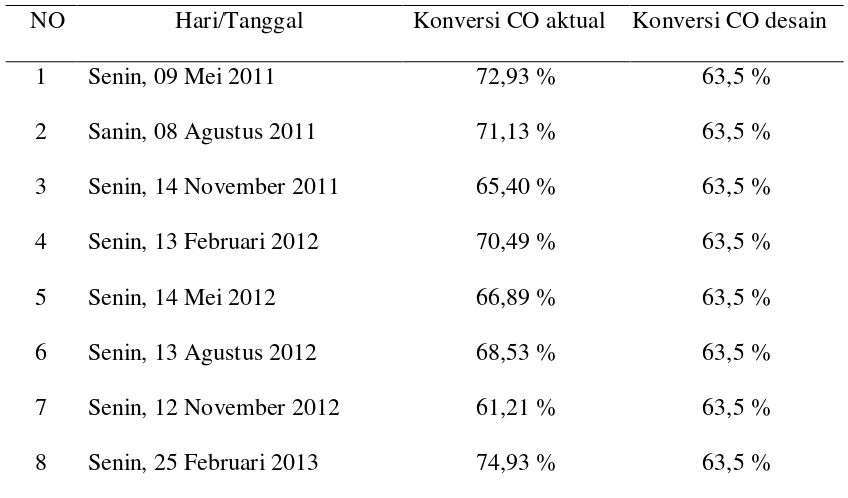
Table 4.1 Hasil perhitungan konversi CO aktual dan konversi CO desain.
NO Hari/Tanggal Konversi CO aktual Konversi CO desain
1 Senin, 09 Mei 2011 72,93 % 63,5 %
2 Sanin, 08 Agustus 2011 71,13 % 63,5 %
3 Senin, 14 November 2011 65,40 % 63,5 %
4 Senin, 13 Februari 2012 70,49 % 63,5 %
5 Senin, 14 Mei 2012 66,89 % 63,5 %
6 Senin, 13 Agustus 2012 68,53 % 63,5 %
7 Senin, 12 November 2012 61,21 % 63,5 %
8 Senin, 25 Februari 2013 74,93 % 63,5 %
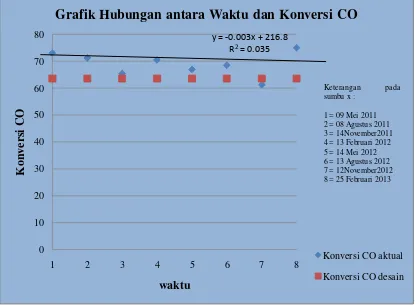
Jika table 4.1 diatas dibuat grafik maka akan diperoleh waktu vs konversi CO
sebagai berikut :
Gambar 4.1. Grafik hubungan antara waktu versus konversi CO
4.3. Pembahasan
Dari grafik 4.1. terlihat bahwa konversi CO berbanding lurus terhadap waktu
artinya semakin lama waktu penggunaan katalis maka konversi CO akan semakin
menurun, hal ini disebabkan katalis yang digunakan pada metanol reaktor samakin
lama semakin berkurang keaktifannya. Tapi untuk data konversi CO pada tanggal 27
Februari 2012 (data No. 4) lebih tinggi dari data pada konversi CO pada tanggal 28
November 2011 (data No. 3), hal ini disebabkan pada tanggal tersebut kondisi operasi Keterangan pada sumbu x :
1 = 09 Mei 2011 2 = 08 Agustus 2011 3 = 14November2011 4 = 13 Februari 2012 5 = 14 Mei 2012 6 = 13 Agustus 2012 7 = 12November2012 8 = 25 Februari 2013 y = -0.003x + 216.8
Grafik Hubungan antara Waktu dan Konversi CO
Konversi CO aktual
reaktor lebih baik sehingga CO yang bereaksi membentuk metanol lebih banyak.
Demikian halnya untuk konversi CO untuk pada tanggal 27 Agustus 2012 (data
No.6). Khusus data konversi CO pada tanggal 25 Februari 2013 (data No. 8) terjadi
peningkatan dari data konversi CO sebelumnya, hal ini disebabkan pemprosesan gas
sebelum masuk reaktor berjalan optimal mengingat pabrik baru selesai TA (Time
Around).
Jika hasil perhitungan konversi CO aktual dibandingkan dengan konversi CO
desain terlihat bahwa konversi CO aktual lebih besar dari pada konversi CO desain,
hal ini disebabkan oleh kondisi katalis yang masih aktif. Tapi untuk data tanggal 12
November 2012 (data No. 7) konversi CO aktual berada dibawah konversi CO
desain. Hal ini disebabkan oleh katalis yang digunakan pada metanol reaktor semakin
lama semakin berkurang keaktifannya, dikarenakan katalis sudah terlalu lama
digunakan. Dan data terakhir pada tanggal 25 Februari 2013 menunjukan bahwa
konversi CO aktual berada diatas konversi CO desain, hal ini dikarenakan gas
sebelum masuk reaktor berjalan optimal mengingat pabrik baru selasai melakukan
BAB 5
KESIMPULAN DAN SARAN
5.1 Kesimpulan
1. Efektifitas katalis dipengaruhi oleh suhu dan umur pemakaiannya, dimana suhu
yang terlalu tinggi akan merusak katalis dan semakin lama pemakaiaan maka
keaktifan katalis akan menurun.
2. Data terakhir menunjukan bahwa konversi CO aktual sebesar 74,93 % berada
diatas konversi CO desain sebesar 63,5 %, artinya kondisi katalis masih layak
digunakan.
5.2 Saran
1. Diharapkan adanya perhitungan konversi gas CO yang merupakan salah satu
komponen bahan baku pembuatan metanol.
DAFTAR PUSTAKA
Davis, M.E. 2003. Fundamentals of Chemical Reaction Engineering. McGraw-Hill. United State.
[KMI] Kaltim Metanol Industri. 1997. Final Dokumen 2 Proses Engineering Vol 4+. Lurgi OI Gas Chemie GmbH. Bontang.
[KMI] Kaltim Metanol Industri. 1997. Final Dokumen 3 Vessel engineering Volume 21. Lurgi OI Gas Chemie GmbH. Bontang.
[KMI] Kaltim Metanol Industri. 1997. Petunjuk Operasi Pabrik Methanol 2000 MTPD Unit 200-synthesis Methanol. Bontang.
Rase, H.F and Barrow, M.H. 1957. Project Engineering of Process Plant. John Wiley and Son, New York.
Rianto,N dan Akbar, A.Y. 2009. Super Genius Olimpiade Kimia SMA Nasional dan Internasional. Pustaka Widyatama. Yogyakarta.
Tim Dosen Kimia Dasar. 2009. Kimia Organik Dasar. UPT MKU Unhas. Makassar.
Twigg,M.V. 1970. Catalyst Handbook. Wolfe Publishing Ltd. London.
Twigg,M.V. 1989. Catalyst Handbook. 2nd Edition. Wolfe Publishing Ltd. London.
Westerterp,K.R. 1963. Chemical Reactor Design and Operation. Jhon Wiley & Sons. New York.
Westerterp,K.R. 1987. Chemical Reactor Design and Operation. Jhon Wiley & Sons. New York.
Winarso,L.dkk. 1998. Operation hand out. PT.Kaltim Methanol industry. Bontang.