1 42
KAJIAN MUTU FISIKOKIMIA DAN SENSORI ES LILIN
DARI CAMPURAN SARI BUAH NENAS DAN WORTEL
DENGAN PENAMBAHAN GELATIN
SKRIPSI
Oleh:
DESI FATWANI SYAHMARA
110305034/ILMU DAN TEKNOLOGI PANGAN
PROGRAM STUDI ILMU DAN TEKNOLOGI PANGAN
FAKULTAS PERTANIAN
UNIVERSITAS SUMATERA UTARA
MEDAN
2 42
KAJIAN MUTU FISIKOKIMIA DAN SENSORI ES LILIN
DARI CAMPURAN SARI BUAH NENAS DAN WORTEL
DENGAN PENAMBAHAN GELATIN
SKRIPSI
Oleh:
DESI FATWANI SYAHMARA
110305034/ILMU DAN TEKNOLOGI PANGAN
Skripsi sebagai salah satu syarat untuk memperoleh gelar sarjana di Fakultas Pertanian
Universitas Sumatera Utara
PROGRAM STUDI ILMU DAN TEKNOLOGI PANGAN
FAKULTAS PERTANIAN
UNIVERSITAS SUMATERA UTARA
MEDAN
3 42
Judul Skripsi : Kajian Mutu Fisikokimia dan Sensori Es Lilin Dari Campuran Sari Buah Nenas dan Wortel Dengan Penambahan Gelatin
Nama : Desi Fatwani Syahmara
NIM : 110305034
Program Studi : Ilmu dan Teknologi Pangan
Disetujui oleh: Komisi Pembimbing
Dr. Ir. Elisa Julianti, MSi Ir. Rona J. Nainggolan, SU
Ketua Anggota
Mengetahui :
Dr. Ir. Herla Rusmarilin, MP Ketua Program Studi
4 42
ABSTRAK
DESI FATWANI SYAHMARA. Kajian Mutu Fisikokimia dan Sensori Es Lilin Dari Campuran Sari Buah Nenas dan Wortel dengan Penambahan Gelatin, dibimbing oleh Elisa Julianti dan Rona J Nainggolan.
Es lilin merupakan salah satu produk water ice yang banyak disukai dari setiap kalangan baik dari anak-anak maupun orang dewasa karena mempunyai rasa yang manis dan warna yang beranekaragam. Produsen es lilin biasanya menggunakan pemanis maupun pewarna sintetis yang berbahaya bagi kesehatan terutama bagi anak-anak. Penelitian ini bertujuan untuk mengetahui kombinasi perlakuan terbaik antara perbandingan sari buah nenas dengan wortel, serta konsentrasi gelatin untuk menghasilkan produk es lilin dengan karakteristik fisikokimia dan sensoris terbaik serta dapat diterima oleh konsumen. Campuran sari buah nenas dan wortel yang digunakan dalam pembuatan es lilin terdiri dari 5 taraf perbandingan yaitu 0:100; 25:75; 50:50; 75:25 dan 100:0. Gelatin ditambahkan sebagai penstabil dengan 3 taraf konsentrasi yaitu 0%, 0,2%, dan 0,4%.
Hasil penelitian menunjukkan bahwa interaksi perbandingan sari buah nenas dan wortel dengan konsentrasi gelatin hanya memberikan pengaruh yang berbeda sangat nyata (P<0,01) terhadap pH, total asam tertitrasi dan kadar vitamin C. Peningkatan jumlah sari buah nenas yang ditambahkan pada perbandingan sari buah nenas dan wortel semakin meningkatkan kecepatan mencair produk, kadar abu, nilai total asam tertitrasi, kadar vitamin C, total padatan terlarut serta meningkatkan kualitas sensori produk es lilin yang dihasilkan. Komposisi produk es lilin dengan mutu terbaik yang dipilih berdasarkan karakteristik sensori melalui uji hedonik sesuai dengan nilai %AI (Acceptable Index) yang diperoleh adalah perlakuan campuran sari buah nenas dan wortel dengan perbandingan 50:50 dan konsentrasi gelatin 0,2%. Hasil pengamatan pada produk es lilin dengan mutu terbaik yaitu yang terbuat dari campuran 50% sari nenas dan 50% sari wortel serta 0,2% gelatin menunjukkan aktivitas antioksidan dengan nilai IC50 sebesar 14,55
bpj, sedangkan es lilin kontrol yang dibuat dari 100% sari buah nenas dan 100% sari wortel masing-masing memiliki nilai aktivitas antioksidan dengan nilai IC50
sebesar 11,62 bpj dan 14,86 bpj. Nilai total mikroba produk es lilin dengan mutu terbaik dan kontrol berturut-turut adalah 2,5396 CFU/ml, 2,5833 CFU/ml, serta 2,6313 CFU/ml. Nilai total mikroba yang diperoleh masih berada di bawah standar batas maksimum yang diizinkan yakni sebesar 1 x 104 CFU/ml. Nilai β – Karoten
produk es lilin dengan mutu terbaik dan kontrol berturut-turut adalah 618,68 mg/100g, 200,88 mg/100g, dan 872,68 mg/100g.
Kata kunci : es lilin, gelatin, nenas, wortel
5 42
ABSTRACT
DESI FATWANI SYAHMARA. The Physcochemical and Sensory Quality of Lollies Ice From The Mixture of Pineapple and Carrot Juices with the addition of Gelatine, supervised by Elisa Julianti and Rona J. Nainggolan.
Lollies ice was a water ice product that was popular in all ages because its sweet taste and colourful appearance. The production of lollies ice usually used additives like colouring and sweetener that might affect to health ecspecially to the children. The aim of this research was to find the best ratio of Pineapple and Carrot juices with the addition of gelatine in producing lollies ice with the best characteristics of physcochemical and sensory quality. The ratio of Pineapple and Carrot juices used were0:100;25:75; 50:50; 75:25 and 100:0. Gelatine was added as a stabilizer with three concentration i.e 0, 0,2 dan 0,4%.
The results showed that the interaction between pineapple and carrot juices with gelatine concentration had highly significant effect(P<0,01) on pH, titrable total acid content, and vitamin C.The increasing amount of pineapple juices increased the melting rate and total ash content, titrable total acid, vitamin C, total soluble solid and sensory characteristics. The best lollies ice (based on sensory characteristics with %AI (Acceptable Index) hedonic test) was the treatment with the ratio of pineapple and carrot juices of 50:50 and 0,2% gelatine which showed the amount of antioxidant activity with IC50 value of 14,55 ppm, whereas the control of lollies ice from 100% pineapple juice and 100% carrot juice had IC50 values of 11,62 ppm and 14,86 ppm respectively. The best quality of lollies ice and control had 2,5396 CFU/ml, 2,5833 CFU/ml, and 2,6313 CFU/ml of total microbes respectively which showed a lower amount than the maximum permissible total microbes standard (1 x 104 CFU/ml). The best quality of lollies ice and control had 618,31 mg/100g, 200,88 mg/100g, and 872,68 mg/100g of β – carotene valuerespectively.
Keywords: carrot, gelatine, lollies ice, pineapple
6 42
RIWAYAT HIDUP
DESI FATWANI SYAHMARA dilahirkan di Pematang Raya pada tanggal 10 Desember 1992, dari Bapak Ahmad Syahruddin, SpdI dan Ibu Marhamah Kamal BA. Penulis merupakan anak ketiga dari lima bersaudara. Penulis menempuh pendidikan di SD Swasta Kartika 1-14 Medan, SMP Negeri 30 Medan, penulis lulus dari SMA Swasta Sultan Iskandar Medan pada tahun 2010 dan pada tahun 2011 penulis berhasil masuk ke Fakultas Pertanian Universitas Sumatera Utara melalui Jalur Seleksi Nasional Masuk Perguruan Tinggi Negeri (SNMPTN) di Program Studi Ilmu dan Teknologi Pangan. Selama mengikuti perkuliahan, penulis aktif sebagai anggota Ikatan Mahasiswa Ilmu dan Teknologi Pangan (IMITP) USU, anggota Badan Kenaziran Musholla Al-Mukhlisin FP-USU, dan sebagai asisten Laboratorium Analisa Kimia Bahan Pangan pada tahun 2013-2015. Penulis telah melaksanakan Praktik Kerja Lapangan (PKL) di PTPN IV (Persero) Unit Kebun Teh Bah Butong di Kecamatan Sidamanik, Medan, Sumatera Utara dari tanggal 15 Juli sampai 15 Agustus 2014. Penulis menyelesaikan tugas akhirnya untuk memperoleh gelar Sarjana Teknologi Pertanian pada Program Studi Ilmu dan Teknologi Pangan, dengan melakukan penelitian yang berjudul “Kajian Mutu Fisikokimia dan Sensori Es Lilin Dari Campuran Sari Buah Nenas dan Wortel dengan Penambahan Gelatin. Penelitian ini dilakukan mulai bulan Mei 2015 sampai dengan Juli 2015 di Laboratorium Analisa Kimia Bahan Pangan, Fakultas Pertanian USU. Pada tahun 2015 penulis memperoleh Hibah Penelitian yang disponsori oleh Tanoto Foundation.
7 42
KATA PENGANTAR
Puji dan syukur penulis ucapkan kehadirat Tuhan Yang Maha Kuasa atas segala rahmat dan karuniaNya sehingga penulis dapat menyelesaikan usulan penelitian yang berjudul “Kajian Mutu Fisikokimia Dan Sensori Es Lilin Dari Campuran Sari Buah Nenas Dan Wortel Dengan Penambahan Gelatin”. Selain itu, banyak pihak yang juga telah membantu penulis selama penyelesaiannya. Pada kesempatan ini penulis menyampaikan ucapan terima kasih yang mendalam kepada :
1. Tanoto Foundation Terima kasih atas dana penelitian yang diberikan. 2. Ibu Dr. Ir. Elisa Julianti, M.Si dan Ibu Ir. Rona J. Nainggolan, SU selaku
Ketua Komisi Pembimbing dan Anggota Komisi Pembimbing Skripsi. Terima kasih atas bimbingan, motivasi, masukan dan saran yang sangat berarti yang selama ini telah ibu berikan.
3. Keluarga tercinta : Kedua Orang Tua, Kak Aghni, Bang Qawy, Mia, Zakiy, Mhd Reza Pramudya, STP. Terimakasih atas cinta, semangat, kasih sayang dan kekuatan doa yang sudah diberikan.
4. Staf Asisten Laboratorium Analisa Kimia Bahan Pangan, teman-teman seperjuangan ITP 2011, adik-adik 2012 hingga 2014. Terima kasih atas kebersamaannya dan semua pihak yang telah membantu dan tidak bisa disebutkan satu persatu.
Semoga skripsi ini dapat bermanfaat bagi pihak yang membutuhkan.
Medan, Agustus 2015
Penulis
8
Kandungan gizi dan manfaat wortel ... 10
Gelatin ... High Fructose Syrup (HFS) ... Proses Pembuatan Es Lilin ... Pengemasan ... Waktu dan Tempat Penelitian ... 19
9
42
Pelaksanaan Penelitian ... 21
Pengamatan dan Metode Pengukuran Data ... 22
Karakteristik fisik ... Penentuan warna (metode hunter) ... 23 23 Penentuan kecepatan mencair ... 23
Karakteristik kimia ... Penentuan pH ... 24 24 Penentuan padatan terlarut ... 24
Penentuan total asam ... 24
Penentuan kadar vitamin C ... 25
Penentuan kadar abu total ... 26
Penentuan kadar abu larut air ... Penentuan kadar abu tidak larut asam ... Uji Organoleptik warna, aroma, rasa dan konsistensi ... 26 27 27 Pengujian perlakuan terbaik ... Penentuan aktivitas antioksidan ... 28 28 Penentuan total mikroba ... 30
Penentuan β – karoten... 30
Skema Penelitian ... 32
HASIL DAN PEMBAHASAN Karakteristik Fisik Es Lilin Dari Campuran Sari Buah Nenas dan Wortel dengan Penambahan Gelatin ... 33
Warna (oHue) ... 33
Kecepatan mencair ... 34
Karakteristik Kimia Es Lilin Dari Campuran Sari Buah Nenas dan Wortel dengan Penambahan Gelatin ... 36
pH ... 37
Total padatan terlarut ... 38
Total asam... 40
Kadar vitamin C... 41
Kadar abu total ... 42
Karakteristik Sensori Es Lilin Dari Campuran Sari Buah Nenas dan Wortel dengan Penambahan Gelatin ... 44
Acceptable Index Warna, aroma, rasa, dan konsistensi ... 45
Kajian Mutu Terbaik dan Kontrol Es Lilin dari Campuran Sari Buah Nenas dan Wortel dengan Penambahan Gelatin ... 49
Aktivitas antioksidan ... 49
10 42
DAFTAR TABEL
No. Hal
1. Kandungan gizi buah nenas (per 100g) ... 9 2. Kandungan gizi wortel (per 100g) ... 11 3. Kemanisan relatif berbagai jenis gula ... 14 4.
5.
Syarat mutu es krim berdasarkan SNI ... Skala hedonik warna, aroma, rasa, dan konsistensi ...
17 28 6. Pengaruh perbandingan sari buah nenas dan wortel pada es lilin
terhadap karakteristik fisik yang diamati ... 33 7. Pengaruh konsentrasi gelatin yang ditambahkan pada es lilin
terhadap karakteristik fisik yang diamati ... 33 8. Pengaruh perbandingan sari buah nenas dan wortel pada es lilin
terhadap karakteristik kimia yang diamati ... 37 9. Pengaruh konsentrasi gelatin yang ditambahkan pada es lilin
terhadap karakteristik kimia yang diamati ... 37 10. Pengaruh perbandingan sari buah nenas dan wortel pada es lilin
terhadap karakteristik sensori yang diamati ... 46 11. Pengaruh konsentrasi gelatin yang ditambahkan pada es lilin
terhadap karakteristik sensori yang diamati ... 46
11 42
DAFTAR GAMBAR
No. Hal
1. Senyawa 2,5 dimetil-4-hidroksi-3(2H)-furanon ... 8 2. Struktur kimia gelatin ... 12 3. Skema pembuatan es lilin ... 32 4. Hubungan perbandingan sari buah nenas dan wortel dengan nilai
warna (oHue) es lilin ... 34 5. Hubungan perbandingan sari buah nenas dan wortel dengan
kecepatan mencair es lilin ... 35 6. Pengaruh interaksi antara perbandingan sari buah nenas dan wortel
dengan penambahan gelatin terhadap pH es lilin ... 38 7. Hubungan perbandingan sari buah nenas dan wortel dengan total
padatan terlarut es lilin ... 39 8. Pengaruh interaksi antara perbandingan sari buah nenas dan wortel
dengan penambahan gelatin terhadap total asam es lilin ... 40 9. Pengaruh interaksi antara perbandingan sari buah nenas dan wortel
dengan penambahan gelatin terhadap kadar vitamin C ... 42 10. Hubungan perbandingan sari buah nenas dan wortel dengan kadar
abu total es lilin ... 43 11. Hubungan perbandingan sari buah nenas dan wortel dengan
Acceptable Index warna, aroma, rasa dan konsistensi es lilin ... 45 12. Pengaruh konsentrasi gelatin terhadap nilai Acceptable Index
warna, aroma, rasa dan konsistensi es lilin ... 48
12
42
DAFTAR LAMPIRAN
No. Hal 1. Kurva standar asam askorbat pada pengujian kadar vitamin C dengan metode kolorimetri ... 612. Format uji organoleptik ... 62
3. Kurva pengujian aktivitas antioksidan dengan metode DPPH ... 63
4. Kurva standar betakaroten ... 64
5. Daftar sidik ragam warna (nilai oHue) es lilin dan uji LSR pengaruh perbandingan sari buah nenas dan sari wortel terhadap Warna (nilai oHue) Es lilin ... 65
6. Daftar sidik ragam kecepatan mencair es lilin dan uji LSR pengaruh perbandingan sari buah nenas dan sari wortel dengan konsentrasi gelatin terhadap kecepatan mencair es lilin ... 66
7. Daftar sidik ragam pH es lilin dan uji LSR pengaruh interaksi perbandingan sari buah nenas dan sari wortel dengan konsentrasi gelatin terhadap pH es lilin ... 67
8. Daftar sidik ragam total padatan terlarut es lilin dan uji Uji LSR pengaruh perbandingan sari buah nenas dan sari wortel terhadap total padatan terlarut ... 68
9. Daftar sidik ragam total asam es lilin dan Uji LSR pengaruh interaksi perbandingan sari buah nenas dan wortel dan konsentrasi gelatin terhadap total asam es lilin ... 69
10. Daftar sidik ragam kadar vitamin C es lilin dan uji LSR pengaruh interaksi pengaruh perbandingan sari buah nenas dan wortel dan konsentrasi gelatin terhadap kadar vitamin C es lilin ... 70
11. Daftar sidik ragam kadar abu total es lilin dan uji LSR pengaruh perbandingan sari buah nenas dan sari wortel dan konsentrasi gelatin terhadap kadar abu total es lilin ... 71
12. Daftar sidik ragam Acceptable Index warna es lilin dan uji LSR pengaruh perbandingan sari buah nenas dan sari wortel terhadap Acceptable Index warna es lilin ... 72
13 pengaruh perbandingan sari buah nenas dan sari wortel terhadap Acceptable Index aroma es lilin... Daftar sidik ragam Acceptable Index rasa es lilin dan uji LSR pengaruh perbandingan sari buah nenas dan sari wortel terhadap Accetable Index rasa es lilin ... Daftar sidik ragam Acceptable Index konsistensi es lilin dan uji LSR pengaruh perbandingan sari buah nenas dan sari wortel terhadap Acceptable Index konsistensi es lilin ... Data pengamatan aktivitas antioksidan es lilin dengan mutu terbaik dan kontrol ... wortel dengan penambahan gelatin perlakuan terbaik ...
4 42
ABSTRAK
DESI FATWANI SYAHMARA. Kajian Mutu Fisikokimia dan Sensori Es Lilin Dari Campuran Sari Buah Nenas dan Wortel dengan Penambahan Gelatin, dibimbing oleh Elisa Julianti dan Rona J Nainggolan.
Es lilin merupakan salah satu produk water ice yang banyak disukai dari setiap kalangan baik dari anak-anak maupun orang dewasa karena mempunyai rasa yang manis dan warna yang beranekaragam. Produsen es lilin biasanya menggunakan pemanis maupun pewarna sintetis yang berbahaya bagi kesehatan terutama bagi anak-anak. Penelitian ini bertujuan untuk mengetahui kombinasi perlakuan terbaik antara perbandingan sari buah nenas dengan wortel, serta konsentrasi gelatin untuk menghasilkan produk es lilin dengan karakteristik fisikokimia dan sensoris terbaik serta dapat diterima oleh konsumen. Campuran sari buah nenas dan wortel yang digunakan dalam pembuatan es lilin terdiri dari 5 taraf perbandingan yaitu 0:100; 25:75; 50:50; 75:25 dan 100:0. Gelatin ditambahkan sebagai penstabil dengan 3 taraf konsentrasi yaitu 0%, 0,2%, dan 0,4%.
Hasil penelitian menunjukkan bahwa interaksi perbandingan sari buah nenas dan wortel dengan konsentrasi gelatin hanya memberikan pengaruh yang berbeda sangat nyata (P<0,01) terhadap pH, total asam tertitrasi dan kadar vitamin C. Peningkatan jumlah sari buah nenas yang ditambahkan pada perbandingan sari buah nenas dan wortel semakin meningkatkan kecepatan mencair produk, kadar abu, nilai total asam tertitrasi, kadar vitamin C, total padatan terlarut serta meningkatkan kualitas sensori produk es lilin yang dihasilkan. Komposisi produk es lilin dengan mutu terbaik yang dipilih berdasarkan karakteristik sensori melalui uji hedonik sesuai dengan nilai %AI (Acceptable Index) yang diperoleh adalah perlakuan campuran sari buah nenas dan wortel dengan perbandingan 50:50 dan konsentrasi gelatin 0,2%. Hasil pengamatan pada produk es lilin dengan mutu terbaik yaitu yang terbuat dari campuran 50% sari nenas dan 50% sari wortel serta 0,2% gelatin menunjukkan aktivitas antioksidan dengan nilai IC50 sebesar 14,55
bpj, sedangkan es lilin kontrol yang dibuat dari 100% sari buah nenas dan 100% sari wortel masing-masing memiliki nilai aktivitas antioksidan dengan nilai IC50
sebesar 11,62 bpj dan 14,86 bpj. Nilai total mikroba produk es lilin dengan mutu terbaik dan kontrol berturut-turut adalah 2,5396 CFU/ml, 2,5833 CFU/ml, serta 2,6313 CFU/ml. Nilai total mikroba yang diperoleh masih berada di bawah standar batas maksimum yang diizinkan yakni sebesar 1 x 104 CFU/ml. Nilai β – Karoten
produk es lilin dengan mutu terbaik dan kontrol berturut-turut adalah 618,68 mg/100g, 200,88 mg/100g, dan 872,68 mg/100g.
Kata kunci : es lilin, gelatin, nenas, wortel
5 42
ABSTRACT
DESI FATWANI SYAHMARA. The Physcochemical and Sensory Quality of Lollies Ice From The Mixture of Pineapple and Carrot Juices with the addition of Gelatine, supervised by Elisa Julianti and Rona J. Nainggolan.
Lollies ice was a water ice product that was popular in all ages because its sweet taste and colourful appearance. The production of lollies ice usually used additives like colouring and sweetener that might affect to health ecspecially to the children. The aim of this research was to find the best ratio of Pineapple and Carrot juices with the addition of gelatine in producing lollies ice with the best characteristics of physcochemical and sensory quality. The ratio of Pineapple and Carrot juices used were0:100;25:75; 50:50; 75:25 and 100:0. Gelatine was added as a stabilizer with three concentration i.e 0, 0,2 dan 0,4%.
The results showed that the interaction between pineapple and carrot juices with gelatine concentration had highly significant effect(P<0,01) on pH, titrable total acid content, and vitamin C.The increasing amount of pineapple juices increased the melting rate and total ash content, titrable total acid, vitamin C, total soluble solid and sensory characteristics. The best lollies ice (based on sensory characteristics with %AI (Acceptable Index) hedonic test) was the treatment with the ratio of pineapple and carrot juices of 50:50 and 0,2% gelatine which showed the amount of antioxidant activity with IC50 value of 14,55 ppm, whereas the control of lollies ice from 100% pineapple juice and 100% carrot juice had IC50 values of 11,62 ppm and 14,86 ppm respectively. The best quality of lollies ice and control had 2,5396 CFU/ml, 2,5833 CFU/ml, and 2,6313 CFU/ml of total microbes respectively which showed a lower amount than the maximum permissible total microbes standard (1 x 104 CFU/ml). The best quality of lollies ice and control had 618,31 mg/100g, 200,88 mg/100g, and 872,68 mg/100g of β – carotene valuerespectively.
Keywords: carrot, gelatine, lollies ice, pineapple
14 42
PENDAHULUAN
Latar Belakang
Es lilin merupakan suatu produk minuman atau jajanan tradisional yang masih digemari dari setiap kalangan baik orang dewasa maupun anak-anak, karena es lilin mempunyai rasa yang manis dan dingin sehingga dapat memberikan kesegaran. Es lilin termasuk salah satu produk water ice, merupakan produk minuman tanpa lemak yang dibekukan hingga menjadi fase padatnya. Warna yang beranekaragam merupakan daya tarik lain dari es lilin. Rasa manis es lilin umumnya berasal dari gula sintetis sedangkan warna yang menarik berasal dari pewarna sintetis yang sering ditambahkan dalam pembuatan es lilin.
Pemanis sintetis yang banyak digunakan dalam pembuatan es lilin adalah siklamat. Menurut Purwaningsih, dkk., (2010) gula siklamat salah satu gula sintetis yang sering digunakan dalam pembuatan es lilin karena mempunyai harga yang relatif murah dan tingkat kemanisannya lebih tinggi, tetapi ini dapat menimbulkan efek yang negatif bagi kesehatan. Produsen biasanya kurang memperhatikan kandungan gizi serta dampak yang ditimbulkan dari penggunaan bahan pemanis sintetis yang penggunaannya diberi secara berlebihan dapat memicu pertumbuhan kanker pada tubuh. Oleh karena itu perlu dicari pemanis alternatif dalam pembuatan es lilin, misalnya High Fructose Syrup (HFS).
Penggunaan flavor dan pewarna sintetis, bagi produsen tertentu bertujuan untuk menghemat biaya produksi. Tetapi, seiring dengan meningkatnya kesadaran masyarakat akan pentingnya pangan yang sehat dan bergizi maka penggunaan
15 42
bahan-bahan sintetis ini harus dikurangi dengan cara penggunaan bahan-bahan alami seperti buah-buahan.
Nenas merupakan salah satu buah-buahan komersial yang banyak dibudidayakan di Indonesia. Perkembangan produksi nenas di Indonesia selama tahun 2000-2011 mengalami peningkatan dengan rata-rata pertumbuhan 16,08% per tahun. Pada tahun 2000 produksi nenas yang ada di Indonesia hanya sebesar 399,299 ton, kemudian pada tahun 2011 meningkat sebesar 9,54% menjadi 1.540,626 ton (Pusdatin, 2013). Di provinsi Sumatera Utara produktivitas buah nenas menduduki peringkat ke-4 tertinggi, yaitu sebesar 183.213 ton pada tahun 2011 (Badan Pusat Statistik Republik Indonesia, 2012).
Buah nenas yang sudah matang mempunyai rasa yang manis, dan ada juga yang manis asam. Nenas yang sudah matang dapat diolah menjadi produk minuman (jus) ataupun kalengan (canning) (Sunarjono, 1997). Rasa yang ada pada buah nenas merupakan perpaduan antara gula dan asam. Kandungan gula dalam nenas yaitu glukosa 2,32%, fruktosa 1,42% dan sukrosa 7,89%. Asam-asam yang terkandung dalam buah nenas adalah Asam-asam sitrat, Asam-asam malat, dan asam oksalat (Irfandi, 2005). Kandungan air yang tinggi pada buah nenas dapat digunakan untuk menggantikan air yang digunakan dalam pembuatan es lilin. Tetapi warna yang dihasilkan dari nenas kurang menarik sehingga perlu dicampur dengan bahan yang mempunyai pewarna alami seperti wortel.
16 42
Fungsi dari antioksidan yaitu untuk menangkap radikal bebas dan dapat mencegah proses oksidasi dalam suatu sistem yang mempunyai tekanan oksigen rendah. Senyawa β-karoten mempunyai aktivitas vitamin A yang tinggi. Di dalam tubuh β-karoten berubah menjadi vitamin A yang akan berhenti jika vitamin A dalam tubuh sudah tercukupi, dan selanjutnya secara utuh β-karoten akan diabsorbsi oleh tubuh (Silalahi, 2006).
Kombinasi antara sari buah nenas dan sari wortel dalam pembuatan es lilin diharapkan akan menghasilkan es lilin dengan flavor dan warna yang disukai oleh konsumen. Sari buah nenas memiliki flavor yang kuat sedangkan sari wortel memberikan warna yang menarik pada es lilin. Oleh karena itu perlu dicari perbandingan sari buah nenas dan sari wortel yang akan menghasilkan es lilin yang disukai oleh konsumen.
Penggunaan penstabil dapat membantu menghasilkan tekstur yang lebih lembut untuk produk-produk sirup selain itu penstabil memiliki kemampuan membengkak dan mengembang di dalam air, dapat membentuk film, dapat melindungi sistem koloid, dan dapat mempengaruhi viskositas suatu bahan (Parker, 1982). Jenis-jenis penstabil yang umum digunakan dalam pembuatan es lilin adalah gelatin, agar-agar, gum, pektin, karaginan, alginat, lesitin, furcelaran, dan Carboxy Methyl Cellulose (CMC).
17 42
pengemulsi dan thickening agent. Pada produk beku penambahan gelatin berfungsi untuk memperbaiki dan meningkatkan kualitas tekstur, dengan cara meningkatkan viskositas, mengikat air dan menstabilkan gelembung udara pada produk bekuan sehingga tidak mudah terlepas memperlambat dalam pembentukan kristal es, memberikan efek meleleh di mulut (mouthfeel), dan juga dapat memperlama daya pelelehan pada produk es lilin yang dibekukan (Mariod dan Adam, 2013).
Perumusan Masalah
Es lilin merupakan produk yang digemari dari setiap kalangan baik dewasa maupun anak-anak. Pada umumnya bahan dasar es lilin adalah flavor, pewarna dan gula sintetis. Beberapa produsen menambahkan bahan-bahan yang dilarang penggunaannya untuk bahan pangan seperti pewarna tekstil dan penambahan pemanis sintetis yang berlebihan untuk menambah rasa manis dari es lilin yang dapat menimbulkan dampak negatif bagi kesehatan konsumennya. Oleh karena itu didalam pembuatan es lilin digunakan campuran buah dan sayuran yaitu nenas dan wortel yang dapat menghasilkan es lilin dengan flavor dan warna yang menarik dan juga kandungan gizi yang tinggi sehingga aman dikonsumsi terutama bagi anak-anak.
Tujuan Penelitian
18 42
tepat dalam pembuatan es lilin serta untuk mempelajari karakteristik fisikokimia dan sensori es lilin dari campuran sari buah nenas dan wortel
Kegunaan Penelitian
Sebagai sumber data dalam penyusunan skripsi di Program Studi Ilmu dan Teknologi Pangan, Fakultas Pertanian, Universitas Sumatera Utara,
Medan, serta menjadi informasi ilmiah dan rekomendasi bagi produsen es lilin dalam menentukan bahan baku pembuatan es lilin untuk meningkatkan nilai gizi, meningkatkan pendapatan petani nenas dan wortel, serta sebagai bahan rujukan bagi penelitian selanjutnya.
Hipotesa Penelitian
Perbedaan perbandingan sari buah nenas, dan sari wortel dalam formulasi dan konsentrasi gelatin sebagai interaksi antara perbandingan sari buah nenas dan sari wortel dengan konsentrasi gelatin memberikan pengaruh terhadap karakteristik fisikokimia dan sensori terhadap es lilin.
19 42
TINJAUAN PUSTAKA
Es Lilin
Es lilin merupakan produk yang dibuat melalui proses pembekuan, dan sudah mempunyai pasar sejak dahulu namun keberadaannya mulai tersaingi dengan produk-produk olahan beku lainnya. Es lilin disajikan dalam keadaan dingin, kemasan yang sederhana dan harga yang relatif murah (Hartono, 2013). Rasa dari es lilin dapat dihasilkan dari berbagai jenis buah bahkan dengan semakin banyaknya permintaan akan varian rasa dari es lilin tersebut maka produsen mencoba mengkombinasikan produk-produk olahan beku tersebut. Produsen es lilin sering sekali menggunakan bahan pemanis dan pewarna sintetis yang dapat menimbulkan bahaya bagi yang mengkonsumsinya (Hary, 2012).
Produsen es lilin sering menggunakan pewarna sintetis karena pewarna sintetis mudah didapatkan di pasar dan di toko, warna yang dihasilkan lebih mencolok dan harganya yang murah. Upaya yang dapat dilakukan untuk menghindari penggunaan pewarna sintetis adalah dengan menggunakan pewarna alami. Beberapa pewarna alami yang dapat dimanfaatkan penggunaannya dalam makanan yaitu pewarna yang berasal dari klorofil, antosianin, flavonoid, quinon, xanthon, dan karotenoid. Wortel merupakan sumber karotenoid yang berpotensi sebagai pewarna alami (Hartono, dkk., 2013).
Nenas
Nenas (Ananas comosus L. Merr) merupakan tanaman herbal yang dapat tumbuh dalam berbagai musim (perennial). Buah nenas digolongkan ke dalam kelas monokotil yang mempunyai sifat tahunan, dimana tanaman nenas
20 42
mempunyai rangkaian bunga dan buah yang terdapat di ujung batang. Tumbuhnya meluas dengan menggunakan tunas samping yang dapat berkembang menjadi cabang-cabang vegetatif. Pada cabang tersebut akan dihasilkan buah nenas (Lisdiana,1997).
Nenas merupakan buah yang cukup diminati oleh kebanyakan masyarakat, ini terbukti dengan banyaknya proses pengolahan yang dilakukan terhadap buah nenas, seperti pengeringan, fermentasi, perebusan, penggilingan, pengeringan, maupun olahan lainnya. Pengolahan ini dilakukan adalah untuk memperpanjang masa simpan nenas dan juga sebagai alternatif untuk mengantisipasi hasil produksi yang melimpah terhadap buah nenas (Fitriani dan Sribudiani, 2009).
Tingkat kematangan buah nenas yang baik untuk dikonsumsi adalah apabila warna kuning pada buahnya mencapai 25% dari total permukaan buah. Pada tingkat ini buah nenas mempunyai keasaman rendah dan total padatan terlarut yang tinggi. Kematangan buah nenas juga dapat dilihat dari warna pada kulit dan mata buah yaitu tidak kurang dari 20% tetapi juga tidak lebih dari 40% mata yang mempunyai bercak kuning (Muchtadi, 1992).
Dari seluruh bagian buah nenas segar, hanya 53% dari buah nenas yang dapat dikonsumsi. Buah nenas mengandung asam sebesar 0,72%, dimana asam tersebut terdiri dari asam sitrat sebesar 83% dan asam malat sebesar 13%. Rasa yang dihasilkan dari buah nenas disebabkan oleh berbagai komponen volatil dan non volatil, dan sebagian besar aroma yang dihasilkan dari nenas disebabkan oleh senyawa 2,5 dimetil-4-hidroksi-3(2H)-furanon (Winarno, 1993).
21 42
Gambar 1. Senyawa 2,5 dimetil-4-hidroksi-3(2H)-furanon (Buttery et al., 2001) Pigmen karotenoid merupakan pigmen dominan yang terdapat dalam buah nenas, dimana pigmen inilah yang satu-satunya menyebabkan warna kuning pada buah nenas. Buah nenas merupakan salah satu buah yang merupakan sumber utama karotenoid bagi manusia. Bentuk karatenoid yang biasa dikonsumsi adalah α-karoten, β-karoten, lutein, likopen dan zeasantin, dan α-karoten, β-karoten inilah yang akan menjadi sumber provitamin A yang didalam tubuh akan dikonversi menjadi retinol (vitamin A). Kelompok Karotenoid dibagi menjadi dua kelompok utama, yaitu karoten (α-karoten, β-karoten, dan likopen) dan santofil (β-kriptosantin, lutein, dan zeasantin) (Muchtadi, 1992).
Manfaat nenas
22 42
penderita sembelit (konstipasi) karena adanya kandungan serat pada buah nenas (Dalimartha, 2000).
Kandungan gizi buah nenas
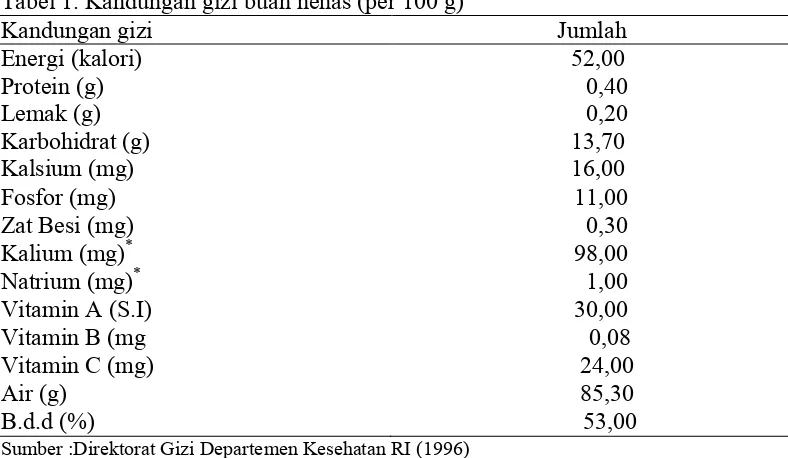
Buah nenas merupakan salah satu buah non klimaterik yang mengandung vitamin C dan vitamin A (retinol) yang masing-masing sebesar 24 mg dan 39 mg dalam setiap 100 g bahan. Kedua vitamin tersebut mempunyai aktivitas sebagai antioksidan yang dapat menghentikan reaksi berantai pada pembentukan radikal bebas di dalam tubuh manusia yang diyakini sebagai pemicu berbagai jenis penyakit (Sibuea, 2008). Adapun kandungan gizi buah nenas dapat dilihat pada Tabel 1.
Tabel 1. Kandungan gizi buah nenas (per 100 g)
Kandungan gizi Jumlah
Sumber :Direktorat Gizi Departemen Kesehatan RI (1996) *) Irfandi, 2005
Wortel
23 42
dikonsumsi (Sunarjono,1984). Wortel termasuk kedalam famili Umbilliferae, yaitu tanaman yang bunganya mempunyai susunan bentuk yang mirip dengan payung, tanaman ini pertama kali ditemukan di Eropa bagian selatan, Afrika utara dan di perbatasan Asia. Tanaman wortel juga telah lama dibudidayakan disekitar jalur Mediterania (Rukmana, 1995).
Tanaman wortel tumbuh baik pada daerah yang mempunyai suhu berkisar antara 16-21oC. Adapun Suhu yang paling baik untuk proses perkecambahan biji
adalah antara 8-18oC (Purseglove, dkk., 1981). Menurut Hukum, dkk (1990) Tanaman wortel dapat tumbuh dengan optimal pada tanah yang mempunyai struktur remah, gembur dan juga kaya akan humus dengan pH berkisar antara 5,5- 6,5. Umbi wortel dapat dipanen setelah berumur kira-kira 2,5-4 bulan. Umbi wortel yang baik dipanen adalah yang masih muda karena umbi yang sudah tua mempunyai tekstur yang keras dan pahit (Rukmana, 1995).
Wortel mengandung hampir seluruh kebutuhan mineral dan β-karoten yang dibutuhkan oleh tubuh. Dimana kandungan terbesar dari wortel adalah vitamin A dalam bentuk β-karoten. Fungsi dari vitamin A sebagai bahan untuk membuat rodopsin yang diperlukan dalam proses penglihatan, pemeliharaan jaringan pelapis, dan juga untuk membantu proses pertumbuhan tubuh. Kekurangan vitamin A dapat menyebabkan gangguan penglihatan, perubahan-perubahan pada jaringan pelapis (epitel) dan juga dapat mengganggu jalannya pertumbuhan tubuh (Moehji, 1986).
Kandungan gizi dan manfaat wortel
24 42
kanker karena wortel mempunyai kandungan betakaroten yang tinggi karena sifat antioksidannya yang melawan kerja destruktif sel-sel kanker, mencegah rabun senja, menurunkan kolesterol darah dan juga wortel mengandung serat yang tinggi yang dapat mencegah terjadinya konstipasi, mencegah stroke karena aktivitas beta karoten yang dapat mencegah terjadinya plak atau timbunan kolesterol yang terdapat dalam pembuluh darah, mengatasi kandungan kulit seperti jerawat, bengkak bernanah ataupun kulit kering, membantu menetralkan asam dalam darah, menghilangkan toksin dalam tubuh karena adanya kandungan kalium dalam wortel (Apriliaw, 2011). Kandungan gizi wortel dapat dilihat pada Tabel 2. Tabel 2. Kandungan gizi wortel (per 100 g)
Kandungan Gizi Jumlah
Energi (kalori) 42,00
25 42
masa simpan dari produk karena dapat mencegah terjadinya kristalisasi es selama proses penyimpanan dan juga mampu untuk meningkatkan kemampuan menyerap air sehingga produk menjadi tidak mudah meleleh (Padaga dan Sawitri, 2006).
Gelatin merupakan derivat protein yang berasal dari serat kolagen yang ada pada kulit, tulang, dan tulang rawan. Gelatin mempunyai susunan asam amino yang hampir mirip dengan kolagen, dimana glisin sebagai asam amino utama dan merupakan 2/3 dari seluruh asam amino yang menyusunnya, sedangkan 1/3 asam amino yang tersisa diisi oleh prolin dan hidroksiprolin (Chaplin, 2005).
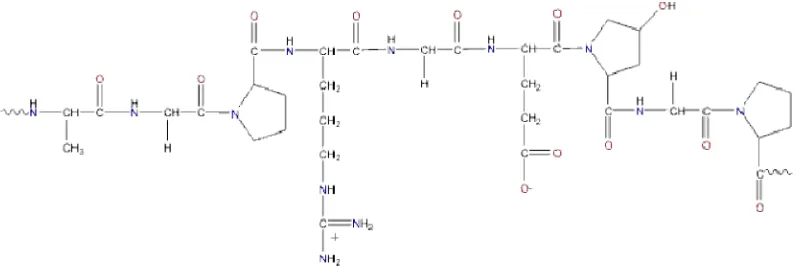
Fungsi dari gelatin mencakup pengatur stabilitas buih, kekenyalan dan tekstur pada industri permen, dapat menggantikan peranan lemak dan juga dapat meningkatkan daya leleh di mulut pada produk es krim maupun jeli, pengikat air pada produk hewani, bahan pengisi pada produk olahan susu, dan berfungsi untuk menjernihkan produk minuman. Konsentrasi penggunaan gelatin sebagai zat penstabil pada produk es krim aktif yaitu sebesar 0,5%. Selain itu gelatin dapat digunakan untuk mencegah kerusakan fisik dari produk buah-buahan maupun produk hewani dengan cara melapisi bagian permukaan produk tersebut (Rahman, 2007). Struktur kimia gelatin dapat dilihat pada Gambar 2.
Gambar 2. Struktur Kimia Gelatin (Belitz, dkk., 2007)
26 42
Gelatin larut dalam air, asam asetat maupun pelarut alkohol seperti gliserol, propilen glycol, manitol dan sorbitol, tetapi gelatin tidak larut dalam alkohol, aseton, karbon tetraklorida, benzen, petroleum eter maupun pelarut organik lainnya. Menurut Norland (1997), gelatin mudah larut pada suhu 71oC
dan pada suhu 48,9oC gelatin cenderung membentuk gel. Sedangkan menurut
Montero dan Gomez-Guillen (2000), suhu yang biasanya melarutkan gelatin sekurang-kurangnya 49 oC atau biasanya pada suhu 60-70oC. Gelatin mempunyai
sifat yang dapat berubah secara reversible dari bentuk sol ke gel, membengkak atau mengembang dalam air dingin, dapat membentuk film, dapat melindungi sistem koloid, dan juga dapat mempengaruhi viskositas suatu bahan (Parker, 1982).
High fructose syrup (HFS)
HFS (High Fructose Syrup) adalah bentuk sediaan fruktosa yang dibuat dengan cara hidrolisis enzimatis pati secara bertingkat. Enzim yang digunakan adalah alpha amylase, amylogkukosidase dan isomerase. Hasil yang diperoleh berupa sirup (72-75%) yang mengandung 52-55% glukosa, 42-45% fruktosa dan sekitar 3% maltosa dan isomaltosa. HFS merupakan sirup yang sangat murni, sehingga bebas dari kandungan logam-logam berat, sisa asam, maupun jasad renik, dan juga warna dari siruf HFS ini sangat jernih sehingga sangat sesuai digunakan untuk kepentigan industri (Soebijanto, 1986).
Sirup fruktosa juga dapat dibuat dari glukosa melalui suatu proses
isomerisasi dengan menggunakan enzim glukosa isomerase. Tingkat kemanisan
sirup fruktosa 2,5 kali lebih tinggi dibanding dengan sirup glukosa dan 1,4-1,8
27 42
glikemik yang lebih rendah (32 ± 2) daripada glukosa (138 ± 4), sedangkan indeks
glikemik untuk sukrosa sebesar 87 ± 2. Sehingga sirup fruktosa dapat digunakan
sebagai pemanis bagi penderita diabetes. Dalam keadaan dingin sirup fruktosa
akan terasa lebih manis. Sehingga sirup fruktosa dapat digunakan dalam produk
minuman ringan, sirup, jeli, jam, koktail, dan sebagainya (Purwandari, 2009).
Penggunaan sirup fruktosa di industri mempunyai beberapa kelebihan bila dibandingkan dengan gula lain seperti glukosa maupun sukrosa, yaitu menghemat waktu produksi dan mudah dicetak maupun dicampurkan, dapat memperbaiki mutu rasa produk akhir, dan dapat memperbaiki penampakan produk akhir. Fruktosa juga mempunyai kelebihan memperbaiki konsistensi produk akhir seperti plastisitas dan tekstur yang lebih baik, memodifikasi viskositas, memperbaiki daya awet produk, dan juga mempunyai tingkat keamanan yang tinggi karena tidak bersifat karsinogenik (Mangunwidjaja, 1993). Perbandingan kemanisan relatif berbagai jenis gula dapat dilihat pada Tabel 3.
Tabel 3. Kemanisan relatif berbagai jenis gula
Jenis gula Tingkat kemanisan
Sukrosa 1.0
Glukosa 0.7
Fruktosa 1.2
Gula invert 1.0
Maltosa 0.5
Laktosa 0.4
Sorbitol 0.5
Sakarin 300.0
Sumber : Nicol (1979)
Proses Pembuatan Es Lilin
28 42
pengawet. Es lilin mempunyai warna yang menarik, rasa yang manis, kemasan yang sederhana dan harga yang murah (Hartono, dkk., 2013). Tahap awal dalam pembuatan es lilin yaitu persiapan sari buah. Sari buah nenas dibuat dengan cara mengupas kulit buah nenas kemudian daging buah nenas dipisahkan dari tulangnya. Sari buah nenas diperoleh dengan cara pengepresan menggunakan alat pengepres (Ardina, dkk., 2014).
Pembuatan sari wortel yaitu wortel yang telah disortasi dibuang bagian yang tidak diolah kemudian wortel dicuci dan diblansir pada suhu 85oC selama lima menit (Aprilianty, 2013). Wortel dihaluskan dengan penambahan air dan kemudian disaring. Blansir bertujuan untuk meningkatan kualitas produk yang akan diolah, tetapi pemblansiran menurunkan kekerasan tekstur serta menurunkan bau langu sehingga lebih sering digunakan untuk sayuran dari pada buah-buahan. Pemblensiran sering diterapkan dengan menggunakan air mendidih dan penguapan (Cotcuera, dkk., 2004).
Pemanasan mempunyai peranan penting dalam pengawetan suatu produk, tetapi penggunaan suhu yang terlalu tinggi juga dapat mengakibatkan penurunan kandungan gizi, senyawa-senyawa volatil dan karakteristik sensori seperti rasa dan warna (Susanti dan Putri, 2014).
29 42
minuman karena bersifat fleksibel, ringan, daya rekat yang baik, dan juga tahan akan suhu rendah (Vaclavik dan Christian, 2008)
Pembekuan merupakan tahap akhir dalam pembuatan es lilin. Menurut Vaclavik dan Christian (2008) pembekuan merupakan salah satu cara untuk memperpanjang masa simpan dari produk dengan cara mengubah wujud air produk dalam bentuk es atau kristal sehingga air yang digunakan untuk pertumbuhan mikroba tidak tersedia sehingga produk lebih awet.
Pengemasan
Pengemasan merupakan salah satu cara pengawetan yang dapat memperpanjang umur simpan dari suatu bahan atau produk, dimana pengemasan dapat mencegah terjadinya kerusakan-kerusakan yang terjadi baik fisik maupun kimia pada suatu bahan (Mailangkay, 2002). Kemasan yang sering digunakan dalam produk makanan adalah plastik seperti Low density Polyethylen (LDPE), High density Polyethylen (HDPE), dan polypropylene (PP).
Kemasan yang sering digunakan pada produk beku adalah jenis kemasan polypropylene (PP). Menurut Robertson dan Gordon (1993) plastik polypropylene memiliki densitas yang lebih rendah dan mempunyai titik lunak yang lebih tinggi bila dibandingkan dengan polietilen, dan juga polypropylene tahan terhadap lemak dan bahan kimia serta mempunyai permiabilitas gas sedang. Kemasan plastik polipropilen bila dibandingkan dengan kemasan polietilen mempunyai plastik yang lebih terang dan kuat serta lebih kaku (Rochman, 2007) sehingga cocok bila digunakan untuk kemasan produk beku seperti es lilin.
30 42
Mutu Es Lilin
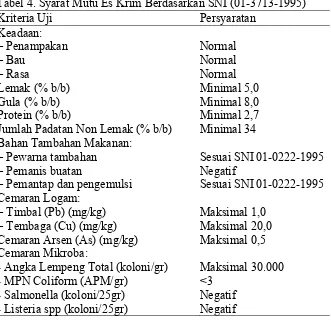
Es lilin merupakan produk minuman beku yang hingga saat ini belum memiliki standar mutu. Oleh karena itu sebagai pembanding digunakan standar mutu es krim (Tabel 4).
Tabel 4. Syarat Mutu Es Krim Berdasarkan SNI (01-3713-1995) Kriteria Uji
Jumlah Padatan Non Lemak (% b/b) Bahan Tambahan Makanan:
- Angka Lempeng Total (koloni/gr) - MPN Coliform (APM/gr)
31 42
dan aroma velva wortel, tetapi berpengaruh terhadap tekstur dan overall serta berpengaruh terhadap overrun dan resistensi (Rini, dkk., 2012).
Penelitian lainnya mengenai sherbet oleh Hartanti, (2014) menyatakan bahwa buah nenas bersifat fungsional untuk diolah menjadi produk minuman beku sherbet karena buah nenas mengandung nutrisi dan kadar air yang tinggi, tetapi kandungan air yang tinggi dapat mengakibatkan terjadinya penurunan tekstur pada produk sehingga untuk menghasilkan tekstur yang lebih lembut diperlukan adanya penambahan gelatin yang mempunyai sifat hidrokoloid yang dapat memperlambat titik beku dari produk. Penelitian Banerjee dan Bhattacharya (2012) menunjukkan bahwa pada suhu pemanasan di atas 45 ºC dan RH 60% gelatin mudah larut, aktivitas enzim, suhu, dan pH mempengaruhi sifat kekuatan gel yang dibentuk, sedangkan menurut penelitian yang dilakukan oleh Ningsih (2007) pada pembuatan sherbet nenas konsentrasi gelatin yang terbaik adalah sebesar 0.3%.
32 42
BAHAN DAN METODA
Waktu dan Tempat Penelitian
Penelitian ini dilaksanakan pada bulan Mei sampai dengan bulan Juli 2015 di Laboratorium Analisa Kimia Bahan Pangan, Laboratorium Teknologi Pangan, dan Laboratorium Mikrobiologi Program Studi Ilmu dan Teknologi Pangan Fakultas Pertanian Universitas Sumatera Utara, Medan.
Bahan Penelitian
Bahan penelitian yang digunakan adalah buah nenas dengan tingkat kematangan morfologis dan wortel. Buah nenas diperoleh dari pasar tradisional dan wortel diperoleh dari pasar swalayan yang ada di Medan. Bahan lain adalah HFS (High Fructose Syrup) merk Rose Brand, gelatin halal merk Gelatina, dan air.
Reagensia
Reagensia yang digunakan dalam penelitian ini adalah NaOH 0,1 N, indikator phenolptaelin 1%, larutan Dye (Di-klorofenil indofenol), asam askorbat, asam oksalat, akuades, HCL 10%, metanol pro analisis, larutan DPPH (1,1-diphenyl-2-picrylhydrazil), KOH 12%, Na2SO4 5%, aseton, kloroform, dan
petroleum eter.
Alat Penelitian
Alat yang digunakan untuk pembuatan produk es lilin yaitu pisau, baskom, gelas ukur, saringan, termometer, kain saring, panci kukus stainless steel, sendok pengaduk, talenan, timbangan dan plastik polipropilen. Peralatan yang digunakan
33 42
untuk analisa mutu fisik produk es lilin meliputi timbangan analitik Sartorius, gelas ukur, corong, dan kromameter Konica Minolta (tipe CR-400, Jepang). Peralatan yang digunakan untuk analisa mutu kimia produk es lilin meliputi timbangan analitik Sartorius, gelas ukur, buret, spektrofotometer UV (Genesys 20), handrefractometer, pH meter, pipet tetes, gelas ukur, erlemenyer, kertas saring bebas abu no.180, labu ukur, vortex tab dancer, corong, kapas, cawan porselen, tanur Carbolite Furnaces (tipe EML 11/2), oven Memmert (tipe BMV 30), pemanas listrik Maspion, dan desikator. Peralatan yang digunakan untuk analisa mutu terbaik dan kontrol yaitu timbangan analitik Sartorius, gelas ukur, tabung reaksi, rak tabung, buret, mikropipet 20µl -200µl, bunsen, autoclave, cawan petridish, colony counter, inkubator, labu pisa, dan kaki tiga
Metode Penelitian
Penelitian ini dilakukan dengan menggunakan rancangan acak lengkap (RAL), yang terdiri dari dua faktor, yaitu:
Faktor I : Perbandingan Sari buah nenas : Sari Wortel (S) S1 = 0 % : 100 %
S2 = 25 % : 75 %
S3 = 50 % : 50 % S4 = 75 % : 25 %
S5 = 100 % : 0 %
Faktor II : Konsentrasi Gelatin (K) K1 = 0% (Kontrol)
K2 = 0,2 %
K3 = 0,4%
34 42
Banyaknya kombinasi perlakuan atau Treatment Combination (Tc) adalah 5x3=15, dengan jumlah ulangan sebanyak 3 kali, sehingga jumlah sampel keseluruhan adalah 45 sampel.
Model Rancangan
Penelitian ini dilakukan dengan model rancangan acak lengkap (RAL) dua faktorial dengan model sebagai berikut:
Ŷijk = µ + αi + βj + (αβ)ij + εijk
dimana:
Ŷijk : Hasil pengamatan dari faktor S pada taraf ke-i dan faktor K pada taraf
ke-j dalam ulangan ke-k µ : Efek nilai tengah
αi : Efek faktor S pada taraf ke-i
βj : Efek faktor K pada taraf ke-j
(αβ)ij : Efek interaksi faktor S pada taraf ke-i dan faktor K pada taraf ke-j
εijk : Efek galat dari faktor S pada taraf ke-i dan faktor K pada taraf ke-j
dalam ulangan ke-k
Apabila diperoleh hasil yang berbeda nyata dan sangat nyata maka uji dilanjutkan dengan uji beda rataan, menggunakan uji Least Significant Range (LSR).
Pelaksanaan Penelitian
35 42
sampai halus, dan disaring. Wortel yang digunakan di kupas, dipotong kecil-kecil dan diblanshing pada suhu 85oC selama 10 menit, kemudian diblender dengan
perbandingan wortel dan air 1 : 1.
Sari nenas dan sari wortel yang dihasilkan di campur dengan 5 jenis perbandingan sesuai pada perlakuan dari total campuran 300 ml untuk tiap perlakuan. Pada setiap campuran ditambahkan high fructosa syrup (HFS) sebesar 10% dari total campuran. Gelatin dengan konsentrasi sesuai perlakuan dicampurkan ke dalam larutan sari buah nenas dan wortel kemudian campuran dipanaskan pada suhu 90oC selama 2 menit. Selanjutnya campuran tersebut
dimixer untuk mengurangi suhunya hingga 50oC. Campuran kemudian dikemas
dengan menggunakan kemasan plastik polipropilen dan disimpan pada lemari pendingin (freezer) dengan suhu -5oC hingga diperoleh produk es lilin. Es lilin
yang dihasilkan di simpan pada suhu beku yang sama selama 3 hari sebelum dianalisa.
Parameter mutu es lilin yang diamati meliputi karakteristik fisik (warna dengan khromameter (nilai L, a, b dan oHue) dan kecepatan mencair), karakteristik kimia (total soluble solid, total asam, kadar vitamin C, kadar abu larut air, kadar abu tidak larut asam, dan pH) dan karakteristik sensori (uji hedonik terhadap warna, aroma, rasa dan konsistensi). Perlakuan yang menghasilkan es lilin dengan mutu terbaik dan disukai panelis kemudian dianalisa kandungan TPC (Total Plate Count), aktivitas antioksidan dan kandungan betakaroten). Setiap perlakuan diulang sebanyak 3 kali.
36 42
Pengamatan dan Metode Pengukuran Data
Pengamatan dan pengukuran data dilakukan dengan cara analisis terhadap parameter sebagai berikut:
Karakteristik fisik Warna (Metode Hunter)
Pengujian warna dilakukan dengan menggunakan kromameter Minolta (tipe CR 200, Jepang). Sejumlah sampel ditempatkan pada wadah yang datar. Pengukuran menghasilkan nilai L, a, b, dan ºH (ºHue). Nilai L menyatakan tingkat kecerahan.Warna kromatik campuran merah hijau ditunjukkan oleh nilai a. Warna kromatik campuran biru kuning ditunjukkan oleh nilai b. Dilakukan perhitungan untuk ºH dengan rumus ºH = tan-1 (b/a).
Penentuan waktu mencair (Innocente, 2002)
Kecepatan mencair adalah penentuan waktu yang dibutuhkan es lilin untuk mencair dengan sempurna. Waktu pencairan dapat diukur dengan menimbang sampel beku sebanyak 35 g, kemudian diletakkan pada corong dan gelas ukur sebagai wadah. Sampel diukur pada suhu ruang dan ditentukan jumlah volume pelelehan sampel setiap selang waktu 5 menit hingga sampel meleleh sempurna. Hubungkan volume pelelehan dan selang waktu diinterpretasikan ke dalam bentuk grafik dan slope dari persaman linear antara volume pelelehan dan selang waktu sebagai kecepatan mencair dalam satuan ml per menit.
37 42
Karakteristik kimia
Penentuan pH (Apriyantono, dkk., 1989)
Penetapan nilai pH dilakukan dengan pH meter yang telah dikalibrasi dengan larutan buffer pada pH 4 dan 7. Suhu sampel diukur menggunakan pengatur suhu pH meter pada suhu terukur, kemudian pH meter dinyalakan dan dibiarkan sampai stabil (15 - 30 menit). Elektroda pada pH meter dibilas dengan akuades dan dikeringkan elektroda dengan kertas tisu. Setelah itu elektroda dicelupkan ke dalam larutan sampel dan di-set pengukur pH – nya. Elektroda dibiarkan tercelup di dalam larutan selama beberapa saat sampai diperoleh pembacaan yang stabil, lalu nilai pH sampel dicatat.
Total padatan terlarut (Muchtadi dan Sugiyono, 1992)
Sampel ditimbang sebanyak 5 g, dimasukkan ke gelas ukur, diberi penambahan akuades sebanyak 20 ml dan diaduk hingga homogen. Diambil satu tetes larutan dan diteteskan pada prisma handrefractometer, dibaca angka di titik terang dan gelap pada skala refraktometer. Nilai total padatan terlarut (TSS) dihitung dengan mengalikan skala refraktometer dengan faktor pengenceran (FP).
TSS (ºBrix) = skala refraktometer x FP
Penentuan total asam (Rangganna, 1977)
Sampel es lilin ditimbang sebanyak 10 g, dimasukkan ke dalam beaker glass dan ditambahkan akuades hingga volume 100 ml. Diaduk hingga merata dan disaring dengan kertas saring dan diambil filtratnya sebanyak 10 ml dan dimasukkan ke dalam erlenmeyer dan ditambahkan phenolptalein 1% sebanyak
38 42
3 tetes. Kemudian dititrasi dengan menggunakan NaOH 0,1N. Titrasi dihentikan setelah muncul warna merah jambu yang stabil.
Total asam = ml NaOH x N NaOH x BM asam dominan x FP x 100 % Berat contoh (gr) x 1000 x valensi asam
FP = faktor pengencer (10)
Asam dominan = Asam sitrat (C6H8O7), BM = 192, valensi = 3
Kadar Vitamin C (Metode Kolorimetri, Apriyantono, dkk., 1989) Pembuatan larutan Dye
Larutan Dye dibuat dengan menimbang 100 mg 2,6-diklorofenol indofenol dan 84 mg Sodium Bikarbonat, dilarutkan dalam akuades dan diterakan hingga 100 ml. Larutan dipipet 25 ml dan ditera pada labu ukur 500 ml.
Pembuatan kurva standar vitamin C
Vitamin C ditimbang 250 mg dan ditambahkan H2C2O4 6% hingga tera
labu ukur 100 ml. Dipipet masing-masing 1 ml, 2 ml, 3ml, 4 ml, dan 5 ml larutan standar, ditera dengan H2C2O4 6% sampai 5 ml. Larutan Dye ditambahkan dengan
cepat sebanyak 10 ml ke larutan standar, dikocok lebih kurang 10detik, dibaca absorbansi sampel padaλ = 518 nm. Data konsentrasi standar diinterpretasikan dengan absorbansi dan diperoleh persamaan dengan nilai regresi 0,9 ≤ R2≤ 1. Kurva standar vitamin C dapat dilihat pada Lampiran 1.
Penentuan kadar vitamin C es lilin
Sampel ditimbang sebanyak 10 g, ditambahkan H2C2O4 6% dan disaring
39 42
dalam persamaan kurva standar sehingga diperoleh konsentrasi asam askorbat yang kemudian dihitung melalui persamaan :
Vitamin C Konsentrasi asam askorbat x volume ekstrak total x 100 (mg/100g/ml sampel) = ml ekstrak sampel x 100 x berat sampel
Kadar abu total (Nielsen, 1998)
Kadar abu sampel dihitung sebagai kadar abu total dikurangi dengan kadar abu larut air dan kadar abu tidak larut asam. Kadar abu total di ukur dengan cara Sampel ditimbang 10 g pada cawan porselen, lalu dibakar hingga sempurna dihotplate hingga hilangnya asap pembakaran, kemudian cawan dimasukkan ke dalam tanur pengabuan dengan suhu hingga 500 ºC dan dihitung selama 5 jam, kemudian suhu diturunkan hingga di bawah 200 ºC, kemudian di desikator 15 menit dan ditimbang hasil kadar abu total dengan rumus sebagai berikut :
Kadar abu total (%) = Berat akhir – berat awal x 100% Berat awal
Kadar abu larut air (Nielsen, 1987)
Penentuan kadar abu larut air dilakukan dengan menimbang berat sampel hasil pengabuan total dan dididihkan dengan 10 ml akuades. Sampel kemudian disaring menggunakan kertas saring bebas abu (ashless paper) dan dikumpulkan bagian yang tidak larut, kemudian dimasukkan dalam oven pengeringan pada suhu yang tidak melebihi 450 ºC selama 15 menit, kemudian dimasukkan dalam desikator 15 menit, ditimbang, dan dilakukan hingga berat konstan. Kadar abu larut air dihitung dengan persamaan berikut :
Kadar abu larut air (%) = Berat awal – berat akhir x 100%
Berat awal
40 42
Kadar abu tidak larut asam (Nielsen, 1987)
Penentuan kadar abu tidak larut asam dilakukan dengan menimbang berat sampel hasil pengabuan total dan dididihkan dengan 25 ml HCl 10% selama 5 menit. Bagian yang tidak larut asam dikumpulkan, disaring menggunakan kertas saring bebas abu (ashless paper), kemudian dicuci beberapa kali dengan akuades panas, dikeringkan dan dipijarkan selama 30 menit hingga berat konstan. Kadar abu yang tidak larut asam dihitung dengan persamaan berikut :
Kadar abu tidak larut asam (%) = Berat awal – berat akhir x 100%
Berat awal
Kadar abu sampel = Kadar abu total – (kadar abu larut air + kadar abu tidak larut asam )
Uji organoleptik warna, aroma, rasa dan konsistensi (Silva, dkk., 2010) Analisis sensoris terhadap sampel es lilin dilakukan dengan menentukan nilai organoleptik warna, aroma, rasa dan konsistensi. Sampel es lilin yang telah diberi kode secara acak, diuji oleh 20 panelis. Pengujian dilakukan secara inderawi (organoleptik) yang ditentukan berdasarkan skala hedonik untuk menentukan nilai acceptable index (AI). Format uji organoleptik disajikan pada Lampiran 2. Nilai AI yang diperoleh harus setara atau lebih besar dari 70%. Untuk skala hedonik disajikan pada Tabel 5. Nilai IP dapat ditentukan melalui persamaan berikut :
AI (%) = Y x 100 Z
Y = rata-rata nilai skala hedonik dari panelis Z = Nilai skala hedonik tertinggi yang diperoleh AI = Acceptable Index
41 42
Tabel 5. Skala nilai hedonik warna, aroma, rasa dan konsistensi
Skala hedonik Keterangan
9 Sangat suka sekali
8 Sangat suka
7 Lebih suka
6 Suka
5 Netral
4 Agak suka
3 Tidak suka 2 Sangat tidak suka
1 Sangat tidak suka sekali
Pengujian perlakuan terbaik
Perlakuan terbaik dipilih berdasarkan karakteristik fisik, kimia dan sensori yang terbaik. Perlakuan terbaik kemudian di analisa aktivitas antioksidan, total mikroba dan pengujian β-karoten.
Uji aktivitas antioksidan dengan metode DPPH (Sumarny, dkk., 2012) Pembuatan larutan DPPH (0,4 mM)
Ditimbang lebih kurang 15,8 mg DPPH (1,1-difenil-2-pikrilhidrazil), kemudian dilarutkan dengan metanol pro analisis hingga 100 ml pada labu ukur, ditempatkan dalam botol gelap.
Pembuatan larutan blanko
Dipipet 1 ml larutan DPPH (0,4 mM) ke dalam labu tentukur 5 ml dan ditambahkan metanol hingga tanda tera, lalu homogenkan.
Pembuatan larutan uji
42 42
masing-masing labu ukur ditambahkan 1 ml larutan DPPH, ditambahkan dengan metanol pro analisis sampai tanda tera, kemudian dihomogenkan.
Pembuatan larutan vitamin C sebagai kontrol positif
Ditimbang 5 mg vitamin C kemudian dilarutkan dalam 5 ml metanol pro analisis (1000 bagian per juta), larutan ini merupakan induk. Dipipet 20 µl, 30 µl, 40 µl, 50 µl dan 60 µl larutan induk (triplo) ke dalam labu ukur 5 ml untuk mendapatkan konsentrasi sampel 4, 6, 8, 10 dan 12 µg/ml ke dalam masing-masing labu ukur ditambahkan 1 ml larutan DPPH dan ditambahkan dengan metanol pro analisis sampai tanda tera kemudian dihomogenkan. Kurva standar antioksidan dilampirkan pada Lampiran 3.
Uji aktivitas antioksidan
Larutan uji dan kontrol positif dengan beberapa konsentrasi diinkubasi pada suhu 37 ºC selama tepat 30 menit, serapan diukur pada panjang gelombang maksimum 517 nm menggunakan spektrofotometri UV-VIS. Persentase inhibisi dihitung menggunakan rumus sebagai berikut :
% hambatan = Absorbansi blanko – absorbansi sampel x 100% Absorbansi blanko
Perhitungan nilai IC50 dengan memasukkan nilai dari konsentrasi larutan
uji (sumbu x) dan % hambatan terhadap DPPH (sumbu y) ke dalam persamaan garis regresi. Semakin rendah nilai IC50 berarti semakin tinggi aktivitas
antioksidan sebagai peredam radikal bebas. Aktivitas suatu senyawa dikatakan memiliki aktivitas tinggi jika mempunyai nilai IC50 di bawah 20 bpj, aktivitas
sedang jika mempunyai nilai IC50 21 – 100 bpj, aktivitas rendah jika mempunyai
nilai IC50 101 – 200 bpj dan tidak aktif jika mempunyai nilai IC50 di atas 200 bpj.
43 42
Pengujian total mikroba (Fardiaz, 1992)
Pengujian total mikroba sampel dilakukan dengan metode Total Plate Count (TPC). Bahan diambil sebanyak 1 g dan dimasukkan ke dalam tabung reaksi kemudian ditambahkan akuades 9 ml dan diaduk sampai merata. Hasil pengenceran ini diambil dengan pipet tetes sebanyak 1 ml kemudian ditambahkan akuades 9 ml. Pengenceran ini dilakukan sampai 100 kali (102).
Dari hasil pengenceran pada tabung reaksi yang terakhir diambil sebanyak 1 ml dan diratakan pada medium agar PCA (Plate Count Agar) (ditimbang 7 g PCA, ditambahkan akuades 250 ml dan kemudian disterilisasikan dalam autoclave pada suhu 121oC selama 15 menit). PCA yang telah disiapkan di atas
cawan petri, selanjutnya diinkubasi selama 24 jam pada suhu 32oC dengan posisi terbalik. Jumlah koloni yang ada dihitung dengan colony counter.
Total Koloni = Jumlah koloni x 1 FP Pengujian β - karoten (Apriyantono, dkk.,1989).
Pembuatan Kurva Standar β - Karoten
Diambil 25 mg β-karoten murni, dan dimasukkan kedalam labu 250 ml, ditambahkan 2,5 ml kloroform, ditambahkan petroleum benzene sampai batas tera, diambil 10 ml larutan tersebut, ditambahkan petroleum benzene sampai batas tera pada labu ukur 100 ml, diambil larutan masing-masing 5 ml, 10 ml, 15 ml, 20 ml dan seterusnya kemudian dimasukkan kedalam labu ukur 100 ml, ditambahkan 3 ml aseton pada masing-masing labu, diencerkan sampai dengan batas tera dengan petroleum Benzene. Kurva standar beta karoten ditunjukkan pada Lampiran 4.
Pengujian Kadar β - Karoten
44 42
Ditimbang bahan sebanyak 5 g, digerus kedalam mortal dengan alu dengan ditambahkan KOH sebanyak 75 ml sedikit demi sedikit, ditunggu hingga 15 menit, dimasukkan kedalam labu pemisah, ditambahkan 15 ml Petroleum benzene lalu dikocok sampai 30 detik sampai di buka tutup, ditambahkan Na2SO4
3 ml dan Petroleum benzene 15 ml lalu dikocok kembali. Disedot 2,5 ml minyak yang memisah dipermukaan, kemudian diletakkan pada erlenmeyer lalu diberi 7,5 ml Petroleum benzene, dan diambil 1,5 ml dari erlenmeyer diletakkan lagi kedalam cuvet diberi 3ml aseton dingin, diambil 2 ml dan ditambahkan 11 ml Petroleum benzene dan dimasukkan kedalam spektrometer dengan absorbansi 273 nm.
Perhitungan Kurva Standar
Dicari persamaan linear dan regresi, dimana nilai r > 0,9 di kurva, dimasukkan absorbansi sampel dan didapat konsentrasi sampel, kandungan β-karoten sampel dihitung dengan rumus :
Rumus : β-karoten (mg/100g) = [ ] sampel x FP x 100 g sampel x 1000
45 42
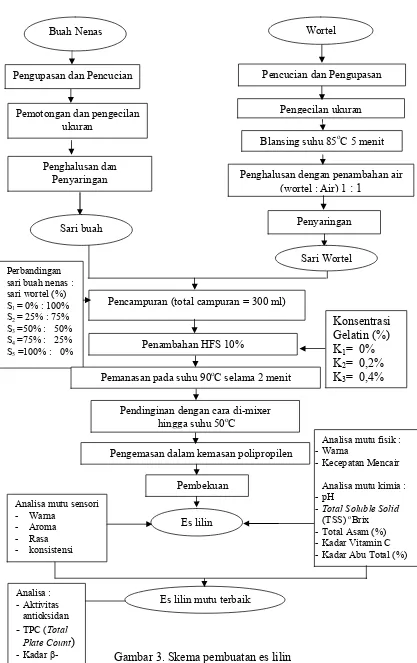
Gambar 3. Skema pembuatan es lilin Penghalusan dan
Pencampuran (total campuran = 300 ml)
Konsentrasi
Pengemasan dalam kemasan polipropilen - Analisa mutu fisik : Warna - Kecepatan Mencair
Pengupasan dan Pencucian Pencucian dan Pengupasan
Pemanasan pada suhu 90oC selama 2 menit
46 42
HASIL DAN PEMBAHASAN
Karakteristik Fisik Es Lilin dari Campuran Sari Buah Nenas dan Wortel dengan Penambahan Gelatin
Dari hasil penelitian terhadap karakteristik mutu fisik es lilin meliputi nilai warna (ºHue) dengan kromameter dan kecepatan mencair (min/g). Pengaruh perbandingan sari buah nenas dan wortel dengan gelatin terhadap karakteristik mutu fisik dari es lilin dapat dilihat pada Tabel 6 dan Tabel 7.
Tabel 6. Pengaruh perbandingan sari buah nenas dan wortel pada es lilin terhadap karakteristik fisik yang diamati
Keterangan: Angka dalam tabel merupakan rataan dari 3 ulangan, ± standard deviasi. Angka yang diikuti dengan huruf yang berbeda dalam satu baris menunjukkan berbeda nyata (P<0,05) (huruf kecil) dan berbeda sangat nyata (P<0,01) (huruf besar) dengan uji LSR.
Tabel 7. Pengaruh konsentrasi gelatin yang ditambahkan pada es lilin terhadap karakteristik fisik yang diamati Keterangan: Angka dalam tabel merupakan rataan dari 3 ulangan, ± standard deviasi. Angka yang diikuti dengan huruf yang berbeda dalam satu baris menunjukkan berbeda nyata (P<0,05) (huruf kecil) dan berbeda sangat nyata (P<0,01) (huruf besar) dengan uji LSR.
Warna (oHue)
Perbandingan sari buah nenas dan wortel memberikan pengaruh yang berbeda sangat nyata (P<0,01) terhadap warna es lilin yang dihasilkan (Tabel 6) tetapi pengaruh konsentrasi gelatin yang ditambahkan memberikan pengaruh yang
47 42
berbeda tidak nyata (P>0,05) terhadap warna es lilin yang dihasilkan (Tabel 7). Interaksi antara perbandingan sari buah nenas dan wortel dengan konsentrasi gelatin memberikan pengaruh yang berbeda tidak nyata (P>0,05) terhadap warna es lilin dapat dilihat pada Lampiran 5. Hubungan perbandingan sari buah nenas dan wortel terhadap warna dapat dilihat pada Gambar 4.
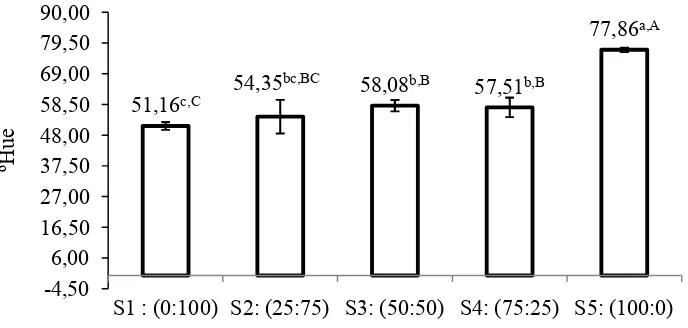
Gambar 4. Hubungan perbandingan sari buah nenas dan wortel dengan nilai warna es lilin (± Error Bar Standar Deviasi)
Gambar 4 menunjukan bahwa es lilin dari S5 (100%) nenas memiliki nilai oHue tertinggi dibandingkan perbandingan lainnya, sedangkan nilai warna yang
terendah yaitu pada perlakuan S1 (100% wortel). Sari wortel memiliki nilai a (+)
yaitu antara 0 sampai 100 yang menunjukkan warna merah (Andarwulan, dkk., 2001). Peningkatan jumlah sari wortel dalam campuran sari buah akan meningkatkan nilai a (+) yang menunjukkan warna es lilin yang dihasilkan cenderung berwarna kemerahan.
Kecepatan Mencair
Perbandingan sari buah nenas dan wortel memberikan pengaruh yang berbeda sangat nyata (P<0,01) terhadap kecepatan mencair es lilin yang
48 42
dihasilkan (Tabel 6) sedangkan konsentrasi gelatin memberikan pengaruh yang berbeda tidak nyata (P>0,05) terhadap kecepatan mencair es lilin yang dihasilkan (Tabel 7). Interaksi antara jenis perbandingan sari buah nenas dan wortel dengan penambahan konsentrasi gelatin memberikan pengaruh yang berbeda tidak nyata (P>0,05) terhadap kecepatan mencair es lilin yang dihasilkan seperti dapat dilihat pada Lampiran 6. Pengaruh perbandingan sari buah nenas dan wortel terhadap
kecepatan mencair es lilin dapat dilihat pada Gambar 5.
Gambar 5. Hubungan perbandingan sari buah nenas dan wortel dengan kecepatan mencair es lilin (± Error Bar Standar Deviasi)
Gambar 5 menunjukkan bahwa perbandingan sari buah nenas dan wortel dengan perbandingan 0%:100% memiliki kecepatan mencair tertinggi di bandingkan perlakuan yang lainnya sedangkan kecepatan mencair yang terendah terdapat pada perlakuan S5 (100%:0%). Peningkatan jumlah sari wortel di dalam
campuran sari buah akan menurunkan waktu pencairan yang menunjukkan waktu yang dibutuhkan untuk mencair menjadi lebih sedikit. Hal ini dikarenakan pengaruh kadar air pada proses pembuatan sari wortel sehingga pada saat pembekuan terbentuk kristal granula yang besar. Hal ini sesuai dengan literatur
0,00
S1: (0:100) S2: (25:75) S3: (50:50) S4: (75:25) S5: (100:0)
K
Perbandingan Sari Buah Nenas dan Wortel
49 42
Blackburn (2012) menyatakan semakin besar kandungan air bahan maka ikatan granula kristal es lebih padat dan cenderung membentuk kristal es yang besar dan lebih lama mencair.
Karakteristik Kimia Es Lilin dari Campuran Sari Buah Nenas dan Wortel dengan Penambahan Gelatin
Perbandingan sari buah nenas dan wortel yang ditambahkan pada es lilin memberikan pengaruh yang berbeda sangat nyata (P<0,01) terhadap pH, total padatan terlarut, total asam, kadar vitamin C, kadar abu total seperti dapat dilihat pada Tabel 8. Perbedaan konsentrasi gelatin yang ditambahkan ke dalam es lilin memberikan pengaruh yang berbeda sangat nyata (P<0,01) terhadap kadar vitamin C, dan kadar abu total dan memberikan pengaruh yang berbeda nyata (P<0,05) terhadap pH dan total asam tetapi memberikan pengaruh yang berbeda tidak nyata (P>0,05) terhadap nilai total padatan terlarut es lilin seperti dapat dilihat pada Tabel 9.
Tabel 8. Pengaruh perbandingan sari buah nenas dan wortel pada es lilin terhadap karakteristik kimia yang diamati
Parameter Mutu
Perbandingan Sari Buah Nenas : Sari Wortel (S)
S1 = 0 :100 S2 = 25 : 75 S3 = 50 : 50 S4 = 75 : 25 S5 = 100 : 0
pH 5,78±0,13a,A 4,49±0,16b,B 4,12±0,07c,C 3,86±0,09d,D 3,71±0,07e,E Total
Padatan Telarut (oBrix)
11,27±2,17d,D 12,20±2,21d,D 15,30±1,39c,C 17,87±0,61b,B 23,08±2,36a,A
Total
Asam (%) 0,30±0,18d,D 0,37±0,08c,C 0,42±0,10b,BC 0,44±0,10b,B 0,61±0,18a,A Kadar
Vitamin C
(mg/100g) 14,40±5,25d,D 16,67±6,71c,C 17,15±2,21c,C 24,11±1,79b,B 27,77±2,41a,A Kadar
Abu (%) 0,21±0,006a,A 0,19±0,008b,B 0,16±0,003c,C 0,14±0,002d,D 0,13±0,01e,D Keterangan : Angka dalam tabel merupakan rataan dari 3 ulangan, ± standard deviasi. Angka yang
diikuti dengan huruf yang berbeda dalam satu baris menunjukkan berbeda nyata (P<0,05) (huruf kecil) dan berbeda sangat nyata (P<0,01) (huruf besar) dengan uji LSR.
50 42
Tabel 9. Pengaruh konsentrasi gelatin yang ditambahkan pada es lilin terhadap karakteristik kimia yang diamati
Parameter Mutu Konsentrasi Gelatin (K)
K1 = 0% K2 = 0,2% K3 = 0,4%
pH 4,43±2,0a,A 4,36±2,35b,B 4,35±2,50c,C
Total Padatan Telarut
(oBrix) 15,79±14,20a,A 15,89±14,38a,A 16,35±14,48a,A Total Asam (%) 0,41±0,38b,A 0,42±0.32ab,A 0,45±0,40a,A Kadar Vitamin C
(mg/100g) 18,15±16,99c,B 20,37±18,28b,A 21,54±16,89a,A Kadar Abu (%) 0,16±0,04a,A 0,16±0,04a,A 0,17±0,05a,A
Keterangan : Angka dalam tabel merupakan rataan dari 3 ulangan, ± standard deviasi. Angka yang diikuti dengan huruf yang berbeda dalam satu baris menunjukkan berbeda nyata (P<0,05) (huruf kecil) dan berbeda sangat nyata (P<0,01) (huruf besar) dengan uji LSR.
pH
Perbandingan sari buah nenas dan wortel memberikan pengaruh yang berbeda sangat nyata (P<0,01) terhadap pH es lilin yang dihasilkan (Tabel 8) dan pengaruh konsentrasi gelatin yang ditambahkan memberikan pengaruh yang berbeda nyata (P<0,05) terhadap pH es lilin yang dihasilkan (Tabel 9). Interaksi antara jenis perbandingan sari buah nenas dan wortel dengan penambahan konsentrasi gelatin memberikan pengaruh yang berbeda nyata (P<0,05) terhadap pH es lilin seperti dapat dilihat pada Lampiran 7. Pengaruh interaksi antara perbandingan sari buah nenas dan wortel dengan penambahan gelatin terhadap pH es lilin dapat dilihat pada Gambar 6.
Dari Gambar 6 dapat dilihat bahwa es lilin dari sari buah nenas dan wortel dengan perbandingan S1 (0%:100%) dengan penambahan gelatin 0% (kontrol)