ABSTRAK
DWI FEBRIYANA. Konstruksi Marka Gen Plantaricin F
Lactobacillus
plantarum
. Dibimbing oleh DJAROT SASONGKO HAMI SENO dan
NOVIK
NURHIDAYAT.
Lactobacillus plantarum
merupakan bakteri yang dapat berperan sebagai
probiotik. Bakteri ini memiliki plantaricin F yang berguna menghambat
pertumbuhan bakteri Gram positif dan negatif. Penelitian ini menggunakan
sepuluh isolat
L. plantarum
(Mar A5, Bst 1, Mar C7, TB(N), Mg Tm 1, Mg PSM
B3, TB(S), MKw 9, Bst 5, Mar B4) yang berasal dari buah-buahan tropis (mangga
kweni, manggis, markisa, dan terong belanda). Penelitian ini dilakukan untuk
konstruksi marka gen
pln F
dan menganalisis ekspresi relatif gen
pln F
serta uji
aktivitas antibakteri. Pengujian gen
pln F
menggunakan RT-PCR menghasilkan
pita DNA berukuran 70 pb. Hasil pengujian ini selanjutnya dipakai untuk
menentukan nilai ekspresi relatif gen
pln F
menggunakan software
CS Analyzer.
Nilai ekspresi relatif gen tertinggi didapat dari isolat TB (S) dengan nilai 28.13
Au. Uji aktivitas antibakteri dilakukan untuk melihat hubungan antara gen
pln F
dengan aktivitas penghambatan isolat terhadap bakteri uji. Uji aktivitas antibakteri
dilakukan terhadap lima bakteri antara lain
Salmonella typhimurium
,
ABSTRACT
DWI FEBRIYANA.
Gene Marker Construction of Plantaricin F
Lactobacillus
plantarum
. Under the supervision of DJAROT SASONGKO HAMI SENO and
NOVIK NURHIDAYAT
masyarakat. Menurut Ogueke et al. (2010), probiotik merupakan mikroorganisme hidup yang dapat meningkatkan kesehatan inangnya. Mikroorganisme tersebut berguna bagi saluran pencernaan karena memiliki kemampuan dalam memperbaiki mikroflora di dalam usus. Mikroorganisme yang bermanfaat sebagai probiotik salah satunya berasal dari golongan bakteri asam laktat (Endaryanto & Harsono 2005). Sifat penting bakteri asam laktat yang berguna sebagai probiotik adalah aktivitasnya dalam menghasilkan beberapa metabolit antimikroba seperti asam organik (asam laktat, asam asetat, dan asam propionat), hidrogen peroksida (H2O2), bakteriosin, dan diasetil (Suskovic et al. 2001). Sifat ini dapat dimanfaatkan dalam menghambat bakteri patogen yang dapat menurunkan kesehatan inangnya (Rohmawati 2010).
Kebanyakan bakteri asam laktat yang digunakan sebagai probiotik berasal dari genus Lactobacillus sp. dengan spesies L. plantarum, L. casei, L. acidophilus, dan L. johnsonii (Ogueke et al. 2010). L. plantarum merupakan salah satu bakteri yang sering digunakan sebagai probiotik. Beberapa penelitian membuktikan bahwa L. plantarum dapat dijumpai pada buah-buahan dan sayur-sayuran. L. plantarum bisa terdapat pada buah-buahan tropis, seperti mangga, markisa, manggis (Widyastuti et al. 1998), dan belimbing (Lu et al. 2003).
Bakteri L. plantarum merupakan salah satu bakteri yang penting dalam bidang industri khususnya fermentasi (Moghadam et al. 2010), pengawetan makanan, dan keamanan pangan (Holo et al. 2001). Beberapa sifat yang menguntungkan dari L. plantarum antara lain kemampuannya yang dapat bertahan pada asam yang tinggi, dan mengeluarkan senyawa antimikroba misalnya bakteriosin (Moghadam et al. 2010). Bakteriosin merupakan protein yang dapat menghambat pertumbuhan mikroba (Prabowo 2010).
Bakteriosin yang terdapat pada L. plantarum dinamakan plantaricin. Beberapa karakteristik yang dimiliki plantaricin yaitu umumnya stabil pada suhu tinggi, kationik, hidrofobik, tahan pada asam yang tinggi (Holo et al. 2001), dan memiliki aktivitas antimikroba (Anderssen et al. 1998). Aktivitas antimikroba yang dihasilkan oleh plantaricin berbeda-beda, misalnya pada plantaricin W
Gram positif dan negatif adalah plantaricin F (Paynter et al. 1997).
Karakteristik yang dimiliki oleh plantaricin F yaitu memiliki 34 residu asam amino, berat 3545 Da, dan titik isoelektrik sebesar 10.7. Plantaricin ini dikode oleh gen pln F. Gen ini berada dalam satu operon dengan pln E dan pln I (Jorgenrud 2009). Bakteriosin ini dapat menghambat beberapa bakteri yang penting penyebab food borne disease, antara lain Listeria monocytogenes, Salmonella sp., Staphylococcus aureus, dan Pseudomonas aeruginosa (Paynter et al. 1997). Kemampuan penghambatan plantaricin ini memiliki spektrum penghambatan bakteri yang luas sehingga dapat menjadi probiotik yang baik.
Penelitian ini bertujuan konstruksi marka gen plantaricin F dengan melakukan perancangan primer untuk gen pln F dan menganalisis ekspresi relatif gen pln F pada isolat L. plantarum yang berasal dari buah-buahan tropis (mangga kweni, manggis, markisa, dan terong belanda). Selain itu, penelitian juga dilakukan untuk menguji aktivitas antibakteri terhadap bakteri uji antara lain Salmonella typhimurium, Staphylococcus aureus, Escherichia coli, Bacillus cureus, dan Pseudomonas flouresense. Hipotesis penelitian ini adalah tiap-tiap isolat yang membawa gen pln F memiliki aktivitas penghambatan terhadap bakteri Gram positif dan negatif. Hasil yang diharapkan dapat teridentifikasi adanya gen pln F pada seluruh isolat yang digunakan dan didukung dengan uji antibakteri L. plantarum sehingga dapat memberikan gambaran untuk dapat dijadikan probiotik yang baik.
TINJAUAN PUSTAKA
Lactobacillus plantarum
masyarakat. Menurut Ogueke et al. (2010), probiotik merupakan mikroorganisme hidup yang dapat meningkatkan kesehatan inangnya. Mikroorganisme tersebut berguna bagi saluran pencernaan karena memiliki kemampuan dalam memperbaiki mikroflora di dalam usus. Mikroorganisme yang bermanfaat sebagai probiotik salah satunya berasal dari golongan bakteri asam laktat (Endaryanto & Harsono 2005). Sifat penting bakteri asam laktat yang berguna sebagai probiotik adalah aktivitasnya dalam menghasilkan beberapa metabolit antimikroba seperti asam organik (asam laktat, asam asetat, dan asam propionat), hidrogen peroksida (H2O2), bakteriosin, dan diasetil (Suskovic et al. 2001). Sifat ini dapat dimanfaatkan dalam menghambat bakteri patogen yang dapat menurunkan kesehatan inangnya (Rohmawati 2010).
Kebanyakan bakteri asam laktat yang digunakan sebagai probiotik berasal dari genus Lactobacillus sp. dengan spesies L. plantarum, L. casei, L. acidophilus, dan L. johnsonii (Ogueke et al. 2010). L. plantarum merupakan salah satu bakteri yang sering digunakan sebagai probiotik. Beberapa penelitian membuktikan bahwa L. plantarum dapat dijumpai pada buah-buahan dan sayur-sayuran. L. plantarum bisa terdapat pada buah-buahan tropis, seperti mangga, markisa, manggis (Widyastuti et al. 1998), dan belimbing (Lu et al. 2003).
Bakteri L. plantarum merupakan salah satu bakteri yang penting dalam bidang industri khususnya fermentasi (Moghadam et al. 2010), pengawetan makanan, dan keamanan pangan (Holo et al. 2001). Beberapa sifat yang menguntungkan dari L. plantarum antara lain kemampuannya yang dapat bertahan pada asam yang tinggi, dan mengeluarkan senyawa antimikroba misalnya bakteriosin (Moghadam et al. 2010). Bakteriosin merupakan protein yang dapat menghambat pertumbuhan mikroba (Prabowo 2010).
Bakteriosin yang terdapat pada L. plantarum dinamakan plantaricin. Beberapa karakteristik yang dimiliki plantaricin yaitu umumnya stabil pada suhu tinggi, kationik, hidrofobik, tahan pada asam yang tinggi (Holo et al. 2001), dan memiliki aktivitas antimikroba (Anderssen et al. 1998). Aktivitas antimikroba yang dihasilkan oleh plantaricin berbeda-beda, misalnya pada plantaricin W
Gram positif dan negatif adalah plantaricin F (Paynter et al. 1997).
Karakteristik yang dimiliki oleh plantaricin F yaitu memiliki 34 residu asam amino, berat 3545 Da, dan titik isoelektrik sebesar 10.7. Plantaricin ini dikode oleh gen pln F. Gen ini berada dalam satu operon dengan pln E dan pln I (Jorgenrud 2009). Bakteriosin ini dapat menghambat beberapa bakteri yang penting penyebab food borne disease, antara lain Listeria monocytogenes, Salmonella sp., Staphylococcus aureus, dan Pseudomonas aeruginosa (Paynter et al. 1997). Kemampuan penghambatan plantaricin ini memiliki spektrum penghambatan bakteri yang luas sehingga dapat menjadi probiotik yang baik.
Penelitian ini bertujuan konstruksi marka gen plantaricin F dengan melakukan perancangan primer untuk gen pln F dan menganalisis ekspresi relatif gen pln F pada isolat L. plantarum yang berasal dari buah-buahan tropis (mangga kweni, manggis, markisa, dan terong belanda). Selain itu, penelitian juga dilakukan untuk menguji aktivitas antibakteri terhadap bakteri uji antara lain Salmonella typhimurium, Staphylococcus aureus, Escherichia coli, Bacillus cureus, dan Pseudomonas flouresense. Hipotesis penelitian ini adalah tiap-tiap isolat yang membawa gen pln F memiliki aktivitas penghambatan terhadap bakteri Gram positif dan negatif. Hasil yang diharapkan dapat teridentifikasi adanya gen pln F pada seluruh isolat yang digunakan dan didukung dengan uji antibakteri L. plantarum sehingga dapat memberikan gambaran untuk dapat dijadikan probiotik yang baik.
TINJAUAN PUSTAKA
Lactobacillus plantarum
mempunyai ukuran sekitar 0.5-10 µm (Suparman 2010).
Peranan L. plantarum sebagai antimikrobial dapat dimanfaatkan dalam fermentasi makanan karena L. plantarum toleran terhadap pH rendah dibandingkan dengan bakteri asam laktat lainnya (Lu et al. 2003). L. plantarum juga dapat memproduksi bakteriosin yang dapat berguna sebagai antimikrobial. Bakteriosin yang dihasilkan oleh Lactobacillus plantarum memiliki banyak jenis, misalnya plantaricin A, plantaricin F, plantaricin W, dan plantaricin NC8 (Cho et al. 2010).
Gambar 1 Lactobacillus plantarum (IGEM 2009).
Probiotik
Probiotik merupakan mikroorganisme bukan patogen yang jika digunakan akan memberikan pengaruh positif terhadap fisiologi dan kesehatan inangnya (Triana et al. 2006). Mikroorganisme ini dapat memperbaiki keseimbangan mikroflora usus. Keseimbangan yang baik dalam ekosistem mikrobiota usus dapat menguntungkan kesehatan. Beberapa karakteristik probiotik yang dapat digunakan antara lain, mempunyai kapasitas untuk bertahan hidup dan melakukan kolonisasi, mampu mempertahankan keseimbangan mikroflora usus yang sehat melalui kompetisi dan inhibisi mikroba patogen, menstimulasi sistem pertahanan tubuh, tidak bersifat toksik dan patogen, mempunyai karakteristik teknologi yang baik yaitu mampu bertahan selama penyimpanan dan penggunaan dalam bentuk preparat makanan yang didinginkan dan dikeringkan, agar dapat disediakan secara masal dalam industri (Aulia 2010).
Probiotik telah digunakan berabad-abad sebagai komponen bahan tambahan makanan. Terdapat tiga mekanisme kerja probiotik, yaitu menekan pertumbuhan mikroorganisme patogen pada saluran pencernaan melalui produksi substansi mikrob (asam laktat, asam asetat, asetaldehida, hidrogen peroksida, dan
bakteriosin), persaingan mendapatkan makanan, persaingan reseptor pada dinding usus; merubah metabolisme mikrobial dengan meningkatkan aktivitas enzim yang bermanfaat atau menekan aktivitas enzim yang tidak bermanfaat; dan merangsang pembentukkan kekebalan tubuh (Suskovic et al. 2001). Bakteri yang paling banyak digunakan sebagai probiotik berasal dari golongan bakteri asam laktat. Bakteri ini penting dalam pengawetan bahan makanan dan melawan bakteri patogen melalui pembentukan senyawa peptida antimikroba (Suparjo 2008).
Plantaricin F
Plantaricin merupakan bakteriosin yang dikeluarkan oleh L. plantarum (Cho et al. 2010). Plantaricin memilki banyak jenis, yaitu plantaricin A, plantaricin B, plantaricin C, plantaricin C19, plantaricin F, plantaricin EF, plantaricin T, plantaricin S, plantaricin 154, plantaricin SA 6, plantaricin KW30, plantaricin UGI, plantaricin 406. Masing-masing plantaricin memiliki aktivitas antimikroba yang berbeda-beda, misalnya pada plantaricin W dapat menghambat pertumbuhan bakteri Gram positif (Holo et al. 2001). Salah satu plantaricin yang memiliki aktivitas antimikroba pada bakteri Gram negatif dan bakteri gram positif adalah plantaricin F. Plantaricin ini memiliki kemampuan stabil pada suhu tinggi dan pH yang rendah sehingga dapat dimanfaatkan untuk keperluan fermentasi. Selain itu, mempunyai aktivitas dalam menghambat bakteri yang menyebabkan food borne disease, antara lain L. monocytogenes, Salmonella sp., P. aeroginosa, dan S. aureus (Paynter et al. 1997).
Mekanisme plantaricin F dalam menyerang inangnya adalah dengan cara membuat pori pada membran. Terdapat dua mekanisme utama, yairtu model barrel stave dan model carpet. Model barrel stave memiliki mekanisme yaitu peptida dari bakteriosin berasosiasi dengan membran target dan membentuk pori pada bagian lapisan lipid, sedangkan model carpet memiliki mekanisme dengan peptida dari bakteriosin tidak menembus bagian lipid bilayer tetapi membungkus membran target (Jorgenrud 2009).
Isolasi RNA
memiliki waktu paruh yang pendek, mudah rusak, dan mudah didegradasi oleh RNase (Wilson & Walker 2000). Secara umum terdapat tiga tahapan yaitu pemecahan sel dan solubilitas membran, isolasi dan pemurnian RNA, dan pemekatan RNA. Pemecahan sel dan solubilitas membran harus dilakukan secara cepat dan tuntas agar menginaktifkan kerja ribonuklease. Pemecahan sel dilakukan dengan menggunakan larutan sodium dedosil sulfat (SDS) 10% dan lisozim 5 mg/mL. SDS 10% merupakan deterjen anionik yang dapat digunakan untuk menghancurkan membran sel dari bakteri(Berg et al. 2005), sedangkan lisozim 5 mg/mL berfungsi untuk mendegradasi ikatan antara asam N-asetilmuramat dan N-asetil-D-glukosamin yang terdapat pada dinding sel bakteri (Murray et al. 2009). Pemurnian dilakukan dengan penambahan fenol dan kloroform yang bertujuan untuk penghilangan protein. Fenol merupakan senyawa yang dapat mendenaturasi protein (Pelczar & Chan 2005), sedangkan tahapan pemekatan dengan isopropanol dan etanol 70%.
Polymerase Chain Reaction
Polymerase Chain Reaction (PCR) adalah suatu metode in vitro untuk amplifikasi sejumlah fragmen DNA spesifik dengan panjang dan sekuen yang telah ditentukan dari sejumlah kecil cetakan (Wirawan 2004). Metode ini memungkinkan amplifikasi fragmen DNA yang diinginkan dengan sensitivitas dan selektivitas yang tinggi serta berlangsung dalam waktu yang cepat (McPherson & Moller 2006).
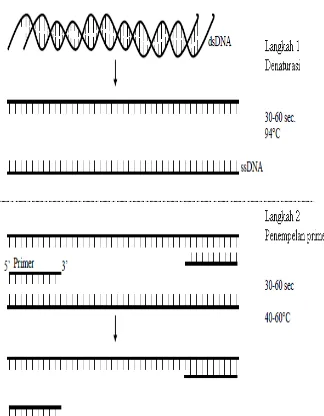
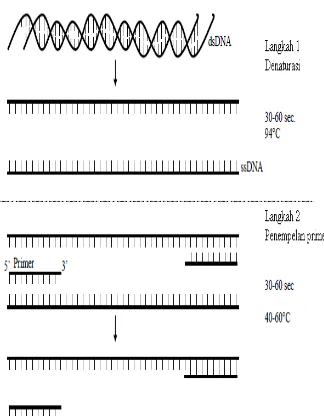
Proses PCR berlangsung dalam beberapa tahap, antara lain tahap denaturasi, penempelan primer, dan sintesis DNA. Tahap denaturasi dimulai DNA utas ganda diurai menjadi DNA utas tunggal dengan tahap proses pemanasan, biasanya suhu yang digunakan 94 OC. Suhu pada denaturasi dijaga pada waktu tertentu sampai DNA menjadi utas tunggal. Waktu tahap denaturasi berkisar 2-5 menit (McPherson & Moller 2006).
Tahap penempelan primer merupakan tahapan kedua dari proses PCR. Temperatur pada tahap ini diturunkan, hal ini dilakukan agar primer dapat menempel secara komplementer dengan templat atau cetakan. Tahapan ketiga dari proses PCR adalah tahap sintesis DNA. Tahapan ini biasanya memerlukan suhu sekitar 72 OC. Suhu ini merupakan suhu yang optimum bagi DNA polymerase dalam melakukan sintesis (Mc Pherson & Moller 2006). Penggunaan DNA
polymerase pada PCR menggunakan Taq polymerase termostabil yang diisolasi dari bakteri thermofilik Thermus aquaticus (Wirawan 2004). Seluruh proses ini dapat dilihat pada Gambar 2 dan 3 yang menjelaskan semua tahap mengenai proses PCR.
Komponen-komponen yang berperan dalam PCR antara lain primer, cetakan atau templat, bufer, dNTPs, dan Thermal Stable Polymerase. Primer dalam PCR terdiri atas sepasang primer dari oligonukleotida sintetik memulai sintesis DNA (Potter et al. 2007).
Gambar 2 Reaksi denaturasi dan penempelan primer pada proses PCR (Potter et al. 2007).
Reverse Transkriptase Polymerase Chain Reaction (RT-PCR)
Reverse Transcriptase Polymerase Chain Reaction (RT-PCR) merupakan metode yang digunakan untuk memperbanyak cDNA dari RNA yang digunakan sebagai cetakan. Metode ini memiliki keunggulan berupa sensitif, cepat, dan fleksibel terhadap gen target dan memberikan informasi mengenai gen target. Reaksi pada RT-PCR didasarkan atas kemampuan enzim reverse transcriptase dalam menghasilkan untai komplementer sehingga terbentuk cDNA dengan menggunakan m-RNA sebagai cetakan atau templat (McPherson & Moller 2006).
Tahapan pada RT-PCR awalnya, primer oligo-dT akan menempel pada bagian poli-A mRNA di ujung 5’. Tahapan berikutnya, terjadi pembentukan utas pertama dan dilakukan penambahan RNase H untuk menyingkirkan RNA serta enzim reverse transcriptase sehingga hasil yang diperoleh adalah cDNA. Molekul cDNA tersebut akan digunakan sebagai cetakan untuk proses PCR selanjutnya. Metode ini biasanya digunakan untuk menentukan ekspresi gen, atau identifikasi sekuen suatu transkripsi RNA, termasuk permulaan transkripsi dan daerah terminasi (Wilson 2000). Proses RT-PCR dijelaskan pada Gambar 4.
Gambar 4 Reaksi RT-PCR (Mc Pherson & Moller 2006).
Elektroforesis
Elektroforesis merupakan suatu teknik pemisahan molekul seluler berdasarkan ukuran dengan menggunakan medan listrik yang dialirkan pada suatu medium yang mengandung sampel yang dipisahkan. Teknik ini dapat digunakan dengan memanfaatkan muatan listrik yang ada pada makromolekul. Teknik elektroforesis dapat digunakan untuk analisis DNA, RNA, maupun protein. Jika
suatu molekul yang bermuatan negatif dilewatkan melalui suatu medium, misalnya gel agarosa, lalu dialirkan arus listrik dari satu kutub ke kutub yang berlawanan muatan maka molekul tersebut akan bergerak dari kutub negatif ke kutub positif (Yuwono 2005).
Elektroforesis berlangsung dalam gel agarosa sebagai medium pemisahan molekul. Molekul DNA atau RNA bermigasi berdasarkan ukuran dan bentuk. Molekul kecil akan berpindah lebih cepat dibandingkan dengan molekul yang lebih besar. Ukuran DNA yang tidak diketahui saat migrasi bisa dibandingkan dengan penanda (Potter et al. 2007).
Elektroforesis dapat digunakan untuk analisis DNA menggunakan gel agarosa. Gel agarosa merupakan suatu bahan semi padat berupa polisakarida yang diekstraksi dari rumput laut. Gel agarosa dibuat dengan melarutkannya pada bufer dan dibantu dengan proses pemanasan. Larutan bufer yang digunakan biasanya menggunakan tris asetat-EDTA (TAE) atau tris borat asetat-EDTA (TBE). Larutan elektroforesis yang telah dicampurkan dengan bufer dan melalui proses pemanasan dituang dalam lempeng dan ditancapkan sisir agar terbentuk lubang-lubang kecil untuk tempat memasukkan sampel. Gel agarosa yang telah terbentuk direndam dalam tangki bersama bufer yang digunakan untuk membuat gel (Yuwono 2005).
Hasil elektroforesis dapat dilihat secara visual dengan menggunakan EtBr (ethidium bromida) dan sinar ultra violet (UV). Ethidium bromida merupakan suatu intercalating agent yang biasanya digunakan dalam mewarnai asam nukleat. Biasanya hasil elektroforesis bila diwarnai dalam EtBr akan berwarna merah keunguan. Senyawa ini mempunyai rumus kimia C21H20BrN3 yang bersifat mutagen sehingga dapat menyebabkan iritasi. Selain itu, senyawa ini bersifat karsinogenik (Lun & Sansone 1987).
Perancangan Primer
(http://www.invitrogen.com/ ) (McPherson & Moller 2006).
Situs lain dalam perancangan primer adalah www.ncbi.nlm.nih.gov, dalam situs ini terdapat BLAST. BLAST merupakan program pencarian kesamaan yang didesain untuk mengeksplorasi semua database sekuen yang diminta, baik itu berupa DNA atau protein. Program BLAST juga dapat digunakan untuk mendeteksi hubungan diantara sekuen pada daerah tertentu yang memiliki kesamaan atau homologi (Aprijani & Efaizi 2004). Peranan BLAST dalam desain primer salah satunya untuk pencarian basis data berdasarkan pada hasil pensejajaran sekuen yang berasal DNA maupun protein. Selain itu, dapat digunakan untuk mengidentifikasi homolog dari molekul baru. Beberapa kriteria dari primer, antara lain % G dan C lebih dari 50%, tidak memiliki kemungkinan saling komplemen antara basa dalam satu rantai primer atau primer lainnya, memiliki 18-25 pasang basa, tidak membentuk primer dimer, waktu melting temperature (Tm) tidak melebihi 700C (Sambrook & Russel 2001).
BAHAN DAN METODE
Alat dan Bahan
Peralatan yang digunakan pada penelitian ini adalah autoklaf, laminar air flow, pipet mikro, cawan Petri, tabung reaksi, inkubator, oven, labu Erlenmeyer, dan spektrofotometer. Alat-alat lain yang digunakan adalah tabung Eppendorf, waterbath, sentrifus 5415 R, termometer, gelas piala, Takara PCR Thermal cycler, elektroforesis ATTO, printgraph ATTO, kertas uji, pinset, densitometer dengan program CS Analyzer, dan gunting.
Tabel 1 Isolat L. plantarum yang digunakan
Kode isolat Asal isolate
Mar A5 Markisa
Bst 1 Manggis
MarC7 Markisa
TB (N) Terong Belanda
Mg Tm 1 Manggis
Mg PSM B3 Manggis
TB(S) Terong Belanda
Mkw 9 Mangga kweni
Bst 5 Manggis
Mar B4 Markisa
Bahan yang digunakan antara lain media glucose yeast extract (GYP), 10 Isolat Lactobacillus plantarum yang berasal dari berbagai macam buah (Tabel 1), 5 isolat bakteri uji (Salmonella typhimurium, Staphylococcus aureus, Escherichia coli, Bacillus cureus, dan Pseudomonas flouresense), potassium asetat, kloramfenikol 30 µg, fenol stop (5% fenol jenuh dalam 95% etanol absolut), kloroform, isopropanol, lisozim 5 mg/mL, SDS 10%, bufer TE pH 8, aqua bidestilata steril, etanol 70%, etanol absolut. Bahan lain yang digunakan adalah Agarosa, bufer Tris Acid EDTA (TAE) 1X, SuperScript III One-Step RT-PCR with Platinum Taq Invitrogen dan, Diethylpyrocarbonat (DEPC).
Metode
Perancangan Primer
Perancangan primer dilakukan dengan mencari sekuen dari plantaricin F menggunakan http:www.ncbi.nlm.nih.gov/
.
Sekuen yang diambil adalah sekuen yang menyandikan gen tersebut. Kehomologian sekuen dicari dengan program BLAST untuk menentukan daerah yang terkonservasi. Daerah yang terkonservasi adalah daerah yang memiliki homologi yang signifikan dengan gen yang berfungsi sama pada spesies lain. Daerah terkonservasi didapatkan setelah melakukan pensejajaran atau multiple aligment dengan Crustal W2 yang dapat digunakan pada situs http:www.ebi.ac.uk. Primer yang dibuat harus memiliki syarat umum yaitu % G dan C lebih dari 50%, tidak memiliki kemungkinan saling komplemen antara basa dalam satu rantai primer atau primer lainnya, memiliki 18-25 pasang basa, tidak membentuk primer dimer, waktu melting temperature (Tm) tidak melebihi 700C (Sambrook & Russel 2001). Hasil rancangan diuji menggunakan bantuan program komputer yaitu gene runner.
Pembuatan Media Glucose Yeast Extract-Peptone (GYP) (Triana et al. 2006)
(http://www.invitrogen.com/ ) (McPherson & Moller 2006).
Situs lain dalam perancangan primer adalah www.ncbi.nlm.nih.gov, dalam situs ini terdapat BLAST. BLAST merupakan program pencarian kesamaan yang didesain untuk mengeksplorasi semua database sekuen yang diminta, baik itu berupa DNA atau protein. Program BLAST juga dapat digunakan untuk mendeteksi hubungan diantara sekuen pada daerah tertentu yang memiliki kesamaan atau homologi (Aprijani & Efaizi 2004). Peranan BLAST dalam desain primer salah satunya untuk pencarian basis data berdasarkan pada hasil pensejajaran sekuen yang berasal DNA maupun protein. Selain itu, dapat digunakan untuk mengidentifikasi homolog dari molekul baru. Beberapa kriteria dari primer, antara lain % G dan C lebih dari 50%, tidak memiliki kemungkinan saling komplemen antara basa dalam satu rantai primer atau primer lainnya, memiliki 18-25 pasang basa, tidak membentuk primer dimer, waktu melting temperature (Tm) tidak melebihi 700C (Sambrook & Russel 2001).
BAHAN DAN METODE
Alat dan Bahan
Peralatan yang digunakan pada penelitian ini adalah autoklaf, laminar air flow, pipet mikro, cawan Petri, tabung reaksi, inkubator, oven, labu Erlenmeyer, dan spektrofotometer. Alat-alat lain yang digunakan adalah tabung Eppendorf, waterbath, sentrifus 5415 R, termometer, gelas piala, Takara PCR Thermal cycler, elektroforesis ATTO, printgraph ATTO, kertas uji, pinset, densitometer dengan program CS Analyzer, dan gunting.
Tabel 1 Isolat L. plantarum yang digunakan
Kode isolat Asal isolate
Mar A5 Markisa
Bst 1 Manggis
MarC7 Markisa
TB (N) Terong Belanda
Mg Tm 1 Manggis
Mg PSM B3 Manggis
TB(S) Terong Belanda
Mkw 9 Mangga kweni
Bst 5 Manggis
Mar B4 Markisa
Bahan yang digunakan antara lain media glucose yeast extract (GYP), 10 Isolat Lactobacillus plantarum yang berasal dari berbagai macam buah (Tabel 1), 5 isolat bakteri uji (Salmonella typhimurium, Staphylococcus aureus, Escherichia coli, Bacillus cureus, dan Pseudomonas flouresense), potassium asetat, kloramfenikol 30 µg, fenol stop (5% fenol jenuh dalam 95% etanol absolut), kloroform, isopropanol, lisozim 5 mg/mL, SDS 10%, bufer TE pH 8, aqua bidestilata steril, etanol 70%, etanol absolut. Bahan lain yang digunakan adalah Agarosa, bufer Tris Acid EDTA (TAE) 1X, SuperScript III One-Step RT-PCR with Platinum Taq Invitrogen dan, Diethylpyrocarbonat (DEPC).
Metode
Perancangan Primer
Perancangan primer dilakukan dengan mencari sekuen dari plantaricin F menggunakan http:www.ncbi.nlm.nih.gov/
.
Sekuen yang diambil adalah sekuen yang menyandikan gen tersebut. Kehomologian sekuen dicari dengan program BLAST untuk menentukan daerah yang terkonservasi. Daerah yang terkonservasi adalah daerah yang memiliki homologi yang signifikan dengan gen yang berfungsi sama pada spesies lain. Daerah terkonservasi didapatkan setelah melakukan pensejajaran atau multiple aligment dengan Crustal W2 yang dapat digunakan pada situs http:www.ebi.ac.uk. Primer yang dibuat harus memiliki syarat umum yaitu % G dan C lebih dari 50%, tidak memiliki kemungkinan saling komplemen antara basa dalam satu rantai primer atau primer lainnya, memiliki 18-25 pasang basa, tidak membentuk primer dimer, waktu melting temperature (Tm) tidak melebihi 700C (Sambrook & Russel 2001). Hasil rancangan diuji menggunakan bantuan program komputer yaitu gene runner.
Pembuatan Media Glucose Yeast Extract-Peptone (GYP) (Triana et al. 2006)
Bahan-bahan ditimbang dan dimasukkan ke dalam gelas piala 1 L. Ditambahkan dH2O sampai dengan 200 mL lalu diaduk sampai homogen. Campuran dipanaskan dan diaduk dengan pengaduk stirer. Sebelum dipindahkan ke dalam cawan Petri terlebih dahulu campuran disterilisasi dengan autoklaf pada suhu 121 0 C selama 15 menit. Media yang telah mengalami proses sterilisasi dipindahkan ke dalam cawan Petri yang telah disterilkan dan dibiarkan hingga membeku. Media GYP yang telah membeku siap digunakan untuk menumbuhkan bakteri.
Pembuatan media GYP cair dilakukan dengan mencampurkan semua bahan kecuali agar dan CaCO3 ke dalam labu Erlenmeyer dan dikocok dengan pengaduk magnetik hingga homogen. Setelah itu dibagi rata ke dalam beberapa tabung reaksi sebanyak 5 mL dan ditutup dengan sumbat kapas. Media cair GYP ini kemudian disterilkan dengan autoklaf pada suhu 1210C selama 15 menit dan digunakan untuk kultivasi bakteri.
Kultivasi Bakteri
Isolat bakteri L. plantarum yang digunakan untuk isolasi RNA terdapat pada Tabel 1. Biakan bakteri yang telah disiapkan digores sebanyak satu ose dalam media GYP padat. Pekerjaan ini dilakukan dalam laminar air flow secara aseptik. Media GYP padat kemudian diinkubasi dalam inkubator selama 24-48 jam pada suhu 370C. Hasil yang terbentuk berupa koloni tunggal yang menunjukkan bahwa koloni tersebut murni. Biakan murni yang tumbuh pada media padat dipindahkan dalam media cair. Pekerjaan ini juga dilakukan dalam Laminar air flow. Media kemudian diinkubasi selama 12-18 jam pada suhu 370C. Hasilnya dapat dilakukan pemanenan sel yang dapat digunakan untuk proses isolasi RNA.
Isolasi Total RNA (Sambrook et al. 1989) Prosedur isolasi total RNA dimulai dengan pemanenan L. plantarum. Kultur bakteri yang telah tumbuh dalam media cair dipindahkan dalam tabung Eppendorf 2 mL dan disentrifus 7000 rpm selama 5 menit. Pelet yang terbentuk ditambahkan dengan 1 mL fenol stop (5% fenol jenuh dalam 95% etanol absolut) dan dicampurkan hingga homogen. Campuran tersebut disentrifus 8000 rpm selama 5 menit.
Pelet yang terbentuk ditambahkan dengan 800 µL lisozim 5 mg/mL lalu dihomogenkan dengan cara dibolak-balik dan di-vortex. Campuran diinkubasi pada suhu 370C selama
15 menit dan ditambahkan 300 µL SDS 10% lalu dihomogenkan kembali. Campuran tersebut diinkubasi kembali pada suhu 650C selama 3 menit dan ditambahkan 200 µL potassium asetat. Campuran tersebut kemudian dipanaskan pada suhu 800C-900C selama 5 menit dan disimpan dalam ice box selama 3 menit. kemudian sebanyak 80 µL hot phenol ditambahkan dalam campuran tersebut.
Campuran dipanaskan pada suhu 800 C-900C selama 5 menit dan disentrifus selama 5 menit pada 8000 rpm. Supernatan diambil dan ditambahkan kloroform dengan perbandingan 1:1 dan dibolak-balik. Campuran disentrifus 8000 rpm selama 5 menit sehingga terbentuk dua lapisan. Lapisan atas diambil dan ditambahkan 500 µL isopropanol lalu dibolak-balik. Hasilnya disentrifus 8000 rpm selama 5 menit. Pelet yang terbentuk ditambahkan sebanyak 500 µL etanol 70% dan disentrifus 8000 rpm selama 5 menit. Tahapan penambahan etanol 70% dilakukan sebanyak dua kali. Pelet yang terbentuk dikeringkan sampai tidak terdapat etanol. Bila sudah kering ditambahkan 50 µL DEPC 0.1%. Hasil isolasi dicek menggunakan agarosa 1.5%.
Pengukuran Kualitas RNA (Microarrays 2000)
Kualitas RNA dapat diukur menggunakan alat spektrofotometer pada panjang gelombang 260 nm/280 nm. Sampel RNA sebanyak 10 µL diambil dan ditambahkan 990 µL air yang telah mendapat perlakuan Diethylpyrocarbonat (DEPC). Kuvet yang digunakan dalam keadaan bersih dari kontaminasi RNase. Baca absorban pada 260 nm/280 nm.
Reverse Transcriptase Polymerase Chain Reaction (RT-PCR) (Invitrogen 2007)
menit, dan 1 siklus 40C. Hasil disimpan pada suhu -200C.
Elektroforesis Hasil PCR
Elektroforesis hasil PCR dimulai dengan menyiapkan agarosa 2%. Sebanyak 2.6 gram agarosa ditimbang dan dilarutkan dalam 130 mL TAE 1X. Campuran kemudian dipanaskan dalam microwave. Campuran ditempatkan pada bak elektroforesis yang telah disusun. Agarosa yang dapat digunakan bila sudah keras. Elektroforesis sampel selama 60 menit pada 100 volt. Hasil dapat dilihat di alat Printgraph ATTO .
Pengukuran Ekspresi gen pln F
(Nurhidayat 2010)
Pengukuran ekspresi gen pln F menggunakan software CS Analyzer. Cara kerja CS Analyser adalah setelah dilakukan analisis elektroforesis gel agarosa, data hasil elektroforesis berupa gambar di scanner dan diubah menjadi data digital untuk mencari data yang diperlukan. Proses perhitungan dimulai dengan mengitung 1 µL RNA dari RNA total dan RNA produk yang dielektroforesis dari hasil CS Analyzer. Hasil yang didapatkan akan menghasilkan ekspresi gen dari plantaricin F dan 16s RNA.
Ekspresi gen
Hasil perhitungan dari ekspresi gen pln F dan 16s RNA dapat menjelaskan ekspresi relatif gen pln F yang terdapat pada masing-masing isolat.
Uji Aktivitas Antibakteri (Gong et al. 2010) Kultur cair dari sepuluh isolat L. plantarum disiapkan dalam tabung Eppendorf ukuran 2 mL dan disentrifus 12000 rpm selama 3 menit. Supernatan yang dihasilkan digunakan pada uji aktivitas. Lalu disiapkan media padat GYP dan dibuat tanda pada cawan Petri untuk kontrol positif, kontrol negatif, dan sampel. Tahapan selanjutnya, bakteri patogen yang telah ditumbuhkan dalam media cair disebar dalam media GYP padat sebanyak 100 µL. Bakteri patogen yang digunakan ialah Escherichia coli, Salmonella typhimurium, Staphylococcus aureus, Pseudomonas flouresense, dan Bacillus cureus. Kertas uji yang telah direndam di dalam isolat Lactobacillus plantarum ditempatkan pada cawan Petri yang telah
diberi tanda. Kontrol positif yang digunakan pada percobaan ini adalah kloramfenikol dan kontrol negatif ialah akuades steril. Lalu inkubasi dalam inkubator selama 1 hari pada suhu 370C.
Pengukuran Aktivitas Antibakteri (Gong et al. 2010)
Hasil dari uji aktivitas yang telah diinkubasi selama satu malam dilihat aktivitas penghambatannya. Aktivitasnya dapat dilihat apabila dari masing-masing sampel yang diuji dapat menghasilkan zona bening. Zona bening yang dihasilkan diukur diameternya dengan menggunakan penggaris. Semakin besar diameter zona bening maka akan semakin tinggi aktivitas penghambatan dari bakteri tersebut. Hasilnya dikoreksi dengan kontrol, yaitu ukuran kertas uji sebesar 0.6 cm.
Diameter Penghambatan
HASIL DAN PEMBAHASAN
RNA Total Lactobacillus plantarum
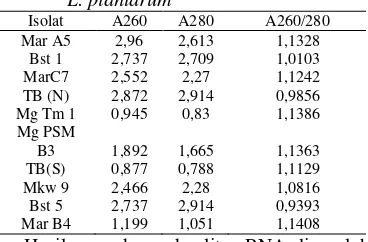
Isolasi RNA total menggunakan elektroforesis gel agarosa 1.5%. Hasil menunjukkan RNA total dari sepuluh isolat L. plantarum yang digunakan dalam percobaan telah berhasil diisolasi. Kualitas RNA yang telah diisolasi diukur menggunakan metode spektrofotometri. Pengukuran kualitas RNA ini sangat diperlukan karena kualitas RNA yang baik akan mempengaruhi keberhasilan sintesis cDNA (Invitrogen 2007).
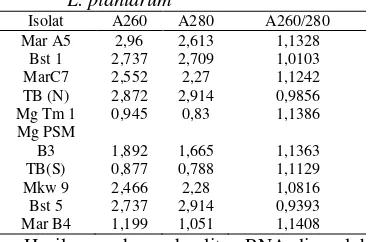
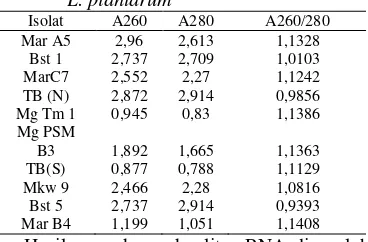
Tabel 2 Kuantifikasi RNA dari sepuluh isolat L. plantarum
Isolat A260 A280 A260/280
Mar A5 2,96 2,613 1,1328
Bst 1 2,737 2,709 1,0103
MarC7 2,552 2,27 1,1242
TB (N) 2,872 2,914 0,9856
Mg Tm 1 0,945 0,83 1,1386
Mg PSM
B3 1,892 1,665 1,1363
TB(S) 0,877 0,788 1,1129
Mkw 9 2,466 2,28 1,0816
Bst 5 2,737 2,914 0,9393
Mar B4 1,199 1,051 1,1408
menit, dan 1 siklus 40C. Hasil disimpan pada suhu -200C.
Elektroforesis Hasil PCR
Elektroforesis hasil PCR dimulai dengan menyiapkan agarosa 2%. Sebanyak 2.6 gram agarosa ditimbang dan dilarutkan dalam 130 mL TAE 1X. Campuran kemudian dipanaskan dalam microwave. Campuran ditempatkan pada bak elektroforesis yang telah disusun. Agarosa yang dapat digunakan bila sudah keras. Elektroforesis sampel selama 60 menit pada 100 volt. Hasil dapat dilihat di alat Printgraph ATTO .
Pengukuran Ekspresi gen pln F
(Nurhidayat 2010)
Pengukuran ekspresi gen pln F menggunakan software CS Analyzer. Cara kerja CS Analyser adalah setelah dilakukan analisis elektroforesis gel agarosa, data hasil elektroforesis berupa gambar di scanner dan diubah menjadi data digital untuk mencari data yang diperlukan. Proses perhitungan dimulai dengan mengitung 1 µL RNA dari RNA total dan RNA produk yang dielektroforesis dari hasil CS Analyzer. Hasil yang didapatkan akan menghasilkan ekspresi gen dari plantaricin F dan 16s RNA.
Ekspresi gen
Hasil perhitungan dari ekspresi gen pln F dan 16s RNA dapat menjelaskan ekspresi relatif gen pln F yang terdapat pada masing-masing isolat.
Uji Aktivitas Antibakteri (Gong et al. 2010) Kultur cair dari sepuluh isolat L. plantarum disiapkan dalam tabung Eppendorf ukuran 2 mL dan disentrifus 12000 rpm selama 3 menit. Supernatan yang dihasilkan digunakan pada uji aktivitas. Lalu disiapkan media padat GYP dan dibuat tanda pada cawan Petri untuk kontrol positif, kontrol negatif, dan sampel. Tahapan selanjutnya, bakteri patogen yang telah ditumbuhkan dalam media cair disebar dalam media GYP padat sebanyak 100 µL. Bakteri patogen yang digunakan ialah Escherichia coli, Salmonella typhimurium, Staphylococcus aureus, Pseudomonas flouresense, dan Bacillus cureus. Kertas uji yang telah direndam di dalam isolat Lactobacillus plantarum ditempatkan pada cawan Petri yang telah
diberi tanda. Kontrol positif yang digunakan pada percobaan ini adalah kloramfenikol dan kontrol negatif ialah akuades steril. Lalu inkubasi dalam inkubator selama 1 hari pada suhu 370C.
Pengukuran Aktivitas Antibakteri (Gong et al. 2010)
Hasil dari uji aktivitas yang telah diinkubasi selama satu malam dilihat aktivitas penghambatannya. Aktivitasnya dapat dilihat apabila dari masing-masing sampel yang diuji dapat menghasilkan zona bening. Zona bening yang dihasilkan diukur diameternya dengan menggunakan penggaris. Semakin besar diameter zona bening maka akan semakin tinggi aktivitas penghambatan dari bakteri tersebut. Hasilnya dikoreksi dengan kontrol, yaitu ukuran kertas uji sebesar 0.6 cm.
Diameter Penghambatan
HASIL DAN PEMBAHASAN
RNA Total Lactobacillus plantarum
Isolasi RNA total menggunakan elektroforesis gel agarosa 1.5%. Hasil menunjukkan RNA total dari sepuluh isolat L. plantarum yang digunakan dalam percobaan telah berhasil diisolasi. Kualitas RNA yang telah diisolasi diukur menggunakan metode spektrofotometri. Pengukuran kualitas RNA ini sangat diperlukan karena kualitas RNA yang baik akan mempengaruhi keberhasilan sintesis cDNA (Invitrogen 2007).
Tabel 2 Kuantifikasi RNA dari sepuluh isolat L. plantarum
Isolat A260 A280 A260/280
Mar A5 2,96 2,613 1,1328
Bst 1 2,737 2,709 1,0103
MarC7 2,552 2,27 1,1242
TB (N) 2,872 2,914 0,9856
Mg Tm 1 0,945 0,83 1,1386
Mg PSM
B3 1,892 1,665 1,1363
TB(S) 0,877 0,788 1,1129
Mkw 9 2,466 2,28 1,0816
Bst 5 2,737 2,914 0,9393
Mar B4 1,199 1,051 1,1408
kemurnian RNA terhadap kontaminasi protein. Nilai yang diharapkan dari pengukuran ini berkisar 1.8-2.1. (Sambrook & Russel 2001). Hasil pengukuran dapat dilihat pada Tabel 2. Hasil pengukuran kuantitas RNA menunjukkan bahwa sampel yang diisolasi tidak memiliki kemurnian yang tinggi terhadap kontaminasi dari protein atau pengotor lain. Kontaminasi protein atau pengotor lain dapat terjadi pada saat ekstraksi dengan kloroform tidak efisien dalam menghilangkan protein ataupun pengotor lain (Song et al. 2011).
Terdapat beberapa tahapan dalam isolasi RNA total, antara lain pemecahan membran dan solubilisasi membran, isolasi dan pemurnian RNA, dan pemekatan RNA. Seluruh tahapan ini memerlukan alat-alat seperti Eppendorf, tip, dan seluruh alat-alat gelas yang telah mendapatkan perlakuan DEPC. DEPC berfungsi untuk menginaktifkan RNase yang dapat mendegradasi RNA yang akan diisolasi pada percobaan.
Gambar 5 Elektroforegram Total RNA L.plantarum.
Hasil Perancangan Primer
Konstruksi marka gen plantaricin F dilakukan dengan perancangan primer. Sepasang primer yang spesifik digunakan untuk amplifikasi gen pln F dengan RT-PCR. Sekuen primer yang digunakan dapat mempengaruhi spesifitas dan sensitivitas reaksi dalam RT-PCR. Primer yang digunakan dirancang menggunakan situs NCBI dari daerah yang terkonservasi untuk gen pln F
dan 16s RNA. Hasil dari perancangan primer dapat dilihat pada Tabel 3.
Primer forward dan reverse dirancang berdasarkan kriteria primer yang dapat digunakan untuk amplifikasi, antara lain memiliki panjang primer berkisar 18-25 pasang basa, memiliki Tm tidak melebihi suhu 700C, % GC sekitar 40-60%, dan antara primer forward dan reverse tidak saling komplemen (Sambrook & Russel 2001). Sekuen yang dirancang terdapat pada Tabel 3. Hasil perancangan primer ini bila dianalisis dengan program Gene Runner akan didapatkan data, yaitu pada primer forward pln F terdapat kemungkinan dimer sekitar 6 pb dan tidak terdapat kemungkinan untuk internal loops dan hairpin loops. Pada primer reverse terdapat 3 hairpin loop, dimer sekitar 4 pb, dan internal loop sekitar 8 pb.
Hasil dari perancangan primer gen pln F ini diharapkan akan dapat menghasilkan produk sekitar 70 pb. Hal ini berdasarkan sekuen yang dapat diapit oleh primer. Perancangan primer ini menggunakan sekuen dengan panjang 156 pb. Pada primer forward sekuen dirancang dari urutan 58 sampai dengan urutan 79, sedangkan primer reverse dirancang dari urutan 127 sampai 107. Hal lain yang harus diperhatikan adalah primer yang dihasilkan. Primer ini menentukan suhu dalam penempelan primer pada proses PCR. Suhu penempelan primer terletak 2-10 dibawah nilai melting tempetrature (Tm) dari primer (Sambrook & Russel 2001). Primer 16s RNA merupakan primer universal. Primer ini digunakan sebagai kontrol positif dalam percobaan ini.
Amplikon dan Ekspresi Gen Pln F dengan RT-PCR
Amplifikasi gen pln F menggunakan sepuluh isolat L. plantarum dengan metode RT-PCR. Primer yang digunakan adalah primer gen pln F dan 16s RNA. Primer 16s RNA berfungsi sebagai kontrol positif dalam reaksi ini. 16s RNA merupakan salah satu ribosomal RNA dan hanya terdapat pada prokariot. 70s RNA yang terdapat dalam prokariot terdiri atas dua subunit, yaitu 30s dan 50s. Komponen dari 30s RNA terdiri atas 16s RNA dan 21 protein (Garrett & Grisham 2007)
Tahap awal dari proses RT-PCR adalah sintesis cDNA yang berasal dari sampel RNA dengan menggunakan m-RNA sebagai cetakan (Hogg 2005). Program yang digunakan dalam reaksi RT-PCR, antara lain
1 2 3 4 5 6 7 8 9 10
Ket: 1= Mar A5 6 = Mg PSM B3 2= Bst 1 7 = TB (S) 3= Mar C7 8 = Mkw 9 4= TB (N) 9 = Bst 5 5= Mg Tm 1 10 = Mar B4 RNA
1 siklus 550C selama 30 menit digunakan untuk sintesis cDNA dari RNA hasil isolasi, 1 siklus 940C selama 4 menit berfungsi dalam tahapan denaturasi atau pemutusan ikatan ganda dari RNA. Selanjutnya, amplifikasi dari PCR dengan menggunakan program 40 siklus yang terdiri atas 940C selama 30 detik untuk denaturasi, 550C selama 30 detik untuk penempelan primer, 720C selama 1 menit untuk sintesis DNA. Tahap akhir dari reaksi adalah 1 siklus 720C selama 7 menit yang digunakan untuk sintesis DNA tahap akhir, dan 1 siklus 40C untuk menjaga agar DNA hasil PCR tidak rusak (Invitrogen 2007).
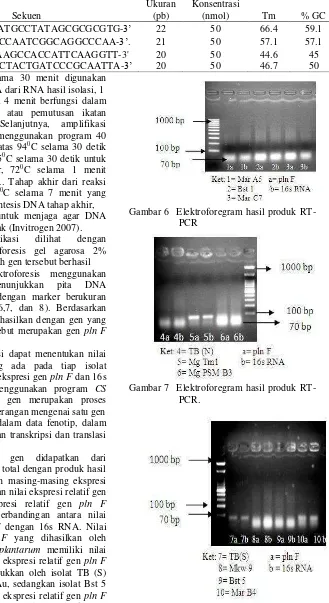
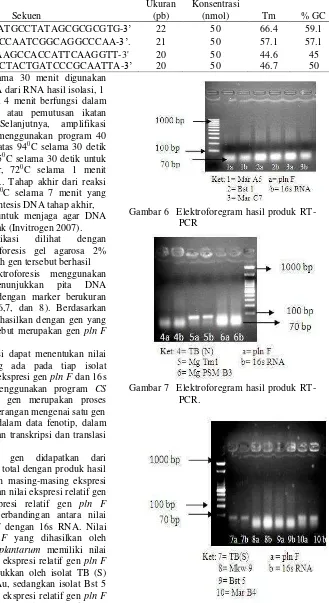
Hasil amplifikasi dilihat dengan melakukan elektroforesis gel agarosa 2% untuk melihat apakah gen tersebut berhasil diamplifikasi. Elektroforesis menggunakan agarosa 2% menunjukkan pita DNA berukuran 70 pb dengan marker berukuran 100 pb (Gambar 6,7, dan 8). Berdasarkan ukuran pita yang dihasilkan dengan gen yang dirancang, gen tersebut merupakan gen pln F yang diinginkan.
Hasil amplifikasi dapat menentukan nilai ekspresi gen yang ada pada tiap isolat L.plantarum. Nilai ekspresi gen pln F dan 16s RNA dianalisis menggunakan program CS Analyzer. Ekspresi gen merupakan proses yang membawa keterangan mengenai satu gen atau lebih gen ke dalam data fenotip, dalam proses ini melibatkan transkripsi dan translasi (Smith et al. 2000).
Hasil ekspresi gen didapatkan dari elektroforesis RNA total dengan produk hasil RT-PCR. Penentuan masing-masing ekspresi ini dapat menentukan nilai ekspresi relatif gen pln F. Nilai ekspresi relatif gen pln F merupakan nilai perbandingan antara nilai ekspresi gen pln F dengan 16s RNA. Nilai ekspresi gen pln F yang dihasilkan oleh sepuluh isolat L. plantarum memiliki nilai berbeda-beda. Nilai ekspresi relatif gen pln F paling tinggi ditunjukkan oleh isolat TB (S) dengan nilai 28.3 Au, sedangkan isolat Bst 5 tidak memiliki nilai ekspresi relatif gen pln F (Gambar 9). Perhitungan dari nilai ekspresi relatif gen pln F terdapat pada Lampiran 6.
Gambar 6 Elektroforegram hasil produk RT- PCR
Gambar 7 Elektroforegram hasil produk RT-PCR.
Gambar 8 Elektroforegram hasil produk RT- PCR.
Sekuen
Ukuran (pb)
Konsentrasi
(nmol) Tm % GC
pln FF:5’-TTCCATGCCTATAGCGCGCGTG-3’ 22 50 66.4 59.1
pln F R: 5’-TGATCCAATCGGCAGGCCCAA-3’. 21 50 57.1 57.1
16S RNA F: 5’-CAAGCCACCATTCAAGGTT-3' 20 50 44.6 45
16S RNA R: 5’pln F R: 5’F:5’ -CCCTACTGATCCCGCAATTA-3’.3’3’ 20 50 46.7 50
16S RNA F: 5’
Gambar 9 Tingkat ekspresi relatif gen pln F dari masing-masing isolat L. plantarum.
Aktivitas Antibakteri Isolat L. plantarum
Terhadap Bakteri Uji
Pengujian aktivitas sepuluh isolat L. plantarum dilakukan terhadap lima bakteri yang mewakili hasil perwarnaan Gram yang berbeda, yaitu bakteri Gram positif dan negatif. Bakteri Gram positif yang diujikan adalah Staphylococcus aureus dan Bacillus cureus. Bakteri Gram negatif yang diujikan antara lain Escherichia coli, Salmonella typhimurium, Pseudomonas flourosense.
Gambar 10 Hasil uji daya hambat isolat L. plantarum terhadap pertumbuhan bakteri P. flouresense dan E. coli.
Pengujian didasarkan atas pembentukan zona bening disekitar kertas uji yang memiliki diameter sekitar 0.6 cm (Gambar 10). Menurut Paynter et al. (2007) isolat yang mengandung plantaricin F dapat menghambat pertumbuhan bakteri Gram positif dan bakteri Gram negatif. Proses penghambatan
plantaricin F dalam menghambat pertumbuhan bakteri dengan menggunakan mekanisme barrel stave. Pada mekanisme ini plantaricin akan berikatan dengan membran target dan membentuk pori sehingga membran target menjadi rusak (Jorgenrud 2009).
Sepuluh isolat pengujian aktivitas L. plantarum (Mar A5, Bst 1, Mar C7, TB(N), Mg Tm 1, Mg PSM B3, TB(S), MKw 9, Bst 5, Mar B4) yang digunakan menghasilkan tingkat penghambatan yang berbeda-beda (Gambar 11). Berdasarkan metode David stout, aktivitas antibakteri dapat dibagi berdasarkan ukuran diameter daerah hambat yang terbentuk. Pembagian diameter berdasarkan metode tersebut antara lain antibakteri yang menghasilkan daerah hambat sebesar <5 mm termasuk sebagai antibakteri yang lemah; 5-10 mm termasuk sebagai antibakteri yang sedang; 10-20 mm termasuk sebagai antibakteri yang kuat; dan > 20 mm termasuk antibakteri yang sangat kuat (Yani 2011).
Hasil penelitian menunjukkan bahwa terdapat beberapa isolat yang tidak dapat menghambat bakteri Staphylococcus aureus antara lain Bst 1, Bst 5, dan Mar B4. Penghambatan tertinggi terhadap bakteri S. aureus terdapat pada isolat Mg PSM B3 dengan diameter penghambatan bakteri uji 2.5 cm. Penghambatan ini termasuk kategori aktivitas antibakteri yang sangat kuat. Pada bakteri B. cureus isolat yang dapat menghambat pertumbuhan paling besar adalah Bst 5 dan Mar B4 dengan diameter penghambatan 0.5 cm. Proses penghambatan termasuk kategori penghambatan antibakteri yang berkekuatan sedang, sedangkan untuk penghambatan terhadap bakteri Gram negatif yang terdiri atas S. typhimurium, E. coli, dan P. flouresense adalah daya hambat paling besar terdapat pada isolat Mar A5. Hasil pengukuran secara berurutan memiliki ukuran penghambatan sekitar 1.33 cm, 1.83 cm, dan 1.16 cm. Penghambatan tertinggi pada ketiga bakteri uji (S. typhimurium, E. coli, dan P. flouresense) ini memiliki daya hambat yang temasuk antibakteri kuat (Yani 2011).
.
Gambar 11 Efektifitas penghambatan isolat L. plantarum terhadap bakteri uji, yaitu S. typhimurium, S. aureus, E. coli, P. flouresense, dan B. cureus.
SIMPULAN DAN SARAN
Simpulan
Marka gen pln F berhasil mengidentifikasi gen pln F dari sepuluh isolat L. plantarum asal buah-buahan tropis (mangga kweni, manggis, markisa, dan terong belanda). Pita hasil pengukuran RT-PCR berukuran sekitar 70 pb. Selain itu, pengukuran uji ekspresi relatif gen pln F menunjukkan isolat TB (S) yang menunujukkan hasil tertinggi. Hasil pengukuran pada RT-PCR didukung dengan hasil uji antibakteri terhadap bakteri Gram positif (Staphylococcus aureus dan Bacillus cureus) dan bakteri Gram negatif (Escherichia coli, Salmonella typimurium, dan Pseudomonas flouresense).
Saran
Penelitian lebih lanjut mengenai L. plantarum yang mengandung gen pln F perlu dilakukan untuk melihat keefektifan dari L. plantarum yang dapat digunakan sebagai probiotik.
DAFTAR PUSTAKA
Anderssen EL, Diep ZB, Nes I, Eijsink VG, Meyer JN. 1998. Antagonistic activity of Lactobacillus plantarum C11:two new bacteriocin two peptida, plantaricin EF and JK, and the induction factor Plantaricin A. Applied and Environmental Microbiology 64:6.
Aprijani DA, Elfaizi MA. 2004. Bioinformatika perkembangan, disiplin ilmu, dan penerapannya di Indonesia.[terhubung berkala]. http://www.gnu.org/copyleft/fdl.html. [29 Januari 2011]
Aulia RY. 2010. Uji efikasi (In vivo) minuman fungsional sari jagung manis probiotik terhadap kesehatan usus Dan pertumbuhan pada tikus konstipasi Sprague dawley [skripsi]. Bogor: Fakultas Teknologi Pertanian, Institut Pertanian Bogor.
Barcena JMB, Sineriz F, Gonzalez D, Rodriguez A, Suarez JE. 1998. Chemostat production of plantaricin C by Lactobacillus plantarum LL441. Applied and Environmental Microbiology 64: 9. Berg JM, Tymoczko JL, Stryer L. 2005.
Biochemistry. Fifth Edition. USA: W.H Freemen And Company.
Clark W, Chistopher K. 2001. An Intoduction to DNA: Spectrophotometry, Degradation, and the’Frankengel’ Experiment. Canada: University of Alberta.
Cho GS, Huch M, Hanak A, Holzaphel W H, Franz CMAP. 2010. Genetic analysis of the plantaricin EFI locus of Lactobacillus plantarum PCS 20 reveals an unsual plantaricin E gene sequence as a result of mutation. International Journal of Food Microbiology 141.
Endaryantio A, Harsono A. 2005. Prospek probiotik dalam pencegahan alergi melalui induksi aktif toleransi imunologis. [terhubung berkala]. http://www. google.com. [29 Januari 2011].
.
Gambar 11 Efektifitas penghambatan isolat L. plantarum terhadap bakteri uji, yaitu S. typhimurium, S. aureus, E. coli, P. flouresense, dan B. cureus.
SIMPULAN DAN SARAN
Simpulan
Marka gen pln F berhasil mengidentifikasi gen pln F dari sepuluh isolat L. plantarum asal buah-buahan tropis (mangga kweni, manggis, markisa, dan terong belanda). Pita hasil pengukuran RT-PCR berukuran sekitar 70 pb. Selain itu, pengukuran uji ekspresi relatif gen pln F menunjukkan isolat TB (S) yang menunujukkan hasil tertinggi. Hasil pengukuran pada RT-PCR didukung dengan hasil uji antibakteri terhadap bakteri Gram positif (Staphylococcus aureus dan Bacillus cureus) dan bakteri Gram negatif (Escherichia coli, Salmonella typimurium, dan Pseudomonas flouresense).
Saran
Penelitian lebih lanjut mengenai L. plantarum yang mengandung gen pln F perlu dilakukan untuk melihat keefektifan dari L. plantarum yang dapat digunakan sebagai probiotik.
DAFTAR PUSTAKA
Anderssen EL, Diep ZB, Nes I, Eijsink VG, Meyer JN. 1998. Antagonistic activity of Lactobacillus plantarum C11:two new bacteriocin two peptida, plantaricin EF and JK, and the induction factor Plantaricin A. Applied and Environmental Microbiology 64:6.
Aprijani DA, Elfaizi MA. 2004. Bioinformatika perkembangan, disiplin ilmu, dan penerapannya di Indonesia.[terhubung berkala]. http://www.gnu.org/copyleft/fdl.html. [29 Januari 2011]
Aulia RY. 2010. Uji efikasi (In vivo) minuman fungsional sari jagung manis probiotik terhadap kesehatan usus Dan pertumbuhan pada tikus konstipasi Sprague dawley [skripsi]. Bogor: Fakultas Teknologi Pertanian, Institut Pertanian Bogor.
Barcena JMB, Sineriz F, Gonzalez D, Rodriguez A, Suarez JE. 1998. Chemostat production of plantaricin C by Lactobacillus plantarum LL441. Applied and Environmental Microbiology 64: 9. Berg JM, Tymoczko JL, Stryer L. 2005.
Biochemistry. Fifth Edition. USA: W.H Freemen And Company.
Clark W, Chistopher K. 2001. An Intoduction to DNA: Spectrophotometry, Degradation, and the’Frankengel’ Experiment. Canada: University of Alberta.
Cho GS, Huch M, Hanak A, Holzaphel W H, Franz CMAP. 2010. Genetic analysis of the plantaricin EFI locus of Lactobacillus plantarum PCS 20 reveals an unsual plantaricin E gene sequence as a result of mutation. International Journal of Food Microbiology 141.
Endaryantio A, Harsono A. 2005. Prospek probiotik dalam pencegahan alergi melalui induksi aktif toleransi imunologis. [terhubung berkala]. http://www. google.com. [29 Januari 2011].
KONSTRUKSI MARKA GEN PLANTARICIN F
Lactobacillus plantarum
DWI FEBRIYANA
DEPARTEMEN BIOKIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
.
Gambar 11 Efektifitas penghambatan isolat L. plantarum terhadap bakteri uji, yaitu S. typhimurium, S. aureus, E. coli, P. flouresense, dan B. cureus.
SIMPULAN DAN SARAN
Simpulan
Marka gen pln F berhasil mengidentifikasi gen pln F dari sepuluh isolat L. plantarum asal buah-buahan tropis (mangga kweni, manggis, markisa, dan terong belanda). Pita hasil pengukuran RT-PCR berukuran sekitar 70 pb. Selain itu, pengukuran uji ekspresi relatif gen pln F menunjukkan isolat TB (S) yang menunujukkan hasil tertinggi. Hasil pengukuran pada RT-PCR didukung dengan hasil uji antibakteri terhadap bakteri Gram positif (Staphylococcus aureus dan Bacillus cureus) dan bakteri Gram negatif (Escherichia coli, Salmonella typimurium, dan Pseudomonas flouresense).
Saran
Penelitian lebih lanjut mengenai L. plantarum yang mengandung gen pln F perlu dilakukan untuk melihat keefektifan dari L. plantarum yang dapat digunakan sebagai probiotik.
DAFTAR PUSTAKA
Anderssen EL, Diep ZB, Nes I, Eijsink VG, Meyer JN. 1998. Antagonistic activity of Lactobacillus plantarum C11:two new bacteriocin two peptida, plantaricin EF and JK, and the induction factor Plantaricin A. Applied and Environmental Microbiology 64:6.
Aprijani DA, Elfaizi MA. 2004. Bioinformatika perkembangan, disiplin ilmu, dan penerapannya di Indonesia.[terhubung berkala]. http://www.gnu.org/copyleft/fdl.html. [29 Januari 2011]
Aulia RY. 2010. Uji efikasi (In vivo) minuman fungsional sari jagung manis probiotik terhadap kesehatan usus Dan pertumbuhan pada tikus konstipasi Sprague dawley [skripsi]. Bogor: Fakultas Teknologi Pertanian, Institut Pertanian Bogor.
Barcena JMB, Sineriz F, Gonzalez D, Rodriguez A, Suarez JE. 1998. Chemostat production of plantaricin C by Lactobacillus plantarum LL441. Applied and Environmental Microbiology 64: 9. Berg JM, Tymoczko JL, Stryer L. 2005.
Biochemistry. Fifth Edition. USA: W.H Freemen And Company.
Clark W, Chistopher K. 2001. An Intoduction to DNA: Spectrophotometry, Degradation, and the’Frankengel’ Experiment. Canada: University of Alberta.
Cho GS, Huch M, Hanak A, Holzaphel W H, Franz CMAP. 2010. Genetic analysis of the plantaricin EFI locus of Lactobacillus plantarum PCS 20 reveals an unsual plantaricin E gene sequence as a result of mutation. International Journal of Food Microbiology 141.
Endaryantio A, Harsono A. 2005. Prospek probiotik dalam pencegahan alergi melalui induksi aktif toleransi imunologis. [terhubung berkala]. http://www. google.com. [29 Januari 2011].
Gong HS, Meng XC, Wang H. 2010. Plantaricin MG active against Gram-negative bacteria produced by Lactobacillus plantarum KLDS1.0391 isolated from ‘‘Jiaoke”, a traditional fermented cream from China. Elsevier, Food Control 21:89-96.
Holo H, Jecnik Z, Daeschal M, Stefanovic S, Nes I. 2001. Plantaricin W from Lactobacillus plantarum belongs to a new family of two peptida lantabiotics. Microbology 147:643-651.
Hoog S. 2005. Essensial Microbiology. England: John Wiley& Sons Ltd.
[Invitrogen]. 2007. SuperScript III One-Step RT- PCR System with Platinum Taq DNA Polymerase. California: Life Technology. IGEM. 2009. Lactobacillus plantarum.
Ottawa: Universitas of Ottawa.
Jorgenrud BM. 2009. Construction of a heterologous expression vector for plantaricin F, one of the peptides constituting the two-peptide bacteriocin Plantaricin EF [thesis]. Universitas Osloensis: Departement Of Moleculer Bioscience.
Lu Z, Breidt F, Fleming HP, Altermann E, Klaenhammer T.R. 2003. Isolation and characterization of a Lactobacillus plantarum bacteriophage Φ JL-1 from a cucumber fermentation. International Of Food Microbiology, Scient Direct. 84:225-235.
Lun G, Sansone EB. 1989. Decontamination of ethidium bromide spills. Appli.ind.Hgy 234-237.
McPherson M, Moller S. 2006. PCR. Second edition. United Kindom: Taylor and Francis Goup.
[Microarrays]. 2000. Isolation Of Total RNA From Escherichia coli For Microarrays. Gross Lab Protocol For Microarrays. Moghadam MS, Foo HL, Leow TC, Rahim
RA, Loh TC. 2010. Novel bacteriocinogenic Lactobacillusplantarum strains and their differentation by sequence analysis of 16S DNA, 16S-23S and 23S-5S intergenic spaces regions and randomly
amplified polymorphic DNA analysis. Food Technol, Biotechnol 48 (4): 476-483 Murray RK, Ganner DK, Rodwell PW. 2009.
Biokimia Harper. Pendit DU, Penerjemah; Wulan N, editor. Jakarta: EGC. Terjemahan dari: Harper’s Illustrated Biochemistry.
Nurhidayat Novik. 2010. Laporan akhir kumulatif kegiatan program kompetitif: domestika bakteri probiotik dari buah-buahan untuk immunomodulator penunjang ketahanan pangan fungsional. Bogor: LIPI Cibinong.
Oguekke CC, Owuamanam CI, Ihediohanma NC, Iwouno JO. 2010. Probiotics and prebiotics: unfolding prospects for better human health. Pakistan Journal of Nutrition 9: 833-843.
Paynter MJB, Brown KA, Hayasaka SS. 1997. Factors affecting the production of an antimicrobial agent , plantaricin F, by Lactobacillus plantarum BF001. Letter in Apllied Microbiology 24:159-165. Pelczar MJ, Chan ECS. 2005. Dasar-Dasar
Mikrobiologi. Jakarta: UI Pr.
Potter JL, Nakhla MK., Rojas M, Gilbertson RL, Maxwell D.P. 2007. Protocols For Detection Of Begomovirus. University of Wisconsin-Madison.
Prabowo SK. 2010. Produksi bakteriosin dari bakteri asam laktat galur SCG 1223 dalam media molasses [skripsi]. Bogor: Fakultas Teknologi Pertanian, Institut Pertanian Bogor.
Reeneen CAV, Dicks LMT, Chinkidas ML. 1998. Isolation, purification, and partial characterization of plantaricin 423, a bacteriosin produced Lactobacillus plantarum. Journal Applied Microbiology 84.
Sambrook J, Russel DW. 2001. Molecular Cloning : A Laboratory Manual. 3rd edition. New York: Cold Spring Harbor Laboratory Pr, Cold Spring Harbor. Smith AD, Datta SP, Smith GH, Campbell
Biochemistry and Moleculer Biology. United States: Oxford University Pr.Inc. Song H, Liu Y, Hu G, Qin Y, Lin S. 2011. An
improved method for total RNA isolation from recalcitrant loquat (Eriobotyra Japonica Lindl.) Buds. Pak J Bot 43: 1163-1171.
Suparjo. 2008. Bakteriosin dan peranannya dalam ekologi mikroba rumen. [terhubung berkala]. http://www.jajo66.wordpress. [28 Januari 2011]
Suskovic J, Kos B, Goreta J, Matosik S. 2001. Role of lactic acid bacteria and Biffidobacteria in synbiotic effect. Food Technol Biotecnol 39: 227-235.
Triana E, Yulianto E, Nurhidayat N. 2006. Uji viabilitas Lactobacillus sp. Mar 8 terenkapsulasi. Biodivesitas 7:114-117. Trizana NM. 2010. Isolasi dan karakterisasi
promotor gen Agamous (TcAG) dari kakao (Theobroma cacao L.) [skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Widyastuti Y, Ratnakomala S, Ekawati F. 1998. Bakteri asam laktat buah-buahan tropis. Pertemuan Ilmiah Tahunan: Bandar Lampung.
Wilson K, Walker J. 2000. Principles and Techniques of Practical Biochemistry. 4rd edition. United Kingdom: Cambridge University.
Wirawan IGP, Sulistyowati L, Wijaya IN. 2004. Penyakit CVPD Pada Tanaman Jeruk Analisis Baru Berbasis Bioteknologi. Denpasar: Direktorat Jendral Bina Produksi Holtikultura, Departemen Pertanian.
Yani A. 2011. Fraksinasi komponen aktif antibakteri ekstrak kulit batang tanaman berenuk (Crescentia cujete L) [skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
KONSTRUKSI MARKA GEN PLANTARICIN F
Lactobacillus plantarum
DWI FEBRIYANA
DEPARTEMEN BIOKIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
ABSTRAK
DWI FEBRIYANA. Konstruksi Marka Gen Plantaricin F
Lactobacillus
plantarum
. Dibimbing oleh DJAROT SASONGKO HAMI SENO dan
NOVIK
NURHIDAYAT.
Lactobacillus plantarum
merupakan bakteri yang dapat berperan sebagai
probiotik. Bakteri ini memiliki plantaricin F yang berguna menghambat
pertumbuhan bakteri Gram positif dan negatif. Penelitian ini menggunakan
sepuluh isolat
L. plantarum
(Mar A5, Bst 1, Mar C7, TB(N), Mg Tm 1, Mg PSM
B3, TB(S), MKw 9, Bst 5, Mar B4) yang berasal dari buah-buahan tropis (mangga
kweni, manggis, markisa, dan terong belanda). Penelitian ini dilakukan untuk
konstruksi marka gen
pln F
dan menganalisis ekspresi relatif gen
pln F
serta uji
aktivitas antibakteri. Pengujian gen
pln F
menggunakan RT-PCR menghasilkan
pita DNA berukuran 70 pb. Hasil pengujian ini selanjutnya dipakai untuk
menentukan nilai ekspresi relatif gen
pln F
menggunakan software
CS Analyzer.
Nilai ekspresi relatif gen tertinggi didapat dari isolat TB (S) dengan nilai 28.13
Au. Uji aktivitas antibakteri dilakukan untuk melihat hubungan antara gen
pln F
dengan aktivitas penghambatan isolat terhadap bakteri uji. Uji aktivitas antibakteri
dilakukan terhadap lima bakteri antara lain
Salmonella typhimurium
,
ABSTRACT
DWI FEBRIYANA.
Gene Marker Construction of Plantaricin F
Lactobacillus
plantarum
. Under the supervision of DJAROT SASONGKO HAMI SENO and
NOVIK NURHIDAYAT
KONSTRUKSI MARKA GEN PLANTARICIN F
Lactobacillus plantarum
DWI FEBRIYANA
Skripsi
sebagai salah satu syarat untuk memperoleh gelar
Sarjana Sains pada
Departemen Biokimia
DEPARTEMEN BIOKIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
Judul Skripsi : Konstruksi Marka Gen Plantaricin F
Lactobacillus plantarum
Nama : Dwi Febriyana
NIM
: G84070045
Disetujui
Komisi pembimbing
Dr. Djarot Sasongko Hami Seno, MS
Dr. Novik Nurhidayat
Ketua
Anggota
Diketahui
Dr.Ir. I Made Artika, M.App.Sc
Ketua Departemen Biokimia
PRAKATA
Puji dan syukur penulis panjatkan kepada Allah SWT atas segala
karunia-Nya, shalawat serta salam semoga selalu tercurah kepada Nabi Muhammad SAW,
keluarga, dan para sahabat sehingga penulis dapat menyelesaikan penelitian ini.
Penelitian ini berjudul Konstruksi Marka Gen Plantaricin F L
actobacillus
plantarum
. Waktu penelitian ini dilakukan dari bulan April hingga Juli 2011,
bertempat di Laboratorium Genetika, Mikrobiologi Pusat Penelitian LIPI,
Cibinong, Bogor.
Penulis mengucapkan terima kasih kepada semua pihak yang telah
membantu dalam penyelesaian penelitian ini, antara lain kepada Dr. Djarot
Sasongko Hami Seno, MS. selaku pembimbing utama dan Dr. Novik Nurhidayat
selaku pembimbing lapangan yang telah memberikan saran, kritik, dan
bimbingannya serta Ibu Neri, Mba Ratih, Ibu Evi, Ibu Ernawati, serta segenap staf
di Laboratorium LIPI Biologi atas peran dan kerjasamanya yang telah banyak
membantu dalam menyelesaikan penelitian ini. Ucapan terima kasih juga penulis
sampaikan kepada orang tua, kakak, ibu Suryani, Maya dan Biokimia 44 untuk
semua doa, dukungan, dan bimbingan yang sangat berarti bagi penulis. Serta
kepada rekan Seperjuangan selama penelitian Tyas, Nindi, Ekky, Chemi, Fina,
Karlina, Christian, Raras, Fauziah dan Wina atas saran dan motivasi yang
diberikan. Penulis berharap semoga karya ilmiah ini dapat memberikan manfaat
bagi semua orang yang memerlukannya.
Bogor, Oktober 2011
RIWAYAT HIDUP
Penulis dilahirkan di Jakarta pada tanggal 13 Februari 1990 dari ayah
Sulaiman dan ibu Wartih. Penulis merupakan anak kedua dari dua bersaudara.
Pendidikan penulis dimulai dari SDN 13 Pagi Rawamangun, kemudian
melanjutkan pendidikan ke SMPN 74 Jakarta, dan SMAN 31 Jakarta. Pada tahun
2007 penulis lulus dari SMAN 31 Jakarta dan lulus seleksi masuk IPB melalui
jalur Undangan Seleksi Masuk IPB (USMI) dengan memilih mayor Biokimia
pada Departemen Biokimia, Fakultas Matematika dan Ilmu Pengetahuan Alam.
DAFTAR ISI
Halaman
DAFTAR GAMBAR ... v
DAFTAR TABEL ... v
DAFTAR LAMPIRAN ... vi
PENDAHULUAN ... 1
TINJAUAN PUSTAKA
Lactobacillus plantarum
... 1
Probiotik ... 2
Plantaricin F ... 2
Isolasi RNA ... 2
Polymerase Chain Reaction
... 3
RT-PCR ... 3
Elektroforesis ... 4
Perancangan Primer ... 4
BAHAN DAN METODE
Alat dan Bahan ... 5
Metode Percobaan ... 5
HASIL DAN PEMBAHASAN ... 7
RNA Total
Lactobacillus plantarum
... 7
Hasil Perancangan Primer ... 8
Amplikon dan Ekspresi Gen
pln F
dengan RT-PCR ... 8
Aktivitas
L. plantarum
Terhadap Pertumbuhan Bakteri Uji